Method Article
리빙 셀의 Subcellular 수준과 초 Timescale에 작은 GTPase 활동의 Spatio-시간적 조작
요약
빛으로 작은 GTPase 활동 spatio-시간적 제어를위한 방법을 설명합니다. 이 방법은 rapamycin-유도 FKBP-FRB의 heterodimerization 및 사진 caging 시스템을 기반으로합니다. 빛을 조사의 최적화는 subcellular 수준에서 작은 GTPases의 spatio-temporally 제어 활성화를 가능하게합니다.
초록
위대한 spatiotemporal 정밀도와 작은 구아 노신의 triphosphatases (GTPases)의 Rho 가족의 동적 규제는 다양한 세포 기능과 이벤트가 1, 2 필수적입니다. 그들의 spatiotemporally 동적 특성은 실시간 3 그들의 활동 및 현지화의 시각화에 의해 발표되었습니다. 분자 수준에서 다양한 세포 기능에서의 역할 깊은 이해를 얻을하려면, 다음 단계는 정확한 subcellular 위치와 타이밍에 단백질 활동의 섭동 있어야합니다.
(1) rapamycin-유도 FKBP-FRB의 heterodimerization와 rapamycin (2) 사진 caging 방법 : 이러한 목표를 달성하기 위해, 우리는 빛을 유발, 두 기술을 결합하여 작은 GTPases의 spatio-temporally 제어 활성화를위한 방법을 개발했습니다. rapamycin-매개 FKBP-FRB의 heterodimerization의 사용으로, 우리는 급속하게 작은 GTPases includi의 활성화 또는 불활 성화를 inducible하는 방법을 개발했습니다NG RAC 4, rapamycin은 FRB가 정박되어 플라즈마 막까지, FKBP-융합된 GTPases, 또는 그들의 activators의 translocation을 유도하는 Cdc42 4, RhoA 4 RAS 5. 이 heterodimerization 시스템과 커플링 들어, 우리는 또한 rapamycin의 analogs의 사진 caging 시스템을 개발했습니다. 사진 갇힌 화합물은 누구 활동 caging 그룹으로 알려진 photocleavable 보호 그룹과 억압되어 작은 분자이다. 완전히 heterodimerization 활동을 억제하기 위해, 우리는 세포 6 안의 화학 dimerizer로 거의없이 백그라운드 작업으로 이어지는, 그 결과 대규모 복합 단지 플라즈마 막 건너없는 그런 macromolecule에 닿는 곳에있다 갇힌 rapamycin을 설계했습니다. 그림 1은 우리의 방식을 보여줍니다 시스템. 이 두 시스템의 결합을 통해, 우리는 로컬 초 timescale에 플라즈마 막에 RAC 활성을 모집하고 subcellular 레바에 빛을 유발 RAC 인증을 획득엘 6.
프로토콜
1. 플라스미드 DNA의 Transfection
- 37.5 μl DH 2 O.로 형광 단백질로 태그 : 플라스미드 DNAs, 0.5 μg 멤브레인-닿는 곳에 FRB (이하 LDR로 지칭)와 0.5 μg FKBP-Tiam1을 (RAC 활성 T-세포 림프종의 침략과 전이 - 유도 단백질 1) 추가 1 μl FuGENE HD를 추가합니다.
- 20 분 동안 상온에서 소용돌이와 부화. 한편, 단계 1.3-1.8로 진행합니다.
- 50 μl 폴리-D-라이신과 8 아니라 챔버의 각 잘 씻으십시오.
- DH 2 O를 사용하여 각 우물의 중심을 씻으
- 80~85% 합류 NIH-3T3 세포를 Trypsinize 10 ML 문화 매체 (10 % FBS가있는 DMEM)에 희석.
- 정지 375 μl를 제거하고 3 분 동안 1,750 rpm으로 원심 분리기.
- 펠렛을 방해하지 않도록주의되는 미디어를 기음.
- DMEM w / 10 % FBS와 resuspend의 750 μl를 추가합니다.
- DH 2 O / 유전자 / FuGENE의 HD 솔루션에 세포 현탁액을 넣고 가볍게 섞는다.
- 250 추가각도에 대한 세포 / DNA를 정지 μl (3 우물까지 작성됩니다.)
- 37 transfected 세포를 품어 ° C와 15-18 시간에 대한 5퍼센트 CO 2.
2. cRb-솔루션의 작성
- 합성 갇힌 rapamycin-비오틴의 adduct (cRb). 자세한 내용은 "cRb의 합성 구조"를 참조하십시오. 간단히, caging 및 비오틴 moieties는 별도로 준비가되어 있습니다. caging 잔기 그때 rapamycin (LC 실험실)에 복합이며, 제품은 이후 cRb를 살만큼 클릭 반응 7 수단을 이용하여 비오틴 잔기에 결합.
- DMSO의 cRb 중 1 μm의 주식 솔루션을 준비합니다.
- 0.5 ML Eppendorf 튜브에 PBS 250 μl에 1mg 아비딘를 해산.
- 녹아 아비딘에 cRb 주식 솔루션 1 μl를 추가합니다. 반전을 여러 번하여 섞는다.
- cRb - 아비딘 켤레축을 (cRb-양보하는 15 분 동안 상온에서 부화) 솔루션입니다.
- 언바운드 작은 분자를 제외하고 정화 cRb - 크기 - 제외 컬럼을 사용합니다.
3. 현미경과 Subcellular 레벨 라이트 일루미 네이션
- 세럼은 12 시간 동안 FBS없이 DMEM에 transfected 세포를 굶어.
- 부드럽게 세포 밖 미디어를 대기음하고 준비한 400 nm의 cRb - 솔루션 (단계 2.6에서) 250 μl를 추가합니다.
- 빛 치료 전후 subcellular 해상도 세포를 생활에 단백질 역학을 시각화하기 위해 회전 디스크 현미경은 (그림 2A) 사용되었다. 자외선 조명은 에피 형광 라이트 (그림 2B)와 자외선 LED가 라이트 (365 나노미터)의 광학 장치를 결합하여 달성되었다.
- MetaMorph 소프트웨어는 transfected 세포의 형광 이미지를 매 15 초 캡처하는 데 사용되었다.
- 자외선에 의해 흥분 형광 염료로 코팅 유리 접시를 사용하여 조명 장소의 좌표와 크기를 정의합니다. 크기는 수다른 배율로 객관 렌즈를 적용하여 서로 다른 코어의 크기와 광학 섬유를 선택하여 다양한됩니다.
- 세포 주변에 막 ruffling, 비추다의 자외선 빛을 배경 수준을 결정 후에. 다음 두 단계화된 효과를 이전 대조하는 것입니다.
- 글로벌 수은 램프에서 제공하는 365 nm의 조명과 함께 세포를 조사하다.
- , uncaged DMSO의 후 PBS (400 nm의 결승전)에 따라서 원래의 rapamycin를 해산하고, 글로벌 효과를 유발하는 이미징 챔버에 솔루션을 추가합니다.
4. 대표 결과
대표적인 결과의 예제는 그림 3에 표시됩니다. 셀룰러 가장자리 근처의 작은 지역에서 자외선의 조사가 급속화된 형성을 유도하는 것은 조사 지역 및 인근에만 주름. 이 whi 모두, 우리는 그때 전세계 자외선으로 세포를 반구, 실제로 현지 활동이었다, 또는 대량 매체에 rapamycin을 추가했는지 확인하려면채널은 세포막에 걸쳐 세계적인 주름 형성을 유도. 정량 분석을 위해, 우리는 네 quadrants로 타겟 세포를 나누어, 그리고 주름의 현지시 각 사분면에 형성뿐만 아니라 컨트롤 (그림 4) 등 다양한 조건 하에서 글로벌 자극을 다음의 주파수를 계산. 그것은 오직이 자외선 조사의 조합, cRb-, 지방 ruffling을 유도 적절한 FKBP-FRB 구조입니다.

그림 1. 갇힌 rapamycin-아비딘 켤레축 (cRb-)과 자외선을 사용 spatially 국한 단백질 dimerization의 도식. 자외선 조사는 화학 dimerizer (HE-Rapa, C40-O-(2 - 히드록시 에틸) rapamycin)과 그 부산물의 릴리스 결과, rapamycin과 비오틴 사이의 링커를 클리브. 발표 dimerizer 다음 세포로 diffuses 및 FKBP-POI (관심있는 단백질)와 플라즈마 memb 사이에 dimerization을 유도rane은 조사 지역 (파란색 동그라미)의 근처에 FRB를 정박. UV 조사없이 FKBP와 FRB는 따라서 아무런 효과를 생산 안되고, (적십자) 연관시키지 않습니다. (저작권 @ ACS2011) 6

그림 2. 맞춤 공촛점 형광 현미경 사진. 공촛점 현미경 () 정면보기 (Axiovert 200, 자이스 혈구를 거꾸로 읽었). 에피 형광 및 자외선 조명을위한 커플링 단위의 (b)는 클로즈업, 최고 볼 수 있습니다.
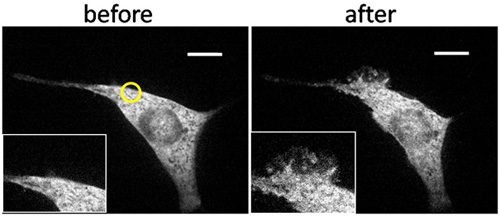
그림화된 자외선 조사에 의해 유도된 transfected NIH3T3 세포 3. Spatially 국한 주름 형성. YFP 태그가 추가된 FKBP-Tiam1 (RAC 활성)과 LDR (FRB를 멤브레인 - 고정)으로 transfected되는 NIH3T3 fibroblast 세포의 공촛점 형광 이미지는 L과의 가장자리 근처의 좁은 지역에서 조사를 받았습니다15 초이 대량 미디어 cRb-켤레축의 면전에서 210 초부터 시작을위한 365 nm의에서 ED 라이트. 이 치료는 1560 초 rapamycin 최종 400 NM의 1063 초 및 글로벌 또한 1 초위한 수은 램프와 글로벌 일루미 네이션 다음되었다. 세포는 처음 ()에서 거의 ruffling 활동을 보여주 없지만 보여주 spatially화된 조명 후에 ruffling 국한 (노란색 동그라미) (B). 세포는 로컬 주름 형성은 RAC의 spatially 제한된 활성화로 인한 것을 나타내는 글로벌 일루미 네이션과 rapamycin (CD)가 추가되는 이후 글로벌 주름 형성을 보여주었다. 스케일 바 : 10 μm의. (저작권 @ ACS2011) 6
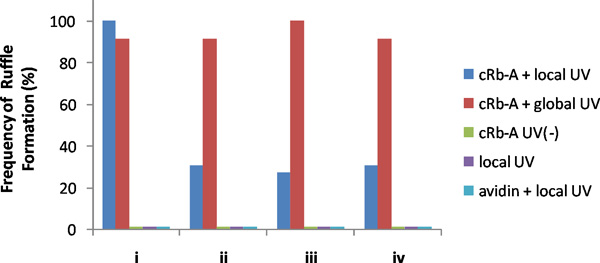
그림 4. transfected NIH3T3 세포의 quadrants의 주름 형성의 빈도. cRb-A와 다음 글로벌 자외선 조사는 13 세포에서 수행되었다. cRb -와 로컬 자외선 조사 또한 (노 자외선 조사)를 trong, 아비딘 여부에 상관없이 현지 자외선 조사는 각각 13, 5, 6 세포에 구현되었다. 관찰된 세포들은 아무도 자외선 조사, 또는 함께 또는 대용량 미디어 아비딘없이 현지 자외선 조사없이 cRb-으로 주름 형성을 보여주 없습니다. 우리는 낮은 배경 주름 형성과 함께 세포에서 데이터를 수집하지만, 그건 우리가 rapamycin (최종 400 NM)의 이외의 결과로 세계적인 주름 형성을 확인하여 각 실험 후 확인 rapamycin 유발 주름 형성의 용량을했습니다. 이러한 결과는 cRb - 지방 자외선 조사가 세포의 지방 주름 형성에 필요한 것을 보여주었다. (저작권 @ ACS2011) 6
약어 :
FKBP : FK506 결합 단백질
FRB : FKBP-rapamycin-결합 단백질
Tiam1 : T-세포 림프종의 침략과 전이 - 유도 단백질 1 (RAC GEF)
LDR : 린 - DSAG 링커-FRB (린 : 린 키나제의 N-터미널 11 아미노산)
HE-Rapa : C40-O - (2 - 히드록시 에틸) rapamycin
cRb : 비오틴 잔기와 갇힌 rapamycin
cRb-: 아비딘하기 cRb 복합
토론
우리는 초 시간 척도에 대한 정밀한 subcellular 위치에 Rho GTPase 활동을 조작하기 위해 FKBP-FRB heterodimerization 시스템 소설 갇힌 화합물을 함께 고용 기법을 설명했다.
현재의 접근 방법의 세 한계가 있습니다. 메서드가 플라즈마 막 걸쳐 dimerizer의 확산을 방지하거나 허용을 기반으로하고 있기 때문에 첫째, 대상 세포 위치는 플라즈마 막 또는 그 주변 있어야합니다. cRb의 화학 구조에 더 최적화 화합물이 빛을 조사까지 dimerization을 유도하지 않고 세포를 입력할 수 있습니다. 이러한 dimerizer으로, 우리는 이론 어디에서나 세포 내부 분자를 신호 활동을 조작할 수 있습니다. 둘째, 화학 dimerizers, FKBP-FRB의 dimerization 복합, 또는 활성 내생 신호 분자의 분자 확산은 크게 의도된 효과의 정확한 감금에 영향을 미칠 수 있습니다. 이 효과는 특히 발음에서 나중에 포인트와 자외선 조사 (예 : 빔 폭, 에너지 및 빔 모드 (연속적인 대 펄스) 등)과 관련된 화합물의 확산 계수와 연관된 매개 변수에 따라 달라집니다. 이러한 매개 변수의 추가 경험적 최적화 신호 활동의 더 엄격한 구속 수 있습니다. 셋째, 자외선은 세포에 비 사소한 phototoxicity을 전시하고 있습니다. 이 문제를 개량하다 한 가지 쉬운 방법 nitrobenzyl caging 그룹을 개방하다 그러한 405 nm의 같은 긴 파장을 사용하는 것입니다. uncaging위한 두 광자 조명도 더 이상 파장뿐만 아니라에서 세포의 극히 국소 영역에서 조명이 가능합니다. 최근 다른 연구자들은 빛을 민감한 식물 단백질에게 8-11를 사용 subcellular 위치에 RAC를 활성화하는 우아한 접근을보고했습니다. 지금까지 애플 리케이션은 몇 가지 단백질로 제한됩니다. 그들의 전략에 비해 우리의 현재 기술은없이 타겟 단백질의 수를 확대하는 것이 더 쉽게 적응하고 광범위한 TI나를 소모 재 엔지니어링. 우리와 다른 사람은 이미 플라즈마 막 5, 6, 12-14에서 다양한 신호 분자의 활동을 조작할 수 dimerization 프로브의 다양한 개발했습니다. Spatiotemporally 역동적인 세포 사건은 이제 직접 testable 수 있습니다.
공개
관심의 어떠한 충돌 선언 없습니다.
감사의 말
이 연구는 NIH 연구 기금 (DK090868과 TI의 GM092930)에 의해 지원되었다. 갇힌 rapamycin 유사체에 대한 출원 특허가있다.
자료
| Name | Company | Catalog Number | Comments |
| 시약 / 장비의 명칭 | 회사 | 카탈로그 번호 | |
| Rapamycin | Tecoland | RAPA99 | |
| FuGENE HD | 로슈 | 04709691001 | |
| 아비딘 | 시그마 | A9275-10MG | |
| DMSO | 시그마 | D2650-5X5ML | |
| 크기 - 배제 칼럼 | GE 헬스케어 | 스핀 트랩 G-25 | |
| 유리 바닥 8 아니라 챔버 | 써모 과학 | 12-565-47 | |
| 간접 형광 현미경 | 자이스 혈구 | Axiovert200M | |
| 자외선은 광원을 LED가 | Rapp Opto 전자 | UVILED | |
| 공촛점 스피닝 디스크 | Yokogawa 전기 주식 회사 | CSU10 | |
| CCD 카메라 | 하마 마츠 Photonics | 오카-ER | |
| 100x 목적 렌즈 | 자이스 혈구 | 계획 고차 색지움 |
cRb의 합성 구조 (저작권 ACS2011) 6

합성 조건 : () BnBr, K 2 CO 3, DMF (B) f.HNO 3 AcOH (C) TFA (D) Propargyl-BR, K 2 CO 3, DMF, (마) 글리세롤, 고양이.에게 pTsA, 톨루엔 (F) NaBH 3 CN, TiCl 4, MeCN (G) TF 2 O, Pyridin (H) 메탄올 HCL,은 (i) LiAlH 4, THF (J) TsCl, 피리딘, 채널이 망할 CIA 2 (K) 앤 3, DMF (L) 8, 2,6 - 디-T-butylpyridine, 채널이 망할 CIA 2 (M) 13 CuSO 4, 아스코 브 산, 2 - 프로파놀, H 2 O, CH 2 CIA 같으니 2.
참고문헌
- Etienne-Manneville, S., Hall, A. Rho GTPases in cell biology. Nature. 420, 629-635 (2002).
- Takai, Y., Sasaki, T., Matozaki, T. Small GTP-binding proteins. Physiol. Rev. 81, 153-208 (2001).
- Kiyokawa, E., Aoki, K., Nakamura, T., Matsuda, M. Spatiotemporal regulation of small GTPases as revealed by probes based on the principle of Forster Resonance Energy Transfer (FRET): Implications for signaling and pharmacology. Annu. Rev. Pharmacol. Toxicol. 51, 337-358 (2011).
- Inoue, T., Heo, W. D., Grimley, J. S., Wandless, T. J., Meyer, T. An inducible translocation strategy to rapidly activate and inhibit small GTPase signaling pathways. Nat. Methods. 2, 415-418 (2005).
- Komatsu, T. Organelle-specific, rapid induction of molecular activities and membrane tethering. Nat. Methods. 7, 206-208 (2010).
- Umeda, N., Ueno, T., Pohlmeyer, C., Nagano, T., Inoue, T. A photocleavable rapamycin conjugate for spatiotemporal control of small GTPase activity. J. Am .Chem. Soc. 133, 12-14 (2011).
- Kolb, H. C., Finn, M. G., Sharpless, K. B. Click Chemistry: Diverse Chemical Function from a Few Good Reactions. Angew. Chem. Int. Ed. Engl. 40, 2004-2021 (2001).
- Kennedy, M. J. Rapid blue-light-mediated induction of protein interactions in living cells. Nat. Methods. 7, 973-975 (2010).
- Levskaya, A., Weiner, O. D., Lim, W. A., Voigt, C. A. Spatiotemporal control of cell signalling using a light-switchable protein interaction. Nature. 461, 997-1001 (2009).
- Wu, Y. I. A genetically encoded photoactivatable Rac controls the motility of living cells. Nature. 461, 104-108 (2009).
- Yazawa, M., Sadaghiani, A. M., Hsueh, B., Dolmetsch, R. E. Induction of protein-protein interactions in live cells using light. Nat. Biotechnol. 27, 941-945 (2009).
- Fegan, A., White, B., Carlson, J. C., Wagner, C. R. Chemically controlled protein assembly: techniques and applications. Chem. Rev. 110, 3315-3336 (2010).
- Suh, B. C., Inoue, T., Meyer, T., Hille, B. Rapid chemically induced changes of PtdIns(4,5)P2 gate KCNQ ion channels. Science. 314, 1454-1457 (2006).
- Varnai, P., Thyagarajan, B., Rohacs, T., Balla, T. Rapidly inducible changes in phosphatidylinositol 4,5-bisphosphate levels influence multiple regulatory functions of the lipid in intact living cells. J. Cell. Biol. 175, 377-382 (2006).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유