Mikro-CT-Bildgebung von Maus-Rückenmark
Überblick
Quelle: Peiman Shahbeigi-Roodposhti und Sina Shahbazmohamadi, Biomedical Engineering Department, University of Connecticut, Storrs, Connecticut
Es ist eine wenig bekannte Tatsache, dass die Entdeckung und (unbeabsichtigte) Verwendung von Röntgenstrahlen den ersten Nobelpreis für Physik überhaupt erhielt. Das berühmte Röntgenbild der Hand von Dr. Röntgens Frau aus dem Jahr 1895, das Schockwellen durch die wissenschaftliche Gemeinschaft schickte, sieht aus wie die meisten modernen 2D-Röntgenbilder. Obwohl es nicht die neueste Technologie ist, ist Röntgenabsorptions-Bildgebung ein unverzichtbares Werkzeug und kann in den weltweit führenden F&E- und Universitätslabors, Krankenhäusern, Flughäfen und anderen Orten gefunden werden. Die wohl fortschrittlichsten Anwendungen der Röntgenabsorptions-Bildgebung beinhalten das Erlangen von Informationen wie in einer medizinischen 2D-Röntgenaufnahme, die aber in 3D durch eine Computertomographie (CT oder Micro-CT) realisiert wurde. Durch eine Reihe von 2D-Röntgenprojektionen ist fortschrittliche Software in der Lage, Daten zu einem 3D-Volumen zu rekonstruieren. Die 3D-Informationen können und werden höchstwahrscheinlich Informationen aus der Innenseite des untersuchten Objekts enthalten, ohne aufgeschnitten werden zu müssen. Hier wird ein Micro-CT-Scan erhalten, und die wichtigsten Faktoren, die die Bildqualität beeinflussen, werden diskutiert.
Grundsätze
Röntgenstrahlen können als Photonen mit einem Energiebereich von 0,1 - 100 keV oder elektromagnetische Wellen mit Wellenlängen von 0,01 - 10 nm betrachtet werden. Röntgenstrahlen können auf verschiedene Arten erzeugt werden, aber hier beschränkt sich die Diskussion auf kontinuierliche Spektrenkegelstrahl-Röntgenaufnahmen. Diese Röntgenstrahlen entstehen durch ein Phänomen, das als "Bremsstrahlung" bekannt ist, was im Deutschen "Bremsstrahlung" bedeutet. Dies tritt auf, wenn ein geladenes Teilchen eine Beschleunigung durchläuft [1]. In einer Röntgenquelle wird ein negativ geladenes Elektron in einem Vakuumrohr aufgenommen und trifft ein Zielmaterial (in der Regel Wolfram, Molybdän, Kupfer oder ein anderes Metall) und emittiert durch seine Verzögerung Photonen im Maßstab einer Röntgenstrahlung. Ein kontinuierliches Spektrum von Röntgenstrahlen wird erzeugt, weil die Verzögerung weder gleichmäßig noch augenblicklich ist, obwohl es Spitzen in der Verteilung gibt, die um die charakteristischen Energien des Zielmaterials zentriert sind, wie in [2] zu sehen ist. Es gibt unterschiedliche Kurven für verschiedene Energien und Zielmaterialien. Dies ist eine sehr wichtige Sache, die bei der Durchführung eines Micro-CT-Scans zu beachten ist und wird in einem späteren Abschnitt behandelt.
Ein typisches Mikro-CT-System verfügt über drei Hauptkomponenten, wie in [3] dargestellt. Zu den Grundkomponenten dieses Systems gehören: a) Röntgenquelle, b) Rotationsstufe für die Probenmontage und c) Flachbildschirm oder optisches Objektiv mit CCD-Detektoren. Röntgenstrahlen verlassen die Quelle und werden entweder von der Probe absorbiert, übertragen oder gestreut, bevor sie am Detektor ankommen. Absorption ist die vorherrschende Wechselwirkung, die in microCT gemessen wird, da verschiedene Materialien im Körper Röntgenstrahlen unterschiedlich absorbieren. Zum Beispiel enthalten Knochen viel atomares Kalzium, das Röntgenstrahlen gut absorbiert. So blockieren Knochen Röntgenstrahlen daran, den Detektor zu erreichen, und zeigen sich am Ende im Bild als Schatten. Die Probe wird dann inkrementell gedreht und der Prozess wird wiederholt, bis die Probe für 360° oder in einigen Fällen 180° abgebildet wurde. Der Ausgang der Tomographie ist eine Reihe von 2D-Projektionen in unterschiedlichen Ausrichtungen, die in einem 3D-Volumen rekonstruiert werden können.
Micro-CT ist eine Form der Mikroskopie, die ihren Namen durch ihre Fähigkeit verdient, Mikro-Skala-Features aufzulösen. Die Begrenzung der Auflösung für diese spezifische Kategorie von Mikro-CT richtet sich nach der Quell-Spotgröße und der Energiestreuung sowie nach Art und Wirksamkeit des Detektors; nicht durch die Wellenlänge des Röntgenbildes. Die bestmögliche Auflösung für diese Kategorie von Mikro-CT ist etwa 500-700 nm in drei Dimensionen. Obwohl, es ist möglich, Features ein Zehntel oder Hundertstel dieser Größe zu erkennen.
Die Vergrößerung erfolgt in den meisten CT-Systemen durch geometrische Vergrößerung. Das Bild in [3] veranschaulicht die Idee der geometrischen Vergrößerung. Es ist leicht als Schatteneffekt vorstellbar. Je näher eine Lichtquelle an einem Objekt liegt; Je größer der Schatten des Objekts ist, desto größer ist der Schatten des Objekts, wird auf einer Wand oder einem Bildschirm angezeigt. Wenn sich diese Wand oder dieser Bildschirm von der stationären Lichtquelle und der Probe entfernen würde, würde der Schatten des Objekts an Größe zunehmen, aber schwächer werden. Die Optimierung der Röntgenquelle und der Arbeitsabstände des Detektors ist eine sehr anspruchsvolle und mental stimulierende Aufgabe, wenn ausreichend Signal, hohe Auflösung und eine kurze Scanzeit gewünscht werden. Wie bei allem gibt es Einschränkungen bei der geometrischen Vergrößerung, wo die Idealisierung einer Punktquelle zerstört wird und Aberrationen überheblich werden.
Eine der vielen Herausforderungen bei micro-CT ist, dass die visuelle Qualität des 3D-Volumens dem Prüfer bis zum Abschluss und der Rekonstruierten etwas unbekannt ist. Obwohl, mit genügend Erfahrung, eine sorgfältige Untersuchung einiger 2D-Projektionen kann genug Informationen liefern, um sich über einen CT-Scan sicher zu fühlen. In den folgenden Abschnitten werden in einer Reihe von Übungen die Auswirkungen verschiedener bildgebender Parameter auf einen Datensatz aufgedeckt und ein Wissenschaftler mit dem Verständnis ausgestattet, das erforderlich ist, um ein sauberes 3D-Volumen zu erhalten. Für die Zwecke dieser Untersuchung werden biologische Proben untersucht, obwohl das Verfahren nicht auf einen Probentyp beschränkt ist.
Das Einhängen eines Samples klingt wie ein trivialer Schritt, ist aber einer der wichtigsten und übersehenen. Unabhängig von der Anwendung sollte die Probe so kompakt wie möglich montiert werden. Stellen Sie sich unter Berücksichtigung des Bildes in [3] vor, ob die Reichweite der Quell- und Detektorpositionen begrenzt wäre, da die Probe in eine Richtung herausragte und wie sich dies auf die geometrische Vergrößerung auswirken würde. Neben dem Arbeitsabstand wirkt sich die Montage stark auf den Durchsatz aus. Wenn es sich bei der Probe um ein intaktes Kniegelenk einer Ratte handelte, wäre es sinnvoll, die Probe so zu montieren, dass Tibia und Oberschenkelknochen aufrecht standen. Auf diese Weise würden die Röntgenstrahlen eine kurze Strecke passieren und es gäbe genügend Signal am Detektor. Das letzte, was bei der Montage einer Probe zu beachten ist Stabilität. Der größte Feind von Micro-CT ist bewegung. Wenn sich die Größe der Probenbewegung der Auflösung des Scans nähert, handelt es sich wahrscheinlich um nutzlose Daten. Die Bewegung sollte durch sichere Haftung an einer Halterung und mit Kontrolle über die Zusammensetzungsänderung der Probe eingeschränkt werden. Bei biologischen Proben bedeutet dies, dass sichergestellt wird, dass die Morphologie nicht durch Verdunstung über die Länge des Scans verändert wird. Die Suspension in Agarose-Gel oder die Umhüllung in einer dünnen Schicht Paraffinfolie sind beide mögliche Ansätze, um Austrocknung und Bewegung zu vermeiden.
Röntgenenergie wird auch einen großen Einfluss auf die Qualität des endgültigen 3D-Volumens haben. Ziel ist es, ein ausreichendes Signal am Detektor zu erfassen und dabei eine ausreichende Dämpfung von der Probe zu haben. Die Röntgendämpfung folgt Gleichung (1), wobei I die endgültige Anzahl der Zählungen (Intensität) ist, I0 die anfangse Anzahl der Zählungen, der Massenabsorptionskoeffizient, der für ein gegebenes Material und röntgenenergetisch (weit veröffentlicht) eindeutig ist, die Dichte des Materials und x die Röntgenweglänge ist.
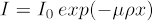 (1)
(1)
Idealerweise sollte i/I0 (auch bekannt als Übertragungswert) zwischen 5 - 95% für die gesamte Ausrichtung der Probe liegen, wobei die besten Ergebnisse im mittleren Bereich vorliegen. Um diesen Wert zu überprüfen, nehmen Sie ein Bild des Beispiels und dividieren Sie dann die Pixelwerte des Bildes durch ein Bild der Luft (d. h. mit dem Beispiel außerhalb des Sichtfelds). Diese Normalisierung findet sich häufig in Systemsoftware-Workflows. Es kommt nicht oft vor, dass biologische Proben die Verwendung von Röntgenfiltern an der Quelle verlangen, so dass dies hier nicht behandelt wird. Neben einem idealen Übertragungswert beträgt die ideale Anzahl der Zählungen für jeden Teil der Probe 5000 Zählungen. Um dies zu gewährleisten, muss möglicherweise die Belichtungszeit pro Projektion erhöht werden. Dadurch wird die Gesamteinscanzeit erhöht. Abbildung 1 zeigt saubere 2D-Projektionen.
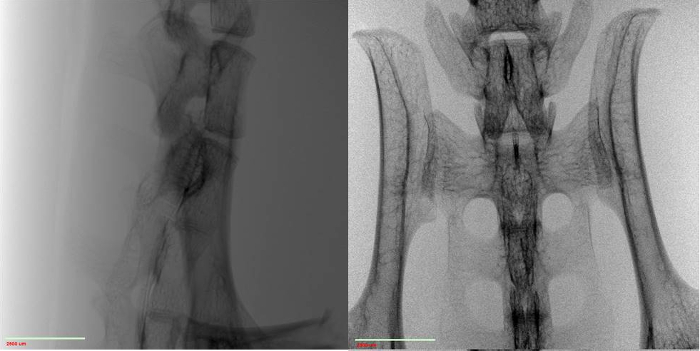
Abbildung 1: 2D-Bilder des Rückenmarks der Maus normalisiert gegen Luft bei 0° (links) und 90° (rechts).
Verfahren
1. Montage einer Probe (Bone)
- Zur Untersuchung eines Knochennetzes, wie einer Wirbelsäule, die Struktur in einem Agarosegel aufhängen und in einem sehr dünnwandigen Kunststoffrohr aushärten lassen (Abbildung 2). Die Dünne der Röhre ist sehr wichtig, was den Signaldurchsatz und die Gesamtbildqualität stark beeinträchtigt. Dies wiederum wirkt sich auf Ihre Fähigkeit zum Auflösen von Features aus. Der Transmissionswert der Röhre sollte so nahe wie möglich bei 100% liegen.
- Montieren Sie das Rohr auf der Probenbühne mit Klebeband oder durch einen benutzerdefinierten Ständer, um letztendlich sicherzustellen, dass die Probe stationär und stabil ist, wenn sich die Bühne dreht.

Abbildung 2: Mauswirbelsäule, die in Agarose-Gel in dünnwandigen Kunststoffrohren auf der Probenstufe des Mikro-CT-Systems hängen.
2. Bildaufnahme
- Schalten Sie die Röntgenquelle auf eine Energie im Bereich von 90 keV (90 kV und 10 W) ein.
- Nachdem sich die Quelle erwärmt und sich auf die Energie einlässt, erwerben Sie ein Bild über die Software des Systems.
- Überprüfen Sie den Übertragungswert, indem Sie das Bild mit einem Luftbild normalisieren. Stellen Sie für die automatische Referenzerfassung und -anwendung sicher, dass sich die Probe in eine bestimmte Richtung bewegen kann, ohne abzustürzen.
- Wenn das Bild zu hoch ist, senken Sie die Energie schrittweise, bis der Übertragungswert ausreicht. Achten Sie darauf, die Belichtungszeit entsprechend zu erhöhen, damit das Bild nicht laut und körnig erscheint. Wenn das Bild eine zu geringe Übertragung hat, erhöhen Sie die Energie schrittweise, bis der Übertragungswert ausreicht.
- Beginnen Sie, die Röntgenquelle näher an die Probe zu bewegen, während Sie sehr vorsichtig sind, sie nicht abzustürzen. Die Quelle so nah wie möglich an die Probe zu bringen, ist ein Schritt in Richtung der Maximierung des Durchsatzes und der Sicherstellung der bestmöglichen Auflösung.
- Verfeinern Sie dabei das Sichtfeld der Probe, indem Sie die Probenstufe mit ihren Linearantrieben verschieben.
- Die Software zeigt einen Parameter, der als Pixelgröße bekannt ist und der aktuellen Auflösung ähnlich behandelt wird (obwohl es in der Tat anders ist).
- Wenn die Zahl immer noch zu groß ist und die Quelle sehr nah ist, kann der Detektor beginnen, sich von der Probe zu entfernen.
- Wenn die Zahl zu klein ist, bewegen Sie den Detektor vorsichtig näher an die Probe.
- Probieren Sie verschiedene optische Objektive und Detektorpositionen aus, aber achten Sie auf die Komplikation, die dies bei der Optimierung der Scanparameter mit sich bringt.
- Überprüfen Sie jede Ausrichtung der Probe, um sicherzustellen, dass es keine Abstürze gibt, um die beste Belichtungszeit zu finden. Dies wird aufgrund der Änderung des Arbeitsabstands, der Pixelgröße und der Stichprobenposition durchgeführt.
- Drehen Sie die Probe langsam um 2-Grad-Schritte, während Sie ihre Position relativ zur Quelle und zum Detektor über die In-Cabinet-Kamera überwachen. Achten Sie darauf, die Quelle und den Detektor weg zu bewegen, wenn eine Kollision auftreten könnte.
- Finden Sie die längste Röntgenpfadlänge, die zu der niedrigsten Anzahl von Zählungen/Übertragungswerten führt, und finden Sie die Belichtungszeit, die erforderlich ist, um überall etwa 5000 Zählungen zu sichern.
3. Tomographie Einreichung und Rekonstruktion
Der Rekonstruktionsprozess aus Benutzersicht ist aus Benutzersicht nicht komplizierter als jede andere Parameterauswahl, die in den früheren Schritten getroffen wurde. Der Programmier- und Rechenaufwand für diesen Prozess ist jedoch recht erheblich. Benutzer müssen darauf abzielen, am besten zu verstehen, was unter der reibungslosen Software-Benutzeroberfläche geschieht und wie sich Entscheidungen auf das Endprodukt auswirken. Viele CT-Systeme verwenden iterative algebraische Rekonstruktionsalgorithmen, bei denen die 2D-Projektionen in eine Reihe linearer Gleichungen umgewandelt werden, die Pixelwerte beschreiben. Einige andere Systeme verwenden gefilterte Rückprojektionsalgorithmen, bei denen Radon-Transformationen die Projektionen in ein Sinogramm konvertieren und dann durch eine Reihe von Linienintegrationsoperationen geleitet werden. Natürlich verwenden einige andere Ansätze und sogar hybride Methoden. Auf der niedrigsten Ebene der Beteiligung an diesen Algorithmen ist bekannt, dass die Anzahl der Projektionen und die gesamte gedrehte Verschiebung einen Einfluss auf das endgültige rekonstruierte Volumen haben.
- Entscheiden Sie zunächst, ob sie basierend auf dem Seitenverhältnis der Probe über 180° oder 360° scannen möchten. Wenn die Probe ein hohes Seitenverhältnis hat, so dass die Röntgenweglänge bei der 90°-Ausrichtung etwa 4 oder mehr mal länger ist als die 0°-Ausrichtung als ein 180°-Scan, wäre eine kluge Wahl. (Das Argument ist, dass die Informationen, die auf der kurzen Röntgenpfadlänge gesammelt werden, nicht so unterschiedlich sind von einer Seite zur anderen. Wenn mehr Projektionen für die langen Röntgenpfadlängenausrichtungen vorgesehen werden können, als der Datensatz davon profitiert. Die Winkelverschiebung zwischen den Projektionen wird niedriger sein, und es werden mehr Informationen aus diesen kniffligen Ausrichtungen in die Rekonstruktionsalgorithmen eingespeist.) Wenn das Seitenverhältnis nicht so hoch ist, verwenden Sie 360°-Scans.
- Wählen Sie als Nächstes die Anzahl der Projektionen und die gesamte Winkelverschiebung aus, die den Winkel zwischen den Projektionen diktieren. Je kleiner dieser Winkel, desto weniger Interpolation wird durchgeführt und weniger feine Feature-Informationen abgeschnitten. (Es muss ein Gleichgewicht hergestellt werden, da mehr Projektionen eine längere Scanzeit bedeuten, was mit einem größeren Fenster korreliert, in dem sich Samples bewegen können, weniger Zeit zum Scannen anderer Dinge und eine kürzere Quelllebensdauer. Eine Faustregel ist, mindestens 800 Projektionen über 360° zu haben und 3200 Projektionen nicht zu überschreiten.
- Senden Sie den Scan.
- Nachdem die Tomographie beendet ist (in der Regel zwischen 4 - 16 Stunden), bringen Sie 2D-Serie von Bildern in das System (oder einige Open-Source) Rekonstruktionssoftware.
- Wählen Sie die optimale Mittelschichtkorrektur aus. Center Shift ist ein Parameter, der die Projekte so ausrichtet, dass sie sich ansieden (denken Sie an ein grob gemischtes Kartenspiel, das gesammelt und ausgerichtet werden muss, um wie ein ordentlicher Stapel zu sitzen). Dieser Wert liegt in der Regel irgendwo zwischen -10 bis 10 Pixeln.
- Wählen Sie den optimalen Strahlhärtekorrekturkoeffizienten aus. Die Strahlhärtekorrektur ist eine künstliche Entfernung des Kontrasts, der durch Probenfilterung erzeugt wird. Wenn eine Probe dick genug ist oder eine Reihe von leichten und schweren Materialien enthält, hat sie einen falschen Kontrast basierend auf der Dämpfung von energiearmen (weichen) Röntgenstrahlen. Dies sollte konservativ angewendet werden. Ein Durchschnittswert liegt irgendwo zwischen 0 - 0,5.
- Reichen Sie die Rekonstruktion ein.
Ergebnisse
Die folgenden Bilder geben einen Überblick über die Ergebnisse, die aus der Verwendung von Micro-CT mit dem oben genannten Verfahren gewonnen werden können. Qualitative Messungen an unterschiedlicher Absorption können anhand dieser Bilder direkt festgestellt werden. Quantitative Daten wie Materialporosität, Feature-Größe und -Verteilung usw. erfordern eine zusätzliche Bildverarbeitung in einer anderen Software.
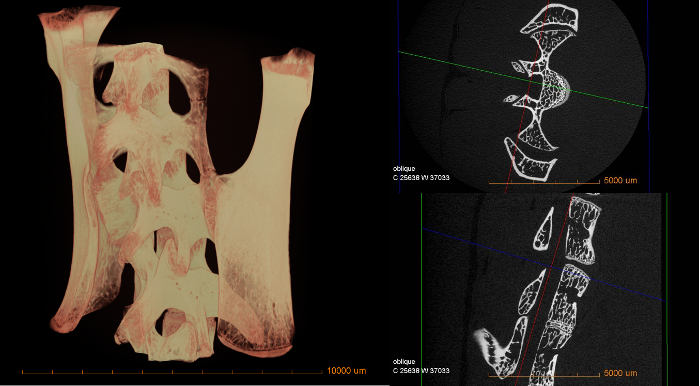
Abbildung 3: 3D-Volumen des Rückenmarks der Maus (links) und zwei digitale Querschnittsscheiben (rechts)
Anwendung und Zusammenfassung
In diesem Experiment wurden die vielen Faktoren untersucht, die bei der Verwendung von Mikro-CT, insbesondere für eine biologische Probe, berücksichtigt werden sollten. Dieses Projekt wurde entwickelt, um dem Prüfer zu helfen, zu verstehen, wie sich seine Entscheidungen auf die Daten auswirken werden, die Micro-CT liefern kann. Wie gezeigt, gibt es viele abhängige und empfindliche Parameter, die berücksichtigt werden sollten, einschließlich: Montage, Röntgenenergie, Belichtungszeit, Quellen- und Detektorpositionierung, Anzahl der Projektionen und gesamtscanische Winkelverschiebung. Diese Übung ist als Einführung gedacht und kratzt nur an der Oberfläche der Kontrolle über einen CT-Datensatz.
Dieses Experiment konzentrierte sich auf eine Einführung in micro-CT in Bezug auf die Bildgebung einer biologischen Probe, aber die Anwendung der 3D-Röntgentomographie erstreckt sich auf die Welten der Mikroelektronik, Geologie, additiveHerstellung, Beschichtungen, Brennstoffzellen und vieles mehr . Diese Mikroskope werden für Inspektionen, Fehleranalysen, Charakterisierungen, Qualitätskontrolle und sogar zerstörungsfreie Prüfungen eingesetzt. Da reale 3D-Informationen nun zerstörungsfrei zugänglich sind, können die aus CT extrahierten Geometrien in Simulationen importiert werden, in denen Objekte virtuell getestet werden können.
pringen zu...
Videos aus dieser Sammlung:

Now Playing
Mikro-CT-Bildgebung von Maus-Rückenmark
Biomedical Engineering
8.3K Ansichten

Bildgebung biologischer Proben mit optischer und konfokaler Mikroskopie
Biomedical Engineering
36.3K Ansichten

SEM-Bildgebung biologischer Proben
Biomedical Engineering
24.1K Ansichten

Biodistribution von Nano-Wirkstoffträgern: Anwendungen von SEM
Biomedical Engineering
9.6K Ansichten

Hochfrequenz-Ultraschall-Bildgebung der Bauchaorta
Biomedical Engineering
14.8K Ansichten

Abbildung der Dehnungsbelastung eines Bauchaortenaneurysmas
Biomedical Engineering
4.6K Ansichten

Photoakustische Tomographie zur Darstellung von Blut und Lipiden in der infrarenalen Aorta
Biomedical Engineering
5.9K Ansichten

Kardiale Magnetresonanztomographie
Biomedical Engineering
15.0K Ansichten

Numerische Strömungsmechaniksimulationen des Blutflusses in einem zerebralen Aneurysma
Biomedical Engineering
12.0K Ansichten

Nahinfrarot-Fluoreszenz-Bildgebung von Abdominalaortenaneurysmen
Biomedical Engineering
8.4K Ansichten

Nichtinvasive Blutdruckmesstechniken
Biomedical Engineering
12.1K Ansichten

Erfassung und Analyse eines EKG-Signals (Elektrokardiographie)
Biomedical Engineering
107.1K Ansichten

Zugfestigkeit resorbierbarer Biomaterialien
Biomedical Engineering
7.7K Ansichten

Visualisierung der Kniegelenksdegeneration nach nicht-invasiver Kreuzbandverletzung bei Ratten
Biomedical Engineering
8.3K Ansichten

Kombinierte SPECT- und CT-Bildgebung zur Visualisierung der Herzfunktionalität
Biomedical Engineering
11.2K Ansichten
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten