Zugfestigkeit resorbierbarer Biomaterialien
Quelle: Peiman Shahbeigi-Roodposhti und Sina Shahbazmohamadi, Biomedical Engineering Department, University of Connecticut, Storrs, Connecticut
Seit über 4000 Jahren werden Nähte als medizinische Intervention verwendet. Die frühesten Aufzeichnungen deuten darauf hin, dass Leinen das Biomaterial der Wahl war. Catgut, das heute noch in Gebrauch ist, wurde Berichten zufolge um 150 n. Chr. zur Behandlung von Gladiatoren verwendet. Heute gibt es zahlreiche Materialien, die für Nähte verwendet werden. Nähte werden nach ihrer Zusammensetzung (natürlich oder synthetisch) und ihrer Absorption (nicht resorbierbar oder resorbierbar) klassifiziert.
Resorbierbare (oder resorbierbare) Nähte verschlechtern sich im Körper entweder durch enzymatischen Abbau oder programmierten Abbau, der durch die Wechselwirkung von Wasser mit bestimmten Gruppen in der Polymerkette verursacht wird. Diese Nähte werden oft aus synthetischen Materialien wie Polyglykolsäure, Polydioxanon und Polycaprolacton oder natürlichen Biomaterialien wie Seide hergestellt. Sie werden in der Regel für bestimmte interne Verfahren verwendet, wie allgemeine Chirurgie. Resorbierbare Nähte halten die Wunde für einen Zeitrahmen zusammen, der lang genug für die Heilung ist, aber dann zerfallen sie schließlich durch den Körper. Auf der anderen Seite, nicht resorbierbaren Nähte nicht abbauen und müssen extrahiert werden. Sie werden in der Regel aus Polypropylen, Nylon und Edelstahl hergestellt. Diese Nähte werden in der Regel für orthopädische und Herzchirurgie implementiert und erfordern einen Arzt, um sie zu einem späteren Zeitpunkt zu entfernen.
Hierbei wird die Zugfestigkeit von zwei Arten von resorbierbaren Nähten getestet, nachdem sie neutralen, sauren und alkalischen Lösungen aussetzt wurden, die den unterschiedlichen pH-Umgebungen im menschlichen Körper entsprechen. Der Test besteht aus zwei Teilen. Zunächst werden Kontrollproben mittels Zugprüfung vorbereitet und analysiert. Anschließend werden die Proben nach der kontinuierlichen Exposition gegenüber Lösungen unterschiedlicher pH-Wert über mehrere Wochen getestet.
Der Materialabbau beschreibt den Leistungsverlust und die Veränderung der Materialeigenschaften, z. B. Zugfestigkeit, Farbe und Form, nach Der in Beziehung zu einem oder mehreren Umgebungsfaktoren. Zu diesen Faktoren gehören Hitze, Licht, mechanische Kräfte oder chemische Exposition, wie Säuren, Laugen oder Salze. Eine Möglichkeit, den Abbau zu kontrollieren, ist die Oberflächentechnik. Dies wird durch Abschirmung einer Oberfläche mit einer Schutzschicht oder durch Änderung des Materials selbst, z. B. durch Vernetzung, erreicht.
Hier bei einem Kraftaufnehmer werden Proben kommerziell erhältlicher Proben in einer Prüfmaschine getestet. Die Proben werden sicher in die Klemmen der Prüfmaschine (UTM) gelegt, die UTM ist auf Null gesetzt und eine Verdrängungsgeschwindigkeit von 6 mm/min wird bis zum Ausfall eingeleitet. Nach dem Ausfall wird die Spitzenkraft aufgezeichnet. Das experimentelle Design ist in der Abbildung unten dargestellt.
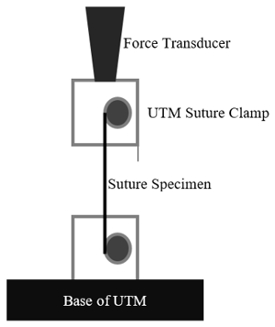
Abbildung 1: Experimentelles Design.
In diesem Experiment werden zwei resorbierbare Nähte verwendet: Polyglyconat-Nähte und Polydioxanon-Nähte. Synthetische Polyglyconat-Nähte werden aus einer Reaktion hergestellt, die Glyolilid und Trimethylencarbonat erfordert. Bei der Bildung von Poly(Glyolid-Co-Trimethylencarbonat) werden sie polymerisiert. Diese Polyglykode haben eine lineare Struktur von (C8H10O7)n, die unten in Abbildung 2 dargestellt ist. Auf der anderen Seite werden PDS II Violet Monofilament Nähte aus Polydioxanon-Polymeren mit einer linearen Struktur von (C4H6O3)nsynthetisiert. Polydioxanon ist unten in Abbildung 3 dargestellt.
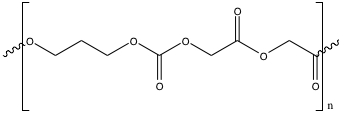
Abbildung 2: Poly (Glykolid-Co-Trimethylencarbonat) zur Polymerisation von Polyglyconat-Nähten.
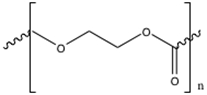
Abbildung 3: Polydioxanon zur Polymerisation von Nähten.
Beide Nähte folgen Hydrolysereaktionen durch den Abbauprozess. Bei Polyglykolid tritt eine zweistufige Hydrolyse auf. Zunächst wird das Polymer durch Spaltung seiner inneren Esterbindungen zunächst in sein Monomer (Glykolsäure) umgewandelt. Dann tritt ein hydrolytischer Angriff auf die kristallinen Teile des Polymers auf. Wenn sich die kristallinen Regionen auflösen, bricht das Polymer zusammen. Ebenso werden Polydioxanon-Nähte sicher durch den Ester-Radikal abgebaut. Die abgebauten Verbindungen aus beiden Nahttypen sind ungiftig und sicher durch Wasserlassen oder Ausatmen abgesondert.
Im Laufe der Zeit wird die Lösung sauer, aufgrund der erhöhten Präsenz von Hydroxylionen. Aus den Enden der degradierten Monomere werden Carbonsäureradikale erzeugt, die den pH-Wert der umgebenden Lösung senken. Jüngste Studien haben gezeigt, dass Polyglykolid- und Polydioxanonstrukturen in vivo schneller abbauen als in vitro, die durch zelluläre enzymatische Aktivität 2 angetriebenwerden. Wirkungen aufgrund des Vorhandenseins biologischer Enzyme werden während dieses In-vitro-Verfahrens nicht beobachtet.
1. Probenvorbereitung
- Erstellen Sie sechs Etiketten mit den folgenden Informationen, und befestigen Sie die Etiketten an Schraub-Top-Reagenzgläsern.
- Datum: Monat und Tag
- Probentyp: Polyglyconat oder Polydioxanon
- Lösungstyp: saure (A), alkalische (B) oder neutrale (N) Lösung mit pH-Wert zwischen 2-14.
- Öffnen Sie die Nahtverpackung und entfernen Sie die Naht. Schneiden Sie die Nadel ab und entsorgen Sie sie in den scharfen Behälter.
- Schneiden Sie die Naht in 3 Stücke, die etwa 10-12 in lang sind.
- Beachten Sie die Farbe und die physikalischen Eigenschaften der Naht.
- Verwenden Sie einen Bremssattel, um den Durchmesser jeder Naht zu messen.
- Wägen Sie jede Naht und legen Sie eine Probe in jedes Reagenzglas.
- Füllen Sie die Reagenzgläser mit der Aufschrift "N" mit genügend entionisiertem Wasser, um die Naht zu bedecken, und verschließen Sie dann die Reagenzgläser.
- Verwenden Sie eine Pipette, um die Reagenzgläser mit der Aufschrift "A" mit einer ausreichenden 0,001 M HCl-Lösung zu füllen, um die Naht zu bedecken. Denken Sie daran, die Reagenzgläser zu verkappen.
- Verwenden Sie eine Pipette, um die Reagenzgläser mit der Bezeichnung "B" mit genügend 0,001 M NaOH-Lösung zu füllen, um die Naht zu bedecken. Denken Sie daran, die Reagenzgläser zu verkappen.
- Legen Sie alle sechs Reagenzgläser im Metallregal bei 37 oC in einen Ofen.
2. Kontrolle Probe Zugprüfung
- Besorgen Sie sich eine frische Naht, die Kontrollprobe, und legen Sie sie in die Halterung des UTM und sichern Sie sie an Ort und Stelle.
- Vor dem Beginn der Spannung auf der Probe, Null die UTM durch Drücken der F1 (Null Kraft) und F2 (Null ext) Tasten. Zeichnen Sie die Einstellung für die Verschiebungsgeschwindigkeit auf dem Datenblatt auf.
- Stellen Sie sicher, dass die Spitzenhaltegriffe auf dem UTM-Display angezeigt wird.
- Starten Sie das UTM, indem Sie die Pfeiltaste nach oben drücken. Die Kraft und Verschiebung beginnt sich auf dem UTM zu ändern.
- Laden Sie die Probe bis zum Ausfall. Beenden Sie dann das UTM.
- Zeichnen Sie die Spitzenkraft von der UTM-Anzeige auf.
3. Stärkeverlust Profil
- Entfernen Sie eine der Proben (A, B, & N) jede Woche für fünf Wochen aus dem Ofen.
- Messen Sie den pH-Wert der Lösung im Reagenzglas mit pH-Papier.
- Spülen Sie die Naht mit entionisiertem Wasser, und notieren Sie alle physikalischen oder Farbänderungen am Material in jeder Probe.
- Bei Bedarf die Probe mit einem Papiertuch trocken klopfen.
- Wägen Sie jede Probe und zeichnen Sie das neue Gewicht auf
- Legen Sie das Exemplar in die Griffe des UTM und verriegeln Sie es.
- Vor dem Beginn der Spannung auf der Probe, Null die UTM durch Drücken der F1 (Null Kraft) und F2 (Null ext) Tasten.
- Stellen Sie sicher, dass die Spitzenhaltetaste auf dem UTM-Display angezeigt wird, und stellen Sie sicher, dass die Verschiebungsgeschwindigkeit auf dem UTM mit der beim Testen des Steuerbeispiels identisch ist.
- Laden Sie die Probe bis zum Ausfall. Beenden Sie dann das UTM.
- Zeichnen Sie die Spitzenkraft bei einem Ausfall von der UTM-Anzeige auf.
Im Laufe von fünf Wochen wurden alle behandelten Proben getestet und analysiert. Aus den Gesamtversuchen wurden die durchschnittlichen Zugfestigkeiten anhand von Gleichung 1 berechnet:
 (1)
(1)
Die Standardabweichungen aller Fehlerkräfte in Bezug auf Nahttyp und Lösungsumgebung wurden ebenfalls berechnet. Schließlich wurde die beibehaltene Perzentfestigkeit anhand der durchschnittlichen Zugfestigkeit bestimmt. Im Folgenden finden Sie die Diagramme mit repräsentativen Ergebnissen.
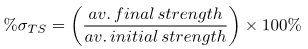 (2)
(2)
Das durchschnittliche Festigkeitsverlustprofil für die Polyglyconat-Nähte über alle pH-Bereiche lag in den ersten vier Wochen bei 81 %, 76 %, 66 % bzw. 54 %. In den ersten vier Wochen des Experiments ist dieses Profil fast identisch mit den Herstellerangaben für diese Nähte. Es ist auch offensichtlich, dass das ursprüngliche Polyglyconat-Profil etwas schneller abnimmt als die experimentellen In-vitro-Nähte. Dies wird auf die Tatsache zurückgeführt, dass der Hersteller In-vivo-Tests durchgeführt hat, bei denen Faktoren wie enzymatische Degradation vorhanden waren. Das Vorhandensein biologischer Enzyme kann die Abbaurate und Reabsorption von Biomaterialien erheblich erhöhen. In-vivo-Tests unterziehen die Probe verschiedenen Belastungen und biochemischen Wechselwirkungen, die in vitro-Verfahren fehlen. In-vivo-Tests werden im Allgemeinen gegenüber In-vitro-Tests bevorzugt, da sie die Beobachtung der Gesamtwirkungen eines Experiments auf ein lebendes Subjekt ermöglichen.

Abbildung 4: Saure Lösung: Nahtzugfestigkeit.

Abbildung 5: Neutrale Lösung, Nahtzugfestigkeit.

Abbildung 6: Alkalische Lösung, Nahtzugfestigkeit.
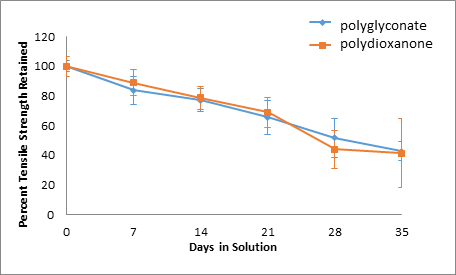
Abbildung 7: Säurelösung, Perzentilzugfestigkeit beibehalten.
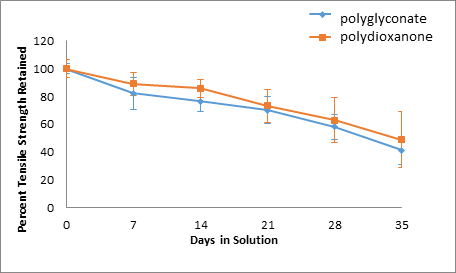
Abbildung 8: Neutrale Lösung, prozentuale Zugfestigkeit beibehalten.
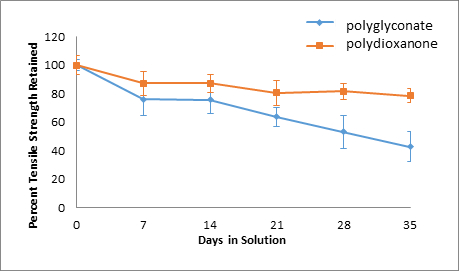
Abbildung 9: Basislösung, Prozentuale Zugfestigkeit beibehalten.
| Steuerung | 7 Tage | 14 Tage | ||||||
| Durchschnittlicher pH-Wert | Durchschnittlicher pH-Wert | Durchschnittlicher pH-Wert | ||||||
| N/A | Säure | Neutral | Basis | Säure | Neutral | Basis | ||
| 5 | 6 | 8 | 4 | 6 | 9 | |||
| Kraft (N) | Kraft (N) | Kraft (N) | ||||||
| 93.63 | 83.67 | 85.67 | 78.40 | 74.63 | 83.53 | 78.40 | ||
| 102.07 | 98.53 | 93.50 | 82.77 | 71.73 | 77.30 | 80.83 | ||
| 101.43 | 78.13 | 81.03 | 86.77 | 75.08 | 81.73 | 80.33 | ||
| 97.80 | 79.50 | 75.73 | 82.40 | 76.50 | 74.67 | 81.17 | ||
| 86.43 | 79.93 | 81.63 | 75.33 | 67.00 | 87.10 | 94.80 | ||
| 94.23 | 96.80 | 98.07 | 89.27 | 91.43 | 87.47 | |||
| 21 Tage | 28 Tage | 35 Tage | ||||||
| Durchschnittlicher pH-Wert | Durchschnittlicher pH-Wert | Durchschnittlicher pH-Wert | ||||||
| Säure | Neutral | Basis | Säure | Neutral | Basis | Säure | Neutral | Basis |
| 4 | 6 | 9 | 4 | 6 | 8 | 4 | 6 | 8 |
| Kraft (N) | Kraft (N) | Kraft (N) | ||||||
| 56.53 | 58.70 | 85.97 | 51.53 | 58.57 | 73.22 | 36.37 | 38.77 | 74.67 |
| 60.73 | 65.33 | 75.80 | 49.70 | 51.43 | 72.20 | 24.20 | 34.83 | 67.70 |
| 58.27 | 63.53 | 69.23 | 56.87 | 72.20 | 83.20 | 36.30 | 42.37 | 73.27 |
| 64.93 | 66.83 | 81.60 | 40.63 | 28.40 | 72.90 | 21.60 | 36.83 | 74.63 |
| 68.57 | 63.90 | 81.90 | 29.70 | 58.70 | 80.93 | 42.00 | 40.97 | 75.67 |
| 75.20 | 76.17 | 61.63 | 20.83 | 69.47 | 83.33 | 31.37 | 45.33 | 81.77 |
| 85.63 | 94.17 | 85.00 | 36.37 | 78.13 | 76.73 | 87.53 | 90.77 | 81.83 |
| 60.33 | 75.83 | 80.47 | 52.33 | 66.67 | 85.83 | |||
Tabelle 1: Insgesamt 5-Wochen-Polydioxanon-Suture-Daten, Kräfte bei Ausfall
| Steuerung | 7 Tage | 14 Tage | ||||||
| Durchschnittlicher pH-Wert | Durchschnittlicher pH-Wert | Durchschnittlicher pH-Wert | ||||||
| N/A | Säure | Neutral | Basis | Säure | Neutral | Basis | ||
| 4 | 6 | 9 | 4 | 6 | 9 | |||
| Kraft (N) | Kraft (N) | Kraft (N) | ||||||
| 170.80 | 131.37 | 147.03 | 146.23 | 122.07 | 117.87 | 135.17 | ||
| 170.93 | 147.70 | 142.60 | 152.63 | 129.30 | 132.13 | 129.87 | ||
| 167.70 | 134.00 | 153.80 | 120.13 | 107.93 | 113.13 | 101.57 | ||
| 162.37 | 112.90 | 102.87 | 111.07 | 139.63 | 120.47 | 111.20 | ||
| 156.70 | 153.20 | 124.63 | 103.80 | 123.80 | 131.47 | 129.57 | ||
| 152.87 | 145.90 | 123.33 | 143.57 | 146.13 | 144.57 | |||
| 21 Tage | 28 Tage | 35 Tage | ||||||
| Durchschnittlicher pH-Wert | Durchschnittlicher pH-Wert | Durchschnittlicher pH-Wert | ||||||
| Säure | Neutral | Basis | Säure | Neutral | Basis | Säure | Neutral | Basis |
| 4 | 6 | 8 | 4 | 6 | 8 | 4 | 5 | 7 |
| Kraft (N) | Kraft (N) | Kraft (N) | ||||||
| 110.63 | 109.13 | 115.27 | 93.67 | 93.40 | 74.57 | 50.43 | 54.03 | 44.80 |
| 115.10 | 113.13 | 87.90 | 75.40 | 100.50 | 77.93 | 82.47 | 78.67 | 78.70 |
| 120.50 | 128.93 | 116.37 | 111.43 | 108.00 | 109.73 | 80.47 | 42.83 | 80.20 |
| 114.03 | 116.43 | 101.03 | 84.23 | 87.17 | 80.10 | 69.40 | 81.13 | 77.10 |
| 118.83 | 110.93 | 107.43 | 51.47 | 66.90 | 81.60 | 68.70 | 81.50 | 46.97 |
| 78.33 | 87.90 | 115.57 | 59.87 | 93.77 | 61.07 | 76.87 | 82.73 | 82.53 |
| 131.20 | 141.07 | 107.83 | 105.60 | 111.73 | 112.21 | 68.00 | 57.27 | 86.23 |
| 80.47 | 122.70 | 91.67 | 103.67 | 110.10 | 105.67 | |||
Tabelle 2: Insgesamt 5-Wochen-Polyglyconat-Suture-Daten, Kräfte bei Ausfall
Im Laufe der Zeit verringerten sich die Zugfestigkeiten aller Nahtproben. Darüber hinaus war bei Polydioxanon-Nähten eine saure Umgebung am schädlichsten, da nur 41,46 % der ursprünglichen Zugfestigkeit beibehalten wurden, während 78,58 % und 48,95 % der ursprünglichen Zugfestigkeit für Polydioxanon-Nähte in Alkali- und neutralen Lösungen. Auf der anderen Seite waren die Festigkeitsretentionsprozentsätze im Laufe der Zeit für Polyglyconat-Nähte über verschiedene pH-Lösungen alle ähnlich. Die größte Abnahme der Zugfestigkeit der Polyglyconatnähte wurde in einer neutralen Umgebung beobachtet, in der nur 41,22 % der ursprünglichen Festigkeit beibehalten wurden. In sauren und alkalischen Umgebungen wurden 42,79 % bzw. 42,81 % der ursprünglichen Zugfestigkeit für die Polyglyconatnähte beibehalten.
Wenn die Nähte bei einer höheren Temperatur inkubiert worden wären, wären sie aufgrund der erhöhten inhärenten Energie, die im System gefunden wird, schneller abgebaut worden. Dies würde eine spontanere Depolymerisation in Monomere ermöglichen. Mit anderen Worten, wenn die Temperatur steigt, wird die Zugfestigkeit negativ beeinflusst. Darüber hinaus, wenn die Nähte bei konstantem Stress gehalten wurden, würde die Wahrscheinlichkeit des Zerfalls auch erhöhen. Dies wäre auf Kriechverformung zurückzuführen; Dehnung der Nähte schafft schwächere Gebietsschemas, die für die Absorption prim sind. Wenn die Nähte in Knoten gebunden werden, würde ein ähnliches Szenario auftreten.
In diesem Experiment wurde die Zugfestigkeit von Nähten in verschiedenen pH-Umgebungen bewertet. Über fünf Wochen wurden die Zugfestigkeiten von zwei verschiedenen Arten von Nähten nach der Exposition gegenüber sauren, alkalischen und neutralen Lösungen untersucht. Die Ergebnisse deuten mit überwältigender Mehrheit darauf hin, dass bioresorbierbare Nähte im Laufe der Zeit in jeder pH-Umgebung abgebaut werden.
Obwohl die Polyglyconat-Nähte schneller abgebaut werden, bleiben die im Vergleich zu den Polydioxanon-Nähten stärker. Die experimentellen Ergebnisse zeigen auch, dass Polydioxanon-Nähte in längeren Zeitrahmen mehr von ihrer Festigkeit behalten als die Polyglyconat-Nähte, da die schnellere Abbaurate von Polyglyozatnähten deutlicher wird. Da das Experiment jedoch in vitrodurchgeführt wurde, können keine wesentlichen Schlussfolgerungen für die Wirksamkeit der Polyglyconat- oder Polydioxanon-Nähte in einem aktiveren biochemischen Modell gezogen werden. Enzymatische Degradation ist ein kritischer Aspekt, der berücksichtigt werden muss. Unabhängig davon sind beide Nähte praktikable Kandidaten für chirurgische Eingriffe. Diese Studie bestätigt die Bedeutung dieser Art von Forschung.
Resorbierbare Nähte bieten vorübergehende Wundunterstützung, so dass die Wunde gut genug heilen kann, um normalen Kräften standzuhalten. Im Allgemeinen werden resorbierbare Nähte für interne Eingriffe verwendet, so dass zusätzliche chirurgische Eingriffe für die Nahtentfernung nicht erforderlich wären. Nach dem Zerfall sind von der Naht kaum spurenspuren übrig. Resorbierbare Nähte werden auch bei Patienten verwendet, die nicht für eine Nahtentfernung summieren können. Auf der anderen Seite werden nicht resorbierbare Nähte häufig in epidermalen würde Verschluss verwendet, wo die Nähte leicht nach einer bestimmten Zeit entfernt werden können. Darüber hinaus werden nicht resorbierbare Nähte häufig auch in stressigen internen Umgebungen verwendet, wenn resorbierbare Nähte nicht in der Lage sind, genügend Wundunterstützung zu bieten. Interne Strukturen wie das Herz, die unterschiedlichen Drücken und Bewegungen konsequent standhalten, erfordern nicht resorbierbare Nähte. Weitere Anwendungen von nicht resorbierbaren Nähten sind orthopädische Operationen und Sternverschluss in Herzoperationen. Da resorbierbare Nähte in inneren und kritischeren Teilen des Körpers verwendet werden, ist es wichtig, ihre Festigkeit zu testen und die Produktqualität zu analysieren.
Materialliste
| Namen | Unternehmen | Katalognummer | Kommentare |
| Ausrüstung | |||
| Naht | |||
| Lineal | |||
| Schere | |||
| Bremssättel | |||
| Pinzette | |||
| Skala | |||
| Tinius Olsen Tester | |||
| Ofen | |||
| Beispielbehälter | |||
| Becher | |||
| Pipette | |||
| Pipettenfüller | |||
| Pipettenrohr | |||
| Glas | |||
| Chemikalien | |||
| Entionisiertes Wasser | |||
| Salzsäure (HCL) | |||
| Natriumhydroxid (NaOH) |
- Wise, Donald L., et al. Encyclopedic Handbook of Biomaterials and Bioengineering. Marcel Dekker, Inc., New York. 1995. 567-569.
- Dattilo, P.P., King, M.W., Cassill, N.L., et al. Medical Textiles: Application of an Absorbable Barbed Bi-directional Surgical Suture. J. Text. & App., Tech. & Mgmt. 2002, 2, 1
pringen zu...
Videos aus dieser Sammlung:

Now Playing
Zugfestigkeit resorbierbarer Biomaterialien
Biomedical Engineering
7.5K Ansichten

Bildgebung biologischer Proben mit optischer und konfokaler Mikroskopie
Biomedical Engineering
35.7K Ansichten

SEM-Bildgebung biologischer Proben
Biomedical Engineering
23.5K Ansichten

Biodistribution von Nano-Wirkstoffträgern: Anwendungen von SEM
Biomedical Engineering
9.3K Ansichten

Hochfrequenz-Ultraschall-Bildgebung der Bauchaorta
Biomedical Engineering
14.4K Ansichten

Abbildung der Dehnungsbelastung eines Bauchaortenaneurysmas
Biomedical Engineering
4.6K Ansichten

Photoakustische Tomographie zur Darstellung von Blut und Lipiden in der infrarenalen Aorta
Biomedical Engineering
5.7K Ansichten

Kardiale Magnetresonanztomographie
Biomedical Engineering
14.7K Ansichten

Numerische Strömungsmechaniksimulationen des Blutflusses in einem zerebralen Aneurysma
Biomedical Engineering
11.7K Ansichten

Nahinfrarot-Fluoreszenz-Bildgebung von Abdominalaortenaneurysmen
Biomedical Engineering
8.2K Ansichten

Nichtinvasive Blutdruckmesstechniken
Biomedical Engineering
11.9K Ansichten

Erfassung und Analyse eines EKG-Signals (Elektrokardiographie)
Biomedical Engineering
104.8K Ansichten

Mikro-CT-Bildgebung von Maus-Rückenmark
Biomedical Engineering
8.0K Ansichten

Visualisierung der Kniegelenksdegeneration nach nicht-invasiver Kreuzbandverletzung bei Ratten
Biomedical Engineering
8.2K Ansichten

Kombinierte SPECT- und CT-Bildgebung zur Visualisierung der Herzfunktionalität
Biomedical Engineering
11.0K Ansichten
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten