Method Article
تطبيق استئصال الطحال الجزئي بالمنظار مع انسداد تدفق الدم الكلي في آفات الطحال الحميدة
In This Article
Summary
في هذه الدراسة ، نصف تقنية التحكم في النزيف أثناء الجراحة لاستئصال الطحال الجزئي بالمنظار ، مما يحسن سلامة ودقة استئصال الطحال.
Abstract
أصبح استئصال الطحال الجزئي بالمنظار (LPS) تدريجيا الطريقة المفضلة لعلاج آفات الطحال الحميدة. ومع ذلك ، نظرا لوفرة إمدادات الدم وملمسها الناعم والهش ، خاصة عندما تكون الآفة بالقرب من نقير الطحال أو تكون كبيرة بشكل خاص ، فإن إجراء استئصال الطحال الجزئي (PS) في الممارسة السريرية يمثل تحديا كبيرا. لذلك ، كنا نستكشف باستمرار ونقوم بتحسين طرق التحكم في النزيف أثناء PS ، ونقترح هنا طريقة لإجراء LPS مع انسداد تدفق الدم الكامل في الطحال.
تصف هذه الدراسة نهجا محسنا للسيطرة على النزيف أثناء الجراحة أثناء LPS. أولا ، يتضمن تشريحا شاملا لأربطة الطحال والفصل الدقيق لذيل البنكرياس عن الطحال. مع التعرض الكامل للنقير الطحال ، نقوم مؤقتا بإغلاق إمدادات الدم بالكامل من الطحال باستخدام مشبك بولدوج بالمنظار. بعد ذلك ، نستخدم الموجات فوق الصوتية أثناء الجراحة لتحديد حدود الآفة واستئصال الجزء المقابل من الطحال تحت التحكم الكامل في تدفق الدم. يجسد هذا النهج جوهر "الحفاظ على الطحال" من خلال التحكم الفعال في النزيف والاستئصال الدقيق. إنه مناسب بشكل خاص للجراحة بالمنظار ويستحق مزيدا من التعزيز السريري.
Introduction
من خلال الفهم العميق للوظائف الفسيولوجية للطحال ، يؤكد البحث على دوره المحوري في الاستجابة المناعية للجسم ، وتكون الدم ، وإزالة خلايا الدمالحمراء 1. تؤثر المضاعفات التي تلي استئصال الطحال ، مثل التهابات ما بعد استئصال الطحال الشديدة (OPSIs) ، وارتفاع ضغط الدم الرئوي ، والجلطات الدموية ، بشكل كبير على اختيار الطرق الجراحية في الممارسة السريرية2،3. وفقا للأدبيات ، يظهر المرضى بعد استئصال الطحال الكلي قدرة منخفضة على التخلص من كرات الدم الحمراء المتطفلة من الملاريا وزيادة خطر الإصابة بالتهاب السحايا والإنتان بعد العدوى بالمكورات العقدية الرئوية والنيسرية السحائية والمستدمية النزلية من النوعB 4. يحافظ PS على وظيفة الطحال مع ضمان فعالية العلاج ، مما يجعله مطبقا على نطاق واسع في الممارسة السريرية.
في عام 1959 ، تم الإبلاغ عن أول PS ناجح بواسطة Cristo5. الطحال هو عضو هش يتكون من أجزاء طحال محددة جيدا ، لكل منها إمدادات شريانية وريدية مميزة ، محددة بمناطق لاوعائية نسبيا6. تؤسس هذه العوامل مجتمعة الأساس التشريحي ل PS. ومع ذلك ، فإن الجراحة المفتوحة التقليدية تحمل عيوبا متأصلة ، بما في ذلك الصدمات الكبيرة والعيوب التجميلية وآلام ما بعد الجراحة. في السنوات الأخيرة ، إلى جانب نضوج الأدوات والتقنيات بالمنظار ، برز LPS كطريقة علاجية مفضلة لآفات الطحال الحميدة. ومع ذلك ، نظرا لإمدادات الدم الغنية بالطحال ، قد يتسبب النزيف الكبير أثناء الجراحة أثناء تنظير البطن في التحول إلى جراحة مفتوحة. رومبولي وآخرون استعرض 457 حالة من LPS ، وكشفوا عن متوسط وقت الجراحة يبلغ حوالي 128 ± 43.7 دقيقة ، وأظهروا أن حوالي 3.9٪ من المرضى يحتاجون إلى التحويل بسبب النزيف ، ومتوسط الإقامة بعد الجراحة هو 4.9 ± 3.8 يوما7. أعاقت المعرفة الشاملة بتشريح الطحال والمهارات الجراحية الدقيقة التطبيق السريري الواسع ل LPS.
للتخفيف من مخاطر النزيف أثناء الجراحة وتسريع منحنى التعلم ، نحاول إجراء LPS مع انسداد تدفق الدم بالكامل. في هذه الدراسة ، نقدم مريضة تبلغ من العمر 72 عاما مصابة بورم وعائي طحالي ضخم يقع في القطب الأوسط العلوي للطحال وبجوار نقير الطحال. تتفوق هذه التقنية الجديدة في التحكم الفعال في النزيف وتضمن السلامة والفعالية ومستوى عال من التكاثر.
Protocol
تتبع هذه الدراسة إرشادات لجنة الأخلاقيات في مستشفى شوندي بالجامعة الطبية الجنوبية. تم الحصول على موافقة مستنيرة من المريض قبل الجراحة على البيانات والفيديو.
1. اختيار المريض
- تطبيق هذه الطريقة الجراحية في الحالات التالية:
- قم بتضمين المرضى الذين يعانون من آلام أو عدم الراحة في البطن ، إلى جانب الفحوصات الإشعاعية التي تؤكد وجود آفات حميدة.
- لا تفرض قيودا محددة على حجم الورم ، ولكن حافظ على حجم الطحال المتبقي يتجاوز 25٪.
- تأكد من أن المرضى يظهرون مستويات طبيعية من AFP و CEA و CA-199 أو تأكيد عدم وجود ورم خبيث.
- ضع في اعتبارك السمنة ، التي تؤدي إلى زيادة الدهون الحشوية التي يحتمل أن تؤثر على التشريح أثناء الجراحة ، لكنها لا تعتبرها قيدا مطلقا.
- استبعاد المرضى من هذه الجراحة في الحالات التالية:
- استبعاد إذا كان المريض يشتبه بشدة في وجود ورم خبيث الطحال من الأورام الخبيثة.
- استبعاد المرضى الذين يعانون من تضخم الطحال الناتج عن أمراض الدم أو سرطان الغدد الليمفاوية.
- استبعاد المرضى الذين يعانون من تضخم الطحال الثانوي لتليف الكبد.
- استبعاد المرضى الذين يعانون من تمزق الطحال الرضحي الذي يهدد حياتهم.
- استبعاد المرضى الذين يعانون من سوء الصحة العامة وعدم القدرة على تحمل الجراحة.
2. التقنية الجراحية
- الإعداد للعملية.
- وضع المريض تحت التخدير العام في وضع Trendelenburg العكسي مع ميل الجانب الأيسر من الجسم حوالي 10-30 درجة.
ملاحظة: قم بإجراء تعديلات في الموضع حسب الحاجة طوال العملية الجراحية. - ضع الجراح الأول والمساعد مع منظار البطن على الجانب الأيمن للمريض والمساعد الأول على الجانب الأيسر للمريض.
- إنشاء والحفاظ على الصفاق الرئوي عند 12-14 مم زئبق.
- قم بتثبيت أربعة منافذ على جدار البطن بمساعدة التصور بالمنظار ، كما هو موضح في الشكل 1.
- وضع المريض تحت التخدير العام في وضع Trendelenburg العكسي مع ميل الجانب الأيسر من الجسم حوالي 10-30 درجة.
- فحص التجويف البريتوني تحت تنظير البطن لتأكيد عدم وجود أورام خبيثة.
- إجراء انسداد مؤقت للشريان الطحالي.
- استخدم نظام ختم الأوعية الدموية لتشريح الرباط المعدي الطحال على طول الانحناء الأكبر للمعدة ، ودخول الكيس الأصغر.
- أمسك المعدة وانقلها إلى الجزء العلوي الأيمن للتعرض بشكل أفضل للمجال الجراحي.
- قم بتشريح الجذع الرئيسي للشريان الطحالي بدقة عند الحافة العلوية للبنكرياس وقم بإغلاقه مؤقتا بمشبك بولدوج.
ملاحظة: بعد انسداد تدفق الدم ، يظهر الطحال انخفاضا في الحجم وملمس أكثر نعومة ، مما يوفر مساحة جراحية كافية.
- تشريح الأربطة حول الطحال ، بما في ذلك الأربطة الطحال والطحال والطحال.
ملاحظة: يجب توخي الحذر عند فصل ذيل البنكرياس عن الطحال ، خاصة في حالات تضخم الطحال أو آفات الطحال الضخمة ، لمنع النزيف غير المنضبط وحدوث ناسور البنكرياس بعد الجراحة (POPF). - قم بإجراء انسداد مؤقت للنقير الطحالي.
- قم بفضح نقير الطحال عن طريق استئصال المرفقات المحيطة به بمشرط بالموجات فوق الصوتية ، ثم قم بتنفيذ انسداد مؤقت للنقير الطحالي بمشبك بولدوج.
ملاحظة: في الحالات التي تحتوي على اختلافات في الأوعية الدموية الطحالية ، فإن مجرد انسداد الشريان الطحالي قد لا يحقق التغيرات الإقفارية الطحالية المرغوبة. - بعد هذه الخطوة ، قم بإجراء إعادة تقييم شاملة للون الطحال وحجمه وملمسه.
- قم بفضح نقير الطحال عن طريق استئصال المرفقات المحيطة به بمشرط بالموجات فوق الصوتية ، ثم قم بتنفيذ انسداد مؤقت للنقير الطحالي بمشبك بولدوج.
- إجراء الموجات فوق الصوتية أثناء الجراحة لتحديد حدود الآفة.
- استخدم الموجات فوق الصوتية أثناء الجراحة لتحديد حدود الآفة أثناء الجراحة.
- استخدم الكي الكهربائي لتحديد خط الترسيم على بعد 1 سم على الأقل من حدود الآفة.
- إجراء تشريح حمة الطحال.
- أدخل جهاز ترددات راديوية ثنائية القطب في حمة الطحال على طول خط الترسيم للتخثر والاستئصال ، مع ضبط طاقة الترددات الراديوية عند 80 واط.
- استخدم مشرطا بالموجات فوق الصوتية لتشريح حمة الطحال في منطقة التخثر النخرية.
- قم بتثبيت القنوات السميكة بإحكام باستخدام مشابك الأوعية الدموية Hem-o-lok ثم قم بقصها بعناية ، مما يضمن استئصال آمن للطحال العلوي الذي يحتوي على الآفة.
ملاحظة: يجب ربط الأوعية التي تزود الجزء المعاد من الطحال بعناية وتثبيتها
- قم بإزالة العينة.
- حرر مشبك البلدغ ، مع ضمان عدم حدوث نزيف من حافة قطع الطحال ، وتأكد من إمداد الطحال بكمية كافية من الدم.
- استخدم الكي الكهربائي ثنائي القطب لكي حافة قطع الطحال وتطبيق عوامل مرقئ قابلة للامتصاص فوقها.
- ضع أنبوب تصريف في حفرة الطحال.
- ضع العينة في كيس عينة ، وقم بتجزئتها بالملقط البيضاوي ، وقم بإزالتها من خلال المنفذ الموسع.
- حرر الالتهاب الرئوي والصفاق وخياطة الجروح الثقبية.
3. تفاصيل ما بعد الجراحة
- إجراء تخطيط كهربية القلب المستمر لمدة 24 ساعة بعد الجراحة. مراقبة العلامات الأساسية ، بما في ذلك معدل ضربات القلب وضغط الدم والتنفس وتشبع الأكسجين والضغط الوريدي المركزي واستجابة الحدقة ومستوى الوعي ، لاكتشاف المضاعفات المبكرة بعد الجراحة في الوقت المناسب.
- يجب إعطاء المضادات الحيوية (سيفوروكسيم الصوديوم، 1.5 جم كل 12 ساعة) ومثبطات مضخة البروتون بشكل روتيني بعد الجراحة.
- قم بإزالة أنبوب المعدة في اليوم الثاني بعد الجراحة والسماح للمريض باتباع نظام غذائي كامل السائل.
- قم بإزالة أنبوب تصريف البطن عندما يكون ناتج التصريف أقل من 100 مل / 24 ساعة.
- حدد موعدا لمتابعة الأشعة المقطعية للبطن بعد شهرين من الجراحة لتقييم حالة البطن.
النتائج
في هذه الحالة ، تم إدخال مريضة تبلغ من العمر 72 عاما بسبب آفة طحال ضخمة تم العثور عليها في فحص روتيني في مستشفى محلي. كان لديها تاريخ من جراحة البطن السابقة. كان تاريخها الطبي غير ملحوظ ، وكان مؤشر كتلة الجسم طبيعيا (20.1 كجم /م 2). أظهر التصوير المقطعي المحوسب المعزز بتباين البطن آفة ضخمة تقع في القطب الأوسط العلوي من الطحال ، بقطر حوالي 15 سم (الشكل 2). لم تكشف التقييمات السابقة للجراحة عن أي دليل على وجود ورم خبيث. نظرا للحجم الكبير للآفة ، بعد مناقشة كاملة ، تمت محاولة LPS مع انسداد تدفق الدم الكامل في الطحال. تظهر الصور الممثلة بالمنظار أثناء الجراحة في الشكل 3.
كان وقت الجراحة 102 دقيقة ، مع فقدان دم أثناء الجراحة قدره 30 مل ، وتم استئصال ما يقرب من 65٪ من الطحال. لم تحدث مضاعفات أثناء الجراحة ، ولم يكن هناك تحويل إلى شق البطن. لم يكن نقل الدم أثناء الجراحة مطلوبا. تمت إزالة استنزاف البطن بعد 4 أيام من الجراحة ، وتم إخراج المريضفي اليوم السابع بعد الجراحة. لم تكن هناك مضاعفات بعد الجراحة، بما في ذلك ناسور البنكرياس بعد الجراحة، أو العدوى داخل الصفاق أو النزيف أو تجلط البابة، أو احتشاء الطحال. ويمكن الاطلاع على تفاصيل محددة في الجدول 1. كان التشخيص المرضي هو الورم الوعائي أظهرت متابعة التصوير المقطعي المحوسب للبطن بعد شهرين أن الطحال المتبقي كان لديه إمدادات دم جيدة ، ولم يلاحظ أي تكرار.
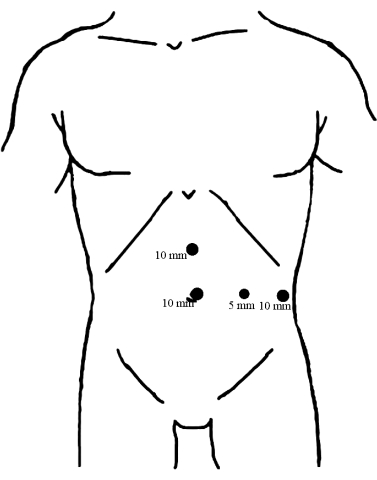
الشكل 1: توزيع المبازل. ضع مبزلا مقاس 10 مم أسفل السرة كمنفذ مراقبة. يتم إدخال المبازل الأخرى مقاس 10 مم ، أحدهما في نقطة المنتصف بين عملية السرة والخنجري والآخر على الخط الإبطي الأمامي الأيسر ، بالتوازي مع السرة ، وكلاهما يعمل كمنافذ التشغيل الرئيسية. بعد ذلك ، تم إدخال المبزل مقاس 5 مم على طول خط الوسط للترقوة اليسرى على مستوى السرة كمنفذ تشغيل مساعد. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
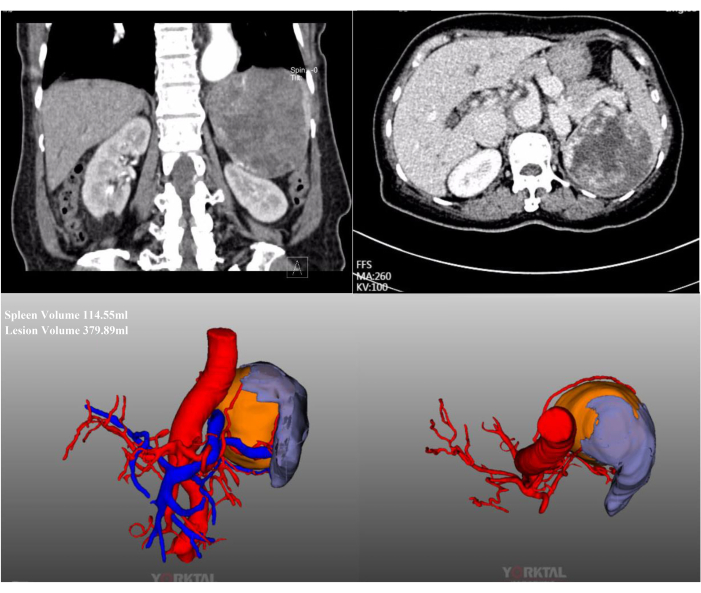
الشكل 2: إعادة بناء التصوير المقطعي المحوسب والتصوير المقطعي المحوسب بتقنية CT-3D. تظهر إعادة بناء التصوير المقطعي المحوسب والتصوير المقطعي المحوسب بتباين البطن آفة ضخمة تقع في القطب الأوسط العلوي من الطحال. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
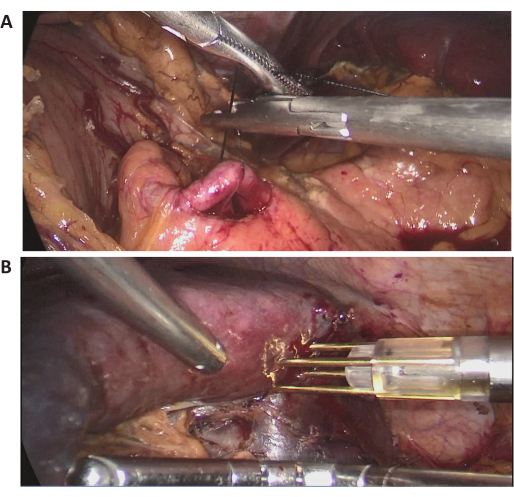
الشكل 3: الصور بالمنظار أثناء الجراحة. (أ ، ب) صور تمثيلية بالمنظار أثناء الجراحة للإجراء الجراحي. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
| العناصر | غب |
| وقت الجراحة (دقيقة) | 102 |
| فقدان الدم أثناء الجراحة (مل) | 30 |
| التحويل إلى شق البطن | لا |
| نقل الدم أثناء الجراحة | لا |
| الإقامة في المستشفى بعد الجراحة (أيام) | 7 |
| مضاعفات ما بعد الجراحة | لا |
الجدول 1: التفاصيل الجراحية وما بعد الجراحة ل LPS.
Discussion
لسنوات ، كان استئصال الطحال الكلي هو العلاج الأساسي لأورام الطحال وتضخم الطحال واضطرابات الدم. ومع ذلك ، مع متابعة الحالات المكثفة ، أثارت المضاعفات بعد استئصال الطحال الكلي ، بما في ذلك المضاعفات المعدية ومضاعفات الانسداد الخثاري ، الانتباهتدريجيا 8. تعد عدوى ما بعد استئصال الطحال الشديدة (OPSIs) أشد المضاعفات بعد استئصال الطحال ، وتتميز بتطور المرض السريع بمعدل وفيات يبلغ حوالي 50٪9. يعزى هذا الخطر المتزايد للعدوى البكتيرية في المرضى الذين يعانون من استئصال الطحال إلى دور خلايا الذاكرة IgM B في المنطقة الهامشية للطحال ، وهو أمر بالغ الأهمية لإزالة البكتيريا المغلفة10،11. علاوة على ذلك ، يجب ملاحظة مضاعفات ما بعد الجراحة مثل تجلط الدم البابي ، وتجلط الجهاز السحري ، والانسداد الرئوي. المرضى الذين يعانون من تليف الكبد الذين يخضعون لاستئصال الطحال لديهم نسبة أعلى من تجلط الطحال12 ، وربما تكون مرتبطة بحالة فرط التخثر13. يمكن أن يحقق PS تأثيرات علاجية مع الحفاظ على وظيفة الطحال. لذلك ، بالنسبة للمرضى المؤهلين ، أصبح PS بديلا مفضلا. تم استخدام الجراحة بالمنظار ، التي تقدم فوائد مثل الحد الأدنى من الصدمات والنتائج الجمالية والإقامة الأقصر بعد الجراحة ، على نطاق واسع في PS في السنوات الأخيرة.
تم الإبلاغ عن LPS لأول مرة بواسطة Poulin في عام 199514. ينطوي LPS على انسداد الأوعية الدموية الانتقائي لأجزاء معينة من الطحال ، متبوعا بالاستئصال على طول خط الترسيم. عادة ما تنقسم الفروع الطرفية للشريان الطحالي إلى 2-3 فروع قبل الدخول إلى أجزاء طحال مميزة. يتم فصل كل جزء عن طريق مناطق الأوعية الدموية نسبيا15. ومع ذلك ، فإن تطبيق LPS يمثل تحديا بسبب النزيف غير المنضبط أثناء الجراحة. استعرض ريناتو 344 حالة من جراحة LPS التي أجريت بين عامي 1960 ويوليو 2017 ، مشيرا إلى أن متوسط فقدان الدم أثناء الجراحة تراوح من 0 إلى 1200 سم مكعب. من بين الحالات ، تطلبت 6.4٪ (22/344) التحويل إلى شق البطن ، و 14 حالة خضعت لاستئصال الطحال الكلي بسبب النزف أثناءالجراحة 16. بناء على تجربتنا ، فإن الأسباب الرئيسية هي كما يلي: (1) يمتلك الطحال إمدادات دم غنية ، كما أن قوامه الرقيق يجعله عرضة للإصابة أثناء الجراحة ، مما يجعل الإرقاء صعبا. (ثانيا) يؤدي تشريح الرباط حول الطحال غير الكافي إلى تعقيد تعبئة الطحال ، مما يؤدي إلى تمزق الطحال المتني. (ثالثا) يشكل تشريح فروع الشريان الطحالي صعوبة كبيرة ويحمل خطرا محتملا لإتلاف هياكل البطن المجاورة.
أبلغت العديد من الدراسات عن طرق لتقليل النزيف أثناء الجراحة أثناء LPS. هناك ثلاث طرق رئيسية رئيسية: انسداد إمدادات الدم الطحالية ، واستخدام أجهزة الترددات الراديوية ، والمساعدة الروبوتية. أبلغ بوري عن انسداد مؤقت للشريان الطحالي باستخدام مشبك حلقي للسيطرة على النزيف أثناء الجراحة أثناء LPS17. في دراسة بينغ18 ، خضع 46 مريضا ل LPS مع انسداد مؤقت للشريان الطحالي. قاموا مؤقتا بإغلاق الشريان الطحالي الرئيسي بمشبك بولدوج قبل تشريح الفروع المقابلة لشريان الطحال. على عكسنا ، تضمنت هذه الدراسة فقط الأورام الموجودة في القطبين العلوي والسفلي من الطحال ، مع أحجام الطحال أقل من 20 سم. كما تمت محاولة الانصمام الوعائي قبل الجراحة للسيطرة على النزيف في LPS19،20 ، مما يدل على نتائج سريرية مرضية. استعرض كاتالين وآخرون 21 10 حالات من PS بمساعدة الروبوت ، والتي كان لديها نزيف أقل أثناء الجراحة وإقامة أقصر بعد الجراحة مقارنة ب LPS. ومع ذلك ، فإن تكلفته العالية تحد من استخدامه على نطاق واسع. كان مركزنا أول من استخدم جهاز الترددات الراديوية Habibi4X لاستئصال الطحال22. يخلق منطقة نخرية تخثرية من خلال الترددات الراديوية ، مما يسمح باستئصال الطحال بدون دماء. لقد أصبحت طريقة موحدة في المركز مع فعالية سريرية ثابتة.
بالنظر إلى قيود الطرق المذكورة أعلاه والتجربة الفريدة لمركزنا ، حاولنا استخدام مشبك البلدغ للانسداد المؤقت لشريان الطحال والنقير ، وإجراء LPS تحت نقص تروية الطحال الكامل. أفادت الدراسة أن 95٪ من جذع الشريان الطحالي الرئيسي يمتد على الحافة العلوية للبنكرياس23. من السهل إجراء الانسداد المؤقت باستخدام مشبك البلدغ بعد التوطين والعزل أثناء الجراحة. ومع ذلك ، من الضروري تسليط النقير الطحالي يتطلب خبرة جراحية كبيرة بالمنظار. يتأثر تعقيد هذا الإجراء بعوامل مثل ارتفاع مؤشر كتلة الجسم ، وآفة تقع بالقرب من نقير الطحال ، وحجم الآفة الكبير ، وتاريخ جراحة البطن. مطلوب تقنية جراحية دقيقة لمنع إصابة ذيل البنكرياس والأوعية المعدية القصيرة. يمكن أن يضمن الحصار الكامل لتدفق الدم الطحال التأثير الإقفاري الطحالي المطلوب ، خاصة عند التعامل مع حالات الأوعية الدموية المختلفة.
تظهر أجهزة الترددات الراديوية أداء ممتازا في الإرقاء24،25. نستخدم بشكل روتيني أجهزة الترددات الراديوية لإدخالها في حمة الطحال على طول الحافة المقطوعة مسبقا للتخثر ، مما يشكل منطقة نخرية تخثرية. بعد ذلك ، نستخدم مشرط بالموجات فوق الصوتية لتشريح حمة الطحال ، وتحقيق استئصال الطحال الجزئي بدون دم. في هذه الدراسة ، أجرينا استئصال آفة طحال كبيرة بمساعدة الترددات الراديوية. كان فقدان الدم أثناء الجراحة 30 مل ، وكان وقت الجراحة 102 دقيقة ، مع عدم التحويل إلى جراحة مفتوحة. تم إخراج المريض بعد 7 أيام من الجراحة دون مضاعفات ما بعد الجراحة ، والتي كانت أفضل بكثير من معظم الدراسات الأخرى16،26. أظهرت متابعة التصوير المقطعي المحوسب في الجزء العلوي من البطن بعد شهرين من العملية عدم تجلط الدم ، وكان الطحال المتبقي لديه إمدادات دم جيدة ، مما يدل على تأثير علاجي مرض.
يشير تيبرمان وآخرون إلى أن الوقت الإقفاري الآمن والدافئ للطحال البشري هو 1 ساعةو 27. بناء على الخبرة الجراحية الواسعة ، يمكننا إكمال تشريح حمة الطحال في وقت آمن. علاوة على ذلك ، أظهرت فحوصات التصوير المقطعي المحوسب للبطن بعد الجراحة باستمرار عدم تجلط الدم أو احتشاء الطحال. هذا يؤكد سلامة LPS تحت انسداد تدفق الدم الطحال الكامل. ومع ذلك ، نوصي بتجنب الحالات الصعبة خلال منحنى التعلم الأولي ، بما في ذلك تلك التي يبلغ مؤشر كتلة الجسم >فيها 25 كجم / متر مربع ، وتاريخ من جراحة البطن ، وآفات نقير كبيرة الحجم أو شبه الطحال ، لمنع الوقت الإقفاري المطول الذي قد يضر بوظيفة الطحال. الطريقة الموصوفة في هذه الدراسة لا تنطبق على الآفات الموجودة في نقير الطحال. كما أن مراقبة ما بعد الجراحة مهمة بنفس القدر للكشف عن الأحداث الضائرة المحتملة.
بالمقارنة مع استئصال الطحال الكلي ، يوفر PS ميزة الحفاظ على الوظيفة الفسيولوجية للطحال مع تحقيق الفعالية العلاجية وتقليل معدلات المضاعفات طويلةالمدى 2. يوصى عموما بأن يتجاوز حجم الطحال المتبقي 25٪ للحفاظ على وظيفة الطحال بشكل فعال. لتقييم حجم الطحال المتبقي ، نستخدم تقنية إعادة بناء CT-3D قبل الجراحة. في الحالات التي تنطوي على آفات طحال ضخمة ، يشكل النهج التقليدي لتحديد وإغلاق فروع الشريان الطحالي المقابلة تحديات في الحفاظ على حمة الطحال الكافية. في هذه الدراسة ، من خلال الجمع بين إعادة بناء CT-3D قبل الجراحة والتقييم بالموجات فوق الصوتية أثناء الجراحة ، قمنا بتحسين نهج LPS لتحقيق أقصى قدر من الحفاظ على أنسجة الطحال الطبيعية. تم استئصال ما يقرب من 65٪ من الطحال ، والتي يمكن أن تحقق كلا من الأهداف العلاجية والحفاظ على وظيفة الطحال.
من أجل ضمان سلامة هذه الطريقة ، نوصي بإجراء فحوصات التصوير المقطعي المحوسب للبطن قبل الجراحة لتوضيح العلاقة بين الآفة والأوعية الطحالية وهياكل البطن المهمة ، وكذلك وجود الأوعية الدموية المختلفة. إذا كان ذلك ممكنا ، يمكن لإعادة بناء CT-3D أن تعزز التقييم قبل الجراحة. من المهم ملاحظة أن هذه الطريقة مناسبة للمرضى الذين يعانون من صدمات محصورة في جانب واحد من الطحال ، ولا ننصح باستخدام هذه الطريقة في حالات تمزق الطحال الرضحي الذي يهدد الحياة أو للمرضى الذين يعانون من اضطرابات الدم. قد يشكل الأول خطر الحفاظ على الطحال غير الضروري الذي يؤدي إلى الوفاة. بالنسبة للمرضى الذين يخضعون لمرض PS بسبب اضطرابات الدم ، أظهرت المتابعة طويلة الأمد خطرا كبيرا للتكرار والتحول اللاحق إلى استئصال الطحالالكلي 2. المؤشر المثالي لهذه الطريقة هو الآفات الحميدة في الطحال. لا تتطلب هذه الطريقة تشريح فروع الشريان الطحالي ، وبالتالي تبسيط منحنى التعلم ل LPS إلى حد ما. ومع ذلك ، يجب توخي الحذر عند اختيار المرضى خلال مرحلة التعلم الأولية.
في الختام ، يعد LPS تحت انسداد تدفق الدم الكلي الطحال طريقة آمنة ومجدية وقابلة للتكرار وتحقق نتائج مرضية. ومع ذلك، لا تزال هناك حاجة إلى مزيد من البحوث المكثفة لتقييم سلامتها وفعاليتها بشكل شامل.
Disclosures
اي
Acknowledgements
اي
Materials
| Name | Company | Catalog Number | Comments |
| Absorbable hemostat | Ethicon, LLC | W1913T | |
| Disposable trocar | Kangji Medical | 101Y.307,101Y.311 | |
| Endo bag | Medtronic | https://www.medtronic.com/covidien/en-us/search.html#q=endo%20bag | specimen bag |
| Jaw sealer/divider | Covidien Medical | LF1737 | |
| Laparoscopic radiofrequency device | AngioDynamics, Inc | Rita 700-103659 | |
| Laparoscopic system | Olympus | WM-NP2 L-RECORDOR-01 | |
| LigaSure | Medtronic | https://www.medtronic.com/covidien/en-us/products/vessel-sealing/ligasure-technology.html | vessel sealing system |
| Ligation clips (Hem-o-lok) | Teleflex Medical | 544240,544230,544220 | |
| Ultrasonic scalpel | ETHICON Medical | HAR36 |
References
- Lewis, S. M., Williams, A., Eisenbarth, S. C. Structure and function of the immune system in the spleen. Sci Immunol. 4 (33), eaau6085 (2019).
- Kristinsson, S. Y., Gridley, G., Hoover, R. N., Check, D., Landgren, O. Long-term risks after splenectomy among 8,149 cancer-free American veterans: a cohort study with up to 27 years follow-up. Haematologica. 99 (2), 392-398 (2014).
- Guizzetti, L. Total versus partial splenectomy in pediatric hereditary spherocytosis: A systematic review and meta-analysis. Pediatr Blood Cancer. 63 (10), 1713-1722 (2016).
- Bronte, V., Pittet, M. J. The spleen in local and systemic regulation of immunity. Immunity. 39 (5), 806-818 (2013).
- Christo, M. C. Partial regulated splenectomies. Preliminary note on the first 3 cases operated on. Hospital (Rio J). 56, 645-650 (1959).
- Redmond, H. P., Redmond, J. M., Rooney, B. P., Duignan, J. P., Bouchier-Hayes, D. J. Surgical anatomy of the human spleen. Br J Surg. 76 (2), 198-201 (2005).
- Romboli, A., et al. Laparoscopic partial splenectomy: A critical appraisal of an emerging technique. A review of the first 457 published cases. J Laparoendosc Adv Surg Tech A. 31 (10), 1130-1142 (2021).
- Buzelé, R., Barbier, L., Sauvanet, A., Fantin, B. Medical complications following splenectomy. J Visc Surg. 153 (4), 277-286 (2016).
- Bisharat, N., Omari, H., Lavi, I., Raz, R. Risk of infection and death among post-splenectomy patients. J Infect. 43 (3), 182-186 (2001).
- Kruetzmann, S., et al. Human immunoglobulin M memory B cells controlling Streptococcus pneumoniae infections are generated in the spleen. J Exp Med. 197 (7), 939-945 (2003).
- Leone, G., Pizzigallo, E. Bacterial infections following splenectomy for malignant and nonmalignant hematologic diseases. Mediterr J Hematol Infect Dis. 7 (1), e2015057 (2015).
- Romano, F., et al. Thrombosis of the splenoportal axis after splenectomy. Langenbecks Arch Surg. 391 (5), 483-488 (2006).
- Watters, J. M., et al. Splenectomy leads to a persistent hypercoagulable state after trauma. Am J Surg. 199 (5), 646-651 (2010).
- Poulin, E. C., Thibault, C., DesCôteaux, J. G., Côté, G. Partial laparoscopic splenectomy for trauma: technique and case report. Surg Laparosc Endosc. 5 (4), 306-310 (1995).
- Ignjatovic, D., Stimec, B., Zivanovic, V. The basis for splenic segmental dearterialization: a post-mortem study. Surg Radiol Anat. 27 (1), 15-18 (2005).
- Costi, R., et al. Partial splenectomy: Who, when and how. A systematic review of the 2130 published cases. J Pediatr Surg. 54 (8), 1527-1538 (2019).
- Borie, F. Laparoscopic partial splenectomy: Surgical technique. J Visc Surg. 153 (5), 371-376 (2016).
- Ouyang, G., et al. Laparoscopic partial splenectomy with temporary occlusion of the trunk of the splenic artery in fifty-one cases: experience at a single center. Surg Endosc. 35 (1), 367-373 (2021).
- Mignon, F., et al. Preoperative selective embolization allowing a partial splenectomy for splenic hamartoma. Ann Chir. 128 (2), 112-116 (2003).
- Zheng, L., et al. Treatment of hemangioma of the spleen by preoperative partial splenic embolization plus laparoscopic partial splenectomy: A case report. Medicine (Baltimore). 97 (17), e0498 (2018).
- Vasilescu, C., Stanciulea, O., Tudor, S. Laparoscopic versus robotic subtotal splenectomy in hereditary spherocytosis. Potential advantages and limits of an expensive approach. Surg Endosc. 26 (10), 2802-2809 (2012).
- Wang, W. -. D., et al. Partial splenectomy using a laparoscopic bipolar radiofrequency device: a case report. World J Gastroenterol. 21 (11), 3420-3424 (2015).
- Liu, D. L., et al. Anatomy of vasculature of 850 spleen specimens and its application in partial splenectomy. Surgery. 119 (1), 27-33 (1996).
- Habib, N. A. How we do a bloodless partial splenectomy. Am J Surg. 186 (2), 164-166 (2003).
- Gumbs, A. A., Bouhanna, P., Bar-Zakai, B., Briennon, X., Gayet, B. Laparoscopic partial splenectomy using radiofrequency ablation. J Laparoendosc Adv Surg Tech A. 18 (4), 611-613 (2008).
- Liu, G., Fan, Y. Feasibility and safety of laparoscopic partial splenectomy: A systematic review. World J Surg. 43 (6), 1505-1518 (2019).
- Teperman, S. H., et al. Bloodless splenic surgery: The safe warm-ischemic time. J Pediatr Surg. 29 (1), 88-92 (1994).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved