Method Article
Generazione di organoidi cardiaci umani auto-assemblanti derivati da cellule staminali pluripotenti
In questo articolo
Riepilogo
Qui, descriviamo un protocollo per creare organoidi cardiaci umani rilevanti per lo sviluppo (hHO) in modo efficiente utilizzando cellule staminali pluripotenti umane mediante auto-organizzazione. Il protocollo si basa sull'attivazione sequenziale dei segnali di sviluppo e produce tessuti cardiaci umani altamente complessi e funzionalmente rilevanti.
Abstract
La capacità di studiare lo sviluppo cardiaco umano in salute e malattia è fortemente limitata dalla capacità di modellare la complessità del cuore umano in vitro. Lo sviluppo di piattaforme simili a organi più efficienti in grado di modellare fenotipi complessi in vivo , come organoidi e organi su chip, migliorerà la capacità di studiare lo sviluppo e le malattie del cuore umano. Questo documento descrive un protocollo per generare organoidi cardiaci umani (hHO) altamente complessi mediante auto-organizzazione utilizzando cellule staminali pluripotenti umane e attivazione graduale del percorso di sviluppo utilizzando inibitori di piccole molecole. I corpi embrioidi (EB) sono generati in una piastra a 96 pozzetti con fondo tondo e pozzi di attacco ultra-bassi, facilitando la coltura in sospensione di costrutti individualizzati.
Gli EB subiscono la differenziazione in hHO mediante una strategia di modulazione del segnale Wnt in tre fasi, che prevede un'attivazione iniziale della via Wnt per indurre il destino del mesoderma cardiaco, una seconda fase di inibizione Wnt per creare linee cardiache definitive e una terza fase di attivazione Wnt per indurre tessuti d'organo proepiardici. Questi passaggi, eseguiti in un formato a 96 pozzetti, sono altamente efficienti, riproducibili e producono grandi quantità di organoidi per corsa. L'analisi mediante imaging a immunofluorescenza dal giorno 3 al giorno 11 della differenziazione rivela le specifiche del primo e del secondo campo cardiaco e tessuti altamente complessi all'interno degli hHO al giorno 15, incluso il tessuto miocardico con regioni di cardiomiociti atriali e ventricolari, nonché camere interne rivestite di tessuto endocardico. Gli organoidi presentano anche un'intricata rete vascolare in tutta la struttura e un rivestimento esterno di tessuto epicardico. Da un punto di vista funzionale, gli hHO battono in modo robusto e presentano una normale attività del calcio come determinato dall'imaging dal vivo Fluo-4. Nel complesso, questo protocollo costituisce una solida piattaforma per studi in vitro in tessuti cardiaci simili a organi umani.
Introduzione
I difetti cardiaci congeniti (CHD) sono il tipo più comune di difetto congenito nell'uomo e colpiscono circa l'1% di tutti i nati vivi1,2,3. Nella maggior parte dei casi, le ragioni dei CHD rimangono sconosciute. La capacità di creare modelli di cuore umano in laboratorio che assomigliano molto al cuore umano in via di sviluppo costituisce un significativo passo avanti per studiare direttamente le cause alla base dei CHD negli esseri umani piuttosto che in modelli animali surrogati.
L'epitome dei modelli tissutali cresciuti in laboratorio sono gli organoidi, costrutti cellulari 3D che assomigliano a un organo di interesse per la composizione cellulare e la funzione fisiologica. Gli organoidi sono spesso derivati da cellule staminali o cellule progenitrici e sono stati utilizzati con successo per modellare molti organi come il cervello4,5, il rene6,7, l'intestino8,9, il polmone10,11, il fegato12,13 e il pancreas14,15 , solo per citarne alcuni. Recenti studi sono emersi dimostrando la fattibilità della creazione di organoidi cardiaci auto-assemblanti per studiare lo sviluppo del cuore in vitro. Questi modelli includono l'utilizzo di cellule staminali embrionali di topo (mESC) per modellare lo sviluppo cardiaco precoce16,17 fino alla specifica atrioventricolare18 e cellule staminali pluripotenti umane (hPSC) per generare organoidi cardiaco-endodermici multi-strato germinale19 e cardioidi camerati20 con composizione cellulare altamente complessa.
Questo documento presenta un nuovo protocollo di modulazione WNT in 3 fasi per generare hHO altamente complessi in modo efficiente ed economico. Gli organoidi sono generati in piastre a 96 pozzetti, risultando in un sistema scalabile e ad alta produttività che può essere facilmente automatizzato. Questo metodo si basa sulla creazione di aggregati hPSC e sull'innesco di fasi di sviluppo della cardiogenesi, tra cui la formazione di mesoderma e mesoderma cardiaco, la specifica del primo e del secondo campo cardiaco, la formazione di organi proepiardici e la specifica atrioventricolare. Dopo 15 giorni di differenziazione, gli hHO contengono tutte le principali linee cellulari presenti nel cuore, camere interne ben definite, camere atriali e ventricolari e una rete vascolare in tutto l'organoide. Questo sistema organoide cardiaco altamente sofisticato e riproducibile è in grado di studiare analisi strutturali, funzionali, molecolari e trascrittomiche nello studio dello sviluppo cardiaco e delle malattie e dello screening farmacologico.
Protocollo
1. Coltura e manutenzione hPSC
NOTA: Le PSC indotte dall'uomo (hiPSC) o le cellule staminali embrionali umane (hESC) devono essere coltivate per almeno 2 passaggi consecutivi dopo lo scongelamento prima di essere utilizzate per generare EB per differenziazione o ulteriore crioconservazione. Le hPSC sono coltivate in terreno PSC (vedi tabella dei materiali) su piastre di coltura a 6 pozzetti rivestite con membrana basale (BM-ECM). Quando si eseguono cambiamenti del mezzo sulle hPSC in piastre a 6 pozzetti, aggiungere il mezzo direttamente sul lato interno del pozzo piuttosto che direttamente sopra le cellule per evitare il distacco o lo stress cellulare indesiderato. Gli utenti dovrebbero diffidare dei supporti PSC pre-riscaldamento che non dovrebbero essere riscaldati a 37 ° C; tutti i supporti PSC utilizzati in questo protocollo erano termostabili.
- Per rivestire le piastre del pozzo con il BM-ECM, scongelare un'aliquota del BM-ECM (conservato a -20 °C secondo le istruzioni del produttore) sul ghiaccio e mescolare 0,5 mg del BM-ECM con 12 ml di mezzo eagle modificato (DMEM)/F12 di Dulbecco freddo (conservato a 4 °C). Distribuire 2 mL della miscela DMEM/F12-BM-ECM su ciascun pozzetto di una piastra a 6 pozzetti e incubare a 37 °C per almeno 2 ore.
- Per scongelare le cellule, in primo luogo, scongelare il crioviale hPSC in un tallone a 37 ° C o a bagnomaria per 1-2 minuti fino a quando non è visibile solo una piccola quantità di ghiaccio. Trasferire le cellule scongelate in un tubo di centrifuga e aggiungere lentamente 8-9 mL del mezzo PSC integrato con 2 μM dell'inibitore ROCK, tiazovivina (Thiaz), e centrifugare a 300 × g per 5 minuti. Rimuovere il surnatante e risospescere il pellet cellulare nel mezzo PSC integrato con 2 μM di Thiaz. Distribuire le cellule nel terreno di coltura in 1-2 pozzetti a seconda della concentrazione e della coltura crioviale a 37 °C, 5% CO2 per 24 ore prima di cambiare il mezzo PSC.
- Cambiare il mezzo sulle celle a intervalli di 48 ore. Eseguire lavaggi e cambi di mezzo utilizzando dmEM/F12 (1 mL/pozzetto) e il mezzo PSC (2 ml/pozzetto), rispettivamente.
NOTA: i lavaggi aiutano a rimuovere i rifiuti cellulari e i detriti, mentre i cambiamenti dei mezzi freschi forniscono alle cellule una rinnovata fonte di sostanze nutritive. - Passare le cellule al subunondanza (60-80% confluente) aspirando il mezzo, quindi lavando ciascun pozzetto con 1 mL di 1x soluzione tamponata con fosfato di Dulbecco (senza calcio, senza magnesio; DPBS). Aspirare il DPBS e aggiungere 1 mL del reagente di dissociazione per le hPSC (vedere la tabella dei materiali), seguito dall'aspirazione di tutti tranne un film sottile del reagente dopo 10 s.
- Incubare per 2-5 minuti con il film sottile del reagente di dissociazione per hPSC fino a quando non si formano spazi tra le cellule.
NOTA: il tempo per interrompere la dissociazione dipende dalla linea cellulare. - Aggiungere 1 mL del mezzo PSC integrato con 2 μM di Thiaz (PSC medium + Thiaz) al pozzo e picchiettare delicatamente la piastra per indurre il distacco cellulare. Pipettare le cellule staccate nel mezzo 1-2 volte per rompere eventuali colonie di grandi dimensioni e risospese le cellule in mezzo PSC + Thiaz in un rapporto pozzo 1: 6 (cellule da 1 pozzo risospese in 12 ml di terreno di coltura). Riplazionare le cellule su pozzetti rivestiti di BM-ECM.
2. Generazione di organoidi cardiaci umani autoassemblanti 3D
- Formazione del corpo embrionale (EB):
NOTA: È imperativo limitare le cellule differenziate osservabili prima della formazione del corpo embrioide. Due o tre pozzetti di una piastra a 6 pozzetti con una confluenza del 60-80% produrranno abbastanza cellule per una singola piastra di organoidi da 96 pozzetti. Tutti i fluidi devono essere aliquotati e riscaldati a 37 °C a bagnomaria prima di qualsiasi cambiamento del mezzo per ridurre al minimo lo shock termico degli EB o degli organoidi (questo non include i reagenti di dissociazione cellulare). Vedere la Figura 1A,B.- Giorno -2
- Per creare EB, il giorno -2, lavare hPSC sub-confluenti (60-80% confluenti) con DPBS per almeno 10 s per lavare eventuali detriti cellulari e aspirare il DPBS.
- Per staccare le cellule e rilasciarle in uno stato a cella singola, aggiungere 1 mL di reagente di dissociazione cellulare a temperatura ambiente (vedere la Tabella dei materiali) a ciascun pozzetto per 3-6 minuti. Picchiettare delicatamente la piastra ~ 5 volte al minuto per indurre il distacco durante il controllo al microscopio. Aggiungere 1 mL di PSC medium+Thiaz per fermare la reazione.
- Per raccogliere le cellule e rompere eventuali aggregati rimanenti, pipettare il fluido su e giù nel pozzo 2-3 volte per generare una sospensione a cella singola. Trasferire la sospensione monocellulare in un tubo centrifuga e ruotare per 5 minuti a 300 × g.
- Per ottenere la concentrazione cellulare desiderata, scartare il surnatante e risospese le cellule in 1 mL di PSC medio + Thiaz. Contare le cellule usando un contatore cellulare o un emocitometro e diluire le cellule in mezzo PSC + Thiaz ad una concentrazione di 100.000 cellule / mL.
- Per distribuire le celle per la formazione di EB, utilizzare una pipetta multicanale per aggiungere 100 μL (10.000 celle) a ciascun pozzetto di una piastra a 96 pozzetti con attacco ultra-basso a fondo tondo. Centrifugare la piastra a 100 × g per 3 min e incubare per 24 ore a 37 °C, 5% CO2.
- Giorno -1
- Rimuovere con cautela 50 μL di terreno da ciascun pozzetto e aggiungere 200 μL di terreno PSC fresco riscaldato a 37 °C per ottenere un volume finale di 250 μL per pozzetto. Incubare le cellule per 24 ore a 37 °C, 5% CO2.
NOTA: Rimuovere e aggiungere il mezzo con attenzione sul lato del pozzetto per evitare di disturbare gli EB nella parte inferiore del pozzo. A causa della natura delicata degli EB e della coltura di sospensione, è necessario lasciare un piccolo volume di liquido in ciascun pozzetto quando si cambia il mezzo per evitare di disturbare gli EB.
- Rimuovere con cautela 50 μL di terreno da ciascun pozzetto e aggiungere 200 μL di terreno PSC fresco riscaldato a 37 °C per ottenere un volume finale di 250 μL per pozzetto. Incubare le cellule per 24 ore a 37 °C, 5% CO2.
- Giorno -2
- Differenziazione dell'organoide del cuore umano (hHO):
NOTA: tutti i supporti devono essere riscaldati a 37 °C a bagnomaria prima di qualsiasi cambio di supporto. Rimuovere e aggiungere il mezzo con attenzione sul lato del pozzetto per evitare di disturbare gli organoidi in via di sviluppo sul fondo del pozzo. I lavaggi non sono necessari tra i cambiamenti dei media per ridurre al minimo l'agitazione e consentire la graduale rimozione di inibitori e fattori di crescita. RPMI con supplemento B-27 al 2% (Table of Materials) è stato utilizzato in tutto il protocollo di differenziazione. Il supplemento di B-27 contiene insulina se non specificato (senza insulina nei giorni 0-5). Vedere la Figura 1C.- Giorno 0
- Per avviare la differenziazione verso un lignaggio mesodermico, rimuovere 166 μL di mezzo da ciascun pozzetto (~2/3 del volume totale del pozzo) e aggiungere 166 μL di RPMI 1640 contenente integratore B-27 insulino-libero, 6 μM CHIR99021, 1.875 ng/mL proteina morfogenetica ossea 4 (BMP4) e 1,5 ng/mL Activin A per una concentrazione finale del pozzo di 4 μM CHIR99021, 1,25 ng/mL BMP4 e 1 ng/mL Activin A. Incubare per 24 ore a 37 °C, 5% CO2.
- Giorno 1
- Rimuovere 166 μL di mezzo da ciascun pozzetto e aggiungere 166 μL di RPMI 1640 fresco con integratore B-27 senza insulina. Incubare per 24 ore a 37 °C, 5% CO2.
- Giorno 2
- Per indurre la specifica del mesoderma cardiaco, rimuovere 166 μL di mezzo da ciascun pozzetto e aggiungere 166 μL di RPMI 1640 contenente integratore B-27 senza insulina e 3 μM Wnt-C59 per una concentrazione finale del pozzo di 2 μM Wnt-C59. Incubare per 48 ore a 37 °C, 5% CO2.
- Giorno 4
- Rimuovere 166 μL di mezzo da ciascun pozzetto e aggiungere 166 μL di RPMI 1640 fresco con integratore B-27 senza insulina. Incubare per 48 ore a 37 °C, 5% CO2.
- Giorno 6
- Rimuovere 166 μL di mezzo da ciascun pozzetto e aggiungere 166 μL di RPMI 1640 con supplemento B-27. Incubare per 24 ore a 37 °C, 5% CO2.
- Giorno 7
- Per indurre la differenziazione proepiardiale, rimuovere 166 μL di mezzo da ciascun pozzetto e aggiungere 166 μL di RPMI 1640 fresco contenente integratore B-27 e 3 μM CHIR99021 per una concentrazione finale del pozzo di 2 μM CHIR99021. Incubare per 1 ora a 37 °C, 5% CO2.
- Rimuovere 166 μL di mezzo da ciascun pozzetto e aggiungere 166 μL di RPMI 1640 fresco contenente supplemento B-27. Incubare per 48 ore a 37 °C, 5% CO2.
NOTA: Si consiglia maggiore cautela in questo secondo cambio medio il giorno 7 poiché gli organoidi sono più inclini al movimento a causa dei cambiamenti dei media. - Dal giorno 7 in poi fino alla raccolta o al trasferimento per analisi o sperimentazioni, eseguire cambi di mezzo ogni 48 ore rimuovendo 166 μL di terreno da ciascun pozzetto e aggiungere 166 μL di RPMI 1640 fresco contenente supplemento B-27.
NOTA: gli organoidi sono pronti per l'analisi e la sperimentazione al giorno 15, a meno che le fasi di sviluppo precedenti non siano di interesse. Possono essere coltivati oltre il giorno 15 per esperimenti di coltura o maturazione a lungo termine.
- Giorno 0
3. Analisi organoide
- Trasferimento di organoidi interi (vivi o fissi)
NOTA: per il trasferimento di organoidi vivi, assicurarsi che le punte delle pipette utilizzate siano sterili.- Tagliare la punta di una punta della pipetta P200 a 5-10 mm dall'apertura della punta, con conseguente ampia apertura di ~ 2-3 mm di diametro.
- Inserire la punta direttamente nel pozzetto a fondo tondo contenente l'organoide in modo che la pipetta sia completamente verticale (perpendicolare alla piastra). Assicurarsi che lo stantuffo della pipetta sia già premuto completamente prima di inserire la punta nel mezzo.
- Rilasciare lentamente lo stantuffo della pipetta, occupando abbastanza mezzo (100-200 μL) per raccogliere l'organoide.
- Trasferire l'organoide in mezzo alla destinazione target (ad esempio, per il fissaggio, l'imaging dal vivo, la registrazione elettrofisiologica, la nuova coltura di piastre).
- Organoidi di fissaggio
NOTA: il fissaggio e la colorazione degli organoidi possono essere eseguiti sia nella piastra di coltura a 96 pozzetti che nei tubi di microcentrifuga. La paraformaldeide (PFA) deve essere maneggiata solo in una cappa aspirante.- Per la fissazione in tubi microcentrifuga, trasferire organoidi vivi in tubi separati con 1-8 organoidi per tubo.
NOTA: Non superare gli 8 organoidi per tubo. - Rimuovere con cura e scartare il più possibile il mezzo dal tubo senza toccare gli organoidi.
- Aggiungere il 4% di PFA a ciascun tubo o pozzetto (300-400 μL per tubo di microcentrifuga e 100-200 μL per pozzetto di una piastra da 96 pozzetti). Incubare a temperatura ambiente per 30-45 min.
NOTA: i tempi di incubazione superiori a 1 ora possono richiedere passaggi di recupero dell'antigene e non sono raccomandati. - Scartare in modo sicuro il PFA senza disturbare gli organoidi. Eseguire 3 lavaggi con DPBS integrato con 1,5 g/L di glicina (DPBS/Gly), utilizzando lo stesso volume utilizzato per il PFA al 4%, aspettando 5 minuti tra un lavaggio e l'altro. Rimuovere DPBS/Gly e procedere all'immunocolorazione o ad altre analisi o aggiungere DPBS e conservare a 4 °C per un uso futuro fino a 2 settimane.
NOTA: la conservazione di organoidi fissi per più di 2 settimane può causare degradazione e contaminazione dei tessuti e non è raccomandata.
- Per la fissazione in tubi microcentrifuga, trasferire organoidi vivi in tubi separati con 1-8 organoidi per tubo.
- Colorazione immunofluorescente a tutto monte
- Aggiungere 100 μL di soluzione di bloccante/permeabilizzazione (10% di siero d'asino normale + 0,5% di albumina sierica bovina (BSA) + 0,5% di Triton X-100 in 1x DPBS) a ciascun pozzetto o tubo contenente gli organoidi fissi. Incubare a temperatura ambiente durante la notte su uno shaker.
NOTA: Non superare gli 8 organoidi per tubo. - Rimuovere con cura e scartare il più possibile la soluzione bloccante senza toccare gli organoidi. Esegui 3 lavaggi con DPBS, aspettando 5 minuti tra un lavaggio e l'altro.
- Preparare la soluzione anticorpale primaria (1% di siero d'asino normale + 0,5% BSA + 0,5% Triton X-100 in 1x DPBS) con gli anticorpi primari desiderati alle concentrazioni raccomandate. Incubare a 4 °C per 24 ore su uno shaker.
- Rimuovere con attenzione ed eliminare il più possibile la soluzione anticorpale senza toccare gli organoidi. Esegui 3 lavaggi con DPBS, aspettando 5 minuti tra un lavaggio e l'altro.
- Preparare una soluzione anticorpale secondaria (1% di siero d'asino normale + 0,5% BSA + 0,5% Triton X-100 in 1x DPBS) con gli anticorpi secondari desiderati alle concentrazioni raccomandate. Se gli anticorpi sono marcati in modo fluorescente, incubare a 4 °C al buio (ad esempio, coperto da un foglio di alluminio) per 24 ore su uno shaker.
- Rimuovere con attenzione ed eliminare il più possibile la soluzione anticorpale senza toccare gli organoidi. Esegui 3 lavaggi con DPBS, aspettando 5 minuti tra un lavaggio e l'altro.
- Preparare vetrini con perline (90-300 μm di diametro) montate in un mezzo di montaggio (vedi tabella dei materiali) vicino ai bordi della slitta dove verrà posizionato il coperchio con gli organoidi.
NOTA: Si consiglia di lasciare asciugare il mezzo di montaggio attorno alle perline prima di procedere; questo impedirà alle perline di muoversi. Vedere la Figura 2. - Trasferire gli organoidi colorati utilizzando una punta di pipetta tagliata sul vetrino, tra le perline, assicurando la spaziatura per evitare il contatto tra gli organoidi una volta sul vetrino. Utilizzare l'angolo di una salvietta da laboratorio arrotolata per rimuovere con cura il liquido in eccesso intorno all'organoide.
- Coprire gli organoidi con un mezzo di compensazione del fruttosio-glicerolo (la soluzione di compensazione del fruttosio-glicerolo è al 60% (vol/vol) e 2,5 M di fruttosio)37 utilizzando 120-150 μL del mezzo di montaggio-clearing per vetrino.
NOTA: si consiglia di utilizzare una punta della pipetta tagliata quando si lavora con il mezzo di montaggio-clearing in quanto è molto viscoso. - Passare il coperchio sopra la slitta con gli organoidi coperti con la soluzione di montaggio-clearing e premere lentamente il coperchio sopra la diapositiva, assicurandosi che gli organoidi si trovino tra le perline montate.
- Sigillare il perimetro del coverslip sulla diapositiva usando lo smalto per unghie top coat. Lasciare asciugare la diapositiva al buio a temperatura ambiente per 1 ora. Conservare a 4 °C al buio per la conservazione a lungo termine.
- Aggiungere 100 μL di soluzione di bloccante/permeabilizzazione (10% di siero d'asino normale + 0,5% di albumina sierica bovina (BSA) + 0,5% di Triton X-100 in 1x DPBS) a ciascun pozzetto o tubo contenente gli organoidi fissi. Incubare a temperatura ambiente durante la notte su uno shaker.
- Imaging transitorio del calcio in organoidi cardiaci vivi
NOTA: Secondo le istruzioni del produttore, Fluo4-AM è stato ricostituito in dimetilsolfossido (DMSO) ad una concentrazione finale di soluzione madre di 0,5 mM. Fluo4-AM è stato aggiunto direttamente al pozzetto organoide nella piastra a 96 pozzetti.- Eseguire 2 lavaggi sugli organoidi utilizzando il mezzo RPMI 1640.
- Rimuovere 166 μL del mezzo esaurito dal pozzo.
- Aggiungere 166 μL di mezzo RPMI 1640 riscaldato, rimuovere 166 μL di mezzo e aggiungere 166 μL di mezzo RPMI 1640 fresco.
NOTA: I lavaggi vengono eseguiti per rimuovere il materiale di scarto e i detriti cellulari. Due terzi del mezzo vengono rimossi dai pozzetti durante i lavaggi per evitare di disturbare gli organoidi sul fondo del pozzo prima del saggio funzionale.
- Aggiungere Fluo4-AM medium agli organoidi.
- Aggiungere Fluo4-AM ricostituito in DMSO a RPMI 1640 contenente supplemento B-27 per preparare una soluzione da 1,5 μM.
- Rimuovere 166 μL di mezzo dal pozzo.
- Aggiungere 166 μL di 1,5 μM Fluo4-AM in RPMI 1640 contenente integratore B-27 per una concentrazione finale del pozzo di 1 μM. Incubare a 37 °C, 5% CO2 per 30 min.
- Eseguire 2 lavaggi come nel passaggio 3.4.1.
- Aggiungere 166 μL di RPMI 1640 contenente supplemento B-27 al pozzo.
- Utilizzando una punta tagliata di una punta per pipetta P200, trasferire l'organoide in una capsula di Petri con fondo di vetro (ad esempio, vetro di copertura a 8 pozzetti con vetro di copertura ad alte prestazioni #1.5) con 100-200 μL di mezzo.
NOTA: Vedere paragrafo 3.1 sul trasferimento di organoidi interi. - Immagina che gli organoidi vivano al microscopio con una camera a temperatura e CO2 controllata a 37 °C, 5% CO2.
- Registra diversi video di 10-20 s in varie posizioni attraverso l'organoide, mostrando l'aumento e la diminuzione dei livelli di intensità di fluorescenza quando il calcio entra ed esce dalle cellule.
NOTA: per le registrazioni ad alta risoluzione, si consiglia di registrare a una velocità di 10 fps o superiore; Si consigliano 50 fps. - Analizza i video utilizzando un software di analisi delle immagini (ad esempio, ImageJ) selezionando le regioni di interesse e misurando i livelli di intensità nel tempo.
- Normalizza le registrazioni di intensità usando ΔF/F0 rispetto al tempo in millisecondi e traccia.
- Eseguire 2 lavaggi sugli organoidi utilizzando il mezzo RPMI 1640.
Risultati
Per ottenere hHO auto-organizzante in vitro, abbiamo modificato e combinato i protocolli di differenziazione precedentemente descritti per la differenziazione monostrato 2D di cardiomiociti21 e cellule epicardiche22 utilizzando modulatori di pathway Wnt e per organoidi precardiac 3D16 utilizzando i fattori di crescita BMP4 e Activin A. Utilizzando il protocollo di differenziazione EB e hHO a piastre a 96 pozzetti descritto qui e mostrato nella Figura 1 , le concentrazioni e le durate di esposizione dell'attivatore della via Wnt CHIR99021 sono state ottimizzate per produrre hHO altamente riproducibili e complessi derivati da PSC umani. hPSC o hESC coltivate in mezzo PSC al 60-80% di confluenza in formazione simile a colonie con differenziazione minima o nulla visibile sono ideali per la generazione di EB (Figura 1B).
Gli EB sono stati autorizzati a incubare per 48 ore con un cambiamento medio dopo 24 ore prima di iniziare la differenziazione al giorno 0. Il giorno 0, gli EB dovrebbero apparire come un aggregato sferico scuro al centro di ciascun pozzo al microscopio ottico (Figura 1B). Il protocollo di differenziazione inizia il giorno 0 con l'attivazione della via Wnt e l'aggiunta del fattore di crescita per esattamente 24 ore. Questa induzione del mesoderma seguita da un'induzione del mesoderma cardiaco il giorno 2 utilizzando l'inibitore della via Wnt Wnt-C59 comporterà un significativo allargamento dell'organoide da ~ 200 μm di diametro a 500-800 μm di diametro al giorno 4 e fino a 1 mm (gli organoidi possono sperimentare una leggera riduzione delle dimensioni entro il giorno 15 (Figura 1C)). L'hHO inizierà a battere già dal giorno 6 (Video 1), con il 100% degli organoidi che mostrano un battito visibile entro il giorno 10 (Video 2) (a meno che non si sottoponga a trattamento farmacologico o se sono state utilizzate hPSC inadeguate per generare gli EB). Questo è stato osservato in 5 distinte linee cellulari hPSC23.
Per valutare la capacità degli hHO di rappresentare varie fasi dello sviluppo fisiologico del cuore, abbiamo raccolto organoidi in vari punti temporali durante il protocollo di differenziazione e cercato la presenza e l'espressione trascrittomica dei marcatori del campo cardiaco. La colorazione immunofluorescente per il marcatore del primo campo cardiaco (FHF), HAND1, e il secondo marcatore del campo cardiaco (SHF), HAND2, hanno rivelato la loro presenza nucleare in queste cellule progenitrici cardiache che si verificano intorno al giorno 3 e al giorno 5, rispettivamente (Figura 3A).
L'espressione di entrambi i marcatori avviene nelle regioni degli organoidi che diminuiscono di dimensioni dopo il giorno 7 per il FHF e dopo il giorno 9 per l'SHF. È interessante notare che le immagini ad alto ingrandimento degli organoidi del giorno 7 hanno rivelato che la maggior parte delle cellule che esprimono HAND1 erano di origine cardiomiocitaria (come mostrato dal marcatore specifico per i cardiomiociti TNNT2). Al contrario, molte delle cellule che esprimono HAND2 non hanno espresso il marcatore dei cardiomiociti (Figura 3B). Questa osservazione è in accordo con gli organoidi precardiaci derivati da ESC di topo che dimostrano lo sviluppo di cellule non miocitarie da cellule progenitrici SHF16. È importante notare che i dati di sequenziamento dell'RNA mostrano che i trascritti di RNA sia per HAND1 che per HAND2 sono stati espressi dal giorno 3 in poi, con il marcatore FHF che è più altamente espresso tra i giorni 3 e 11 e il marcatore SHF è più altamente espresso dopo il giorno 13 (Figura 3C).
La colorazione a immunofluorescenza ha rivelato la presenza di marcatori di vari lignaggi di tipo cellulare che compongono il cuore umano. Tessuto miocardico (identificabile utilizzando il marcatore cardiomiocitario specifico TNNT2) adiacente al tessuto epicardico (marcato dal fattore di trascrizione nucleare WT1 e dal marcatore della membrana epiteliale TJP1) (Figura 4A). Le cellule endocardiche che esprimono NFATC1 sono state rilevate rivestendo le pareti di strutture interne simili a camere all'interno degli organoidi (Figura 4B). Le cellule endoteliali in una rete simile a un vaso possono essere viste già al giorno 13 della differenziazione (Figura 4C). Infine, riportiamo la presenza di fibroblasti cardiaci mescolati in tutto l'organoide (Figura 4D). Questi marcatori di tipo cellulare sono stati osservati anche nei profili di espressione genica RNA-Seq (Figura 4E). La composizione dei tipi di cellule negli organoidi, misurata dall'area dell'organoide che occupano, è risultata essere ~ 58% di cardiomiociti, con il resto composto da cellule cardiache non miocitarie, tra cui cellule epicardiche (~ 15%), cellule endocardiche (~ 13%), fibroblasti cardiaci (~ 12%) e cellule endoteliali (~ 1%) (Figura 4F).
La funzione elettrofisiologica degli organoidi è stata misurata mediante imaging di calcio vivo di singole cellule in organoidi interi. L'intensità di fluorescenza del fluo-4 varia nel tempo a causa dell'ingresso e dell'uscita del calcio dalla cellula, rivelando potenziali d'azione regolari (Figura 5A). Le mappe di calore che mostrano le intensità di calcio su una regione ad alto ingrandimento dell'organoide mostrano l'aumento dell'intensità a causa dei transitori di calcio nelle singole cellule (Figura 5B e Video 3).
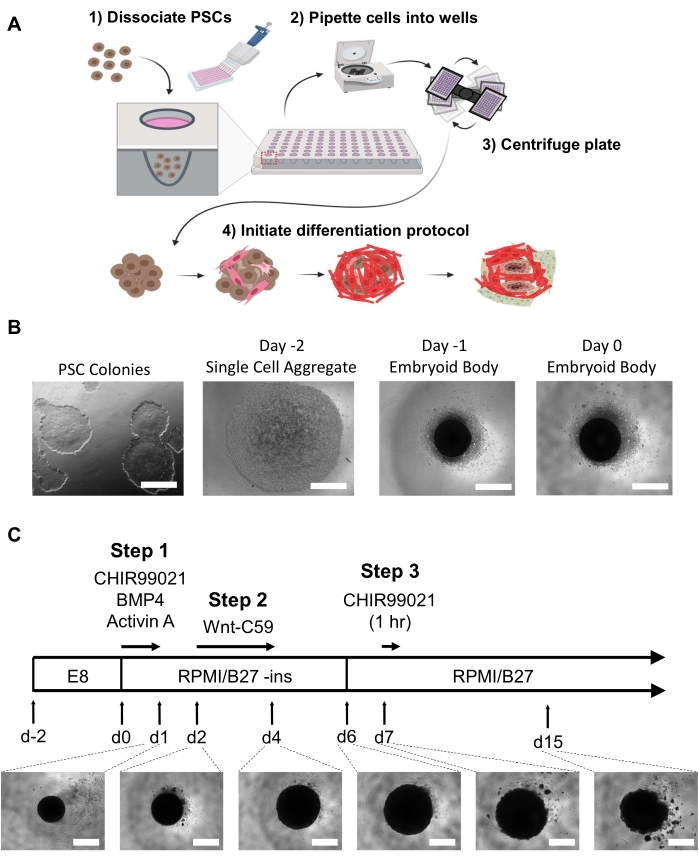
Figura 1: Generazione del corpo embrionale e fasi di differenziazione degli organoidi cardiaci. (A) (1-2) Le cellule dissociate vengono seminate nei pozzetti di una piastra di attacco ultra-bassa a 96 pozzetti tramite una pipetta multicanale. (3) La piastra a 96 pozzetti viene quindi centrifugata, il che consente alle cellule di aggregarsi al centro. (4) Nel corso del tempo, a seguito dell'aggiunta di fattori di crescita e modulatori di percorso, il corpo embrioide inizia a differenziarsi in diversi lignaggi cardiaci e forma popolazioni cellulari distinte spazialmente e fisiologicamente rilevanti che circondano le microcamere interne. (B) Immagini rappresentative della progressione della generazione del corpo embrioide, che inizia con la coltura iPSC a 2 dimensioni (a sinistra) e termina con un corpo embrioide day 0 (a destra); barra di scala = 500 μm. (C) Riassunto del protocollo di differenziazione degli organoidi del cuore umano, compresi i modulatori e gli inibitori delle vie chimiche con i rispettivi punti temporali, durate e lo sviluppo di immagini organoidi in microscopia ottica dal giorno 1 al giorno 15; barra della scala = 500 μm. Fare clic qui per visualizzare una versione più grande di questa figura.
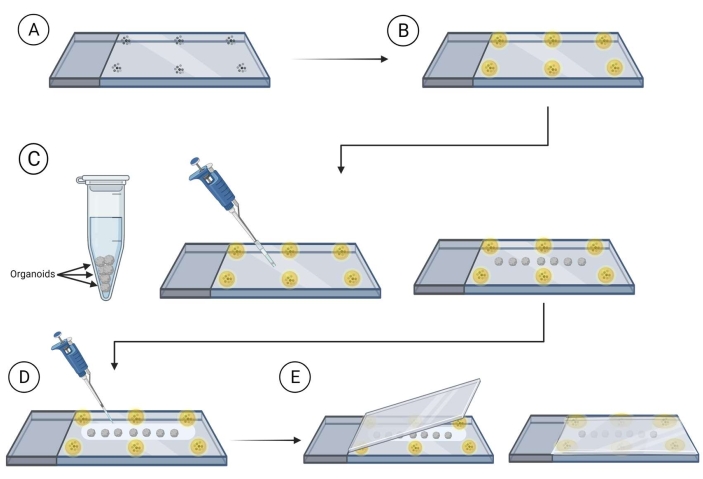
Figura 2: Montaggio di organoidi interi su vetrini per l'imaging. Passaggi per la preparazione di vetrini e il montaggio di organoidi per l'imaging. (A) Posizionamento di microsfere alla periferia di un vetrino. (B) Coprire le microsfere con un mezzo di montaggio. (C) Trasferire gli organoidi sul vetrino tra le perline e rimuovere il liquido in eccesso che circonda gli organoidi. (D) Coprire gli organoidi con un mezzo di compensazione/montaggio. (E) Posizionare il coperchio sopra il vetrino con organoidi e perline. Fare clic qui per visualizzare una versione più grande di questa figura.

Figura 3: La specifica del primo campo cardiaco e del secondo campo cardiaco negli hHO ricapitola lo sviluppo fisiologico del cuore umano. (A) Immagini di immunofluorescenza confocale dal giorno 3 al giorno 11 hHO che mostrano la formazione di FHF (HAND1, in alto) e SHF (HAND2, in basso), cardiomiociti (TNNT2) e colorante nucleare DAPI; barre di scala = 500 μm. (B) Immagini ad alto ingrandimento degli organoidi del giorno 7 che mostrano la co-localizzazione di HAND1 e HAND2 con il marcatore cardiomiocitario TNNT2; barre di scala = 50 μm. (C) Profili di espressione genica RNA-Seq del marcatore FHF HAND1 (rosso) e del marcatore SHF HAND2 (blu) dal giorno 0 al giorno 19. Abbreviazioni: hHOs = organoidi cardiaci umani; FHF = primo campo cardiaco; SHF = secondo campo cardiaco; HAND = derivati del cuore e della cresta neurale espressi; TNNT2 = troponina cardiaca T2; DAPI = 4',6-diamidino-2-fenilindolo. Fare clic qui per visualizzare una versione più grande di questa figura.

Figura 4: gli hHO sviluppano lignaggi cardiaci multipli. (A-D) Immagini di immunofluorescenza confocale del giorno 15 hHO che mostrano la formazione di cardiomiociti (TNNT2) e la colorazione con colorante nucleare DAPI in cellule cardiache non miocitarie. (A) Organoide intero e alto ingrandimento del marcatore epicardico WT1 (verde) e del marcatore della membrana epiteliale TJP1 (bianco) che mostra cellule epicardiche di origine epiteliale sulla parte superiore e adiacente al tessuto miocardico; scala bar = 500 μm, inserto = 50 μm. (B) Marcatore endocardico NFATC1 (verde) espressione sul rivestimento delle camere; barra di scala = 500 μm. (C) Rete di vasi endoteliali in hHOs mostrati da PECAM1 (verde). Barra della scala = 500 μm. (D) Marcatori dei fibroblasti cardiaci THY1 e VIM mostrati rispettivamente in verde e bianco distribuiti in tutto l'organoide. Scala bar = 500 μm. (E) Profili di espressione genica RNA-Seq dei principali tipi cellulari presenti negli hHO dai giorni 0 a 19 di differenziazione. Abbreviazioni: hHOs = organoidi cardiaci umani; TNNT2 = troponina cardiaca T2; DAPI = 4',6-diamidino-2-fenilindolo; WT1 = fattore di trascrizione tumore-1 di Wilm; NFATC1 = fattore nucleare citoplasmatico delle cellule T attivate; PECAM1 = molecola di adesione delle cellule endoteliali piastriniche-1; VIM = vimentina. (F) Grafico a torta della composizione media del tipo di tessuto in hHO, calcolato come area percentuale con il rispettivo marcatore cellulare su un intero organoide mediante colorazione nucleare su tre piani z in tutto l'organoide usando ImageJ. Fare clic qui per visualizzare una versione più grande di questa figura.

Figura 5: Registrazioni transitorie di calcio vivo Fluo-4 in organoidi cardiaci umani vivi. (A) Registrazioni transitorie rappresentative di calcio di singoli cardiomiociti all'interno di organoidi interi. (B) Mappa termica che mostra livelli di calcio bassi e di picco tra i potenziali d'azione determinati dall'intensità di Fluo-4; barre di scala = 10 μm. Fare clic qui per visualizzare una versione più grande di questa figura.
Video 1: Imaging dal vivo di organoidi rappresentativi derivati da hPSC al giorno 6 di differenziazione al microscopio ottico a temperatura ambiente. Abbreviazione: hPSC = cellula staminale pluripotente umana. Clicca qui per scaricare questo video.
Video 2: Imaging dal vivo di organoidi rappresentativi derivati da hPSC al giorno 15 di differenziazione al microscopio ottico a temperatura ambiente. Abbreviazione: hPSC = cellula staminale pluripotente umana. Clicca qui per scaricare questo video.
Video 3: Registrazione dal vivo dell'organoide del giorno 10 che mostra la mappa di calore dei transienti di calcio al microscopio a fluorescenza. Clicca qui per scaricare questo video.
Discussione
I recenti progressi nei cardiomiociti derivati da cellule staminali umane e in altre cellule di origine cardiaca sono stati utilizzati per modellare lo sviluppo del cuore umano22,24,25 e la malattia26,27,28 e come strumenti per lo screening di terapie29,30 e agenti tossici31,32 . Qui riportiamo un protocollo facile da implementare e altamente riproducibile per generare e differenziare gli EB in hHO altamente complessi. Questo protocollo ha avuto successo in più linee cellulari, tra cui hPSC e hESCs23, mostrando frequenze di battimento coerenti e organizzazione del tipo di cellula. Questo protocollo trae aspetti dai protocolli precedentemente descritti per la differenziazione dei cardiomiociti24, la differenziazione delle cellule epicardiche22 e gli organoidi precardiaci derivati dalle ESC di topo16 e ottimizza la modulazione graduale della segnalazione WNT canonica utilizzando inibitori chimici e fattori di crescita in un mezzo completamente definito. Diverse metodologie di ottimizzazione sono state impiegate nella generazione di questo protocollo.
In primo luogo, le concentrazioni e le durate di esposizione degli inibitori chimici, nonché l'aggiunta di fattori di crescita, sono state ottimizzate per l'ambiente 3D e sono discusse in lavori precedenti23. Questi sono stati ottimizzati per chiarire strutture con complessità fisiologica e rappresentazione del cuore umano in vivo, con composizione fisiologica e rapporti tra cardiomiociti e tipi di cellule cardiache non miocitarie (cellule epicardiche, fibroblasti cardiaci). In secondo luogo, la strategia di cambio medio di due terzi consente un'agitazione minima degli EB / organoidi, poiché si trovano in sospensione vicino al fondo del pozzo, facilitando anche un'esposizione graduale a inibitori chimici e fattori di crescita quando il mezzo viene rinfrescato. La combinazione della differenziazione del mesoderma cardiaco attraverso l'attivazione della via Wnt, seguita dall'inibizione24, e la successiva induzione della specifica proepicardiale tramite una seconda attivazione della via Wnt22, consente a un singolo protocollo di produrre hHO altamente complessi. Gli organoidi crescono fino a 1 mm dopo 15 giorni di differenziazione e possono essere facilmente trasferiti per analisi e saggi vivi o fissi. In terzo luogo, date le grandi dimensioni degli organoidi, l'uso di microsfere o altre strutture simili per mantenere lo spazio tra la diapositiva e il coverslip è stato trovato per preservare meglio la struttura 3D degli organoidi e migliorare il processo di imaging.
Questo modello di cuore umano in via di sviluppo consente l'accesso a stadi altrimenti inaccessibili dello sviluppo cardiaco, come le specifiche del primo e del secondo campo cardiaco precoce - osservate tra i giorni 3 e 9 di differenziazione - e l'organizzazione in cellule progenitrici cardiache che danno origine a tessuti cardiaci, tra cui il miocardio, l'endocardio, l'epicardio, la vascolarizzazione endoteliale e i fibroblasti cardiaci di supporto, che sono stati osservati il giorno 15 della differenziazione. I tipi di tessuto presenti negli organoidi cardiaci derivati da questo protocollo sono altamente rappresentativi del cuore fetale umano sia nella composizione33 che nel profilo trascrittomico23,34. Possono quindi facilitare le interazioni tessuto-tessuto e cellula-cellula di ordine superiore simili a quelle del cuore in vivo. Questo protocollo era altamente efficiente e riproducibile attraverso esperimenti e linee cellulari, producendo organoidi che comprendono principalmente cardiomiociti e includono cellule cardiache non miocitarie, come cellule epicardiche, cellule endocardiche, fibroblasti cardiaci e cellule endoteliali, che rappresentano la composizione fisiologica23,33,35.
Le analisi dell'ultrastruttura dei cardiomiociti in formazione tramite microscopia elettronica a trasmissione e lo sviluppo di camere e di una rete vascolare tramite tomografia a coerenza ottica e imaging confocale sono discusse in dettaglio in lavori precedenti23. Un grande vantaggio di questo protocollo organoide cardiaco rispetto ad altri protocolli esistenti recentemente pubblicati17,18,19,20,36,37 è la robusta formazione di una rete endoteliale in tutto l'organoide, consentendo la capacità di indagare lo sviluppo vascolare e la malattia nel cuore umano precoce, senza la necessità di ulteriori induzioni esterne al protocollo. Infine, l'analisi funzionale degli organoidi cardiaci è realizzabile attraverso vari approcci, tra cui l'uso di un colorante sensibile al calcio per tracciare i transitori di calcio nei cardiomiociti attraverso l'organoide. Utilizzando la microscopia ad alta risoluzione, abbiamo registrato l'intensità di fluorescenza delle cellule in entrata e in uscita dal calcio e osservato potenziali d'azione altamente rappresentativi. Altri possibili metodi di analisi funzionale includono l'uso di una linea transgenica con un indicatore sensibile al calcio o la registrazione diretta utilizzando un array di microelettrodi23.
Gli organoidi cardiaci qui descritti sono riepilogativi del cuore fetale umano in via di sviluppo, ma sono limitati nel dimostrare caratteristiche più mature e adulte. I protocolli futuri potrebbero basarsi sul protocollo qui descritto per indurre la maturazione in questi organoidi e produrre costrutti che modellano meglio il cuore adulto. Inoltre, questo protocollo è progettato per creare modelli in miniatura del cuore umano ed è limitato a studi di ricerca sullo sviluppo cardiaco e sulle malattie o per lo screening farmaceutico e potrebbe non essere adatto come mezzo di intervento clinico come la sostituzione del tessuto cardiaco tramite trapianto. Nel complesso, descriviamo qui un protocollo facile da seguire ed economico per generare organoidi cardiaci umani altamente riproducibili e sofisticati che possono facilitare studi di ricerca sullo sviluppo del cuore umano, l'eziologia della malattia e lo screening farmacologico.
Divulgazioni
Gli autori non hanno conflitti di interesse da dichiarare.
Riconoscimenti
Questo lavoro è stato supportato dal National Heart, Lung, and Blood Institute del National Institutes of Health con i numeri di premio K01HL135464 e R01HL151505 e dall'American Heart Association con il numero di premio 19IPLOI34660342. Desideriamo ringraziare il MSU Advanced Microscopy Core e il Dr. William Jackson presso il Dipartimento di Farmacologia e Tossicologia della MSU per l'accesso ai microscopi confocali, al Nucleo di Microscopia QI e al Nucleo di Genomica MSU per i servizi di sequenziamento. Desideriamo anche ringraziare tutti i membri dell'Aguirre Lab per i loro preziosi commenti e consigli.
Materiali
| Name | Company | Catalog Number | Comments |
| Antibodies | |||
| Alexa Fluor 488 Donkey anti- mouse | Invitrogen | A-21202 | 1:200 |
| Alexa Fluor 488 Donkey anti- rabbit | Invitrogen | A-21206 | 1:200 |
| Alexa Fluor 594 Donkey anti- mouse | Invitrogen | A-21203 | 1:200 |
| Alexa Fluor 594 Donkey anti- rabbit | Invitrogen | A-21207 | 1:200 |
| Alexa Fluor 647 Donkey anti- goat | Invitrogen | A32849 | 1:200 |
| HAND1 | Abcam | ab196622 | Rabbit; 1:200 |
| HAND2 | Abcam | ab200040 | Rabbit; 1:200 |
| NFAT2 | Abcam | ab25916 | Rabbit; 1:100 |
| PECAM1 | DSHB | P2B1 | Rabbit; 1:50 |
| TNNT2 | Abcam | ab8295 | Mouse; 1:200 |
| THY1 | Abcam | ab133350 | Rabbit; 1:200 |
| TJP1 | Invitrogen | PA5-19090 | Goat; 1:250 |
| VIM | Abcam | ab11256 | Goat; 1:250 |
| WT1 | Abcam | ab89901 | Rabbit; 1:200 |
| Media and Reagents | |||
| Accutase | Innovative Cell Technologies | NC9464543 | cell dissociation reagent |
| Activin A | R&D Systems | 338AC010 | |
| B-27 Supplement (Minus Insulin) | Gibco | A1895601 | insulin-free cell culture supplement |
| B-27 Supplement | Gibco | 17504-044 | cell culture supplement |
| BMP-4 | Gibco | PHC9534 | |
| Bovine Serum Albumin | Bioworld | 50253966 | |
| CHIR-99021 | Selleck | 442310 | |
| D-(-)-Fructose | Millipore Sigma | F0127 | |
| DAPI | Thermo Scientific | 62248 | 1:1000 |
| Dimethyl Sulfoxide | Millipore Sigma | D2650 | |
| DMEM/F12 | Gibco | 10566016 | |
| Essential 8 Flex Medium Kit | Gibco | A2858501 | pluripotent stem cell (PSC) medium containing 1% penicillin-streptomycin |
| Fluo4-AM | Invitrogen | F14201 | |
| Glycerol | Millipore Sigma | G5516 | |
| Glycine | Millipore Sigma | 410225 | |
| Matrigel GFR | Corning | CB40230 | Basement membrane extracellular matrix (BM-ECM) |
| Normal Donkey Serum | Millipore Sigma | S30-100mL | |
| Paraformaldehyde | MP Biomedicals | IC15014601 | Powder dissolved in PBS Buffer – use at 4% |
| Penicillin-Streptomycin | Gibco | 15140122 | |
| Phosphate Buffer Solution | Gibco | 10010049 | |
| Phosphate Buffer Solution (10x) | Gibco | 70011044 | |
| Polybead Microspheres | Polysciences, Inc. | 73155 | 90 µm |
| ReLeSR | Stem Cell Technologies | NC0729236 | dissociation reagent for hPSCs |
| RPMI 1640 | Gibco | 11875093 | |
| Thiazovivin | Millipore Sigma | SML1045 | |
| Triton X-100 | Millipore Sigma | T8787 | |
| Trypan Blue Solution | Gibco | 1525006 | |
| VECTASHIELD Vibrance Antifade Mounting Medium | Vector Laboratories | H170010 | |
| WNT-C59 | Selleck | NC0710557 | |
| Other | |||
| 1.5 mL Microcentrifuge Tubes | Fisher Scientific | 02682002 | |
| 15 mL Falcon Tubes | Fisher Scientific | 1495970C | |
| 2 mL Cryogenic Vials | Corning | 13-700-500 | |
| 50 mL Reagent Reservoirs | Fisherbrand | 13681502 | |
| 6-Well Flat Bottom Cell Culture Plates | Corning | 0720083 | |
| 8 Well chambered cover Glass with #1.5 high performance cover glass | Cellvis | C8-1.5H-N | |
| 96-well Clear Ultra Low Attachment Microplates | Costar | 07201680 | |
| ImageJ | NIH | Image processing software | |
| Kimwipes | Kimberly-Clark Professional | 06-666 | laboratory wipes |
| Micro Cover Glass | VWR | 48393-241 | 24 x 50 mm No. 1.5 |
| Microscope Slides | Fisherbrand | 1255015 | |
| Moxi Cell Counter | Orflo Technologies | MXZ001 | |
| Moxi Z Cell Count Cassette – Type M | Orflo Technologies | MXC001 | |
| Multichannel Pipettes | Fisherbrand | FBE1200300 | 30-300 µL |
| Olympus cellVivo | Olympus | For Caclium Imaging, analysis with Imagej | |
| Sorvall Legend X1 Centrifuge | ThermoFisher Scientific | 75004261 | |
| Thermal Mixer | ThermoFisher Scientific | 13-687-717 | |
| Top Coat Nail Varish | Seche Vite | Can purchase from any supermarket |
Riferimenti
- Hoffman, J. I. E., Kaplan, S. The incidence of congenital heart disease. Journal of the American College of Cardiology. 39 (12), 1890-1900 (2002).
- Wu, W., He, J., Shao, X. Incidence and mortality trend of congenital heart disease at the global, regional, and national level, 1990-2017. Medicine. 99 (23), 20593 (2020).
- Fahed, A. C., Gelb, B. D., Seidman, J. G., Seidman, C. E. Genetics of congenital heart disease: the glass half empty. Circulation Research. 112 (4), 707-720 (2013).
- Lancaster, M. A., et al. Cerebral organoids model human brain development and microcephaly. Nature. 501 (7467), 373-379 (2013).
- Mansour, A. A., et al. An in vivo model of functional and vascularized human brain organoids. Nature Biotechnology. 36, 432-441 (2018).
- Homan, K. A., et al. Flow-enhanced vascularization and maturation of kidney organoids in vitro. Nature Methods. 16 (3), 255-262 (2019).
- Uchimura, K., Wu, H., Yoshimura, Y., Humphreys, B. D. Human pluripotent stem cell-derived kidney organoids with improved collecting duct maturation and injury modeling. Cell Reports. 33 (11), 108514 (2020).
- Serra, D., et al. Self-organization and symmetry breaking in intestinal organoid development. Nature. 569, 66-72 (2019).
- Mithal, A., et al. Generation of mesenchyme free intestinal organoids from human induced pluripotent stem cells. Nature Communications. 11, 215 (2020).
- Porotto, M., et al. Authentic modeling of human respiratory virus infection in human pluripotent stem cell-derived lung organoids. mBio. 10 (3), 00723 (2019).
- Dye, B. R., et al. In vitro generation of human pluripotent stem cell derived lung organoids. Elife. 4, 05098 (2015).
- Mun, S. J., et al. Generation of expandable human pluripotent stem cell-derived hepatocyte-like liver organoids. Journal of Hepatology. 71 (5), 970-985 (2019).
- Vyas, D., et al. Self-assembled liver organoids recapitulate hepatobiliary organogenesis in vitro. Hepatology. 67 (2), 750-761 (2018).
- Dossena, M., et al. Standardized GMP-compliant scalable production of human pancreas organoids. Stem Cell Research & Therapy. 11, 94 (2020).
- Georgakopoulos, N., et al. Long-term expansion, genomic stability and in vivo safety of adult human pancreas organoids. BMC Developmental Biology. 20 (1), 4 (2020).
- Andersen, P., et al. Precardiac organoids form two heart fields via Bmp/Wnt signaling. Nature Communications. 9, 3140 (2018).
- Rossi, G., et al. Capturing cardiogenesis in gastruloids. Cell Stem Cell. 28 (2), 230-240 (2021).
- Lee, J., et al. In vitro generation of functional murine heart organoids via FGF4 and extracellular matrix. Nature Communications. 11 (1), 4283 (2020).
- Drakhlis, L., et al. Human heart-forming organoids recapitulate early heart and foregut development. Nature Biotechnology. 39 (6), 737-746 (2021).
- Hofbauer, P., et al. Cardioids reveal self-organizing principles of human cardiogenesis. Cell. 184 (12), 3299-3317 (2021).
- Bao, X., et al. Directed differentiation and long-term maintenance of epicardial cells derived from human pluripotent stem cells under fully defined conditions. Nature Protocols. 12 (9), 1890-1900 (2017).
- Bao, X., et al. Long-term self-renewing human epicardial cells generated from pluripotent stem cells under defined xeno-free conditions. Nature Biomedical Engineering. 1, 0003 (2016).
- Lewis-Israeli, Y., et al. Self-assembling human heart organoids for the modeling of cardiac development and congenital heart disease. Nature Communications. 12, 5142 (2021).
- Lian, X., et al. Robust cardiomyocyte differentiation from human pluripotent stem cells via temporal modulation of canonical Wnt signaling. Proceedings of the National Academy of Sciences of the United States of America. 109 (27), 1848-1857 (2012).
- Burridge, P. W., Keller, G., Gold, J. D., Wu, J. C. Production of de novo cardiomyocytes: Human pluripotent stem cell differentiation and direct reprogramming. Cell Stem Cell. 10 (1), 16-28 (2012).
- Hashem, S. I., et al. Impaired mitophagy facilitates mitochondrial damage in Danon disease. Journal of Molecular and Cellular Cardiology. 108, 86-94 (2017).
- Sun, N., et al. Patient-specific induced pluripotent stem cells as a model for familial dilated cardiomyopathy. Science Translational Medicine. 4 (130), (2012).
- Stroud, M. J., et al. Luma is not essential for murine cardiac development and function. Cardiovascular Research. 114 (3), 378-388 (2018).
- Liang, P., et al. Drug screening using a library of human induced pluripotent stem cell-derived cardiomyocytes reveals disease-specific patterns of cardiotoxicity. Circulation. 127 (16), 1677-1691 (2013).
- Mills, R. J., et al. Functional screening in human cardiac organoids reveals a metabolic mechanism for cardiomyocyte cell cycle arrest. Proceedings of the National Academy of Sciences of the United States of America. 114 (40), 8372-8381 (2017).
- Braam, S. R., et al. Prediction of drug-induced cardiotoxicity using human embryonic stem cell-derived cardiomyocytes. Stem Cell Research. 4 (2), 107-116 (2010).
- Burridge, P. W., et al. Human induced pluripotent stem cell-derived cardiomyocytes recapitulate the predilection of breast cancer patients to doxorubicin-induced cardiotoxicity. Nature Medicine. 22 (5), 547-556 (2016).
- Pinto, A. R., et al. Revisiting cardiac cellular composition. Circulation Research. 118 (3), 400-409 (2017).
- Bertero, A., et al. Dynamics of genome reorganization during human cardiogenesis reveal an RBM20-dependent splicing factory. Nature Communications. 10 (1), 1538 (2019).
- Gilbert, S. F. Lateral plate mesoderm: Heart and Circulatory System. Developmental Biology. 6th edition. , 591-610 (2000).
- Richards, D. J., et al. Human cardiac organoids for the modelling of myocardial infarction and drug cardiotoxicity. Nature Biomedical Engineering. 4 (4), 446-462 (2020).
- Lewis-Israeli, Y. R., Wasserman, A. H. Heart Organoids and Engineered Heart Tissues: Novel Tools for Modeling Human Cardiac Biology and Disease. Biomolecules. 1277, (2021).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Tutti i diritti riservati
Utilizziamo i cookies per migliorare la tua esperienza sul nostro sito web.
Continuando a utilizzare il nostro sito web o cliccando “Continua”, accetti l'utilizzo dei cookies.