Method Article
תצפית ישירה ומדידה אוטומטית של תגובות סטומאטליות למזרקי Pseudomonas PV . עגבניה DC3000 ב Arabidopsis thaliana
In This Article
Summary
כאן, אנו מציגים שיטה פשוטה לתצפית ישירה ומדידה אוטומטית של תגובות סטומאטליות לפלישת חיידקים ב - Arabidopsis thaliana. שיטה זו ממנפת מכשיר הדמיה סטומטלי נייד, יחד עם צינור ניתוח תמונה המיועד לתמונות עלים שצולמו על ידי המכשיר.
Abstract
סטומטות הן נקבוביות מיקרוסקופיות המצויות באפידרמיס עלי הצמח. ויסות הצמצם הסטומטלי חיוני לא רק לאיזון ספיגת פחמן דו-חמצני לצורך פוטוסינתזה ואיבוד מים טרנספירטיביים, אלא גם להגבלת פלישת חיידקים. בעוד שצמחים סוגרים פיוניות עם זיהוי חיידקים, חיידקים פתוגניים, כגון מזרקי Pseudomonas pv . עגבניה DC3000 (Pto), פתח מחדש את הפיוניות הסגורות כדי לקבל גישה לפנים העלה. בבדיקות קונבנציונליות להערכת תגובות סטומאטליות לפלישת חיידקים, קליפות אפידרמיס עלים, דיסקיות עלים או עלים מנותקים צפים על תרחיף חיידקי, ולאחר מכן נצפו פיוניות תחת מיקרוסקופ ואחריו מדידה ידנית של צמצם סטומטלי. עם זאת, בדיקות אלה מסורבלות ועשויות שלא לשקף תגובות סטומאטליות לפלישה חיידקית טבעית בעלה המחובר לצמח. לאחרונה פותח מכשיר הדמיה נייד שיכול לצפות בפיוניות על ידי צביטת עלה מבלי לנתק אותו מהצמח, יחד עם צינור ניתוח תמונה מבוסס למידה עמוקה שנועד למדוד באופן אוטומטי את הצמצם הסטומטלי מתמונות עלים שצולמו על ידי המכשיר. כאן, בהתבסס על התקדמות טכנית זו, שיטה חדשה להערכת תגובות stomatal לפלישת חיידקים Arabidopsis thaliana מוצג. שיטה זו מורכבת משלושה שלבים פשוטים: חיסון ריסוס של Pto המחקה תהליכי זיהום טבעיים, תצפית ישירה של פיוניות על עלה של צמח מחוסן Pto באמצעות מכשיר הדמיה נייד, ומדידה אוטומטית של צמצם stomatal על ידי צינור ניתוח תמונה. שיטה זו שימשה בהצלחה כדי להדגים סגירה סטומטית ופתיחה מחדש במהלך פלישת Pto בתנאים המחקים באופן הדוק את האינטראקציה הטבעית בין צמחים לחיידקים.
Introduction
סטומטות הן נקבוביות מיקרוסקופיות המוקפות בזוג תאי שמירה על פני השטח של עלים וחלקים אוויריים אחרים של צמחים. בסביבות המשתנות ללא הרף, ויסות הצמצם הסטומטלי הוא מרכזי עבור צמחים כדי לשלוט בספיגת הפחמן הדו-חמצני הנדרשת לפוטוסינתזה על חשבון איבוד מים באמצעות טרנספירציה. לפיכך, כימות הצמצם הסטומטלי סייע להבנת ההסתגלות הסביבתית של הצמח. עם זאת, כימות הצמצם הסטומטלי הוא מטבעו זמן רב ומסורבל מכיוון שהוא דורש עבודה אנושית כדי לזהות ולמדוד נקבוביות סטומטליות בתמונת עלה שצולמה במיקרוסקופ. כדי לעקוף מגבלות אלה, פותחו שיטות שונות כדי להקל על כימות הצמצם הסטומטלי ב- Arabidopsis thaliana, צמח מודל המשמש באופן נרחב לחקר ביולוגיה סטומטית 1,2,3,4,5,6. לדוגמה, ניתן להשתמש בפורומטר כדי למדוד את קצב השעתוק כמדד של מוליכות סטומטלית. עם זאת, שיטה זו אינה מספקת מידע ישיר על מספר הסטומטלית והצמצם הקובעים את המוליכות הסטומטלית. מחקרים מסוימים השתמשו בטכניקות מיקרוסקופיה קונפוקלית המדגישות נקבוביות סטומאטליות באמצעות סמן אקטין פלואורסצנטי, צבע פלואורסצנטי או אוטופלואורסצנטיות של דופן התא 1,2,3,4,5. בעוד שגישות אלה מקלות על איתור פיוניות, העלות הן של הפעלת מתקן מיקרוסקופיה קונפוקלית והן של הכנת דגימות מיקרוסקופיה יכולה להוות מכשול ליישום שגרתי. בעבודה פורצת דרך של סאי ואחרים, פותח מודל רשת עצבית עמוקה למדידה אוטומטית של צמצם סטומטלי מתמונות מיקרוסקופיות בשדה בהיר של קליפות אפידרמיס A. thaliana 6. עם זאת, חידוש זה אינו פוטר חוקרים מהמשימה של הכנת קליפת אפידרמיס לתצפית מיקרוסקופית. לאחרונה, התגברו על מכשול זה על ידי פיתוח מכשיר הדמיה נייד שיכול לצפות בפיוניות על ידי צביטת עלה של A. thaliana, יחד עם צינור ניתוח תמונה מבוסס למידה עמוקה המודד באופן אוטומטי צמצם סטומטלי מתמונות עלים שצולמו על ידי המכשיר7.
סטומטות תורמות לחסינות מולדת של הצמח מפני פתוגנים חיידקיים. המפתח לתגובה חיסונית זו הוא סגירה סטומטית המגבילה את כניסת החיידקים דרך הנקבובית המיקרוסקופית אל פנים העלה, שם פתוגנים חיידקיים מתרבים וגורמים למחלות8. סגירה סטומטית נגרמת על ידי זיהוי של דפוסים מולקולריים הקשורים למיקרובים (MAMPs), מולקולות אימונוגניות המשותפות לעתים קרובות לסוג של מיקרובים, על ידי קולטני זיהוי תבניות מקומיות של קרום פלזמה (PRR)9. אפיטופ של 22 חומצות אמינו של שוטון חיידקי המכונה flg22 הוא MAMP טיפוסי הגורם לסגירה סטומטית באמצעות זיהויו על ידי PRR FLS210. כאמצעי נגד, פתוגנים חיידקיים כגון מזרקי Pseudomonas pv. עגבניה DC3000 (Pto) ו-Xanthomonas campestris pv. Vesicatoria פיתחו מנגנוני אלימות כדי לפתוח מחדש פיוניות 9,11,12. תגובות סטומאטליות אלה לפתוגנים חיידקיים נותחו באופן קונבנציונלי בבדיקות שבהן קליפות אפידרמיס עלים, דיסקיות עלים או עלים מנותקים צפים על תרחיף חיידקי, ולאחר מכן נצפו פיוניות תחת מיקרוסקופ ואחריו מדידה ידנית של צמצם סטומטלי. עם זאת, בדיקות אלה מסורבלות ועשויות שלא לשקף תגובות סטומאטליות לפלישת חיידקים טבעית המתרחשת בעלה המחובר לצמח.
כאן, מוצגת שיטה פשוטה לחקור סגירה סטומטית ופתיחה מחדש במהלך פלישת Pto במצב המחקה באופן הדוק את האינטראקציה הטבעית בין צמחים לחיידקים. שיטה זו ממנפת את מכשיר ההדמיה הנייד לתצפית ישירה על פיוניות A. thaliana על עלה המחובר לצמח המחוסן ב-Pto, יחד עם צינור ניתוח התמונה למדידה אוטומטית של צמצם סטומטלי.
Protocol
1. גידול צמחים
- כדי לשבור תרדמה, להשהות מחדש זרעי A. thaliana (Col-0) במים deionized לדגור אותם ב 4 ° C במשך 4 ימים בחושך.
- לזרוע את הזרעים על הקרקע ולגדול בחדר מצויד אור פלורסנט לבן. שמרו על תנאי הגידול הבאים: טמפרטורה של 22°C, עוצמת אור של 6,000 לוקס (כ-100 μmol/m/m/s) למשך 10 שעות, ולחות יחסית של 60%.
- בעת הצורך, השקו את הצמחים בדשן נוזלי. יש להימנע מהשקיה משבוע עד יומיים לפני החיסון ולהשקות היטב יום אחד לפני החיסון.
2. הכנת חיסון חיידקי
- פס Pto ממלאי גליצרול על מדיום King's B (KB) מוצק (20 גרם טריפטון, 1.5 גרם K2HPO4, ו 15 גרם גליצרול עבור 1 ליטר, 1.5% אגר) עם 50 מיקרוגרם / מ"ל ריפמפיצין ולדגור ב 28 ° C במשך יומיים.
- יש לחסן מושבה בודדת עד 5 מ"ל של מדיום נוזלי KB עם ריפמפיצין של 50 מיקרוגרם/מ"ל ולדגור ב-28°C עם ניעור ב-200 סל"ד עד לשלב הצמיחה הלוגריתמי המאוחר.
- צנטריפוגו את התרבית ב 6,000 x גרם במשך 2 דקות, להשליך את supernatant, ו resuspend את הגלולה ב 1 מ"ל של מים סטריליים. חזור על שלב זה פעם נוספת.
- הסר את הסופרנטנט, השהה מחדש את הגלולה ב- 1 מ"ל של חיץ פתיחת הפיוניות (25 mM MES-KOH pH 6.15, 10 mM KCl), ומדוד את OD600.
- דללו את המתלה ל-OD600 0.2 עם חיץ פתיחת פיוניות המכיל 0.04% סיליקון פעילי שטח.
3. חיסון ריסוס של חיידקים
- מיום אחד לפני החיסון ועד סוף הניסוי, יש לחשוף את הצמחים לעוצמת אור של כ-10,000 לוקס (כ-170 מיקרומול/מ"ר2/שנייה).
- כדי להבטיח שרוב הפיוניות פתוחות, יש לשמור את הצמחים על מגש מכוסה במכסה שקוף מתחת לאור לפחות 3 שעות לפני החיסון בריסוס.
- הסירו את המכסה והשתמשו במברשת אוויר כדי לרסס את הצד האבקסיאלי של העלים בתרחיף חיידקי של 2.5 מ"ל לכל שלושה צמחים על עציץ אחד.
- דגרו על הצמחים המחוסנים על מגש מכוסה במכסה שקוף כדי לשמור על לחות יחסית של כ-85%.
- רכוש תמונות של פיוניות בשעה אחת ושלוש שעות לאחר חיסון בתרסיס בשיטה המתוארת בסעיף 4.
4. תצפית ישירה על הפיוניות באמצעות מכשיר הדימות הנייד
הערה: התקן ההדמיה הסטומטלית הנייד מצויד באור LED ובמודול מצלמה ויכול לרכוש 2,592 תמונות × 1,944 (גובה × רוחב; פיקסלים) ברזולוציה של כ- 0.5 מיקרומטר לפיקסל.
- חבר את התקן ההדמיה הסטומטלית הנייד למחשב אישי (PC) המצויד בתוכנה לרכישת תמונה.
- מוציאים בעדינות אך לחלוטין טיפות מים מהעלים המחוסנים בעזרת פיסת נייר.
- פתחו את הכיסוי העליון של המכשיר, הניחו את העלה על הבמה וסגרו את הכיסוי העליון (איור 1).
- כוונן את מוקד התמונה על-ידי מניפולציה של בורג הכוונן, ולאחר מכן לחץ על הלחצן שמור תמונה במסך המחשב. התמונה תירכש באופן מיידי. בדרך כלל, תמונה ממוקדת מכילה כ-10 פיוניות הניתנות לניתוח. כדי לקבל תוצאות חזקות, רכשו תמונות סטומטליות משישה עלים של שלושה צמחים שונים (שני עלים לכל צמח).
5. מדידה ידנית של צמצם סטומטלי
הערה: ניתן להוריד את תוכנת ImageJ בכתובת https://imagej.nih.gov/ij/download.html
- פתח קובץ תמונה ב- ImageJ.
- פתח את מנהל החזר ההשקעה על-ידי בחירה באפשרות נתח כלי > > מנהל החזר ההשקעה.
- השתמש בכלי בחירת הקו הישר כדי לצייר קו המתאים לרוחב הסטומה (איור 2) ולרשום את החזר ההשקעה על-ידי לחיצה על הוסף במנהל החזר ההשקעה.
- צייר קו המתאים לאורך אותה סטומה (איור 2A) ורשום את החזר ההשקעה כמתואר בשלב 5.3.
- לחץ על מדידה במנהל החזר ההשקעה כדי למדוד את הרוחב והאורך.
- חלק את הרוחב באורך כדי לקבל את הצמצם הסטומטלי (יחס). לכימות חזק, השתמש ב- 60 פיוניות או יותר עבור כל טיפול ונקודת זמן. אל תבחרו פיוניות מוקדמות או מעורפלות לניתוח (איור 2B, C).
6. מדידה אוטומטית של צמצם סטומטלי
הערה: צינור ניתוח התמונות פועל ב- Google Colaboratory, סביבת הפעלה של שפת תכנות Python בענן. למשתמשים חייב להיות חשבון Google חוקי עם כונן Google פעיל, דפדפן Google Chrome וחיבור אינטרנט יציב כתנאי מוקדם.
- הורד את המחשב הנייד Google Colaboratory מ-Zenodo (https://doi-org.remotexs.ntu.edu.sg/10.5281/zenodo.8062528) ופתח את המחברת.
- צור עותק מקומי של המחשב הנייד ב-Google Drive על ידי לחיצה על קובץ > שמירת עותק ב-Drive. לאחר הופעת כרטיסיה חדשה, סגור בבטחה את הכרטיסיה של המחברת המקורית.
- לחץ על לחצן הפעל פעם אחת מתחת למקטע הגדרת סביבה במחברת מבלי לפתוח את בלוקי התאים כדי לייבא את הספריות הדרושות.
- הפעילו את המקטע 'הגדרות ספרייה ' כדי ליצור שלוש תיקיות המשמשות לניתוח (למשל, example_result, inference_results ודגם) ב-Google Drive.
הערה: במקרה זה, התיקיות הנקראות example_result, inference_results ו - model משמשות כספריית הורים, המאחסנות תוצאות הסקה ומודלים מאומנים, בהתאמה. מחברת זו מציגה דוגמה לבניית ספריות כהליך מייצג. כדי לשנות את השם, כתוב מחדש את הנתיב pardir, infdir או modeldir . - על פי החלק הכנת התמונות , העבר את התמונות שנרכשו ל- example_result, מקובצות בכותרות תמונות לפי טיפול או מדגם (למשל, mock_1h_XXXXXX.jpg) עבור יצירת הגרף הסופי. תמונות לדוגמה זמינות באתר Zenodo (https://doi-org.remotexs.ntu.edu.sg/10.5281/zenodo.8062528).
- בצע את החלק הורד מודלים מאומנים כדי להוריד את קבצי ONNX של הדגמים המאומנים מ- Zenodo (https://doi-org.remotexs.ntu.edu.sg/10.5281/zenodo.8062528) ולמקם אותם תחת ספריית הדגמים .
- הפעל את החלק Inference and Measurement of Stomatal Aperture כדי לכמת את הצמצם הסטומטלי מתמונות בודדות. תמונות התוצאה עם הסקה שכבת-על וקובץ csv בשם example_result.csv ייוצאו לספריית inference_results.
- הפעילו את המקטע 'יצירת תרשימים ' ליצירת גרף על יחס הצמצם הסטומטי, המיוצא לספריית inference_results .
תוצאות
לאחר חיסון ריסוס של Pto, פיוניות על עלים המחוברים לצמחים המחוסנים נצפו ישירות על ידי מכשיר הדמיה סטומטלי נייד. באמצעות מדידות ידניות ואוטומטיות, אותן תמונות עלים שימשו לחישוב צמצם סטומטלי על ידי לקיחת יחסים של רוחב לאורך של כ -60 פיוניות. מדידות ידניות ואוטומטיות הצביעו באופן עקבי על ירידה בצמצם הסטומטלי בצמחים שחוסנו ל-Pto בהשוואה לצמחים מחוסנים מדומה שעה אחת לאחר החיסון (hpi) (איור 3A,B), מה שמצביע על כך שצמחי תאליאנה נסגרים בפיוניות בתגובה לפלישת פטו. ב-3 hpi, הצמצם הסטומטי בצמחים שחוסנו ב-Pto ובצמחים שחוסנו ב-Mock היה כמעט זהה (איור 3C,D), מה שמזכיר את הפתיחה מחדש של הסטומטלית על-ידי Pto. למרבה הפלא, המדידה האוטומטית של צמצם סטומטלי ארכה רק כ-5 שניות לעיבוד תמונה אחת (טבלה 1), מה שקיצר את זמן המדידה ביותר מ-95% בהשוואה למדידה הידנית. לפיכך, פרוטוקול זה מציע אמצעי פשוט מבחינה תפעולית וחוסך עבודה כדי לעקוב אחר תגובות stomatal דינמיות של A. thaliana לפתוגן חיידקי.

איור 1: מכשיר הדמיה נייד. תמונות המתארות את מכשיר ההדמיה הנייד עם דף מוצב על הבמה (משמאל) ועם הכריכה העליונה סגורה (מימין). אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
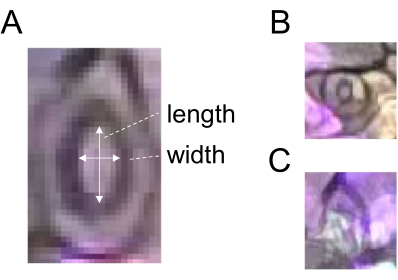
איור 2: דיאגרמה סכמטית של מדידת צמצם סטומטלי. (A) צמצם סטומטלי נקבע על ידי חישוב היחס בין רוחב לאורך סטומה, כפי שמצוין על ידי חיצים לבנים. (B) יש להוציא מהמדידה פיוניות מוקדמות ו-(ג) מעורפלות. אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.

איור 3: תגובות סטומאטליות ל-Pto בצמח שלם שלם. צמחי A. thaliana רוססו ב-mock או Pto, ופיוניות על עלים שהוצמדו לצמחים המחוסנים נצפו ישירות ב-(A,B) 1 hpi ו-(C,D) 3 hpi על ידי מכשיר הדמיה סטומטלי נייד. צמצם סטומטלי (יחס) חושב על ידי מדידות ידניות (A,C) ו-(B,D) אוטומטיות. ערכי P חושבו על ידי מבחן t דו-זנבי. אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
| זמן עיבוד (ים) | ||
| שיטת | התכוון | SD |
| ידני | 130.1 | 48.8 |
| אוטומטיות | 4.7 | 0.8 |
טבלה 1: זמן עיבוד למדידות ידניות ואוטומטיות של צמצם סטומטלי לכל תמונה. אמצעים וסטיות תקן (SD) של זמן עיבוד חושבו מתוך מדידות של תשע תמונות מייצגות.
Discussion
מחקרים קודמים השתמשו בקליפות אפידרמיס, דיסקיות עלים או עלים מנותקים כדי לחקור תגובות סטומאטליות לפלישות חיידקים 9,11,12. לעומת זאת, השיטה המוצעת במחקר זה ממנפת את מכשיר הדימות הסטומטלי הנייד כדי לצפות ישירות בפיוניות על עלה המחובר לצמח לאחר חיסון בתרסיס של Pto, המחקה תנאים טבעיים של פלישת חיידקים. בנוסף, מכיוון ששיטה זו אינה כרוכה בתהליכי הכנת דגימות הרסניים כגון ניתוק עלים, כריתת דיסק עלה וקילוף אפידרמיס, ניתן להימנע מפצעים ואיבוד מים הקשורים לתהליכי הכנת הדגימות. אין להקל ראש בהשפעות אלה, שכן פציעה ואיבוד מים מייצרים בהכרח אותות שמקורם בצמחים כגון פיטוהורמונים יסמונאט וחומצה אבסציסית המשפיעים על תנועות סטומטליות13,14.
ישנן מספר הנחיות לשימוש מיטבי במכשיר הדמיה סטומטלית נייד. ראשית, הסרה יסודית של טיפות מים ממשטחי העלים היא בעלת חשיבות עליונה לקבלת תמונות של בהירות ומיקוד אופטימליים. שנית, מומלץ לצלם תמונות מרובות מאזורי עלים זהים על ידי מניפולציה של בורג הכוונון כדי לכוונן את המיקוד. פרקטיקה זו צפויה להגדיל את מספר הפיוניות הניתנות לניתוח לכל אזור עלה, ובכך להפחית הטיות דגימה פוטנציאליות. לבסוף, כאשר צובטים עלה עם המכשיר, נדרש טיפול זהיר כדי למנוע גרימת נזק לעלה. זה קריטי מכיוון שפציעה היא אחד הרמזים שמעוררים סגירה סטומטית14.
הצמצם הסטומטלי נטה להיות משתנה יותר במדידה האוטומטית מאשר במדידה הידנית (איור 3). ישנן מספר סיבות אפשריות לכך. בעבר דווח כי נקבוביות סטומטליות המוסקות על ידי צינור ניתוח התמונה כוללות לעתים קרובות קירות תאים ו / או צללים של תאי שמירה המקיפים את נקבובית סטומטל7, מה שאינו המקרה במדידה ידנית על ידי עיניים אנושיות. סטומטות עם צורות חריגות עשויות להשפיע גם על השונות בין מדידות ידניות ואוטומטיות, אם כי מודל זיהוי הפיוניות אומן להוציא פיוניות כאלה מהניתוח7. מספר פיוניות קיבלו ערכי אפס עבור צמצם סטומטלי במדידה האוטומטית, אך אף אחת מהן לא בוצעה במדידה הידנית מסיבות לא ידועות. ייתכן שיהיה צורך בעדכונים עתידיים של המודלים כדי לטפל בבעיות אלה. עם זאת, מכיוון שמדידת הצמצם הסטומטלית האוטומטית תאמה למעשה את המדידה הידנית, הגרסה הנוכחית של צינור ניתוח התמונה היא שימושית מעשית.
התצפית הישירה והמדידה האוטומטית של צמצם סטומטלי ב- A. thaliana המתוארים במחקר זה טומנים בחובם יישומים שונים להבהרת תפקיד הפיוניות בהסתגלות סביבתית של צמחים. לדוגמה, השיטה המוצגת צריכה להיות ישימה באופן נרחב לכימות מהיר של צמצם סטומטלי במערכת צמחית שלמה שלמה לאחר חשיפה לעקות ביוטיות כגון MAMPs ופתוגנים מיקרוביאליים, כמו גם לעקות אביוטיות כגון בצורת. כדי לתמוך בכך, מחקר קודם יישם בהצלחה את צינור ניתוח התמונות כדי לכמת במדויק את הצמצם הסטומטלי של "דיסקי עלים" שטופלו ברעל הפטרייתי פוסיקוצין שגורם לפתיחת סטומטלית או בהורמון הלחץ חומצה אבסציסית שגורם לסגירת סטומטלית7. יתר על כן, באופן עקרוני, מכשיר ההדמיה הנייד מאפשר ניתוח ארוך טווח של הצמצם הסטומטלי על עלה זהה יחיד המחובר לצמח. זה עשוי לשפוך אור על היבטים חדשים של אינטראקציות צמחים-מיקרואורגניזמים מאחר שרוב המחקרים התמקדו בתגובות סטומאטליות לפתוגנים חיידקיים בשעות הראשונות של האינטראקציה 9,10,11. יהיה מעניין גם להשתמש ולשנות את השיטה המוצגת כדי לחקור תגובות סטומאטליות לפלישת חיידקים בתנאים סביבתיים שונים. זה רלוונטי במיוחד להבנת ההשפעות של גורמים סביבתיים כגון טמפרטורה, לחות וזמינות מי קרקע המשפיעים על תנועות סטומטליות והתפתחות מחלות על ידי פתוגנים חיידקיים 8,15. לסיכום, השיטה המוצגת צפויה להאיץ את המחקר על תפקודים סטומטיים באינטראקציות צמחים-מיקרואורגניזמים ומעבר להם תחת סביבות ניסוי שלא ניתן היה להשיג עד כה.
Disclosures
למחברים אין ניגודי עניינים להצהיר.
Acknowledgements
אנו מודים לכל חברי פרויקט המחקר, "יצירה משותפת של תכונות אדפטיביות צמחיות באמצעות הרכבה של הולוביונט צמחי-מיקרובי", על דיונים פוריים. עבודה זו נתמכה על ידי Grant-in-Aid for Transformative Research Areas (21H05151 ו-21H05149 עד A.M. ו-21H05152 ל-Y.T.) ו-Grant-in-Aid for Challenge Exploratory Research (22K19178 to A. M).
Materials
| Name | Company | Catalog Number | Comments |
| Agar | Nakarai tesque | 01028-85 | |
| Airbrush kits | ANEST IWATA | MX2900 | Accessory kits for SPRINT JET |
| Biotron | Nippon Medical & Chemical Instruments | LPH-411S | Plant Growth Chamber with white fluorescent light |
| Glycerol | Wako | 072-00626 | |
| Half tray | Sakata | 72000113 | A set of tray and lid |
| Hyponex | Hyponex | No catalogue number available | Dilute the solution of Hyponex at a ratio of 1:2000 in deionized water for watering plants |
| Image J | Natinal Institute of Health | Download at https://imagej.nih.gov/ij/download.html | Used for manual measurement of stomatal aperture |
| K2HPO4 | Wako | 164-04295 | |
| KCl | Wako | 163-03545 | |
| KOH | Wako | 168-21815 | For MES-KOH |
| MES | Wako | 343-01621 | For MES-KOH |
| Portable stomatal imaging device | Phytometrics | Order at https://www.phytometrics.jp/ | Takagi et al.(2023) doi: 10.1093/pcp/pcad018. |
| Rifampicin | Wako | 185-01003 | Dissolve in DMSO |
| Silwet-L77 | Bio medical science | BMS-SL7755 | silicone surfactant used in spray inoculation |
| SPRINT JET | ANEST IWATA | IS-800 | Airbrush used for spray inoculation |
| SuperMix A | Sakata seed | 72000083 | Mix with Vermiculite G20 in equal proportions for preparing soil |
| Tryptone | Nakarai tesque | 35640-95 | |
| Vermiculite G20 | Nittai | No catalogue number available | Mix with Super Mix A in equal proportions for preparing soil |
| White fluorescent light | NEC | FHF32EX-N-HX-S | Used for Biotron |
References
- Shimono, M., Higaki, T., Kaku, H., Shibuya, N., Hasezawa, S., Day, B. Quantitative evaluation of stomatal cytoskeletal patterns during the activation of immune signaling in Arabidopsis thaliana. PLoS One. 11, e0159291 (2016).
- Bourdais, G., et al. The use of quantitative imaging to investigate regulators of membrane trafficking in Arabidopsis stomatal closure. Traffic. 20 (2), 168-180 (2019).
- Higaki, T., Kutsuna, N., Hasezawa, S. CARTA-based semi-automatic detection of stomatal regions on an Arabidopsis cotyledon surface. Plant Morphology. 26 (1), 9-12 (2014).
- Eisele, J. F., Fäßler, F., Bürgel, F., Chaban, C. A. A rapid and simple method for microscopy-based stomata analyses. PLoS One. 11, e0164576 (2016).
- Chitraker, R., Melotto, M. Assessing stomatal response to live bacterial cells using whole leaf imaging. Journal of Visualized Experiments. 44, 2185 (2010).
- Sai, N., et al. StomaAI: an efficient and user-friendly tool for measurement of stomatal pores and density using deep computer vision. New Phytologist. 238 (2), 904-915 (2023).
- Takagi, M., et al. Image-based quantification of Arabidopsis thaliana stomatal aperture from leaf images. Plant and Cell Physiology. pcad018, (2023).
- Melotto, M., Zhang, L., Oblessuc, P. R., He, S. Y. Stomatal defense a decade later. Plant Physiology. 174 (2), 561-571 (2017).
- Melotto, M., Underwood, W., Koczan, J., Nomura, K., He, S. Y. Plant stomata function in innate immunity against bacterial invasion. Cell. 126 (5), 969-980 (2006).
- Zeng, W., He, S. A prominent role of the flagellin receptor FLAGELLIN-SENSING2 in mediating stomatal response to Pseudomonas syringae pv tomato DC3000 in Arabidopsis. Plant Physiology. 153 (3), 1188-1198 (2010).
- Zheng, X. Y., et al. Coronatine promotes Pseudomonas syringae virulence in plants by activating a signaling cascade that inhibits salicylic acid accumulation. Cell Host and Microbe. 11 (6), 587-596 (2012).
- Raffeiner, M., et al. The Xanthomonas type-III effector XopS stabilizes CaWRKY40a to regulate defense responses and stomatal immunity in pepper (Capsicum annuum). The Plant Cell. 34 (5), 1684-1708 (2022).
- Munemasa, S., Hauser, F., Park, J., Waadt, R., Brandt, B., Schroeder, J. I. Mechanisms of abscisic acid-mediated control of stomatal aperture. Current Opinion in Plant Biology. 28, 154-162 (2015).
- Förster, S., et al. Wounding-induced stomatal closure requires jasmonate-mediated activation of GORK K+ channels by a Ca2+ sensor-kinase CBL1-CIPK5 complex. Developmental Cell. 48 (1), 87-99 (2018).
- Cheng, Y. T., Zhang, L., He, S. Y. Plant-microbe interactions facing environmental challenge. Cell Host and Microbe. 26 (2), 183-192 (2019).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved