Method Article
תפקיד של דיפוזיה MRI המתיחה בניתוח בסיס גולגולת אנדוסקופי
* These authors contributed equally
In This Article
Summary
אנו מציגים פרוטוקול לשילוב מדרכיית MRI של דיפוזיה בעבודה של המטופל לניתוח אנדוסקופי אנדונאסלי לגידול בבסיס הגולגולת. השיטות לאימוץ מחקרי הדמיה מוחית אלה בשלבים הטרום-אופרטיביים מתוארות.
Abstract
ניתוח אנדוסקופי אנדונסאלי קיבל תפקיד בולט בניהול גידולים מורכבים בבסיס הגולגולת. זה מאפשר כריתה של קבוצה גדולה של נגעים שפירים ומאירים דרך מסלול אנטומי טבעי חוץ גולגולתי, המיוצג על ידי חללי האף, הימנעות נסיגה מוחית ומניפולציה נוירווסקולרית. זה בא לידי ביטוי על ידי ההתאוששות הקלינית המהירה של המטופלים ואת הסיכון הנמוך של sequelae נוירולוגי קבוע, המייצג את האזהרה העיקרית של ניתוח בסיס הגולגולת קונבנציונאלי. ניתוח זה חייב להיות מותאם לכל מקרה ספציפי, בהתחשב בתכונותיו ובקשריו עם המבנים העצביים שמסביב, המבוססים בעיקר על דימות מוחי לפני הניתוח. טכניקות MRI מתקדמות, כגון המתיחה, אומצו לעתים רחוקות בניתוח בסיס הגולגולת עקב בעיות טכניות: תהליכים ארוכים ומסובכים ליצירת שחזורים אמינים להכללה במערכת הנוירונים.
מאמר זה נועד להציג את הפרוטוקול המיושם במוסד ומדגיש את שיתוף הפעולה הסינרגיסטי ואת עבודת הצוות בין נוירוכירורגים לצוות הדמיה העצבית (נוירולוגים, נוירורדולוגים, נוירופסיכולוגים, פיזיקאים וביו-הנדסה) במטרה הסופית לבחור את הטיפול האופטימלי לכל מטופל, לשפר את התוצאות הניתוחיות ולקדם רפואה מותאמת אישית בתחום זה.
Introduction
האפשרות להתקרב לבסיס הגולגולת באזורים האמצעיים והפרמדיים דרך מסלול אחורי, לאמץ את פוסה האף כחללים טבעיים, ישהיסטוריהארוכה, שראשיתה יותר ממאה ואחת . עם זאת, ב -20 השנים האחרונות, ההדמיה והטכנולוגיות האופרטיביות השתפרו מספיק כדי להרחיב את האפשרות שלהם לכלול את הטיפול בגידולים המורכבים ביותר כגון מנינגיומות, אקורדומות, כונדרוסארקומות וקרניופרינגיומות1 בשל (1) הקדמה של האנדוסקופ, המעניק מבט פנורמי ומפורט 2D / 3D של אזורים אלה למנתח, (2) פיתוח מערכות נוירונים תוך ניתוחיות, ו-(3) יישום מכשירים כירורגיים ייעודיים. כפי שהוכח בקפדנות על ידי קסאם ואח ' ואושר על ידי ביקורות מרובות ומטא-ניתוחים, היתרונות של גישה כירורגית זו מיוצגים בעיקר על ידי סיכוייה לכרות גידולים מאתגרים בבסיס הגולגולת, הימנעות מכל נסיגה מוחית ישירה או מניפולציה עצבית, ובכך להפחית את הסיכון לסיבוכים כירורגיים והמשך נוירולוגי וחזותי לטווח ארוך2,3,4, 5,6,7,8,9,10,11,12.
עבור מספר גידולים בגולגולת וגידולים יותרת המוח-דיאנספליים, המטרה הכירורגית האידיאלית השתנתה בשנים האחרונות מהסרת הגידול הנרחבת ביותר האפשרית להסרה הבטוחה ביותר עם שימור התפקודים הנוירולוגיים כדי לשמור על איכות החיים של המטופל3. מגבלה זו יכולה להיות מפוצה על ידי טיפולים אדג'ובנטיים חדשניים ויעילים, כגון הקרנות (אימוץ חלקיקים מסיביים כגון פרוטון או יונים פחמן בעת הצורך) ועל ניאופלסמות נבחרות, על ידי כימותרפיה כמעכבים של מסלול BRAF / MEK עבור craniopharyngiomas13,14,15.
עם זאת, כדי לרדוף אחר מטרות אלה, הערכה טרום ניתוחית זהירה היא קריטית, כדי להתאים את האסטרטגיה הכירורגית לתכונה הספציפית של כל מקרה2. ברוב המרכזים, פרוטוקול טרום הניתוח MRI מבוצע בדרך כלל רק עם רצפים מבניים סטנדרטיים, המספקים את האפיון המורפולוגי של הנגע. עם זאת, עם טכניקות אלה לא תמיד ניתן להעריך את היחסים האנטומיים של הגידול עם מבנים סמוכיםאמין 3. יתר על כן, כל מטופל עשוי להציג פרופילי ארגון מחדש פונקציונליים שונים הנגרמים על ידי פתולוגיה הניתנים לזיהוי רק עם משטח MRI דיפוזיה ו- MRI תפקודי (fMRI), אשר ניתן להשתמש בהם כדי לספק הדרכה הן בתכנון הניתוח והן בשלבים תוך ניתוחיים16,17.
נכון לעכשיו, fMRI הוא המודאליות הדמיה המוחית הנפוצה ביותר למיפוי פעילות תפקודית המוח וקישוריות, כהנחיה לתכנון כירורגי18,19 ולשפר את התוצאה שלהחולים 20. fMRI מבוסס משימה הוא המודאליות של בחירה לזהות אזורי מוח "רהוטים" המעורבים מבחינה תפקודית בביצועי משימה ספציפיים (למשל, הקשה על האצבעות, שטף פונטי), אך אינו ישים לחקר גידולים בבסיס הגולגולת.
דיפוזיה MRI המתירה שחזור ויוו ולא פולשני של קשרים במוח החומר הלבן, כמו גם עצבים גולגולתיים, לחקור את המבנה hodological המוח21. אלגוריתמים שונים של המתיחה פותחו כדי לשחזר מסלולים אקסונליים על ידי קישור פרופילי דיפוזיה של מולקולות מים, המוערכים בתוך כל ווקסל במוח. המתיחה הדטרמיניסטית עוקבת אחר כיוון הדיפוזיה הדומיננטי, ואילו המתיחה הפרוצדורלית מעריכה את התפלגות הקישוריות של מסלולים אפשריים. בנוסף, ניתן ליישם מודלים שונים כדי להעריך דיפוזיה בתוך כל voxel, וניתן להגדיר שתי קטגוריות עיקריות: מודלים סיבים יחידים, כגון מודל טנסור דיפוזיה, שבו מוערך כיוון סיב יחיד, ומודלים מרובי סיבים, כגון דה-קונבולציה כדורית, שבהם משוחזרים מספר כיוונים של סיבים חוצים22,23. למרות הוויכוח המתודולוגי על מדרכיית MRI דיפוזיה, התועלת שלה בזרימת העבודה הנוירוכירורגית מבוססת כיום. ניתן להעריך את פריקת דרכי החומר הלבן ואת המרחק לגידול, תוך שמירה על קשרים ספציפיים של חומר לבן. יתר על כן, ניתן ליישם מפות הדמיית טנזור דיפוזיה (DTI), במיוחד אניזוטרופיה חלקית (FA) ודיפוזיה ממוצעת (MD), כדי להעריך שינויים בחומר הלבן מיקרו-מבני הקשורים לחדירה אפשרית לגידול ולניטור דרכי האורך. כל התכונות הללו הופכות את ה- MRI של דיפוזיה לכלי רב עוצמה הן לתכנון טרום ניתוחי והן לקבלת החלטות תוך-ניתוחיות באמצעות מערכות נוירונוביגציה24.
עם זאת, היישום של טכניקות המתיחה לניתוח בסיס הגולגולת הוגבל על ידי הצורך בידע טכני מיוחד ואת העבודה גוזלת זמן כדי לייעל רכישת רצף MRI דיפוזיה, פרוטוקול ניתוח, ושילוב תוצאות המתיחה במערכות neuronavigation25. לבסוף, מגבלות נוספות נובעות מהקשיים הטכניים המרחיבים ניתוחים אלה ממבני חומר לבן תוך-פרנשיליים עד לא-פרו-פריצ'ימליים, כעצבי גולגולת. ואכן, רק מחקרים אחרונים הציגו תוצאות ראשוניות המנסות לשלב ניתוח MRI ובסיס גולגולת מתקדם26,27,28.
המאמר הנוכחי מציג פרוטוקול לניהול רב תחומי של גידולים בבלוטת יותרת המוח ובסיס הגולגולת באמצעות מדרכי MRI דיפוזיה. יישום פרוטוקול זה במוסד נבע משיתוף הפעולה בין נוירוכירורגים, נוירו-אנדוקרינולוגים וצוות הדמיית המוח (כולל מומחיות קלינית וביואינפורמטיקה) כדי להציע גישה רב-צירית משולבת יעילה לחולים אלה.
במרכז שילבנו פרוטוקולים רב תחומיים לניהול מטופלים עם גידולים בבסיס הגולגולת, כדי לספק את התיאור האינפורמטיבי ביותר האפשרי, להתאים ולהתאים אישית את התוכנית הכירורגית. אנו מראים כי פרוטוקול זה יכול להיות מאומץ הן קליני ואת הגדרת המחקר עבור כל חולה עם גידול בסיס הגולגולת כדי להנחות את אסטרטגיית הטיפול ולשפר את הידע על השינויים במוח המושרה על ידי נגעים אלה.
Protocol
הפרוטוקול פועל על פי אמות המידה האתיות של ועדת המחקר המקומית ועם הצהרת הלסינקי מ-1964 והתיקונים המאוחרים יותר שלה או סטנדרטים אתיים דומים.
1. בחירת המטופלים
- לאמץ את קריטריוני ההכללה הבאים: חולים מעל גיל 18, שיתוף פעולה מלא, הצגת גידול של בסיס הגולגולת, או אזור יותרת המוח-diencephalic.
- לא לכלול חולים עם התווית נגד MRI (כלומר, קוצב לב או חומר פרומגנטי) או הצגת מצבים קליניים המתעוררים (כלומר, יתר לחץ דם תוך גולגולתי, אובדן ראייה חריף הדורש ניתוח מיידי), או נשים בהריון, או חולים עם מחלת נפש, או אלה שמסרבים במפורש להשתתף בפרוטוקול זה.
2. הכנה לבדיקת MRI
- לפני בדיקת ה-MRI, יש לנהל את טופס הבטיחות כדי לא לכלול התוויה משמעותית להזרקת סוכן הבדיקה וניגודיות: אין חומרים פרומגנטיים בגוף, הערכה של מכשירי MRI, בטוחים או מותנים, ללא קוצב לב, אין עדשות מגע עין.
- אם הסורק המשמש לרכישת MRI הוא שדה גבוה (לדוגמה, 3 T, ראה טבלת חומרים), שקול כל התוויות נגד פוטנציאליות נוספות הקשורות, למשל, להתקני גירוי עצבי.
- בדוק אם לחולה יש קלסטרופוביה.
- ודא שהמטופל קרא וחתם על טופס ההסכמה ל- MRI כדי להכיר בסיכונים וביתרונות של בדיקת ההדמיה.
- יש נוירופסיכולוג לבצע הערכה כללית והערכה נוירו-קוגניטיבית ממוקדת בהתבסס על מיקום הגידול.
- לנהל את המלאי אדינבורו כדי להעריך את הדומיננטיות של מסירות29.
3. מיקום המטופל בסורק
- תן אטמי אוזניים למטופל כדי להפחית את רעשי ה- MRI.
- תנועות ראש יכולות להשפיע על איכות ההדמיה; לכן, להשתמש רפידות קצף כדי להפחית את תנועות הראש, לשתק את הראש בתוך סליל MRI.
- ספק לחצן אזעקת חירום למטופל במקרה הצורך להפריע לבחינה.
- הפעילו את המצלמה והמיקרופון בתוך הסורק כדי לנטר, לדבר ולהאזין למטופל מחדר רכישת ה-MRI מחוץ לסורק.
4. פרמטרי הגדרת פרוטוקול MRI ורכישה של המוח
- השג סורק שדה גבוה סטנדרטי של פרוטוקול MRI מרובה מודים (1.5 T או 3T). פרמטרי הרצף הבאים מתייחסים ל- MRI 3 T, באמצעות סליל מערך בצפיפות גבוהה (64 ערוצים).
- לרכוש רצפים אנטומיים ברזולוציה גבוהה ונפחית: T1 משוקלל לפני ופוסט-gadolinium ניהול סוכן ניגודיות ו FLAIR T2 משוקלל.
- עבור תמונות משוקללל T1 ו- T2 לרכוש פרוסות קשת רציפות מתן רזולוציה איזוטרופית של 1x1x1 מ"מ3 זמן סריקה של כ 5 דקות לכל רצף.
- לרכוש רצף T2-weighted ברזולוציה גבוהה ולהתאים את אזור הגידול להדמיה עצבית גולגולתית: CISS נפחי (הפרעה בונה במצב יציב) עם ממד voxel של 0.5x0.5x0.5 מ"מ3 (זמן סריקה של כ 9 דקות).
- לרכוש רצפים משוקלל דיפוזיה באמצעות תמונות הד-planar חד זריקה אחת (EPI), ממד voxel של 2x2x2 מ"מ3, 64 כיווני מעבר צבע מגנטי עם ערך b של 2000 s/mm2, זמן הד של 98 אלפיות שני, וזמן הרפיה של 4300 ms.
- רכוש חמישה אמצעי אחסון עם ערך b null בתחילת הרכישה המשוקללת דיפוזיה עם כיוון קידוד פאזה מוגדר הקדמי-אחורי (עבור דיפוזיה משוקלל תמונות זמן סריקה כולל של 5 דקות).
- בנוסף, לרכוש שלושה אמצעי אחסון עם ערך b null אבל הפוך כיוון קידוד פאזה, אחורי-הקדמי, כדי לתקן עיוותי הדמיה עקב רכישת EPI (זמן סריקה של 42 שניות). פרוסות כמעט ציריות רציפות נרכשות.
- לרכוש רצפים נוספים כדי לחקור תכונות גידול ספציפיות, כגון MRI-ספקטרוסקופיה מרובה או יחיד-voxel מקומי באזור הגידול.
הערה: משך זמן הסריקה הכולל הוא כ-30 דקות, לא כולל הכנת המטופל לבדיקת ה-MRI.
5. תמונות MR במוח עיבוד מראש
- המר את נתוני ה- MRI מתבנית ההדמיה שאומצה על-ידי קונסולות רכישת MRI, DICOM ( .dcm), לתבנית NIFTI ( .nii) המשמשת ניתוחי הדמיה מתקדמים.
- הפעל את הפונקציה dcm2niix (https://github.com/rordenlab/dcm2niix). הגדר כקבצי קלט תמונות dicom וכפלט קבצי .nii המתאימים: T1.nii, Flair.nii, T1_contrast.nii, DTI_b2000.nii ו- DTI_b0_flip.nii.
- התקן את תוכנת FSL (https://fsl.fmrib.ox.ac.uk/fsl/fslwiki) ו- MRtrix3 (https://www.mrtrix.org) הדרושה עבור ניתוחי ההדמיה המתקדמים.
- רשום את Flair.nii ו- T1_contrast.nii לתמונת T1.nii על-ידי הפעלת הפונקציה FSL-flirt, המבצעת רישום תמונה ליניארי.
- רשום את תמונת DTI_b2000.nii ל- T1.nii על-ידי הפעלת הפונקציה FSL-epi_reg, שלוקחת בחשבון ממצאי עיוות הדמיית EPI.
- הפעל את הפונקציה FSL-topup כדי לתקן פריטי כיוונים של קידוד פאזה המציגים את תמונת DTI_b2000.nii. הגדר את רכישת קידוד השלב ההפוכה DTI_b0_flip.nii כקובץ הקלט "in_main".
- הפעל את הפונקציה MRtrix3-dwidenoise להדמיה עם מידול רעש רכיבים עיקרי.
- כדי לתקן את זרם מערבולת וחפץ הנשירה של האות, הפעל את הפונקציה FSL-eddy, ולתפקוד תקין של האות MRtrix3-dwibias.
- הפעל את פונקציית ההימור FSL כדי להסיר את אות הקרקפת המציג את תמונת T1.nii ולשנות את שם קובץ הפלט באמצעות הסיומת "_brain": T1_brain.nii.
6. פילוח גידולים
- התקן את תוכנת הצמדת איציק (http://www.itksnap.org) 30.
- לאחר התקנת תוכנת ה-ITK-snap, הקש קובץ - פתח את התמונה הראשית ובחר את תמונת T1.nii ולאחר מכן הקש על קובץ - הוסף Imager אחר והעלה את התמונות Flair.nii ו- T1_contrast.nii, הגדרת אפשרות שכבת-העל השקופה למחצה.
- בדוק את הגידול בתמונות T1.nii, Flair.nii ו- T1_contrast.nii. בחר את המישור האנטומי לעקוב בעת ציור הנגע, למשל, צירי.
- מקם את המצביע בפרוסה צירית אחת כדי להתחיל. בסרגל הכלים הראשי, בחר את סמל מפקח המצולע והתחל לצייר גבולות גידול באמצעות סגנון ציור ביד חופשית - עקומת חלקה או מצולע.
- לאחר סיום ציור היקף הגידול, סגור את העקומה המקשרת בין הנקודות הראשונות והאחרונות, הקש קבלוהמשיך לצייר בפרוסה הבאה. עבור נגעים גדולים בגידול, כדי להאיץ את תהליך הציור, דלג על כמה פרוסות ציריות (למשל, שלוש), וצייר את היקף הנגע בפרוסות משולבות.
- בסוף הציור ההיקפי הנגע, בחר כלים - תוויות אינטרפולציה, הגדר את התווית ל/ עם אינטרפולאט כמו נגע הגידול ואת האינטרפולציה לאורך ציר אחד כמו כיוון הציר ואחריו ציור גבולות הגידול.
- בחר פילוח - שמור תמונת פילוח ותן שם לפילוח הגידול כ- Tumor_mask.nii על-ידי בחירה באפשרות תבנית Nifti לשמירה.
7. ניתוח מתיחות
- הפעל את פונקציית ה- FSL-dtifit כדי לדגמן דיפוזיה ואת הכיוונים המרחביים השונים ולקבל את מפות הטנסור הבאות של דיפוזיה: FA.nii, MD.nii ו- V1.nii. להעריך מפות DTI אלה כדי לגשת לערכי דיפוזיה חריגים שעלולים להתרחש בנוכחות בצקת גידול או חדירה.
- הפעל את הפונקציה MRtrix3-tckgen עם הגדרת ברירת המחדל "ifod2" כדי לבצע מתיחות פרוצדורליסטית ולשחזר את נתיבי החומר הלבן על ידי מידול בעיות סיבים חוצים31.
- לאמץ גישה של יעד זרע על ידי הגדרת האפשרויות "-seed_image" ו-"כולל" המבוססות על ידע אנטומי של פריורי.
- צייר באופן ידני אזורי עניין (ROIs) המוגדרים כזרע או כיעד עבור המתיחה. לחלופין, השתמש ב- ROIs מבוססי אטלס. ראה מורמינה et at. 32 עבור מערכת הקרינה האופטית, היילס ואח'33 עבור כיאסם אופטי ועצבי גולגולת ראייה אופטיים, ו Testa ואח' 34 עבור דרכי הפירמידה.
- הפעל את מציג התמונות FSL-fsleyes, בחר פתחובחר תמונות לבדיקה חזותית.
- במציג FSL- fsleyes, עבור אל הגדרה - תצוגת Ortho 1 והפעל את הכלי מצב עריכה.
- לחץ על סמל העיפרון FSL-fsleyes וצייר את ההשערות על המתיחה.
- התקן את תוכנת Https://surfer.nmr.mgh.harvard.edu) של Freesurfer.
- הפעל את הפונקציה Freesurfer-Recon-all בתמונת T1.nii כדי לקבל את הפילוח האוטומטי של אזור קליפת המוח שישמש כ- ROIs של המתיחה.
- הפעל את הפונקציה FSL-epi_regregistration, הגדרת תמונת קלט T1.nii, ותמונה התייחסות DTI_b2000.nii, שמור את מטריצת פלט הרישום (T1_onto_DTI.mat).
- השתמש במטריצה T1_onto_DTI.mat שהתקבלה כדי לרשום את ההבשלה לפלח לתמונת DTI_b2000.nii.
- הפעל את המתיחה באמצעות הפונקציה MRtrix3-tckgen.
- הפעל את הפונקציה MRtrix3-tckmap כדי להמיר את פלט ה- ".tck" מייעל את פלט המתיחה בתמונה "תבנית FA.nii".
- הפעל את הפונקציה FSL-flirt כדי לרשום באופן ליניארי את תמונת T1.nii בתבנית MNI152_T1_2mm_brain.nii.
- שמור את מטריצת הפלט כ- T1_onto_MNI.mat. הפעל את הפונקציה FSL-convert_xfm הגדרת האפשרות "-concat" כמו T1_onto_MNI.mat ו- T1_onto_DTI.mat, שמור את מטריצת הפלט כ- DTI_onto_MNI.mat.
8. מתיחות: ניתוח לאורך העלונים
- לקבלת תיאור מדויק של פרמטרי DTI, השתמש באלגוריתמים לאורך העלונים, כגון האלגוריתם מבוסס Matlab שמדגים את גיאומטריית דרכי השטח עם מאפייני המפעיל הלפלאצי35.
- התקן את תוכנת Matlab (https://matlab.mathworks.com) ובקש את הקוד לאורך העלון למחברים המתפתחים35.
- לחלופין, השתמש בפונקציה MRtrix3-tcksample לניתוח לאורך העלונים מכיוון שמטלאב דורש רישיון.
תצוגה חזותית של עיבוד .3D 9
- התקן את תוכנת Surf Ice (https://www.nitrc.org/plugins/mwiki/index.php/surfice:MainPage).
- בחלונית הפקודה Surf Ice, לחץ על מתקדם - המר voxelwise כדי רשת,בחר את תמונת nifti להמרה, שמור את קובץ .obj המתקבל.
- בחלונית הפקודה Surf Ice, לחץ על קובץ - פתחובחר בקובץ .obj כדי להציג באופן חזותי את עיבוד אמצעי האחסון בתלת-ממד.
10. בדיקות קליניות טרום הניתוח
- בצע הערכה אנדוקרינולוגית ביו-הומוריסטית, המורכבת פרולקטין, TSH, freeT4, ACTH, קורטיזול, GH, LH, FSH, ובדיקות סרום סך טסטוסטרון / אסטרדיול, בהתאמה אצל גברים ונשים.
- לנתח את נפח השתן 24 שעות ביממה ואת סרום ו osmolality שתן ורמות נתרן כדי לקבוע את נוכחותו של תפל סוכרת.
- בצע הערכה עיניים, כולל מדידת חדות ראייה, הערכת שדה ראייה ממוחשבת וטומוגרפיה של קוהרנטיות אופטית ברשתית (OCT).
- בצע בדיקה גופנית נוירולוגית, עם אוסף של מידע anamnestic על עלייה במשקל, תחושת הרעב, ניטור מתמיד של טמפרטורה רקטלית כל 2 דקות במשך 24 שעות באמצעות מכשיר נייד כדי להעריך את שעון הטמפרטורה היממה, והקלטת מחזור שינה-ערות 24 שעות (כולל אלקטרואנצפלוגרמה, אלקטרו-אוקולוגרמה ימין ושמאל, אלקטרוקרדיוגרמה, ואלקטרומיוגרמה של שרירי מילוהיואיד ושרירי טיביאליס שמאל וימין)36, 37,38.
11. תכנון כירורגי
- דיון בצוות שיתוף מפגש כל מועמד חולה לניתוח, בהתבסס על התוצאות של פילוח הגידול ויחסים עם המבנים העצביים הרהוטים התפקודיים (עצבים אופטיים וכיאסם, גבעול יותרת המוח, חדר שלישי, עורק עורק ראשי פנימי, עורק עורק המוח-עורקים-עורקים עצביים עצביים (ACA-ACoA) מורכב, עורק בזיליקום, עצבים גולגולתיים III, IV, VI, גופים ממילריים, דרכי חומר לבן, ואזורים קליפתיים פונקציונליים) כדי לקבוע את הגישה הניתוחית המתאימה ביותר.
- בחר את המסדרון הכירורגי עם הסיכון המינימלי לפציעות של מבנים עצביים39.
- הגדר את אזור כריתה בטוח עבור כל מקרה, לוקליזציה של המבנה העצבי הקריטי (כגון chiasm, גוף ממילרי) שתחתי קרבתו יש לעצור את כריתת כדי למנוע נזק בלתי הפיך39.
- למזג את רצפי MRI הרלוונטיים ביותר ולייבא אותם לתוך מערכת neuronavigation של השלב האופרטיבי.
12. הכנה לניתוח
- לגרום להרדמה כללית אימוץ הרדמה תוך ורידי הכוללת עם פרופופול ו remifentanil (הוכח כי סוכני הרדמה אחרים הם בין הגורמים הקריטיים ביותר המשפיעים על אמינות ניטור תוך ניתוחי, הגדלת שיעור כוזב שלילי), הימנעות myorelaxant40.
- בצע צנרול אורו-קנה הנשימה עם גזות באורופרנקס כדי למנוע דליפת דם או נוזלים בבטן או בדרכיהנשימה 41.
- הגדר את הניטור הנוירופיזיולוגי, עם הקלטה רציפה של פוטנציאלים מוטוריים (MEPs) ופוטנציאלים מעוררים סומטוסנסוריים (SEPs) ואלקטרומיוגרפיה חופשית (EMG) לעצבים גולגולתיים.42
- יבא את נתוני ה- MRI, כולל שחזורי המתיחה, במערכת הנוירונים (טבלת החומרים).
- בחר את שיטת הרישום האלקטרומגנטית של ניתוח המוח במערכת הנוירונים.
- רשום את מערכת neuronavigation על המטופל, אימוץ טכניקת מעקב חופשי או סמנים חיצוניים.
- לשלוט בדיוק של הרישום שהושג, בדיקת המיקום של סמנים חיצוניים (כלומר, האוזן או האף) על MRI המיובא; אם התוצאה אינה מקובלת, חזור על הרישום.
- מניחים את המטופל בתנוחת ישיבה למחצה; השימוש של מייפילד כדי לתקן את הראש אינו נחוץ43.
- ניהול קורטיקוסטרואידים (flebocortid אנדובוס, מינון בהתאם למשקל המטופל) ואנטיביוטיקה (2 גרם של חומצה אמוקצילין-קלבולנית)44.
13. ניתוח אנדונוסל אנדוסקופי
- התחל עם אנדוסקופ של 0°(טבלת חומרים).
- קציר את דש האף-מחיצה45.
- בצע ספנואידטומיה הקדמית, ואחריו ספטוסטומיה אחורית ואתמוידקטומיה עם שימור הטורבינאט האמצעי, במידת האפשר43.
- פתחו את עצם סלאר ושחפת41.
- תצר את שכבת הדורה בצורת H, לאחר קרישה של הסינוס הבין-חוליני העליון41.
- תבקע את הגידול על ידי מישור ארכנואידי43.
- במרכז debulk הגידול43.
- הסר את הקפסולה שלה מהמבנים העצביים הדיאנספליים שמסביב, עוצר את כריתת הרקמה במקרה של הידבקות בגידול למבנים רהוטים שדמיינו תחת הנחיית נוירונביגציה43.
- לחקור את החלל הכירורגי עם אופטיקה זוויתית(שולחן החומרים)46.
- ודא hemostasis עם קרישה דו קוטבית או סוכנים hemostatic.
- סגרו את פתח אוסטאו-מינג'אל עם שכבה תוך גולגולתית תוך גולגולתית של תחליף דוראל43.
- מניחים שכבה תוך גולגולתית של תחליף dural, פיגומים עם שומן בטן ובסופו של דבר עצם(שולחן החומרים)43.
- כסו את הסגירה עם דש האף-ספט43.
14. בדיקה היסתולוגית
- לתקן דגימות גידול עם 10% פורמלין ולהטביע אותם בפרפין מיד לאחר הניתוח.
- חותכים רקמה לחלקים של 4 מיקרומטר עובי וכתם עם המטוקסילין ואוסין. האבחנה ההיסתולוגית חייבת להתבסס על הגרסה העדכנית ביותר של סיווג WHO של גידולי מוח (2016)47.
- בצע כתמים אימונוהיסטוכימיים דגימה על ידי מכשיר הכתמה אימונוהיסטוכימי אוטומטי, באמצעות תיוג אבידין-ביוטין ודיאמינובנזידין כריגנט גילוי. עבור craniopharyngiomas, לאמץ אנטי בטא קטנין, אנטי BRAF v600E מוטציה epitope, ונוגדנים נגד Ki67 עבור כתמים אימונוהיסטוכימיים(שולחן החומרים).
- להעריך את מדד Ki-67 באמצעות הספירה הידנית של תאים סרטניים חיוביים48.
15. ניהול מטופלים לאחר ניתוח
- להעיר את המטופל מיד לאחר הניתוח.
- שחזרו את הנשימה הספונטנית מהפה על ידי מילוי חללי האף בחומר נספג ולא נספג.
- ניטור פרמטרים חיוניים (לחץ דם, קצב לב, רוויית חמצן ומצב תודעה) במשך 6-12 השעות הבאות בטיפול נמרץ.
- לשחזר האכלה דרך הפה לאחר 12 שעות.
- בצע סריקת CT לאחר 6-9 שעות.
- לשמור על מנוחה במיטה במשך שלושה ימים עם טיפול הפרין.
- לשלוט באיזון נוזלים כל 12 שעות ולהעריך אלקטרוליטים בסרום כל 24 שעות.
- ניהול טיפול בקורטיקוסטרואידים (פלבוקורטיד אנדובני ב -24 השעות הראשונות, ולאחר מכן אצטט קורטון אוראלי 30 +15 מ"ג ליום).
- בצעו בדיקת MRI עם/בלי גדליניום תוך 72 שעות לאחר הניתוח.
- שחרר את החולה ביוםהרביעי.
16. מעקב מוקדם
- חזור על ההערכה האנדוקרינולוגית המלאה 30 יום לאחר ניתוח43.
- חזור על ההערכה הרפואת עיניים שלושה חודשים לאחר ניתוח43.
- חזור על הבדיקה הגופנית הנוירולוגית והטמפרטורה ומקצבי שינה-ערות פונקציה חקירות שלושה חודשים לאחר ניתוח46.
- בצע את ה- MRI עם / ללא גדליניום שלושה חודשים לאחר ניתוח46.
17. טיפול אדג'ובנטי
- להעריך את נוכחותה של התקדמות הגידול מוקדם, ואם הוא מצוין, להפנות את המטופל לטיפול קרינה43.
18. מעקב ארוך טווח
- חזור על ההערכות הקליניות, האנדוקרינולוגיות והרפואת עיניים מדי שנה43.
- בצע MRI שנתי עם / ללא גדליניום: במקרה של הישנות, המטופל יכול להיות מנותח מחדש ולאחר מכן התייחס הקרנות או מופנה ישירות הקרנות43.
תוצאות
אישה בת 55 הציגה ליקויים חזותיים מתקדמים. ההיסטוריה הרפואית שלה לא הייתה ראויה לציון. בהערכה עיניים, הפחתה דו-צדדית של חדות הראייה (6/10 בעין ימין ו-8/10 בעין שמאל) התגלתה, והשדה החזותי הממוחשב הראה הומיאנופיה נשיכה מלאה. לא ניכרו ליקויים נוספים בבדיקה נוירולוגית, אך החולה דיווח על אסטוניה מתמשכת ועל עלייה בתחושת הרעב והצמא בחודשיים-שלושה הקודמים, עם עלייה במשקל של 4-5 ק"ג והתעוררויות תכופות בלילה לצורך להשתין. על הערכה אנדוקרינולוגית, היפרקורטיות מרכזית וסוכרת תפלת נחשפו. המטופל טופל בקורטיקוסטרואידים (הידרוקורטיזון 30+15 מ"ג ליום ודסמופרסין 30+30 מיקרוגרם ליום). במחזור שינה-ערות של 24 שעות וניטור טמפרטורה, לא נצפו שינויים משמעותיים לאחר האופטימיזציה של הטיפול בתחליפי הורמונים.
MRI המוח הדגים גידול על-פסלרי הכובש את הבור האופטו-צ'יאזמטי ופלוש לחדר השלישי, עם מורפולוגיה פוליציסטית לא סדירה, שיפור לאחר גדליניום, החשוד כהשערה הראשונה לקרניופרינגיומה (איור 1A-C). ניתוחי הדמיה מתקדמים בוצעו, כפי שמודגם בפרוטוקול הנוכחי. פילוח ליבת הגידול הדגיש את ספיגת הגדוליניום והתכתב לנפח של 7.92 ס"מ3 (איור 1D-E).
המסלולים החזותיים היו הקריטיים ביותר להערכה בתכנון טרום ניתוחי של המטופל הזה. העלונים הפירמידליים שוחזרו גם כדי להעריך את הקורלציה המיקרו-מבנית של עליית האות שזוהתה בתמונה המשוקללת FLAIR T2 ברמה של מערכת הימין.
שחזור המתיחה של המסלול האופטי נחקר, במיוחד פריקת הצ'יאזמה האופטית בנוכחות מסת הגידול. גם עצבי הגולגולת האופטיים הדו-צדדיים שוחזרו. בממשק שבין המוח, העצמות וכלי הדם, ממצאי הרגישות לא אפשרו שחזור מלא של הסיבים המחברים את הכיאסם האופטי לעצבי הראייה(איור 2).
פרופיל הדיפוזיה של עלונים פירמידליים נחקר עם סטטיסטיקת מפת DTI לאורך עלון. ברמת הגפה האחורית הימנית של הקפסולה הפנימית, היה קיים hyperintensity משוקלל FLAIR T2 מוקד, המקביל לעלייה של 5% של מדד MD הימני (5th-7מקטעים) לעומת הצד השמאלי(איור 3).
על ידי בחינת יחסים כאלה בין גידול למבנים עצביים, נבחרה גישת ההשתלה/ טרנסוברקולום אנדוסקופית אנדוסקופית. הסרת הגידול בוצעה בטכניקה מיקרו-כירורגית של שתי ידיים. בתחילה, הגידול היה מפורק באופן מרכזי, גם ניקז את הרכיב הציסטי שלה (איור 4). לאחר מכן, ניתן היה לנתק בהדרגה את הקרניופרינגיומה מהמבנים העצביים, תוך אימוץ הארכנואיד כמישור מחשוף(איור 5). בסוף הניתוח הושגה הסרת גידול מלאה עם השימור האנטומי של ההיפותלמוס (איור 6). התיקון של הפגם האוסטאו-דוראל בוצע עם שומן בטן ודש האף-מחיצה(איור 7).
הקורס שלאחר הניתוח היה ללא אירועים מיוחדים, והמטופל שוחרר לאחר ארבעה ימים בתנאים הקליניים הנכונים. הגידול התברר להיות craniopharyngioma אדמנטינומטי (WHO כיתה 1) בבדיקה היסתולוגית.
המטופל פיתח פאנהיפופיטאריות מלאה במעקב והיה תחת טיפול החלפה מלא עם הידרוקורטיזון, דסמופרסין ולבוטירוקסין. ליקויים חזותיים נסוגו לחלוטין, ולא זוהו שינויים בבדיקה נוירולוגית, מחזור שינה-ערות 24 שעות ביממה וניטור טמפרטורה. שלושה חודשים של MRI במוח הדגימו הסרת גידול מלאה, ללא שריד או הישנות. לכן, לא הומלץ על טיפול אדג'ובנטי, והמטופל נמצא במעקב אחר בדיקות קליניות ונוירודיולוגיות שנתיות(איור 8).

איור 1. רצפי MRI אנטומיים לפני הניתוח (F/55 שנים). תצוגה צירית של T1 משוקלל (A) ו FLAIR T2 משוקלל (B); צירי(C, D)ו sagittal (E) T1 - לאחר ניהול גדליניום (0.1 מ"מ / קילוגרם). פילוח הגידול (אדום) עם התמונה המשוקללת T1 המשופרת של גדליניום מוצג ב- D ו- E. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 2. עיבוד תלת-ממדי טרום-הפעלה של מסלולים אופטיים, מדרכיה ופיילוח גידולים. (A)פרוסה צירית של התמונה המשוקללת FLAIR T2 מכסת את המתיחה של כיאסם אופטי, מקומית באופן עורירי לגידול. (B)עיבוד נפח תלת-ממדי של התמונה המשוקללת FLAIR T2, בחירת מישור צירי ו- overlaid המסלולים האופטיים המתיחה. (C)עיבוד נפח תלת- ממדי של פני המוח, מסלולים אופטיים, וסגמנטציה של גידולים באדום. כל דרכי ההתייעלות של הלוחות נצבעות במפת הצבעים של כיווני ה-RGB (אדום: לרוחב-לרוחב, ירוק: אחורי-אחורי וכחול: נחות-מעולה). אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
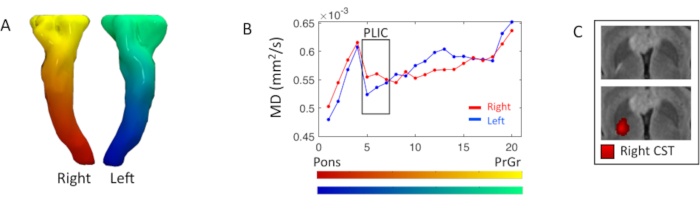
איור 3. ניתוח מדד DTI לאורך הפירמידה לאורך העלון. (A)עיבוד תלת-ממדי של דרכי הפירמידה הדו-צדדיות או מערכת הקורטיקוספינל (CST), הנצבעת בהתבסס על שיפוע הפילוח הנחות-עליון של לפלאציה. (B)פרופילי CST מימין (אדום) ושמאל (כחול) פירושם דיפוזיה (MD) הנובעים מחלוקת החלקה של העלון לעשרים מקטעים המוצגים במפות הצבעים ב- A; מקטעים מתחילים ברמה של pons לכיוון gyrus precentral (PrCr). הקופסה השחורה מדגישה את המקטעים בגפה האחורית של הקפסולה הפנימית (PLIC) (5-7th). (C)תצוגה צירית של תמונה משוקללת FLAIR T2 ברמת PLIC, עם ובלי מפת הקישוריות הנכונה של CST, שבה עוצמה אדומה בהירה יותר תואמת לצפיפות התייעלות גבוהה יותר. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 4. תמונות אנדוסקופיות תוך-מבצעיות. (A)0° היקף, לאחר פתיחת dural, הגידול נותק בתחילה על ידי chiasm, אימוץ arachnoid כמישור מחשוף. (B) ו (C),לאחר מכן, זה היה debulked מרכזי, ואת הציסטה היה מנוקז בהדרגה. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 5. תמונות אנדוסקופיות תוך-מבצעיות. (A)0° היקף, craniopharyngioma הוא בקע על ידי המישור arachnoidal בעזרת neuronavigation, מראה את הגידול ואת המבנים העצביים (מזוהה על פי הפרוטוקול הנוכחי שלנו). לכן, ניתן לחסוך את הגופים הממילריים כדי למנוע נזקים היפותלמיים קבועים. (B) ו - (C)לאחר מכן, ניתן היה לכרות את הגידול על ידי המשטח ההיפותלמי המהודל, תוך הימנעות ממתיחה כלשהי שלא לפגוע במבנה העצבי הזה. (D)במהלך הסרת החלק התוך חדרי של הגידול, טיפול מסוים שולם בפתיחה מחדש של אמת המים המוחית ומונרו פורמינה כדי למנוע הידרוצפלוס חריף לאחר הניתוח. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
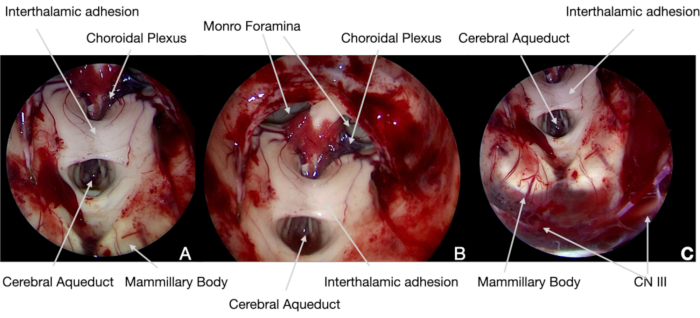
איור 6. תמונות אנדוסקופיות תוך-מבצעיות. (A) ו (B) היקף 30°, בסוף הניתוח, המבנה העצבי של החדר3 rd נחקר עם אופטיקה זוויתית כדי לאשר את הסרת הגידול המלא ולהדגים את שלמותו האנטומית. (C)בתחתית השדה הכירורגי, ניתן היה לזהות את CN III, תחת קרום ליליקוויסט: תפקידו, כמו MEPs, SEPs, ו- CNs אחרים, נשלט ברציפות עם ניטור נוירופיזיולוגי תוך ניתוחי. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 7. תמונות אנדוסקופיות תוך-מבצעיות. (A)היקף של 0°, סגירת פגם אוסטאו-dural דורש טכניקה רב שכבתית, אימוץ תחליף dural, שומן בטן, בסופו של דבר עצם, ודש naso-septal. השכבה הראשונה נוצרת על ידי מיקום תוך גולגולתי של השכבה הראשונה של תחליף dural. (B)השלב הבא מיוצג על ידי מיקום שומן בבטן כדי למלא את החלל הכירורגי; יש לשלם טיפול מסוים כדי למנוע אריזת יתר. (C)השכבה השנייה של תחליף dural מאומצת כדי לכסות את השומן, וזה יכול להישמר בעמדה בזכות פיגום נוקשה, כמו חתיכת עצם או סחוס (טכניקת אטם אטם). (D)לבסוף, דש האף-septal או השתלה חופשית של מחיצה או טורבינט באמצע משמש כדי לכסות את הסגירה הרב שכבתית. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 8. MRI, מבט קשתי T1 משוקלל לאחר מתן גדליניום (0.1 מ"מ/ק"ג). (A)MRI לפני הניתוח מדגים את הגידול. (B)לאחר הניתוח, הסרת הגידול המלאה עם השימור האנטומי של גופי המלילארי והמבנים ההיפותלמיים נראים לעין. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
Discussion
היישום של הפרוטוקול המוצג הביא לטיפול בטוח ויעיל של אחד הגידולים תוך גולגולתיים המאתגרים ביותר כגון craniopharyngioma פולש לחדר 3rd, אולי לפתוח אופק חדש עבור נגע שהוגדר על ידי H. Cushing לפני כמאה שנה כמו neoplasm תוך גולגולתי מבלבל ביותר1. השילוב של תכנון טרום ניתוחי מדויק, שילוב טכניקות MRI מתקדמות והערכות קליניות רב תחומיות אפשרו לנולהתאיםאת האסטרטגיה הניתוחית, לזהות את המסדרון הכירורגי המתאים ביותר ולמזער את הסיכון לנזק למבנה העצבי 2,49,50,51. שלא כמו פרוטוקולי MRI אחרים שדווחו בספרות, הכללת רצפים מהירים, כגון סריקות קידוד הפוך שלב עבור תמונות משוקלל דיפוזיה, מאפשרת תיקוני לאחר עיבוד מתקדמים52. הליך זה תמיד צריך להיות מאומץ, במיוחד בשדה בעצימות גבוהה (למשל, 3 T ומעלה) שבו עיוותי הדמיה קיימים.
יתר על כן, השימוש בגישה של מדרכיה פרוצדורלית המבוססת על דקונסטרוקציה כדורית מוגבלת אפשר עלייה באיכות שחזור הסיבים בהשוואה למודלים דטרמיניסטיים אחרים53. חוץ מזה, העיבוד 3D המוצע, ניתוחים כמותיים הגדילו את הדיוק של הערכת המטופל לפני הניתוח. מחקר הדמיה מוחית זה, יחד עם ניטור נוירופיזיולוגי, ייצג מדריך עבור המנתח, ועזר לו להחליט אם והיכן לעצור את כריתת הניתוח במטרה הסופית של הימנעות ליקויים נוירולוגיים קבועים של חולים.
ואכן, כריתת הגידול האגרסיבית ביותר עבור craniopharyngiomas ננטשה לאחרונה בהדרגה לטובת טכניקה חוסכת ההיפותלמוס, המורכבת ממעצר הגידול שהוסר לפני כל נזק עצבי קבוע54. עם זאת, בפרקטיקה קלינית סטנדרטית, זה לעתים קרובות מסובך עבור נוירוכירורג להחליט מתי לעצור את הסרת הגידול מלהשיג את כריתה בטוחה מקסימלית, לחשוף את המטופל לסיכון, מצד אחד, של השארת שארית גידול גדול מהמתוכנן או, מצד שני, של גרימת פגיעה היפותלמית קבועה, עם איכות חיים מזיקה כתוצאה מכך.
הפרוטוקול המוצג סיפק מודל של שילוב נתונים קליניים ונוירודיולוגיים שמטרתם לספק שיטה מעשית וקלה לאימוץ לניהול גידולים בבלוטת יותרת המוח ובסיס הגולגולת. עם זאת, אנו מדגישים כי הוא מציג כמה נקודות קריטיות: הצורך בציוד הולם, כגון מגנט שדה גבוה (3 T), סליל ערוץ ברזולוציה גבוהה ותוכנת הדמיה מתקדמת לפני עיבוד.
רצפי ה- MRI בפרוטוקול המוצג ניתנים לרכישה גם ב- 1.5 T, אך יש לשנות את פרמטרי הרכישה המדווחים בשלב 4 כדי להשיג יחס אות לרעש טוב: עבור רצפי דיפוזיה משוקללים, מוצע ערך b נמוך יותר (לדוגמה, 1000 s/mm2). יתר על כן, יישום הניתוחים המוצעים לדימות מוחי והכנסתם בפרקטיקה הקלינית דרשו הן מומחיות טכנית והן MRI טכנית ומדעי המחשב, בפרט לעיבוד ההדמיה. רוב התוכנה שדווחה זמינה באופן חופשי (למשל, FSL, MRtrix3), אך פיתוח צינורות homebrew נדרש כדי לנהל ערכות נתונים ספציפיות או ניתוחי הדמיה.
יתר על כן, הנקודה הקריטית הנוספת היא שלמרות שטכנולוגיה זו מייצגת תמיכה מכרעת עבור המנתח, היא לא יכלה להחליף את עקומת הלמידה שלהם. מסיבות אלה, ניתוח מתקדם זה צריך להיות שמור רק כמה או שלישוני מרכזי הפניה, מומחים מיוחדים מאוד ייעודיים.
לבסוף, המטרה העתידית היא לשפר את השחזור של מבני חומר לבן חוץ-צחיח, כעצבי גולגולת. המתיחה של מבנים אלה נפגעת כיום על ידי הממד הקטן של העצבים הגולגולתיים ועל ידי נוכחות של ממצאי רגישות שהפחיתו באופן דרמטי את אות ה- MRI לנוכחות של אוויר ועצמות55.
לסיכום, שיתוף הפעולה הסינרגיסטי בין נוירוכירורגים לצוות הדמיה מוחית חיוני למטרות קליניות ומחקריות, ומאפשר תכנון בדיוק הגבוה ביותר האסטרטגיה הכירורגית היעילה ביותר עבור כל מטופל ותורם לקידום הרפואה המותאמת אישית בתחום זה.
Disclosures
למחברים אין מה לחשוף
Acknowledgements
ברצוננו להודות לטכנאי הרדיולוגיה ולצוות האחיות של האזור הנוירורדיולוגי, IRCCS Istituto delle Scienze Neurologiche di Bologna, ולמתאם שלהם ד"ר מריה גרציה קרפלדי, על שיתוף הפעולה ביניהם.
Materials
| Name | Company | Catalog Number | Comments |
| BRAF V600E-specific clone VE1 | Ventana | ||
| Dural Substitute | Biodesign, Cook Medical | ||
| Endoscope | Karl Storz, 4mm in diameter, 18 cm in length, Hopkins II – Karl Storz Endoscopy | ||
| Immunohistochemical staining instrument | Ventana Benchmark, Ventana Medical Systems | ||
| MRI | 3T Magnetom Skyra, Siemens Health Care | ||
| Neuronavigator | Stealth Station S8 Surgical Navigation System, MEDTRONIC |
References
- Wang, A. J., Zaidi, H. A., Laws, E. D. History of endonasal skull base surgery. Journal of Neurosurgical Sciences. 60 (4), 441-453 (2016).
- Kassam, A. B., Gardner, P., Snyderman, C., Mintz, A., Carrau, R. Expanded endonasal approach: fully endoscopic, completely transnasal approach to the middle third of the clivus, petrous bone, middle cranial fossa, and infratemporal fossa. Neurosurgical Focus. 19 (1), 6(2005).
- Schwartz, T. H., Morgenstern, P. F., Anand, V. K. Lessons learned in the evolution of endoscopic skull base surgery. Journal of Neurosurgery. 130 (2), 337-346 (2019).
- Cossu, G., et al. Surgical management of craniopharyngiomas in adult patients: a systematic review and consensus statement on behalf of the EANS skull base section. Acta Neurochirurgica. 162 (5), 1159-1177 (2020).
- Komotar, R. J., Starke, R. M., Raper, D. M., Anand, V. K., Schwartz, T. H. Endoscopic endonasal compared with microscopic transsphenoidal and open transcranial resection of craniopharyngiomas. World Neurosurgery. 77 (2), 329-341 (2012).
- Clark, A. J., et al. Endoscopic surgery for tuberculum sellae meningiomas: a systematic review and meta-analysis. Neurosurgical Review. 36 (3), 349-359 (2013).
- Ditzel Filho, L. F., et al. Endoscopic Endonasal Approach for Removal of Tuberculum Sellae Meningiomas. Neurosurgical Clinics of North America. 26 (3), 349(2015).
- Labidi, M., et al. Clivus chordomas: a systematic review and meta-analysis of contemporary surgical management. Journal of Neurosurgical Science. 60 (4), 476-484 (2016).
- Cannizzaro, D., et al. Microsurgical versus endoscopic trans-sphenoidal approaches for clivus chordoma: a pooled and meta-analysis. Neurosurgical Review. , (2020).
- Fujii, T., Platt, A., Zada, G. Endoscopic Endonasal Approaches to the Craniovertebral Junction: A Systematic Review of the Literature. Journal of Neurological Surgery: Part B Skull Base. 76 (6), 480-488 (2015).
- Tubbs, R. S., Demerdash, A., Rizk, E., Chapman, J. R., Oskouian, R. J. Complications of transoral and transnasal odontoidectomy: a comprehensive review. Child's Nervous System. 32 (1), 55-59 (2016).
- Zoli, M., et al. Endoscopic approaches to orbital lesions: case series and systematic literature review. Journal of Neurosurgery. 3, 1(2020).
- Jensterle, M., et al. Advances in the management of craniopharyngioma in children and adults. Radiology and Oncology. 53 (4), 388-396 (2019).
- Roque, A., Odia, Y. BRAF-V600E mutant papillary craniopharyngioma dramatically responds to combination BRAF and MEK inhibitors. CNS Oncology. 6 (2), 95-99 (2017).
- Marucci, G., et al. Targeted BRAF and CTNNB1 next-generation sequencing allows proper classification of nonadenomatous lesions of the sellar region in samples with limiting amounts of lesional cells. Pituitary. 18 (6), 905-911 (2015).
- Silva, M. A., See, A. P., Essayed, W. I., Golby, A. J., Tie, Y. Challenges and techniques for presurgical brain mapping with functional MRI. NeuroImage Clinical. 17, 794-803 (2017).
- Duffau, H. Lessons from brain mapping in surgery for low-grade glioma: insights into associations between tumor and brain plasticity. The Lancet Neurology. 4 (8), 476-486 (2005).
- Maesawa, S., et al. Evaluation of resting state networks in patients with gliomas: connectivity changes in the unaffected side and its relation to cognitive function. PloS One. 10 (2), 0118072(2015).
- Gonen, T., et al. Intra-operative multi-site stimulation: Expanding methodology for cortical brain mapping of language functions. PloS One. 12 (7), 0180740(2017).
- Pillai, J. J. The evolution of clinical functional imaging during the past 2 decades and its current impact on neurosurgical planning. American Journal of Neuroradiology. 31 (2), 219-225 (2010).
- Bizzi, A. Presurgical mapping of verbal language in brain tumors with functional MR imaging and MR tractography. Neuroimaging Clinics of North America. 19 (4), 573-596 (2009).
- Dell'Acqua, F., Tournier, J. D. Modelling white matter with spherical deconvolution: How and why. NMR in Biomedicine. 32 (4), 3945(2019).
- Maier-Hein, K. H., et al. The challenge of mapping the human connectome based on diffusion tractography. Nature Communications. 8 (1), 1349(2017).
- Costabile, J. D., Alaswad, E., D'Souza, S., Thompson, J. A., Ormond, D. R. Current Applications of Diffusion Tensor Imaging and Tractography in Intracranial Tumor Resection. Frontiers in Oncology. 9, 426(2019).
- Jacquesson, T., et al. Full tractography for detecting the position of cranial nerves in preoperative planning for skull base surgery: technical note. Journal of Neurosurgery. , 1-11 (2019).
- Zolal, A., et al. Comparison of probabilistic and deterministic fiber tracking of cranial nerves. Journal of Neurosurgery. 127 (3), 613-621 (2017).
- Ung, N., et al. A Systematic Analysis of the Reliability of Diffusion Tensor Imaging Tractography for Facial Nerve Imaging in Patients with Vestibular Schwannoma. Journal of Neurological Part B Skull Base. 77 (4), 314-318 (2016).
- Anik, I., et al. Visual Outcome of an Endoscopic Endonasal Transsphenoidal Approach in Pituitary Macroadenomas: Quantitative Assessment with Diffusion Tensor Imaging Early and Long-Term Results. World Neurosurgery. 12, 691-701 (2018).
- Oldfield, R. C. The assessment and analysis of handedness: the Edinburgh inventory. Neuropsychologia. 9 (1), 97-113 (1971).
- Yushkevich, P. A., et al. User-Guided Segmentation of Multi-modality Medical Imaging Datasets with ITK-SNAP. Neuroinformatics. 17 (1), 83-102 (2019).
- Tournier, J. D., Calamante, F., Connelly, A. Robust determination of the fibre orientation distribution in diffusion MRI: non-negativity constrained super-resolved spherical deconvolution. NeuroImage. 35 (4), 1459-1472 (2007).
- Mormina, E., et al. Optic radiations evaluation in patients affected by high-grade gliomas: a side-by-side constrained spherical deconvolution and diffusion tensor imaging study. Neuroradiology. 58 (11), 1067-1075 (2016).
- Hales, P. W., et al. Delineation of the visual pathway in paediatric optic pathway glioma patients using probabilistic tractography, and correlations with visual acuity. Neuroimage Clinical. 11 (17), 541-548 (2017).
- Testa, C., et al. The effect of diffusion gradient direction number on corticospinal tractography in the human brain: an along-tract analysis. Magma. 30 (3), 265-280 (2017).
- Talozzi, L., et al. Along-tract analysis of the arcuate fasciculus using the Laplacian operator to evaluate different tractography methods. Magnetic Resonance Imaging. 54, 183-193 (2018).
- Zoli, M., et al. Postoperative outcome of body core temperature rhythm and sleep-wake cycle in third ventricle craniopharyngiomas. Neurosurgical Focus. 41 (6), 12(2016).
- Foschi, M., et al. Site and type of craniopharyngiomas impact differently on 24-hour circadian rhythms and surgical outcome. A neurophysiological evaluation. Autonomic Neuroscience. 208, 126-130 (2017).
- Mojón, A., Fernández, J. R., Hermida, R. C. Chronolab: an interactive software package for chronobiologic time series analysis written for the Macintosh computer. Chronobiology International. 9 (6), 403-412 (1992).
- Hardesty, D. A., Montaser, A. S., Beer-Furlan, A., Carrau, R. L., Prevedello, D. M. Limits of endoscopic endonasal surgery for III ventricle craniopharyngiomas. Journal of Neurosurgical Sciences. 62 (3), 310-321 (2018).
- Lee, W. H., et al. Effect of Dexmedetomidine Combined Anesthesia on Motor evoked Potentials During Brain Tumor Surgery. World Neurosurgery. 123, 280-287 (2019).
- Barazi, S. A., et al. Extended endoscopic transplanum-transtuberculum approach for pituitary adenomas. British Journal of Neurosurgery. 27 (3), 374-382 (2013).
- Singh, H., et al. Intraoperative Neurophysiological Monitoring for Endoscopic Endonasal Approaches to the Skull Base: A Technical Guide. Scientifica. , 1751245(2016).
- Mazzatenta, D., et al. Outcome of Endoscopic Endonasal Surgery in Pediatric Craniopharyngiomas. World Neurosurgery. 134, 277-288 (2020).
- Milanese, L., et al. Antibiotic Prophylaxis in Endoscopic Endonasal Pituitary and Skull Base Surgery. World Neurosurgery. 106, 912-918 (2017).
- Hadad, G., et al. A novel reconstructive technique after endoscopic expanded endonasal approaches: vascular pedicle nasoseptal flap. Laryngoscope. 116 (10), 1882-1886 (2006).
- Zoli, M., et al. Cavernous sinus invasion by pituitary adenomas: role of endoscopic endonasal surgery. Journal of Neurosurgical Sciences. 60 (4), 485-494 (2016).
- Louis, D. N., et al. The 2016 World Health Organization classification of tumors of the central nervous system: a summary. Acta Neuropathologica. 131 (6), 803-820 (2016).
- Coury, J. R., Davis, B. N., Koumas, C. P., Manzano, G. S., Dehdashti, A. R. Histopathological and molecular predictors of growth patterns and recurrence in craniopharyngiomas: a systematic review. Neurosurgical Review. 43 (1), 41-48 (2020).
- Prieto, R., et al. Craniopharyngioma adherence: a comprehensive topographical categorization and outcome-related risk stratification model based on the methodical examination of 500 tumors. Neurosurgical Focus. 41 (6), 13(2016).
- Cagnazzo, F., Zoli, M., Mazzatenta, D., Gompel, J. J. V. Endoscopic and Microscopic Transsphenoidal Surgery of Craniopharyngiomas: A Systematic Review of Surgical Outcomes Over Two Decades. Journal of Neurological Surgery: part A Central European Neurosurgery. 79 (3), 247-256 (2018).
- Cavallo, L. M., et al. The endoscopic endonasal approach for the management of craniopharyngiomas: a series of 103 patients. Journal of Neurosurgery. 121, 100-113 (2014).
- Andersson, J. L., Skare, S., Ashburner, J. How to correct susceptibility distortions in spin-echo echo-planar images: application to diffusion tensor imaging. Neuroimage. 20 (2), 870-888 (2003).
- Castellano, A., Cirillo, S., Bello, L., Riva, M., Falini, A. Functional MRI for Surgery of Gliomas. Current Treatment Options in Neurology. 19 (10), 34(2017).
- Elowe-Gruau, E., et al. Childhood craniopharyngioma: hypothalamus-sparing surgery decreases the risk of obesity. Journal of Clinical Endocrinology and Metabolism. 98 (6), 2376-2382 (2013).
- Jacquesson, T., et al. Overcoming Challenges of Cranial Nerve Tractography: A Targeted Review. Neurosurgery. 84 (2), 313-325 (2019).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved