Separación de mezclas por precipitación
Fuente: Laboratorio de la Dr. Ana J. García-Sáez, Universidad de Tübingen
Mayoría de las muestras de interés es mezclas de muchos componentes diferentes. Preparación de la muestra, un paso clave en el proceso de análisis, elimina interferencias que pueden afectar el análisis. Como tal, desarrollando técnicas de separación es un esfuerzo importante no sólo en el ámbito académico, sino también en la industria.
Una forma de separar mezclas es utilizar sus propiedades de solubilidad. En este breve documento, se tratará con soluciones acuosas. La solubilidad de un compuesto de interés depende de la fuerza (1) iónica de la solución, (2) pH y temperatura (3). Mediante la manipulación de estos tres factores, una condición en la que el compuesto es insoluble puede utilizarse para eliminar el compuesto de interés del resto de la muestra. 1
Un número de parámetros puede utilizarse para separar una muestra de interés de impurezas reduciendo su solubilidad, y de una solución como un sólido, como se muestra en la figura 1. En primer lugar, la fuerza iónica de la solución puede cambiar una solubilidad de sustancias. Esto a menudo implica la adición de sal extra (también llamado Salar hacia fuera), o la adición de un Counter-ion, que forma una especie menos soluble con el compuesto de interés. 2

Figura 1. Equilibrios de solubilidad son afectados por la temperatura, fuerza iónica y pH. Un compuesto de interés (amarillo) se separa de las impurezas (rojo) cambiando su solubilidad en un solvente dado.
Puede cambiar el pH de una solución, la carga neta del compuesto. A un determinado pH, la carga neta se hace cero (también llamado punto isoeléctrico) y se convierte en el compuesto menos soluble en agua, eventualmente formando un sólido. Temperatura también afecta la solubilidad, como la mayor temperatura aumenta la solubilidad de los sólidos.
La tasa de formación sólida determina pureza relativa (figura 2). En general, el término precipitación se refiere a la formación de un sólido a un ritmo rápido, produciendo una muestra amorfa con algunas impurezas atrapadas dentro. Esto es común en salazón y procesos inducidos por el cambio de pH. Cuando este proceso se ralentiza, las impurezas no están atrapadas dentro del complejo y se produce un sólido relativamente puro. Esta técnica se emplea en la recristalización. En este proceso, un compuesto se disuelve en suficiente solvente para ser justo en el punto de saturación a una temperatura elevada. Esto saturado solución entonces es dejar enfriar lentamente. Como la solución se enfría, disminuye la solubilidad del componente, y compuesto por encima de la solubilidad forma un sólido ordenado (si no conocido como cristales) en lugar de un sólido amorfo. Impurezas en la solución no es atrapadas, el lento proceso permite la eliminación de estas impurezas en la superficie del sólido antes de que se encuentran atrapados. 1

Figura 2. Diferencia entre precipitación y recristalización.
Una vez que ha formado el sólido (como un cristal o como un precipitado), debe ser separado del resto de la mezcla. La filtración es una manera de separarlos. Este emplea un material poroso que inhibe selectivamente el paso de material sólido, pero no la solución.
Centrifugación es otra manera de separar el precipitado del resto de la mezcla. Centrifugación usa aceleración centrípeta para separar mezclas basados en sus densidades. Desde el sólido es más denso que la solución acuosa, los sedimentos sólidos en el fondo del recipiente. El sólido también se llama la pastilla y la solución acuosa, el sobrenadante. El sobrenadante puede entonces ser decantado o extraído por medio de una pipeta o jeringa. Los cristales son frágiles y centrifugación a menudo no se emplea para separar de la solución.
Este video cubre diferentes métodos de separación de compuestos a través de sólida formación (Salar hacia fuera, cambios en el pH y recristalización) y su posterior retirada de la solución acuosa por filtración o centrifugación.
1. precipitación de CaCO3
- Preparar 5 mL de 1 M de CaCl2.
- Prepare 5 mL M 1 Na2CO3.
- En un tubo de centrífuga pequeña (1,5 mL), añadir 750 μl de CaCl2 y 750 μl de Na2CO3.
- Esperar 2 minutos para la reacción ocurrir. La solución debe resultar turbia.
- Centrifugar la mezcla a 10.000 x g durante 5 minutos.
- Decantar el sobrenadante.
- Añadir 1 mL de agua fría a la pelotilla.
- Resuspender el precipitado al mezclar en un vórtex durante 10 s.
- Centrifugar la mezcla a 10.000 x g durante 5 minutos.
- Decantar el sobrenadante.
2. precipitación de proteínas de la leche
- Vierta la leche en un vaso de precipitados y agregar una barra de agitación.
- Leche caliente suavemente hasta 40 ° C en una placa de agitación. No calentar sobre 40 ° C.
- Preparar un 15% (v/v) de ácido acético por mezcla 7,5 mL de ácido acético y diluir en agua suficiente para llegar a 50 mL.
- Sumerja el electrodo de un pHmetro en leche caliente y vigilar el pH.
- Agregar el ácido acético mediante goteo a la leche hasta que se alcance un pH de 4.6.
- Filtración de la leche
- Flauta de un pedazo de papel de filtro y colocarlo en un embudo.
- Coloque el embudo en un frasco y verter la solución de leche acidificada en el embudo.
- Como la solución se vierte, el papel de filtro puede conseguir tapado. Con una varilla, se agita la solución y el papel de filtro de vez en cuando para desatascar. Si no mejora el paso de la solución, cambiar el papel de filtro.
- Coloque un nuevo filtro de papel sobre la mesa y transferencia tanto de la húmeda sólida para el nuevo papel de filtro. Esto debe absorber más agua del sólido.
- Si el nuevo papel de filtro se moja demasiado, seguir a cambiar hasta que haya una cantidad mínima de humedad en el papel de filtro. Presione ligeramente para absorber más agua si es necesario.
- Tomar el sólido seco y vuelva a suspender en cerca de 70% etanol. Filtrar el sólido otra vez siguiendo los pasos 2.6.1 a 2.6.5.
- Centrifugación de la leche (como alternativa a la filtración)
- Transferir porciones de 50 mL de la mezcla a tubos de centrífuga de 50 mL.
- Centrifugue a 4.500 × g por 10 min, luego decantar el sobrenadante.
- Añadir 50 mL de etanol de 70% para el pellet.
- Con una varilla, Resuspender el precipitado en el etanol.
- Centrifugar esta suspensión siguiente paso 2.7.2.
- Resuspender el precipitado en tampón para su posterior análisis como SDS-PAGE, de lo contrario almacenarla a 4 ° C.
3. recristalización de KCl
- Pesar 50 g de KCl en un matraz Erlenmeyer y añadir 100 mL de agua
- Calentar la mezcla hasta que el agua hierve. Asegúrese de que se disuelva todo el polvo de KCl. Algunas impurezas no se pueden disolver en agua.
- Otro matraz de Erlenmeyer (vacío) junto con la mezcla de calor y mantener muy caliente.
- Coloque un embudo con papel filtro en el matraz caliente, vacíelo.
- Verter la solución a través del papel filtro para eliminar impurezas no disueltas. El recipiente se mantiene caliente para asegurarse de que no hay cambios de temperatura ocurren durante la filtración, de lo contrario que se formará un precipitado crudo. Si esto ocurre, vuelva a calentar la mezcla hasta que se disuelva todo el precipitado.
- Retirar el matraz con la solución del fuego.
- Mantener en un lugar fresco en la habitación y deje que se enfríe lentamente durante 30 minutos, o hasta que ya no esté caliente al tacto.
- Una vez enfriado a temperatura ambiente, colocar el matraz en un baño de hielo para reducir aún más la temperatura. Alternativomente, uno puede dejar el frasco dentro de la nevera o una sala de control de temperatura a 4 ° C.
- Cristales pueden ser cosechados por filtración como en los pasos 3.4 – 3.5 (puede utilizarse un matraz y embudo a temperatura ambiente).
Equilibrios de solubilidad se emplea en muchos procesos de purificación. Calcio puede removerse del agua con carbonato de sodio. El producto de solubilidad (Ksp) de CaCO3 es 4,8 x 10-9. Mezcla de 1 M de CaCl2 y 1 M de Na2CO3 produce precipitado de CaCO3 . El precipitado fue separado del resto de la solución mediante centrifugación.
Caseína (una proteína clave en la leche) tiene un punto isoeléctrico a pH 4,6 y cuajada insoluble en este pH. La cuajada se separa del resto de la solución (también llamado suero) mediante filtración o centrifugación (figura 3a). La cuajada se lavó con etanol para eliminar los fosfolípidos y otros compuestos solubles en agua que también quedaron atrapados en la cuajada. Centrifugación previene pérdida de mejores que la filtración de proteínas ya que hay algunas proteínas que pegada al papel de filtro. Los componentes separados se analizaron mediante SDS-PAGE (figura 3b), que muestra que la reacción de precipitación separados la mayor parte de la caseína del suero de la leche. Otras proteínas de la leche, como globulinas, precipitan junto con caseína. Otras medidas pueden aplicarse para aislar caseína del resto de las proteínas.
Precipitación elimina más impurezas del sólido, sin embargo también pueden atrapar algunas impurezas dentro de la matriz. La recristalización se emplea a menudo para purificar más lejos un sólido (figura 4). En este experimento, el sólido fue mezclado con un solvente en el que el sólido no es muy soluble. Entonces fue levantada la temperatura de la mezcla al punto de ebullición del solvente y se añade bastante sólido para saturar el solvente caliente. Otras impurezas insolubles pueden quitarse mediante un paso de filtración. La solución caliente fue gradualmente enfriada a temperatura ambiente y refrigerada en baño de hielo y sala refrigerador frío. El lento proceso dio lugar a cristales en vez de precipitado amorfo. Las impurezas solubles no fueron incorporadas en el enrejado cristalino y los cristales resultantes eran relativamente más puros que el precipitado crudo. Los cristales se cosecharon entonces usar filtración y a la izquierda para secar el aire (o en vacío).
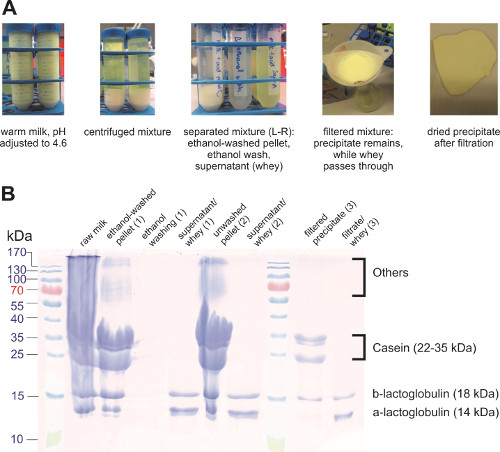
Figura 3. Precipitación de proteínas de la leche. (A) fotos de distintos pasos aislados de proteína de leche. (B) SDS-PAGE de las diferentes muestras.

Figura 4. Recristalización de KCl.
Reacciones de precipitación se aplican a muchos procesos de preparación de la muestra. Como se mencionó anteriormente, puede utilizarse para eliminar sales o iones específicos dependiendo de sus equilibrios de solubilidad. También puede utilizarse para quitar las proteínas y otras biomoléculas de mezclas.
La recristalización se emplea a menudo para purificar aún más sólidos. Este proceso elimina las impurezas atrapadas dentro del sólido. Entre otros, la recristalización puede utilizarse para purificar sales y moléculas orgánicas.
Técnicas de centrifugación y filtración son aplicables a la mayoría las demandas de preparación de muestra para separar componentes insolubles en el solvente. Filtración es de uso frecuente en química orgánica para separar compuestos cristalizados puros de su disolvente. También se utiliza después de extracciones sólido-líquido en química de productos naturales o en química analítica. Centrifugación se utiliza a menudo para separar mezclas de diferentes densidades y como se muestra aquí aplicado a la separación de componentes de la leche y la sal precipitada.
En Bioquímica, la mayoría de los procesos tales como proteínas, lípidos y ADN implica reacciones de precipitación, centrifugación y filtración métodos para purificar muestras. Y aunque la mayoría de estos procesos ha sido estandarizada completamente en kits comerciales, todavía hay mucho espacio para la optimización, como moléculas biológicas diferentes requieren diferentes condiciones.
- Kotz, J., Treichel, P., Townsend, J. Chemistry and Chemical Reactivity. 8th ed. Brooks/Cole, Belmont, CA (2012).
- Arakawa, T., Timasheff, S.N. Mechanism of Protein Salting In and Salting Out by Divalent Cation Salts: Balance between Hydration and Salt Binding. Biochemistry. 23, 5912-5923 (1984).
Saltar a...
Vídeos de esta colección:

Now Playing
Separación de mezclas por precipitación
Organic Chemistry
157.2K Vistas

Introducción a la catálisis
Organic Chemistry
34.1K Vistas

Montaje de un sistema de reflujo para reacciones químicas calientes
Organic Chemistry
166.3K Vistas

Realizar reacciones por debajo de la temperatura ambiente
Organic Chemistry
70.3K Vistas

Líneas de Schlenk para transferencia de disolventes
Organic Chemistry
41.5K Vistas

Desgasificación de líquidos con ciclos de congelación-bomba-descongelación
Organic Chemistry
55.9K Vistas

Preparación de equipos y reactivos anhidros
Organic Chemistry
79.1K Vistas

Purificación de compuestos por recristalización
Organic Chemistry
705.3K Vistas

Extracción sólido-líquida
Organic Chemistry
237.1K Vistas

Evaporación rotatoria para eliminar solventes
Organic Chemistry
212.3K Vistas

Destilación fraccionada
Organic Chemistry
332.8K Vistas

Crecimiento de cristales para el análisis de difracción de rayos x
Organic Chemistry
32.3K Vistas

Performing 1D Thin Layer Chromatography
Organic Chemistry
288.4K Vistas

Cromatografía en columna
Organic Chemistry
358.4K Vistas

Espectroscopia de resonancia magnética nuclear (RMN)
Organic Chemistry
246.7K Vistas
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados