הפרדת תערובות באמצעות משקעים
Overview
מקור: המעבדה של ד"ר אנה גארסיה-סאז — אוניברסיטת טובינגן
רוב הדגימות של עניין הם תערובות של רכיבים רבים ושונים. הכנת דוגמה, שלב מפתח בתהליך האנליטי, מסירה הפרעות שעשויות להשפיע על הניתוח. ככזה, פיתוח טכניקות הפרדה הוא מאמץ חשוב לא רק באקדמיה, אלא גם בתעשייה.
דרך אחת להפריד תערובות היא להשתמש במאפייני המסיסות שלהם. במאמר קצר זה נעסוק בפתרונות מימיים. המסיסות של תרכובת עניין תלויה (1) כוח יוני של פתרון, (2) pH, ו -(3) טמפרטורה. על ידי מניפולציה עם שלושת הגורמים האלה, מצב שבו המתחם הוא מסיס יכול לשמש כדי להסיר את תרכובת העניין משאר המדגם. 1
Principles
ניתן להשתמש במספר פרמטרים כדי להפריד מדגם של עניין ממאמצים על ידי הפחתת המסיסות שלו, והסרתו מפתרון כמוצק, כפי שמוצג באיור 1. ראשית, שינוי הכוח היוני של הפתרון יכול לשנות מסיסות חומרים. זה כרוך לעתים קרובות בתוספת של מלח נוסף (המכונה גם מלח החוצה), או תוספת של יון נגדי, אשר יוצר מינים פחות מסיסים עם תרכובת עניין. 2

איור 1. מסיסות שווי משקל מושפעים כוח יוני, pH, וטמפרטורה. תרכובת עניין (צהובה) מופרדת מ זיהומים (אדומים) על ידי שינוי המסיסות שלה בממס נתון.
שינוי ה- pH של פתרון עשוי לשנות את הטעינה נטו של המתחם. ב- pH מסוים, המטען נטו הופך לאפס (המכונה גם נקודה איזואלקטרית) והתרכובת הופכת פחות מסיסה במים, ובסופו של דבר יוצר מוצק. הטמפרטורה משפיעה גם על מסיסות, כמו טמפרטורה גבוהה יותר מגביר מסיסות של מוצקים.
קצב היווצרות מוצק קובע טוהר יחסי (איור 2). באופן כללי, המונח משקעים מתייחס להיווצרות מוצק בקצב מהיר, ובכך לייצר מדגם אמורפי עם כמה זיהומים לכודים בפנים. זה נפוץ בהמלחה החוצה ותהליכים מושרה שינוי pH. כאשר תהליך זה הואט, זיהומים אינם לכודים בתוך המתחם מוצק טהור יחסית מיוצר. טכניקה זו משמשת בנסיגה. בתהליך זה, תרכובת מומסת מספיק ממס כדי להיות רק בנקודת הרוויה בטמפרטורה גבוהה. פתרון רווי זה מותר אז להתקרר לאט. ככל שהתמיסה מתקררת, המסיסות של הרכיב פוחתת, והתרכובת העולה על המסיסות יוצרת מוצק מסודר היטב (הידוע גם כגבישים) במקום מוצק אמורפי. זיהומים בפתרון אינם נלכדים כמו התהליך האיטי מאפשר הסרת זיהומים אלה על פני השטח של המוצק לפני שהם לכודים. 1

איור 2. ההבדל בין משקעים לנסיגה.
לאחר מוצק נוצר (אם כקריסטל או כמשקעים), זה צריך להיות מופרד משאר התערובת. סינון הוא דרך אחת להפריד ביניהם. זה מעסיק חומר נקבובי אשר מעכב באופן סלקטיבי את המעבר של החומר המוצק אבל לא את הפתרון.
צנטריפוגה היא דרך נוספת להפריד את המשקעים משאר התערובת. צנטריפוגה משתמשת בתאוצה צנטריפטל להפריד תערובות בהתבסס על הצפיפות שלהם. מאז מוצק הוא צפוף יותר מאשר הפתרון מימי, משקעים מוצקים בתחתית המיכל. המוצק נקרא גם הכדור והפתרון המ מימי, סופרננט. לאחר מכן ניתן לתנודד-על או לחלץ אותו באמצעות צינור או מזרק. גבישים הם שבירים וצנטריפוגה לעתים קרובות לא מועסקת כדי להפריד אותם מהפתרון.
וידאו זה יכסה שיטות שונות של הפרדת תרכובות באמצעות היווצרות מוצקה (מלח החוצה, pH שינויים, ו recrystallization) ואת הסרתם לאחר מכן מן הפתרון מימי באמצעות סינון או צנטריפוגה.
Procedure
1. משקעים של CaCO3
- הכן 5 מ"ל של 1 M CaCl2.
- הכן 5 מ"ל 1 MNa 2CO3.
- בצינור צנטריפוגה קטן (1.5 מ"ל), להוסיף 750 μL של CaCl2 ו 750 μL של Na2CO3.
- המתן 2 דקות עד שהתגובה תתרחש. הפתרון צריך להפוך מעונן.
- צנטריפוגות התערובת ב 10,000 × גרם במשך 5 דקות.
- דקאנט סופר-טבעי.
- מוסיפים 1 מ"ל של מים קרים לכדור.
- Resuspend הכדור על ידי ערבוב במערבל מערבולת במשך 10 s.
- צנטריפוגות התערובת ב 10,000 × גרם במשך 5 דקות.
- דקאנט סופר-טבעי.
2. משקעים של חלבוני חלב
- יוצקים את החלב לתחבת ומוסיפים בר ערבוב.
- מחממים חלב בעדינות עד 40 מעלות צלזיוס בצלחת חמה ומערבבת. אין לחמם מעל 40 °C (60 °F).
- הכן 15% (v/v) של חומצה אצטית על ידי ערבוב 7.5 מ"ל של חומצה אצטית ודילול במספיק מים כדי להגיע 50 מ"ל.
- לטבול את האלקטרודה של מד pH בחלב חם, ולנטר את ה- pH.
- מוסיפים את החומצה האצטית טיפה-חכם לחלב עד pH של 4.6 הוא הגיע.
- סינון חלב
- חליל פיסת נייר סינון ומניחים אותו במשפך.
- מניחים את המשפך בבקבוקון, ויוצקים את תמיסת החלב החומצית למשפך.
- כאשר הפתרון נשפך, נייר המסנן עלול להיסתם. בעזרת מוט ערבוב, להסעיר את הפתרון ולסנן נייר מדי פעם כדי לפתוח. אם זה לא משפר את המעבר של פתרון, לשנות את נייר הסינון.
- מניחים נייר סינון חדש על הספסל העליון ומעבירים כמה שיותר מהתמצית הרטובה לנייר המסנן החדש. זה צריך לספוג יותר מים מהתמצית.
- אם נייר הסינון החדש נרטב מדי, המשיכו לשנות אותו עד שתהיה כמות מינימלית של רטיבות על נייר הסינון. לחץ עליו קלות כדי לספוג יותר מים במידת הצורך.
- קח את מוצק מיובש להשעות מחדש על 70% אתנול. סנן שוב את המוצק לאחר שלבים 2.6.1 עד 2.6.5.
- צנטריפוגה של חלב (כחלופה לסינון)
- מעבירים 50 מ"ל חלקים מהתערובת לצינורות צנטריפוגות של 50 מ"ל.
- צנטריפוגה ב 4,500 × g במשך 10 דקות, ולאחר מכן decant supernatant.
- מוסיפים 50 מ"ל 70% אתנול לכדור.
- בעזרת מוט ערבוב, יש להקנות מחדש את הכדור באתנול.
- צנטריפוגה השעיה זו בעקבות שלב 2.7.2.
- יש תחסן מחדש את הכדור במאגר לניתוח נוסף כגון SDS-PAGE, אחרת אחסן אותו ב- 4°C.
3. נסיגה של KCl
- שוקלים 50 גרם של KCl בבקבוק ארלנמייר, ומוסיפים 100 מ"ל מים
- מחממים את התערובת עד שהמים רותחים. ודאו שכל אבקת ה-KCl מומסת. זיהומים מסוימים עשויים לא להתמוסס במים.
- מחממים בקבוקון נוסף (ריק) של ארלנמאייר יחד עם התערובת ושומרים עליו חם מאוד.
- מניחים משפך עם נייר סינון בבקבוקון החם והריק.
- יוצקים את הפתרון דרך נייר הסינון כדי להסיר זיהומים לא פתורים. הבקבוקון המקבל נשמר חם כדי לוודא שלא יתרחשו שינויי טמפרטורה במהלך הסינון, אחרת ייווצר מזרז גולמי. אם זה קורה, לחמם מחדש את התערובת עד שכל המשקעים מתמוססים.
- הסר את הבקבוקון עם הפתרון מהחום.
- שמור אותו במקום קריר בחדר ולתת לו להתקרר לאט במשך כ 30 דקות, או עד שהוא כבר לא חם למגע.
- לאחר התקררות לטמפרטורת החדר, מניחים את הבקבוק באמבט קרח כדי להוריד עוד יותר את הטמפרטורה. לחלופין, ניתן להשאיר את הבקבוק בתוך המקרר או חדר מבוקר טמפרטורה בטמפרטורה של 4 מעלות צלזיוס.
- ניתן לקצור גבישים על ידי סינון כמו בשלבים 3.4-3.5 (השתמש בקבוקון משפך בטמפרטורת החדר).
Results
שווי משקל מסיס מועסק בתהליכי טיהור רבים. סידן ניתן להסיר מהמים באמצעות נתרן פחמתי. מוצר המסיסות(Ksp)של CaCO3 הוא 4.8 × 10-9. ערבוב 1 M של CaCl2 ו 1 M של Na2CO3 המיוצר CaCO3 משקעים. המשקעים הופרדו משאר הפתרון באמצעות צנטריפוגה.
קזאין (חלבון מפתח בחלב) יש נקודה איזואלקטרית ב pH 4.6 ויצר גבינה בלתי מסיסת ב- pH זה. לאחר מכן הופרדו המנסרים משאר הפתרון (המכונה גם מי גבינה) באמצעות סינון או צנטריפוגה(איור 3a). התספורת נשטפה עם אתנול כדי להסיר פוספוליפידים ותרכובות מסיסות במים אחרות שנלכדו גם הן בפח. צנטריפוגה מנעה אובדן חלבונים טוב יותר מאשר סינון שכן היו כמה חלבונים שנדבקו לנייר המסנן. הרכיבים המופרדים נותחו באמצעות SDS-PAGE (איור 3b), מה שמראה שתגובת המשקעים הפרידה בין רוב הקזאין לבין מי הגבינה. חלבוני חלב אחרים, כגון גלובולינים, מזרזים יחד עם קזאין. ניתן להחיל צעדים נוספים לבידוד קזאין משאר החלבונים.
משקעים מסיר את רוב זיהומים מן המוצק, עם זאת זה יכול גם ללכוד כמה זיהומים בתוך המטריצה. לעתים קרובות משתמשים ב-Recrystallization כדי לטהר עוד יותר מוצק(איור 4). בניסוי זה, המוצק היה מעורבב עם ממס שבו מוצק לא היה מסיס מאוד. טמפרטורת התערובת הועלתה אז לנקודת הרתיחה של הממס ומספיק מוצק מתווסף כדי להרוות את הממס החם. זיהומים בלתי מסיסים אחרים יכולים להיות מוסרים לאחר מכן באמצעות שלב סינון. הפתרון החם התקרר בהדרגה לטמפרטורת החדר והתקרר עוד יותר במקרר / חדר קר / אמבט קרח. התהליך האיטי הביא גבישים במקום משקעים אמורפיים. ההטמאות המסיסות לא שולבו בסריג הגביש והגבישים שהתקבלו היו טהורים יחסית מהמים הגסים. לאחר מכן נקצרו הגבישים באמצעות סינון והושארו להתייבש באוויר (או בוואקום).
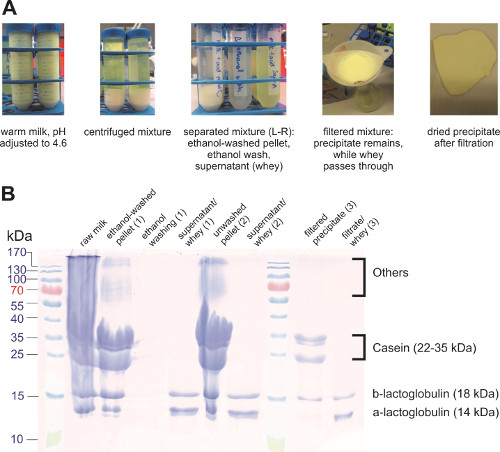
איור 3. משקעים של חלבוני חלב. (A) תמונות של שלבים שונים בבידוד חלבון חלב. (B) SDS-PAGE של הדגימות השונות.

איור 4. נסיגה של KCl.
Application and Summary
תגובות משקעים מוחלות על תהליכי הכנה מדגם רבים. כפי שהוזכר קודם לכן, הם יכולים לשמש כדי להסיר מלחים או יונים ספציפיים בהתאם שוויון המסיסות שלהם. הם יכולים לשמש גם כדי להסיר חלבונים ביומולקולים אחרים מתערובות.
Recrystallization משמש לעתים קרובות כדי לטהר עוד יותר מוצקים. תהליך זה מסיר זיהומים לכודים בתוך המוצק. בין היתר, recrystallization יכול לשמש כדי לטהר מלחים ומולקולות אורגניות.
טכניקות צנטריפוגה וסינון חלות על רוב דרישות הכנת המדגם כדי להפריד רכיבים מסיסים מן הממס. סינון משמש לעתים קרובות בכימיה אורגנית כדי להפריד תרכובות מגובשת טהורה מן הממס שלה. הוא משמש גם לאחר עקירות נוזל מוצק בכימיה מוצרים טבעיים או כימיה אנליטית. צנטריפוגה משמשת לעתים קרובות להפרדת תערובות של צפיפות שונה וכפי שמוצג כאן מוחל על הפרדה של רכיבי חלב ומלח מזרז.
בביוכימיה, רוב התהליכים כגון חלבון, שומנים בדם ובידוד DNA כרוכים בתגובות משקעים, צנטריפוגה ושיטות סינון לטיהור דגימות. ובעוד שרוב התהליכים האלה עברו תיקון מלא לערכות מסחריות, עדיין יש הרבה מקום לאופטימיזציה, שכן מולקולות ביולוגיות שונות דורשות תנאים שונים.
Disclosures
לא הוכרזו ניגודי אינטרסים.
Tags
Skip to...
Videos from this collection:

Now Playing
הפרדת תערובות באמצעות משקעים
Organic Chemistry
158.1K Views

מבוא קטליזה
Organic Chemistry
34.7K Views

הרכבה של מערכת ריפלוקס לתגובות כימיות מחוממות
Organic Chemistry
168.6K Views

ביצוע תגובות מתחת לטמפרטורת החדר
Organic Chemistry
70.7K Views

העברת קווי שלנק של ממיסים
Organic Chemistry
41.7K Views

דיית נוזלים עם רכיבה על אופניים להפשרת משאבת הקפאה
Organic Chemistry
56.4K Views

הכנת ריאגנטים וציוד נטולי מים
Organic Chemistry
79.4K Views

טיהור תרכובות על ידי תיקון
Organic Chemistry
710.6K Views

מיצוי נוזלי מוצק
Organic Chemistry
238.3K Views

אידוי סיבובי להסרת ממס
Organic Chemistry
213.0K Views

זיקוק שברים
Organic Chemistry
335.0K Views

גידול גבישים לניתוח עקיפה של קרני רנטגן
Organic Chemistry
32.9K Views

Performing 1D Thin Layer Chromatography
Organic Chemistry
290.2K Views

כרומטוגרפיה של עמודה
Organic Chemistry
361.3K Views

ספקטרוסקופיית תהודה מגנטית גרעינית (NMR)
Organic Chemistry
249.1K Views
Copyright © 2025 MyJoVE Corporation. All rights reserved