Method Article
Tıklanabilir Kafesli Bileşiklerin Tasarımı, Sentezi ve Fotokimyasal Özellikleri
Bu Makalede
Özet
Modüler kafesli bileşiklerin tıklanabilir moieties ile fotokimyasal özelliklerinin sentezi ve ölçümü için bir protokol sunulmuştur.
Özet
Kafesli bileşikler yüksek spatiotemporal çözünürlük ile hücre fizyolojisinin fotoğraf aracılı manipülasyon sağlar. Ancak, şu anda mevcut caging gruplarının sınırlı yapısal çeşitliliği ve fotolik verimliliklerinden ödün vermeden sentetik modifikasyondaki zorluklar, canlı hücre için kafesli bileşiklerin repertifesini genişletmenin önündeki engellerdir. Uygulama. Coumarin tipi foto-caging gruplarının kimyasal modifikasyonu, çeşitli fiziksel ve kimyasal özelliklere sahip kafesli bileşiklerin hazırlanması için umut verici bir yaklaşım olduğundan, değiştirilebilir tıklanabilir kafesli bileşiklerin sentezi için bir yöntem rapor ediyoruz. bakır(I)-katalize Huisgen siklizasyon yoluyla çeşitli fonksiyonel birimleri ile kolayca. Modüler platform molekülü bir (6-bromo-7-hydroxycoumarin-4-yl)metil (Bhc) grubu bir foto-caging grubu olarak içerir, hangi geleneksel 2-nitrobenzyls göre yüksek fotoliz verimliliği sergiler. Amin, alkol ve karboksilat içeren tıklanabilir kafesli bileşiklerin hazırlanması için genel prosedürler sunulmaktadır. Su çözünürlüğü ve hücre hedefleme yeteneği gibi ek özellikler kolayca tıklanabilir kafesli bileşikler dahil edilebilir. Ayrıca, fotolik kuantum verimi de dahil olmak üzere fiziksel ve fotokimyasal özellikleri ölçüldü ve ilgili Bhc kafesli bileşiklerin daha üstün olduğu bulunmuştur. Bu nedenle açıklanan protokol, mevcut kafesli bileşiklerdeki yapısal çeşitliliğin olmaması için potansiyel bir çözüm olarak düşünülebilir.
Giriş
Kafesli bileşikler, orijinal işlevleri kovalent olarak bağlı foto çıkarılabilir koruma grupları tarafından zamansal olarak maskelenen sentetik moleküller olarak tasarlanmıştır. İlginçtir, biyolojik olarak ilgili moleküllerin kafesli bileşikler hücresel fizyoloji1,2,3,4,5 spatiotemporal kontrolü için vazgeçilmez bir yöntem sağlar ,6. 1977 yılında, Engels ve Schlaeger cAMP bir membran geçirgen ve fotolabile türevi cAMP72-nitrobenzyl ester bildirdi. Ertesi yıl Kaplan, ATP'nin (NPE-ATP) 1-(2-nitrofenil)etil esterini rapor etti ve bu bileşiği "kafesli" ATP8olarak adlandırdı. O zamandan beri, fotokimyasal olarak çıkarılabilir koruma grupları 2-nitrobenzyls, p-hidroksifenil9, 2-(2-nitrofenil)ethyls10,11, 7-nitroindolin-1-yls12, 13, ve (coumarin-4-yl)metiller14,15,16 kafesli bileşiklerin hazırlanması için kullanılmıştır.
Membran geçirgenliği, suda çözünürlüğü ve hücresel hedefleme yeteneği gibi arzu edilen ek özelliklere sahip kafesli bileşiklerin sentezinin hücre biyolojik uygulamalarını kolaylaştırması beklenmektedir. Bu moleküllerin fiziksel ve fotokimyasal özellikleri öncelikle onları hazırlamak için kullanılan fotokimyasal çıkarılabilir koruma gruplarının kimyasal yapısına bağlı olduğundan, foto-caging gruplarının farklı bir repertoire gereklidir. Ancak, yüksek fotolik verimliliği sergileyen mevcut caging gruplarının yapısal çeşitliliği sınırlıdır. Bu kafesli bileşiklerin kullanımını artırmak için bir engel olabilir.
Bu sorunu gidermek için, foto-caging grupların repertuarı mevcut fotoremovable koruma gruplarının kimyasal modifikasyonu veya üstün fotofizik ve fotokimyasal özelliklere sahip yeni fotolabile kromoforların tasarımı ile genişletildi. Örnekler nitrodibenzofuran (NDBF)17, [3-(4,5-dimethoxy-2-nitrofenil)-2-butil] (DMNPB)18,19, kalsiyumduyarlı 2-nitrobenzyl fotocage20, yerine komarinylmeethyls (DEAC45021 , DEAdcCM22, 7-azetidinyl-4-methylcoumarin23, ve styryl coumarins24), siyanür türevleri (CyEt-pan)25, ve BODIPY türevleri26,27.
Buna ek olarak, daha önce (6-bromo-7-hydroxycoumarin-4-yl)metil (Bhc) grubu geliştirdik ve başarılı nörotransmitterlerin çeşitli kafesli bileşikler sentezlenmiş28, ikinci haberciler29,30, ve oligonükleotidler31,32,33 büyük bir ve iki foton uyarma kesitleri sergileyen. Ek özellikler onların Fotosensitivite ödün vermeden caging gruplarına kolayca kurulabilir, o zaman kafesli bileşiklerin repertoiregenişletilebilir 34,35,36, 37,38,39. Bu nedenle üç bölümden oluşan modüler kafesli bileşikler tasarladık, yani bir fotoğraf duyarlı çekirdek olarak Bhc grubu, ek işlevlerin kurulumu için kimyasal kolları, ve maskelenecek moleküller40, 41. yıl.
Böylece, bu makalede biyolojik olarak ilgili moleküllerin kafesli bileşiklerin hazırlanması için pratik bir yöntem sağlar. Bu protokol, foto-caging grupları için tıklanabilir bir platform hazırlanması için yöntemler açıklar, kafesli bileşiklerin repertuarGenişletmek için ek işlevlerin giriş, fiziksel ve fotokimyasal ölçümü özellikleri ve daha fazla hücresel uygulama için tıklanabilir kafesli bileşiğin hücre tipi seçici hedefleme.
Protokol
1. Tıklanabilir kafesli bileşikler için modüler caging paBhc grubunun sentezi28,41
-
(6-bromo-7-hidroksicoumarin-4-yl)metil klorür (Bhc-CH2Cl) hazırlanması
- 4-bromoresorcinol (9.742 g, 51.5 mmol) bir karıştırıcı çubuğu ile donatılmış 100 mL yuvarlak dipli şişe yerleştirin.
- Şişeye Conc. H2SO4 (%98, 30 mL) ekleyin ve karışımı eritmek için karıştırın.
- Etil 4-kloroasetasetat (10 mL, 74 mmol) damla ekleyin.
- Karışımı ortam sıcaklığında 5 gün karıştırmaya devam edin.
- Ayrıca, ezilmiş buz küplerini (~200 mL) 500 mL Erlenmeyer şişesine yerleştirin.
- Buz içine reaksiyon karışımı dökün ve ince toz çökelti elde edilene kadar 30 dakika boyunca şiddetle karıştırın.
- Vakum filtrasyon yoluyla çökelti toplamak. Açık kahverengi çökeltiyi beş kez suyla yıkayın.
- BhcCH2Cl'yi açık kahverengi toz (13,57 g, 46,9 mmol) olarak vermek için bir gecede vakum altında çökeltiyi kurulayın.
-
(6-bromo-7-hidroksicoumarin-4-yl)metanol (BhcCH2OH)
- Hazırlanan BhcCH2Cl (1,1440 g, 3,95 mmol) ve 1 M HCl (300 mL) bir Dimroth kondansatör ile donatılmış 1 L yuvarlak dipli şişe yerleştirin. Karışımı 140 °C'de 5 gün karıştırın. Bu süre sonunda karışımı ortam sıcaklığına kadar soğutun.
- BhcCH2OH(1) açık kahverengi toz (1.0359 g, 3.82 mmol, % 97 verim) olarak verim vakum altında döner buharlaşma ile reaksiyon dan su çıkarın.
NOT: BhcCH2Cl'nin 1 g'ı başına 250 mL 1 M HCl kullanılması tatmin edici bir sonuç verir.
-
Mannich reaksiyonu ile paBhcCH2OH (2) hazırlanması
- Paraformaldehit (446.4 mg, 14.9 mmol) 50 mL yuvarlak dipli bir şişeye yerleştirin. Şişeye susuz etanol (5 mL) ve N-metilpropargylamine (1,25 mL, 14,8 mmol) ekleyin.
- Ar atmosferi altında 1 saat ortam sıcaklığında karışımı karıştırın.
- BhcCH2OH(1)(1,367 g, 5,04 mmol) şişeye ekleyin. Karışımı bir blok ısıtıcı aparatı ile 80 °C'ye ısıtın ve ar atmosferi altında 80 °C'de 2 saat boyunca karışımı karıştırmaya devam edin.
- Blok ısıtıcıyı durdurun ve reaksiyon karışımını oda sıcaklığına kadar soğutun.
- Vakum filtrasyon ile ortaya çıkan açık kahverengi-sarı çökelti toplayın. Çökeltiyi az miktarda susuz etanol (her seferinde 1 mL) ile iki kez yıkayın.
- PaBhcCH2OH (2) (1,393 g, 3,96 mmol) verim için vakum altında aşırı etanol çıkarın.
2. Tıklanabilir kafesli bileşiklerin hazırlanması
NOT: Hidroksil, amino ve karboksil fonksiyonel gruplar içeren diğer tıklanabilir kafesli bileşiklerin hazırlanmasında aşağıdaki işlemler uygulanabilir.
-
Genel Prosedür 1: Tıklanabilir kafesli amin hazırlanması
- Yer paBhcCH2OH (2) (709.6 mg, 2.02 mmol) ve N,N'-karbonil diimidazol (CDI, 397.6 mg, 2.45 mmol) bir 30 mL yuvarlak dipli şişe. Kuru CH2Cl2 (6 mL) ekleyin ve çözeltiyi ortam sıcaklığında 1 saat karıştırın.
- 4-dimethylaminopyridine (4-DMAP, 324.8 mg, 2.66 mmol) ve tert-butil (6-aminoheksil)karbamate (533.1 mg, 2.46 mmol) ekleyin. Çözeltiyi ortam sıcaklığında 3 saat karıştırın.
- Vakum altında bir döner evaporatör kullanarak çözücü ve diğer uçucu malzemeleri çıkarın. Doğrudan silika jel flaş sütun kromatografisi kullanarak kalıntı arındırın.
-
Genel Prosedür 2: Tıklanabilir kafesli alkol hazırlanması
- Paclitaxel yerleştirin (PTX, 48.7 mg, 0.057 mmol) üç yönlü stopcock ve Ar balonu ile donatılmış bir 30 mL yuvarlak dipli şişe. Kuru CH2Cl2 (1 mL), 4-DMAP (17.1 mg, 0.14 mmol) ve 4-nitrofenil kloroformate (26.0 mg, 0.13 mmol) ekleyin.
- Ar atmosferi altında 2,5 saat ortam sıcaklığında çözeltiyi karıştırın.
- Çözeltiye 4-DMAP (15.7 mg, 0.13 mmol) ve paBhcCH2OH(2) (39.1 mg, 0.111 mmol) ekleyin. 17 saat ortam sıcaklığında karışımı karıştırmaya devam edin.
- Karışıma CHCl3 (10 mL) ve %15 sulu NaHCO3 (5 mL) ekleyin. Karışımı yaklaşık 3 dk kadar şiddetle karıştırın. Sulu katmanı pipetle çıkarın.
- Organik tabaka içeren şişeye 0,5 M sitrik asit (5 mL) ekleyin. Karışımı karıştırın ve yukarıdaki gibi sulu tabaka kaldırın.
- Faz ayırma sütunu kullanarak organik katmanı ayırın. Vakum altında bir döner evaporatör ile çözücüler çıkarın. Ürünü standart silika jel flash kolon kromatografisi kullanarak arındırın.
-
Genel Prosedür 3: Tıklanabilir kafesli karboksilik asit hazırlanması
- Kuru CH2Cl2 (2 mL) araşidonik asit (33.0 μL, 0.100 mmol), paBhcCH2OH(2) (39.6 mg, 0.112 mmol) ve 4-DMAP (14.1 mg, 0.115 mmol) eritin. N,Nt-diisopropilkarbodiimide (DIPC, 17.0 μL, 0.110 mmol) ekleyin ve 140 dk boyunca ortam sıcaklığında çözeltiyi karıştırın.
- Vakum altında çözücü çıkarın. Doğrudan silika jel flaş sütun kromatografisi kullanarak kalıntı arındırın.
3. Tıklanabilir kafesli bileşikler içine fonksiyonel bir birim kurulumu
- 0.1 M CuSO4 çözeltisi vermek için iyon değişimi (IEW, 10 mL) içinde bakır(II) sülfat pentahidrat (249 mg) çözün.
- 20-paBhcmoc-PTX (8.0 mg, 6.5 μmol), tris (3-hidroksipropilrinolylmethyl)amin (THPTA, 17.5 mg, 40.3 μmol), sodyum l-askorbat (162.4 mg, 0.825 mmol) ve 15-kloro-3,6,9-triksapentadecyl azid (3.1 mg, 11 μmol) 0.1 M fosfat karışık çözücü tampon (2,5 mL, pH 7.2) ve dimetil sülfoksit (DMSO, 0.5 mL).
- Reaksiyon karışımına 0,1 M CuSO4 çözeltisini (81,2 μL, 8,1 μmol) ekleyin. Karışımı 80 dakika ortam sıcaklığında karıştırın. Yüksek performanslı sıvı kromatografisi (HPLC) kullanarak reaksiyonun ilerlemesini izleyin.
- %75 asetonitril/su çözeltisi (3,5 mL) ekleyerek çökeltileri çözün. Elde edilen çözümü, istenilen ürünü arındırmak için doğrudan yarı preparative HPLC sistemine uygulayın.
NOT: Reaksiyon karışımının tert-butanol ilavesi ile çözünürasyonu reaksiyonun ilerlemesini hızlandırabilir.
4. Kafesli bileşiklerin fotolitik uncaging reaksiyonu
- Stok çözümlerinin hazırlanması
- 10 mM'lik bir stok çözeltisi hazırlamak için istenilen kafesli bileşiği (5 μmol) DMSO'da (500 μL) çözün. Her çözeltinin (10 μL) bir aliquot'u 1,5 mL'lik mikrosentrifuge tüpüne dağıtın ve kullanmadan hemen öncesine kadar dondurucuda (−20 °C) saklayın.
- 6 mM K3[Fe(C2O4)3] ( 100 mL): 80 mL suda yeniden kristalize potasyum ferrioksalat (0,295 g, 0,675 mmol) çözünür. Hacmi 100 mL'ye çıkarmak için 0,5 M H2SO4 (10 mL) ve uygun miktarda IEW ekleyin.
NOT: Potasyum ferrioksalat sıcak sudan rekristalizasyon yoluyla arıtılmalı ve karanlıkta depolanmalıdır. Rekristalize potasyum ferrioksalat trihidrat olarak elde edilir; bu nedenle formülü K3[Fe(C2O4)3]·3H2O'dur ve stok çözeltisinin hazırlanması sırasında 491,24 formül ağırlığı düşünülmelidir. 510 nm'de emilimini ölçerek 6 mM çözeltinin saflığını kontrol edin. Emicilik <0.02 ise, deneyde kullanıma uygundur. - %0.1 Tampon-phen (30 mL): Çözün NaOAc·3H2O (7.35 g), 1,10-fenanthroline (fen)· H2O (30 mg) ve conc. H2SO4 (0.9 mL) IEW (20 mL). Hacmi 30 mL'ye çıkarmak için IEW ekleyin.
NOT: Çözelti 1.8 M NaOAc, 0.54 M H2SO4ve %0.1 1,10-fenantropin içerir.
- Ferrioksalat aktinometrisi kullanan fotonların sayısının ölçülmesi
- 6 mM K3[Fe(C2O4)3](V1 L) bir kuvars cuvette yerleştirin. Çözeltiyi 5 s için 350 nm ışıkla ışınlayın.
- Işınlanmış çözeltiyi l [cm] yol uzunluğuna sahip bir Pyrex cuvette'ye aktarın.
- Işınlanmış numune çözeltisine %0,1 Tampon-phen(V2 L) ekleyin ve pipetleme ile iyice karıştırın. Numunenin emiciliğini 510 nm olarak ölçün. Birim zaman başına ortalama soğurma değişimini hesaplayın (ΔA510 [s−1]).
- Oluşturulan Fe2+ iyonlarının birim zaman başına mol sayısını aşağıdaki denkleme göre hesaplayın:
nFe2+ [mol s−1] = ((V1 + V2) [L] × ΔA510 [s−1])/( l [cm] × ε510 [L mol−1 cm−1 ]),
nerede (V1 + V2) emme ölçümü için numunenin hacmi, l cuvette optik yol uzunluğu ve ε510 Fe 2+molar absorptivity olduğunu - 510 nm fen kompleksi.
NOT: Tipik deneysel koşullarda V1 = 2,0 × 10−3 L, V2 = 0,33 × 10−3 L, l = 1,0 cm ve ε510 = 1,1 × 104 L mol−1 değerleri cm−1 kullanılmıştır. - Aşağıdaki formülü kullanarak örneğe ulaşan fotonların mol sayısını(I0)hesaplayın:
I0 [einstein cm−2 s−1] = nFe2+/Φ350
Φ 350 350 nm ferrioksilin fotonüksiyon kuantum verimliliği nerede.
NOT: Potasyum ferrioksalat aktinometrenin 350 nm'deki kuantum verimi bildirilmemiş olsa da, 358 nm'de 1.2542'lik bildirilen değer kullanıldı.
- Kuantum verimliliği ölçümleri 350 nm
- K-MOPS'de %0,1 DMSO içeren 10 μM çözeltisi vermek için numune stok çözeltisini (DMSO, 10 μL'de) K-MOPS tamponu (pH 7.2, 10 mL) ile seyreltin.
NOT: K-MOPS tamponu 100 mM KCl ve 10mM 3-(N -morfolino)propansülfonik asit (Paspaslar) koh ile pH 7.2 titrated oluşuyordu. - Çözeltinin(V1 L) bir aliquot'unun kimyasal aktinometrenin fotoreaksiyonunda kullanılan aynı cuvette aktarılması. Adım 4.2.1'de açıklandığı gibi aynı kurulumu kullanarak örnek çözümünü ışınlayın.
- Radyasyonlu çözeltiden periyodik olarak bir aliquot (50 μL) çıkarın ve HPLC kullanarak analiz edin.
- Başlangıç materyalinin %90'ının(t%90)başlangıç materyalinin zamana bağlı kayboluşunun çizimlerini takarak tepki verdiği ışınlama süresini saniyecinsinden belirleyin.
NOT: Radyasyonun iç filtrelemesi ihmal edilebilsin diye ışınlanan numunenin absorbesi <0.1'de muhafaza edilmelidir. Başlangıç materyalinin fotolitik tüketiminin tek üstel bozunma ile yaklaşık olarak tahmin edilebildiği, böylece fotolyzin işlemini engelleyen istenmeyen ikincil etki olmaması istenir. - Aşağıdaki denklemi kullanarak kaybolma kuantum verimi hesaplamak (Φdis)28:
Φdis = 1/(t%90 × I0 × σ350)
t%90 [s] başlangıç materyalinin% 90 tüketilen ışınlama süresi ise, I0 [einstein cm−2 s−1] foton benlerinin sayısı ve σ350 [cm 2 mol−1] 350 nm'deki numunenin dekadik yok olma katsayısıdır.
NOT: σ350 [cm2 mol−1] = 103ε350 [M−1 cm−1].
- K-MOPS'de %0,1 DMSO içeren 10 μM çözeltisi vermek için numune stok çözeltisini (DMSO, 10 μL'de) K-MOPS tamponu (pH 7.2, 10 mL) ile seyreltin.
5. HaloTag ligand ile tıklanabilir kafesli bir bileşiğin hedeflemi
NOT: Kullanmadan önce, Dulbecco'nun modifiye Eagle ortamda (DMEM, düşük glikoz, sodyum pirüuvat, l-glutamin) %10 oranında fetal sığır serumu (FBS) içeren hela hücrelerini %1 antibiyotik (streptomisin sülfat, penisilin G ve amfetamin) 37 °C ve %5 CO2.
- Orta yı çıkarın ve 37 °C'de tripsin-etilendiamintetraasetik asit (EDTA, 1 mL) ile 1 dk. Hücrelere DMEM (4 mL) ekleyin ve yavaşça borular atarak hücreleri yeniden askıya alın. Tohum yaklaşık 5 × 105 hücre dmem içinde 35 mm cam alt yemekleri içine (2 mL) 24 saat transfection önce.
- Dört tabak için, 1,5 mL mikrosantrifüj tüp, plazmid DNA seyreltmek (pcDNA3-Halo-EGFR, 14 μg) azaltılmış serum ortamda (700 μL). Ayrıca, indirgenmiş serum ortamındaki (150 μL) lipofection reaktifini (5 μL) dört tüpün her birine seyreltin ve 5 dakika ortam sıcaklığında durmalarını bekleyin.
- Seyreltilmiş plazmid DNA'sının (150 μL) bir kısmını seyreltilmiş lipofection reaktif örneklerinin her birine ekleyin. 5 dakika ortam sıcaklığında kuluçka.
- Hücreleri 37 °C ve %5 CO2'de 24 saat boyunca koruduktan sonra DMEM'i aspire edin ve fosfat tamponlu salin (PBS, 2 mL) ile hücreleri durulayın. Azaltılmış serum ortamını (1,5 mL) ekleyin.
- Her çanağa plazmid-lipofection reaktifi (150°L) kompleksi ekleyin. Hücreleri 37 °C ve %5 CO2'de 48 saat boyunca koruyun.
- Ortamı aspire edin, 2 μM paBhc-hex-FITC/Halo içeren taze hazırlanmış DMEM'in (1 mL) bir kısmını ekleyin ve hücreleri 37 °C ve %5 CO2'de 30 dakika kuluçkaya yatırın.
- Kafesli bileşiği içeren ortamı aspire edin ve hücreleri iki kez PBS+ (durulama başına 1 mL) ile durulayıp bağlanmamış bileşikleri temize çıkarın. Azaltılmış serum ortamını (500 μL) ekleyin ve hücrelere giren bileşikleri çıkarmak için hücreleri 37 °C ve %5 CO2'de 30 dakika kuluçkaya yatırın.
NOT: PBS+ 2 mM CaCl2 ve 1 mM MgCl2ile takviye fosfat tamponlu salindir. - Ortamı çıkarın ve PBS+ (1 mL) ile hücreleri iki kez durula. Fenol kırmızısı içermeyen bir orta (1 mL) bölümünü ekleyin. Lazer tarama confocal floresan mikroskopi ile floresan görüntüleri kaydedin.
6. Tıklanabilir kafesli bileşik kullanarak kinaz lokalizasyonunun fotoaracımodülasyonu
NOT: Kullanmadan önce Ham'ın F-12 ortamındaki CHO-K1 hücrelerini 37 °C'de %10 FBS ve %5 CO2ile desteklenerek muhafaza edin.
- DMSO'da 100× çalışma çözeltisi (1 mM)paBhc-AA(5)hazırlayın.
NOT: Bileşiğin 10 mM'lik stok çözeltisi hazırlanır ve dondurucuda (-20 °C) saklanır. - Tohum yaklaşık 5 × 105 hücre dmem içinde 35 mm cam alt yemekleri içine (2 mL) 24 saat transfection önce.
- Transfect CHO-K1 hücreleri gfp-DGKγ için bir plazmid kodlama ile 48 h uncaging deneyler önce.
NOT: Transfeksiyon 5.2-5.5 adımlarına göre yapılır. - Orta ortamı azaltılmış bir serum ortamı (2 mL) ile değiştirin. 100× paBhc-AA çalışma çözeltisini (20 μL) ekleyin ve hücreleri 37 °C ve %5 CO2'de 5 dakika ile 1 saat arasında kuluçkaya yatırın.
NOT: Yükleme süresi kullanılan bileşiğe bağlıdır. - Hücreleri, çift ışık kaynağı floresan aydınlatıcı ile donatılmış ters floresan mikroskobun nesnel aşamasına yerleştirin.
- Floresan görüntü alın her 10 s. Uygun bir süre için bir mikroskop hedefi ile 330-385 nm ışık ile hücreleri ışın. Alternatif olarak, esnek kuvars lifleri ile xe lamba kullanarak 405 nm ışık ile hücreleri ışın.
- 10 dakika boyunca floresan görüntüleri kaydetmeye devam edin.
Sonuçlar
Araşidonik asit ve paklitaksel gibi biyolojik olarak ilginç moleküllerin tıklanabilir kafesli bileşikleri başarıyla sentezlendi (Şekil 1)28,41. Su çözünürlüğü ve hücresel hedefleme yeteneği gibi ek özellikler bakır(I)-katalize Huisgen siklizasyon ("Click" reaksiyonu)(Şekil 2)ile paBhcmoc-PTX'e girmiştir. Bu tıklanabilir kafesli PTX'ler daha sonra 350 nm(Şekil 3)ışınlama üzerine ana PTX'lerini üretmek için fotoize edildi ve tıklanabilir kafesli bileşiklerin fiziksel ve fotokimyasal özellikleri Tablo 1'de özetlenmiştir. Tıklanabilir kafesli bileşiklerin kuantum verimleri 20-glc-paBhcmoc-PTX (Φdis 0.14) ve paBhc-AA(Φdis 0.083) iki katından fazla geleneksel Bhc kafesli bileşikler 20-Bhcmoc-PTX (Φdis 0.040) ve Bhc-AA (Φdis 0.038)43. Buna ek olarak, bir glikoz moiety içeren 20 glc-paBhcmoc-PTX için geliştirilmiş bir su çözünürlüğü gözlenmiştir.
Canlı hücre deneylerinde, halotag proteininin füzyon proteinini ve epidermal büyüme faktörü reseptörünün (EGFR) geçici olarak ifade ettiği kültürlü memeli hücrelerine paBhc-hex-FITC/Halo'nun hedefleştirilmesi başarıyla sağlanmıştır. Hücre zarında paBhc-hex-FITC/Halo floresanının yeşil floresansı gözlendi (Şekil 4). Bir kininin hücre altı lokalizasyonunun foto-aracılı modülasyonu paBhc kafesli bir bileşik kullanılarak elde edilmiştir. Diacylglycerol kigaz γ translokasyonu (DGKγ) araşidonik asit varlığında aktive olduğu bildirilmiştir (AA)44. GFP-DGKγ'i geçici olarak ifade eden CHO-K1 hücreleri AA veya paBhc-AA(5)ile tedavi edildi. AA eklenmesi DGKγ alt hücreli lokalizasyonumodülasyonu neden oldu (Şekil 5A,B). UV ışığına maruz kaldıktan sonra paBhc-AA ile tedavi edilen hücrelerde DGKγ lokalizasyonunda benzer değişiklikler gözlenmiştir(Şekil 5C,D).
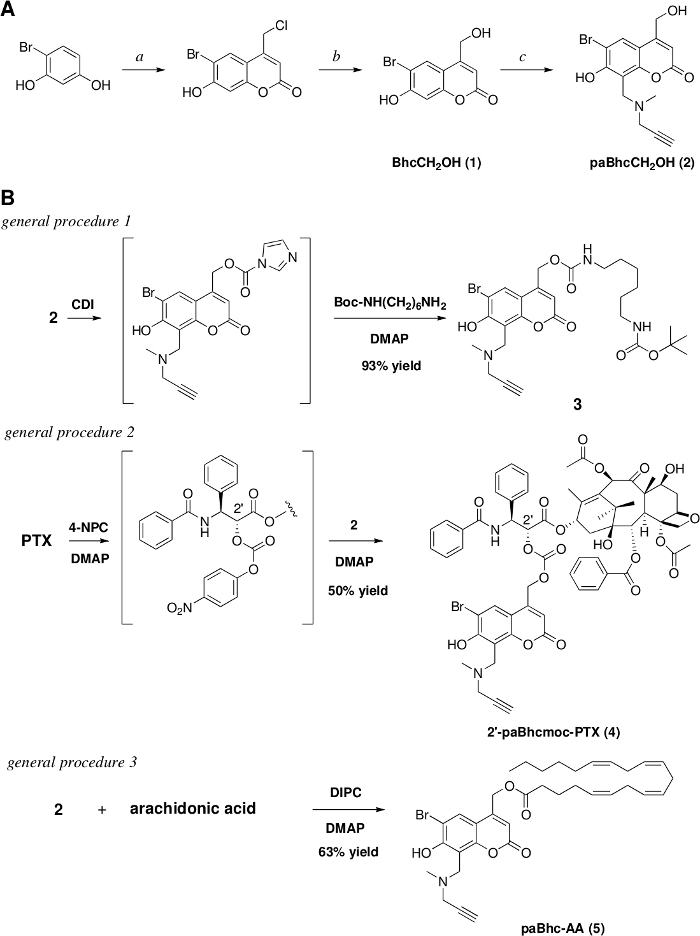
Şekil 1: Tıklanabilir kafesli bileşiklerin hazırlanması.
(A) Reaktifler ve koşullar: a. etil 4-kloroasetasetat/conc. H2SO4/rt/7 gün/91% verim, b. 1 M HCl/reflü/3 gün/97% verim. c. N-metilpropargylamin /HCHO/EtOH, sonra ekleyin (1) ve reflü ısı 17 h/79% verim için. (B) Tıklanabilir kafesli amin, PTX ve araşidonik asit sentezleri. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 2: Fonksiyonel ünitelerin tıklanabilir kafesli bileşiklere yerleştirilmesi.
(A) Bakır(I)-katalize Huisgen siklizasyon yoluyla suda çözünen kafesli PTX sentezi. (B) Hücresel hedefleme için HaloTag ligand içeren tıklanabilir kafesli bileşiklerin yapıları. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
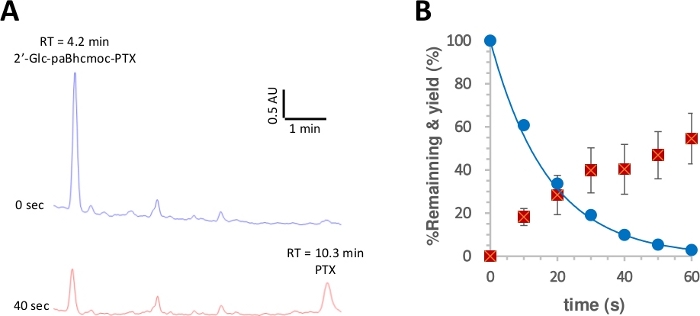
Şekil 3: 20-glc-paBhcmoc-PTX fotolisisi (6).
K-MOPS çözeltisindeki (pH 7.2) numuneler (10 μM) 350 nm'de ışınlandı. (A) 6 fotoliz için tipik HPLC izleri (254 nm olarak ölçülür). Numuneler belirtilen ışınlama zamanında analiz edildi. (B) Fotolilyz için zaman kursu 6. Mavi daireler tüketimini gösterir 6. Düz çizgi, basitbir çürüyen üstel 6 için uygun en az kareler eğrisi gösterir. Kırmızı kareler PTX'in verimini gösterir. Hata çubukları standart sapmayı (±SD) temsil eder. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 4: PaBhc-hex-FITC/Halo ile kuluçkaya yatan kültürlü memeli hücrelerinin floresan görüntüleri (8).
PCDNA3-Halo-EGFR ile transfeced hücreler 30 dakika boyunca 37 °C'de 8 mm bileşik 8'in 2 μM çözeltisi ile inküküle edildi. Görüntüler PBS+ ile tekrar tekrar yıkandıktan sonra elde edilmiştir. Mock-treated HEK293T hücreleri (A: diferansiyel girişim kontrastı (DIC) görüntü ve D: floresan görüntü). HEK293T hücreleri(B ve E) ve HeLa hücreleri (C ve F) geçici olarak Halo-EGFR(B ve C: DIC görüntüleri ve E ve F: floresan görüntüleri) ifade eder. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 5: BHC kafesli araşidonik asit ile inkübe CHO-K1 hücrelerinin UV ışınlama sonra Floresan görüntüleri. CHO-K1 hücreleri bir füzyon proteini DGKγ-EGFP ile transfekslendi.
(A) Transfected hücrelerin floresan görüntüsü. (B) 100 s araşidonik asit 10 μM çözeltisi ilave sonra. (C) Hücreler, 20'li UV ışınlamadan (330-385 nm)sonra 37 °C'de 10 μM'lik paBhc-AA çözeltisi ile(D) 100 s'lik bir tüp altında kuvedilmiştir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
| Bileşik | λmax (nm)a | εmax (M-1 cm-1)b | φdisc | εφdisd | Çözünürlük (μM)e |
| Ptx | 1.0 | ||||
| 2'-Bhcmoc-PTX | 340 | 10500 | 0.040 | 400 | 55 |
| 2'-paBhcmoc-PTX | 359 | 9300 | 0.059 | 670 | 8.3 |
| 2'-glc-Bhcmoc-PTX | 373 | 12300 | 0.14 | 1280 | 650 |
| Bhc-AA | 341 | 10800 | 0.038 | 390 | |
| paBhc-AA | 366 | 10300 | 0.083 | 750 |
Tablo 1: Tıklanabilir kafesli bileşiklerin fiziksel ve fotokimyasal özellikleri.
a. Absorpsiyon maksimum (nm), b. Λmax (M−1 cm−1), c. Başlangıç malzemelerinin 350 nm'de kaybolmasının kuantum verimi, d. Molar absorptivity ürünü ve 350 nm, e de kaybolma kuantum verimi. K-MOPS'deki doymuş çözeltinin konsantrasyonu (pH 7.2) (μg mL−1).
Tartışmalar
Daha önce yüksek fotolitik verimlilik28,45,46,47sergileyen çeşitli biyolojik olarak aktif moleküllerin Bhc kafesli bileşikler geliştirdi. Bhc caging gruplarının repertoire genişletilmesi amacı ile, biz de çeşitli fonksiyonel birimlerin tanıtımı ile kolayca değiştirilebilir modüler kafesli bileşiklerin platformları bildirdi32,40,41. Bu nedenle bu protokol, bakır(I)-katalize Huisgen siklizasyonu ile değiştirilebilen Bhc caging gruplarının tıklanabilir bir öncüsünün sentezi için bir yöntem temsil eder. Tıklanabilir öncül sentezi, paBhcCH2OH (2), ticari olarak kullanılabilir 4-bromoresorcinol başlayan dört adımlı reaksiyon dizisi ile elde edildi (Şekil 1A). Mevcut protokolün avantajı, zahmetli arınma adımlarının (örneğin, sütun kromatografik ayrımları) gerekli olmamasıdır.
Tıklanabilir öncül paBhcCH2OH (2) çeşitli fonksiyonel grupları maskelemek için kullanılabilir gibi, aminlerin tıklanabilir kafesli bileşikler, alkoller, ve karboksilik asitler öncüsü olarak 2 kullanılarak sentezlendi (Şekil 1B). Aminler karbamates olarak modifiye edildi, alkoller ise karbonat olarak modifiye edildi. Genel prosedürler 1 ve 2'de tıklanabilir karbamatelerin hazırlanmasında CDI, karbonatların hazırlanmasında ise 4-nitrofenil kloroformate kullanılmıştır. Reaksiyon mekanizmasından da anlaşılarak, her iki reaktif de karbatür ve karbonat ların hazırlanmasında kullanılabilir. Ayrıca istenilen kafesli bileşiğin verimi kafesli edilecek molekülün kimyasal yapısına bağlıdır unutulmamalıdır. Diğer örnekler önceki raporlarımızda görülebilir28,30,33,48.
Tıklama modifikasyonu daha sonra bildirilen yordamın küçük bir değişiklik kullanılarak yapıldı49. Tris (triazolylmethyl)amin bazlı ligands eklenmesi yüksek verim iyi istenilen ürünleri elde etmek için gereklidir. Çeşitli azideler hem ticari kaynaklardan hem de literatür prosedürlerinden kolayca elde edilebildiği için, su çözünürlüğü ve hücresel hedefleme yeteneği gibi ek özelliklere sahip çeşitli modüler kafesli bileşikler hazırlayabiliriz(Şekil 2).
Fotolik kuantum verimi daha sonra bildirilenprosedür28,50göre ölçüldü . Şekil 3, 20-glc-paBhcmoc-PTX'in fotolitik tüketimi ve PTX salınımının sırasıyla tek üstel bozunma ve yükselme ile yaklaşık olarak, radyasyonun iç filtreleme veya istenmeyen ikincil etkilere işaret ettiğini göstermektedir. Geliştirilmiş fotolik kuantum verimleri(Φ) ve fotolik isbik verimlilikleri(εΦ)daha önce bildirilen Bhc kafesli bileşikler(Tablo 1)41 ile karşılaştırıldığında tıklanabilir paBhc kafesli bileşikler için gözlendi , 43- Bhc kafesli bileşiklerin fotolik verimi(εΦ)2-nitrobenzil tipi kafeslibileşikler48'denyüz kat daha yüksek olduğundan, paBhc caging gruplarının varlığından kaynaklanan belirgin iyileşme açıkça bu sistem için bir avantaj.
Kavram kanıtı deneyi olarak 20-paBhcmoc-PTX(4)içine hidrofilik moiety, bileşik 3'e hücresel hedefleme ligandı(Şekil 2)getirilmiştir. 20-glc-paBhcmoc-PTX'in su çözünürlüğü ana PTX'ten 650 kat daha yüksekti (Tablo 1). Selektif hücresel hedefleme bir etiket-prob sistemi kullanılarak elde edildi ve HaloTag ligand'ı taşıyan paBhcmoc-hex-FITC/Halo(8)HaloTag/EGFR füzyon proteinini ifade eden kültürlü memeli hücrelerinin hücre zarına başarıyla hedeflenmiştir ( Şekil 4). Bir kizazın hücre altı lokalizasyonunun foto-aracılı modülasyonu da tıklanabilir kafesli bileşik 5 kullanılarak elde edilmiştir(Şekil 5).
Sonuç olarak, biyolojik olarak ilginç moleküllerin foto kafesli bileşikleri için tıklanabilir platformların hazırlanması için bir yöntem başarıyla gösterdik. hedefleme yeteneği. PaBhc caging grubu değiştirilebilir fonksiyonel gruplara sahip molekülleri hazırlamak için kullanılabildiğinden, mevcut protokolün uygulanması burada tanımlanan moleküllerle sınırlı değildir. Modüler bir platform kullanarak, yani paBhc caging grubu, istenilen kafesli bileşikler kolayca hazırlanabilir, ve fiziksel ve kimyasal özellikleri tıklama modifikasyonu ile modüle edilebilir.
Açıklamalar
Açıklayacak bir şeyimiz yok.
Teşekkürler
Bu çalışma JSPS KAKENHI hibe numarası JP16H01282 (TF), Yenilikçi Alanlar "Bellek Dinamizm bilimsel araştırma için hibe-in-Aid" ve JP19H05778 (TF), "MolMovies tarafından desteklenmiştir."
Malzemeler
| Name | Company | Catalog Number | Comments |
| acetonitrile, EP | Nacalai | 00404-75 | |
| acetonitrile, super dehydrated | FUJIFILM Wako | 010-22905 | |
| Antibiotic-Antimycotic, 100X | Thermo Fisher | 15240062 | |
| 4-bromoresorcinol | TCI Chemicals | B0654 | |
| N,N’-carbonyldiimidazole | FUJIFILM Wako | 034-10491 | |
| chloroform | Kanto | 07278-71 | |
| Copper (II) Sulfate Pentahydrate, 99.9% | FUJIFILM Wako | 032-12511 | |
| dichloromethane, dehydrated | Kanto | 11338-05 | |
| N,N'-Diisopropylcarbodiimide (DIPC) | TCI Chemicals | D0254 | |
| 4-dimethylaminopyridine | TCI Chemicals | D1450 | |
| dimethylsulfoxide, dehydrated -super- | Kanto | 10380-05 | |
| DMEM - Dulbecco's Modified Eagle Medium | Sigma | D6046-500ML | |
| dual light source fluorescence illuminator, IX2-RFAW | Olympus | ||
| Ethanol (99.5) | FUJIFILM Wako | 054-07225 | |
| Ethyl 4-Chloroacetoacetate | TCI Chemicals | C0911 | |
| Ham's F-12 with L-Glutamine and Phenol Red | FUJIFILM Wako | 087-08335 | |
| hydrochloric acid | FUJIFILM Wako | 087-01076 | |
| inverted fluorescent microscope IX-71 | Olympus | ||
| ISOLUTE Phase Separator, 15 mL | Biotage | 120-1906-D | |
| L-(+)-Ascorbic Acid Sodium Salt | FUJIFILM Wako | 196-01252 | |
| laser scanning fluorescence confocal microscopy, FLUOVIEW FV1200/IX-81 | Olympus | ||
| Lipofectamine 2000 Transfection Reagent | Thermo Fisher | 11668027 | lipofection reagent |
| 3-(N-morpholino)propanesulfonic acid | Dojindo | 345-01804 | MOPS |
| 4-nitrophenylchloroformate (4-NPC) | TCI Chemicals | C1400 | |
| Opti-MEM I Reduced Serum Medium, no phenol red | Thermo Fisher | 11058021 | reduced serum medium contains no phenol red |
| 1,10-Phenanthroline Monohydrate | Nacalai | 26707-02 | |
| Photochemical reactor with RPR 350 nm lamps | Rayonet | ||
| Potassium Trioxalatoferrate (III) trihydrate | FUJIFILM Wako | W01SRM19-5000 | |
| Sodium Acetate Trihydrate | Nacalai | 31115-05 | |
| Sodium Bicarbonate | FUJIFILM Wako | 199-05985 | |
| Sulfuric Acid, 96-98% | FUJIFILM Wako | 190-04675 | |
| Tris(3-hydroxypropyltriazolylmethyl)amine (THPTA) | ALDRICH | 762342-100MG | |
| tri-Sodium Citrate Dihydrate | Nacalai | 31404-15 | |
| Xenon light source, MAX-303 | Asahi Spectra |
Referanslar
- Mayer, G., Heckel, A. Biologically active molecules with a "light switch". Angewandte Chemistry International Edition. 45 (30), 4900-4921 (2006).
- Bort, G., Gallavardin, T., Ogden, D., Dalko, P. I. From One-Photon to Two-Photon Probes: Caged” Compounds, Actuators, and Photoswitches. Angewandte Chemistry International Edition. 52 (17), 4526-4537 (2013).
- Klan, P., et al. Photoremovable Protecting Groups in Chemistry and Biology: Reaction Mechanisms and Efficacy. Chemical Reviews. 113 (1), 119-191 (2013).
- Abe, M., et al. Design and Synthesis of Two-Photon Responsive Chromophores for Near-Infrared Light-Induced Uncaging Reactions. Synthesis-Stuttgart. 49 (15), 3337-3346 (2017).
- Ankenbruck, N., Courtney, T., Naro, Y., Deiters, A. Optochemical Control of Biological Processes in Cells and Animals. Angewandte Chemistry International Edition. 57 (11), 2768 (2018).
- Hou, Y., Zhou, Z., Huang, K., Yang, H., Han, G. Long Wavelength Light Activated Prodrug Conjugates for Biomedical Applications. ChemPhotoChem. 2, 1005 (2018).
- Engels, J., Schlaeger, E. J. Synthesis, structure, and reactivity of adenosine cyclic 3',5'-phosphate benzyl triesters, Rapid photolytic release of adenosine 5'-triphosphate from a protected analogue: utilization by the Na:K pump of human red blood cell. Journal of Medicinal Chemistry. 20 (7), 907-911 (1977).
- Kaplan, J. H., Forbush, B., Hoffman, J. F. Rapid photolytic release of adenosine 5'-triphosphate from a protected analogue: utilization by the Na:K pump of human red blood cell ghosts. Biochemistry. 17 (10), 1929-1935 (1978).
- Park, C. H., Givens, R. S. New Photoactivated Protecting Groups. 6. p-Hydroxyphenacyl: A Phototrigger for Chemical and Biochemical Probes. Journal of the American Chemical Society. 119 (10), 2453-2463 (1997).
- Hasan, A., et al. Photolabile protecting groups for nucleosides: synthesis and photo-deprotection rates. Tetrahedron. 53 (12), 4247-4264 (1997).
- Heckel, A., Mayer, G. Light regulation of aptamer activity: an anti-thrombin aptamer with caged thymidine nucleobases. Journal of the American Chemical Society. 127 (3), 822-823 (2005).
- Papageorgiou, G., Corrie, J. E. T. Effects of aromatic substituents on the photocleavage of 1-acyl-7-nitroindolines. Tetrahedron. 56 (41), 8197-8205 (2000).
- Matsuzaki, M., Ellis-Davies, G. C., Nemoto, T., Miyashita, Y., Iino, M., Kasai, H. Dendritic spine geometry is critical for AMPA receptor expression in hippocampal CA1 pyramidal neurons. Nature Neuroscience. 4 (11), 1086-1092 (2001).
- Givens, R. S., Matuszewski, B. Photochemistry of phosphate esters: an efficient method for the generation of electrophiles. Journal of the American Chemical Society. 106 (22), 6860-6861 (1984).
- Furuta, T., Torigai, H., Sugimoto, M., Iwamura, M. Photochemical Properties of New Photolabile cAMP Derivatives in a Physiological Saline Solution. Journal of Organic Chemistry. 60 (13), 3953-3956 (1995).
- Hagen, V., Frings, S., Wiesner, B., Helm, S., Kaupp, U. B., Bendig, J. 7-(Dialkylamino)coumarin-4-yl]methyl-Caged Compounds as Ultrafast and Effective Long-Wavelength Phototriggers of 8-Bromo-Substituted Cyclic Nucleotides. ChemBioChem. 4 (5), 434-442 (2003).
- Momotake, A., Lindegger, N., Niggli, E., Barsotti, R. J., Ellis-Davies, G. C. The nitrodibenzofuran chromophore: a new caging group for ultra-efficient photolysis in living cells. Nature Methods. 3 (1), 35-40 (2006).
- Specht, A., et al. New photoremovable protecting groups for carboxylic acids with high photolytic efficiencies at near-UV irradiation. Application to the photocontrolled release of L-glutamate. ChemBioChem. 7 (11), 1690-1695 (2006).
- Petersen, S., Alonso, J. M., Specht, A., Duodu, P., Goeldner, M., del Campo, A. Phototriggering of cell adhesion by caged cyclic RGD peptides. Angewandte Chemistry International Edition. 47 (17), 3192-3195 (2008).
- Heckman, L. M., et al. Design and Synthesis of a Calcium-Sensitive Photocage. Angewandte Chemistry International Edition. 55 (29), 8363-8366 (2016).
- Olson, J. P., Banghart, M. R., Sabatini, B. L., Ellis-Davies, G. C. Spectral Evolution of a Photochemical Protecting Group for Orthogonal Two-Color Uncaging with Visible Light. Journal of the American Chemical Society. 135 (42), 15948-15954 (2013).
- Gandioso, A., et al. Sequential Uncaging with Green Light can be Achieved by Fine-Tuning the Structure of a Dicyanocoumarin Chromophore. ChemistryOpen. 6 (3), 375-384 (2017).
- Bassolino, G., Nancoz, C., Thiel, Z., Bois, E., Vauthey, E., Rivera-Fuentes, P. Photolabile coumarins with improved efficiency through azetidinyl substitution. Chemical Science. 9 (2), 387-391 (2018).
- Lin, Q. N., et al. Coumarin Photocaging Groups Modified with an Electron-Rich Styryl Moiety at the 3-Position: Long-Wavelength Excitation, Rapid Photolysis, and Photobleaching. Angewandte Chemistry International Edition. 57 (14), 3722-3726 (2018).
- Nani, R. R., et al. In Vivo Activation of Duocarmycin-Antibody Conjugates by Near-Infrared Light. ACS Central Science. 3 (4), 329-337 (2017).
- Umeda, N., et al. Boron Dipyrromethene As a Fluorescent Caging Group for Single-Photon Uncaging with Long-Wavelength Visible Light. ACS Chemical Biology. 9 (10), 2242-2246 (2014).
- Slanina, T., et al. In Search of the Perfect Photocage: Structure–Reactivity Relationships in meso-Methyl BODIPY Photoremovable Protecting Groups. Journal of the American Chemical Society. 139 (42), 15168-15175 (2017).
- Furuta, T., et al. Brominated 7-hydroxycoumarin-4-ylmethyls: Photolabile protecting groups with biologically useful cross-sections for two photon photolysis. Proceedings of the National Academy of Sciences of the United States of America. 96 (4), 1193-1200 (1999).
- Furuta, T., et al. Bhc-cNMPs as either water-soluble or membrane-permeant photoreleasable cyclic nucleotides for both one- and two-photon excitation. ChemBioChem. 5 (8), 1119-1128 (2004).
- Suzuki, A. Z., et al. Coumarin-4-ylmethoxycarbonyls as phototriggers for alcohols and phenols. Organic Letters. 5 (25), 4867-4870 (2003).
- Ando, H., Furuta, T., Tsien, R. Y., Okamoto, H. Photo-mediated gene activation using caged RNA/DNA in zebrafish embryos. Nature Genetics. 28 (4), 317-325 (2001).
- Teraoka, A., Murakoshi, K., Fukamauchi, K., Suzuki, A. Z., Watanabe, S., Furuta, T. Preparation and affinity-based purification of caged linear DNA for light-controlled gene expression in mammalian cells. Chemical Communications. 50 (6), 664-666 (2014).
- Watanabe, T., et al. Synthesis of nucleobase-caged peptide nucleic acids having improved photochemical properties. Organic and Biomolecular Chemistry. 12 (28), 5089-5093 (2014).
- Horinouchi, T., Nakagawa, H., Suzuki, T., Fukuhara, K., Miyata, N. A novel mitochondria-localizing nitrobenzene derivative as a donor for photo-uncaging of nitric oxide. Bioorganic & Medicinal Chemistry Letters. 21 (7), 2000-2002 (2011).
- Leonidova, A., et al. Photo-induced uncaging of a specific Re(I) organometallic complex in living cells. Chemical Science. 5 (10), 4044-4056 (2014).
- Nadler, A., et al. Exclusive photorelease of signalling lipids at the plasma membrane. Nature Communications. 6, 10056 (2015).
- Feng, S. H., et al. Mitochondria-specific photoactivation to monitor local sphingosine metabolism and function. Elife. 7, e34555 (2018).
- Wagner, N., Stephan, M., Hoglinger, D., Nadler, A. A Click Cage: Organelle-Specific Uncaging of Lipid Messengers. Angewandte Chemistry International Edition. 57 (40), 13339-13343 (2018).
- Feng, S., Harayama, T., Chang, D., Hannich, J. T., Winssinger, N., Riezman, H. Lysosome-targeted photoactivation reveals local sphingosine metabolism signatures. Chemical Science. 10 (8), 2253-2258 (2019).
- Furuta, T., Manabe, K., Teraoka, A., Murakoshi, K., Ohtsubo, A., Suzuki, A. Design, synthesis, and photochemistry of modular caging groups for photoreleasable nucleotides. Organic Letters. 14 (24), 6182-6185 (2012).
- Suzuki, A. Z., et al. A clickable caging group as a new platform for modular caged compounds with improved photochemical properties. Chemical Communications. 55 (4), 451-454 (2019).
- Hatchard, C. G., Parker, C. A. A new sensitive chemical actinometer - II. Potassium ferrioxalate as a standard chemical actinometer. Proceedings of the Royal Society A. 235 (1203), 518-536 (1956).
- Furuta, T., Nishiyama, K., Manabe, A., Fukuoka, M., Iwamura, M. Design, synthesis and photochemical properties of caged compounds of lipid mediators. Proceedings of the ISBC. , 124-125 (2003).
- Shirai, Y., Segawa, S., Kuriyama, M., Goto, K., Sakai, N., Saito, N. Subtype-specific Translocation of Diacylglycerol Kinase ? and ? and Its Correlation with Protein Kinase C. The Journal of Biological Chemistry. 275 (32), 24760-24766 (2000).
- Furuta, T., Noguchi, K. Controlling cellular systems with Bhc-caged compounds. TrAC, Trends in Analytical Chemistry. 23 (7), 511-519 (2004).
- Furuta, T. Designing caged compounds for spatiotemporal control of cellular chemistry. Journal of the Synthetic Organic Chemistry Japan. 69 (11), 1164-1169 (2012).
- Furuta, T., Goeldner, M., Givens, R. S. Coumarin-4-ylmethyl Phototriggers. Dynamic Studies in Biology: Phototriggers, Photoswitches and Caged Biomolecules. , 29-55 (2005).
- Furuta, T., Watanabe, T., Tanabe, S., Sakyo, J., Matsuba, C. Phototriggers for Nucleobases with Improved Photochemical Properties. Organic Letters. 9 (23), 4717-4720 (2007).
- Manova, R., van Beek, T. A., Zuilhof, H. Surface Functionalization by Strain-Promoted Alkyne–Azide Click Reactions. Angewandte Chemistry International Edition. 50 (24), 5428-5430 (2011).
- Adams, S. R., Kao, J. P. Y., Grynkiewicz, G., Minta, A., Tsien, R. Y. Biologically Useful Chelators That Release Ca2+ Upon Illumination. Journal of the American Chemical Society. 110 (10), 3212-3220 (1988).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır