Method Article
Оптимизация доставки внеклеточных везикул с помощью каркаса с 3D-биопечатью для лечения хронических ран
В этой статье
Резюме
В этом исследовании представлен протокол изготовления каркасов с 3D-биопечатью в оболочке ядра для заживления хронических ран. Внеклеточные везикулы выделяют из мезенхимальных стволовых клеток и загружают в ядро (альгинат) оболочку, состоящую из карбоксиметилцеллюлозы и альгинатлиазы. Такая конструкция позволяет контролировать деградацию скаффолда и эффективно выпускать электромобили.
Аннотация
В этом исследовании изложен подробный протокол изготовления каркасов с 3D-биопечатью, предназначенных для улучшения заживления хронических ран. Протокол включает выделение внеклеточных везикул (ВВ) из мезенхимальных стволовых клеток (МСК), известных своими регенеративными и иммуномодулирующими свойствами. Затем эти электромобили встраиваются в уникальную конструкцию каркаса. Каркас имеет сердцевину, состоящую из альгината, загруженного EV, окруженную оболочкой из карбоксиметилцеллюлозы и альгинатлиазы. Эта инновационная конструкция обеспечивает контролируемую деградацию каркаса, способствуя эффективному и контролируемому выбросу электромобилей в месте раны. Протокол охватывает ключевые этапы, включая подготовку и определение характеристик электромобилей, разработку биочернил для 3D-биопечати и оптимизацию параметров печати для достижения желаемой архитектуры ядра-оболочки. Сочетая в себе структурную целостность и биологическую активность, каркас направлен на устранение ограничений обычных повязок для ран, предлагая целенаправленный подход к ускорению регенерации тканей и уменьшению воспаления в хронических ранах. Этот метод обеспечивает воспроизводимую и масштабируемую стратегию для разработки передовых биоматериалов с потенциальным клиническим применением в лечении хронических ран. В протоколе также освещаются критически важные соображения для достижения стабильных результатов, обеспечивая адаптируемость к будущим терапевтическим приложениям.
Введение
Хронические раны, часто связанные с чрезмерным воспалением, требуют своевременного лечения для предотвращения серьезных осложнений, таких как инфекции и некроз тканей, которые могут привести к ампутациям. Несмотря на достижения, современные методы лечения остаются дорогостоящими, неудобными, имеют побочные эффекты и ограниченную эффективность, что подчеркивает потребность в более лечебных повязках 1,2,3. Разработка нового поколения повязок для ран, специально предназначенных для хронических ран, имеет важное значение для решения этих проблем. Кроме того, сложный характер заживления ран требует перевязочных материалов с целым рядом свойств, включая увлажнение, гибкость, адгезию, биологическую активность и биоразлагаемость4. Это исследование направлено на разработку биоинженерной раневой повязки, которая объединяет внеклеточные везикулы (EV) с каркасом, напечатанным на 3D-биопринтере, для обеспечения контролируемой терапевтической среды и ускорения заживления хронических ран.
ВВ, полученные из стволовых клеток, способствуют заживлению хронических ран, способствуя противовоспалительным реакциям, росту клеток, миграции и образованию кровеносных сосудов5. Кроме того, ВВ могут доставлять биологически активные молекулы, в том числе низкомолекулярные препараты, гены и белковые конструкции для лечения хронических ран6. Кроме того, их способность защищать груз от ферментативного разложения повышает стабильность и биодоступность терапевтических агентов, предлагая явные преимущества по сравнению с обычными факторами роста и низкомолекулярными препаратами, которые часто быстро разлагаются in vivo7. Несмотря на эти преимущества, эффективная и устойчивая доставка ВВ к тканям-мишеням остается серьезной проблемой.
Каркасы для 3D-биопечати могут служить платформой для доставки электромобилей для усиления их терапевтического эффекта8. Эти каркасы имитируют естественную клеточную среду и позволяют осуществлять контролируемое высвобождение EV 9,10. Они также защищают ВВ от деградации, повышая стабильность их микроРНК и белков11. Хан и др. продемонстрировали, что электромобили могут быть эффективно высвобождены из 3D-биопечатных скаффолдов GelMA. Это высвобождение привело к улучшению прикрепления клеток и усилению экспрессии генов, связанных с путями механотрансдукции в мезенхимальных стволовых клетках буккального жирового пакета человека (hBFP-MSCs), засеянных на каркасы12. Born et al., оптимизируя концентрацию сшивающего агента, добились контролируемого высвобождения EV. Этот подход продемонстрировал свою эффективность в стимулировании ангиогенеза и является перспективным методом регулируемой доставкиВВ13.
3D-биопечать сердцевины позволяет создавать сложные структуры из нескольких материалов путем печати материала сердцевины, заключенного в оболочку. Ядро может включать клетки, факторы роста или лекарства, в то время как оболочка обеспечивает механическую поддержку и защиту или действует как барьер. Этот метод находит применение в тканевой инженерии и регенеративной медицине, таких как разработка сосудистых сетей, имитация естественных тканевых структур и создание систем доставки лекарств. Это позволяет точно контролировать распределение и состав материала, повышая функциональность и биологическую значимость конструкций. По сравнению с альтернативными методами, 3D-биопечать с помощью стержневой оболочки обеспечивает точный контроль над распределением и составом материала, улучшая функциональность и биологическую значимость конструкций14,15.
Искусственная деградация раневых повязок дает такие преимущества, как снижение дискомфорта во время изменений, влажная среда для заживления и контроля инфекций, своевременная терапевтическая доставка и оптимальная регенерация тканей 16,17,18. Альгинатные (Alg) и карбоксиметилцеллюлозные (CMCh) гидрогели биосовместимы и эффективны для доставки внеклеточных везикул (EV) в раны, способствуя заживлению за счет клеточной коммуникации и уменьшая воспаление18. В этом исследовании ВВ были интегрированы в ядро Alg, в то время как оболочка из CMCh и AlgLyase (AlgLyase) использовалась для обеспечения быстрой деградации повязки и доставки ВВ. Такая конструкция стержня и оболочки способствует быстрому высвобождению EV в ответ на деградацию каркаса, повышая их терапевтическую эффективность и устраняя ограничения существующих методов лечения хронических ран. Основной целью данного исследования является разработка биоинженерной повязки, которая улучшает заживление ран за счет интеграции контролируемого высвобождения ВВ с быстро разлагаемым каркасом, что в конечном итоге улучшает результаты лечения хронических ран.
протокол
Исследования на животных проводились в полном соответствии с этическими стандартами, установленными Национальным комитетом по биоэтике и Комитетом по этике животных Университета Низвы. Этическое одобрение для этого исследования было предоставлено в соответствии с допуском ID: VCGSR, AREC/01/2023. Все животные содержались в стандартных лабораторных условиях, обеспечивая оптимальный контроль окружающей среды, надлежащее питание и всесторонний уход для обеспечения их благополучия на протяжении всего исследования. Все процедуры с участием животных строго соответствовали политике учреждения, международным стандартам ухода за животными и рекомендациям ARRIVE.
1. Культура клеток
- Достаньте флакон с МСК (отрывок #2) из хранилища жидкого азота и обращайтесь с ним с помощью асептических методов, чтобы предотвратить загрязнение. Быстро разморозьте клетки на водяной бане при температуре 37 °C, убедившись, что удалите их, как только останется небольшой фрагмент льда.
- Приготовьте полноценную среду, включающую базальную среду MSC SFM, с добавлением 1% (v/v) добавки MSC SFM XenoFree, 1% (v/v) GlutaMAX и 0,01% (v/v) гентамицина. Добавьте в флакон 1 мл предварительно подогретой (37 °C) готовой среды со скоростью от 3 до 5 капель каждые 5 с, а затем аккуратно перемешайте. Переложите все содержимое флакона MSC в коническую пробирку объемом 15 мл, содержащую 4 мл предварительно подогретой полной среды, в асептических условиях в шкафу биобезопасности класса II.
- Центрифугируйте ячейки при давлении 200 x g в течение 5 минут при комнатной температуре. Убедитесь, что центрифуга правильно сбалансирована.
- Аспирируйте надосадочную жидкость и ресуспендируйте клетки в 1 мл предварительно подогретой полной среды. Затем переложите клетки в колбу T25, содержащую 4 мл готовой среды.
- Осторожно наклоните колбу, чтобы обеспечить равномерное распределение ячеек. Инкубируйте колбу при 37 °C с 5%CO2.
- Меняйте среду каждые 2 дня, заменяя ее свежей, предварительно подогретой, готовой средой. Используйте щадящее пипетирование, чтобы избежать разрушения клеток. По достижении 70%-80% конфлюенции аспирируйте отработанную среду из колбы Т25.
- Промойте клетки 3 мл свежего PBS для удаления остатков. Обеспечьте полное покрытие колбы во время стирки.
- Добавьте в колбу Т25 1 мл 0,25% раствора трипсина, инкубируйте при 37 °С в течение 3-7 мин и внимательно следите за отслоением под микроскопом при 4-кратном увеличении.
- При необходимости осторожно постучите по колбе, чтобы обеспечить полное отделение ячейки. Добавьте предварительно подогретую среду в колбу и проводите пипеткой вверх и вниз по поверхности, чтобы помочь отделить ячейки. Затем переложите клеточную суспензию в центрифужную пробирку объемом 15 мл.
- Центрифугируйте пробирку при давлении 200 х г в течение 5 минут при комнатной температуре. Суспендируйте клеточную гранулу в свежей полноценной среде и подсчитайте клетки с помощью гемоцитометра Нейбауэра. Переложите ячейки в колбу T75. Обеспечьте плотность посева 5 000 клеток/см2 для оптимального роста.
- Инкубируйте клетки при 37 °C с 5%CO2. После 72 ч инкубации клеток соберите кондиционированную среду из клеток для выделения ВВ. Используйте сразу после сбора.
2. Изоляция электромобилей
- Центрифугируйте 13 мл собранной кондиционированной среды при давлении 800 x g в течение 15 мин для удаления клеточного мусора. Аккуратно отфильтруйте надосадочную жидкость с помощью шприцевого фильтра 0,22 мкм, чтобы удалить крупные частицы.
- Добавьте 5 мл буфера для осадков в отфильтрованную кондиционированную среду и тщательно перемешайте. Убедитесь, что раствор однороден.
- Инкубируйте смесь в течение ночи при температуре 4 °C, чтобы электромобили выпали в осадок. Центрифугируйте смесь при давлении 3 220 x g в течение 30 мин при 20 °C. Проверьте баланс трубок.
- Осторожно выбросьте надосадочную жидкость, не потревожив гранулы. Снова центрифугируйте гранулу при давлении 3 220 x g в течение 5 с, чтобы удалить остатки жидкости.
- Осторожно нанесите гранулу EV в 200 мкл PBS, чтобы избежать повреждения EV. Измерьте концентрацию белка EVs, следуя инструкциям производителя (набор для анализа белка BCA).
- Выполните вестерн-блоттинг для выявления маркеров, специфичных для ЭВ (CD63, CD81 и CD9), чтобы подтвердить фенотипВВ 18. Анализ подтвердил наличие этих маркеров, подтвердив принадлежность электромобилей19.
- Чтобы свести к минимуму риск заражения РНКазой, рекомендуется использовать ее непосредственно без дополнительного хранения. В случае необходимости храните электромобили при температуре -80 °C для дальнейшего использования. Аликвотируйте суспензию электромобилей в объеме 40 μл, чтобы избежать повторных циклов замораживания-оттаивания.
3. Маркировка электромобилей с помощью PKH-26
- Подготовка буфера
- Растворите 0,238 г HEPES примерно в 90 мл стерильной сверхчистой воды в стерильной емкости. Используйте свежеприготовленный раствор HEPES. Добавьте в раствор HEPES 0,85 г NaCl.
- Отрегулируйте pH до 7,4 с помощью 1 М NaOH или HCl, в зависимости от необходимости, с помощью откалиброванного pH-метра. Добавьте деионизированную воду, чтобы довести общий объем до 100 мл. Отфильтруйте раствор через фильтр 0,22 мкм для его стерилизации.
- Разведите 4 мкл красителя PKH-26 в 1 мл приготовленного буфера. Тщательно перемешайте пипеткой, чтобы обеспечить однородность.
- Ресуспендируйте очищенные ВВ в 1 мл PBS в концентрации 700 мкг/мл. Добавьте 1 мл суспензии ЭВ в 1 мл приготовленного раствора ПХ-26. Для контрольной группы, в которой используются только красители, добавьте 1 мл полной среды без EV в 1 мл раствора PKH-26. Все последующие шаги выполняются и для контрольной группы, чтобы учесть потенциальную неспецифическую агрегацию или образование мицелл.
- Тщательно перемешайте электромобили, аккуратно перевернув трубку в 10-15 раз. Инкубируйте смесь в течение 3-5 минут при комнатной температуре, обеспечивая равномерное воздействие красителя на EV.
- Приготовьте 2 мл свежего 1% раствора BSA с использованием стерильной сверхчистой воды и добавьте его к 2 мл полученной смеси для гашения реакции мечения. Аккуратно перемешайте, чтобы предотвратить агрегацию.
- Концентрируйте электромобили с маркировкой PKH-26 в соответствии с вышеуказанным протоколом (шаги 2.2-2.7). Ресуспендируйте маркированные электромобили в 300 мкл PBS. Пипеткой нанесите образец EVs с маркировкой PKH-26 в пробирку с фильтром емкостью 30 кДа.
- Центрифугируйте образец при 3 220 x g в течение 30 мин при 4 °C. На этом этапе свободный краситель PKH-26 и малые молекулы будут проходить через мембрану в фильтрат, в то время как меченые PKH-26 EV будут удерживаться в ретентате.
- После первоначального центрифугирования выбросьте фильтрат и добавьте в ретентат 300 мкл PBS. Аккуратно ресуспендируйте электромобили в PBS, пипетируя вверх и вниз.
- Снова центрифугируйте образец при 3 220 x g в течение 30 минут при 4 °C, чтобы смыть оставшийся свободный краситель или мелкие молекулы.
- Подтвердите отсутствие PKH-26 в растворе фильтрата с помощью флуоресцентного микроскопа. Если обнаружен какой-либо краситель, повторите шаги стирки.
- Соберите верхний раствор с помощью микропипетки и снимите фильтр со сборной трубки. Аккуратно переверните фильтр (переверните его вверх дном).
- Центрифугируйте инвертированный фильтр при давлении 800 x g в течение 5 минут при 4 °C. Это поможет собрать оставшиеся ПХ-26-ЭВ с фильтрующей мембраны в новую сборную трубку. Используйте PKH-26-EV непосредственно для следующего шага.
4. 3D Биопечать
- Препарат Bioinks
- Приготовьте свежий 4,5% (масс./об.) раствор натрия Alg в стерильной сверхчистой воде. Перемешайте в течение ночи при температуре 60 °C, чтобы раствор полностью растворился.
- Растворите CMCh в стерильной сверхчистой воде до получения раствора 3,8% (w/v). Готовьте свежие. Перемешайте в течение ночи при температуре 60 °C до полного растворения.
- Центрифугируйте приготовленные биочернила при температуре 3 220 x g в течение 10 минут при 25°C, чтобы удалить любые пузырьки, которые могут помешать процессу печати.
- Смешайте приготовленные 3 мл раствора Alg с маркированными EV или контролем только красителя с помощью шприцевого смесителя до достижения концентрации EV 0,01% (w/v). Обеспечьте равномерное распределение путем бережного перемешивания.
- С помощью шприцевого миксера смешайте 1 мл КМЧ со свежеприготовленным раствором АльгЛиазы в стерильной сверхчистой воде до достижения конечной концентрации 0,5 мЕд/мл.
- Как показано на рисунке 1A, одновременно загрузите биочернила Alg/Exo в основную часть и биочернила CMCh/AlgLyase в часть оболочки шприца с керном/оболочкой.
- Перед печатью дайте биочернилам отдохнуть в течение 15 минут.
- Настройка 3D-биопринтера
- С помощью программного обеспечения 3D-биопринтера создайте структуру каркаса, выбрав цилиндрическую форму с диагональным заполнителем. Для этого установите диаметр и высоту цилиндра на 20 мм, и 1,1 мм соответственно. Отрегулируйте размер пор на 1 мм.
- Установите скорость откачки сердцевины и форсунки оболочки на 1 мм/с при толщине 0,25 мм на слой и установите скорость перемещения на 6 мм/с. Напечатайте четыре слоя толщиной 0,25 мм каждый при комнатной температуре.
- Начните печатать на полиэфирной пленке.
- Используйте увлажнитель с аэрозольным хлоридом кальция (2,2%) для сшивания каркаса в процессе экструзии. Расположите сопло увлажнителя на расстоянии примерно 20 см от экструзионной головки, чтобы обеспечить эффективную сшивку без ущерба для конструкции каркаса. Для дальнейшего сшивания скаффолд погрузить в раствор хлорида кальция (2,2%) на 10 мин.
- Промойте каркас 3 раза стерильной ультрачистой водой, чтобы удалить избыток хлорида кальция и несвязанных биочернил.
- Убедитесь, что каркас хранится в стерильной среде при температуре 4 °C, чтобы сохранить целостность и функциональность каркаса в течение трех месяцев.
5. Отслеживание выпуска электромобилей
- Создание модели круговой кожной раны
- Обезболивание самцов гетерозиготных мышей с диабетом акита (8 недель) путем внутрибрюшинной инъекции кетамина (70 мг/кг) и ксилазина (10 мг/кг). Подтвердите надлежащую анестезию, оценив отсутствие рефлекторных реакций (например, защемление пальца ноги) и контролируя частоту дыхания. Чтобы предотвратить сухость роговицы во время анестезии, наносите на глаза стерильную ветеринарную офтальмологическую мазь.
- Подготовьте участок кожи тыльной стороны, предварительно побрив его с помощью электрической машинки для стрижки. Избегайте раздражения кожи или травм. Простерилизовать выбритый участок с помощью раствора повидон-йода.
- С помощью стерильного захвата создайте круглую кожную рану толщиной 6 мм на тыльной поверхности каждой мыши.
- Аккуратно поместите напечатанный на 3D-принтере каркас с электромобилями с маркировкой PKH непосредственно на раневое ложе. Убедитесь, что каркас полностью покрывает раневую поверхность с минимальным количеством воздушных карманов, слегка надавливая стерильными щипцами. Убедитесь, что животное находится под пристальным наблюдением после процедуры и остается под присмотром до тех пор, пока оно полностью не придет в сознание и не сможет поддерживать лежачее положение за грудиной.
- Флуоресцентная визуализация
- Через 2 ч, 4 ч, 8 ч, 24 ч после имплантации обезболить мышей изофлураном. Для индукции анестезии поместите мышей в камеру системы визуализации in vivo (IVIS) и подвергните их воздействию 2%-3% изофлурана в кислороде. Нанесите офтальмологическую мазь на глаза мышей, чтобы предотвратить сухость. После обезболивания переведите мышей в систему IVIS и поддерживайте их 1%-2% изофлураном в кислороде, доставляемым через носовые каналы. Убедитесь, что животные полностью обезболены и стабильны, прежде чем приступать к визуализации.
- Используйте систему IVIS для захвата флуоресцентных сигналов от электромобилей с маркировкой PKH, выпущенных из каркаса. В мастере визуализации выберите опцию «Флуоресцентная визуализация » и активируйте фильтры возбуждения и излучения для красителя PKH. Отрегулируйте параметры камеры, включая поле зрения и высоту объекта, для оптимизации обнаружения сигнала. Обеспечьте согласованное позиционирование во всех временных точках изображения для точного сравнения. Начните получать изображения и сохраняйте полученные данные.
- Количественное определение интенсивности флуоресцентного сигнала с помощью программного обеспечения IVIS. Это позволит отслеживать выпуск электромобилей с течением времени.
Результаты
Высвобождение ВВ in vivo из каркасов Alg-EVs/CMCh и Alg-EVs/CMCh-AlgLyase показано на рисунке 1B, C. Как и ожидалось, каркас Alg-EVs/CMCh-AlgLyase продемонстрировал более быстрый профиль высвобождения по сравнению с Alg-EVs/CMCh, особенно в моменты времени 2 ч и 4 ч. Высвобождение EV из гидрогелей регулируется комбинацией физико-химических механизмов, включая диффузию, набухание, эрозию и деградацию. Используя Alglyase, каркас облегчает расщепление Alg, ускоряя высвобождение EV для эффективного контроля хронического воспаления на ранних стадиях заживления ран. Ранний выпуск электромобилей имеет решающее значение для смягчения чрезмерного воспаления, которое может замедлить заживление 21,22,23. Чтобы учесть потенциальную неспецифическую агрегацию или образование мицелл, контрольная группа также была проанализирована, выявив пренебрежимо малые флуоресцентные сигналы. Это наблюдение подтверждает, что обнаруженные сигналы в основном исходят от маркированных электромобилей.
Эти результаты отражают критическую роль состава скаффолда в регулировании скорости высвобождения электромобилей. Более быстрое высвобождение, наблюдаемое в каркасе Alg-EVs/CMCh-AlgLyase, объясняется ферментативным распадом Alg Alglyase, что усиливает деградацию гидрогеля. Такое быстрое высвобождение ВВ особенно полезно для борьбы с воспалительной фазой заживления ран24. Хронические раны часто страдают от длительного воспаления, которое ухудшает заживление; раннее и контролируемое высвобождение ВВ может смягчить этот процесс, модулируя воспалительные реакции и способствуя созданию прорегенеративной среды22,25.
Чтобы проанализировать эти результаты, исследователи должны количественно оценить интенсивность флуоресценции, полученную с помощью системы IVIS, коррелируя силу сигнала с концентрацией ВВ с течением времени. Данные должны быть построены на графике, иллюстрирующем кинетику высвобождения, что позволяет сравнивать различные составы каркасов. Вариации профилей высвобождения также могут быть оценены в отношении целостности каркаса и активности ферментов, что позволяет лучше понять основные механизмы высвобождения.
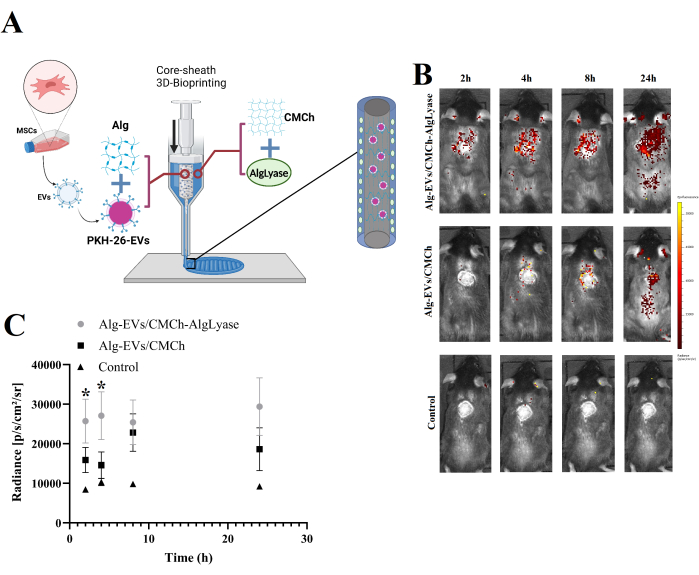
Рисунок 1: Обзор изготовления каркаса и профиля выпуска электромобилей in vivo . (A) Схематическое изображение процесса изготовления каркаса Alg-EVs/CMCh-AlgLyase с помощью 3D-биопечати. (B) Профиль высвобождения in vivo меченых PKH EV из каркаса Alg-EVs/CMCh-AlgLyase по сравнению со скаффолдом Alg-EVs/CMCh и контрольным каркасом, состоящим только из красителей (контроль). Цветные полосы указывают на уровни интенсивности флуоресценции. (C) Количественный анализ интенсивности выброса PKH-EVs (n=3). Полосы погрешностей представляют собой стандартное отклонение, а для оценки статистической значимости использовался односторонний ANOVA. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
Обсуждение
Ключевым аспектом протокола является конструкция каркаса «ядро-оболочка», которая имеет важное значение для достижения эффективной доставки электромобилей. Конструкция включает в себя Alg в качестве основного материала и комбинацию CMCh с Alglyase в качестве оболочки. Такая конфигурация обеспечивает контролируемый и быстрый выпуск электромобилей. Основной материал, Alg, инкапсулирует электромобили, обеспечивая их защиту и локализованную доставку. Оболочка, состоящая из CMCh и Alglyase, обеспечивает ускоренную деградацию ядра Alg, что имеет решающее значение для своевременного выпуска электромобилей. В нашей предыдущей публикации18 мы оценили кинетику высвобождения in vitro ВВ из аналогичной системы скаффолда и продемонстрировали профиль контролируемого высвобождения в течение длительного периода времени, подчеркнув потенциал этого подхода для устойчивого терапевтического эффекта. Это контролируемое разложение и высвобождение достигаются благодаря точным методам составления рецептуры и инкапсуляции. Эти данные позволят коррелировать динамику высвобождения ВВ с прогрессированием заживления ран, что позволит глубже понять клинический потенциал скаффолда.
Система с более медленным высвобождением дает преимущества в терапевтических применениях, где устойчивые, более низкие концентрации препарата или фактора роста могут повысить эффективность при одновременном снижении риска побочных эффектов. Например, постепенное высвобождение может обеспечить непрерывную стимуляцию клеточных процессов в течение более длительного периодавремени26, избегая высоких концентраций, которые могут привести ктоксичности27. Тем не менее, конкретные потребности приложения диктуют идеальный профиль выпуска. В некоторых случаях может быть предпочтительным быстрое высвобождение для обеспечения немедленного терапевтического эффекта28.
Важнейшие этапы в рамках протокола включают подготовку и нанесение слоев материалов биочернил для каркаса керна-оболочки. Поддержание точных концентраций Alg, CMCh и Alglyase во время подготовки биочернил обеспечивает структурную стабильность и эффективную инкапсуляцию EV. Еще одним важным шагом является оптимизация параметров 3D-биопечати, включая скорость сопел и условия сшивки, чтобы обеспечить однородную геометрию и функциональные характеристики каркаса. Оптимизация процесса мечения PKH-26 имеет важное значение для избавления от свободного красителя и нежелательных частиц. Этот процесс повысит точность отслеживания электромобилей.
Протокол был оптимизирован для повышения стабильности каркаса и согласованности выпуска электромобиля. Например, избыток свободного красителя PKH-26 во время мечения был снижен за счет оптимизации соотношения красителя к EV и использования альтернативного метода выделения EVs, лаблированного PKH-26. Для поддержания эффективности каркаса применялась регулярная корректировка параметров 3D-биопечати.
Вязкость биочернил должна быть оптимизирована, чтобы предотвратить засорение во время печати. Для контроля скорости деградации требуется настройка концентрации AlgLyase. Для устранения неполадок с механическими свойствами каркаса необходимо было сбалансировать продолжительность сшивания хлорида кальция, чтобы избежать хрупких или слишком мягких скаффолдов. На этапах маркировки электромобилей, фильтрации и центрифугирования снижение загрязнения свободными красителями и повышение точности результатов визуализации.
В дополнение к прямым преимуществам использования разлагаемых повязок для заживления хронических ран, скорость деградации каркаса значительно влияет на кинетику высвобождения электромобилей. Эта скорость деградации может быть отрегулирована в соответствии с конкретными потребностями раны. Оптимизируя концентрацию AlgLyase в оболочке, скорость деградации ядра Alg может быть точно настроена, что позволяет настроить профиль высвобождения29. Тем не менее, эффективность метода в различных физиологических условиях до сих пор не до конца изучена, поскольку такие факторы, как pH и ферментативная активность в различных типах ран, могут влиять на производительность каркаса. Поэтому следует учитывать изменчивость производительности каркаса при различных физиологических условиях. Такие факторы, как pH, ферментативная активность и колебания температуры в хронических ранах, могут влиять на деградацию каркаса, а EV высвобождают кинетику, потенциально снижая терапевтическую эффективность.
В то время как повязки на основе гидрогеля широко используются благодаря своей биосовместимости и способности поддерживать влажную среду в ране, им часто не хватает способности обеспечивать контролируемую и локализованную доставку биологически активных молекул, таких как EV. Включение ВВ в систему каркаса дает уникальное преимущество, сочетая структурную поддержку с биологически активным терапевтическим компонентом клеточного происхождения, который может модулировать иммунные реакции и усиливать регенерацию тканей.
Аналогичным образом, системы доставки, опосредованные наночастицами, очень эффективны в нацеливании на конкретные клеточные пути; Тем не менее, они могут сталкиваться с проблемами удержания в месте раны и часто требуют дополнительных стабилизирующих агентов для поддержания биологическойактивности30. В отличие от этого, представленная система скаффолдов обеспечивает защитную микросреду, сохраняющую биологическую активность электромобилей во время доставки24.
Несмотря на то, что этот протокол предлагает многообещающие результаты, существуют некоторые ограничения, которые следует учитывать. Одна из проблем заключается в достижении равномерного распределения электромобилей в рамках строительных лесов. Изменения в процессе смешивания могут привести к несоответствиям в концентрации EV по всему каркасу, что может повлиять на воспроизводимость. Для преодоления этой проблемы техника смешивания шприцев является преимуществом. Кроме того, точный контроль условий гелеобразования и сшивки, таких как концентрация ионов кальция в альгинатных каркасах, имеет решающее значение для обеспечения оптимальных механических свойств и структурной целостности. Отклонения в этих параметрах могут ухудшить производительность каркаса. Еще одним ограничением является потенциальная потеря электромобилей во время подготовки каркаса, так как они могут прилипать к пластиковой посуде на этапах мойки. Наконец, срок годности подготовленных скаффолдов относительно короткий, так как гидрогелевые матрицы со временем могут деградировать или потерять функциональность. Таким образом, рекомендуется немедленное использование или кратковременное хранение при температуре 4 °C. Для подтверждения их стабильности требуется периодическое тестирование биологической активности инкапсулированных электромобилей18. Устраняя эти ограничения и применяя предложенные стратегии устранения неполадок, исследователи могут улучшить воспроизводимость и эффективность этого протокола в своих приложениях.
Метод проектирования каркаса с керновой оболочкой представляет собой значительный шаг вперед в доставке лекарств по сравнению с традиционными конструкциями каркасов, в которых отсутствуют механизмы контролируемого высвобождения31. В отличие от однофазных каркасов, которые могут не обеспечивать адекватное или своевременное высвобождение терапевтических агентов, этот метод предлагает динамический подход к доставке ВВ с повышенной точностью. Использование быстро разрушающегося материала сердцевины и функциональной оболочки позволяет проводить более целенаправленное и эффективное терапевтическое вмешательство по сравнению с традиционными методами, которые часто требуют ручной или последовательной корректировки.
В то время как материалы каркаса, используемые в этом исследовании, такие как Alg и CMCh, известны своей биосовместимостью, для клинического применения необходима более тщательная оценка их долгосрочной биосовместимости в условиях хронических ран. В нашей предыдущей работе мы исследовали in vivo эффекты скаффолда на доклинической животной модели и не наблюдали токсических эффектов или значительных иммунных реакций, что позволяет предположить, что материалы хорошо переносятся вкраткосрочной перспективе. Тем не менее, долгосрочная биосовместимость, включая потенциальные иммунные реакции и последствия побочных продуктов распада, требует дальнейшего изучения. Деградация материалов каркаса потенциально может привести к высвобождению побочных продуктов, которые могут повлиять на процесс заживления ран или спровоцировать хроническое воспаление, особенно в контексте диабетических или стареющих моделей, где иммунный ответ может быть изменен. Поэтому крайне важно провести дополнительные исследования, чтобы оценить, как продукты распада влияют на микроокружение раны и общую регенерацию тканей. Мы признаем, что дальнейшие испытания на биосовместимость, включая долгосрочные исследования in vivo , сосредоточенные на иммунных реакциях и деградации каркаса, имеют важное значение для понимания безопасности и клинической значимости этого подхода для заживления хронических ран.
Эта конструкция каркаса особенно важна в области тканевой инженерии и регенеративной медицины. Его способность быстро и контролируемо доставлять электромобили делает его ценным для таких применений, как заживление хронических ран, восстановление хрящей идругие усилия по регенерации тканей. Решая проблемы, связанные с деградацией каркаса и высвобождением ВВ, метод обещает улучшить результаты лечения пациентов в этих областях. Кроме того, его потенциал для кастомизации и адаптации к различным типам тканей подчеркивает его универсальность и актуальность в развитии персонализированной медицины.
Использование модели мышей с диабетом акита в этом исследовании обеспечивает ценную платформу для изучения заживления хронических ран при диабетических состояниях. Эта модель имитирует ключевые патофизиологические характеристики диабетических ран человека, включая стойкую гипергликемию, замедленный ангиогенез и нарушение восстановления тканей33,34. Кроме того, он обладает преимуществом генетической согласованности и спонтанного возникновения диабета без необходимости внешней химической индукции и, следовательно, снижает вариабельностьрезультатов эксперимента. Тем не менее, важно признать ограничения этой модели при переносе результатов на хронические раны человека. Архитектура кожи мыши отличается от человеческой кожи, в частности, более тонким эпидермисом, более рыхлой структурой дермы и преобладающей ролью сокращения раны, а не повторной эпителизации вовремя заживления. Кроме того, иммунные реакции и воспалительные профили мышей не в полной мере репрезентативны по сравнению с теми, которые наблюдаются у людей, что может влиять на интерпретацию иммуномодулирующейтерапии. Несмотря на эти различия, модель акиты остается широко признанным и эффективным инструментом для доклинических исследований благодаря своей способности повторять системные диабетические осложнения, занимающие центральное место в патогенезе хронических ран. Для дальнейшей проверки трансляционного потенциала предложенного терапевтического подхода необходимы будущие исследования, которые дополнят результаты модели Akita. Дополнительные системы, имеющие отношение к человеку, такие как модели кожи человека ex vivo или модели крупных животных с диабетом, будут очень полезны.
В заключение следует отметить, что предложенная конструкция каркаса с контролируемым выбросом ВВ знаменует собой значительный прогресс в доставке терапевтических агентов. Несмотря на технические сложности, этот инновационный подход имеет значительные преимущества по сравнению с существующими методами и обладает большим потенциалом для улучшения повязок на хронических ранах.
Раскрытие информации
Авторы заявляют, что у них нет конфликта интересов.
Благодарности
Особая благодарность Саиду Аль-Хашми и Абдулрахману Альмхарби из Happy Production за отличную работу в кино. Мы также выражаем благодарность Министерству высшего образования, исследований и инноваций и Университету Низвы за их финансовую поддержку и предоставление необходимых ресурсов.
Материалы
| Name | Company | Catalog Number | Comments |
| 23 G Purple precision conical Nozzle | Cellink | KT0000002000 | To provide precise extrusion of bioinks with minimal clogging |
| Alginate lyase (AlgLyase) | Sigma Aldrich | A1603-100MG | Algyase is an enzyme that degrades alginate. |
| Amicon Ultra Centrifugal Filter, 30 kDa MWCO | Merck | UFC9030 | Used to wash PKH-26 labeled-EVs |
| BCA assay Kit | Thermo Scientific | 10678484 | To determine the protein/EVs concentration |
| Bioprinting System | Regemat | V1 | To fabricate core-sheath scaffold |
| Bovine serum albumin (BSA) | sigma-aldrich | 05470-5G | To stop PKH 26 reaction |
| Calcium chloride | Sigma Aldrich | C3306-100G | To crosslink and stabilize bioinks in tissue engineering |
| Centrifuge | Sigma | 2-16P | Used for EVs isolation |
| Centrifuge 5810 R | Eppendorf | 22625101 | Used for cell culture |
| Class II Biological Safety Cabinet | Telstar | Bio II Advance | Cell culture |
| CryoCube F570 Series - ULT Freezer | Eppendorf | F571240035 | To store EVs |
| fluorescent microscope | OLYMPUS | IX73P1F | Used to check the residual PKH-26 in the filtrate |
| Gentamicin (50 mg/mL) | Thermofisher | 15750 | Antibiotic for cell culture media |
| GlutaMAX-I CTS, (100X), liquid | Thermofisher | A12860 | Cell culture media supplement |
| HCl | Sigma Aldrich | 7647-01-0 | Buffer preparation |
| HEPES | Carl Roth | Art. No. 6763.3 | Buffer preparation |
| High viscous carboxymethyl cellulose (CMCh) | BDH | 27929 4T | CMCh is a water-soluble cellulose derivative. |
| Incubator | New Brunswick | NB-170R | Cell culture |
| Invivo imaging | PerkinElmer | IVIS Lumina XRMS Series III | To track EVs release, in vivo |
| Magnet stirer | SalvisLAB | MC35 | For Bioinks preparation |
| miRCURY Exosome Kits for Exosome Isolation | Qiagen | 76743 | Evs isolation |
| NaOh | Daejung | 1310-73-2 | Buffer preparation |
| phosphate buffered saline(PBS) | Thermo Scientific | J61196.AP | Cell culture |
| PKH 26 | MCE | 154214-55-8 | Red fluorescent dye for labeling theEVs |
| Sodium alginate (Alg) | Sigma Aldrich | A0682-100G | Natural polysaccharide derived from brown seaweed. |
| Sodium chloride (NaCl) | Carl Roth | Art-Nr-P029.1 | Buffer preparation |
| StemPro BM Mesenchymal Stem Cells | Thermofisher | A1382901 | Mesenchymal stem cells |
| StemPro MSC SFM XenoFree | Thermofisher | A1067501 | Cell culture media |
| Trypsin 0.25% | Thermofisher | 25050014 | Cell dissociation |
| Vortex-Mixer | Daihan Scientific | VM-10 | Used to mix precipitation buffer with the conditioned media |
Ссылки
- Falanga, V., et al. Chronic wounds. Nat Rev Disease Primers. 8 (1), 50 (2022).
- Tran, H. Q., Shahriar, S. S., Yan, Z., Xie, J. Recent advances in functional wound dressings. Adv Wound Care. 12 (7), 399-427 (2023).
- Shao, M., et al. Emerging trends in therapeutic algorithm of chronic wound healers: Recent advances in drug delivery systems, concepts-to-clinical application and future prospects. Crit Rev Ther Drug Carrier Syst. 34 (5), 385-452 (2017).
- Rezvani Ghomi, E., Khalili, S., Nouri Khorasani, S., Esmaeely Neisiany, R., Ramakrishna, S. Wound dressings: Current advances and future directions. J Appl Poly Sci. 136 (27), 47738 (2019).
- Ding, J. Y., et al. Mesenchymal stem cell-derived extracellular vesicles in skin wound healing: Roles, opportunities and challenges. Military Med Res. 10 (1), 36 (2023).
- Sharma, D., Kumar, A., Mostafavi, E. Extracellular vesicle-based biovectors in chronic wound healing: Biogenesis and delivery approaches. Mol Ther Nucleic Acids. 32, 822-840 (2023).
- Vader, P., Mol, E. A., Pasterkamp, G., Schiffelers, R. M. Extracellular vesicles for drug delivery. Adv Drug Delivery Rev. 106, 148-156 (2016).
- Han, P., Ivanovski, S. 3d bioprinted extracellular vesicles for tissue engineering-a perspective. Biofabrication. 15 (1), 013001 (2022).
- Annabi, N., et al. 25th anniversary article: Rational design and applications of hydrogels in regenerative medicine. Adv Mater. 26 (1), 85-124 (2014).
- Zheng, Y., Pan, C., Xu, P., Liu, K. Hydrogel-mediated extracellular vesicles for enhanced wound healing: The latest progress, and their prospects for 3d bioprinting. J Nanobiotechnol. 22 (1), 57 (2024).
- Keener, A. B. How extracellular vesicles can enhance drug delivery. Nature. 582 (7812), S14-S14 (2020).
- Han, P., et al. 3d bioprinted small extracellular vesicles from periodontal cells enhance mesenchymal stromal cell function. Biomater Adv. 158, 213770 (2024).
- Born, L. J., et al. Sustained released of bioactive mesenchymal stromal cell-derived extracellular vesicles from 3d-printed gelatin methacrylate hydrogels. J Biomed Mater Res A. 110 (6), 1190-1198 (2022).
- Kjar, A., Mcfarland, B., Mecham, K., Harward, N., Huang, Y. Engineering of tissue constructs using coaxial bioprinting. Bioact Mater. 6 (2), 460-471 (2021).
- Gao, Q., He, Y., Fu, J. Z., Liu, A., Ma, L. Coaxial nozzle-assisted 3d bioprinting with built-in microchannels for nutrients delivery. Biomaterials. 61, 203-215 (2015).
- Deshayes, S., Kasko, A. M. Polymeric biomaterials with engineered degradation. J Poly Sci A Poly Chem. 51 (17), 3531-3566 (2013).
- Xu, Q., et al. Injectable hyperbranched poly (β-amino ester) hydrogels with on-demand degradation profiles to match wound healing processes. Chem Sci. 9 (8), 2179-2187 (2018).
- Vakilian, S., et al. Engineered local delivery of extracellular vesicles loaded with si-tnf-α, via a core-sheath 3d-bio-printed scaffold as an effective wound dressing. J Drug Delivery Sci Technol. 101, 106189 (2024).
- Mirsanei, Z., et al. Synergistic effects of mesenchymal stem cell-derived extracellular vesicles and dexamethasone on macrophage polarization under inflammatory conditions. Inflammopharmacology. 32 (2), 1317-1332 (2024).
- Ma, Y., Brocchini, S., Williams, G. R. Extracellular vesicle-embedded materials. J Controlled Release. 361, 280-296 (2023).
- Jia, Q., Zhao, H., Wang, Y., Cen, Y., Zhang, Z. Mechanisms and applications of adipose-derived stem cell-extracellular vesicles in the inflammation of wound healing. Front Immunol. 14, 1214757 (2023).
- Lou, P., et al. Extracellular vesicle-based therapeutics for the regeneration of chronic wounds: Current knowledge and future perspectives. Acta Biomater. 119, 42-56 (2021).
- Cai, Y., Chen, K., Liu, C., Qu, X. Harnessing strategies for enhancing diabetic wound healing from the perspective of spatial inflammation patterns. Bioactive Mater. 28, 243-254 (2023).
- Li, Z., et al. Multifunctional hydrogel-based engineered extracellular vesicles delivery for complicated wound healing. Theranostics. 14 (11), 4198 (2024).
- Cabral, J., Ryan, A. E., Griffin, M. D., Ritter, T. Extracellular vesicles as modulators of wound healing. Adv Drug Delivery Rev. 129, 394-406 (2018).
- Moghadasi Boroujeni, S., Mashayekhan, S., Vakilian, S., Ardeshirylajimi, A., Soleimani, M. The synergistic effect of surface topography and sustained release of tgf-β1 on myogenic differentiation of human mesenchymal stem cells. J Biomed Mater Res A. 104 (7), 1610-1621 (2016).
- Jayaraman, P., et al. Controlled release of drugs in electrosprayed nanoparticles for bone tissue engineering. Adv Drug Delivery Rev. 94, 77-95 (2015).
- Huang, X., Brazel, C. S. On the importance and mechanisms of burst release in matrix-controlled drug delivery systems. J Controlled Release. 73 (2-3), 121-136 (2001).
- Smith, A. M., Senior, J. J. Alginate hydrogels with tuneable properties. Adv Biochem Eng Biotechnol. 178, 37-61 (2021).
- Yan, X., Sha, X. Nanoparticle-mediated strategies for enhanced drug penetration and retention in the airway mucosa. Pharmaceutics. 15 (10), 2457 (2023).
- Pant, B., Park, M., Park, S. -. J. Drug delivery applications of core-sheath nanofibers prepared by coaxial electrospinning: A review. Pharmaceutics. 11 (7), 305 (2019).
- Pinheiro, A., et al. Extracellular vesicles: Intelligent delivery strategies for therapeutic applications. J Controlled Release. 289, 56-69 (2018).
- Yoshioka, M., Kayo, T., Ikeda, T., Koizuni, A. A novel locus, mody4, distal to d7mit189 on chromosome 7 determines early-onset niddm in nonobese c57bl/6 (akita) mutant mice. Diabetes. 46 (5), 887-894 (1997).
- Fang, R. C., et al. Limitations of the db/db mouse in translational wound healing research: Is the noncnzo10 polygenic mouse model superior. Wound Repair Regen. 18 (6), 605-613 (2010).
- Zomer, H. D., Trentin, A. G. Skin wound healing in humans and mice: Challenges in translational research. J Dermatol Sci. 90 (1), 3-12 (2018).
- Sellers, R. S. Translating mouse models: Immune variation and efficacy testing. Toxicol Pathol. 45 (1), 134-145 (2017).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены