Method Article
使用核心鞘 3D 生物打印支架优化细胞外囊泡递送用于慢性伤口管理
摘要
本研究提出了一种制造用于慢性伤口愈合的核心护套 3D 生物打印支架的方案。从间充质干细胞中分离出细胞外囊泡,并用由羧甲基纤维素和海藻酸盐裂解酶制成的鞘装入核心(海藻酸盐)。这种设计允许受控的支架降解和高效的 EV 释放。
摘要
本研究概述了制造芯鞘 3D 生物打印支架的详细方案,旨在增强慢性伤口愈合。该方案涉及从间充质干细胞 (MSC) 中分离细胞外囊泡 (EV),MSC 以其再生和免疫调节特性而闻名。然后将这些 EV 整合到独特的支架结构中。该支架具有一个由载有 EV 的海藻酸盐组成的核心,周围环绕着由羧甲基纤维素和海藻酸盐裂解酶制成的护套。这种创新设计确保了受控的支架降解,同时促进了 EV 在伤口部位的高效和受控释放。该协议涵盖了关键步骤,包括 EV 的制备和表征、用于 3D 生物打印的生物墨水的配方以及打印参数的优化以实现所需的核心鞘结构。通过结合结构完整性和生物活性,该支架旨在解决传统伤口敷料的局限性,提供一种有针对性的方法来加速组织再生并减少慢性伤口的炎症。该方法为开发具有潜在临床应用在慢性伤口管理中的先进生物材料提供了一种可重复和可扩展的策略。该方案还强调了获得一致结果的关键考虑因素,确保对未来治疗应用的适应性。
引言
慢性伤口通常与过度炎症有关,需要及时处理以防止感染和组织坏死等严重并发症,这可能导致截肢。尽管取得了进步,但目前的治疗方法仍然昂贵、不方便、有副作用且疗效有限,这凸显了对更多治愈性敷料的需求 1,2,3。开发专为慢性伤口设计的新一代伤口敷料对于应对这些挑战至关重要。此外,伤口愈合的复杂性要求敷料材料具有一系列特性,包括保湿性、柔韧性、粘附性、生物活性和生物降解性4。本研究旨在开发一种生物工程伤口敷料,将细胞外囊泡 (EV) 与核心鞘 3D 生物打印支架相结合,以提供受控的治疗环境并加速慢性伤口愈合。
源自干细胞的 EV 通过促进抗炎反应、细胞生长、迁移和血管形成来帮助慢性伤口愈合5。此外,EV 可以递送生物活性分子,包括用于慢性伤口管理的生物活性分子、基因和蛋白质构建体 6。此外,它们保护货物免受酶降解的能力提高了治疗剂的稳定性和生物利用度,与传统生长因子和小分子药物相比具有明显的优势,后者通常在体内迅速降解7。尽管有这些优势,但将 EV 高效、持续地递送到靶组织仍然是一个重大挑战。
3D 生物打印支架可以作为 EV 的递送平台,以提高其治疗效果8。这些支架模拟自然细胞环境,并允许 EV 的受控释放 9,10。它们还可以保护 EV 免于降解,增强其 microRNA 和蛋白质的稳定性11。Han 等人证明,EV 可以从 3D 生物打印的 GelMA 支架中有效释放。这种释放导致细胞粘附得到改善,并增强了与接种到支架上的人口腔脂肪垫间充质干细胞 (hBFP-MSCs) 中的机械转导途径相关的基因表达12。Born 等人通过优化交联剂的浓度,实现了 EV 的受控释放。这种方法已被证明在促进血管生成方面有效,并为 EV 的调节递送提供了一种有前途的方法13。
芯鞘 3D 生物打印通过打印包裹在鞘中的芯材,可以创建复杂的多材料结构。核心可以包括细胞、生长因子或药物,而护套提供机械支撑和保护或充当屏障。该方法在组织工程和再生医学中具有应用,例如开发血管网络、模拟自然组织结构和创建药物递送系统。它允许精确控制材料分布和组成,增强结构的功能和生物学相关性。与其他技术相比,芯鞘 3D 生物打印提供了对材料分布和组成的精确控制,从而提高了结构的功能和生物学相关性14,15。
伤口敷料中的工程降解具有减少变化期间的不适感、用于愈合和感染控制的潮湿环境、及时的治疗输送以及最佳的组织再生等好处 16,17,18。海藻酸盐 (Alg) 和羧甲基纤维素 (CMCh) 水凝胶具有生物相容性,可有效将细胞外囊泡 (EV) 输送到伤口,通过细胞通讯和减少炎症来促进愈合18。在这项研究中,EV 被整合到 Alg 的核心中,而 CMCh 和 AlgLyase (AlgLyase) 的鞘被用于实现快速敷料降解和 EV 递送。这种核心鞘设计有助于响应支架降解而快速释放 EV,增强其治疗效果并解决现有慢性伤口治疗的局限性。本研究的主要目的是开发一种生物工程敷料,通过将受控的 EV 释放与响应性可降解的支架相结合来促进伤口愈合,最终改善慢性伤口的治疗结果。
研究方案
动物研究完全按照国家生物伦理委员会和尼兹瓦大学动物伦理委员会制定的道德标准进行。本研究的伦理批准是在许可 ID:VCGSR, AREC/01/2023 下授予的。所有动物都被饲养在标准的实验室条件下,确保最佳的环境控制、适当的营养和全面的照顾,以在整个研究过程中保护它们的福利。所有涉及动物的程序都严格遵守机构政策、国际动物护理标准和 ARRIVE 指南。
1. 细胞培养
- 从液氮储存中取出一小瓶 MSC(传代 #2),并使用无菌技术处理以防止污染。在 37 °C 水浴中快速解冻细胞,确保在有小冰碎片残留时立即将其取出。
- 制备完全培养基,包括 MSC SFM 基础培养基,补充有 1% (v/v) MSC SFM XenoFree 补充剂、1% (v/v) GlutaMAX 和 0.01% (v/v) 庆大霉素。以每 5 秒 3 至 5 滴的速率向样品瓶中加入 1 mL 预热 (37 °C) 完全培养基,然后轻轻混合。在无菌条件下,将 MSC 样品瓶的全部内容物转移到 II 级生物安全柜中,放入装有 4 mL 预热完全培养基的 15 mL 锥形管中。
- 在室温下以 200 x g 离心细胞 5 分钟。确保离心机平衡正确。
- 吸出上清液,并将细胞重悬于 1 mL 预热的完全培养基中。然后,将细胞转移到含有 4 mL 完全培养基的 T25 培养瓶中。
- 轻轻倾斜培养瓶以确保细胞均匀分布。将培养瓶在 37 °C 和 5% CO2 下孵育。
- 每 2 天更换一次培养基,换上新鲜的、预热的完全培养基。使用轻柔的移液以避免细胞破裂。达到 70%-80% 汇合度后,从 T25 培养瓶中吸出用过的培养基。
- 用 3 mL 新鲜 PBS 洗涤细胞以去除残留物。确保在洗涤过程中完全覆盖培养瓶。
- 向 T25 培养瓶中加入 1 mL 0.25% 胰蛋白酶溶液,在 37 °C 下孵育 3-7 分钟,并在显微镜下以 4 倍放大倍率仔细监测分离。
- 如果需要,轻轻敲击培养瓶以确保细胞完全分离。将预热的完全培养基加入培养瓶中,并在表面上下移液以帮助分离细胞。然后,将细胞悬液转移到 15 mL 离心管中。
- 在室温下以 200 x g 离心管 5 分钟。将细胞沉淀悬浮在新鲜的完全培养基中,并使用 Neubauer 血细胞计数器对细胞进行计数。将细胞转移到 T75 培养瓶中。确保接种密度为 5,000 个细胞/cm2 以实现最佳生长。
- 将细胞在 37 °C 和 5% CO2 下孵育。细胞孵育 72 小时后,从细胞中收集条件培养基用于 EV 分离。采集后立即使用。
2. 电动汽车隔离
- 将收集的 13 mL 条件培养基以 800 x g 离心 15 分钟以去除细胞碎片。使用 0.22 μm 注射器过滤器轻轻过滤上清液以去除大颗粒。
- 向过滤后的调节培养基中加入 5 mL 沉淀缓冲液,并充分涡旋混合。确保溶液是均匀的。
- 将混合物在 4 °C 下孵育过夜,以使 EV 沉淀。将混合物在 20 °C 下以 3,220 x g 离心 30 分钟。 检查管子的平衡。
- 小心丢弃上清液,不要干扰沉淀。将沉淀再次以 3,220 x g 离心 5 秒以去除残留液体。
- 在 200 μL PBS 中轻轻移液 EV 沉淀,以避免损坏 EV。按照制造商的说明(BCA 蛋白质测定试剂盒)测量 EVs 蛋白浓度。
- 进行蛋白质印迹以检测 EV 特异性标志物(CD63、CD81 和 CD9),以验证 EV 表型18。分析证实了这些标记的存在,验证了 EV 的身份19。
- 为了最大限度地降低 RNase 污染的风险,建议直接使用,无需额外储存。如果需要,请将 EV 储存在 -80 °C 以备进一步使用。将 EV 悬浮液分装成 40 μL 体积,以避免重复冻融循环。
3. 使用 PKH-26 标记 EV
- 缓冲液制备
- 将 0.238 g HEPES 溶于无菌容器中约 90 mL 的无菌超纯水中。使用新鲜制备的 HEPES 溶液。向 HEPES 溶液中加入 0.85 g NaCl。
- 根据需要,使用校准的 pH 计,使用 1 M NaOH 或 HCl 将 pH 调节至 7.4。加入去离子水,使总体积达到 100 mL。通过 0.22 μm 过滤器过滤溶液以对其进行消毒。
- 在 1 mL 制备的缓冲液中稀释 4 μL PKH-26 染料。用移液管充分混合以确保均匀性。
- 将纯化的 EV 重悬于 1 mL 浓度为 700 μg/mL 的 PBS 中。将 1 mL EVS 悬浮液添加到 1 mL 制备的 PKH-26 溶液中。对于仅染料对照组,将 1 mL 不含 EV 的完全培养基添加到 1 mL PKH-26 溶液中。对对照组执行所有后续步骤,以考虑潜在的非特异性聚集或胶束形成。
- 通过轻轻将试管倒置 10 倍至 15 倍,将 EV 彻底混合。在室温下将混合物孵育 3-5 分钟,确保 EV 均匀暴露于染料中。
- 使用无菌超纯水制备 2 mL 新鲜的 1% BSA 溶液,并将其添加到 2 mL 所得混合物中以淬灭标记反应。轻轻混合以防止聚集。
- 根据上述方案(步骤 2.2-2.7)浓缩 PKH-26 标记的 EV。将标记的 EV 重悬于 300 μL PBS 中。将 PKH-26 标记的 EV 样品移液到 30 kDa 过滤管中。
- 将样品在 4 °C 下以 3,220 x g 离心 30 分钟。 在此步骤中,游离的 PKH-26 染料和小分子将穿过膜进入滤液,而 PKH-26 标记的 EV 将保留在截留物中。
- 初次离心后,弃去滤液,向截留物中加入 300 μL PBS。通过上下移液轻轻地将 EV 重悬于 PBS 中。
- 在 4 °C 下以 3,220 x g 再次离心样品 30 分钟,以洗去任何残留的游离染料或小分子。
- 通过荧光显微镜确认滤液溶液中缺乏 PKH-26。如果检测到任何染料,请重复洗涤步骤。
- 用微量移液器收集顶部溶液,并从收集管中取出过滤器。小心地反转过滤器(将其倒置)。
- 将倒置过滤器在 4 °C 下以 800 x g 离心 5 分钟。 这将有助于将保留的 PKH-26-EV 从滤膜收集到新的收集管中。直接使用 PKH-26-EV 进行下一步。
4. 3D 生物打印
- 生物墨水制备
- 使用无菌超纯水制备新鲜的 4.5% (w/v) Alg 钠溶液。在 60 °C 下搅拌过夜,使溶液完全溶解。
- 将 CMCh 溶解在无菌超纯水中,以获得 3.8% (w/v) 的溶液。新鲜准备。在 60 °C 下搅拌过夜以完全溶解。
- 将制备好的生物墨水在 25°C 下以 3,220 x g 离心 10 分钟,以去除任何可能干扰打印过程的气泡。
- 使用注射器混合器将制备的 3 mL Alg 溶液与标记的 EV 或仅染料对照混合,以达到 0.01% (w/v) 的 EV 浓度。通过温和混合确保均匀分布。
- 使用注射器混合器,将 1 mL CMCh 与新鲜制备的 AlgLyase 溶液在无菌超纯水中混合,以达到 0.5 mU/mL 的最终浓度。
- 如图 1A 所示,同时将 Alg/Exo 生物墨水加载到核心部分,将 CMCh/AlgLyase 生物墨水加载到核心/鞘管注射器设置的护套部分。
- 打印前让生物墨水静置 15 分钟。
- 3D 生物打印机设置
- 使用 3D-bioprinter 软件,通过选择 具有对角填充图案的圆柱形来创建脚手架结构。为此,请将圆柱体直径和高度分别设置为 20 mm 和 1.1 mm。将孔径配置为 1 mm。
- 将核心和护套喷嘴抽速设置为 1 mm/s,每层厚度为 0.25 mm,并将移动速度设置为 6 mm/s。在室温下打印四层,每层厚度为 0.25 毫米。
- 开始在聚酯薄膜上打印。
- 在挤出过程中,使用含气雾剂氯化钙 (2.2%) 的加湿器交联支架。将加湿器喷嘴放置在距离挤出头约 20 cm 的位置,以确保在不影响支架结构的情况下有效交联。为了进一步交联,将支架浸入氯化钙溶液 (2.2%) 中 10 分钟。
- 用无菌超纯水冲洗支架 3 次,以去除任何多余的氯化钙和未结合的生物墨水。
- 确保将支架存放在 4 °C 的无菌环境中,以保持支架的完整性和功能长达三个月。
5. 跟踪电动汽车的发布
- 创建圆形皮肤伤口模型
- 通过腹膜内注射氯胺酮(70 mg / kg)和甲苯噻嗪(10 mg / kg)麻醉雄性秋田杂合糖尿病小鼠(8周)。通过评估无反射反应(例如,脚趾捏合)来确认适当的麻醉并监测呼吸频率。为防止麻醉期间角膜干燥,请在眼睛上涂抹无菌兽用眼药膏。
- 首先使用电动剪刀剃须背侧皮肤区域。避免皮肤刺激或受伤。使用聚维酮碘溶液对剃光区域进行消毒。
- 使用无菌 seizer,在每只小鼠的背面创建一个 6 mm 的圆形全层皮肤伤口。
- 将含有 PKH 标记的 EV 的 3D 生物打印支架直接轻轻地放在伤口床上。使用无菌镊子轻轻按压,确保支架完全覆盖伤口表面,气穴最小。确保在手术后密切观察动物并保持照料状态,直到它完全恢复意识并可以保持胸骨卧位。
- 荧光成像
- 在植入后 2 小时、4 小时、8 小时、24 小时,使用异氟醚麻醉小鼠。为了诱导麻醉,将小鼠置于 体内 成像系统 (IVIS) 的腔室中,并将它们暴露于 2%-3% 异氟醚的氧气中。在小鼠的眼睛上涂抹眼药膏以防止干燥。麻醉后,将小鼠转移到 IVIS 系统,并用通过鼻通道输送的 1%-2% 异氟醚氧气维持它们。在进行成像之前,请确认动物已完全麻醉且稳定。
- 使用 IVIS 系统捕获来自支架释放的 PKH 标记 EV 的荧光信号。在成像向导中,选择 Fluorescence Imaging(荧光成像 )选项并激活 PKH 染料的激发和发射滤光片。调整相机设置,包括视野和被摄体高度,以优化信号检测。确保所有成像时间点的定位一致,以实现准确的比较。开始采集图像并保存结果数据。
- 使用 IVIS 软件量化荧光信号强度。这将允许跟踪 EV 随时间的释放。
结果
Alg-EVs/CMCh 和 Alg-EVs/CMCh-AlgLyase 支架的 EV 在体内释放如图 1B、C 所示。正如预期的那样,与 Alg-EVs/CMCh 相比,Alg-EVs/CMCh-AlgLyase 支架表现出更快的释放曲线,尤其是在 2 h 和 4 h 时间点。EV 从水凝胶中释放受物理化学机制的组合控制,包括扩散、溶胀、侵蚀和降解20。通过利用 Alglyase ,支架促进 Alg 的分解,加速 EV 的释放,从而在伤口愈合的早期阶段有效控制慢性炎症。EV 的早期释放对于减轻过度炎症至关重要,过度炎症会延迟愈合 21,22,23。为了解释潜在的非特异性聚集或胶束形成,还分析了对照组,揭示了可忽略不计的荧光信号。这一观察结果证实,检测到的信号主要来自标记的 EV。
这些结果反映了支架组合物在调节 EV 释放率中的关键作用。在 Alg-EVs/CMCh-AlgLyase 支架中观察到的更快释放归因于 Alglyase 对 Alg 的酶促分解,这增强了水凝胶降解。这种快速释放的 EV 对于解决伤口愈合的炎症阶段特别有利24。慢性伤口通常患有长期炎症,这会损害愈合;EV 的早期和受控释放可以通过调节炎症反应和促进再生环境来缓解这种情况22,25。
为了分析这些结果,研究人员应量化使用 IVIS 系统捕获的荧光强度,将信号强度与 EV 浓度随时间相关联。应绘制数据以说明释放动力学,以便比较不同的支架配方。还可以评估支架完整性和酶活性的释放曲线变化,从而进一步了解潜在的释放机制。
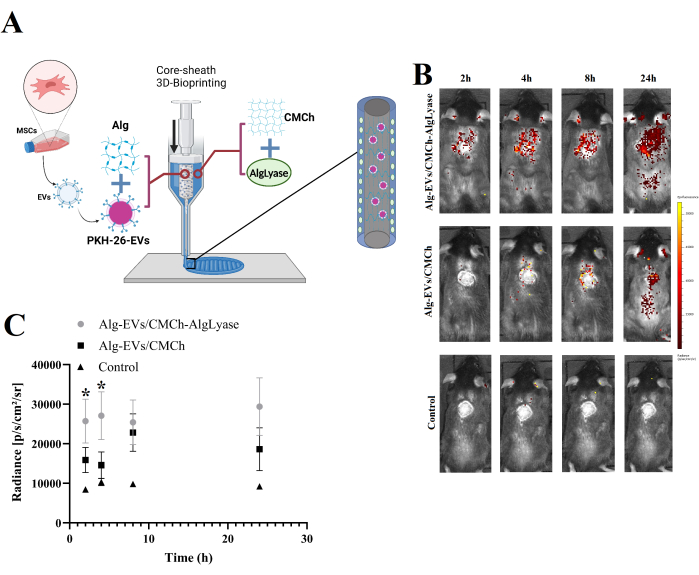
图 1:支架制造和 体内 EV 释放概况概述。 (A) Alg-EVs/CMCh-AlgLyase 3D 生物打印支架的制造过程示意图。(B) 与 Alg-EVs/CMCh-AlgLyase 支架和仅染料对照支架(对照)相比,Alg-EVs/CMCh-AlgLyase 支架中 PKH 标记的 EV 的 体内 释放曲线。颜色条表示荧光强度水平。(C) PKH-EVs 释放强度的定量分析 (n=3)。误差线代表标准差,单因素方差分析用于评估统计显著性。 请单击此处查看此图的较大版本。
讨论
该协议的一个关键方面是核心护套支架设计,这对于实现高效的电动汽车交付至关重要。该设计以 Alg 为核心材料,将 CMCh 与 Alglyase 相结合作为鞘。这种设置有助于 EV 的受控和快速释放。核心材料 Alg 封装了 EV,确保其保护和本地化交付。该鞘由 CMCh 和 Alglyase 组成,能够加速 Alg 核心的降解,这对于及时释放 EV 至关重要。在我们之前的出版物18 中,我们评估了来自类似支架系统的 EV 的 体外 释放动力学,并证明了长时间的控释曲线,突出了这种方法获得持续治疗效果的潜力。这种受控的降解和释放是通过精确的配方和封装技术实现的。这些数据将使 EV 释放动力学与伤口愈合进展相关联,从而更深入地了解支架的临床潜力。
较慢的释放系统在治疗应用中具有优势,在这些应用中,持续、较低浓度的药物或生长因子可以提高疗效,同时降低副作用的风险。例如,逐渐释放可以确保在较长时间内持续刺激细胞过程26,避免可能导致毒性的高浓度27。但是,应用程序的特定需求决定了理想的发布配置文件。在某些情况下,快速释放可能是提供即时治疗效果的首选28。
该协议中的关键步骤包括为核心护套支架准备和分层生物墨水材料。在生物墨水制备过程中保持 Alg、CMCh 和 Alglyase 的精确浓度可确保结构稳定性和有效的 EV 包封。另一个关键步骤是优化 3D 生物打印参数,包括喷嘴速度和交联条件,以确保一致的支架几何形状和功能性能。优化 PKH-26 标记工艺对于去除游离染料和不需要的颗粒至关重要。这个过程将提高 EV 的跟踪精度。
该协议已经过优化,以增强基架的稳定性和 EV 发布的一致性。例如,通过优化染料与 EV 比率并使用替代的 PKH-26 标记的 EVs 分离方法,可以减轻标记过程中过量的游离 PKH-26 染料。定期调整 3D 生物打印参数以保持支架的有效性。
应优化生物墨水的粘度,以防止打印过程中堵塞。需要调整 AlgLyase 浓度以控制降解速率。对支架的机械性能进行故障排除涉及平衡氯化钙交联持续时间,以避免支架变脆或过于柔软。在 EV 标记过程中,过滤和离心步骤减轻了游离染料污染,提高了成像结果的准确性。
除了使用可降解敷料进行慢性伤口愈合的直接好处外,支架的降解速率还显着影响 EV 的释放动力学。这种降解速率可以调整以满足伤口的特定需求。通过优化鞘中 AlgLyase 的浓度,可以微调 Alg 核心的降解速率,从而允许自定义释放曲线29。然而,该方法在不同生理条件下的有效性仍不完全清楚,因为不同类型伤口中的 pH 值和酶活性等因素可能会影响支架的性能。因此,应考虑不同生理条件下支架性能的可变性。慢性伤口的 pH 值、酶活性和温度变化等因素可能会影响支架的降解和 EV 释放动力学,从而可能降低治疗效果。
虽然基于水凝胶的伤口敷料因其生物相容性和维持湿润伤口环境的能力而被广泛使用,但它们通常缺乏提供生物活性分子(如 EV)的受控和局部递送的能力。将 EV 整合到支架系统中提供了独特的优势,它将结构支持与生物活性的细胞衍生治疗成分相结合,可以调节免疫反应并增强组织再生。
同样,纳米颗粒介导的递送系统在靶向特定细胞通路方面非常有效;然而,它们可能面临在伤口部位保留的挑战,并且通常需要额外的稳定剂来维持生物活性30。相比之下,所提出的支架系统提供了一个保护性微环境,可在交付过程中保持 EV 的生物活性24。
虽然该协议提供了有希望的结果,但也应考虑一些限制。一个挑战在于在支架内实现 EV 的均匀分布。混合过程的变化可能导致整个支架上 EV 浓度不一致,从而影响可重复性。为了克服这一挑战,注射器混合技术是一个优势。此外,精确控制凝胶化和交联条件,例如藻酸盐支架的钙离子浓度,对于确保最佳机械性能和结构完整性至关重要。这些参数的偏差可能会影响基架性能。另一个限制是在脚手架准备过程中 EV 的潜在损失,因为它们在清洗步骤中会粘附在塑料器皿上。最后,制备的支架的保质期相对较短,因为水凝胶基质可能会随着时间的推移而降解或失去功能。因此,建议立即使用或在 4 °C 下短期储存。需要对封装的 EV 进行定期生物活性测试,以确认其稳定性18。通过解决这些限制并采用建议的故障排除策略,研究人员可以提高该方案在其应用中的可重复性和有效性。
与缺乏控释机制的传统支架设计相比,核心-鞘护支架设计方法在药物递送方面取得了重大进步31。与可能无法提供充分或及时释放治疗剂的单相支架不同,这种方法提供了一种具有更高精度的 EV 递送的动态方法。与传统方法相比,使用快速降解的核心材料和功能性护套可以进行更针对性和更有效的治疗干预,传统方法通常需要手动或顺序调整。
虽然本研究中使用的支架材料(如 Alg 和 CMCh)以其生物相容性而闻名,但需要更彻底地评估它们在慢性伤口环境中的长期生物相容性对于临床转化是必要的。在我们之前的工作中,我们在临床前动物模型中研究了支架的 体内 效应,没有观察到毒性作用或显着的免疫反应,这表明这些材料在短期内具有良好的耐受性18。然而,长期的生物相容性,包括潜在的免疫反应和降解副产物的影响,需要进一步探索。支架材料的降解可能会释放出可能影响伤口愈合过程或引发慢性炎症的副产物,尤其是在糖尿病或老年模型的情况下,免疫反应可能会发生变化。因此,进行额外的研究以评估降解产物如何影响伤口微环境和整体组织再生至关重要。我们承认,进一步的生物相容性测试,包括专注于免疫反应和支架降解的长期 体内 研究,对于了解这种方法对慢性伤口愈合的安全性和临床相关性至关重要。
这种支架设计在组织工程和再生医学领域尤为重要。它能够以受控方式快速输送 EV,使其在慢性伤口愈合、软骨修复和其他组织再生工作等应用中很有价值32。通过解决与支架降解和 EV 释放相关的问题,该方法有望改善这些领域的患者预后。此外,它对不同组织类型的定制和适应潜力强调了它在推进个性化医疗方面的多功能性和相关性。
本研究中使用秋田糖尿病小鼠模型为研究糖尿病条件下的慢性伤口愈合提供了一个有价值的平台。该模型模拟了人类糖尿病伤口的关键病理生理学特征,包括持续性高血糖、血管生成延迟和组织修复受损33,34。此外,它提供了遗传一致性和糖尿病自发性的优势,无需外部化学诱导,从而减少了实验结果的可变性33。然而,在将研究结果转化为人类慢性伤口时,重要的是要承认该模型的局限性。小鼠皮肤结构与人类皮肤不同,特别是其表皮较薄、真皮结构较松散,以及伤口收缩而不是愈合过程中再上皮化的主要作用35。此外,小鼠免疫反应和炎症特征不能完全代表在人类中观察到的免疫反应和炎症特征,这可能会影响免疫调节疗法的解释36。尽管存在这些差异,但秋田模型仍然是临床前研究的广泛接受和有效的工具,因为它能够概括慢性伤口发病机制的核心全身性糖尿病并发症。为了进一步验证所提出的治疗方法的转化潜力,有必要进行未来的研究以补充秋田模型的发现。其他与人类相关的系统,例如离体人体皮肤模型或糖尿病大型动物模型,将具有高度支持性。
总之,拟议的具有 EV 受控释放的支架设计标志着治疗剂递送的重大进步。尽管技术复杂,但与现有方法相比,这种创新方法具有显着优势,并且在改善慢性伤口敷料方面具有巨大潜力。
披露声明
作者声明他们没有利益冲突。
致谢
特别感谢 Happy Production 的 Said Al-Hashmi 和 Abdulrahman Almharbi 在拍摄中的出色工作。我们还感谢高等教育、研究和创新部以及 Nizwa 大学提供的财政支持和提供所需的资源。
材料
| Name | Company | Catalog Number | Comments |
| 23 G Purple precision conical Nozzle | Cellink | KT0000002000 | To provide precise extrusion of bioinks with minimal clogging |
| Alginate lyase (AlgLyase) | Sigma Aldrich | A1603-100MG | Algyase is an enzyme that degrades alginate. |
| Amicon Ultra Centrifugal Filter, 30 kDa MWCO | Merck | UFC9030 | Used to wash PKH-26 labeled-EVs |
| BCA assay Kit | Thermo Scientific | 10678484 | To determine the protein/EVs concentration |
| Bioprinting System | Regemat | V1 | To fabricate core-sheath scaffold |
| Bovine serum albumin (BSA) | sigma-aldrich | 05470-5G | To stop PKH 26 reaction |
| Calcium chloride | Sigma Aldrich | C3306-100G | To crosslink and stabilize bioinks in tissue engineering |
| Centrifuge | Sigma | 2-16P | Used for EVs isolation |
| Centrifuge 5810 R | Eppendorf | 22625101 | Used for cell culture |
| Class II Biological Safety Cabinet | Telstar | Bio II Advance | Cell culture |
| CryoCube F570 Series - ULT Freezer | Eppendorf | F571240035 | To store EVs |
| fluorescent microscope | OLYMPUS | IX73P1F | Used to check the residual PKH-26 in the filtrate |
| Gentamicin (50 mg/mL) | Thermofisher | 15750 | Antibiotic for cell culture media |
| GlutaMAX-I CTS, (100X), liquid | Thermofisher | A12860 | Cell culture media supplement |
| HCl | Sigma Aldrich | 7647-01-0 | Buffer preparation |
| HEPES | Carl Roth | Art. No. 6763.3 | Buffer preparation |
| High viscous carboxymethyl cellulose (CMCh) | BDH | 27929 4T | CMCh is a water-soluble cellulose derivative. |
| Incubator | New Brunswick | NB-170R | Cell culture |
| Invivo imaging | PerkinElmer | IVIS Lumina XRMS Series III | To track EVs release, in vivo |
| Magnet stirer | SalvisLAB | MC35 | For Bioinks preparation |
| miRCURY Exosome Kits for Exosome Isolation | Qiagen | 76743 | Evs isolation |
| NaOh | Daejung | 1310-73-2 | Buffer preparation |
| phosphate buffered saline(PBS) | Thermo Scientific | J61196.AP | Cell culture |
| PKH 26 | MCE | 154214-55-8 | Red fluorescent dye for labeling theEVs |
| Sodium alginate (Alg) | Sigma Aldrich | A0682-100G | Natural polysaccharide derived from brown seaweed. |
| Sodium chloride (NaCl) | Carl Roth | Art-Nr-P029.1 | Buffer preparation |
| StemPro BM Mesenchymal Stem Cells | Thermofisher | A1382901 | Mesenchymal stem cells |
| StemPro MSC SFM XenoFree | Thermofisher | A1067501 | Cell culture media |
| Trypsin 0.25% | Thermofisher | 25050014 | Cell dissociation |
| Vortex-Mixer | Daihan Scientific | VM-10 | Used to mix precipitation buffer with the conditioned media |
参考文献
- Falanga, V., et al. Chronic wounds. Nat Rev Disease Primers. 8 (1), 50 (2022).
- Tran, H. Q., Shahriar, S. S., Yan, Z., Xie, J. Recent advances in functional wound dressings. Adv Wound Care. 12 (7), 399-427 (2023).
- Shao, M., et al. Emerging trends in therapeutic algorithm of chronic wound healers: Recent advances in drug delivery systems, concepts-to-clinical application and future prospects. Crit Rev Ther Drug Carrier Syst. 34 (5), 385-452 (2017).
- Rezvani Ghomi, E., Khalili, S., Nouri Khorasani, S., Esmaeely Neisiany, R., Ramakrishna, S. Wound dressings: Current advances and future directions. J Appl Poly Sci. 136 (27), 47738 (2019).
- Ding, J. Y., et al. Mesenchymal stem cell-derived extracellular vesicles in skin wound healing: Roles, opportunities and challenges. Military Med Res. 10 (1), 36 (2023).
- Sharma, D., Kumar, A., Mostafavi, E. Extracellular vesicle-based biovectors in chronic wound healing: Biogenesis and delivery approaches. Mol Ther Nucleic Acids. 32, 822-840 (2023).
- Vader, P., Mol, E. A., Pasterkamp, G., Schiffelers, R. M. Extracellular vesicles for drug delivery. Adv Drug Delivery Rev. 106, 148-156 (2016).
- Han, P., Ivanovski, S. 3d bioprinted extracellular vesicles for tissue engineering-a perspective. Biofabrication. 15 (1), 013001 (2022).
- Annabi, N., et al. 25th anniversary article: Rational design and applications of hydrogels in regenerative medicine. Adv Mater. 26 (1), 85-124 (2014).
- Zheng, Y., Pan, C., Xu, P., Liu, K. Hydrogel-mediated extracellular vesicles for enhanced wound healing: The latest progress, and their prospects for 3d bioprinting. J Nanobiotechnol. 22 (1), 57 (2024).
- Keener, A. B. How extracellular vesicles can enhance drug delivery. Nature. 582 (7812), S14-S14 (2020).
- Han, P., et al. 3d bioprinted small extracellular vesicles from periodontal cells enhance mesenchymal stromal cell function. Biomater Adv. 158, 213770 (2024).
- Born, L. J., et al. Sustained released of bioactive mesenchymal stromal cell-derived extracellular vesicles from 3d-printed gelatin methacrylate hydrogels. J Biomed Mater Res A. 110 (6), 1190-1198 (2022).
- Kjar, A., Mcfarland, B., Mecham, K., Harward, N., Huang, Y. Engineering of tissue constructs using coaxial bioprinting. Bioact Mater. 6 (2), 460-471 (2021).
- Gao, Q., He, Y., Fu, J. Z., Liu, A., Ma, L. Coaxial nozzle-assisted 3d bioprinting with built-in microchannels for nutrients delivery. Biomaterials. 61, 203-215 (2015).
- Deshayes, S., Kasko, A. M. Polymeric biomaterials with engineered degradation. J Poly Sci A Poly Chem. 51 (17), 3531-3566 (2013).
- Xu, Q., et al. Injectable hyperbranched poly (β-amino ester) hydrogels with on-demand degradation profiles to match wound healing processes. Chem Sci. 9 (8), 2179-2187 (2018).
- Vakilian, S., et al. Engineered local delivery of extracellular vesicles loaded with si-tnf-α, via a core-sheath 3d-bio-printed scaffold as an effective wound dressing. J Drug Delivery Sci Technol. 101, 106189 (2024).
- Mirsanei, Z., et al. Synergistic effects of mesenchymal stem cell-derived extracellular vesicles and dexamethasone on macrophage polarization under inflammatory conditions. Inflammopharmacology. 32 (2), 1317-1332 (2024).
- Ma, Y., Brocchini, S., Williams, G. R. Extracellular vesicle-embedded materials. J Controlled Release. 361, 280-296 (2023).
- Jia, Q., Zhao, H., Wang, Y., Cen, Y., Zhang, Z. Mechanisms and applications of adipose-derived stem cell-extracellular vesicles in the inflammation of wound healing. Front Immunol. 14, 1214757 (2023).
- Lou, P., et al. Extracellular vesicle-based therapeutics for the regeneration of chronic wounds: Current knowledge and future perspectives. Acta Biomater. 119, 42-56 (2021).
- Cai, Y., Chen, K., Liu, C., Qu, X. Harnessing strategies for enhancing diabetic wound healing from the perspective of spatial inflammation patterns. Bioactive Mater. 28, 243-254 (2023).
- Li, Z., et al. Multifunctional hydrogel-based engineered extracellular vesicles delivery for complicated wound healing. Theranostics. 14 (11), 4198 (2024).
- Cabral, J., Ryan, A. E., Griffin, M. D., Ritter, T. Extracellular vesicles as modulators of wound healing. Adv Drug Delivery Rev. 129, 394-406 (2018).
- Moghadasi Boroujeni, S., Mashayekhan, S., Vakilian, S., Ardeshirylajimi, A., Soleimani, M. The synergistic effect of surface topography and sustained release of tgf-β1 on myogenic differentiation of human mesenchymal stem cells. J Biomed Mater Res A. 104 (7), 1610-1621 (2016).
- Jayaraman, P., et al. Controlled release of drugs in electrosprayed nanoparticles for bone tissue engineering. Adv Drug Delivery Rev. 94, 77-95 (2015).
- Huang, X., Brazel, C. S. On the importance and mechanisms of burst release in matrix-controlled drug delivery systems. J Controlled Release. 73 (2-3), 121-136 (2001).
- Smith, A. M., Senior, J. J. Alginate hydrogels with tuneable properties. Adv Biochem Eng Biotechnol. 178, 37-61 (2021).
- Yan, X., Sha, X. Nanoparticle-mediated strategies for enhanced drug penetration and retention in the airway mucosa. Pharmaceutics. 15 (10), 2457 (2023).
- Pant, B., Park, M., Park, S. -. J. Drug delivery applications of core-sheath nanofibers prepared by coaxial electrospinning: A review. Pharmaceutics. 11 (7), 305 (2019).
- Pinheiro, A., et al. Extracellular vesicles: Intelligent delivery strategies for therapeutic applications. J Controlled Release. 289, 56-69 (2018).
- Yoshioka, M., Kayo, T., Ikeda, T., Koizuni, A. A novel locus, mody4, distal to d7mit189 on chromosome 7 determines early-onset niddm in nonobese c57bl/6 (akita) mutant mice. Diabetes. 46 (5), 887-894 (1997).
- Fang, R. C., et al. Limitations of the db/db mouse in translational wound healing research: Is the noncnzo10 polygenic mouse model superior. Wound Repair Regen. 18 (6), 605-613 (2010).
- Zomer, H. D., Trentin, A. G. Skin wound healing in humans and mice: Challenges in translational research. J Dermatol Sci. 90 (1), 3-12 (2018).
- Sellers, R. S. Translating mouse models: Immune variation and efficacy testing. Toxicol Pathol. 45 (1), 134-145 (2017).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。