Method Article
Дополнительная диодная лазерная терапия и пробиотическая лактобактериальная терапия в лечении пародонтита и периимплантации
В этой статье
Резюме
В этой статье описываются два протокола: 1) дополнительная диодная лазерная терапия для лечения пародонтита и 2) пробиотическая лактобацилла для лечения периимплантного заболевания с акцентом на режим использования лазера (внутри или снаружи кармана), режим применения лазера (один или несколько сеансов) и пробиотический протокол профессионального и домашнего администрирования.
Аннотация
Пародонтальные и периимплантные заболевания являются бляшечными инфекциями с высокой распространенностью, серьезно ухудшающими качество жизни людей. Диодный лазер уже давно рекомендован в качестве вспомогательной терапии при лечении пародонтита. Однако оптимальное сочетание режима использования (внутри или снаружи пародонтального кармана) и режима применения (однократный или многократный сеанс назначения) подробно не описано. Между тем, пробиотик Lactobacillus рассматривается как потенциальный адъювант в лечении периимплантного заболевания. Тем не менее, подробный протокол для эффективного применения пробиотиков отсутствует. Эта статья направлена на обобщение двух клинических протоколов. Для пародонтита определено оптимальное взаимодействие режима использования лазера и режима применения. В отношении периимплантного мукозита была установлена комбинированная терапия, содержащая профессиональное местное применение и домашнее введение пробиотика Lactobacillus . Этот обновленный лазерный протокол проясняет взаимосвязь между режимом лечения (внутри или снаружи пародонтального кармана) и количеством назначений лазера, дополнительно совершенствуя существующую диодную лазерную терапию. Для внутреннего карманного облучения предлагается один сеанс лазерного лечения, тогда как для наружного карманного облучения несколько сеансов лазерного лечения обеспечивают лучшие эффекты. Улучшенная пробиотическая терапия Lactobacillus привела к исчезновению отека периимплантной слизистой оболочки, уменьшению кровотечения при зондировании (BOP), а также к очевидному уменьшению и хорошему контролю зубного налета и пигментации; однако глубина зондирования кармана (PPD) имела ограниченное улучшение. Нынешний протокол следует рассматривать в качестве предварительного и его можно было бы еще больше усовершенствовать.
Введение
Пародонтоз является хронической многофакторной инфекцией, приводящей к прогрессирующему разрушению пародонта1. Его тяжелая форма, периодонтит, поражает до 50% населения во всем мире2 и рассматривается как основная причина потери зубов у взрослых3. Замена отсутствующих зубов зубными имплантатами была широко распространена по сравнению с традиционными вариантами4. Имплантаты демонстрируют выдающиеся функциональные и эстетические характеристики с долгосрочной выживаемостью 96,1% после 10 лет 5,6. Имплантаты, однако, могут страдать от периимплантного заболевания, приводящего к воспалению слизистой оболочки (периимплантный мукозит) или окружающей потере костной массы (периимплантит)7, что может привести к отказу имплантата8. Поэтому крайне необходимо эффективно управлять пародонтальными и периимплантными заболеваниями, чтобы сохранить естественные зубы или улучшить выживаемость зубных имплантатов.
Пародонтальные и периимплантные заболевания имеют схожую этиологию9, т.е. оба инициируются воздействием зубного налета, состоящего в основном из анаэробных и микроаэрофильных бактерий10. Механическая санация считается надежным способом достижения эффективного разрушения патогенных отложений на поверхностях корней или имплантатов11. Тем не менее, он имеет ограниченную доступность с использованием инструментов при наличии сложной анатомии зуба (т.е. фуркации корней и бороздок), что приводит к недостаточной дезактивации12. В этом контексте появилось применение лазеров и пробиотиков в дополнение к механической санации13,14.
Для лечения пародонта были предложены различные лазеры, такие как Nd:YAG; СО2; Эр:ЯГ; Er,Cr:YSGG; и диодный лазер15. Среди них диодный лазер является наиболее популярным выбором для клинического лечения из-за его портативности и низкой стоимости16. Диодный лазер был рекомендован в качестве идеального дополнения в разрушении биопленок, устранении воспаления и облегчении заживления ран благодаря его фотобиомодуляции и фототермическим эффектам12,13. Тем не менее, разнообразие использования лазеров приводит к значительной клинической гетерогенности среди текущих исследований. Таким образом, в нашей недавней публикации мы оценили 30 клинических испытаний и обобщили оптимальное сочетание режима использования лазера и режима применения12. Тем не менее, немногие исследования сообщают о подробной процедуре комбинированного протокола. С другой стороны, пробиотик Lactobacillus привлекает все большее внимание в качестве потенциального адъюванта в лечении периимплантного заболевания из-за его противомикробных и противовоспалительных характеристик17,18. Клинические преимущества, однако, не достигли приемлемого консенсуса. Один критический отчет относился к разнообразию протоколов введения пробиотиков17.
Основываясь на имеющихся данных, в данной статье описаны два модифицированных клинических протокола: существующий протокол использования адъюнктивного диодного лазера при лечении пародонтита усовершенствован на основе двух режимов использования лазера (внутри или снаружи кармана) и двух режимов применения (один или несколько сеансов назначения)12. Для дополнительной пробиотической терапии Lactobacillus при лечении периимплантного заболевания описана комбинация профессионального местного применения и домашнего введения пробиотика17.
протокол
Это исследование было одобрено Советом по институциональному обзору Колледжа стоматологии Сианского университета Цзяотун (xjkqll[2022]NO.034). Информированное согласие было получено от пациентов, участвовавших в этом исследовании.
1. Дополнительная диодная лазерная терапия в безоперационном лечении пародонтита
- Критерии
- Используйте следующие критерии включения: возраст ≥ 18 лет; глубина зондирующего кармана (PPD) ≥ 5 мм; обнаруживаемая клиническая потеря прикрепления (CAL) и рентгенографическая потеря костной массы (RBL).
- Используют следующие критерии исключения: пациенты с систематическими заболеваниями или под медикаментозным лечением, которые могут повлиять на воспаление и процесс заживления; пациенты, получившие лечение пародонта в течение 6 месяцев; курильщики или алкоголики; беременные или кормящие пациентки; пародонтально-эндодонтические комбинированные поражения; подвижность зубов III класса.
- Клиническое обследование
- Измерьте полный рот PPD, кровотечение при зондировании (BOP) в шести местах на зуб (т. Е. Мезиобуккальный, щечный, дистобуккальный, дистолингвальный, лингвальный и мезиолингвальный) и подвижность каждого зуба, исключая третьи моляры. Измерьте CAL для зубов с PPD ≥ 5 мм. Обнаружение соединения цементоэмали путем зондирования для расчета CAL.
- Запишите базовые параметры на пародонтальной диаграмме (Дополнительный файл 1).
- Дезинфекция и анестезия
- Полоскать горло 3% перекисью водорода в течение 1 мин, а затем чистой водой. Продезинфицируйте рабочую зону 1% йодофором. Ввести местную инъекцию адреналина примакайна для анестезии.
- Механическая санация путем масштабирования и корневого строгания (SRP)
ПРИМЕЧАНИЕ: SRP необходим для лечения пародонтита, включая ультразвуковую или ручную очистку. Зубной налет и зубной камень удаляют зубной камень с поверхности зуба выше и ниже линии десен. Строгание корней обычно следует за зубным шелушением и пытается сгладить шероховатую поверхность корня и помогает деснам повторно прикрепляться к зубам.- Во-первых, используйте ультразвуковое устройство для выполнения SRP для зубов с PPD > 3 мм. Во-вторых, используйте ручные инструменты (Gracey curettes 5/6, 7/8, 11/12 и 13/14) для выполнения SRP для зубов с PPD > 3 мм (рисунок 1). В-третьих, используйте ультразвуковое устройство для выполнения SRP для этих зубов во второй раз.
ПРИМЕЧАНИЕ: Диодный лазер сам по себе не эффективен в устранении исчисления, поэтому тщательный SRP не может быть опущен. Если у пациента большое количество пораженных зубов, на каждом приеме можно лечить только один квадрант. Ультразвуковой и ручной SRP может быть выполнен в течение 1-4 приемов. - Промыть пародонтальные карманы 3% перекисью водорода и полоскать горло чистой водой.
- Нанесите полировальную пасту на поверхность зубов, отполируйте поверхности зубов с помощью низкоскоростного наконечника с резиновым колпачком, а затем полоскайте горло чистой водой.
- Во-первых, используйте ультразвуковое устройство для выполнения SRP для зубов с PPD > 3 мм. Во-вторых, используйте ручные инструменты (Gracey curettes 5/6, 7/8, 11/12 и 13/14) для выполнения SRP для зубов с PPD > 3 мм (рисунок 1). В-третьих, используйте ультразвуковое устройство для выполнения SRP для этих зубов во второй раз.
- Дополнительная диодная лазерная терапия
ПРИМЕЧАНИЕ: Выбирайте зубы с PPD ≥ 5 мм для лазерного лечения. Выберите один из следующих двух режимов использования (например, шаги 1.5.1 или 1.5.2).- Внутреннее карманное лазерное облучение (рекомендуется только один сеанс лазерного назначения на зуб) (Рисунок 2А).
- Убедитесь, что и оператор, и пациент носят защитные очки для защиты глаз от повреждения лазером.
- Подготовьте диодное лазерное устройство (длина волны = 980 нм, выходная мощность = 1 Вт, плотность мощности = 1414,7 Вт/см2, непрерывная волна, волоконно-оптическая система доставки 300 мкм).
ПРИМЕЧАНИЕ: Неправильное увеличение мощности может привести к тепловому повреждению; пожалуйста, проконсультируйтесь с производителем лазера и следуйте инструкциям производителя перед использованием. - Откалибруйте длину волокнистого наконечника, подвергшегося воздействию, на 1 мм меньше измеренного PPD (рисунок 2B).
ПРИМЕЧАНИЕ: Чтобы предотвратить кровотечение из-за введения кончика волокна слишком глубоко в пародонтальный карман, обычно рекомендуется, чтобы длина открытого наконечника волокна была на 1 мм меньше, чем измеренная глубина пародонтального кармана. - Осторожно вставьте наконечник волокна в пародонтальный карман на 1 мм меньше, чем измеренный PPD, и медленно проведите наконечником как в мезиально-дистальном, так и в апикально-корональном направлениях в течение 30 с на зуб (рисунок 2B, C).
ПРИМЕЧАНИЕ: Во время этого процесса введение волокна слишком глубоко в пародонтальный карман может раздражать пародонтальное кровотечение и, таким образом, препятствовать действию лазера. Удалите грануляцию, прикрепленную к наконечнику волокна, используя ватный тампон, содержащий 75% спирта, чтобы не поставить под угрозу эффективность лазера.
- Наружное карманное лазерное облучение (в общей сложности предлагается 3-5 сеансов лазерных назначений на зуб) (Рисунок 3А).
- Убедитесь, что и оператор, и пациент носят защитные очки для защиты глаз от повреждения лазером.
- Подготовьте диодное лазерное устройство (длина волны = 980 нм, выходная мощность = 0,4 Вт, плотность мощности = 566,2 Вт/см2, непрерывная волна, волоконно-оптическая система доставки 300 мкм).
- Облучают десновую поверхность кармана в течение приблизительно 15 с на карман, с помощью наконечника лазерного волокна на расстоянии 5 мм (2-10 мм) от поверхности десен и направленного под углом 90° (рисунок 3B,C).
- Повторите ту же наружную карманную лазерную обработку через 1, 3, 5 и 7 дней.
- Внутреннее карманное лазерное облучение (рекомендуется только один сеанс лазерного назначения на зуб) (Рисунок 2А).
- Дайте инструкцию по гигиене полости рта (OHI) каждому пациенту, включая технику чистки басса, межзубную нить и щетку19.
- Клиническое обследование
- Измерьте PPD, CAL и BOP для каждого зуба через 4-6 недель, 3 месяца и 6 месяцев после лечения пародонта. Запишите послеоперационные параметры на новую пародонтальную карту (Дополнительный файл 1).
- Сравните базовые и послеоперационные параметры.
2. Дополнительная пробиотическая терапия в нехирургическом лечении периимплантного мукозита (рисунок 4А)
- Критерии
- Используйте следующие критерии включения: возраст ≥ 18 лет; по меньшей мере один имплантат с эритемой, отеком, нагноением или BOP в периимплантационной слизистой оболочке; рентгенологическая потеря костной массы (RBL) < 2 мм.
- Используют следующие критерии исключения: периимплантит (РБЛ ≥ 2 мм); имплантаты с подвижностью; пациентам с систематическими заболеваниями или под медикаментозным лечением, которые могут повлиять на процесс воспаления и заживления; пациенты, получившие лечение пародонта в течение 6 месяцев; курильщики или алкоголики; беременные или кормящие пациентки.
- Клиническое обследование
- Измерьте клинические параметры PPD, BOP на шести участках на имплантат (т.е. мезиобуккальный, буккальный, дистобуккальный, дистолингвальный, лингвальный и мезиолингвальный) и индекс бляшек (PI) на четырех участках на имплантат (т.е. мезиальный, буккальный, дистальный и лингвальный).
- Запишите базовые параметры на пародонтальной диаграмме (Дополнительный файл 1).
- Для дезинфекции полоскать горло 3% перекисью водорода в течение 1 мин, а затем чистой водой.
- Механическая санация с помощью наддесневого масштабирования
- Используйте титановый ультразвуковой наконечник для выполнения наддесневого масштабирования имплантатов мукозита, регулируя режим до средней мощности (рисунок 4B). Промыть карманы 3% перекисью водорода, а затем полоскать горло чистой водой.
ПРИМЕЧАНИЕ: Наддесневое масштабирование удаляет налет и зубной камень с поверхности протеза имплантата над линией десен.
- Используйте титановый ультразвуковой наконечник для выполнения наддесневого масштабирования имплантатов мукозита, регулируя режим до средней мощности (рисунок 4B). Промыть карманы 3% перекисью водорода, а затем полоскать горло чистой водой.
- Профессиональное введение пробиотика
- Измельчите пробиотическую таблетку в порошок с использованием стерилизованного раствора (рисунок 4С).
ПРИМЕЧАНИЕ: Если в порошке есть кусковые частицы, они могут легко засорить шприц. - Сделайте раствор пробиотического порошка и стерильного физиологического раствора в соотношении 1:3 (рисунок 4D). Доставьте пробиотический раствор в периимплантируемую борозду с помощью шприца объемом 5 мл с притупленным и мягким наконечником (рисунок 4E).
- Измельчите пробиотическую таблетку в порошок с использованием стерилизованного раствора (рисунок 4С).
- Домашний прием пробиотиков
- Проинструктируйте пациентов растворять одну таблетку в течение примерно 10 мин в ротовой полости каждые 12 ч, два раза в день в течение 1 месяца (рисунок 4А).
- Дайте OHI каждому пациенту, включая технику чистки Басса, межзубную нить и щетку19.
- Клиническое обследование
- Измерьте PPD, PI и BOP для каждого имплантата через 4-6 недель, 3 месяца и 6 месяцев после лечения. Запишите послеоперационные параметры на новую пародонтальную карту (Дополнительный файл 1).
- Сравните базовые и послеоперационные параметры.
Результаты
Пародонтальные карманы с PPD ≥ 5 мм требуют лазерного облучения после SRP, так как трудно получить полную санацию только SRP (рисунок 1A, B). После SRP, если пародонтальные карманы обильно кровоточат и сгущаются на поверхности зуба, оператору необходимо остановить кровотечение и удалить сгусток путем полоскания и полоскания горла несколько раз. Это связано с тем, что большое количество крови будет препятствовать работе лазера (рисунок 1C, D).
Открытый волоконный наконечник откалиброван на 1 мм меньше, чем измеренный PPD. Параметры лазера были установлены на уровне 1 Вт с использованием непрерывной волны (рисунок 2B). Для рекомендуемых параметров лазера следует обратиться к рекомендациям производителя и соответствующим образом скорректировать параметры для различных клинических сценариев. Наконечник волокна находился на расстоянии 5 мм от поверхности десен и был направлен под углом 90° (рисунок 3B).
Полностью измельченный пробиотический порошок не содержит кусковых частиц (рисунок 4C). Растворение его в физиологическом растворе (1:3) приводит к получению зеленого раствора (рисунок 4D).
По сравнению с предоперационным (рисунок 5A,C), диодная лазерная SRP-терапия (внутри или снаружи) эффективно удаляла патогенную биопленку бляшек и устраняла воспаление у пациентов с пародонтитом, достигая значительных улучшений (т.е. в отношении эритемы, отека, PPD, BOP) (Рисунок 5B, D). По сравнению с предоперационным периодом (рисунок 5Е) пробиотическая терапия приводила к исчезновению отека периимплантной слизистой оболочки, снижению БОП, а также к очевидному уменьшению и хорошему контролю зубного налета и пигментации; однако существенных изменений в ПРД не произошло (диаграмма 5F).
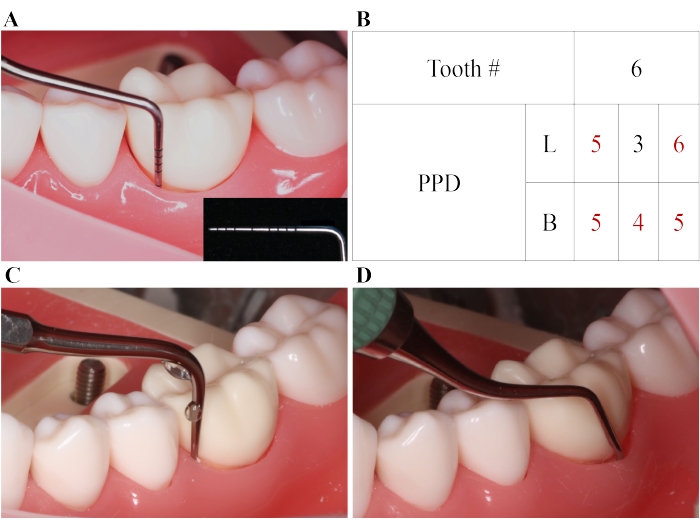
Рисунок 1: SRP для пародонтита. (A) Пародонтальный карман с PPD = 5 мм. (B) PPD номера тестируемого зуба (мм). SRP выполняется для кармана с PPD ≥ 4 мм, а дополнительная диодная лазерная обработка проводится для кармана с PPD ≥ 5 мм. (C) SRP с ультразвуковыми инструментами. D) ПСП с ручными инструментами. B: буккальный; L: лингвальный; SRP: масштабирование и корневое строгание. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 2: Дополнительная лазерная терапия внутри пародонтального кармана. (А) Фазы лазерного лечения с внутренним режимом. (B) Калибровка открытого наконечника волокна (4 мм) для измерения на 1 мм меньше PPD (5 мм). Волоконный наконечник диаметром 300 мкм вставляется в пародонтальный карман (на 1 мм короче измеренного PPD). (C) Наконечник волокна проносится в кармане в мезиально-дистальном и апикально-корональном направлениях (зеленая кривая указывает путь кончика волокна). Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
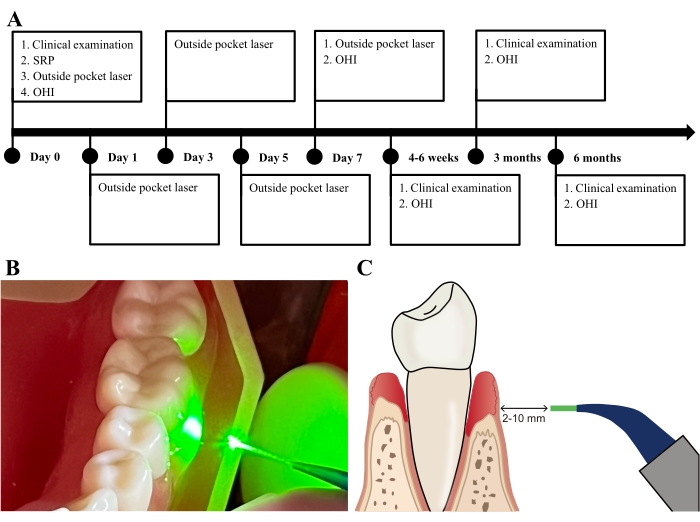
Рисунок 3: Дополнительная лазерная терапия вне пародонтального кармана. (А) Фазы лазерного лечения с наружным режимом. (B) Наконечник волокна облучает карман на расстоянии 5 мм от поверхности десен. (C) Расстояние между наконечником волокна и поверхностью десен колеблется в пределах 2-10 мм, а наконечник направлен под углом 90°. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
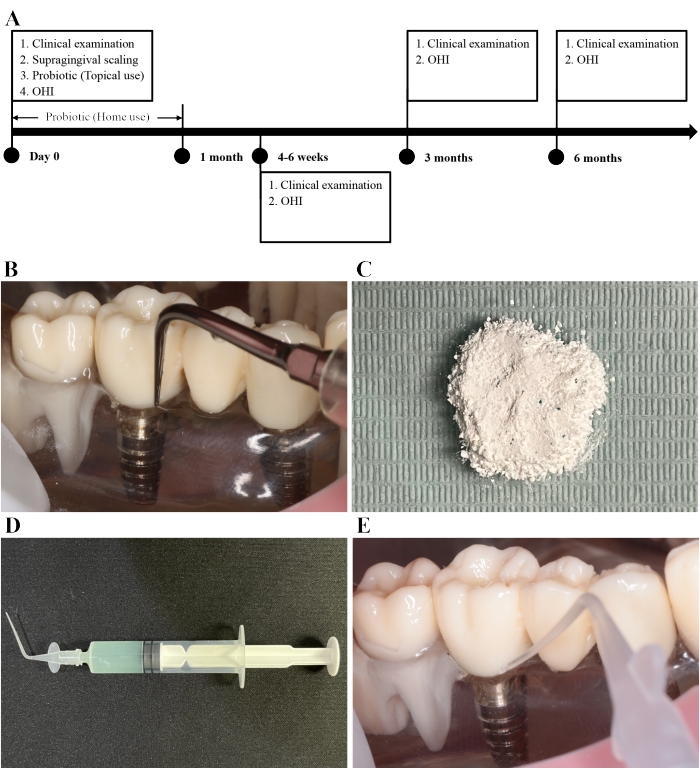
Рисунок 4: Супрагингивальное масштабирование и дополнительная пробиотическая лактобациллная терапия. (A) Фазы терапии пробиотическими лактобациллами . (B) Титановый ультразвуковой наконечник используется для выполнения наддесневого накипания имплантатов мукозита. (C) Пробиотический порошок. (D) Пробиотический раствор зеленого цвета. (E) Пробиотический раствор подается в периимплантированную борозду с притупленным и мягким кончиком. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 5: Клиническое обследование до и через 1 месяц после лечения. (А) Через месяц после лазерного лечения в режиме внутреннего применения исчезла десневая эритема и отек, а PPD и BOP были значительно снижены по сравнению с (B) предоперационным состоянием. (C) Через месяц после лазерного лечения в режиме наружного использования эритема десен и отек улучшились, а PPD и BOP снизились по сравнению с (D) предоперационным состоянием. (E) После 1 месяца пробиотической терапии периимплантационный отек слизистой оболочки исчез, пигментация и бляшки были уменьшены и хорошо контролировались, а BOP был снижен по сравнению с (F) предоперационным состоянием; однако существенных изменений в PPD по сравнению с предоперационным состоянием (F) не произошло. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Дополнительный файл 1: Пародонтальная диаграмма. B: буккальный; БОП: кровотечение при зондировании; CAL: клиническая потеря привязанности; L: лингвальный; PI: индекс бляшек; PPD: зондирование глубины кармана. Пожалуйста, нажмите здесь, чтобы загрузить этот файл.
Дополнительный файл 2: Характеристика исследований, относящихся к дополнительной лазерной терапии. Пожалуйста, нажмите здесь, чтобы загрузить этот файл.
Дополнительный файл 3: Характеристика исследований, относящихся к дополнительной пробиотической терапии lactobacillus . Пожалуйста, нажмите здесь, чтобы загрузить этот файл.
Обсуждение
Хотя диодный лазер широко используется в пародонтальной терапии, клиническая эффективность остается спорной среди текущих клинических испытаний15,20. Как показано, режим использования лазера и режим применения оказывают существенное влияние на эффективность пародонтальной лазерной терапии12. Большинство исследователей, однако, игнорируют потенциальную роль, вызывая результаты, которые трудно объяснить. При различных режимах использования чрезмерное или недостаточное действие лазера может привести к отрицательному результату21. Только при оптимальном сочетании режима использования и режима применения лазер может максимизировать свои терапевтические преимущества12. По-видимому, существует острая необходимость в улучшении существующего протокола диодной лазерной терапии. Поэтому в этой статье описаны два режима использования пародонтального лазера (внутренний карман или внешний карман) с учетом фотобиомодуляции и фототермических эффектов. Кроме того, на основе опубликованных рандомизированных контролируемых испытаний было предложено предлагаемое число сеансов назначения лазеров в рамках двух режимов использования; для внутреннего карманного использования рекомендуется один сеанс применения лазера, тогда как для наружного карманного использования несколько (3-5) сеансов применения лазера обеспечивают лучший клинический эффект.
Важно отметить, что параметры лазера также влияют на эффективность лазера. Общие параметры пародонтального лазера относятся к длине волны, плотности энергии и выходной мощности22. В большинстве исследований использовались диодные лазеры с длиной волны 808-980 нм и сообщалось о хороших клинических результатах23. Было подтверждено, что диодный лазер в диапазоне 600-100 нм проникает глубоко в ткани, воздействуя на эпителиальные и соединительные ткани десны20. Плотность энергии варьировалась от 1,6-24,84 Дж/см2 (внутренний режим) и 3-10 Дж/см2 (внешний режим). Сообщалось, что лазеры плотностью 1,5-16 Дж/см2 обладали хорошими противовоспалительными свойствами24. Сообщалось, что выходная мощность колеблется в пределах 0,5-2,5 Вт для внутреннего применения, в то время как для наружного применения она была намного ниже (0,01-0,5 Вт). Учитывая, что рекомендуемые параметры частично различаются у разных производителей лазеров, неправильное увеличение мощности лазера может привести к тепловому повреждению тканей пародонта во время подметания внутреннего кармана25,26. Настоятельно рекомендуется проконсультироваться с производителем лазера и определить соответствующие параметры перед использованием. В этом протоколе для внутреннего режима был выбран безопасный уровень мощности 1 Вт.
Учитывая, что введение пробиотиков Lactobacillus дает надежные результаты в лечении гингивита и пародонтита, ожидается, что он будет оказывать аналогичные терапевтические преимущества при периимплантируемых заболеваниях. Тем не менее, ограниченное количество исследований затрудняет оценку эффективности пробиотика Lactobacillus17,27, особенно для запущенной формы заболевания, периимплантита 17,28,29. Таким образом, протокол введения пробиотиков предлагался только пациентам с периимплантным мукозитом. Учитывая очевидное клиническое разнообразие в опубликованных исследованиях, крайне важно установить рациональный протокол с воспроизводимым эффектом. В результате мы систематически рассматривали связанные исследования и предлагали усовершенствованный протокол, включая комбинацию профессионального местного использования и домашнего введения пробиотика Lactobacillus и усиления OHI.
По опыту авторов, при выборе внутреннего карманного режима лазерной терапии крайне важно добиться мягкого введения и непрерывного движения кончика волокна. Тяжелое или глубокое введение волокна вызовет пародонтальное кровотечение, что может ослабить лазерный эффект. Следовательно, предполагается, что глубина вставки должна быть на 1 мм короче, чем измеренный PPD. Длительное действие определенного участка в кармане может вызвать чрезмерные фототермические эффекты (более 10 ° C), что приводит к боли в пародонте и даже постоянному повреждению пародонтальной связки и кости30. Во время этого сеанса оператор должен регулярно проверять наконечник волокна. Как только сгусток крови прикреплен к наконечнику, его необходимо вытереть ватным тампоном, смоченным 75% спиртом, чтобы избежать препятствования действию лазера. Что касается профессионального применения пробиотической терапии, то концентрация пробиотического раствора не должна быть слишком высокой; в противном случае он легко заблокирует инъекционную иглу.
В качестве модифицированного протокола для существующих исследований пробиотическая терапия в этой статье направлена на снижение клинической гетерогенности и способствует реализации будущих клинических исследований в этой области. Текущий результат показал, что пробиотическая терапия лактобактериями привела к исчезновению периимплантного отека слизистой оболочки, снижению БОП, а также к очевидному снижению и отличному контролю зубного налета и пигментации после 1-месячного наблюдения. Это продемонстрировало эффективность пробиотиков в борьбе с периимплантированным воспалением слизистой оболочки. Однако улучшение PPD было ограниченным. Поскольку периимплантный мукозит не вызывает потери костной массы, он проявляется только в виде эритемы слизистой оболочки, отека или кровотечения, и обычно нет глубокого периимплантного кармана31. У пациента в этом случае до начала лечения наблюдался лишь легкий отек слизистой оболочки, и поэтому предоперационные и послеоперационные изменения ПРД не были значительными. Кроме того, этот протокол следует рассматривать как предварительный и может быть дополнительно улучшен (например, путем использования полоскания горла хлоргексидина, увеличения частоты местного использования пробиотиков, улучшения активных ингредиентов пробиотических таблеток и т. Д.). 32,33.
Некоторые ограничения все еще существуют в протоколе пробиотической терапии. В повседневной клинической практике на гигиеническое поведение пациентов влияют различные факторы. Некоторые испытывают трудности с выполнением адекватного управления гигиеной полости рта, несмотря на профессиональное обучение. Недостаточная домашняя чистка полости рта подрывает преимущества профессионального лечения пародонта и даже ухудшает состояние, особенно для пробиотической терапии. Таким образом, рекомендуется усиливать OHI при каждом последующем посещении и просить пациентов снова практиковать процедуру. Кроме того, пробиотическая терапия в данной статье не вводится пациентам с периимплантитом, в связи с его более сложной патологией и противоречивыми результатами клинических испытаний17. Необходимы дальнейшие исследования для изучения протокола пробиотической терапии периимплантита.
Чтобы облегчить доступ к существующим исследованиям, связанным с диодным лазерным лечением пародонтита и пробиотической терапией периимплантных заболеваний, резюме этих исследований 14,28,32,33,34,35,36,37,38,39,40,41,42, 43,44,45,46,47,
48,49,50,51,52,53,54 представлено в Дополнительном файле 2 и Дополнительном файле 3, соответственно.
Раскрытие информации
У авторов нет конфликта интересов.
Благодарности
Эта работа была поддержана Национальным фондом естественных наук Китая (номера грантов 82071078, 81870798 и 82170927).
Материалы
| Name | Company | Catalog Number | Comments |
| 1% iodophor | ADF, China | 21031051 | 100 mL |
| 3% hydrogen peroxide | Hebei Jianning, China | 210910 | 500 mL |
| 75% alcohol | Shandong Anjie, China | 2021100227 | 500 mL |
| Diode laser (FOX 980) | A.R.C, Germany | PS01013 | 300-μm fiber tip |
| Gracey curettes | Hu-Friedy, USA | 5/6, 7/8, 11/12, 13/14 | |
| Low-speed handpiece | NSK, Japan | 0BB81855 | |
| Periodontal probe | Shanghai Kangqiao Dental Instruments Factory, China | 44759.00 | |
| Periodontal ultrasonic device (PT3) | Guilin zhuomuniao Medical Instrument, China | P2090028PT3 | |
| Polishing paste | Datsing, China | 21010701 | |
| Primacaine adrenaline | Produits Dentaires Pierre Rolland, France | S-52 | 1.7 mL |
| Probiotic | Biogaia, Sweden | Prodentis | 30 probiotic tablets (24 g) |
| Titanium ultrasound tip (P59) | Guilin Zhuomuniao Medical Instrument, China | 200805 |
Ссылки
- Papapanou, P. N., et al. Periodontitis: consensus report of workgroup 2 of the 2017 world workshop on the classification of periodontal and peri-implant diseases and conditions. Journal of Clinical Periodontology. 45, 162-170 (2018).
- Peres, M. A., et al. Oral diseases: a global public health challenge. Lancet. 394 (10194), 249-260 (2019).
- Nazir, M. A. Prevalence of periodontal disease, its association with systemic diseases and prevention. International Journal of Health Sciences (Qassim). 11 (2), 72-80 (2017).
- Khoury-Ribas, L., Ayuso-Montero, R., Willaert, E., Peraire, M., Martinez-Gomis, J. Do implant-supported fixed partial prostheses improve masticatory performance in patients with unilateral posterior missing teeth. Clinical Oral Implants Research. 30 (5), 420-428 (2019).
- Bohner, L., Hanisch, M., Kleinheinz, J., Jung, S. Dental implants in growing patients: a systematic review. The British Journal of Oral & Maxillofacial Surgery. 57 (5), 397-406 (2019).
- Jemt, T. Implant survival in the edentulous jaw: 30 years of experience. Part ii: a retro-prospective multivariate regression analysis related to treated arch and implant surface roughness. The International Journal of Prosthodontics. 31 (6), 531-539 (2018).
- Muñoz, V., Duque, A., Giraldo, A., Manrique, R. Prevalence of peri-implant disease according to periodontal probing depth and bleeding on probing: a systematic review and meta-analysis. The International Journal of Oral & Maxillofacial Implants. 33 (4), 89-105 (2018).
- Larsson, L., et al. Regenerative medicine for periodontal and peri-implant diseases. Journal of Dental Research. 95 (3), 255-266 (2016).
- Salvi, G. E., Cosgarea, R., Sculean, A. Prevalence and mechanisms of peri-implant diseases. Journal of Dental Research. 96 (1), 31-37 (2017).
- Asa'ad, F., Garaicoa-Pazmiño, C., Dahlin, C., Larsson, L. Expression of micrornas in periodontal and peri-implant diseases: a systematic review and meta-analysis. International Journal of Molecular Sciences. 21 (11), 4147 (2020).
- Sculean, A., et al. Effectiveness of photodynamic therapy in the treatment of periodontal and peri-implant diseases. Monographs in Oral Science. 29, 133-143 (2021).
- Yu, S., et al. Clinical effectiveness of adjunctive diode laser on scaling and root planing in the treatment of periodontitis: is there an optimal combination of usage mode and application regimen? A systematic review and meta-analysis. Lasers in Medical Science. 37 (2), 759-769 (2022).
- Cobb, C. M., Low, S. B., Coluzzi, D. J. Lasers and the treatment of chronic periodontitis. Dental Clinics of North America. 54 (1), 35-53 (2010).
- Mongardini, C., Pilloni, A., Farina, R., Di Tanna, G., Zeza, B. Adjunctive efficacy of probiotics in the treatment of experimental peri-implant mucositis with mechanical and photodynamic therapy: a randomized, cross-over clinical trial. Journal of Clinical Periodontology. 44 (4), 410-417 (2017).
- Cobb, C. M. Lasers and the treatment of periodontitis: the essence and the noise. Periodontology 2000. 75 (1), 205-295 (2017).
- Slot, D. E., Jorritsma, K. H., Cobb, C. M., Vander Weijden, F. A. The effect of the thermal diode laser (wavelength 808-980 nm) in non-surgical periodontal therapy: a systematic review and meta-analysis. Journal of Clinical Periodontology. 41 (7), 681-692 (2014).
- Gao, J., et al. Does probiotic lactobacillus have an adjunctive effect in the nonsurgical treatment of peri-implant diseases? A systematic review and meta-analysis. Journal of Evidence Based Dental Practice. 20 (1), 101398 (2020).
- Staab, B., Eick, S., Knöfler, G., Jentsch, H. The influence of a probiotic milk drink on the development of gingivitis: a pilot study. Journal of Clinical Periodontology. 36 (10), 850-856 (2009).
- . Oral hygiene instruction online Available from: https://www.oralhygiene-instruction.com/en/ (2022)
- Zhao, P., et al. Effect of adjunctive diode laser in the non-surgical periodontal treatment in patients with diabetes mellitus: a systematic review and meta-analysis. Lasers in Medical Science. 36 (5), 939-950 (2021).
- Huang, Y. Y., Sharma, S. K., Carroll, J., Hamblin, M. R. Biphasic dose response in low level light therapy-an update. Dose-Response. 9 (4), 602-618 (2011).
- Passanezi, E., Damante, C. A., de Rezende, M. L., Greghi, S. L. Lasers in periodontal therapy. Periodontology 2000. 67 (1), 268-291 (2015).
- Qadri, T., Javed, F., Johannsen, G., Gustafsson, A. Role of diode lasers (800-980 nm) as adjuncts to scaling and root planing in the treatment of chronic periodontitis: a systematic review. Photomedicine and Laser Surgery. 33 (11), 568-575 (2015).
- Ren, C., McGrath, C., Jin, L., Zhang, C., Yang, Y. Effect of diode low-level lasers on fibroblasts derived from human periodontal tissue: a systematic review of in vitro studies. Lasers in Medical Science. 31 (7), 1493-1510 (2016).
- Angiero, F., Parma, L., Crippa, R., Benedicenti, S. Diode laser (808 nm) applied to oral soft tissue lesions: a retrospective study to assess histopathological diagnosis and evaluate physical damage. Lasers in Medical Science. 27 (2), 383-388 (2012).
- Gutiérrez-Corrales, A., et al. Comparison of diode laser - Oral tissue interaction to different wavelengths. In vitro study of porcine periodontal pockets and oral mucosa. Medicina Oral, Patología Oral y Cirugía Bucal. 25 (2), 224-232 (2020).
- Zhao, R., Hu, H., Wang, Y., Lai, W., Jian, F. Efficacy of probiotics as adjunctive therapy to nonsurgical treatment of peri-implant mucositis: a systematic review and meta-analysis. Frontiers in Pharmacology. 11, 541752 (2020).
- Galofré, M., Palao, D., Vicario, M., Nart, J., Violant, D. Clinical and microbiological evaluation of the effect of Lactobacillus reuteri in the treatment of mucositis and peri-implantitis: A triple-blind randomized clinical trial. Journal of Periodontal Research. 53 (3), 378-390 (2018).
- Tada, H., et al. The effects of Lactobacillus reuteri probiotics combined with azithromycin on peri-implantitis: A randomized placebo-controlled study. Journal of Prosthodontic Research. 62 (1), 89-96 (2018).
- Kwon, S. J., et al. Thermal irritation of teeth during dental treatment procedures. Restorative Dentistry and Endodontics. 38 (3), 105-112 (2013).
- Berglundh, T., et al. Peri-implant diseases and conditions: consensus report of workgroup 4 of the 2017 world workshop on the classification of periodontal and peri-implant diseases and conditions. Journal of Clinical Periodontology. 45, 286-291 (2018).
- Hallström, H., Lindgren, S., Widén, C., Renvert, S., Twetman, S. Probiotic supplements and debridement of peri-implant mucositis: a randomized controlled trial. Acta Odontologica Scandinavica. 74 (1), 60-66 (2016).
- Peña, M., et al. Evaluation of the effect of probiotics in the treatment of peri-implant mucositis: a triple-blind randomized clinical trial. Clinical Oral Investigations. 23 (4), 1673-1683 (2019).
- Alzoman, H. A., Diab, H. M. Effect of gallium aluminium arsenide diode laser therapy on Porphyromonas gingivalis in chronic periodontitis: a randomized controlled trial. International Journal of Dental Hygiene. 14 (4), 261-266 (2016).
- Angiero, F., et al. Evaluation of bradykinin, VEGF, and EGF biomarkers in gingival crevicular fluid and comparison of photobiomodulation with conventional techniques in periodontitis: a split-mouth randomized clinical trial. Lasers in Medical Science. 35 (4), 965-970 (2019).
- Balasubramaniam, A. S., Thomas, L. J., Ramakrishnanan, T., Ambalavanan, N. Short-term effects of nonsurgical periodontal treatment with and without use of diode laser (980 nm) on serum levels of reactive oxygen metabolites and clinical periodontal parameters in patients with chronic periodontitis: a randomized controlled trial. Quintessence International. 45 (3), 193-201 (2014).
- De Micheli, G., et al. Efficacy of high intensity diode laser as an adjunct to non-surgical periodontal treatment: a randomized controlled trial. Lasers in Medical Science. 26 (1), 43-48 (2011).
- Dukić, W., Bago, I., Aurer, A., Roguljić, M. Clinical effectiveness of diode laser therapy as an adjunct to non-surgical periodontal treatment: A randomized clinical study. Journal of Periodontology. 84 (8), 1111-1117 (2013).
- Euzebio Alves, V. T., et al. Clinical and microbiological evaluation of high intensity diode laser adjutant to non-surgical periodontal treatment: A 6-month clinical trial. Clinical Oral Investigations. 17 (1), 87-95 (2013).
- Gündoğar, H., Şenyurt, S. Z., Erciyas, K., Yalım, M., Üstün, K. The effect of low-level laser therapy on non-surgical periodontal treatment: a randomized controlled, single-blind, split-mouth clinical trial. Lasers in Medical Science. 31 (9), 1767-1773 (2016).
- Jose, K. A., et al. Management of chronic periodontitis using chlorhexidine chip and diode laser-a clinical study. Journal of Clinical and Diagnostic Research. 10 (4), (2016).
- Lin, J., Bi, L., Song, Y., Ma, W., Wang, N. Gingival curettage with diode laser: clinical study. Zhong Guo Ji Guang Yi Xue Za Zhi/Chinese Journal of Laser Medicine & Surgery (in Chinese. 18 (06), 353-357 (2009).
- Makhlouf, M., Dahaba, M. M., Tuner, J., Eissa, S. A., Harhash, T. A. Effect of adjunctive low level laser therapy (LLLT) on nonsurgical treatment of chronic periodontitis. Photomedicine and Laser Surgery. 30 (3), 160-166 (2012).
- Manjunath, S., Singla, D., Singh, R. Clinical and microbiological evaluation of the synergistic effects of diode laser with nonsurgical periodontal therapy: A randomized clinical trial. Journal of Indian Society of Periodontology. 24 (2), 145-149 (2020).
- Matarese, G., Ramaglia, L., Cicciù, M., Cordasco, G., Isola, G. The effects of diode laser therapy as an adjunct to scaling and root planing in the treatment of aggressive periodontitis: a 1-year randomized controlled clinical trial. Photomedicine and Laser Surgery. 35 (12), 702-709 (2017).
- Pamuk, F., et al. The effect of low-level laser therapy as an adjunct to non-surgical periodontal treatment on gingival crevicular fluid levels of transforming growth factor-beta 1, tissue plasminogen activator and plasminogen activator inhibitor 1 in smoking and non-smoking chronic periodontitis patients: a split-mouth, randomized control study. Journal of Periodontal Research. 52 (5), 872-882 (2017).
- Pejcic, A., Mirkovic, D. Anti-inflammatory effect of low level laser treatment on chronic periodontitis. Medical Laser Application. 26 (1), 27-34 (2011).
- Saglam, M., Kantarci, A., Dundar, N., Hakki, S. S. Clinical and biochemical effects of diode laser as an adjunct to nonsurgical treatment of chronic periodontitis: a randomized, controlled clinical trial. Lasers in Medical Science. 29 (1), 37-46 (2014).
- Shi, Z., Jiang, C., Xu, Y., Sun, Y. Effects of diode laser on the treatment for moderate to severe chronic periodontitis. Kou Qiang Yi Xue/Stomatology. 34 (4), 245-248 (2014).
- Üstün, K., et al. Clinical and biochemical effects of 810 nm diode laser as an adjunct to periodontal therapy: a randomized split-mouth clinical trial). Photomedicine and Laser Surgery. 32 (2), 61-66 (2014).
- Zhang, L., Shi, J., Guo, J., Zhang, N. Clinical evaluation of diode laser assisted treatment of chronic periodontitis. Shi Yong Kou Qiang Yi Xue Za Zhi/Journal of Practical Stomatology. 34 (3), 404-406 (2018).
- Alqahtani, F., et al. Efficacy of mechanical debridement with adjunctive probiotic therapy in the treatment of peri-implant mucositis in cigarette-smokers and never-smokers. Clinical Implant Dentistry and Related Research. 21 (4), 734-740 (2019).
- Flichy-Fernández, A. J., et al. The effect of orally administered probiotic Lactobacillus reuteri-containing tablets in peri-implant mucositis: a double-blind randomized controlled trial. Journal of Periodontal Research. 50 (6), 775-785 (2015).
- Calderín, S., García-Núñez, J. A., Gómez, C. Short-term clinical and osteoimmunological effects of scaling and root planing complemented by simple or repeated laser phototherapy in chronic periodontitis. Lasers in Medical Science. 28 (1), 157-166 (2013).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены