Method Article
Цельноклеточной патч-зажим Записи в головном мозге Ломтики
В этой статье
Резюме
Этот протокол описывает основные процедурные шаги для выполнения целой клетки записи патч-зажим. Эта методика позволяет исследовать электрического поведения нейронов, и когда выполняется в срезах мозга, позволяет оценить различные нейронные функции от нейронов, которые до сих пор интегрированы в относительно хорошо сохранившихся контуров мозга.
Аннотация
Цельноклеточная записи патч-зажим является электрофизиологические метод, который позволяет исследовать электрические свойства существенной части нейрона. В этой конфигурации микропипетки находится в плотном контакте с клеточной мембраной, которая предотвращает утечку тока и тем самым обеспечивает более точные измерения ионного тока, чем ранее использовавшейся внутриклеточного острого способа записи электрода. Классически, запись поклеточного может быть выполнена на нейронах в различных типах препаратов, в том числе моделей клеточных культур, диссоциированных нейронов, нейронов в срезах мозга, и в интактных анестезированных или бодрствующих животных. Таким образом, эта методика очень способствовало пониманию пассивных и активных биофизических свойств возбудимых клеток. Главным преимуществом этого метода является то, что она предоставляет информацию о том , как конкретные манипуляции (например, фармакологические, экспериментатор-индуцированные пластичностью) могут изменять специфические нейронные функции или Сhannels в режиме реального времени. Кроме того, значительное открытие плазматической мембраны позволяет внутреннее решение пипеткой свободно диффундировать в цитоплазме, обеспечивая средство для введения лекарственных средств, например, агонисты или антагонисты специфических внутриклеточных белков, и манипулировании этих целей , не изменяя их функции в соседних сотах. В данной статье основное внимание будет уделено записи целых клеток проводили на нейроны в срезах мозга, препарат , который имеет преимущество записи нейронов в относительно хорошо сохранившихся контуров мозга, т.е. в физиологически соответствующем контексте. В частности, когда в сочетании с соответствующим фармакологию, этот метод является мощным инструментом, позволяющим идентифицировать конкретных neuroadaptations, которые имели место после любого типа опыта, таких как обучение, воздействие наркотиков злоупотребления и стресса. Таким образом, цельноклеточная патч-зажим записи в срезах мозга обеспечивают средства для измерения в бывших естественных условиях подготовки длительных измененийв нейрональных функций, которые развивались в неповрежденных бодрствующих животных.
Введение
Метод патч-зажим, электрофизиологическое технология , которая была разработана в конце 1970 - х 1,2, является основным инструментом для изучения одного или нескольких функций ионных каналов в живой ткани. Среди различных конфигураций накладными, которые могут быть достигнуты, поклеточного патч-зажим записи позволяют исследование электрического поведения значительной части нейроне. Классически, эта техника выполняется в пробирке или на срезах мозга, свеже диссоциированных нейронов, или на моделях клеточных культур 3. При использовании на нейроны в срезах мозга, эта методика представляет несколько преимуществ. В частности: (I) нейроны записываются в относительно сохраненными участки мозга , которые в некоторой степени, и по сравнению с препаратами для культивирования клеток, обеспечивают среду , которая является физиологически отношение 3. Это позволяет захватывать рано, или даже мониторинг в режиме реального времени, клеточные и молекулярные события, которые вызываются любым типом острого pharmacologческие манипуляции - временное разрешение , которое не может быть достигнуто с помощью классического в условиях естественных условиях; (б) возможность визуально определить области мозга в срезах мозга обеспечивает высокую региональную специфику 3 как для региона мозга изучены и для конкретных нейронов , когда они выражают флуоресцентные маркеры; ( в ) получать доступ к внутриклеточное пространство клетки, открывая значительную часть плазматической мембраны (в отличие от прокалывания мембраны с резким микропипетки для внутриклеточных записей) 4. В свою очередь, это позволяет содержание или концентрацию определенных ионов, образующих внутреннее решение, чтобы быть модифицирован таким образом молекулярные мишени или клеточные механизмы могут быть изучены при различных условиях. Например, при создании конфигурации целой клетки, любой специфический фармакологический агент (например, антагонисты) , которые можно добавить к микропипетки записи (патч пипетки) решение будет непосредственно диффундируют в цитоплазму и действовать на его putatив внутриклеточные мишени без изменения целевой функции в соседних ячейках. Кроме того, по сравнению с резким записи микропипетки, большое отверстие в кончике электрода зажим заплата обеспечивает более низкое сопротивление, менее конкурирующими шум, и , таким образом , лучший электрический доступ к внутренней части клетки 4. Тем не менее, отметим , что большое отверстие в наконечнике пипетки может привести к клеточной диализе, и , таким образом , потеря внутриклеточного молекулярного механизма , который может иметь решающее значение для выражения биологических явлений , которые находятся в стадии изучения 5,6. В этом случае, острые записи электрода может быть более подходящим. Этот тип записи требует микропипетки с поры, что значительно меньше, чем те, которые используются для записи целых клеток, предотвращая тем самым большую часть ионного обмена между внутриклеточным пространством и внутренним раствором пипеткой.
Любые формы опыта (острый или хронический), в том числе обучение 7-10, воздействие наркотиков злоупотребления 11,12, напряжение 13,14 и т.д., могут изменять различные аспекты функции нейронов в определенных областях мозга. Поскольку эти изменения часто требуют времени для разработки (часов до нескольких дней), записи целых клеток в срезах мозга от животных, которые претерпели определенный опыт позволяют исследователям идентифицировать эти изменения. В принципе, многие (если не все) компонентов , которые участвуют в нейрональных функций (например, лиганд-активированных ионных каналов, напряжения закрытого ионных каналов, нейромедиаторных транспортерные), и , таким образом , цепь активности мозга и поведение, могут быть изменены с помощью опыта (зависящий от опыта пластичность) 10,15-17. На нейронном уровне, схема активность мозга возникает из постоянных взаимодействий между Synaptic (например, передачи глутамат) и внутренних факторов , клеточная возбудимость (например, axosomato-дендритных ионных каналов: натрий, Na +, калия, K +, а также кальция, Ca 2+ ). При определенных условиях с использованием WholE-Cell патч-зажим электрофизиологические методы, сигнальные изменения, происходящие в частности, от изменений в синаптической против собственного возбудимости может быть выделен.
В большинстве случаев синаптическую возбудимость оценивается с использованием цельноклеточной метода фиксации. Этот режим записи позволяет измерять ионные токи [например, опосредованных рецепторами α-амино-3-гидрокси-5-метил-4-изоксазолпропионовой кислоты ( АМРА-рецепторов) и рецепторов N-метил-D-аспарагиновой кислоты (NMDA-рецепторы)] через нейронную мембрану плазмы, удерживая мембранный потенциал на установленном напряжении. Здесь, экспериментаторы используют внутренние решения микропипетка , которые содержат цезий (Cs +), широкий блокатор K + каналов (ключевые внутренние факторы возбудимость). При создании конфигурации целых клеток, диффузия Cs + в межклеточном пространстве будет блокировать K + каналы, и тем самым позволит как относительно эффективное пространство-зажим и предварительноотдушина влияние внутренних факторов на возбудимость других измерений. Вопросы Пространственно-зажим, то есть трудность напряжения-зажим вся клетка, возникают при записи неправильной формы клетки (например, нейроны) и особенно нейроны с обширной и сложной дендритов 18,19. Поскольку соматический зажим напряжение плохо контролирует напряжение в дереве дендритов нейронов, различные аспекты дендритных электрических сигналов исследуемых искажаются в дендритной расстояния-зависимым образом. В сочетании с фармакологическими средствами , такими как пикротоксином (гамма-аминомасляная кислота, ГАМК антагонист рецепторов) или кинуреновой кислоты (широкий блокатора рецепторов глутамата) , растворенного во внеклеточном растворе (искусственный спинномозговой жидкости, ACSF), эта методика позволяет измерять глутамата ГАМК и рецептором A R-опосредованной токи , соответственно.
В противоположность этому, внутренняя возбудимости обычно оценивается в режиме записи ток-зажим.В отличие от записи напряжения зажимом, этот режим записи позволяет измерять вариации мембранных потенциалов, вызванных ионных токов, протекающих через нейронную мембрану плазмы. Как правило, изменение в собственном возбудимости оценивается через изменения в способности для нейронов генерировать потенциалы действия, которые необходимы как Na + и K + каналы. Таким образом, при выполнении текущего хомута записи, микропипетки заполнены внутренним раствором , который содержит K + вместо Cs +. В сочетании с фармакологическими препаратами , которые блокируют глутамата и ГАМК токи рецептор-опосредованной , растворенные в ACSF, этот экспериментальный дизайн позволяет измерять вклад внутренних факторов (например, K + каналов) к нейрональной обжиге без загрязнена потенциальных изменений в синаптической возбудимости факторы.
В этой статье будут описаны основные необходимые процедурные шаги то (я) подготовить здоровые срезах мозга; (II) достижения конфигурации целой клетки, и (III) осуществляет мониторинг основных параметров для оценки синаптических и внутреннюю возбудимость.
протокол
Все эксперименты проводились в соответствии с протоколами, утвержденными Institutional уходу и использованию животных комитета Техасском путем, и были выбраны таким образом, чтобы свести к минимуму стресс, дискомфорт и боли, испытываемой экспериментальных животных.
1. Решения
Примечание: Подготовить микропипетки внутренние решения заранее. Для большинства основных экспериментальных целей, два вида решений должно быть достаточно: Cs + и K основанное + -На решений.
- -На Решения используют Cs + (например, Cs + раствор глюконата см Материалы) для напряжения прижимных экспериментов. Готовят при комнатной температуре.
- Приготовьте 117 мМ раствор Cs-глюконат путем смешивания 4,62 г D-глюконовой кислоты (~ 3.696 мл) с 3,54 г CsOH (~ 2,01 мл).
- Добавить DDH 2 O до 90 мл и дайте ему уравновешиваться в течение 30 мин.
- Добавьте твердые ингредиенты (20 мМ Hepes = 0,476 г; 0,4 мМ EGTA = 15,2 мг, 2,8 мМ NaCl, = 16,4 мг; 5 мМ тетраэтиламмония (ТЭА) Хлорид = 83 мг).
- Добавить DDH 2 O до ~ 97 мл.
- Доводят рН раствора с помощью 50% CsOH до 7,2 - 7,3.
- Проверьте осмолярность и правильно , если это необходимо с DDH 2 O.
Примечание: Хороший диапазон составляет ~ 280 - 285 мОсм. Оптимальная осмолярность должна быть 15 - 20 мОсм ниже осмолярности стандартного ACSF (обычно 300 - 310 мОсм, 300 мОсм в нашей лаборатории). Осмолярность может варьироваться в зависимости от решений конкретных композиций. - Аликвоты до 1000 мкл и хранить при температуре не выше -20 ° С.
- Приготовьте, аликвоты, замораживание, и добавить ATP / GTP для внутреннего решения в день записи.
- Добавить 64,63 мг АТФ до 10 мг ГТФ и растворяют в 637.11 мкл DDH 2 O.
- Готовят 10 мкл аликвоты и хранят при температуре или ниже -20 ° C. Смешайте каждый 100x аликвоты с 1000 мкл внутреннего раствора на день эксперимента. После того, как АТФ / ГТФ добавляется к внутреннему решению, поддерживать его на лед, чтобы предотвратить АТФ / GTP degradatiна.
- -На Решения Используйте K + (например, K-глюконат раствор, см Материалы) для обоих current- и напряжения зажим экспериментов , где K + кондактансы остаются функциональными , так что нейронная стрельбы может быть оценена. Готовят при комнатной температуре.
- Взвесить все материалы, в зависимости от желаемого конечного объема. Для приготовления 90 мл раствора, 120 мМ K-глюконат = 2,81 г; 20 мМ KCl = 0,149 г; 10 мМ HEPES = 0,238 г; 0,2 мМ EGTA = 0,008 г; 2 мМ MgCl 2 = 0,021 г.
- Используйте достаточно DDH 2 O , чтобы достигнуть 90% от конечного объема раствора. Это должно гарантировать, что достаточно места остается для рН и осмолярности регулировки.
- После добавления и смешивания всех ингредиентов, убедитесь, что раствор прозрачен перед измерением рН.
- Постоянно перемешивая раствор, доведения рН до 7,2 - 7,3 с использованием гидроксида K + (КОН).
- После доведения рН, используйте осмометр и объявлениепросто осмолярности до 280 - 285 мОсм.
Примечание: Оптимальная осмолярность должна быть 15 - 20 мОсм ниже осмолярности стандартного ACSF (обычно 300 - 310 мОсм, 300 мОсм в нашей лаборатории). Осмолярность может варьироваться в зависимости от решений конкретных композиций. - Аликвоты до 1000 мкл и хранить при температуре не выше -20 ° С.
- Приготовьте, аликвоты, замерзнет, и добавьте ATP / GTP к внутреннему раствору в день записи (см шаг 1.1.8).
- Готовят 1 л стандартного ACSF (см Материалы).
Примечание: Мы используем этот рецепт в нашей лаборатории при записи медиальных шиповатых нейронов (MSNs) в срезах мозга, однако, рецепты могут различаться в разных лабораториях, и, следовательно, мы рекомендуем экспериментатору использовать рецепт, который обычно используется при записи область мозга интереса , - Подготовьте рассечение ACSF (нарезки раствор, ~ 125 мл. Примечание: Точный объем будет зависеть от размера нарезания камеры, как она должна полностью погрузить мозг) для использования вшаги 2.2 - 2.8.
- Приготовьте 5 мМ кинуреновой кислоты (блокировать глутамат рецептор-индуцированных экзайтотоксическим процессов) в стандартном ACSF в достаточном объеме, чтобы погрузить мозг во время нарезки. Используйте для обработки ультразвуком, чтобы помочь растворить кинуреновой кислоту.
Примечание: Длина ультразвуковой обработки может изменяться в зависимости от объема и количества твердых веществ в растворе. Растворы должны быть ясно, к концу процесса (около 1 - 2 мин в наших условиях). - Охладить при продувании с 95% O 2, 5% газообразного СО 2 в ведро со льдом , пока температура не достигнет 0 - 2 ° C.
- Приготовьте 5 мМ кинуреновой кислоты (блокировать глутамат рецептор-индуцированных экзайтотоксическим процессов) в стандартном ACSF в достаточном объеме, чтобы погрузить мозг во время нарезки. Используйте для обработки ультразвуком, чтобы помочь растворить кинуреновой кислоту.
- Подготовка ACSF для записи.
- Взять 1 л стандартного ACSF (или любой другой влево из раствора, полученного на стадии 1.3), к которым соответствующие фармакологические агенты могут быть добавлены в зависимости от планируемых экспериментов.
- Например, добавьте 100 мкМ пикротоксином при записи возбуждающие постсинаптические токи или потенциалы (EPSCs или EPSPS), антагонисты рецепторов глутамата (kynureНИК кислота, 2 мМ; или сочетание D-APV 50 мкМ с CNQX 10 мкМ) при записи ингибирующие постсинаптические токи или потенциалы (ИПСК или IPSPs), и оба антагонисты рецептора пикротоксином и глутамата при оценке нейронную обжиг при отсутствии какого-либо влияния синаптических событий.
- Взять 1 л стандартного ACSF (или любой другой влево из раствора, полученного на стадии 1.3), к которым соответствующие фармакологические агенты могут быть добавлены в зависимости от планируемых экспериментов.
2. Кусочек Подготовка
- Построить или получить камеру регенерации срез.
Примечание: Принцип для восстановления камеры проста и может быть сделано в лаборатории (рисунок 1). Вкратце, камера представляет собой сосуд, в котором корзина вставляется держать ломтики мозга на уровне, который ниже, чем на поверхности ACSF. Различные научные компании продают камеры восстановления срез.- В качестве примера, получаем четыре кольца (4 - 6 мм высотой) (Фигура 1А, вид сбоку, б, вид сверху) путем разрезания 30 куб.см шприца. Затем клей растянуты сети (например, вырезанные из нейлона шлюшкид) на одной стороне кольца , чтобы удерживать срезы головного мозга (рис 1б) и склеивают кольца вместе.
Примечание: клей пистолет может быть использован. - После того, как все четыре кольца приклеены, клей изогнутую равнобедренной трапеции-образной пластиковой стенки до двух колец (рис 1А и В) , чтобы отвлечь пузырьков кислорода от выздоравливающих срезах мозга (рис 1C и D). Как показано на рисунке 1D, вставить кислорода диффундирующих систему ( в данном случае , газораспределительную трубку) на той же стороне, что и пластиковые стенки.
- В качестве примера, получаем четыре кольца (4 - 6 мм высотой) (Фигура 1А, вид сбоку, б, вид сверху) путем разрезания 30 куб.см шприца. Затем клей растянуты сети (например, вырезанные из нейлона шлюшкид) на одной стороне кольца , чтобы удерживать срезы головного мозга (рис 1б) и склеивают кольца вместе.
- До нарезка, кислородсодержащих соединений (95% O 2/5% CO 2) и охлаждения раствора для нарезки (см шаг 1.4) к 0 - 2 ° C.
- Заполните пользовательскую камеру регенерации со стандартным ACSF при комнатной температуре. Убедитесь, что ACSF хорошо насыщенной кислородом (20 - 30 мин, время может меняться в зависимости от объема камеры) до размещения ломтики в камере регенерации. Убедитесь в том, что пузырьки газа не вступают в прямой контактичность ломтиками или нарушать их.
- Линия vibratome льда лоток со льдом и залить холодной водой так, чтобы одна треть к половине нарезания камеры погружен в воду. Осторожно установите систему доставки кислорода (например, диффузию газа камень) и датчик температуры в камере нарезания так что ни деталь препятствует движению лезвия или манипуляции среза.
- Подготовьте область рассечение и инструменты, необходимые для извлечения мозга и рассечение нужную область мозга.
Примечание: Точная рассечение выполняется будет зависеть от конкретного региона мозга изучали , как различные мозговые структуры потребует нарезка в разных плоскостях (например, корональные, сагиттальной или горизонтальных слоев.).- Поместите следующие инструменты на лежащей снизу: головы мечом ножницы, скальпель, небольшие прямые острый кончик ножницы, катетеризация сосуда щипцы (или любого хирургического инструмента с широким наконечником, такие как кусачек, который больше подходит для черепов крыс), изогнутые кровоостанавливающие пинцеты, ТВтeezers, шпатель, черпая шпатель, фильтровальная бумага, чашки Петри, единственное лезвие края, и цианакрилатный клей.
- Когда температура достигает 0 - 2 ° C, перенесите нарезки решение нарезка камеры (буферный лоток).
- Обезболить мышь в высыханию камере с использованием изофлуран. Точное количество может изменяться в зависимости от размера камеры, используемой, но для небольшой обувной коробки клетки используют несколько капель (~ 3 - 4). Оставьте мышь в клетке, пока иммобилизовали (не отвечая на тактильные раздражители, около 15 сек для условий, описанных здесь). Выполните хвост и ноги прижимные испытания для того чтобы обеспечить животное глубоко под наркозом, то обезглавить перед тем сердце перестает биться (повышает жизнеспособность клеток).
Примечание: При наличии соответствующего обоснования, некоторые лаборатории получить разрешение на выполнение живого обезглавливание, чтобы минимизировать как можно больше экзайтотоксическим процессов и повышения жизнеспособности клеток. - Выполните рассечение.
Примечание: мозг должен бытьбыстро экстрагируют (<45 сек).- Используя скальпель отрезать поверхностную кожу на верхней части черепа от ростральной до хвостового.
- Очистите кожу головы на каждой стороне головы.
- Используя небольшие прямые острый кончик ножницы, разрезать interparietal пластину вдоль ламбдовидного швом, чтобы удалить мозжечок. Удалить затылочной кости.
- Используя те же ножницы, разрезать стреловидного шва.
- Двигайте канюляция судно щипцов (или кусачек, если поломка крыса череп) под каждым теменных костей и тянуть подвергать мозг.
- Использование изогнутых гемостаза щипцами, щепотка лобные кости, чтобы разорвать их, а затем использовать пинцет или катетеризация сосуда щипцов для удаления сломанных костей. Вырезать и удалить твердую мозговую оболочку как можно более осторожно, как это может помешать рассечение.
- Вставьте лопаточку ниже мозга и осторожно потяните мозг из черепа, чтобы поместить его в камеру нарезки (буфер лоток), предварительно заполненной ледяным ACSF. Пусть мозгостыть в течение 1 - 2 мин.
- Подготовьте рассечение платформу, заполняя чашку Петри со льдом и немного воды со льдом, чтобы позволить большую поверхность контакта, накройте ее крышкой и поместить фильтровальную бумагу на вершине. Смочить фильтровальную бумагу с холодным ACSF.
- После того, как мозг охлаждается, поместите мозг на льду заполненные чашки Петри, и быстро выполнить соответствующую рассечение для получения желаемой плоскости нарезания.
- Для получения сагиттальных, содержащих прилежащем ядре (NAC), использование одного края лезвия бритвы вырезать и удалить обонятельные бугорки и мозжечок, если они все еще присутствуют. Затем выполните сагиттальный разрез 2 - 3 мм от боковой границы правого полушария, чтобы получить плоскую поверхность, которая будет приклеена на образце крепежной пластиной (см шаг 2.8.11).
Примечание: Режущий только 2 - 3 мм от боковой границы полушария позволит обеспечить сбор срезов, содержащих NAC из обоих полушарий. Соответствующая рассечение будет зависетьна области мозга, которая исследуется. Здесь, рассечение выполняется так NAC нейроны могут быть записаны в сагиттальных срезах мозга. - Быстро клей (клей с помощью цианакрилатного прикладывается к образцу удерживающей пластине) плоской поверхности среза головного мозга на пластину в соответствии с желаемой плоскости нарезку. Для получения сагиттальных срезах мозга смотри стадию 2.8.10.
- Сразу же место и закрепить образец, удерживающие пластины в камере нарезания поэтому мозг разрезается ростро-каудально (для безопасности, установить держатель лезвия только тогда, когда образец пластина прикреплена).
- Установите vibratome с соответствующими параметрами нарезке (параметры , используемые в лаборатории для vibratome упомянутых в материалах: скорость 3 - 4, вибрации 9-10, и ломтик толщиной 250 мкм).
- После нарезки, используйте пластиковые урезанные пипетки передачи для передачи срезах мозга в камере регенерации (при комнатной температуре) (см шаг 2.3). Время восстановления может изменяться в зависимости от нейрональной типа, который при изучении(Как правило, 30 - 90 мин).
3. Запись Дозаторы и установка Подготовка
- Обратитесь к конкретным руководящим принципам руководства пользователя Съемник для получения требуемых свойств микропипетка.
Примечание: Для получения множественных абонентских номеров, мы используем диапазон сопротивления пипетку 3.2-4.0 МОм. - Оксигенировать ACSF и регулировать поток до 2 мл / мин. Вакуумный ACSF с помощью перистальтического насоса или вакуумных линий, установленных на объекте.
- Включите контроллер нагревателя перфузионного и регулировать настройки температуры для получения желаемой температуры (например, 31,8 - 32,2 ° C).
Примечание: Температурная стабильность зависит от наличия как постоянный уровень ACSF и скорость постоянного потока в камере. Так как несколько биофизических свойств нейронов (например, входное сопротивление, R я, также называется сопротивление мембраны, R м) являются чувствительным к температуре, поддержание стабильной температуры имеет важное значение. - Включите COMPUтер управляемый усилитель, камера, микроманипулятор и микроскоп фоновый свет. При выполнении эксперимента, который требует электрической стимуляции ткани, включите контроллер стимула и блока изоляции.
Примечание: Некоторые усилители от других производителей рекомендуют "разминка" перед использованием, поэтому рекомендуется обратиться к руководству для точной операционной процедуры. - Запустить захват камеры, обнаружение сигнала и программного обеспечения усилителя.
- Кусочек Размещение и визуализация:
- С помощью пипетки передачи пластиковые отделан кончиком, аккуратно потянуть в один срез мозга из камеры восстановления.
- Поместите передачи пипетки в записи камеры и слегка сжать кусочек из пипетки на покровное выстилающей дно камеры.
Примечание: Пока нет переполнения не происходит, она безвредна иметь некоторую ACSF из камеры восстановления разливая в ванну. - Используйте пинцет, чтобы изменить положение НарезкаO желаемая область будет помещена точно в центре камеры записи. С помощью микроскопа малой мощности (4X) объектив и окуляр для помощи в позиционировании.
- После того, как желаемое положение достигнуто, зафиксировать положение среза мозга с ломтиком прижимом (также известный как "арфа") в камере.
- Переключиться на высокой мощности (40х) объектива и аккуратно опустите его до контакта образуется с ACSF в камере.
- С помощью точной регулировки колеса, чтобы принести ткани в фокусе. В то время как в контакте с ACSF, не используйте грубой настройки колеса на микроскоп как снижение объектива чрезмерно может раздавить срез или даже сломать крышку релайнинг в нижней части камеры, что может привести к ACSF проливать на конденсаторе и повредить его.
- Когда фокус находится на уровне тканей, наблюдать клетки в целевой области для формы. Мертвые клетки легко идентифицировать по их опухшей плазматической мембраны и ядра (<сильный> Рисунок 1E). Здоровые клетки должны появиться как круглые, яйцевидные или эллиптические однородных структур (рис 1E).
- Посмотрите на клетку-мишень. Отметьте его на экране компьютера для того, чтобы помочь микропипетки записи. При использовании программного обеспечения, таких как QCapture, нарисуйте квадрат вокруг клетки-мишени, удерживая левую кнопку мыши.
- Поднимите линзу объектива, так что будет достаточно свободного пространства в конус, образованный линзой объектива, находящейся в контакте с ACSF размещать и перемещать микропипетки записи.
- Микропипетки Размещение и позиционирование
- С помощью 1 мл шприц, неметаллический микрошприцом иглу и специальный фильтр, заполнить микропипетки с внутренним раствором , приготовленным заранее в соответствии с запланированным экспериментом (K + или Cs основанное + -На внутреннее решение, см шаги 1.1., 1.2 и материалы для композиции). Используйте достаточное количество раствора таким образом, внутреннийРешение вступает в контакт с хлоридом покрытием серебряной проволоки электрода в держателе микропипетки.
Примечание: серебряный электрод провод может быть хлорируют, погрузив его в бытовой отбеливатель. Нуклеозидтрифосфатов (АТФ и ГТФ) могут быть добавлены к внутренним раствором непосредственно перед использованием. Держите шприц, содержащий раствор на льду для предотвращения деградации АТФ / ГТФ. - Убедитесь, что нет воздушных пузырьков в микропипетки, поскольку они могут выйти в то время как микропипетка находится в ткани и затенить срез.
- Поместите микропипетки в держатель электрода, так что раствор вступает в контакт с хлоридом покрытием из серебра электродной проволоки.
- Затянуть пипеток колпачок таким образом, чтобы конус шайба образует уплотнение вокруг микропипетки.
- Нанести положительное давление перед погружением микропипетки в ACSF, чтобы предотвратить попадание посторонних частиц пипетку.
- Поместите headstage в запертом положении (обращенной к камере), и с помощью микроманипулятора, гТ О Р А его вниз по направлению к камере, так что примерно под центром погруженной цели.
- При перемещении микропипетки с микроманипулятора (устанавливается на средней и высокой скорости), использовать экран компьютера, чтобы определить местонахождение микропипетки и направлять его в сторону расположения ячейки на оси XY.
- Измерьте сопротивление микропипетки путем применения шагового напряжения (например, 4 мВ в течение 100 мс), что может быть осуществлено вручную или автоматически с помощью специального программного обеспечения , такие , как режим "ванна" при использовании "пленочного Test" в программном обеспечении Clampex (см также этап 4) , Для того , чтобы убедиться , что нет воздушных пузырьков или любые другие посторонние предметы не блокируют микропипетки, применять положительное давление с помощью заполненных воздухом шприц (например, 30 мл шприц) , соединенный с держателем микропипетки с полиэтиленовой трубкой.
- После очистки микропипетки, выполнить напряжение смещения, чтобы уменьшить пипеток тока до нуля, что можно осуществить вручную или с помощью специального программного обеспечения, такие как & #39; пипетку смещение 'на командира усилителя с компьютерным управлением.
Примечание: Эта функция будет компенсировать любое напряжение , вызванное концентрацией различий между ванной и микропипетки решений (то есть, потенциал перехода жидкости 20).
- С помощью 1 мл шприц, неметаллический микрошприцом иглу и специальный фильтр, заполнить микропипетки с внутренним раствором , приготовленным заранее в соответствии с запланированным экспериментом (K + или Cs основанное + -На внутреннее решение, см шаги 1.1., 1.2 и материалы для композиции). Используйте достаточное количество раствора таким образом, внутреннийРешение вступает в контакт с хлоридом покрытием серебряной проволоки электрода в держателе микропипетки.
4. Тест Мембрана
Примечание: Этот шаг относится к усилителю упоминаемых в материалах.
- При использовании командира усилителя с компьютерным управлением, всегда устанавливайте его на режиме напряжения зажим для проведения испытания мембраны.
Примечание: Если тест мембрана находится в режиме "Баня", тест мембрана позволяет измерять сопротивление микропипетки и сопротивление уплотнения, когда образуется уплотнение. - После того , как мембрана разрушается (см шаг 5.8), переключить тест мембраны в режим "Cell" , так что последовательное сопротивление (R S) (также называемое сопротивлением доступа, R а), R I и мембранные емкости (С р)быть получены.
5. Окончательный подход, печать Формирование и получение конфигурации цельноклеточная
- Использование тонкой фокусировки колесо, начать фокусировку вниз при одновременном снижении микропипетки постепенно. Всегда фокусируйтесь вниз, а затем опустить микропипетки вниз к плоскости фокуса. Это гарантирует, что кончик микропипетки не будет внезапно проникать в срезе.
- Когда микропипетка приходит в контакт с поверхностью среза, замедлить скорость Микроманипулятор в режиме средней низкой.
- Осторожно применять легкое положительное давление со шприца заполненного воздухом, соединенным с держателем пипеткой, чтобы очистить любой мусор с траектории захода на посадку.
- Подход клетки либо чередованием с помощью ручек управления XYZ, или путем обращения к диагонали (если модель микроманипулятор позволяет), когда обе оси XZ изменяются с вращением ручки оси Z. Последний метод предотвращает вертикальное сжатие ткани.
Примечание: В данном случае цель состоит в томприближаться к клетке, нанеся минимальный ущерб среза. Когда микропипетки находится достаточно близко к камере появляется ямка (круглой обесцвечиванию поверхности клетки , вызванного положительным давлением , приложенным через кончик микропипетки) (рисунок 2). - При появлении ямка (Рисунок 2-1), нанесите его слабое и кратко отсоса через трубку, которая соединена с всасывающей трубкой держатель пипетки, чтобы создать уплотнение (Рисунок 2-2). Продолжайте мониторинг тест мембраны.
Примечание: Если частичное уплотнение образуется (<1 ГОм), инъекционные отрицательные токи за счет снижения удерживающий потенциал (на командира усилителя с компьютерным управлением) может способствовать формированию уплотнения и достичь gigaohms сопротивления ( "gigaohm печать" или "gigaseal"> 1 - 5 ГОм). Высокое сопротивление уплотнения (> 1 ГОм) оба загрязнения ограничения шума записанного сигнала и внести свой вклад в механическую устойчивостьпатч. - В то время как gigaseal формируется, с помощью управляемого компьютером командира усилителя , чтобы довести удерживающую потенциал ячейки как можно ближе к физиологическому потенциал покоя (V покоя), чтобы предотвратить внезапные изменения , как только мембрана разрушается. Например, MSNs, как правило , напряжения зажимается при -70 или -80 мВ (физиологический V покоя: от -70 до -90 мВ).
- После того, как gigaseal сформировал, компенсировать быстрой и медленной емкости вручную или автоматически. При использовании командира усилителя с компьютерным управлением, такие как командующий Multiclamp, нажмите кнопку 'Auto' для 'Cp Fast' и 'Cp Slow ".
- Если уплотнение остается стабильной и выше 1 ГОм (или инъекций менее 10 - 20 мкА , чтобы держать клетку на желаемом мембранного потенциала), применяют краткое и сильное всасывание через такой же трубы , как в 5.5 , чтобы привести к разрыву плазматической мембраны (рисунок 2 -3).
Примечание: Это может занять несколько судебных процессов. Хороший разрыв мембраны достигается шКурица всасывания выполняется достаточно сильно , так что разорванная мембрана не закупоривает микропипетки (что может привести к увеличению R s во время записи), но достаточно слабо для того , чтобы не втягивать значительной части мембраны или клетки. - После достижения успешной конфигурации целой клетки, регулярно контролировать местоположение микропипетки для оценки и коррекции существенного дрейфа, поскольку это может привести к потере патча. Амплитуда Дрейф может варьироваться в зависимости от нескольких факторов, например, качество монтажа буровой установки и тянущие усилия на headstage. В идеале, дрейф должен быть почти не существует.
- При переключении в режим "Cell" в тесте мембраны, просматривать различные параметры ячейки , такие как R I, R s и C р. Мониторинг этих параметров во время записи.
Примечание: Все эти параметры могут помочь оценить начальное состояние здоровья клеток и типов клеток (см "тест мембрана" раздел, шаг 4). - После того, как гое выше шаги будут завершены, остаются в режиме напряжения зажим для измерения токов (например, EPSCs, ИПСК), или перейти в режим текущего зажима , если планирование для измерения изменений мембранного напряжения (например, потенциал действия стрельбы). Что касается последнего, придать положительный или отрицательный ток, чтобы держать ячейку в требуемое напряжение мембраны (чтобы выполнить этот шаг, обратитесь к усилителю руководство).
Результаты
Температура, фактор , который легко управляется экспериментатором, влияет на биофизические свойства ионных каналов и рецепторов, и , таким образом , форма волны постсинаптических токов (ЧОК) (EPSC и иПСК) и способности нейронов , чтобы вызвать спайки. Рисунок 3 и на фиг 4 показано влияние температуры на нейрональные стрельбы и наклон вызванных EPSCs (eEPSCs) соответственно. Схема обжига (рисунок 3) (то есть, задержка на 1 - й шип, шип количество, частоту и потенциал действия сигнала) формируется приурочено и скоординированным открытия и закрытия конкретных напряжения закрытого ионных каналов (Na +, Ca 2 + и K +), процесс чувствителен к температуре. на рисунке 3 показано , как среднее число спайка увеличивается с ростом температуры. Обратите внимание, что в экспериментальных условиях, описанных здесь (MSNs записи) хотя и шип frequeNCY - видимому, не может быть изменен при subphysiological температуре (28 ° C), она значительно возрастает , когда температура достигает физиологически соответствующего уровня (32 ° С). На фиг.4А показан пример того , как наклон eEPSCs, параметр , который обычно используется для оценить синаптическую силу, увеличивается с ростом температуры.
Хотя R s может быть в некоторой степени контролируемыми экспериментатором, т.е. посредством эффективного открытия мембраны при переходе от состояния уплотнения конфигурации цельноклеточная, R обычно S медленно увеличивается во время записи. Это может быть результатом различных неконтролируемых событий, например, мембранные повторного закрытия или остатков засорение наконечника пипетки во время записи. Попытка повторно открыть мембрану, применяя легкое отсасывание, хотя это может поставить под угрозу исправление, иногда может помочь поддерживать стабильный R S. Во всех случаях, так как изменения R S может альтер формы волны электрического сигнала исследуемого, его необходимо тщательно контролировать, и в частности , при записи ЧОК (режим фиксации потенциала). На рисунке 4 показано , что при увеличении R S (фиг.4В), амплитуда глутаматом токов рецептор-опосредованного (eEPSCs ) уменьшается (рис 4C, D). Как правило, экспериментаторы отбросить данные , когда изменения в R с превышает 15% (например, эта лаборатория), однако некоторые лаборатории делают это от изменения 20%. Этот критерий должен быть указан в методе разделе статьи.
Для определенного нейрона, R я может зависеть от нескольких факторов, включая температуру, здоровье клеток и качество пластыря. В частности, когда R I уменьшается, PSC амплитуды или способность нейронов генерировать шипы также уменьшается. Например, на рисунке 4Е показывает , что , когда R я не сильно различаются, тысе число шипов остаются относительно стабильными (Neuron 1); и когда R I увеличивается, число шипов также увеличивается (Neuron 2). Поэтому и аналогично R S, R я должен тщательно контролироваться, так как 10% изменения являются достаточными для данных смещения.
Как описано выше, имеет решающее значение для контроля или мониторинга температуры, R S и R я во время записи. Например, наблюдаемые изменения в сигнале , который находится в стадии изучения (ЧОК или обжига) может быть связано с изменениями (или отсутствие контроля) этих факторов , а не влияние экспериментальных манипуляций, например, по сравнению с пред - пост-эффекты от препарат применение ванны.

Рисунок 1. выполненное на заказ Восстановление палаты (AD) и изображение мозга Кусочек на 400X Показаны здоровых и мертвых Нейроны (E). ОБЪЯВЛЕНИЕ)Процедура , чтобы сделать камеру восстановления пользовательских описана в шаге 2.1. E) Изображение NAC медиальной оболочки множественных абонентских номеров в срезе мозга на 400X показывая примеры здоровых (красные стрелки) против мертвых нейронов (синие стрелки). Следует отметить, что хотя некоторые клетки обозначены как здоровые, их сферическая аспект показывают, что они не могут быть столь же здоровым, как желательно (красные стрелки с звездочками). Состояние здоровья Окончательный оценивается на основе V покоя и R я после достижения конфигурации целой клетки. Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.

Рисунок 2. Диаграмма Изображая Основные процедурные шаги по получению Gigaseal и установления конфигурации цельноклеточная. Когда микропипетка находится достаточно близко к йе клеток, чтобы создать впадину в плазменной мембране (шаг 1, подход), нанесите краткий и нежный отсасывание для создания плотного контакта между микропипетки и плазматической мембраны. Если выполнены должным образом, контакт укрепит и сопротивление будет возрастать и достигнет 1 ГОм (gigaseal) или более (шаг 2, образование уплотнений). После того, как уплотнение является стабильной и выше 1 ГОм, нанесите краткое и сильное всасывание к разрыву плазматической мембраны (стадия 3, конфигурации цельноклеточная). Достижение конфигурации целой клетки позволит непрерывность между цитоплазмой и внутренней микропипетки. Для получения дополнительной информации см шаг протокола 5.1-5.8. Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
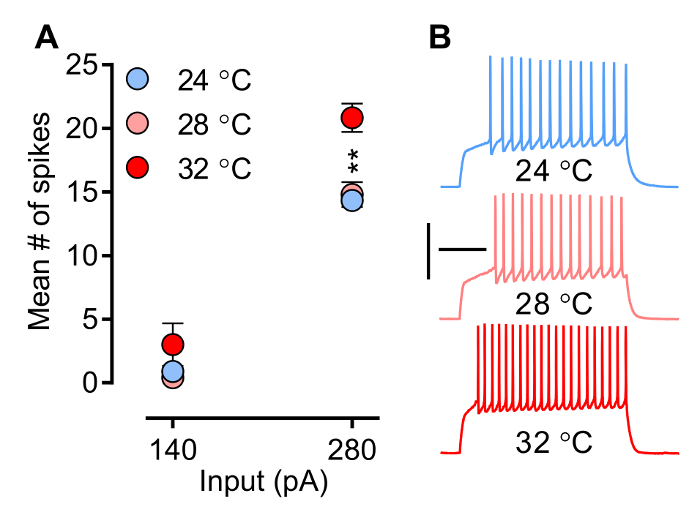
Рисунок 3. Нейрональная розжига (искробезопасности возбудимость) оценивается в вольт-моллюск р Mode. Здесь, предопределенные и инкрементный ряд текущих шагов задается для того , чтобы выявить изменения мембранного напряжения, и тем самым вызвать потенциалы действия. А) Среднее число спайка увеличивается с ростом температуры. B) Образец следов при 280 мкА от NAc срединные MSNs оболочки при трех различных температурных настроек (24 ° C, N = 9; 28 ° C, N = 5, и 32 ° C, N = 6). Температура в камере записи непосредственно влияет на частоту шипа. Тем не менее, обратите внимание, что, хотя пик частоты, кажется, не может быть изменен при температуре subphysiological, она значительно возрастает, когда температура достигает 32 ° C, физиологически соответствующую температуру. Нейроны проводятся при -80 мВ. Двусторонний ANOVA: взаимодействие, р <0,0001; Влияние температуры, р = 0,0041; Постфактум испытания: 24 ° C и 28 ° C оба значительно отличается от 32 ° С, ** р <0,01. Данные представлены в виде среднего значения ± SEM. Калибровка: 200 мс, 50 мВ.jove.com/files/ftp_upload/54024/54024fig3large.jpg "целевых =" _blank "> Пожалуйста, нажмите здесь, чтобы посмотреть увеличенную версию этой фигуры.

Рисунок 4. Влияние температуры, R s и R I на форме волны электрического сигнала на стадии изучения. А) Пример eEPSC амплитуды от одного NAc MSN оболочки. Повышение температуры от 24 до 28 ° С и до 32 ° С увеличивает наклон eEPSCs. Обратите внимание, что температурные изменения наклона eEPSCs происходят быстро. Здесь склон eEPSCs оценивается в режиме напряжения зажим. Калибровка: 5 мс, 100 пА BD) Пример eEPSCs наклона от одного NAc MSN оболочки.. При увеличении R S (B), наклон eEPSCs уменьшается (C). D) корреляционный анализ наклона eEPSC как функция Rs. Пирсона R = -0,5717, р <0,0001. Нейроны напряжения зажимается при -80 мВ. Е) Пример следов от двух нейронов , показывающих влияние R I на способность нейрона генерировать шипы. Нейроны тока зажаты, и выдерживают при -80 мВ. Калибровка:. 200 мсек, 50 мВ Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
Обсуждение
Этот протокол описывает основные процедуры для выполнения целого клеточных экспериментов патч-зажим на нейроны в срезах мозга. Однако сложность, потенциал и чувствительность данного метода не может быть полностью описана в этой статье. Здесь мы попытались обрисовать самые основные шаги и подчеркнуть важные параметры, которые должны контролироваться для достижения успешных и точных записей целых клеток. Для дальнейшего теоретического обучения, много книг и статей были опубликованы на обоих цельноклеточной записи патч-зажим в мозговых срезах 3,21-24 и о методах , которые могут уточнить решения , используемые 25-27 в целях повышения жизнеспособности клеток. Для того, чтобы регулярно выполнять соответствующие записи, совершенствование технических навыков посредством интенсивной практики требуется. Тем не менее, при правильном применении шагов уже упоминалось, клетки могут быть исправлен часов некропсический, обеспечивая важную информацию об изменениях в синаптических функций и внутренней excitabiмируемости.
В общем, помимо важности тщательно готовились как ACSF и внутренние микропипетка решения, каждый шаг от рассечения мозга, нарезка, достижение успешной конфигурации целой клетки, а также получение строгой и объективной информации требует интенсивной практики. В первую очередь, это имеет решающее значение для создания здоровых срезов мозга. Вкратце, быстрое рассечение мозга (в идеале <45 сек), поддержание низкой температуры (0 - 2 ° C), тогда как нарезка, а также соответствующие решения по нарезке все играют важную роль в обеспечении здоровья клеток. Следует отметить, отметить, что нарезка решения могут различаться между лабораториями и в зависимости от типа клеток и / или области мозга, который будет исследован. При нарезке НСС или спинной полосатого тела, наша лаборатория и другие используют кинуреновой кислоту для решения нарезания , чтобы свести к минимуму процессы экзайтотоксическим 28-33, однако, могут быть также использованы и другие методы, такие как растворы на основе сахарозы 34, высокое Mg 2+ / низкие растворы Ca 2+ 35, и т.д.. Это всего лишь несколько примеров , и могут быть скорректированы в зависимости от чувствительности мозга или головного мозга региона к экзайтотоксическим процессов (например, из - за возраста). Для получения дополнительной информации о решениях и жизнеспособности клеток, пожалуйста , см 25-27. В конечном счете, концентрация анионов, катионов и других лекарственных средств (например, аскорбиновая кислота, антагонисты рецептора глутамата), составляющие SLICING решения определяют таким образом, что он имитирует спинномозговой жидкости и сводит к минимуму как можно больше экзайтотоксическим процессов , которые происходят во время нарезания. Протокол , представленные в этой статье описаны стандартные решения , которые были обычно используемые в предыдущих исследованиях авторов 28-31 при записи с в множественных абонентских номеров НСС или спинной стриатуме в срезах мозга. Кроме того, правильная настройка осмолярности для обоих ACSF и внутренние микропипетки решения имеют решающее значение для формирования успешного уплотнения и поддержания целых клеток конфiguration. Чтобы создать градиент концентрации от внеклеточного раствора к интра-пипеток раствора, ACSF осмолярность должна быть выше, чем для внутренних решений микропипетки. В идеале, разница может быть в диапазоне от 10 до 30 мОсм.
Достижение успешной конфигурации целой клетки является еще одним важным шагом для проведения эффективных записей. Во-первых, пипетка емкость можно регулировать как только пипеткой помещают в ванну. Несмотря на то, автоматические настройки, как правило, правильно установлено, желательно использовать быстрые и медленные корректировки емкость ячейки с осторожностью, поскольку они могут привести к повреждению клетки, когда не выполняются соответствующим образом. Во-вторых, кратко мембрана всасывания, которая необходима, чтобы привести к разрыву мембраны приведет к значительному открытию мембраны, и тем самым обеспечить хорошее взаимодействие между внутриклеточным и внутри микропипетки среды. Это гарантирует , что R s будет оставаться относительно стабильным на протяжении записи. При использовании Cs на основе решения микропипетки,мембранный потенциал покоя следует оценивать сразу же после установления конфигурации цельноклеточной (этап 5.8). Действительно, диффузия Cs + внутри клетки приводит к потере мембранного потенциала покоя. Для того, чтобы определить надлежащий потенциал покоя, стык потенциал жидкость должна быть оценена 20. Тем не менее, экспериментатор может сообщить о том, что потенциал покоя наблюдается после разрыва мембраны (после шага 5.8) и выбрать не отрегулировать для потенциала жидкостного соединения. Во всех случаях он должен быть упомянут в методе разделе статьи. После установления конфигурации цельноклеточной, С р также могут быть получены и могут быть использованы в качестве косвенного показателя для оценки состояния здоровья клеток и / или типа клеток. В-третьих, когда началась запись, другие параметры должны быть строго контролироваться. Критические факторы , которые должны контролироваться при оценке нейронную возбудимость температуры, R s и R я.
В видеупоминалось выше, R I и С р может быть показателем здоровья клеток и / или клеточного типа. Например, плазматическая мембрана, действуя в качестве изоляционного материала, отделяет заряд (в результате различного состава внутриклеточным и внеклеточным решений), которые вместе составляют мембранную емкость. Чем больше поверхности мембраны (нейронный-специфических), тем выше емкость. Тогда не удивительно , что специфические типы нейронов демонстрируют С р и R я (математически связан с C р) , которые находятся в том же диапазоне. R s непосредственно связан с размером кончика пипетки, и поэтому, как правило , указывает на качество или размер отверстия мембраны. Если коротко, то при установлении конфигурации целой клетки, цитоплазма становится электрически непрерывным с раствором в микропипетки и полностью изолированы от внешней среды. R S (или R а) берет свое начало от сопротивления для Currenт вытекать из пипетки в цитоплазму. Для некоторых условий съемки (например, текущий режим зажим или напряжения зажим записи напряжения закрытого ионных токов), R s должны быть компенсированы должным образом (см Ref. 3,21-24 или усилителю руководство для компенсации надлежащего R S) ,
Как описано на рисунке 4, R s имеет особенно важное значение , поскольку это может существенно повлиять на электрическую форму сигнала, например, EPSC амплитуду. Тем не менее, R s необходимо тщательно следить за офф-лайн интерпретации любых наблюдаемых эффектов. В случае , если мембрана не была разорвана должным образом, микропипетка наконечник засорение или повторное закрытие мембраны может произойти, в котором увеличивается случай г с и смещения формы волны электрического сигнала при исследовании (рис 4В-D). Таким образом, многочисленные проблемы могут встречаться во время записи, и те, как правило, делятся на три категории: I) ткани, связанной с, Например, увеличение смертности клеток из - за плохого рассечения, дезадаптации ACSF осмолярности и гипоксии; б) оборудование , связанные, например, шум и проблемы с заземлением, контроль температуры, срез и микропипетка позиционирование и т.д..; и III) интерпретации данных, например, наблюдаемые изменения могут быть результатом нежелательных экспериментальных артефактов смещая данные , такие как изменения в электрических осциллограмм изменяющие параметров (R I, R s, температура, смотри рисунок 3 и 4) , а не в результате экспериментальных манипуляциями.
Хотя запись цельноклеточная в срезах мозга является мощным средством для оценки зависящей от опыта пластичности, этот подход ограничивает интерпретацию данных. В частности, три важных ограничения метода записи целых клеток является то, что: (I) изменения уровня функциональных и экспрессии специфических белков (например, ионные каналы) не могут быть выделены; (II), так как этотМетодика оценивает протекание тока через всю мембрану (или значительную часть), она не обеспечивает точного субклеточном локализации ионных токов или изменений, которые наблюдаются; и (III) инвазивность конфигурации целых клеток приводит к диализу содержимого клеток, и, таким образом, к нарушению внутриклеточных молекулярных механизмов, необходимых для некоторых явлений для разработки или быть выражены. Один из способов избежать диализ является использование острых записи электрода или перфорированную технику патч 3,21,23. Что касается последнего, порообразующих антибиотические молекулы, такие как нистатин могут быть добавлены в раствор пипеткой. Формирование этих пор позволит запись токов, не нарушая второй механизмы мессенджеров внутри клетки. Тем не менее, последние достижения в области нанотехнологий и развитие наноэлектродов 36 предоставляют мощные инструменты для улучшения нейронные записи. Такой технический прогресс в области неврологии все еще находятся под РАЗРАБОТКАт и теперь положить в нашей досягаемости возможность проведения патч-зажим и внутриклеточные записи с минимальной инвазивности, то есть, сохраняя внутриклеточный среду нетронутыми, и исследование функции ионных каналов в субклеточных отсеков , которые были до сих пор не доступны с классическим патч-зажим электродов 37.
Раскрытие информации
Ни один из авторов не имеют конкурирующие интересы или противоречащие друг другу интересы.
Благодарности
Это исследование было поддержано за счет средств запуска UT Юго-Западного (SK).
Материалы
| Name | Company | Catalog Number | Comments |
| Isolated pulse stimulus generator | A.M.P.I | Master-8 | |
| Isolation unit (ISO-Flex) | A.M.P.I | ISO-Flex | |
| Computer controlled Amplifier | Molecular Devices | Multiclamp 700B | |
| Digital Acquisition system | Molecular Devices | Digidata 1500 | |
| Microscope | Olympus | BX-51 | |
| Micromanipulator | Sutter Instruments | MPC-200 | |
| Chamber and in-line Heater | Warner Instruments | TC-344B | |
| Vibratome Slicer | Leica | VT1000 S | |
| Micropipette Puller | Narishige | PC-10 | |
| Imaging Camera | Q Imaging | QIClick-F-M-12 | |
| Narishige pipette puller PC-10 | Narishige | PC-10 | |
| Glass capillaries | WPI | TW150F-3 | |
| Slice hold-down (harp) | Warner Instruments | 64-0255 | |
| Slice Chamber | Warner Instruments | RC-26 | |
| Nonmetallic syringe needle | World Precision Instruments | MF28G67-5 | |
| Syringe filters | Nalgene | 176-0045 | |
| Glue Gun | Home Depot | various | |
| Gas dispersion tube | Ace Glass Inc. | various | |
| Decapitation scissors | Home Depot | 100649198 | |
| Scalpel Handle #3 | World Precision Instruments | 500236 | |
| Small straight sharp tips scissors | World Precision Instruments | 14218 | |
| Vessel canulation forceps | World Precision Instruments | 500453 | |
| Curved hemostatic forceps | World Precision Instruments | 501288 | |
| Economy Tweezers #3 | World Precision Instruments | 501976-6 | |
| Spatula | Fisher Scientific | 14357Q | |
| Scooping spatula | Fisher Scientific | 14-357Q | |
| Petri dish | Fisher Scientific | 08-747B | |
| Filter paper | Lab Depot | CFP1-110 | |
| Solutions | |||
| Cs-Gluconate internal solution (pH 7.2–7.3, 280–290 mOsm) | |||
| D-gluconic acid 50% | Sigma Aldrich/various | G1951 | |
| Cesium-OH (CsOH) 50% | Sigma Aldrich/various | 232041 | |
| NaCl, 2.8 mM | Sigma Aldrich/various | S7653 | |
| HEPES, 20 mM | Sigma Aldrich/various | H3375 | |
| EGTA, 0.4 mM | Sigma Aldrich/various | E4378 | |
| tetraethylammonium-Cl, 5 mM | Sigma Aldrich/various | T2265 | |
| Na2GTP, 0.3 mM | Sigma Aldrich/various | G8877 | |
| MgATP, 2 mM | Sigma Aldrich/various | A9187 | |
| K-Gluconate internal solution (pH 7.2–7.3, 280–290 mOsm) | |||
| K D-gluconate, 120 mM | Sigma Aldrich/various | G4500 | |
| KCl, 20 mM | Sigma Aldrich/various | P3911 | |
| HEPES, 10 mM | Sigma Aldrich/various | H3375 | |
| EGTA, 0.2 mM | Sigma Aldrich/various | E4378 | |
| MgCl2 | Sigma Aldrich/various | M8266 | |
| Na2GTP, 0.3 mM | Sigma Aldrich/various | G8877 | |
| MgATP, 2 mM | Sigma Aldrich/various | A9187 | |
| Standard artificial cerebrospinal fluid (ACSF, osmolarity ≈ 300-310 mOsm) | |||
| KCl, 2.5 mM | Sigma Aldrich/various | P3911 | |
| NaCl, 119 mM | Sigma Aldrich/various | S7653 | |
| NaH2PO4•H2O, 1 mM | Sigma Aldrich/various | S9638 | |
| NaHCO3, 26.2 mM | Sigma Aldrich/various | S8875 | |
| Glucose, 11 mM | Sigma Aldrich/various | G8270 | |
| MgSO4-7H2O, 1.3 mM | Sigma Aldrich/various | 230391 | |
| CaCl2-2H2O, 2.5 mM | Sigma Aldrich/various | C3881 | |
| Additional compounds used for solutions preparation | |||
| KOH | various | ||
| Kynurenic acid | Sigma Aldrich/various | K3375 | |
Ссылки
- Neher, E., Sakmann, B. Single-channel currents recorded from membrane of denervated frog muscle fibres. Nature. 260 (5554), 799-802 (1976).
- Sakmann, B., Neher, E. Patch clamp techniques for studying ionic channels in excitable membranes. Annu Rev Physiol. 46, 455-472 (1984).
- Cahalan, M., Neher, E. Patch clamp techniques: an overview. Methods Enzymol. 207, 3-14 (1992).
- Staley, K. J., Otis, T. S., Mody, I. Membrane properties of dentate gyrus granule cells: comparison of sharp microelectrode and whole-cell recordings. J Neurophysiol. 67 (5), 1346-1358 (1992).
- Horn, R., Marty, A. Muscarinic activation of ionic currents measured by a new whole-cell recording method. J Gen Physiol. 92 (2), 145-159 (1988).
- Pusch, M., Neher, E. Rates of diffusional exchange between small cells and a measuring patch pipette. Pflugers Arch. 411 (2), 204-211 (1988).
- Kandel, E. R., Dudai, Y., Mayford, M. R. The molecular and systems biology of memory. Cell. 157 (1), 163-186 (2014).
- Kourrich, S., Bonci, A. Chapter 5: Synaptic and Neural plasticity. Neurobiology of Mental Illness. 4th edn. , (2013).
- Mozzachiodi, R., Byrne, J. H. More than synaptic plasticity: role of nonsynaptic plasticity in learning and memory. Trends Neurosci. 33 (1), 17-26 (2010).
- Zhang, W., Linden, D. J. The other side of the engram: experience-driven changes in neuronal intrinsic excitability. Nat Rev Neurosci. 4 (11), 885-900 (2003).
- Kourrich, S., Calu, D. J., Bonci, A. Intrinsic plasticity: an emerging player in addiction. Nat Rev Neurosci. 16 (3), 173-184 (2015).
- Luscher, C., Malenka, R. C. Drug-evoked synaptic plasticity in addiction: from molecular changes to circuit remodeling. Neuron. 69 (4), 650-663 (2011).
- McEwen, B. S., Morrison, J. H. The brain on stress: vulnerability and plasticity of the prefrontal cortex over the life course. Neuron. 79 (1), 16-29 (2013).
- Sandi, C., Haller, J. Stress and the social brain: behavioural effects and neurobiological mechanisms. Nat Rev Neurosci. 16 (5), 290-304 (2015).
- Kim, S. J., Linden, D. J. Ubiquitous plasticity and memory storage. Neuron. 56 (4), 582-592 (2007).
- Ganguly, K., Poo, M. M. Activity-dependent neural plasticity from bench to bedside. Neuron. 80 (3), 729-741 (2013).
- Kullmann, D. M., Moreau, A. W., Bakiri, Y., Nicholson, E. Plasticity of inhibition. Neuron. 75 (6), 951-962 (2012).
- Bar-Yehuda, D., Korngreen, A. Space-clamp problems when voltage clamping neurons expressing voltage-gated conductances. J Neurophysiol. 99 (3), 1127-1136 (2008).
- Williams, S. R., Mitchell, S. J. Direct measurement of somatic voltage clamp errors in central neurons. Nat Neurosci. 11 (7), 790-798 (2008).
- Neher, E. Correction for liquid junction potentials in patch clamp experiments. Methods Enzymol. 207, 123-131 (1992).
- Defelice, L. J. . Electrical Properties of Cells-Patch Clamp for Biologists. , (1997).
- Kornreich, B. G. The patch clamp technique: principles and technical considerations. J Vet Cardiol. 9 (1), 25-37 (2007).
- Molleman, A. . Patch Clamping: An Introductory Guide To Patch Clamp Electrophysiology. , (2003).
- Neher, E., Sakmann, B. The patch clamp technique. Sci Am. 266 (3), 44-51 (1992).
- Richerson, G. B., Messer, C. Effect of composition of experimental solutions on neuronal survival during rat brain slicing. Exp Neurol. 131 (1), 133-143 (1995).
- Tanaka, Y., Tanaka, Y., Furuta, T., Yanagawa, Y., Kaneko, T. The effects of cutting solutions on the viability of GABAergic interneurons in cerebral cortical slices of adult mice. J Neurosci Methods. 171 (1), 118-125 (2008).
- Ye, J. H., Zhang, J., Xiao, C., Kong, J. Q. Patch-clamp studies in the CNS illustrate a simple new method for obtaining viable neurons in rat brain slices: glycerol replacement of NaCl protects CNS neurons. J Neurosci Methods. 158 (2), 251-259 (2006).
- Kourrich, S., et al. Dynamic interaction between sigma-1 receptor and Kv1.2 shapes neuronal and behavioral responses to cocaine. Cell. 152 (1-2), 236-247 (2013).
- Kourrich, S., Klug, J. R., Mayford, M., Thomas, M. J. AMPAR-Independent Effect of Striatal aCaMKII Promotes the Sensitization of Cocaine Reward. J Neurosci. , (2012).
- Kourrich, S., Rothwell, P. E., Klug, J. R., Thomas, M. J. Cocaine experience controls bidirectional synaptic plasticity in the nucleus accumbens. J Neurosci. 27 (30), 7921-7928 (2007).
- Kourrich, S., Thomas, M. J. Similar neurons, opposite adaptations: psychostimulant experience differentially alters firing properties in accumbens core versus shell. J Neurosci. 29 (39), 12275-12283 (2009).
- Rothwell, P. E., Kourrich, S., Thomas, M. J. Environmental novelty causes stress-like adaptations at nucleus accumbens synapses: implications for studying addiction-related plasticity. Neuropharmacology. 61 (7), 1152-1159 (2011).
- Rothwell, P. E., Kourrich, S., Thomas, M. J. Synaptic adaptations in the nucleus accumbens caused by experiences linked to relapse. Biol Psychiatry. 69 (11), 1124-1126 (2011).
- Koya, E., et al. Silent synapses in selectively activated nucleus accumbens neurons following cocaine sensitization. Nat Neurosci. 15 (11), 1556-1562 (2012).
- Conrad, K. L., et al. Formation of accumbens GluR2-lacking AMPA receptors mediates incubation of cocaine craving. Nature. 454 (7200), 118-121 (2008).
- Kruskal, P. B., Jiang, Z., Gao, T., Lieber, C. M. Beyond the patch clamp: nanotechnologies for intracellular recording. Neuron. 86 (1), 21-24 (2015).
- Novak, P., et al. Nanoscale-targeted patch-clamp recordings of functional presynaptic ion channels. Neuron. 79 (6), 1067-1077 (2013).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены