뉴클레오필성 대체
Overview
출처: 비 M. 동과 김 다니엘, 캘리포니아 대학, 어바인, 캘리포니아
뉴클레오필성 대체 반응은 유기 화학에서 다루는 가장 기본적인 주제 중 하나입니다. 뉴클레오필성 대체 반응은 뉴클레오필(전자가 풍부한 루이스 베이스)이 탄소 원자에서 떠나는 그룹을 대체하는 반응이다.
SN1 (S = 대체, N = 뉴클레오필, 1 = 1차 운동학)
SN2 (S = 대체, N = 뉴클레오필, 2 = 2차 운동학)
이 비디오는 SN1과 SN2 반응 사이의 미묘한 차이와 뉴클레오필성 대체 반응의 각 유형을 가속화하는 데 도움이되는 요인을 시각화하는 데 도움이됩니다. 첫 번째 섹션은 뉴클레오포성 대체 반응에 대해 더 잘 이해하고 배우는 데 도움이되는 반응에 초점을 맞출 것입니다. 두 번째 섹션은 대체 반응의 실제 예제에 초점을 맞출 것입니다.
Principles
뉴클레오필성 대체 반응에서 뉴클레오필은 탄소 원자에 떠나는 그룹을 대체합니다. 1단계 뉴클레오필릭 대체는 SN2기전의 예이다. 이러한 반응은 채권이 끊기고 형성되는 동시에 발생하는 공동 반응이다. 명심해야 할 한 가지는 반응에 관여하는 분자 궤도가 핵형성 공격이 떠나는 단으로부터 180°에서 와야 함을 나타낸다는 것입니다. 따라서 SN2반응의일부 별명은 "백사이드 공격"에 반응합니다. 이 백사이드 공격은 반응탄소의 스테레오케미케를 반전시다. 이것은 반응의 개시에 있는 입체화학이 반응 후에 입체화학의 결과를 지시하는 입체특이적인 반응의 예입니다.

2단계 뉴클레오필식 대체는 SN1 메커니즘의 예이다. 첫 번째 단계에서, 떠나는 그룹은 카보케이션이라고 불리는 중간체를 떠난다. 두 번째 단계에서, 뉴클레오필은 카보케이션을 공격한다. 카보양이 치랄이 아니기 때문에 반응 의 시작 부분에 있는 모든 입체화학이 손실됩니다. 이 제품은 여전히 키랄이지만 지금은 racemic 혼합물이라고 불리는 두 상안제의 균일 한 혼합물입니다. SN1 반응은 스테레오특이성이 아닙니다.
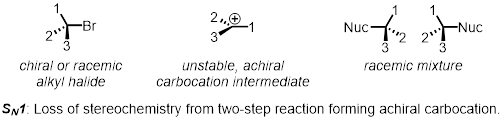
두 부분에서 는 SN1 및 SN2 반응의 상대적 속도에 영향을 미치는 요인을 검사합니다.
1부에서는 11개의 시험관 반응을 사용하여 SN1반응을 연구할 것입니다. 모든 반응은 동일한 일반적인 반응 체계를 가지고 있습니다.
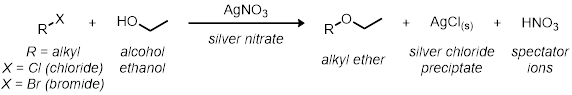
반응의 모든 속도는 서로 에 상대적입니다. 반응 속도는 반응의 시각적 지표에 의해 결정됩니다. 은염화물은 용액에서 침전되기 때문에 반응이 맑고 흐린 순간 상대 반응 속도를 시각적으로 나타냅니다.
시험관 반응의 세 가지에서, 알킬 할리드 구조가 반응의 속도에 역할을 하는 방법은 시험될 것이다. 동일한 조건하에서 세 가지 다른 알킬 염화물이 테스트됩니다.
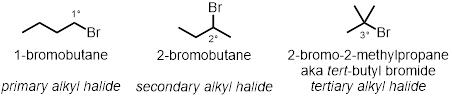
시험관 반응의 두 가지에서, 반응에 대한 용매 극성 효과는 시험될 것이다. 두 개의 서로 다른 용매가 테스트됩니다.
| 시험관 | 용매 | 용매의 종류 |
| 1 | 100% 에탄올 | 극성 프로틱 |
| 2 | 5% 에탄올:95% 아세톤 | 대부분 극성 아프로틱 |
시험관 반응의 두 에서, 떠나는 그룹 효과 테스트 됩니다. 두 개의 다른 알킬 할리드가 사용됩니다.

마지막으로, 4개의 시험관이 반응의 속도 법칙을 측정하는 데 사용될 것입니다. 반응의 속도는 요오드 화 나트륨 용액과 1-브로모부탄 용액의 다양한 농도로 측정될 것이다.
| 시험관 |
테르부틸 염화물 농도 |
실버 질산염 농도 |
강수량까지의 시간 |
| 1 | 0.1 M | 0.1 M | |
| 2 | 0.2M | 0.1 M | |
| 3 | 0.1 M | 0.1 M | |
| 4 | 0.1 M | 0.05 M |
2부에서는 11개의 시험관 반응을 사용하여 SN2반응을 연구할 것입니다. 모든 반응은 동일한 일반적인 반응 체계를 가지고 있습니다.
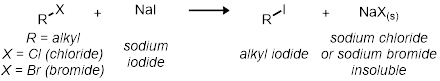
반응의 모든 속도는 서로 에 상대적입니다. 반응 속도는 염화나트륨 또는 브로마이드 나트륨의 시각적 지표에 의해 결정됩니다. 이것은 반응이 맑고 흐린 때 표시됩니다.
시험관 반응의 세 가지에서, 알킬 할리드 구조가 반응의 속도에 역할을 하는 방법은 시험될 것이다. 이것은 브롬에 묶여 있는 탄소의 황질한 효력을 비교할 것입니다. 동일한 조건하에서 세 가지 다른 알킬 염화물이 테스트됩니다.

시험관 반응의 두 가지에서, 알킬 할리드의 이차 적인 비약효과 시험될 것이다. 이들은 브로마이드에 결합된 탄소를 포함하지 않는 분자에 대한 황체 효과입니다. 동일한 조건에서 두 개의 다른 기본 알킬 브로마이드가 테스트됩니다.

시험관 반응의 두 에서, 떠나는 그룹 효과 테스트 됩니다. 두 개의 다른 알킬 할리드가 사용됩니다.

마지막으로, 4개의 시험관이 반응의 속도 법칙을 측정하는 데 사용될 것입니다. 반응의 속도는 요오드 화 나트륨 용액과 1-브로모부탄 용액의 다양한 농도로 측정될 것이다.
| 시험관 |
요오드 나트륨 농도 |
1-브로모부탄 농도 |
강수량까지의 시간 |
| 1 | 15% | 1.0 M | |
| 2 | 15% | 2.0 M | |
| 3 | 15% | 1.0 M | |
| 4 | 7.5% | 1.0 M |
Procedure
1부: SN1반응 연구
알킬 할리데 구조:
- 절대 에탄올에 실버 질산염의 0.1 M 용액의 2mL를 세 개의 시험관 각각에 측정한다.
- 첫 번째 테스트 튜브에 1-브로모부탄 2 방울을 추가합니다. 두 번째 테스트 튜브에 2 방울의 브로모부탄을 추가합니다.
- 최종, 세 번째 테스트 튜브에 2-브로모-2-메틸프로판 2 방울을 추가합니다.
- 스토퍼와 각 테스트 튜브를 흔들어.
- 흐림 또는 침전물의 첫 징후가 나타나는 시간을 유의하십시오.
그룹 효과 떠나기:
- 절대 에탄올에서 실버 질산염의 0.1 M 용액의 2mL를 각각 두 개의 시험관에 측정합니다.
- 첫 번째 테스트 튜브에 2-브로모-2-메틸프로판 2 방울을 추가하고 두 번째 테스트 튜브에 2-클로로-2-메틸프로판 2 방울을 넣습니다.
- 스토퍼와 각 테스트 튜브를 흔들어.
- 흐림 또는 침전물의 첫 징후가 나타나는 시간을 유의하십시오.
용매 극성 효과:
- 제1 시험관에 절대 에탄올로 실버 질산염0.1M 용액의 2mL를 측정하고, 2차 시험관에 5% 에탄올/95% 아세톤으로 은 질산염의 0.1M 용액의 2mL를 측정한다.
- 두 테스트 튜브에 2-브로모-2-메틸프로판 2 방울을 추가합니다.
- 스토퍼와 각 테스트 튜브를 흔들어.
- 흐림 또는 침전물의 첫 징후가 나타나는 시간을 유의하십시오.
SN1 요금법 결정:
- 에탄올에서 2-클로로-2-메틸프로판의 0.1 M 용액의 0.5mL을 제1 시험관으로 측정한다.
- 에탄올에서 2-클로로-2-메틸프로판의 0.2 M 용액의 0.5mL을 제2 시험관으로 측정한다.
- 절대 에탄올에 실버 질산염0.1M 의 용액을 두 테스트 튜브에 넣습니다.
- 흐리거나 강수량을 관찰하는 데 걸리는 시간을 신중하게 측정합니다.
- 에탄올의 은 질산염 0.1M 용액의 1.0mL을 제3 시험관으로 측정한다.
- 제4 시험관에, 에탄올에 실버 질산염의 0.1 M 용액의 0.5mL을 측정하고 에탄올의 추가 0.5 mL을 추가합니다.
- 두 테스트 튜브에 0.1 M 2-클로로-2-메틸프로판의 1.0mL을 에탄올에 넣고 흐리거나 강수량을 관찰하는 데 걸리는 시간을 신중하게 측정합니다.
2부: SN2반응 연구
알킬 할리데 구조:
- 아세톤에서 요오드 나트륨 15%의 2mL을 각각 3개의 시험관에 측정합니다.
- 첫 번째 테스트 튜브에 1-브로모부탄 2 방울을 추가합니다.
- 두 번째 테스트 튜브에 2 방울의 브로모부탄을 추가합니다.
- 마지막으로, 최종, 세 번째 테스트 튜브에 2-브로모-2-메틸프로판 2 방울을 추가합니다.
- 스토퍼와 각 테스트 튜브를 흔들어.
- 흐림 또는 침전물의 첫 징후가 나타나는 시간을 유의하십시오.
스티릭 효과:
- 아세톤 용액의 15% 나트륨 요오드 1mL을 각각 두 개의 테스트 튜브에 측정합니다.
- 첫 번째 테스트 튜브에 1-브로모부탄 2 방울을 넣고 두 번째 테스트 튜브에 2 방울의 네펜틸 브로마이드를 추가합니다.
- 스토퍼와 각 테스트 튜브를 흔들어.
- 흐림 또는 침전물의 첫 징후가 나타나는 시간을 유의하십시오.
그룹 효과 떠나기:
- 아세톤 용액의 15% 나트륨 요오드 1mL을 각각 두 개의 테스트 튜브에 측정합니다.
- 첫 번째 테스트 튜브에 1-브로모부탄 2 방울을 넣고 두 번째 테스트 튜브에 1-클로로부탄 2 방울을 추가합니다.
- 스토퍼와 각 테스트 튜브를 흔들어.
- 흐림 또는 침전물의 첫 징후가 나타나는 시간을 유의하십시오.
SN2 요금법 결정:
- 아세톤 용액의 15% 나트륨 요오드제 1.0mL을 두 개의 테스트 튜브로 측정합니다.
- 아세톤에 1-브로모부탄의 1.0M 용액0.1mL을 첫 번째 테스트 튜브에 넣습니다.
- 흐림의 첫 징후를 관찰하는 데 걸리는 시간을 신중하게 측정합니다.
- 두 번째 테스트 튜브에 아세톤에 브로모부탄 1-브로모부탄2.0M 용액의 0.1 mL을 추가합니다.
- 흐림의 첫 징후를 관찰하는 데 걸리는 시간을 신중하게 측정합니다.
- 아세톤에서 1.0 M 1-브로모부탄의 1.0mL을 세 번째 및 네 번째 테스트 튜브로 측정합니다.
- 아세톤 용액에 7.5% 나트륨 요오드의 0.1mL을 제3 시험관에 넣습니다.
- 흐림의 첫 징후를 관찰하는 데 걸리는 시간을 신중하게 측정합니다.
- 네 번째 테스트 튜브에 아세톤 용액에 15% 나트륨 요오드의 0.1 mL을 추가하고 흐림의 첫 징후를 관찰하는 데 걸리는 시간을 신중하게 측정합니다.
Results
1부: SN1반응 연구
알킬 할리데 구조:

그룹 효과 떠나기:

용매 극성 효과:

SN1 요금법 결정:
| 시험관 |
실버 질산염 농도 |
1-브로모부탄 농도 |
강수량까지의 시간 |
| 1 | 0.1 M | 0.1 M | 20 s |
| 2 | 0.1 M | 0.2M | 10 s |
| 3 | 0.1 M | 0.1 M | 20 s |
| 4 | 0.05 M | 0.1 M | 20 s |

2부: SN2반응 연구
알킬 할리데 구조:
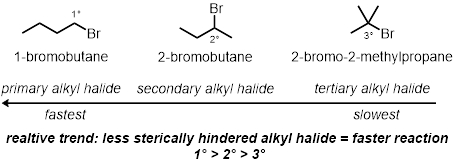
스티릭 효과:
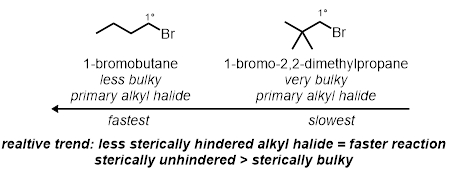
그룹 효과 떠나기:

SN2 요금법 결정:
| 시험관 |
요오드 나트륨 농도 |
1-브로모부탄 농도 |
강수량까지의 시간 |
| 1 | 15% | 1.0 M | 20 s |
| 2 | 15% | 2.0 M | 10 s |
| 3 | 15% | 1.0 M | 20 s |
| 4 | 7.5% | 1.0 M | 40 s |

Application and Summary
이 실험은 뉴클레오필성 대체 반응의 동향을 신속하게 보여주기 위해 고안되었습니다. 이러한 추세를 실험적으로 테스트하면 SN1과 SN2 반응 간의 미묘한 차이를 더 잘 이해하는 데 도움이 됩니다. 화학자들은 반응 상태를 개발하고 최적화하는 법을 배웠습니다. 그것은 모든 반응을 먼저 이해에서 유래: 어떤 속도 또는 반응을 느리게 하 고 어떻게 그것을 활용할 수 있습니까? 최고의 용매, 온도 또는 시약의 농도를 선택하면 반응이 얼마나 빨리 끝날지에 크게 영향을 줄 수 있습니다. 시간이 지남에 따라, 화학자는 속도뿐만 아니라, 선택성과 수율에 관심을 가지고있다. 뉴클레오필성 대체 반응은 합성 문학 전반에 걸쳐 발견될 수 있으므로 배울 수 있는 중요한 반응이다.
이 데모는 뉴클레오필성 대체 반응을 위한 자원으로 사용될 수 있다; 그러나, 그것은 어떤 유기 반응을 공부 하는 방법에 대 한 거친 개요. 반응 조건을 변경하는 방법 (한 번에 하나의 변수를 변경) 자신의 영향을 관찰하는 것은 과학적 방법을 사용하는 기초입니다. 이는 대체 반응 외에 다른 유형의 반응, 예를 들어 방향족 대체 반응 및 아실 대체 반응과 같은 다른 대체 반응에 적용될 수 있다.
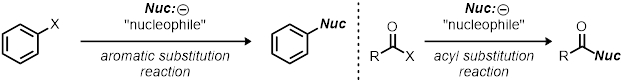
반응은 수율, 선택성 및 속도(효율성)에 최적화되어 있습니다. 화학자는 촉매, 온도, 용매 및 방치 그룹 능력과 같은 반응 파라미터를 변경하는 방식은 크게 반응에 영향을 미칠 수 있습니다. 반응의 운동학을 아는 것은 반응에 대한 귀중한 정보를 빌려 줄 수 있으며, 일반적으로 이것은 반응의 메커니즘을 이해하는 시작입니다.
Tags
건너뛰기...
이 컬렉션의 비디오:

Now Playing
뉴클레오필성 대체
Organic Chemistry II
99.5K Views

유리 제품 청소
Organic Chemistry II
123.5K Views

에이전트 감소
Organic Chemistry II
43.0K Views

그리나드 반응
Organic Chemistry II
149.0K Views

n-부틸리튬 티티네이션
Organic Chemistry II
47.7K Views

딘 스타크 트랩
Organic Chemistry II
100.2K Views

알케네스의 오조노리시스
Organic Chemistry II
67.0K Views

오가노카타리시스
Organic Chemistry II
16.6K Views

팔라듐-촉매 크로스 커플링
Organic Chemistry II
34.3K Views

고체 위상 합성
Organic Chemistry II
41.0K Views

수소 첨가
Organic Chemistry II
49.6K Views

중합
Organic Chemistry II
93.8K Views

녹는점
Organic Chemistry II
149.8K Views

적외선 분광기
Organic Chemistry II
214.6K Views

폴라리미터
Organic Chemistry II
99.9K Views
Copyright © 2025 MyJoVE Corporation. 판권 소유