Method Article
Preparazione di biomassa mesoporosi carbonio con più alto azoto-/ ossigeno-chelante di adsorbimento per cu (II) attraverso pre-pirolisi forno a microonde
In questo articolo
Riepilogo
Qui, presentiamo un protocollo per sintetizzare carbonio dual-drogati mesoporosi azoto/ossigeno da biomassa di attivazione chimica in modi diversi pirolisi seguita da modifiche. Dimostriamo che la pirolisi di microonde benefici del processo di modifica successivi per introdurre contemporaneamente più gruppi di funzionali di azoto e ossigeno sul carbonio.
Abstract
Una tecnica di protezione ambientale-amichevole per la sintetizzazione mesoporosi basati sulla biomassa carbone con alta azoto - attivo / ossigeno-chelante di adsorbimento per cu (II) è proposto. Bagassa impregnata con acido fosforico è utilizzata come precursore. Per pyrolyze il precursore, vengono utilizzate due modalità di riscaldamento separati: forno a microonde pirolisi e pirolisi elettrico-riscaldamento convenzionale. I campioni di carbonio derivato da bagassa risultante vengono modificati con modifica di nitrificazione e riduzione. Azoto (N) / gruppi funzionali di ossigeno (O) sono introdotti contemporaneamente sulla superficie del carbone attivo, migliorando il suo adsorbimento di Cu (II) di agenti complessanti e scambio ionico. Caratterizzazione ed esperimenti di adsorbimento di rame vengono eseguiti per indagare le proprietà fisico-chimiche dei quattro campioni di carbonio preparato e determinare quale metodo di riscaldamento favorisce la successiva modifica per doping di gruppi funzionali N/O. In questa tecnica, basata sull'analisi dei dati di adsorbimento di azoto, spettroscopia a infrarossi trasformata di Fourier ed esperimenti di adsorbimento di batch, è dimostrato che forno a microonde-pirolizzato carbonio ha più siti di difetto e, pertanto, risparmiatrice di tempo efficace a microonde pirolisi contribuisce più specie di N/O al carbonio, anche se conduce ad una minore superficie specifica. Questa tecnica offre una promettente via agli adsorbenti di sintesi con azoto più alto e tenore di ossigeno e una maggiore capacità di adsorbimento di ioni di metalli pesanti nelle applicazioni di bonifica delle acque reflue.
Introduzione
Carbone attivo ha la proprietà di adsorbimento univoco, ad esempio una struttura porosa sviluppata, un'elevata superficie specifica e vari gruppi funzionali superficiali; Pertanto, è impiegato come un adsorbente in acqua trattamento o depurazione1,2,3,4. Oltre a suoi vantaggi fisici, carboni è conveniente e innocui per l'ambiente e relativa materia prima (ad es., biomassa) è abbondante e facilmente ottenuto5,6. Le proprietà fisico-chimiche del carbonio attivato dipendono sui precursori che vengono utilizzati nella sua preparazione e le condizioni sperimentali di attivazione processo7.
Due metodi sono in genere utilizzati per preparare CARBONI: un One-Step e un two-step approccio8. L'approccio di uno stadio di termine si riferisce ai precursori essere carbonizzato e attivate simultaneamente mentre l'approccio in due fasi che si riferisce in modo sequenziale. In considerazione di risparmio energetico e tutela ambientale, l'approccio One-Step è più comodo per la sua bassa temperatura e pressione più esigenti.
Inoltre, l'attivazione fisica e chimica sono utilizzate per migliorare le proprietà tessiturale di carbone attivo. Attivazione chimica possiede vantaggi apparenti sopra l'attivazione fisica a causa della sua bassa temperatura di attivazione, tempo di attivazione più breve, maggiore resa di carbonio e più struttura di poro sviluppata e controllabile in un certo grado9. È stato testato che attivazione chimica può essere eseguita da impregnante biomassa utilizzata come materia prima con H3PO4, ZnCl2o altri prodotti chimici specifici, seguiti da pirolisi per aumentare la porosità del carbone attivo, perché lignocellulosiche componenti della biomassa possono essere facilmente rimosso da un trattamento di riscaldamento successivo, a causa della capacità di deidrogenazione di questi prodotti chimici10,11. Quindi, attivazione chimica notevolmente migliora la formazione dei pori del carbone attivo o migliora le prestazioni adsorbente a contaminanti12. Un attivatore acido è preferito a H3PO4, a causa della sua relativamente bassa domanda di energia, aumentare il rendimento e un minore impatto sul ambiente13.
Pirolisi di forno a microonde ha la superiorità in risparmio di tempo, uniforme riscaldamento interno, efficienza energetica, riscaldamento selettivo, che lo rende un metodo di riscaldamento alternativo a sintesi-attivato del carbonio14,15. Rispetto al riscaldamento elettrico convenzionale, forno a microonde pirolisi può migliorare i processi termochimici e promuovere determinate reazioni chimiche16. Recentemente, studi approfonditi sono concentrati sulla preparazione di carbone attivo di attivazione chimica da biomassa usando un solo passaggio a microonde pirolisi9,17,18,19. Quindi, è notevolmente istruttivo e rispettosi dell'ambiente di sintesi basati sulla biomassa carboni da assistita da microonde attivazione di H3PO4 .
Inoltre, per migliorare l'affinità di adsorbimento del carbone attivo verso specifici ioni di metalli pesanti, è stata proposta la modifica apportata dal doping eteroatomo [N, O, zolfo (S), ecc.] in strutture in carbonio, e questo ha dimostrato di essere un metodo desiderabile 20,21,22,23,24,25,26. Siti difettosi in o ai bordi di uno strato di grafite possono essere sostituiti da eteroatomi per generare gruppi funzionali27. Quindi, modifica di nitrificazione e riduzione vengono utilizzati per modificare i campioni di carbonio risultante per dope gruppi funzionali N/O che svolgono un ruolo cruciale nel coordinare in modo efficiente con metalli pesanti per formare agenti complessanti e scambio ionico28.
Basato sui risultati di cui sopra, vi presentiamo un protocollo per sintetizzare carbonio mesoporosi dual-drogati N/O da biomassa di attivazione chimica e due metodi diversi di pirolisi seguite da modifiche. Questo protocollo determina anche quale metodo di riscaldamento favorisce la conseguente modifica per doping dei gruppi funzionali N/O e, quindi, migliorare le prestazioni di adsorbimento.
Protocollo
1. preparazione di base di bagassa carboni
-
Preparazione del precursore per carboni attivi basati su bagassa
- Risciacquare la bagassa (ricavata da una fattoria nella provincia di Jiangsu, Cina) con acqua deionizzata e mettere i campioni in un forno a 100 ° C per 10 h.
- Schiacciare la bagassa secca con una smerigliatrice e setacciare la polvere attraverso un setaccio di 50 maglie.
- Posto 30 g di polvere di bagassa bene in una soluzione di acido fosforico (H3PO4) di % wt 15 in un rapporto di 1:1 in peso per 24 h. asciugare il composto in un forno a 105 ° C per 6 h. raccogliere il prodotto risultante come il precursore per carboni attivi basati su bagassa (BAC).
-
Pirolisi di elettrico-riscaldamento convenzionale del precursore
- Mettere 15 g del precursore in una barca di quarzo e quindi inserire la barca quarzo in un tubo di vetro al quarzo di un forno elettrico.
- Impostare la velocità di riscaldamento del forno a 5 ° C min-1 per carbonizzare il campione. Quando la temperatura raggiunge i 500 ° C, mantenere la temperatura per 90 min e quindi consentire al campione di carbone attivo risultante raffreddare a temperatura ambiente in azoto. Assicurare un flusso di azoto di 80 mL min-1 con un flussometro di rotore durante il processo di complessivo.
- Triturare e raccogliere l'elettrico-forno-pirolizzato basati su bagassa Carboni (EBAC) in un becher e poi riscaldarlo in un forno di essiccazione a vuoto a 105 ° C per 24 h.
-
Forno a microonde pirolisi del precursore
- Mettete 15 g del precursore nel forno a microonde (con una frequenza di 2,45 GHz).
- Impostare la potenza del forno a microonde a 900 W per pyrolyze il campione per 22 min e garantire il tasso di flusso di azoto a 20 mL min-1 con un flussometro di rotore. La presa d'aria del rotore flussometro è collegata ad una bombola di azoto utilizzando un tubo flessibile, mentre lo scarico è collegato alla presa d'aria del forno a microonde.
- Consentire il carbonio risultante raffreddare a temperatura ambiente in azoto. Triturare e raccogliere il campione di carbonio in un becher e poi aggiungere 300 mL di acido cloridrico (0,1 M). Mescolare la miscela con un agitatore magnetico (a 200 giri/min) per più di 12 ore a temperatura ambiente.
- Il carbonio del filtro di carta da filtro con filtrazione sotto vuoto e sciacquare il campione con acqua deionizzata fino a quando il valore pH dell'acqua di lavaggio è > 6. Asciugare il forno a microonde-pirolizzato basati su bagassa Carboni (MBAC) in un forno di essiccazione a vuoto a 105 ° C per 24 h.
2. modifica di elettrico-forno-pirolizzato basati su bagassa carboni e forno a microonde-pirolizzato basati su bagassa carboni
Nota: La modifica dei due campioni è stata condotta secondo la letteratura29.
-
Nitrificazione
- Miscelare 50 mL di concentrato solforico e 50 mL di acidi nitrico concentrati in un becher a 0 ° C (in un bagno di ghiaccio).
Attenzione: Quando si mescola la miscela di acido solforico concentrato e acido nitrico concentrato, l'acido solforico concentrato deve essere lentamente aggiunto all'acido nitrico concentrato e mescolato con una bacchetta di vetro e raffreddato in tempo. - Aggiungere 10 g di EBAC/MBAC per la soluzione mista. Utilizzare un agitatore magnetico a mescolare il composto per 120 min (a 200 giri/min).
- Filtrare il nitrificato EBAC/MBAC carta da filtro con filtrazione sotto vuoto. Lavare il carbonio con acqua deionizzata fino a quando l'acqua di lavaggio raggiunge pH 6 e poi asciugare in un forno di essiccazione a 90 ° C per 24 h.
- Miscelare 50 mL di concentrato solforico e 50 mL di acidi nitrico concentrati in un becher a 0 ° C (in un bagno di ghiaccio).
-
Modifica riduttiva
- In un pallone a tre-con il collo, aggiungere il 5,05 g di prodotto risultante, 50 mL di acqua deionizzata e 20 mL di soluzione di ammoniaca (15 M). Mescolate il composto per 15 minuti con un agitatore magnetico (a 200 giri/min), poi aggiungere 28 g di Na2S2O4e lasciare la miscela in agitazione a temperatura ambiente per 20 h.
- Montare un condensatore a riflusso nel matraccio e riscaldare la miscela fino a 100 ° C utilizzando un bagno d'olio. Aggiungere 120 mL di CH3COOH (2,9 M) al pallone e lasciare che la miscela sotto agitazione per 5 ore con un agitatore magnetico (a 200 rpm) sotto riflusso.
- Rimuovere il bagno d'olio per consentire la soluzione raffreddare a temperatura ambiente. Filtrare il campione di carbonio e lavarlo con acqua deionizzata fino al soluzione pH > 6. Asciugare l'EBAC/MBAC modificate a 90 ° C e indichiamo come "EBAC-N/MBAC-N".
3. adsorbente caratterizzazione
-
Strutturali c haracterization — Isoterme di adsorbimento/desorbimento di azoto
- Pesare una provetta vuota. Aggiungere un campione di carbonio (~0.15 g) nella provetta.
- Degassare il campione a 110 ° C per 5 h nel vuoto. Pesare la provetta contenente carbonio. Calcolare il peso del campione di carbonio.
- Installare il tubo di campionamento nella zona di prova dell'analizzatore superficie e porosimetria usando azoto liquido per misurarla a-196 ° C30.
-
Caratterizzazione chimica — Trasformata di Fourier spettroscopia infrarossa
- Controllo della temperatura e igrometro e osservare se l'ambiente soddisfa i requisiti: la temperatura dovrebbe essere 16-25 ° C e l'umidità relativa 20% - 50%.
- Rimuovere l'essiccante e parapolvere in un magazzino, campione.
- Essiccare il campione di carbonio e il bromuro di potassio a 110 ° C per 4 h evitare l'effetto dell'acqua sullo spettro. Mescolare il campione di carbonio con bromuro di potassio e quindi utilizzare un meccanismo di stampa per preparare il campione di prova.
- Mettere il campione nell'area test e impostare i parametri del software.
- Salvare gli spettri e togliere il campione. Eseguire un'elaborazione dei dati necessaria per il31di spettri.
4. Cu (II)-esperimenti di adsorbimento
-
Isoterma di adsorbimento
- Mettere 0,05 g di adsorbente in ciascuna delle beute coniche, che contengono 25 mL di una soluzione di CuSO4 (pH 5) con una concentrazione iniziale selezionata (10, 20, 30, 40, 50, 60, 80 e 100 mg L-1). Utilizzare un 0,1 M HNO3 e la soluzione di NaOH 0,1 M per aggiustare il pH di ogni soluzione di rame.
Nota: Una soluzione con la concentrazione iniziale selezionata viene diluita con una soluzione 1 g L-1 CuSO4 , che si compone di un g 3,90625 disciolto di vetriolo azzurro solida utilizzando il vaso con un volume di 1.000 mL. - Montare i coperchi sulle beute e metterli in un agitatore orbitale termostatico (con un tasso di agitazione di 150 giri/min) a 5 ° C/25 ° C/45 ° C per 240 min.
- Utilizzare filtri a membrana 0,22 μm per separare gli adsorbenti dalla soluzione.
- Utilizzare un spettrofotometria di assorbimento atomico della fiamma per determinare la concentrazione di rame del filtrato.
Nota: Tutti gli esperimenti sono stati effettuati in triplice copia e i dati sono stati in media. La capacità di adsorbimento di Cu (II), qe, è stata calcolata come segue: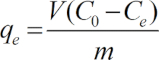 (1)
(1)
Qui,
C0 = la concentrazione iniziale di rame (mg L-1),
Ce = la concentrazione finale (mg L-1),
V = volume della soluzione, e
m = peso del ogni adsorbente (g).
- Mettere 0,05 g di adsorbente in ciascuna delle beute coniche, che contengono 25 mL di una soluzione di CuSO4 (pH 5) con una concentrazione iniziale selezionata (10, 20, 30, 40, 50, 60, 80 e 100 mg L-1). Utilizzare un 0,1 M HNO3 e la soluzione di NaOH 0,1 M per aggiustare il pH di ogni soluzione di rame.
-
Influenza del pH
- Inserire 0,05 g di adsorbente in ciascuna delle beute, contenenti 25 mL di una soluzione di CuSO4 (40 mg L-1) con un pH iniziale selezionata (2, 3, 4, 5, 6 e 7).
- Montare coperchi sulle beute e metterli in un agitatore orbitale termostatico (con un tasso di agitazione di 150 giri/min) a 25 ° C per 24 h raggiungere condizioni di equilibrio di adsorbimento.
- Ripetere il passo 4.1.3-4.1.4.
-
Cinetica di adsorbimento
- Posto 0,25 g di adsorbente in un becher contenente 125 mL di una soluzione di CuSO4 (30 mg L-1 o 100 mg L-1, pH 5) in un bagno di acqua di 25 ° C con magnetico agitazione (a 200 giri/min).
- Utilizzo di pipette per disegnare 5 mL della soluzione quando il tempo di contatto raggiunge 0,5, 1, 2.5, 5, 10, 30, 60, 120 e 180 min.
- Ripetere il passo 4.1.3-4.1.4.
Risultati
Isoterme di adsorbimento/desorbimento di azoto di quattro campioni sono presentate nella Figura 1. Tutte le isoterme di adsorbimento mostrano un rapido aumento in basso P/P0 regione e queste isoterme appartengono al tipo IV (classificazione di IUPAC) dimostrando la loro struttura di poro che consiste di micropori e dominante mesopori32.
I parametri fisici di superficie per tutti i campioni ottenuti dalle isoterme di adsorbimento di azoto sono riportati nella tabella 1. Pirolisi di forno a microonde e modifica che entrambi contribuiscono a una più piccola superficie Brunauer-Emmett-Teller (BET) e totale del poro volume, cambiare la morfologia fisica dei campioni.
Spettri di Fourier transform a infrarossi (FTIR) di quattro campioni sono riportati nella Figura 2. Bande di MBAC a 1167 cm-1 [carbonio (C) - O stretching vibrazione], 1620 cm-1 (C = O stretching vibrazioni), 2852 cm-1 [N - idrogeno (H) allungamento vibrazione], 2922 cm-1 (C - H stretching vibrazione) e 3442 cm-1 (O - H lo stretching vibrazione) sono più intensi rispetto EBAC. Questi possono essere attribuiti per la pirolisi di forno a microonde che contribuiscono di più gruppi funzionali di ossigeno alla superficie di BAC. EBAC-N e MBAC-N, bande intorno 1573 cm-1 e 1400 cm-1 probabile rappresentano C = N e N - H gruppi, rispettivamente. Può essere trovato che i materiali di carbonio modificate hanno ottenuto gruppi funzionali distinti azoto/ossigeno, e il forno a microonde-pirolizzato carbonio ottiene più, che è in conformità con l'analisi elementare, come illustrato nella tabella 1. Può essere speculato che pirolisi di forno a microonde è più adeguata per attivare il precursore e laici radice per ulteriori modifiche di pirolisi elettrico-riscaldamento convenzionale. MBAC-N possiede principalmente dell'idrossile, carbossilico, aminoacidi e immina gruppi funzionali.
La figura 3 Mostra la capacità di adsorbimento dei quattro campioni in condizioni di pH diversi. Gli quattro adsorbenti raggiungono la capacità di adsorbimento ottimale a pH 5, quindi i seguenti esperimenti di adsorbimento vengono tutte effettuati a pH 5. I campioni preparati da pirolisi di forno a microonde ha esibito il migliore capacità di adsorbimento di Cu (II) prima e dopo la modifica, anche se avevano un volume più basso specifico superficie area e poro. In generale, l'adsorbimento di adsorbenti dipende i gruppi funzionali poro struttura e superficie. Pertanto, la capacità di adsorbimento alta del MBAC-N è attribuita ai gruppi di superficie N/O più abbondanti. I risultati confermano che la pirolisi di microonde benefici l'introduzione di follow-up di superficie gruppi funzionali per migliorare la capacità di adsorbimento più di pirolisi elettrico-riscaldamento.
Le isoterme di adsorbimento del MBAC-N su cu (II) a 5 ° C, 25 ° C e 45 ° C sono mostrate in Figura 4a. Le proprietà di adsorbimento dei campioni per cu (II) diventano meglio quando la temperatura aumenta. Confrontando i parametri di isoterma nella tabella 2, è chiaro che il modello di isoterma di Langmuir indica un più elevato coefficiente di correlazione lineare (R2) che è sopra 0,99 (la linea di montaggio in Figura 4b) e l'adsorbimento misurato capacità (q0mea) è identico con il calcolato uno (q0cal). Di conseguenza, il modello è più adatto rispetto ai modelli di isoterma di Freundlich e Temkin, che indica che l'assorbimento di Cu (II) è un processo di adsorbimento chimico33.
Come illustrato nella Figura 4 c, MBAC-N può raggiungere circa il 75% di Cu (II) capacità di adsorbimento di equilibrio entro 15 min, e può raggiungere quasi l'equilibrio di adsorbimento di Cu (II) in circa 50 min a differenti concentrazioni di iniziale. Queste dimostrano che MBAC-N ha proprietà eccellenti di adsorbimento. Come si può vedere dalla tabella 3, il modello di pseudo-second-ordine è superiore rispetto ai modelli Lagergren ed Elovich con R2 = 0.999 (la linea di montaggio in Figura 4D). I risultati sopra confermano che l'adsorbimento di Cu (II) il MBAC-N è Chemiassorbimento. Quindi, il meccanismo di interazione chimica di Cu (II) dal carbonio modificato è proposto nella Figura 5. Tabella 4 mette a confronto la capacità di adsorbimento di Cu (II) di biomassa carbone attivo segnalato in recenti riferimenti34,35,36,37,38. Si trova che MBAC-N ha una maggiore capacità di adsorbimento di altri adsorbenti segnalati nella letteratura, che dimostrano come un promettente adsorbente per la rimozione di Cu (II).

Figura 1: isoterme di adsorbimento/desorbimento di azoto di atomi di carbonio. Il grafico di inserto nella Figura 1 Mostra l'isoterma di adsorbimento/desorbimento di azoto del MBAC-N in una più piccola gamma dell'ordinata. I dati sono stati ottenuti dal software di supporto di superficie e porosimetria analyzer. Questa figura è stata modificata da Wan e Li27. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 2: spettri FTIR di EBAC, EBAC-N, MBAC e MBAC-N. Gli spettri possono confermare le composizioni chimiche e gruppi funzionali superficie dei campioni. Questa figura è stata modificata da Wan e Li27. Clicca qui per visualizzare una versione più grande di questa figura.
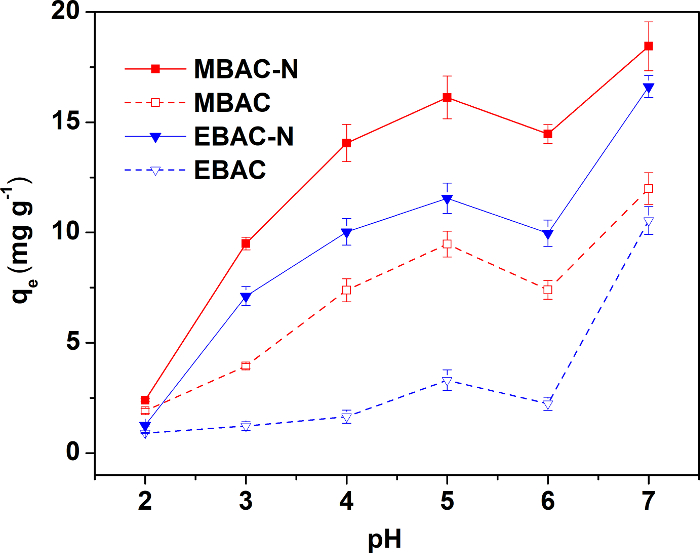
Figura 3: effetto del pH di soluzione sull'adsorbimento di Cu (II). La concentrazione di rame nelle soluzioni è 40 mg L-1. Il test è condotto a 25 ° C e a 150 giri/min per 24 h, per raggiungere l'equilibrio di adsorbimento. Questa figura è stata modificata da Wan e Li27. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 4: analisi di proprietà di adsorbimento rappresentante del MBAC-N. (un) questo pannello mostra le isoterme di adsorbimento di Cu (II) il MBAC-N a 5 ° C, 25 ° C e 45 ° C. (b) questo pannello mostra il risultato di raccordo per adsorbimento rame utilizzando l'isoterma di Langmuir. (c) questo pannello mostra la cinetica di Cu (II) il MBAC-N alle concentrazioni iniziali di 30 mg L-1 e 100 mg L-1. (d) questo pannello mostra il risultato di raccordo per adsorbimento rame a 25 ° C utilizzando il modello di Pseudo-second-ordine. Questa figura è stata modificata da Wan e Li27. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 5: proposto meccanismo per adsorbimento di Cu (II) di carbonio modificato. In questo processo di reazione, l'adsorbimento chimico consiste essenzialmente di scambio ionico e complessanti. Clicca qui per visualizzare una versione più grande di questa figura.
| Adsorbenti | EBAC | EBAC-N | MBAC | MBAC-N |
| Parametri della struttura dei pori | ||||
| Area di superficie di scommessa (m2 g− 1) | 978 | 609 | 543 | 61 |
| Volume totale dei pori (cm3 g− 1) | 1.22 | 0,59 | 0,68 | 0.13 |
| Mesoporosi volume (cm3 g− 1) | 1.09 | 0,47 | 0,58 | 0,11 |
| Media dei pori di dimensione DP (nm) | 4,97 | 3.84 | 5.01 | 8.89 |
| Tasso di mesoporosi (%) | 89.52 | 80.24 | 85,32 | 84.61 |
| Contenuto elementare (wt %) | ||||
| C | 92,23 | 79,31 | 87,28 | 72,44 |
| H | 1.76 | 1.26 | 1.65 | 1.12 |
| N | 0.08 | 4.01 | 0,58 | 5,52 |
| O | 5,82 | 15.15 | 10,33 | 20,54 |
| S | 0,11 | 0,27 | 0.16 | 0,38 |
| Rendimento (%) | 53,35 | / | 57.23 | / |
Tabella 1: caratteristiche strutturali e composizioni elementare di EBAC, EBAC-N, MBAC e MBAC-N. I dati strutturali sono analizzati utilizzando il metodo di scommessa. La percentuale del peso relativo degli elementi è calcolata sulla base secca senza ceneri. Questa tabella è stata modificata da Wan e Li27.
| MBAC-N | ||||
| Modelli di isoterma | Parametri | 5 ° C | 25 ° C | 45 ° C |
| Langmuir | q0cal (mg g− 1) | 20,82 | 24.09 | 25,97 |
| q0mea (mg g− 1) | 20,23 | 23,47 | 25.12 | |
| b (L mg− 1) | 0,73 | 0.51 | 0,49 | |
| R2 | 0,999 | 0,996 | 0.995 | |
| Freundlich | KF (L mg− 1) | 8.802 | 9.65 | 10.56 |
| n | 3,937 | 3.902 | 4.032 | |
| R2 | 0.907 | 0,967 | 0,987 | |
| Temkin | UnaT (L mg− 1) | 29,57 | 32,3 | 49,8 |
| B (L mg− 1) | 2.94 | 3.19 | 3.16 | |
| R2 | 0,969 | 0.985 | 0,955 | |
Tabella 2: parametri di isoterma di Cu (II) il MBAC-N a diverse temperature. I parametri di misura sono da modelli di adsorbimento di Langmuir e Freundlich Temkin linearizzati. Questa tabella è stata modificata da Wan e Li27.
| MBAC-N | |||
| Modelli cinetici | Parametri | 30 mg L− 1 | 100 mg L− 1 |
| Lagergren | k1 (min− 1) | 0,037 | 0,045 |
| R2 | 0,714 | 0.934 | |
| qe, mea (mg g− 1) | 13,39 | 22,69 | |
| Pseudo-second-ordine | qe, cal (mg g− 1) | 13,44 | 23,25 |
| k2 (g (mg min)− 1) | 0.08676 | 0.03031 | |
| R2 | 0,999 | 0,999 | |
| qe, mea (mg g− 1) | 13,39 | 22,69 | |
| Elovich | ΑE (g (mg min)− 1) | 379.73 | 312.25 |
| ΒE (mg g− 1) | 0.738 | 0.411 | |
| R2 | 0.799 | 0.901 | |
Tabella 3: parametri cinetici di Cu (II) il MBAC-N a differenti concentrazioni iniziali. I parametri di misura sono da linearizzato Lagergren, Pseudo-second-ordine e modelli di Elovich. Questa tabella è stata modificata da Wan e Li27.
| Adsorbenti | pH | qe (mg g− 1) | Riferimenti |
| A base di legno carbone attivo granulare | 5.5 | 6.016 | 34 |
| Frutto di Baobab shell-derivato carbonio attivato | 6 | 3.0833 | 35 |
| Pietra verde oliva AC (COSAC) | 5 | 17.08 | 36 |
| Carbonfrom attivato Data pietre | 5.5 | 18,68 | 37 |
| Gusci di noce basato su carbone attivo | 5 | 9.3 | 38 |
| Al plasma per volta carboni | 21,4 | ||
| MBAC-N | 5 | 25.12 | Questo studio |
Tabella 4: confronto tra la capacità di adsorbimento di Cu (II) su diversi adsorbenti. La capacità del carbone attivo per rimuovere cu (II) è significativamente influenzata dal pH della soluzione, quindi la capacità di adsorbimento dei materiali di carbonio derivato dalla biomassa di contrasto dovrebbe essere ottenuta vicino pH 5.
Discussione
In questo protocollo, una delle fasi critiche è la corretta preparazione di carbonio mesoporosa con proprietà fisico-chimiche di meglio da un approccio One-Step, dove necessario determinare le condizioni sperimentali ottimali. Così, in un precedente studio28, abbiamo effettuato esperimenti di pirolisi a microonde matrice ortogonale, considerando l'effetto del rapporto impregnazione della bagassa e acido fosforico, tempo di pirolisi, forno a microonde potenza e tempo di asciugatura. Inoltre, grande cura deve essere presa nel noioso Cu (II)-esperimenti di adsorbimento, soprattutto quando il valore del pH della soluzione è regolato, perché il valore del pH ha una grande influenza su cu (II) rimozione di carbone attivo (Figura 3). È indispensabile per verificare l'effettiva concentrazione di rame di CuSO4 soluzione con una concentrazione iniziale definita e utilizzare questo valore come C0 nell'equazione (1).
Una più grande superficie specifica e maggiore volume dei pori del carbone attivo di biomassa può essere ottenuti dall'attivazione chimica. Tuttavia, la superficie specifica e il volume totale dei pori sia diminuire durante il processo di pirolisi e modifiche successivo, che è probabilmente dovuto il crollo e l'ostruzione dei pori27, con conseguente riduzione della capacità di adsorbimento. Di conseguenza, ulteriore lavoro è tenuto a redigere basati sulla biomassa mesoporosi carbonio con sia un'elevata area superficiale e abbondanti gruppi funzionali.
Forno a microonde pirolisi viene verificata che per più adeguatamente sintetizzare carbonio mesoporosi basati sulla biomassa con un più elevato adsorbimento di azoto/ossigeno-chelante per cu (II), che ha molti vantaggi rispetto ai metodi di riscaldamento convenzionale ampiamente usato. Tuttavia, non è possibile controllare con precisione la temperatura istantanea durante il processo di pirolisi di forno a microonde. La biomassa è un materiale di assorbimento di buon forno a microonde, cui la temperatura può aumentare rapidamente sotto l'effetto di un forno a microonde. Chiaramente, lavoro futuro deve esaminare come la temperatura di pirolisi colpisce le proprietà fisico-chimiche del carbonio derivato dalla biomassa.
Una descrizione dettagliata del meccanismo di modifica è oltre la portata di questo articolo, ma può essere trovato in precedenza letteratura pubblicata27. L'importanza potenziale di modificazione di nitrificazione e riduzione che può instaurare efficacemente più gruppi funzionali di N/O contemporaneamente sulla superficie dei campioni di carbonio è la pena di apprezzare. Tuttavia, il processo di modifica contiene numerose fasi sperimentali e l'utilizzazione di acido forte concentrato pericoloso. Un metodo di modifica più semplice e più efficace dell'azoto/ossigeno può essere testato e adottato in ulteriori studi.
Ci hanno dimostrato un metodo efficiente rispettosi dell'ambiente per la preparazione di carbonio derivato dalla biomassa mesoporosi tramite pirolisi forno a microonde e dope gruppi N/O contemporaneamente sul carbonio utilizzando un percorso di nitrificazione e riduzione. Tali carboni di N/O dual-drogati possiede una maggiore capacità di adsorbimento di ioni di metalli pesanti in soluzione acquosa, che è applicabile per il risanamento delle acque reflue. Ci aspettiamo che questo protocollo fornirà idee per la preparazione rapida di alto-adsorbente carbonio da biomassa da pirolisi a microonde risparmio di tempo, efficace e sarà ottimizzato in futuro.
Divulgazioni
Gli autori non hanno nulla a rivelare.
Riconoscimenti
Gli autori riconoscono la fondamentale ricerca fondi per le Università centrale della Cina (No.KYZ201562), China post-dottorato Science Fund (n ° 2014 M 560429) e il piano di ricerca e sviluppo di chiave della provincia di Jiangsu (No. BE2018708).
Materiali
| Name | Company | Catalog Number | Comments |
| All chemicals and reagents (phosphoric acid, etc.) | Nanjing Chemical Reagent Co., Ltd | Analytical grade | |
| Electric furnace | Luoyang Bolaimaite Experiment Electric Furnace Co., Ltd | ||
| Microwave oven | Nanjing Yudian Automation Technology Co., Ltd | 2.45 GHz frequency | |
| Surface-area and porosimetry analyzer | Beijing Gold APP Instrument Co., Ltd | Vc-Sorb 2800TP | |
| Fourier transform infrared (FTIR) spectrometer | Nicolet | 6700 | |
| Flame atomic absorption spectrophotometry | Beijing Purkinje General Instrument Corporation | A3 | |
| Element Analyzer | Germany Heraeus Co. | CHN-O-RAPID |
Riferimenti
- Saleh, T. A., Gupta, V. K. Processing methods, characteristics and adsorption behavior of tire derived carbons: a review. Advances in Colloid & Interface Science. 211, 93(2014).
- Mohammadi, N., Khani, H., Gupta, V. K., Amereh, E., Agarwal, S. Adsorption process of methyl orange dye onto mesoporous carbon material-kinetic and thermodynamic studies. Journal of Colloid & Interface Science. 362 (2), 457(2011).
- Saleh, T. A., Gupta, V. K. Column with CNT/magnesium oxide composite for lead(II) removal from water. Environmental Science & Pollution Research. 19 (4), 1224-1228 (2012).
- Asfaram, A., Ghaedi, M., Agarwal, S., Tyagi, I., Kumargupta, V. Removal of basic dye Auramine-O by ZnS:Cu nanoparticles loaded on activated carbon: optimization of parameters using response surface methodology with central composite design. RSC Advances. 5 (24), 18438-18450 (2015).
- Gupta, V. K., Saleh, T. A. Sorption of pollutants by porous carbon, carbon nanotubes and fullerene- an overview. Environmental Science and Pollution Research. 20 (5), 2828-2843 (2013).
- Ahmaruzzaman, M., Gupta, V. K. Rice Husk and Its Ash as Low-Cost Adsorbents in Water and Wastewater Treatment. Industrial & Engineering Chemistry Research. 50 (24), 13589-13613 (2011).
- Ahmed, M. J., Theydan, S. K. Adsorption of cephalexin onto activated carbons from Albizia lebbeck seed pods by microwave-induced KOH and K2CO3 activations. Chemical Engineering Journal. 211 (22), 200-207 (2012).
- Liew, R. K., et al. Production of activated carbon as catalyst support by microwave pyrolysis of palm kernel shell: a comparative study of chemical versus physical activation. Research on Chemical Intermediates. , 1-17 (2018).
- Lam, S. S., et al. Microwave-assisted pyrolysis with chemical activation, an innovative method to convert orange peel into activated carbon with improved properties as dye adsorbent. Journal of Cleaner Production. 162, 1376-1387 (2017).
- Jin, H., Wang, X., Gu, Z., Polin, J. Carbon materials from high ash biochar for supercapacitor and improvement of capacitance with HNO3 surface oxidation. Journal of Power Sources. 236, 285-292 (2013).
- Chen, H. Research Methods for the Biotechnology of Lignocellulose. Biotechnology of Lignocellulose: Theory and Practice. , Springer. Dordrecht, Netherlands. 403-510 (2014).
- Sayğılı, H., Güzel, F. High surface area mesoporous activated carbon from tomato processing solid waste by zinc chloride activation: process optimization, characterization and dyes adsorption. Journal of Cleaner Production. 113, 995-1004 (2016).
- Cao, Q., Xie, K. C., Lv, Y. K., Bao, W. R. Process effects on activated carbon with large specific surface area from corn cob. Bioresource Technology. 97 (1), 110-115 (2006).
- Xiao, X., et al. Adsorption behavior of phenanthrene onto coal-based activated carbon prepared by microwave activation. Korean Journal of Chemical Engineering. 32 (6), 1129-1136 (2015).
- Ge, X., et al. Adsorption of naphthalene from aqueous solution on coal-based activated carbon modified by microwave induction: Microwave power effects. Chemical Engineering & Processing Process Intensification. 91, 67-77 (2015).
- Yao, S., et al. Removal of Pb(II) from water by the activated carbon modified by nitric acid under microwave heating. Journal of Colloid and Interface Science. 463, 118-127 (2016).
- Ali, A., Idris, R. Utilization Of Low-cost Activated Carbon From Rapid Synthesis Of Microwave Pyrolysis For WC Nanoparticles Preparation. Advanced Materials Letters. 08 (1), 70-76 (2016).
- Puchana-Rosero, M. J., et al. Microwave-assisted activated carbon obtained from the sludge of tannery-treatment effluent plant for removal of leather dyes. Colloids and Surfaces A: Physicochemical and Engineering Aspects. 504, 105-115 (2016).
- Du, Z. L., Zheng, T., Wang, P., Hao, L. L., Wang, Y. X. Fast microwave-assisted preparation of a low-cost and recyclable carboxyl modified lignocellulose-biomass jute fiber for enhanced heavy metal removal from water. Bioresource Technology. 201, 41-49 (2016).
- Ge, X., et al. Microwave-assisted modification of activated carbon with ammonia for efficient pyrene adsorption. Journal of Industrial & Engineering Chemistry. 39, 27-36 (2016).
- Ghaedi, M., et al. Modeling of competitive ultrasonic assisted removal of the dyes - Methylene blue and Safranin-O using Fe3O4 nanoparticles. Chemical Engineering Journal. 268, 28-37 (2015).
- Gupta, V. K., Nayak, A. Cadmium removal and recovery from aqueous solutions by novel adsorbents prepared from orange peel and Fe2O3 nanoparticles. Chemical Engineering Journal. 180 (3), 81-90 (2012).
- Robati, D., et al. Removal of hazardous dyes-BR 12 and methyl orange using graphene oxide as an adsorbent from aqueous phase. Chemical Engineering Journal. 284 (7), 687-697 (2016).
- Ali, I., Alothman, Z. A., Sanagi, M. M. Green Synthesis of Iron Nano-Impregnated Adsorbent for Fast Removal of Fluoride from Water. Journal of Molecular Liquids. 211, 457-465 (2015).
- Gupta, V. K., Kumar, R., Nayak, A., Saleh, T. A., Barakat, M. A. Adsorptive removal of dyes from aqueous solution onto carbon nanotubes: A review. Advances in Colloid & Interface Science. 193 (6), 24(2013).
- Mittal, A., Mittal, J., Malviya, A., Gupta, V. K. Adsorptive removal of hazardous anionic dye "Congo red" from wastewater using waste materials and recovery by desorption. Journal of Colloid and Interface Science. 340 (1), 16-26 (2009).
- Wan, Z., Li, K. Effect of pre-pyrolysis mode on simultaneous introduction of nitrogen/oxygen-containing functional groups into the structure of bagasse-based mesoporous carbon and its influence on Cu(II) adsorption. Chemosphere. 194, 370-380 (2018).
- Li, K., Li, J., Lu, M., Li, H., Wang, X. Preparation and amino modification of mesoporous carbon from bagasse via microwave activation and ethylenediamine polymerization for Pb(II) adsorption. Desalination and Water Treatment. 57 (50), 24004-24018 (2016).
- Yantasee, W., et al. Electrophilic Aromatic Substitutions of Amine and Sulfonate onto Fine-Grained Activated Carbon for Aqueous-Phase Metal Ion Removal. Separation Science and Technology. 39 (14), 3263-3279 (2004).
- Quantachrome Autosorb-1 Series User's Guide. , Available from: http://www.umich.edu/~techserv/gasAdsorp/Autosorb-1.pdf (2007).
- Nicolet FT-IR User's Guide. , Available from: http://chemistry.unt.edu/~verbeck/LIMS/Manuals/6700_User.pdf (2015).
- Li, Y. B., Li, K. Q., Wang, X. H., Li, J. Ethylenediamine Modification of Hierarchical Mesoporous Carbon for the Effective Removal of Pb (II) and Related Influencing Factors. International Journal of Material Science. 6 (1), 58-65 (2016).
- Georgakopoulos, E., Santos, R. M., Chiang, Y. W., Manovic, V. Two-way Valorization of Blast Furnace Slag: Synthesis of Precipitated Calcium Carbonate and Zeolitic Heavy Metal Adsorbent. Journal of Visualized Experiments. (120), e55062(2017).
- Loganathan, P., et al. Modelling equilibrium adsorption of single, binary, and ternary combinations of Cu, Pb, and Zn onto granular activated carbon. Environmental Science & Pollution Research. (15), 1-12 (2018).
- Vunain, E., Kenneth, D., Biswick, T. Synthesis and characterization of low-cost activated carbon prepared from Malawian baobab fruit shells by H3PO4 activation for removal of Cu(II) ions: equilibrium and kinetics studies. Applied Water Science. 7 (8), 4301-4319 (2017).
- Bohli, T., Ouederni, A., Villaescusa, I. Simultaneous adsorption behavior of heavy metals onto microporous olive stones activated carbon: analysis of metal interactions. Euro-Mediterranean Journal for Environmental Integration. 2 (1), 19(2017).
- Bouhamed, F., Elouear, Z., Bouzid, J., Ouddane, B. Multi-component adsorption of copper, nickel and zinc from aqueous solutions onto activated carbon prepared from date stones. Environmental Science & Pollution Research. 23 (16), 1-6 (2016).
- Wu, L., et al. Surface modification of phosphoric acid activated carbon by using non-thermal plasma for enhancement of Cu(II) adsorption from aqueous solutions. Separation & Purification Technology. 197, (2018).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon