Method Article
Tomografía optoacústica multiespectral para imágenes funcionales en investigación vascular
En este artículo
Resumen
El presente protocolo describe la adquisición de imágenes optoacústicas multiespectrales de vasculatura cutánea humana in vivo . Estos incluyen la cuantificación de hemoglobina y melanina, considerados como cromóforos de interés para el análisis funcional.
Resumen
El deterioro microcirculatorio ha sido reconocido en varios procesos de enfermedad, subyacente a este tema creciente dentro de la investigación vascular. En los últimos años, el desarrollo de sistemas de imagen en vivo ha marcado el ritmo (analítico) tanto en la investigación básica como en la clínica, con el objetivo de crear nuevos instrumentos capaces de proporcionar puntos finales cuantificables en tiempo real con interés y aplicación clínica. La espectroscopia de infrarrojo cercano (NIRS), la tomografía por emisión de positrones (PET), la tomografía computarizada (TC) y la resonancia magnética (RM) están disponibles, entre otras técnicas, pero el costo, la resolución de la imagen y el contraste reducido se reconocen como desafíos comunes. La tomografía optoacústica (OT) ofrece una nueva perspectiva sobre la imagen funcional vascular, combinando capacidades de absorción óptica y resolución espacial de última generación (desde resolución óptica micrométrica hasta resolución acústica milimétrica) con profundidad tisular. En este estudio, probamos la aplicabilidad de la tomografía optoacústica multiespectral (MSOT) para imágenes funcionales. El sistema utiliza un oscilador paramétrico óptico sintonizable (OPO) bombeado por un láser Nd: YAG, que proporciona pulsos de excitación detectados por una sonda 3D en longitudes de onda de 680 nm a 980 nm. Las imágenes obtenidas del antebrazo humano se reconstruyeron a través de un algoritmo específico (suministrado dentro del software del fabricante) basado en la respuesta de cromóforos específicos. La hemoglobina oxigenada máxima (HbO2 máxima) y la hemoglobina desoxigenada (Hb máxima), la hemoglobina total (HbT) y la saturación media de oxígeno (mSO2) a la densidad vascular (μVu), las distancias promedio entre unidades (ζAd) y el volumen sanguíneo capilar (mm3) se pueden medir utilizando este sistema. El potencial de aplicabilidad encontrado con este sistema OT es relevante. Los desarrollos de software en curso seguramente mejorarán la utilidad de este sistema de imágenes.
Introducción
Las enfermedades cardiovasculares son las principales causas recurrentes de muerte en todo el mundo y representan una enorme carga para cualquier sistema de salud 1,2. La tecnología ha contribuido en gran medida a la expansión de nuestra comprensión de la fisiopatología cardíaca y vascular fundamental, proporcionando herramientas de diagnóstico más precisas y la posibilidad de detección temprana de enfermedades y un manejo más efectivo. Las técnicas de imagen ofrecen la posibilidad de medir no solo el rendimiento cardíaco y de los vasos principales, sino también, en una escala mucho menor, calcular la densidad capilar, la perfusión local y el volumen, y la disfunción endotelial, entre otras características. Estas tecnologías han ofrecido los primeros conocimientos cuantitativos sobre biología vascular con aplicación clínica directa. Los cambios en la densidad capilar, la reducción de la perfusión local o la oclusión probablemente corresponden a una condición isquémica, lo que ayuda a explicar el creciente papel de la imagen, convirtiéndose en una herramienta indispensable en la investigación y práctica cardiovascular 3,4,5.
En los últimos años, la imagen funcional ha marcado constantemente el ritmo de la innovación tecnológica, con ultrasonido (EE. UU.), espectroscopía de infrarrojo cercano (NIRS), tomografía por emisión de positrones (PET), tomografía computarizada (TC) e imágenes de resonancia magnética (MRI) como algunos ejemplos bien conocidos. Sin embargo, múltiples preocupaciones limitan su aplicación, desde el costo y la seguridad del paciente (así como la comodidad) hasta el contraste de imagen y la resolución 6,7. La tomografía optoacústica (OT) ha surgido recientemente como una nueva dirección en la investigación vascular óptica. Esta tecnología, centrada en la detección de ondas ultrasónicas generadas por la expansión termoelástica del tejido impactado con pulsos láser ultracortos, se conoce desde hace algún tiempo 6,8. Esta reacción física de desarrollo de calor y expansión tisular evoca una señal acústica detectada por un transductor de ultrasonido. El uso de pulsos de luz desde el visible hasta el infrarrojo cercano y la ausencia de una señal acústica de fondo benefician la profundidad de resolución. El contraste detectado resulta de los cromóforos más importantes presentes (hemoglobina o melanina). En comparación con otras tecnologías, OT tiene las ventajas de (1) no necesitar contraste (imágenes sin etiqueta), (2) mejor contraste y resolución con menos artefactos que la ecografía, y (3) menor precio, y adquisición más rápida y facilidad de operación 6,9,10,11.
La tomografía optoacústica multiespectral (MSOT) se encuentra entre la generación más reciente de instrumentos OT. Construido con un oscilador paramétrico óptico sintonizable (OPO) bombeado por un láser Nd: YAG que proporciona pulsos de excitación, una imagen 3D se adquiere mediante señales resueltas en el tiempo detectadas a partir de pulsos de excitación ultrasónica de alta frecuencia en longitudes de onda de 680 nm a 980 nm con una tasa de repetición de hasta 50 Hz12. La plataforma de imágenes optoacústicas proporciona la cuantificación de diferentes cromóforos en profundidad (tan solo 15 mm). Variables como HbO2, Hb y melanina son fácilmente accesibles. Otras variables de interés, como la hemoglobina oxigenada máxima (HbO máxima2) y la hemoglobina desoxigenada (Hb máxima), también están disponibles. Los algoritmos de reconstrucción del software del fabricante permiten el cálculo de otras variables como la densidad vascular (μVu), la distancia media entre unidades (ζAd) y el volumen capilar (mm3).
El presente estudio explora los aspectos operativos esenciales de este nuevo sistema para comprender mejor sus aspectos prácticos y posibles aplicaciones en la investigación preclínica cardiovascular.
Protocolo
El protocolo experimental fue aprobado previamente por el Comité de Ética de la Facultad de Ciencias de la Salud de la Universidad (EC. ECTS/P10.21). Los procedimientos respetaron plenamente los principios de buenas prácticas clínicas definidos para la investigación en humanos13. Se eligió de la comunidad universitaria una muestra conveniente de seis participantes sanos de ambos sexos (n = 3 por sexo) con una edad media de 32,8 ± 11,9 años. Se requirió que los participantes seleccionados fueran normotensos, no fumadores y libres de cualquier medicamento o suplemento alimenticio. También se registraron la presión arterial, la frecuencia cardíaca y el índice de masa corporal. Todos los participantes fueron informados previamente de los objetivos y la duración del estudio y dieron su consentimiento informado por escrito.
NOTA: Este estudio se realizó utilizando MSOTAcuity (ver Tabla de materiales), en adelante referida como la plataforma de imágenes optoacústicas.
1. Preparación para la adquisición
Nota: En la descripción experimental que sigue, los comandos de pantalla están en negrita.
- Carga de la información del sujeto: Encienda el equipo de imágenes optoacústicas. Mientras el equipo se está calentando, presente la información del participante. La ventana principal de bienvenida del software se abre a la descripción general de escaneo. Introduzca los datos (incluido el nombre, la denominación del estudio, los datos personales y cualquier observación relevante) después de hacer clic en ID del paciente y finalice la solicitud presionando Seleccionar.
- Selección preestablecida: asegúrese de que aparezca el mensaje Laser is Ready (El láser está listo ) en la pantalla del equipo. Después del tiempo de calentamiento, la barra de estado del láser en la pantalla del equipo debe cambiar de Laser Standby a Laser is Ready. Para este protocolo, el ajuste preestablecido está diseñado para los cromóforos Hb, HbO2 y melanina. Después de seleccionar el ajuste preestablecido correcto, se probará la potencia del láser.
- En este punto, asegúrese de que haya un mensaje en la pantalla que recuerde a todos los participantes en la sala que apliquen gafas de seguridad láser. Presione el pedal del interruptor láser (encendido) y espere la autocomprobación de potencia del láser. Después de unos segundos, aparece una ventana con el estado actual del láser con un informe de chequeo. Suelte esta ventana pulsando el botón OK disponible.
NOTA: La plataforma de imágenes optoacústicas utiliza un láser Nd: YAG, considerado un láser de clase 4 particularmente peligroso para el ojo humano. Por lo tanto, este láser debe manejarse con el cuidado adecuado.
PRECAUCIÓN: No se debe realizar ninguna adquisición sin asegurarse de que se implementen todos los procedimientos de seguridad, incluida la protección ocular adecuada.
2. Posicionamiento y adquisición de imágenes
- Aclimatar al participante al ambiente del laboratorio (21 °C ± 1 °C; 40%-60% de humedad relativa), eligiendo una posición cómoda para minimizar el movimiento innecesario. Asegúrese de que el área a escanear se limpie previamente.
NOTA: Se recomienda la recomendación del fabricante de limpiar el área a fotografiar con una solución de etanol/agua al 70%. Además, para una mejor adquisición de imágenes, se sugiere la eliminación del vello (cuando corresponda). - Soporte de sonda y estabilización de imagen
- Aplique una capa delgada de gel de ultrasonido a la copa 3D. La estabilización de imagen requiere sostener la copa 3D en la posición de imagen deseada. Coloque y estabilice un brazo bloqueable para el área de interés. El brazo utilizado en este estudio fue diseñado internamente y construido con componentes de perfil de aluminio (Figura 1).
- Después de colocar la copa 3D en el área de interés, bloquee parcialmente el bloqueo del brazo estabilizador para la adquisición de imágenes.
NOTA: La calidad y la aplicación uniforme del gel de ultrasonido es crítica; La presencia de burbujas de aire puede comprometer la definición de la imagen.
- Adquisición de imágenes para condiciones dinámicas, mediante la maniobra de hiperemia reactiva postoclusiva (PORH), en la pestaña del menú Examen .
- Adquiera el escaneo de control de línea base. Después de encontrar un campo de visión para la obtención de imágenes, con el manguito de presión arterial desinflado en su lugar, bloquee de forma segura el brazo de posicionamiento de la copa 3D.
- Aplique una presión mínima en el sitio de imágenes, ya que las presiones más altas podrían comprometer las lecturas. Empuje el ajuste preestablecido predeterminado del fabricante Hb, HbO 2 y melanina que mide simultáneamente los cromóforos de Hb, HbO2 y melanina.
PRECAUCIÓN: Es obligatorio proteger los ojos con gafas de seguridad adecuadas durante la operación.
NOTA: Los fototipos de piel IV a VI (piel oscura) son propensos a la lectura errónea, lo que requiere una imagen de control de referencia para su posterior procesamiento. El uso de gafas de seguridad durante la adquisición de imágenes (cuando el láser está activo) solo permite que el ojo humano reconozca los colores amarillo y azul. Los colores se pueden editar durante el procesamiento de imágenes. - Seleccione el área anatómica para la adquisición de imágenes de referencia. Para fines exploratorios, se recomienda el antebrazo ventral. Proceda presionando el pedal del pedal láser.
NOTA: El botón de la pantalla táctil etiquetado Ver (color amarillo), que muestra la imagen en vivo en la pantalla cuando se presiona. El estado de estabilidad de la imagen se muestra como una barra gris en el centro de la pantalla táctil, lo que indica la estabilidad de la sonda 3D.- Cuando se maximice la estabilidad de la imagen, tome (o capture) una instantánea del área presionando el botón Instantánea en la pantalla táctil. Cada escaneo adquirirá 10-12 fotogramas a una profundidad acústica de 150 mm para cada longitud de onda definida dentro del preajuste durante un tiempo de adquisición de 2 s. Este escaneo de adquisición de línea base incluirá un total de 30-36 cuadros.
NOTA: Se recogen 10 fotogramas para cada cromóforo detectado (Hb,HbO2 y melanina) con una profundidad máxima de 15 mm. - Continúe presionando el pedal del pedal láser para la adquisición continua de video y preste atención al botón Ver (de color amarillo) en la pantalla táctil. Aparecerá la imagen estabilizada. Presione Grabar (color azul) para comenzar la grabación de imágenes en vivo.
- Detenga la grabación pulsando el botón Detener (de color negro). La plataforma de imágenes optoacústicas detendrá la grabación y renderizará automáticamente el video en modo de vista previa.
- Cuando se maximice la estabilidad de la imagen, tome (o capture) una instantánea del área presionando el botón Instantánea en la pantalla táctil. Cada escaneo adquirirá 10-12 fotogramas a una profundidad acústica de 150 mm para cada longitud de onda definida dentro del preajuste durante un tiempo de adquisición de 2 s. Este escaneo de adquisición de línea base incluirá un total de 30-36 cuadros.
- Mediciones dinámicas (ilustración PORH): ajuste el manguito de presión al brazo del paciente por encima del codo para ilustrar esta maniobra. Infle el manguito con presión suprasistólica (~200 mmHg) y proceda de acuerdo con los pasos 2.3.1 a 2.3.3.1 para adquirir la vasculatura fotografiada bajo presión.
- Para adquirir un video para evaluar el impacto de la liberación de presión en la vasculatura de la imagen, abra la válvula de presión mientras adquiere el video como en 2.3.3.2. Como antes, siga la imagen en vivo en la pantalla.
NOTA: Para ejecutar esta maniobra, la presión suprasistólica debe mantenerse durante 1-5 min; Es importante tener en cuenta que esta presión puede inducir diferentes grados de tolerancia e incomodidad en el paciente. Este aspecto debe ser manejado cuidadosamente durante los experimentos.
3. Protocolo de análisis de imágenes
- Copie los escaneos grabados en una carpeta seleccionada/dedicada para realizar copias de seguridad y análisis adicionales en una estación de trabajo informática independiente utilizando el software analítico dedicado del fabricante. Cada escaneo se almacena por tiempo de adquisición y ordenado por el programa en una carpeta de estudio con un código en ejecución.
NOTA: Se recomienda encarecidamente una copia de seguridad. Trabajar directamente con los datos sin procesar grabados es posible, pero se desaconseja encarecidamente, ya que cualquier posible bloqueo del disco duro podría dañar los datos sin procesar. - Abra el programa de análisis en el equipo de la estación de trabajo. Elija el menú del programa > Abrir estudio para importar archivos y acceder a los escaneos de copia de seguridad. Abra el estudio y desplácese hasta la parte inferior de la carpeta (con escaneos grabados) para encontrar archivos con un archivo . NOD extensión. Este es el único tipo de archivo reconocido por el software para abrir un estudio.
NOTA:. Los archivos NOD se nombran automáticamente con un número de ejecución dado a cada estudio y no llevan información del paciente en el nombre del archivo. - Para la reconstrucción de imágenes, abra el módulo de análisis de imágenes accediendo al menú del software > procesamiento avanzado.
- Asegúrese de que las pestañas del flujo de trabajo del programa estén visibles (de color negro) en la barra de menú superior (Figura complementaria 1): Menú; Descripción general del análisis; Reconstrucción; Corrección de la fluencia; Desmezcla espectral; Visualización y análisis. Durante el análisis, cualquier pestaña de flujo de trabajo activada es de color azul.
NOTA: Si no se abre el procesamiento avanzado , el software solo muestra Descripción general del escaneo y Visualización y análisis.
- Asegúrese de que las pestañas del flujo de trabajo del programa estén visibles (de color negro) en la barra de menú superior (Figura complementaria 1): Menú; Descripción general del análisis; Reconstrucción; Corrección de la fluencia; Desmezcla espectral; Visualización y análisis. Durante el análisis, cualquier pestaña de flujo de trabajo activada es de color azul.
- Reconstruya la imagen a través de la pestaña Reconstrucción del software. Seleccione los escaneos para reconstruir desde el lado izquierdo del menú principal del programa. Los escaneos cargados aparecen en el lado derecho de la pantalla. Deje las seis longitudes de onda de emisión optoacústica predeterminadas (700, 730, 760, 800, 850 y 900 nm), ya que incluyen la señal optoacústica máxima para HbO2 a 900 nm, para Hb a 760 nm y melanina a 700 nm.
- Realice la reconstrucción del escaneo utilizando el icono en el lado derecho. Siga el flujo de trabajo del programa seleccionando el ajuste preestablecido Escanear y el Campo de visión (resolución). La información se presenta en la esquina superior izquierda de la pantalla principal. Ajuste la velocidad del sonido para ajustar el enfoque del escaneo (Figura complementaria 2). El panel Reconstrucción también muestra el número de fotogramas de cada escaneo adquirido y permite analizar la selección de las repeticiones (si es necesario).
NOTA: Cada escaneo se carga con una velocidad de sonido predeterminada de -90, que debe ser ajustada por el usuario. La velocidad del sonido también se puede ajustar automáticamente con una función de enfoque automático (AF).
- Realice la reconstrucción del escaneo utilizando el icono en el lado derecho. Siga el flujo de trabajo del programa seleccionando el ajuste preestablecido Escanear y el Campo de visión (resolución). La información se presenta en la esquina superior izquierda de la pantalla principal. Ajuste la velocidad del sonido para ajustar el enfoque del escaneo (Figura complementaria 2). El panel Reconstrucción también muestra el número de fotogramas de cada escaneo adquirido y permite analizar la selección de las repeticiones (si es necesario).
- Presione el botón Reconstruir escaneos en la parte superior de la pantalla para avanzar a la reconstrucción de escaneo. Aparecerá un panel temporal con el mensaje Procesamiento de trabajos. También se puede acceder a este panel desde el Menú > Estado de procesamiento. Después de terminar la reconstrucción, el análisis de post-procesamiento de imágenes debe avanzar a Fluence Correction.
- Active Fluence Correction de imágenes reconstruidas en el menú del tablero. Las imágenes reconstruidas deben cargarse para la corrección de fluidez. Estos aparecen con una bandera junto a cada número de escaneo. Los archivos cargados se mostrarán inmediatamente en el lado derecho de la pantalla como Reconstrucciones seleccionadas. Active Fluence Correction interactuando con el icono en el lado derecho de la pantalla (Figura complementaria 3). Empuje las correcciones de Save Fluence para que progresen.
- Después de guardar la corrección de fluencia, realice la desmezcla espectral del preajuste adquirido (Hb, HbO2 y melanina). Seleccione la ficha Desmezcla espectral para abrir la lista de Reconstrucciones seleccionadas para la desmezcla espectral. Se mostrará una lista con cada escaneo del estudio seleccionado con el historial de los pasos anteriores de procesamiento de imágenes.
- Cargue los archivos de corrección de fluencia guardados anteriormente. Los escaneos cargados se mostrarán inmediatamente en el lado derecho de la pantalla como Reconstrucciones seleccionadas (Figura complementaria 4). Active la desmezcla espectral presionando el icono en el lado derecho de la pantalla.
- Observe las longitudes de onda que se van a mezclar. Las seis longitudes de onda de emisión optoacústica (700, 730, 760, 800, 850 y 900 nm) tomadas en la etapa de reconstrucción (paso 3.4) se eligen automáticamente para la mezcla espectral. Edite los espectros deseados para procesar (por ejemplo, espectros: Hb, HbO2 y melanina) utilizando el icono XYZ , si es necesario.
- Después de confirmar los parámetros ajustados, haga clic en Iniciar desmezcla espectral para que la mezcla espectral progrese. Aparece una barra de menú de procesamiento que muestra el progreso de la operación.
NOTA: Varios ajustes de parámetros son posibles durante la mezcla espectral, y varios métodos de desmezcla están disponibles. En este protocolo, el método de regresión lineal se utiliza como estándar para desmezclar Hb, HbO2 y melanina.
- Acceda a la pestaña Visualización y análisis . Haga clic en un escaneo activado para mostrar toda la información del tema y los comentarios introducidos en el paso 1.1 (Figura complementaria 5).
NOTA: Se pueden visualizar varios escaneos en paralelo.- Pulse el botón + para crear un análisis de escaneo múltiple. En esta ventana, introduzca una vista de escaneo múltiple y presione el botón Guardar . Después de guardar el nombre de la vista, se muestra un nuevo panel de control, que incluye todos los escaneos del estudio que se está analizando.
- Seleccione cada escaneo deseado para Agregar (cada uno) a la Vista de análisis guardada. Agregue escaneos adicionales en el icono de la esquina superior izquierda y se mostrarán automáticamente en la Vista de análisis.
- En la vista de análisis, establezca tablas de búsqueda de color adecuadas para preparar la imagen para el análisis. Haga clic en Más opciones de control de imagen en la barra de menú superior y active el icono Proyección de intensidad máxima . Asigne colores a las capas presionando el icono disponible en la esquina inferior derecha de la visualización de la imagen, adyacente a la visualización de la imagen 2D+.
- Seleccione Más para editar los colores de todos los canales simultáneamente. Este menú muestra todos los cromóforos sin mezclar y permite la selección de múltiples capas para su visualización.
NOTA: Al mover el ratón sobre los iconos del software se muestra su nombre en gris como se muestra en el protocolo. - Ajusta la intensidad de color de cada capa con las herramientas disponibles en la parte inferior izquierda de la pantalla.
NOTA: El ajuste con interpolación mínima/máxima para cada canal generalmente produce buenos resultados.
4. Análisis de la región de interés (ROI)
NOTA: La selección de una región de interés (ROI) es obligatoria para el análisis de datos.
- Identificar el ROI a analizar. Rodee el ROI con las formas disponibles (dentro de la barra de menús) en la imagen XY mientras traza el mismo ROI dentro de las vistas ortogonales disponibles en los ejes XZ e YZ (Figura complementaria 6).
NOTA: Se utilizó una forma de polígono para el análisis de ROI actual.- Siga la forma ROI en los ejes XZ e YZ restantes (ejemplo en la Figura 2) mientras coloca varias capas poligonales con la función Agregar interpolar y quitar subregiones . Los datos se pueden trazar después de definir/seleccionar el ROI deseado.
- Pulse el icono Importar región de interés a la cuantificación y observe el componente multiespectros que se muestra en el lado derecho de la pantalla como un detalle gráfico del ROI seleccionado.
- Exporte los datos de ROI presionando el icono de Excel en la parte inferior de la vista gráfica de los datos de ROI. Todo el paquete de datos de todas las regiones se exporta como un paquete a una hoja de cálculo para su posterior análisis. La Figura 3 muestra los datos de un participante que se sometió a un manguito de presión inflado a 200 mmHg y la vasculatura se analizó en comparación con el estado de reposo de la vasculatura a 0 mmHg.
- Cuantifique múltiples objetos de ROI simultáneamente siguiendo los pasos 4.1-4.1.3.
- Exporte imágenes desde el mismo menú que los archivos TIFF con todos los datos incrustados y el esquema de ROI incorporado (Figura 2).
Resultados
Los datos proporcionados por las imágenes optoacústicas se pueden analizar en imágenes de exportación postprocesadas (Figura 2) y datos graficados (Figura 3). El propósito aquí era introducir el funcionamiento de la imagen funcional optoacústica y explorar su aplicación en la investigación vascular más comúnmente conocida. Para eso, comparamos las imágenes adquiridas durante el reposo y después de una oclusión de 200 mmHg de una arteria principal (Figura 2). Estas observaciones se pueden cuantificar después del análisis del ROI y la exportación. En el plano XY, se puede observar la señal más alta de melanina en comparación con los planos YZ y XZ, lo que indica el límite de la epidermis. La oclusión de la arteria braquial (brazo) provoca cierta estasis en los vasos antes de la colocación de la sonda OT (antebrazo ventral). En consecuencia, detectamos un aumento en las señales generales mostradas como un aumento de azul (Hb) y rojo (HbO2) en los ejes XY, YZ y XZ. La estasis se puede seguir en el plano XY mientras se mantiene la presión de 200 mmHg dentro del manguito. Los ejes YZ y XZ representan un aumento del volumen sanguíneo debido a la oclusión anterior en comparación con las condiciones normales de perfusión (sin oclusión), resaltadas por las áreas enmascaradas magenta.
El análisis de ROI exportado de la misma área de microvasculatura cuantifica los cromóforos HbO 2 (rojo), Hb (azul) y HbT (rosa), mSO2 (rojo intenso) y melanina (amarillo) a partir de imágenes estabilizadas recolectadas durante 8.6 s. La liberación de presión se detecta inmediatamente; La Figura 3 muestra la evolución posterior a la oclusión de la recuperación de Hb, HbO2 y HbT, mientras que la salida de datos optoacústica sigue las observaciones de la Figura 1. El software calcula la saturación de oxígeno en sangre (mSO 2) y los valores de HbT a partir de la adición de las señales arbitrarias de Hb y HbO2. La concentración de melanina permanece constante dentro de la oclusión de 200 mmHg y en el estado de reposo dentro del intervalo de tiempo de adquisición de la imagen.
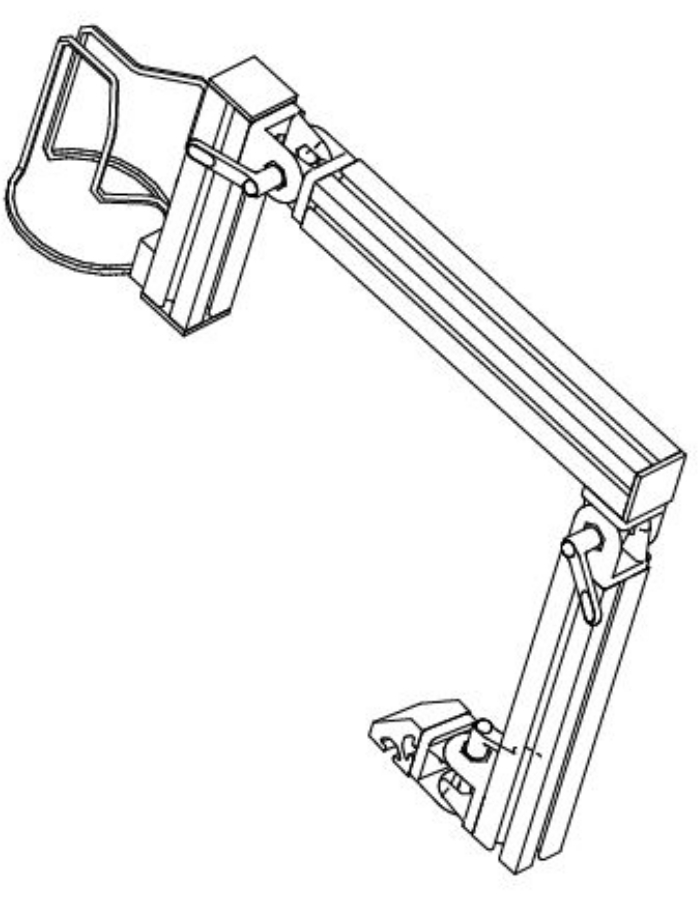
Figura 1: Diagrama esquemático que representa el brazo flexible diseñado para sostener la sonda de medición en contacto estabilizado con la piel del participante. Haga clic aquí para ver una versión más grande de esta figura.

Figura 2: Imágenes optoacústicas representativas que resaltan cambios de la vasculatura en reposo o bajo presión de 200 mmHg. La imagen que se muestra incluye tres colores, que representan Hb (azul), HbO2 (rojo) y melanina (amarillo), como se describe en el análisis de imágenes en la sección 4. Cada imagen optoacústica representa una proyección de máxima intensidad de todos los planos asociados con cada cromóforo escaneado. (A) El plano XY de la adquisición optoacústica. (B) La vista ortogonal YZ del mismo sitio de imágenes optoacústicas. (C) La vista XZ del área escaneada. Las flechas magenta apuntan a las áreas con mayor estasis; El área enmascarada magenta marca el aumento del volumen de sangre atrapada dentro de los vasos debido a la oclusión de la arteria braquial en comparación con las condiciones normales de perfusión (sin oclusión). Haga clic aquí para ver una versión más grande de esta figura.
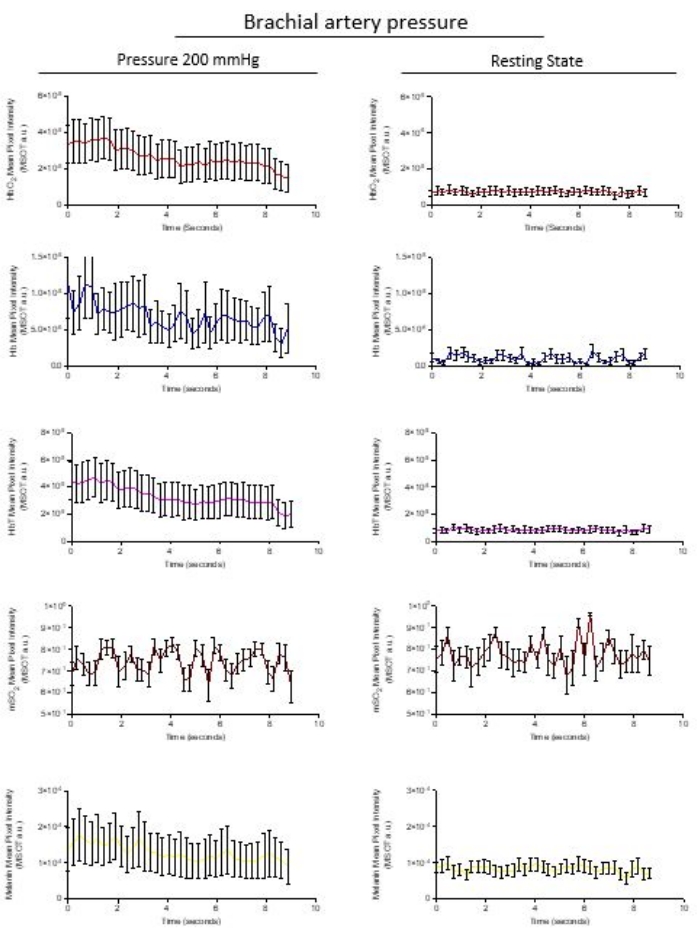
Figura 3: Exportación de datos representativos de un ROI cuantificado. Los cromóforos naturales de HbO 2 (rojo), Hb (azul) y HbT (rosa), mSO2 (rojo intenso) y melanina (amarillo) se representan a partir de los datos extraídos de las imágenes estabilizadas recogidas durante 8,6 s. Los gráficos de Hb, HbO2 y HbT muestran una pendiente de recuperación desde la oclusión hacia el estado de reposo no ocluido. La oxigenación sanguínea calculada mSO2 y la concentración de melanina permanecen constantes dentro de la oclusión de 200 mmHg y en el estado de reposo dentro del intervalo de tiempo de adquisición de la imagen. Las imágenes extraídas son puntos de datos representados como media ± sd de n = 10 imágenes por fotograma. Haga clic aquí para ver una versión más grande de esta figura.
Figura complementaria 1: Panel de descripción general del escaneo y menú principal del software de análisis. Al presionar el botón Menú (en negro), el menú principal desplegará opciones para seleccionar el estudio seleccionado. Esta acción seleccionará y cargará el archivo ".nod" reconocido por el software. La descripción general de la exploración (en azul) muestra todas las exploraciones del estudio. Los detalles (negro) aparecen a la derecha. Haga clic aquí para descargar este archivo.
Figura complementaria 2: Flujo de trabajo de análisis de reconstrucción. Panel 1 - Seleccione el escaneo a reconstruir y presione la flecha hacia la derecha en el lado derecho de la pantalla (flecha púrpura) para avanzar. Panel 2 - Observe la velocidad del sonido y ajuste el control deslizante al mejor enfoque (flecha azul); a) enfoque ajustado que se muestra en el lado derecho de la ventana; b) seleccionar las repeticiones a analizar (flecha amarilla); c) pulse el botón Reconstruir escaneos para continuar (flecha verde). Haga clic aquí para descargar este archivo.
Figura complementaria 3: Flujo de trabajo del panel de corrección de fluidez. Panel 1 - Seleccione los escaneos que desea corregir y presione la flecha hacia la derecha en el lado derecho de la pantalla. Panel 2 - presione Save Fluence Correction(s) para continuar (flecha verde). Haga clic aquí para descargar este archivo.
Figura complementaria 4: Flujo de trabajo del panel de desmezcla de espectros. Panel 1 - Seleccione los escaneos para desmezclar y presione la flecha hacia la derecha (flecha púrpura). Panel 2 a) seleccione el escaneo para desmezclar (flecha azul) y se mostrará una vista previa de la imagen ajustada en el lado derecho; b) Seleccione las repeticiones para desmezclar (flecha amarilla); c) pulse Iniciar desmezcla espectral para continuar (flecha verde). Haga clic aquí para descargar este archivo.
Figura complementaria 5: Panel de visualización y selección de colores cromóforos. Panel 1) Seleccione los escaneos para mostrar con un doble clic (flecha púrpura); Panel 2) Imagen adquirida en el eje XY (cuadrado azul), XZ (cuadrado amarillo) e YZ (cuadrado verde); 2a) Botón de análisis de imágenes que muestra las longitudes de onda adquiridas; 2b) elija Más opciones de control de imagen en la barra de menú superior y active el icono Proyección de intensidad máxima ; selecciona Más para editar los colores de los canales. Haga clic aquí para descargar este archivo.
Figura complementaria 6: Selección de la región de interés (ROI). Seleccione la herramienta lazo (flecha amarilla) y defina los límites del ROI dentro del eje XY (flecha magenta). Es posible definir varias áreas de forma (polígono, rectángulo, cuadrado, círculo o elipse). Siga el ROI en los ejes XZ e YZ y agregue subregiones (flecha verde) a la selección inicial. Se muestran varias subregiones (flecha cian). Para extraer datos del ROI seleccionado, presione el icono Importar región de interés a la cuantificación y continúe. Haga clic aquí para descargar este archivo.
Discusión
Este protocolo enfatiza los pasos de trabajo considerados como requisitos prácticos para operar este nuevo instrumento de imagen optoacústica, desde el posicionamiento adecuado (participante, sonda) necesario para la estabilización de la sonda de copa 3D hasta la adquisición de imágenes, la selección de ROI y la reconstrucción y análisis de imágenes.
El enfoque experimental propuesto, utilizando adquisiciones "instantáneas" junto con imágenes obtenidas en condiciones dinámicas, ilustra el interés y la utilidad de este instrumento para acceder in vivo a la fisiología vascular humana. Como se muestra, la resolución de imagen acústica de 150 μm recogida en un volumen de hasta 15mm3 no tiene comparación con otras técnicas de tomografía.
Es necesario prestar especial atención a (i) la importancia de la estabilización de la sonda para la adquisición de imágenes; el uso de un soporte de sonda flexible y seguro mejora claramente la adquisición de imágenes; ii) la correcta identificación de las estructuras vasculares; Las referencias ecográficas como la melanina en la transición epidérmica-dérmica podrían usarse como marcador para identificar los vasos del plexo superior en la piel; y (iii) el análisis funcional de imágenes realizado a través del software de reconstrucción del fabricante.
El análisis avanzado de los datos de ROI y la exportación de imágenes requiere una comprensión más profunda del software dedicado y los algoritmos desarrollados. El instrumento de imagen optoacústica actual es capaz de reconstruir un volumen 3D de 15 mm3 de tejido con una resolución de 150 μm. Esta capacidad debe potenciarse para cuantificar mejor la(s) función(es) microvascular(es) en profundidad. Sin embargo, la operación básica permite la observación directa de cromóforos de referencia y la adquisición de múltiples presets de la misma área, proporcionando un escaneo rápido y grabaciones de video en vivo.
El potencial de aplicabilidad encontrado con el sistema de imágenes optoacústicas es relevante. Los desarrollos de software en curso seguramente mejorarán la utilidad de este sistema de imágenes.
Divulgaciones
Los autores no informan conflictos de intereses.
Agradecimientos
Esta investigación es financiada por ALIES y COFAC principales proveedores de la tecnología en estudio, y por la Fundação para a Ciência e a Tecnologia (FCT) a través de la subvención UIDB/04567/2020 a CBIOS.
Materiales
| Name | Company | Catalog Number | Comments |
| Cuff | PIC | 107001 | |
| Drapes | Pajunk | 021151-1501 | |
| Ethanol 70% | Sigma Aldrich | EX0281 | |
| Gogless | Univet | 559G.00.00.201 | |
| Kimwipes | Amoos | 5601856202331.00 | |
| MSOT | iThera | MSOTAcuity | |
| Stabilizing arm | ITEM | Self designed and assemble | |
| Ultrasound gel | Parker Laboratories | 308 | |
| Waxing cream | Veet | kkdg08hagd |
Referencias
- Iskander-Rizk, S., vander Steen, A. F. W., van Soest, G. Photoacoustic imaging for guidance of interventions in cardiovascular medicine. Physics in Medicine and Biology. 64 (16), (2019).
- Cakmak, H. A., Demir, M. MicroRNA and cardiovascular diseases. Balkan Medical Journal. 37 (2), 60-71 (2020).
- Li, Z., Gupte, A. A., Zhang, A., Hamilton, D. J. Pet imaging and its application in cardiovascular diseases. Methodist DeBakey Cardiovascular Journal. 13 (1), 29-33 (2017).
- Karlas, A., et al. Cardiovascular optoacoustics: From mice to men - A review. Photoacoustics. 14, 19-30 (2019).
- MacRitchie, N., Noonan, J., Guzik, T. J., Maffia, P. Molecular imaging of cardiovascular inflammation. British Journal of Pharmacology. 178 (21), 4216-4245 (2021).
- Granja, T., Andrade, S., Rodrigues, L. Optoaccoustic tomography - good news for microcirculatory research. Biomedical and Biopharmaceutical Research. 18 (2), 1-13 (2022).
- Tan, H., et al. Total-body PET/CT: Current applications and future perspectives. American Journal of Roentgenology. 215 (2), 325-337 (2020).
- Masthoff, M., et al. Multispectral optoacoustic tomography of systemic sclerosis. Journal of Biophotonics. 11 (11), 201800155 (2018).
- Hu, S., Wang, L. V. Photoacoustic imaging and characterization of the microvasculature. Journal of Biomedical Optics. 15 (1), 011101 (2010).
- Wu, M., Awasthi, N., Rad, N. M., Pluim, J. P. W., Lopata, R. G. P. Advanced ultrasound and photoacoustic imaging in cardiology. Sensors (Basel). 21 (23), 7947 (2021).
- Yang, H., et al. Soft ultrasound priors in optoacoustic reconstruction: Improving clinical vascular imaging. Photoacoustics. 19, 100172 (2020).
- Dean-Ben, X. L., Gottschalk, S., Mc Larney, B., Shoham, S., Razansky, D. Advanced optoacoustic methods for multiscale imaging of in vivo dynamics. Chemical Society Reviews. 46 (8), 2158-2198 (2017).
- World Medical Association. World Medical Association Declaration of Helsinki: ethical principles for medical research involving human subjects. JAMA. 310 (20), 2191-2194 (2013).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados