Method Article
Dreidimensionaler Lokalisierungsansatz mit Seidenfaden-geführter laparoskopischer Segmentektomie bei Lebertumor
In diesem Artikel
Zusammenfassung
Der Einsatz von 3D-Rekonstruktionen und virtuellen Simulationen in der präoperativen Planung von Leberresektionen stellt einen bedeutenden Fortschritt in der chirurgischen Onkologie dar. Die 3D-LAST-Technik (dreidimensionaler Ortungsansatz mit dem Seidenfaden) unseres Teams ermöglicht eine sichere, effiziente und präzise Tumorentfernung mit praktischer intraoperativer Navigation und verspricht eine breite medizinische Akzeptanz.
Zusammenfassung
Bei der Durchführung einer Hepatektomie zur Behandlung von Lebertumoren ist die genaue Bestimmung des Resektionsrandes und die Sicherstellung der Angemessenheit des verbleibenden Leberparenchyms von größter Bedeutung. Gegenwärtig sind der intraoperative Ultraschall und die Indocyaningrün-Fluoreszenznavigation häufig eingesetzte Methoden. Bestimmte technische Randbedingungen stehen einer flächendeckenden Anwendung jedoch entgegen. Für die präzise Lebertumorresektion haben wir die 3D-LAST-Technik entwickelt. Bei dieser Technik wird die Computernachbearbeitung genutzt, um Merkmale aus Computertomographie-Scans (CT) zu extrahieren und volumetrische Bilder zu erzeugen, wodurch dreidimensionale (3D) Visualisierungen erstellt werden. Dies stellt eine wertvolle Ressource für die klinische Entscheidungsfindung dar, da es komplexe innere anatomische Strukturen intuitiv und stereoskopisch anschaulich darstellen kann. In dieser Studie wurde eine präoperative 3D-Positionierung an Patienten mit einem einzelnen Lebertumor durchgeführt, um anatomische Orientierungspunkte zu identifizieren und den Resektionsbereich zu berechnen. Während des chirurgischen Eingriffs wurden Randlinien mit Längen festgelegt, die von einer präoperativen 3D-Software berechnet wurden, und Seidenfaden zur Markierung der Ränder verwendet. Dieser Ansatz bietet eine zeitsparende und genaue Möglichkeit, die optimale Schnittebene zu bestimmen. Das Ziel dieses Artikels ist es, die Machbarkeit der Anwendung von 3D-LAST in der laparoskopischen Segmentektomie bei Lebertumoren zu demonstrieren. Die Forschungsergebnisse deuten darauf hin, dass 3D-LAST eine sichere, effektive und praktische neue Methode für die intraoperative Lebernavigation ist und ein großes Potenzial für eine breite Verbreitung hat.
Einleitung
Die Hepatektomie ist nach wie vor ein Eckpfeiler der Behandlung von Lebertumoren. In den letzten Jahrzehnten haben sich chirurgische Ansätze von unregelmäßigen Resektionen zu präzisen anatomischen Resektionen entwickelt, angetrieben durch Fortschritte bei assistiven Technologien wie der intraoperativen Ultraschall- (IOUS) und der Indocyaningrün-Fluoreszenzbildgebung (ICG) 1,2. Trotz dieser Innovationen bleibt das Erreichen optimaler Resektionsränder bei gleichzeitiger Beibehaltung eines ausreichenden funktionellen Lebervolumens eine entscheidende Herausforderung. Das übergeordnete Ziel unserer vorgeschlagenen 3D-LAST-Technik (dreidimensionaler Ortungsansatz mit Seidenfaden) ist es, eine präzise, kostengünstige und universell zugängliche intraoperative Navigationsmethode für die Lebertumorresektion bereitzustellen, die den Einsatz von Spezialgeräten minimiert und gleichzeitig die räumliche Genauigkeit verbessert.
Der Grund für die Entwicklung von 3D-LAST ergibt sich aus den Einschränkungen der aktuellen Techniken. IOUS ist zwar wertvoll für die Echtzeit-Tumorlokalisierung, erfordert aber erfahrene Sonographen für die Bildinterpretation und hat Probleme mit der zweidimensionalen (2D) räumlichen Visualisierung, was die Operationszeit oft verlängert 3,4. Die ICG-Fluoreszenznavigation ist zwar bei oberflächlichen Tumoren wirksam, aber durch ihre begrenzte Eindringtiefe des Gewebes (5-10 mm) eingeschränkt, was sie für tiefere Läsionen unzuverlässig macht 5,6. Beide Methoden hängen von teurer, spezialisierter Hardware ab, was ihre Einführung in Umgebungen mit begrenzten Ressourcen einschränkt.
Die Vorteile von 3D-LAST gegenüber bestehenden Techniken sind vielfältig. Die dreidimensionale Visualisierung, die aus präoperativen Computertomographie-Rekonstruktionen (CT) abgeleitet wurde, überwindet die räumliche Mehrdeutigkeit der 2D-Bildgebung, indem sie eine stereoskopische anatomische Führung bietet. Im Gegensatz zu ICG, bei dem es an Tiefenauflösung mangelt, ermöglicht 3D-LAST eine präzise Planung der volumetrischen Resektion, wodurch das Risiko positiver Ränder oder eines übermäßigen Parenchymverlusts reduziert wird. Darüber hinaus macht die Verwendung von Seidengarn für die intraoperative Markierung Echtzeit-Bildgebungsgeräte überflüssig, was den Arbeitsablauf rationalisiert und die Kosten senkt.
3D-LAST eignet sich besonders für Zentren, die über keine fortschrittliche Bildgebungsinfrastruktur oder Erfahrung in komplexer intraoperativer Navigation verfügen. Es ist ideal für Einzeltumorresektionen, bei denen anatomische Orientierungspunkte in der präoperativen CT erkennbar sind und bei denen die Minimierung der prozeduralen Komplexität im Vordergrund steht. Durch die Überwindung der Einschränkungen aktueller Methoden und die Nutzung validierter 3D-Technologien stellt 3D-LAST einen pragmatischen Fortschritt bei der präzisen Leberchirurgie mit breiter klinischer Anpassungsfähigkeit dar.
Präsentation des Falles:
Bei einem 59-jährigen Mann mit Oberbauchbeschwerden wurde ein 2,7 cm x 1,6 cm großer Lebertumor in der rechten Leber diagnostiziert. Bei der Patientin wurde zuvor ein Adenokarzinom des Magens diagnostiziert und sie wurde einer radikalen Gastrektomie wegen Magenkrebs unterzogen, gefolgt von einer routinemäßigen Chemotherapie. Im präoperativen kontrastmittelverstärkten CT-Scan wurden keine extrahepatischen Metastasen gefunden. CA19-9, CA15-3, CA72-4, AFP und CEA waren normal.
Protokoll
Die Studie wurde vom Überprüfungsausschuss des Westchinesischen Krankenhauses der Universität Sichuan genehmigt. Vor der Operation wurde die Einverständniserklärung des Patienten eingeholt.
1. Präoperative Vorbereitung
- Erhalten Sie hochauflösende CT-Scans der Leber des Patienten im DICOM-Format (Abbildung 1A).
- Starten Sie die Mimics-Software, erstellen Sie ein neues Projekt und importieren Sie die DICOM-Dateien, um sicherzustellen, dass alle Bilddaten für die 3D-Rekonstruktion und -Analyse korrekt geladen werden.
- Rekonstruieren Sie die dreidimensionale Struktur der Leber, der Gefäße und des Tumors. Markieren Sie die Leber in rosa, die Pfortader in blau, die Arterie in rot, die Lebervene und die untere Hohlvene in blau und den Tumor in gelb (Abbildung 1B).
- Platzieren Sie drei kleine virtuelle Stäbchen auf dem 3D-Lebermodell und erhalten Sie vier Schlüsselpunkte (S1, S2, S3, S4) auf der Oberfläche der Leber (Abbildung 2A-B).
- Diese virtuellen Stäbchen fungieren als digitale Orientierungspunkte, die den Chirurgen bei der Bestimmung der genauen Position und Ausrichtung des beabsichtigten Schnitts unterstützen. Platzieren Sie die virtuelle Stabmarkierung des Resektionspunktes 1 cm vom Tumorrand entfernt und den Mittelpunkt des Leberrandes am unteren Ende der Gallenblase.
HINWEIS: Durch die Markierung dieser Schlüsselpunkte können Chirurgen sicherstellen, dass sie sich während der Operation auf den Zielbereich konzentrieren, wodurch das Risiko unnötiger Gewebeschäden minimiert wird.
- Diese virtuellen Stäbchen fungieren als digitale Orientierungspunkte, die den Chirurgen bei der Bestimmung der genauen Position und Ausrichtung des beabsichtigten Schnitts unterstützen. Platzieren Sie die virtuelle Stabmarkierung des Resektionspunktes 1 cm vom Tumorrand entfernt und den Mittelpunkt des Leberrandes am unteren Ende der Gallenblase.
- Verbinden Sie die vier Schlüsselpunkte mit Linien auf der Leberoberfläche und messen Sie ihre Längen (S1-S2 = 9,8 cm, S1-S3 = 7,2 cm, S2-S3 = 10,4 cm, S4-S2 = 8,2 cm, S4-S3 = 6,5 cm), wie in Abbildung 2C-D gezeigt. Diese Linien stellen den vorgeschlagenen Resektionspfad dar und leiten den Chirurgen bei der Visualisierung der Form und Kontur der Leber nach der Resektion an.
- Messen Sie die Länge jeder Linie sorgfältig, um Genauigkeit und Konsistenz zu gewährleisten. Diese Messung ist von entscheidender Bedeutung, da sie es dem Chirurgen ermöglicht, Seidenfäden mit genau der gleichen Länge herzustellen, die intraoperativ zur Führung des Leberschnitts verwendet werden.
2. Operatives Vorgehen
- Positionieren Sie den Patienten in Rückenlage, mit gespreizten Beinen und nach rechts geneigt (Abbildung 3A). Verabreichen Sie eine Standard-Vollnarkose, einschließlich trachealer Intubation und kontrollierter Beatmung.
- Desinfizieren Sie die Haut mit einem 3x igen Peeling auf 0,5%iger Jodbasis im Bereich der Brustwarzenverbindung, der Symphyse des Schambeins, der rechten Mittelaxillerie und der linken Mittelklavikularlinie.
- Ordnen Sie das Operationsteam mit dem Chirurgen auf der rechten und der Assistentin auf der linken Seite an. Positionieren Sie die Kamera mittig zwischen den Trokarstellen, wobei die Kamerahalterung ebenfalls in der Mitte steht.
- Machen Sie einen 12 mm langen Schnitt unterhalb des Nabels als laparoskopisches Loch (H1), einen 12 mm und einen 5 mm gebogenen Schnitt (H2 und H3) als Hauptoperationslöcher, einen weiteren 12 mm und einen 5 mm (H4 und H5) als zusätzliche Operationslöcher (Abbildung 3B).
- Führen Sie fünf Trokare (12 mm, 12 mm, 12 mm, 5 mm und 5 mm) in die Einschnitte ein, wie in Abbildung 3B dargestellt. Schalten Sie das Pneumoperitoneum-System ein und injizieren Sie 100 % Kohlendioxidgas durch den Trokar, um das Pneumoperitoneum auf einem Druck von etwa 12 mmHg zu halten.
- Führen Sie eine explorative Untersuchung der Bauchhöhle durch, beginnend mit dem linken Epigastrium und nach rechts hinunter zum Hypogastrium, um das Vorhandensein von Aszites, Zirrhose und Metastasen festzustellen.
- Befreien Sie abdominale Adhäsionen, lösen Sie das runde Band der Leber, befreien Sie das rechte Leberband und die Verwachsungen und legen Sie das Lebersegment V mit einem Ultraschallmesser vollständig frei.
- Verwenden Sie ein Ultraschallmesser, um das Gallenblasendreieck zu präparieren und den Gallenblasengang und die Arterie freizulegen. Anschließend werden diese Strukturen mit kleinen Hemo-Lock-Clips ligiert, bevor die Gallenblase herausgeschnitten wird.
- Bereiten Sie drei Seidenfäden mit den Längen S1-S2 = 9,8 cm, S1-S3 = 7,2 cm und S2-S3 = 10,4 cm vor. Punkt S4 befindet sich am Hals der Gallenblase, bereiten Sie also keine Seidenfäden für S4-S2 = 8,2 cm und S4-S3 = 6,5 cm vor.
- Platzieren Sie die drei Seidenfäden an der anatomischen Position auf der Leberoberfläche, die dem präoperativ geplanten Resektionspfad entspricht, wie in Abbildung 4 gezeigt. Durch die Verwendung von Seidenfäden als physikalische Führung können Chirurgen den geplanten Resektionspfad während der Operation präziser visualisieren und verfolgen.
HINWEIS: Dieser Schritt schließt die Lücke zwischen der virtuellen Planung und dem tatsächlichen chirurgischen Eingriff. - Verwenden Sie ein elektrisches Messer, um die Leber zu kauterisieren, indem Sie Markierungen entlang des Seidenfadens auf der Oberfläche der Leber schneiden (Abbildung 4D) und nähen Sie ein Gummiband auf die Leber, um sie zu ziehen (Abbildung 5A).
- Verwenden Sie ein Ultraschallmesser, um das Leberparenchym entlang der Markierungslinien zu durchschneiden. Schneiden Sie Gefäße, die beim Home-o-Lock-Clipping auftreten, verwenden Sie einen Aspirator, um das Blut abzusaugen, und verwenden Sie eine bipolare Pinzette, um die Blutung zu stoppen (Abbildung 5B).
- Legen Sie die Probe in einen Beutel und machen Sie einen 4 cm langen Schnitt mit dem Skalpell am Oberbauch, um die Probe zu entfernen. Bestätigen Sie, dass keine aktive Blutung in der Bauchhöhle vorhanden ist, geben Sie hämostatische Materialien auf die Leberdurchtrennungsfläche und einen Drainageschlauch, der aus dem rechten Unterbauch austritt.
- Entfernen Sie die Trokar- und Nahtschnitte mit 3-0 resorbierbaren Nähten Schicht für Schicht. Untersuchen Sie die Probe, um die Unversehrtheit der Tumorkapsel zu überprüfen, und messen Sie die Größe des Tumors (Abbildung 5C-D).
3. Management nach Hepatektomie
- Verlegen Sie den Patienten nach erfolgreicher Genesung von der Narkose auf die Station und beobachten Sie die Vitalparameter des Patienten mit einer ununterbrochenen Herzüberwachung während der ersten 24 Stunden nach der Operation.
- Führen Sie während des 1. postoperativen Tages eine prophylaktische antimikrobielle Therapie durch intravenöse Infusion durch, um mögliche septische Komplikationen zu reduzieren.
- Entfernen Sie die Harnkatheterisierung 24 Stunden nach dem Eingriff. Führen Sie 72 Stunden nach der Operation eine einfache Computertomographie durch (Abbildung 6). Evakuieren Sie chirurgische Drainagen 4 Tage nach der Operation ohne massiven Aszites und Gallenverlust.
Ergebnisse
Die Gesamtoperationszeit betrug 150 min, mit einem Blutverlust von 50 ml, der keine Bluttransfusion erforderte. Das intraoperative Urinvolumen betrug 500 ml und das intraoperative Infusionsvolumen 800 ml. Am 1. Tag nach der Operation zeigten die Bluttestergebnisse einen leichten Anstieg der Transaminasespiegel. Die CT-Untersuchung des Abdomens zeigte eine vollständige Resektion des Lebertumors und keinen signifikanten Aszites 3 Tage nach der Operation. Die Drainage wurde am 4. postoperativen Tag entfernt. Die Patientin hatte einen ereignislosen postoperativen Verlauf und wurde am 5. Tag nach der Operation entlassen. Die postoperative grobpathologische Probe zeigte, dass die Tumorgröße 1,5 cm x 1,5 cm betrug, was die R0-Resektion bestätigte, wie in Tabelle 1 gezeigt.
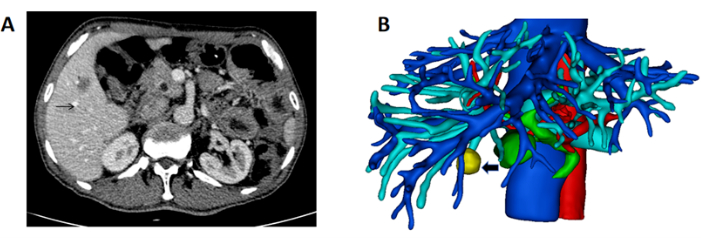
Abbildung 1: CT zeigt die Masse und 3D-Rekonstruktion der Leber und der Masse. (A) Der CT-Scan zeigt den Tumor in der rechten Leber (schwarzer Pfeil zeigt die Masse). (B) 3D-Rekonstruktion von Leber, Gefäß und Masse (schwarzer Pfeil zeigt die Masse an). Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 2: Markieren Sie die Resektionslinie auf dem 3D-Modell. (A-D) Rekonstruieren Sie die Struktur des intrahepatischen Gangs und den Tumor in 3D und markieren Sie die Schlüsselpunkte (S1, S2, S3, S4) der Schneide mit einem kleinen Stäbchen. Zeichnen Sie Leberlinien entlang der Schlüsselpunkte auf der Oberfläche des virtuellen Lebermodells und messen Sie die Länge jeder Linie (S1-S2 = 9,8 cm, S1-S3 = 7,2 cm, S2-S3 = 10,4 cm, S4-S2 = 8,2 cm, S4-S3 = 6,5 cm). Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 3: Intraoperatives Layout der Chirurg, des Patienten und der Trokarplatzierung. (A) Der operierende Chirurg befindet sich rechts, der Assistent links und der Kameramann zwischen den Beinen. (B) Die laparoskopische Hepatektomie wird mit einer Fünf-Port-Technik durchgeführt. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 4: Seidenfaden zur Markierung der Resektionslinie. (A-D) Bei der Leberoperation die Schneide mit Seidenfaden markieren, Seidenfäden gleicher Länge vorbereiten und an der anatomischen Position auf der Leberoberfläche platzieren. Die Form, die vom Seidenfaden umschlossen wird, ist die Schnittlinie für die Leber. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 5: Leberresektion und Probe. (A) Nähen Sie ein Gummiband an die Leber, um die Traktion zu gewährleisten. (B) Legen Sie die mittlere Lebervene in der Leberresektionsebene frei (schwarzer Pfeil zeigt die mittlere Lebervene). (C-D) Vollständige Resektion der Lebermasse (schwarzer Pfeil), die Schnittansicht des Tumorrandes ist intakt und entspricht dem präoperativ geplanten Rand. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 6: Postoperativer CT-Scan. Die CT-Untersuchung zeigte eine erfolgreiche Tumorentfernung ohne perihepatische Flüssigkeitsansammlung am postoperativen Tag 3. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
| Parameter | Befund |
| Dauer der Operation | ca. 150 Minuten |
| Blutverlust | 50 mL |
| Postoperative Leberfunktion | ALT 222 IU/L, AST 217 IU/L |
| Postoperative CT-Untersuchung | KASTEN 3 |
| Bewegung des Abflussrohrs | KASTEN 4 |
| Tag der Entlassung | KASTEN 5 |
| Größe des Tumors | 1,5 cm x 1,5 cm |
| Pathologischer Typ | Adenokarzinom |
Tabelle 1: Die chirurgischen Ergebnisse des Patienten. Abkürzungen: ALT = Alanin-Aminotransferase; AST = Aspartat-Aminotransferase; POD = Postoperativer Tag.
Diskussion
Mit der Entwicklung der Technologie und der Anhäufung von Erfahrungen ist die laparoskopische Leberresektion immer häufiger geworden, und ihre Indikationen sind fast so umfangreich wie die der offenen Chirurgie. Im Vergleich zur Laparotomie hat die laparoskopische Leberresektion viele Vorteile, wie z. B. weniger Schmerzen, weniger perioperative Komplikationen und eine schnellere Genesung 7,8,9. Die laparoskopische Leberresektion ist jedoch auch mit einigen inhärenten Schwierigkeiten konfrontiert. Der Mangel an Tast- und Tiefenwahrnehmung, der begrenzte Operationsraum und das eingeschränkte Gesichtsfeld stellen eine Herausforderung für die weit verbreitete Verwendungdar 10,11,12. Um diese Probleme zu lösen, wurden in den letzten Jahren IOUS- und ICG-Fluoreszenzbildgebung als Echtzeit-Navigationswerkzeuge eingesetzt. IOUS kann, wenn es direkt auf die Leberoberfläche aufgetragen wird, die Genauigkeit der Läsionserkennung und -lokalisation verbessern13,14.
Da sie jedoch in der Regel von Sonographen operiert wird, müssen Chirurgen die Operation oft unterbrechen, um auf sie zu warten, was nicht nur die Operationszeit verlängert, sondern auch die Abhängigkeit von der Ultraschalltechnologie erhöht. Darüber hinaus kann IOUS in zirrhotischen Lebern regenerative Knötchen als Tumoren fehlinterpretieren, was zu einer Überdiagnose führt 15,16,17. ICG, ein harmloses wasserlösliches Nahinfrarot-Fluoreszenzmittel, kann helfen, anatomische Strukturen während der Operation durch spezielle Endoskope sichtbar zu machen. Seine hohe Empfindlichkeit und sein klarer Kontrast machen es zu einem beliebten Werkzeug für die chirurgische Navigation bei verschiedenen Leberoperationen. Aufgrund der begrenzten Gewebedurchdringung durch Nahinfrarotlicht (bis zu 10 mm) ist seine Anwendung bei der Detektion tiefliegender Leberläsionen jedoch eingeschränkt. Darüber hinaus kann eine übermäßige Dosis von ICG zu falsch-positiven Ergebnissen führen, und der Erfolg der Tumorfärbung hängt mit Faktoren wie Blutversorgung, Leberzirrhose und Nekrose zusammen 18,19,20. Daher ist die Entwicklung einer innovativen, effizienten und genauen Methode zur Lokalisation tiefsitzender Lebertumoren von großer klinischer Bedeutung.
In dieser Studie wurde die präoperative 3D-Positionierung verwendet, um anatomische Orientierungspunkte zu identifizieren und die Resektionsfläche für Patienten mit solitären Lebertumoren zu berechnen. Während der Operation wurden die Randlinien der von der präoperativen 3D-Software berechneten Längen angeordnet und Seidenfaden zur Markierung der Kanten verwendet. Dieses Verfahren bietet eine zeiteffiziente und genaue Möglichkeit, die optimale Schnittebene21 zu navigieren. Die Operationszeit in unserer Studie war signifikant kürzer als in Studien mit IOUS und ICG-gesteuerter Hepatektomie. Dieser Ansatz reduziert die Abhängigkeit von IOUS, spart chirurgische Zeit und senkt die technischen und konditionellen Anforderungen. Es kann auf verschiedene Situationen der Navigation von Lebertumoren angewendet werden, unabhängig von der Größe und Tiefe des Tumors.
Trotz seiner Vorteile hat dieser Ansatz seine Grenzen. Erstens hängt die Genauigkeit von der präoperativen Bildgebungsqualität ab. Bewegungsartefakte oder Scans mit niedriger Auflösung können die Wiedergabetreue des 3D-Modells beeinträchtigen. Zweitens geht die Technik von einer statischen Leberanatomie aus, während Atembewegungen oder chirurgische Manipulationen die Tumorpositionen verschieben können, was Anpassungen in Echtzeit erforderlich macht. Drittens kann die Lernkurve für die Bedienung von 3D-Software und die intraoperative räumliche Übersetzung die Einführung in der Chirurgie ohne spezielle Ausbildung einschränken. Darüber hinaus ist die Stichprobengröße dieser Studie relativ klein, und zukünftige groß angelegte prospektive Studien sind erforderlich, um die Wirksamkeit dieser Methode weiter zu überprüfen. Die Entwicklung eines einfachen und breit anwendbaren 3D-Rekonstruktionsprogramms ist auch ein wichtiges Ziel für die zukünftige Forschung.
Offenlegungen
Die Autoren berichten von keinem Interessenkonflikt.
Danksagungen
Diese Arbeit wurde unterstützt durch das Projekt des Wissenschafts- und Technologiefonds der Gesundheitskommission der Provinz Guizhou (gzwkj2025-300), das Projekt des Ministeriums für Wissenschaft und Technologie der Provinz Guizhou (Qian Ke He Cheng Guo, LC[2024]109).
Materialien
| Name | Company | Catalog Number | Comments |
| BiClamp LAP | ERBE Company | No.20195-132 | |
| Laparoscopic system | Olympus | VISERA OTV-S400 | |
| Ultrasonic knife | Johnson and Johnson MedTech | ETHICON HARMONIC |
Referenzen
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten