Method Article
ACT1-CUP1 Testleri, Tomurcuklanan Mayadaki Splisozomal Mutantların Substrata Özgü Hassasiyetlerini Belirler
Bu Makalede
Özet
Bir bakır büyüme testi olan ACT1-CUP1 testi, öncü mesajcı RNA (pre-mRNA) eklemesinin ve mutant ekleme faktörlerinin spleozomal fonksiyon üzerindeki etkisinin hızlı bir şekilde okunmasını sağlar. Bu çalışma bir protokol sağlar ve ilgilenilen ekleme sorusunu ele almak için mümkün olan özelleştirmeyi vurgular.
Özet
Splisozomda veya substratında ortaya çıkan mutasyonlar, splisozomal fonksiyonun inceliklerini anlamamıza önemli ölçüde katkıda bulunmuştur. Hastalıkla ilişkili veya fonksiyonel olarak seçilmiş olsun, bu mutasyonların çoğu, model organizma Saccharomyces cerevisiae'de (maya) büyüme tahlilleri kullanılarak incelenmiştir. Eklemeye özgü bakır büyüme testi veya ACT1-CUP1 testi, fenotipik düzeyde mutasyonun kapsamlı bir analizini sağlar. ACT1-CUP1 testi, doğru şekilde eklendiğinde bakır toleransı sağlayan muhabirleri kullanır. Bu nedenle, bakır varlığında, maya canlılığındaki değişiklikler, ekleme yoluyla mRNA üretimindeki değişikliklerle ilişkilidir. Tipik bir deneyde, maya ekleme uzmanına, farklı konsensüs dışı ekleme muhabirleri ve ekleme üzerindeki herhangi bir sinerjik veya antitetik etkiyi tespit etmek için ilgi çekici ekleme faktörü mutasyonu ile meydan okunur. Burada bakır levha hazırlama, maya hücrelerinin kaplanması ve veri değerlendirmesinin tam bir açıklaması verilmiştir. ACT1-CUP1 muhabirlerinin çok yönlülüğünü vurgulayan bir dizi ücretsiz deney anlatılmıştır. ACT1-CUP1 testi, mutasyonel etkilerin doğrudan okunması ve sahada devam eden kullanımdan elde edilen karşılaştırmalı olasılıklar sayesinde ekleme araç kutusunda kullanışlı bir araçtır.
Giriş
Splisozom, öncü mesajcı RNA'da (pre-mRNA) intronların, kodlamayan bölgelerin uzaklaştırılmasını katalize eden büyük, biyolojik bir makinedir1,2. Yaklaşık 100 proteinin 1'inde ve 5 kodlamayan RNA'da tek bir nokta mutantının etkisini karakterize etmek, protein veya RNA'yı izole ederken genellikle belirsizdir. Mutasyona uğramış bileşenin işlevindeki değişiklik, tam, işleyen spliceozom bağlamında in vivo olarak en iyi şekilde değerlendirilebilir.
Burada açıklanan bakır büyüme testi, Saccharomyces cerevisiae veya tomurcuklanan mayadaki ekleme verimliliğinin hızlı bir göstergesidir. C.F. Lesser ve C. Guthrie tarafından geliştirilen ve 1993 yılında yayınlanan bu tahlil, basit bir model organizma ile çalışma kolaylığını ve hücre canlılığının doğrudan okunmasınıbirleştirir 3. Canlılık, bu hücrelerdeki splisozomların muhabir transkriptini ne kadar iyi tanıyabileceği ve ekleyebileceği ile ilişkilidir.
Bu bakır büyüme testine daha yaygın olarak ACT1-CUP1 testi denir. ACT1-CUP1 adı, ekleme verimliliğinin bir raporlayıcısını oluşturmak için kaynaşmış iki genden kaynaklanmaktadır. ACT1, mayanın aktin genidir, bu da yüksek oranda eksprese edilir ve verimli bir şekilde eklenmiş bir intron 4,5'e sahiptir. Cup1p, düzenli hücresel fonksiyonlara müdahale edilmesini önlemek için hücredeki bakırı tutan bir bakır şelatördür 6,7,8. ACT1-CUP1 muhabiri bu genleri sırayla içerir, öyle ki CUP1 sadece ACT1'in intronunun mRNA öncesi eklenmesi durumunda uygun okuma çerçevesinde olur (Şekil 1). Elde edilen füzyon proteini, aktinin ilk 21 amino asidini ve bakır bakımından zengin bir ortamda maya canlılığını artıran tam uzunlukta Cup1p proteinini içerir3. Bu nedenle, muhabirin ekleme miktarındaki bir artış, daha yüksek bir Cup1p konsantrasyonu ve daha yüksek bir bakır direnci ile sonuçlanır (Şekil 1). Diğer muhabir genlerle karşılaştırıldığında, CUP1 düşük seviyelerde bile hücre canlılığını etkiler, geniş bir duyarlılık aralığına sahiptir ve 3,6,7 mutasyonlarını eklemek için doğrudan seçmek için kullanılabilir. Ek olarak, CUP1 standart maya büyümesi için gerekli değildir ve bu nedenle hücresel homeostaz bu tahlilin kurulumu sırasında etkilenmez. Delesyon veya sıcaklık büyüme testlerini tamamlayan ACT1-CUP1, aksi takdirde optimal maya büyüme koşulları altında ekleme üzerindeki etkileri hakkında bilgi sağlar.
Eklem, substratını üç intronic dizi aracılığıyla tanır: 5' ekleme bölgesi (5' SS), dal-site (BS) ve 3' ekleme bölgesi (3' SS). Bu sitelerde fikir birliği olmayan diziler içeren çok sayıda ACT1-CUP1 muhabiri oluşturulmuştur. En yaygın ACT1-CUP1 muhabirlerinin bir seçkisi Şekil 1 ve Tablo 1'de gösterilmiştir. Ekleme döngüsünün farklı noktalarında her bir ekleme bölgesi ile benzersiz bir şekilde etkileşime girdiğinden, spliceosome'un sağlamlığı, konsensüs dışı raporlayıcının kullanıldığı farklı adımlarda test edilebilir. Konsensüs dışı muhabirler, intron içindeki mutasyona uğramış pozisyon ve mutasyona uğradığı taban için adlandırılır. Örneğin, A3c, 5' SS'de bir mutasyona sahip bir muhabirdir, özellikle konsensüs adenozinden bir sitozine kadar 3. konumdadır. Bu muhabir, 5' SS seçimini ve kullanımını etkileyen splisozom mutasyonları ile güçlü bir şekilde etkileşime girecektir. İlk çalışmalarında, Lesser ve Guthrie, hangi 5' SS mutasyonlarının ekleme3'ü inhibe ettiğini belirledi. Aynı yılın ilerleyen zamanlarında, her üç ekleme bölgesinde de fikir birliği olmayan muhabirler, Burgess ve Guthrie tarafından ATPase Prp16p9'daki mutasyonların baskılayıcı bir ekranında yayınlandı. Konsensüsü fikir birliği olmayan muhabirlerle karşılaştıran ACT1-CUP1 testi, maya ekleyicisinin sağlamlığını ve seçiciliğini anlamak ve diğer ökaryotların ek parçalarının işlevini çıkarmak için önemli bir anahtar olmuştur.
Konsensüs dışı ACT1-CUP1 muhabirleri splisozomu daha fazla bozulmaya duyarlı hale getirdikçe, tek bir ekleme faktörü mutasyonunun etkisi, olumlu veya olumsuz etkilediği muhabirler aracılığıyla karakterize edilebilir. Bu, araştırma sorularını çeşitli şekillerde eklemeye uygulanmıştır. İlk olarak, ACT1-CUP1 testi, ekleme faktörlerindeki mutasyonlar için genetik bir tarama olarak kullanılabilir ve kullanılmıştır. Örneğin, en büyük ekleme proteini olan Prp8p, splisozomun RNA çekirdeğinin ekleme reaksiyonunu katalize ettiği bir platform görevi görür. Bu, kısmen, Prp8p mutantlarının farklı ACT1-CUP1 muhabirlerinin 10,11,12,13,14,15,16,17 eklenmesini nasıl geliştirdiği veya azalttığı ile çıkarıldı. Eklemlemenin diğer protein bileşenleri de Hsh155p, Cwc2p, Cef1p ve Ecm2p 18,19,20,21,22,23,24,25 dahil olmak üzere ACT1-CUP1 kullanılarak araştırılmıştır. Prp16p ve spliceosomal geçişte yer alan diğer dört ATPazın enerjik eşikleri de bu tahlil 9,26,27,28,29,30 ile incelenmiştir. Küçük nükleer RNA'lar (snRNA'lar), koordine ettikleri pre-mRNA dizilerini ve snRNA'ların 3,31,32,33,34,35,36,37 ekleme sırasında maruz kaldıkları ikincil yapıdaki değişiklikleri tanımlamak için ACT1-CUP1 kullanılarak kapsamlı bir şekilde incelenmiştir.
ACT1-CUP1 testi, CUP1 geninin tüm kopyalarının nakavt edildiği bir maya suşu gerektirir. CUP1, 6,38 kopya numarasına sahip olabileceğinden, tam bir nakavt suşunun hazırlanması birden fazla tur veya kapsamlı tarama gerektirebilir. Sonuç olarak, cup1Δ maya suşları, muhabirler gibi laboratuvarlar arasında sıklıkla paylaşılmıştır.
Bir ekleme faktöründeki mutasyon (lar) bir plazmid kopyasından değerlendiriliyorsa, bu faktör için vahşi tip gen nakavt edilmelidir. Ek olarak, maya arka planı, biri ACT1-CUP1 muhabiri içeren, tarihsel olarak bir lösin besin seçimi plazmidi üzerinde ve diğeri çalışılacak ekleme makinesinde bir mutasyon veya pertürbasyon içeren en az iki plazmidin seçilmesine izin vermelidir (Şekil 2). Genellikle, tek bir tahlilde, her biri sorgu ekleme pertürbasyonunu (QSP) ve farklı bir raporlayıcıyı taşıyan birden çok maya türü, sorgunun ekleme üzerindeki etkisini test eder.
ACT1-CUP1 tahlilindeki bağımsız değişkenler, bir araştırmacının QSP'nin ciddiyetini değerlendirmesine izin verir. Bu bağımsız değişkenler, bakır konsantrasyonu ve birden fazla konsensüs dışı ekleme muhabirinin seçimidir. İlk olarak, maya suşları bir dizi bakır konsantrasyonu içeren plakalar üzerinde yetiştirildiğinden (Şekil 2), tahlilin kurulması, kullanılan konsantrasyonların gradyanının seçilmesini içerir. Çalışmalar, canlılığın ilk okumasını elde etmek için bir kurs bakır konsantrasyon gradyanı kullanabilir ve daha sonra ince canlılık farklılıklarını tanımlamak için tahlili daha ince bir gradanla tekrarlayabilir. İkinci değişken, test edilmesi mümkün olan çok çeşitli ACT1-CUP1 muhabirleridir (Şekil 1 ve Tablo 1). QSP, yabani tipe karşı fikir birliği olmayan bir muhabirin varlığında maya canlılığını farklı şekilde etkilerse, QSP'nin, intron'un bu bölgesinin tanınması veya işlenmesi sırasında önemli olan eklemedeki bir adımı veya spliceosome'un bir bölgesini etkilediği sonucuna varılabilir.
Maya alet kutusu kapsamlıdır ve ACT1-CUP1 testi, ekleme araştırmasının ayrılmaz bir parçasıdır. ACT1-CUP1 testi genellikle bir QSP'nin etkisi üzerinde daha derinlemesine genetik, yapısal ve / veya biyokimyasal bir analizle birlikte gerçekleştirilir. Bu daha ayrıntılı çalışmalar genellikle daha uzun bir prosedüre ve / veya daha yüksek fiyat etiketine sahip olduğundan, sık bir yaklaşım ilk önce ACT1-CUP1 ile ilginç mutantları taramaktır.
Burada bakır levha hazırlığı da dahil olmak üzere bir ACT1-CUP1 tahlil protokolü verilmiştir. Bu tahlil, araştırmacılara QSP'nin ekleme üzerindeki etkisine ve hangi intronic bölgelerinin pertürbasyondan en çok etkilendiğine dair ilk cevabı verir.
Protokol
1. Maya suşu yapımı
- Arka planı leu2 ve cup1Δ içeren bir S. cerevisiae suşu oluşturun veya elde edin. Bu arka planı oluşturmak için, lityum asetat ve tek sarmallı DNA39 kullanan köklü maya yöntemini kullanın.
NOT: Haploid maya suşları CUP1 6,38'in bir, iki veya daha fazla kopyasını içerebilir. CUP1 gen konumlarını kuşatmak için nakavt primerler tasarlarken seçilen maya suşu için genomik bilgilere bakın. - QSP'yi genomik birleştirme yoluyla veya bir plazmid üzerinde birleştirmek için bir maya dönüşümü gerçekleştirin. Önceki araştırmalarda açıklananlar gibi köklü bir protokol kullanın40,41,42.
- Adım 1.2'den itibaren ortaya çıkan suş(lar) ile bir maya dönüşümü gerçekleştirin. İstenilen ACT1-CUP1 muhabir plazmidini eklemek için.
NOT: Bu dönüşümü takiben ACT1-CUP1 muhabir plazmidlerinin tutulmasını sağlamak için hücreler lösin bırakma (-Leu) plakaları ve ortam üzerinde tutulmalıdır. - 1.2 adımlarını gerçekleştirin. ve 1.3. kontrol suşları da dahil olmak üzere test edilecek her QSP ve her ACT1-CUP1 muhabir plazmidi için.
2. Bakır levha hazırlama
- Test edilecek muhabirlere uygun bir bakır konsantrasyon aralığı seçin (sık kullanılan muhabirlerin öldürücülüğü için Tablo 1'e bakınız).
NOT: Kapsamlı bir bakır konsantrasyon aralığına örnek olarak 0 mM, 0,025 mM, 0,05 mM, 0,075 mM, 0,1 mM, 0,15 mM, 0,2 mM, 0,25 mM, 0,3 mM, 0,35 mM, 0,4 mM, 0,45 mM, 0,5 mM, 0,6 mM, 0,7 mM, 0,8 mM, 0,9 mM, 1,0 mM, 1,1 mM, 1,2 mM, 1,3 mM, 1,4 mM, 1,5 mM, 1,6 mM, 1,7 mM, 1,8 mM, 1,9 mM, 2,0 mM, 2,25 mM ve 2,5 mM Cu2+. - 0,22 μm PES (polietersülfon) steril filtreden 1 M CuSO4 ve steril filtreden oluşan bir stok çözeltisi yapın.
- İstenilen bakır plaka başına, CuSO4 stoğunun steril suda 2 mL'lik bir seyreltilmesini hazırlayın.
NOT: 0 mM Cu 2+ plaka her zaman referans olarak analiz edileceğinden ve görüntüleneceğinden, biri kaplama adımının başında diğeri sonunda olmak üzere iki adet 0 mM Cu2+ plaka yapılması önerilir (adım 3.4.).- Plaka hacminin 40 mL'sinde istenen son bakır konsantrasyonu için stok miktarını hesaplayın (Ek Tablo 1).
- Hesaplanan miktarda steril su ve 1 M CuSO4 stoğunu steril, 2 mL'lik bir tüpe ekleyin.
- ACT1-CUP1 testi için plakaları dökün.
NOT: Aşağıdaki protokole bir alternatif, her plaka için farklı bakır konsantrasyonları elde etmek için başlangıçta medyayı ve agar'ı büyük bir kapta ve daha küçük kaplara otoklavlamadan sonra aliquot'ta birleştirmektir. Hangi yöntem alınırsa alınsın, her biri farklı bir bakır konsantrasyonuna sahip olmasına rağmen, ortam konsantrasyonunun tüm plakalar arasında tutarlı olmasını sağlamak önemlidir.- Dökülecek her boş plakayı, içereceği son bakır konsantrasyonu ile etiketleyin. Test edilecek bakır konsantrasyonu başına en az bir kare plaka hazırlayın.
- Test edilecek bakır konsantrasyonu başına 100 mL'lik bir şişeyi etiketleyin.
- Her şişeye 790 mg agar (% 2 w / v agar) ve bir karıştırma çubuğu ekleyin.
- Büyük bir beherde, dökülecek tüm bakır plakalar için -Leu büyüme ortamını birleştirin. Yapılacak plaka başına, 265 mg maya azot bazını (YNB) ve 64 mg damlama karışımı eksi lösin (ve QSP plazmidini hücrelerde tutmak için gerekli olabilecek diğer besin maddelerini) 34 mL deiyonize suda çözün.
- Hazırlanan her 100 mL şişeye 34 mL -Leu büyüme ortamı çözeltisi ekleyin ve alüminyum folyo ile kapağa ekleyin. Folyoyu amaçlanan bakır konsantrasyonu ile etiketleyin.
- Otoklav için önerilen sıvı döngüsünü kullanarak agar'ı sterilize etmek ve çözmek için otoklav.
- Mümkün olan en kısa sürede, her şişeye 4 mL% 20 w / v glikoz (steril filtrelenmiş) ekleyin.
- Etiketleri eşleştirin ve CuSO4'ün 2 mL seyreltilerini amaçlanan şişeye ekleyin.
NOT: Her biri farklı bir konsantrasyona sahip onlarca bakır plaka aynı anda yapılabildiğinden, tüm şişeleri, tüpleri ve plakaları amaçlanan bakır konsantrasyonuyla açıkça etiketlemek, plaka dökme sırasında karışıklığı önleyecektir. - ~ 30 sn karıştırmak için bir karıştırma plakası kullanın ve kabarcıkları önleyerek etiketli plakaya 35 mL dökün veya pipetleyin. Saklamadan veya kullanmadan önce soğumaya bırakın.
NOT: Sıklıkla, plakalar tahlilden 1 gün veya 2 gün önce yapılır ve kullanımdan birkaç saat öncesine kadar 4 ° C'de saklanır. Kaplama başlamadan önce plakalar oda sıcaklığında (RT) olmalıdır (adım 3.4.).
3. ACT1-CUP1 testi
- İstenilen suşları -Leu plakaları üzerinde çizin.
NOT: Kriyografya stoklarından çalışıyorsanız, kaplamadan önce hücrelerin depolamadan yeterince canlandırılmasını sağlamak için özen gösterilmelidir. Bunun için önerilen bir prosedür, kriyojenik stoktan çizgi çizmek ve 30 ° C'de 3-5 gün boyunca büyümesine izin vermektir. Ardından, küçük bir renk örneğini dinlendirin ve 30 ° C'de 2-3 gün daha büyümesine izin verin. - 10 mL medyada bir gecede kültürler yetiştirin.
- Adım 2.4.2'de açıklananlarla aynı oranları kullanarak -Leu büyüme ortamını hazırlayın. 10 mL ortam başına, 9 mL deiyonize suya 66 mg maya azot baz (YNB) ve 16 mg damlama karışımı eksi lösin ekleyin. 0,22 μm PES steril filtreden geçirin.
- Maya suşu başına, steril 50 mL konik tüpe 9 mL -Leu büyüme ortamı ve 1 mL w / v glikoz (steril filtrelenmiş) % 20 ekleyin.
- Steril bir çubuk veya pipet ucu kullanarak, küçük (~ 1 mm yuvarlak) bir maya örneği toplayın ve ortamı aşılayın.
- Tüm gece kültürlerini 180 rpm ve 30 ° C'de çalkalayın.
NOT: Varsa, çalkalayıcı yerine rotatörler kullanılabilir.
- Suşları% 10 gliserol içinde OD600 0.5 ± 0.05'e seyreltin.
- Suş başına, 900 μL su içeren bir küvete 100 μL kültür ekleyin.
- OD600'ü bir spektrofotometre ile ölçün.
- 2 mL'lik son hacimdeOD 600 / 0,5'te olması gereken seyreltmeyi hesaplayın.
- Her suşu %10 gliserol (steril) içinde OD600 0.5'e kadar seyreltin.
- Hücre yoğunluğunun istenen0,5 ± 0,05 aralığında olduğunu doğrulamak için OD 600'ü yeniden ölçün.
- Bakır plakalar üzerindeki suşları plakalayın.
NOT: Suşları plakalamak için 5-10 μL hacimlerde elle pipetleme, tekrarlama veya çok kanallı pipetleyici kullanma veya pim çoğaltıcıyla damgalama gibi çeşitli yöntemler kullanılabilir. Bu son yöntem aşağıda açıklanmıştır, ancak çoğu adım yöntemden bağımsız olarak benzer olacaktır.- Steril bir çalışma yeri ve yanan bir Bunsen brülörü ayarlayın.
- 48 pimli bir çoğaltıcı için, seyreltilmiş her bir gerinimin 200 μL'sini 96 delikli bir plakanın ayrı bir kuyucuğuna pipetleyin. 6 x 8 ızgaradaki boş alanları 200 μL% 10 gliserol (steril) ile doldurun.
NOT: Dokuz maya suşu için bir kaplama şeması örneği Ek Tablo 2'dedir. - Sterilize etmek için çoğaltıcıyı% 95 (v / v) etanol ve alevden oluşan sığ bir kaba batırın. Isı hücreleri şok etmesini önlemek için alev söndükten sonra en az 2 dakika soğumaya bırakın.
- Brülörün yanına dört plaka yerleştirin ve kapakları çıkarın.
- Çoğaltıcıyı 96 delikli plakaya batırın ve tek bir hızlı hareketle yukarı kaldırın.
- Yavaşça plakaya yerleştirin ve iyi bir aktarımı kolaylaştırmak için hafifçe ileri geri sallayın.
- Tek bir hızlı hareketle yukarı kaldırın ve 96 delikli plakaya tam olarak aynı yönde yerleştirin.
- En fazla üç plaka için tekrarlayın. Çoğaltıcıyı etanol içine batırma, sterilize etmek için alevlendirme ve her dört plakada bir soğumayı bekleme işlemini tekrarlayın.
- Bir plaka kaplandıktan sonra, yana doğru yumuşak bir hareketle hareket edin, ancak yine de alevin sterilizasyon şemsiyesi içinde hareket edin.
NOT: Maya seyreltmelerinin ve kaplamanın bir alevin yakınında yapılması önerilir. Plakalar kururken kolayca kirlenebilir. - Kapakları yerleştirmeden önce plakaları tamamen kurumaya bırakın, genellikle 3-5 dakika.
- Plakaları 30 ° C'de 3 gün boyunca inkübe edin.
4. Veri toplama ve analizi
- Plakaları inkübatörden çıkarın ve görsel olarak inceleyin.
- Plakaların görüntülerini mevcut bir kamera veya başka bir dijital görüntüleme sistemi ile kaydedin.
- Her bir suş için rekor (veya skor) son bakır konsantrasyonu gözle görülür büyüme gözlenir.
NOT: Hücreler bu konsantrasyona kadar eklenebilir ve canlı kalabilir. Tutarlılık için, en son uygulanabilir bakır konsantrasyonunu puanlamak için her zaman gözle veya plaka görüntülerinden aynı yöntemi kullanın. Çok küçük koloniler bazen gözle görülebilir, ancak görüntüde görünmez. Doğrudan görsel inceleme veya görüntülerden kayıt arasındaki fark küçüktür, genellikle gradyanda bir adımdır. Kolonilerin görüntüleri yayınlarda sıklıkla kullanıldığından, görüntülerin puanlanması önerilir. - QSP'nin eklemeyi nasıl etkilediği hakkında sonuçlar çıkarmak için aynı suş için birden fazla ACT1-CUP1 tahlilinden elde edilen verileri birleştirin.
NOT: Yayın rakamları geleneksel olarak maya kolonilerinin görüntülerini 0 mM Cu2+ konsantrasyonunda, son uygulanabilir bakır konsantrasyonunda ve koloninin öldüğü sonraki konsantrasyonda gösterir. Veriler, çoğaltmalar arasındaki standart sapma için hata çubukları içeren bir çubuk grafik olarak da görüntülenebilir. Verilerin normalleştirilmesine gerek yoktur, ancak WT ekleme faktörü kontrolünün uygulanabilirliğini 1'e ayarlayarak ve ortaya çıkan mutasyonların etkisini karşılaştırarak olabilir.
Sonuçlar
ACT1-CUP1 gibi büyüme tahlilleri, çoklu kolonilerin görsel, karşılaştırmalı değerlendirmesini gerektirir. Burada, her bir suş gece boyunca doygunluğa büyütüldü, 0.5'lik bir OD600'e seyreltildi ve 0 mM ila 1.1 mM CuSO4 arasında bir dizi bakır konsantrasyonu içeren 20 plaka üzerine kaplandı (Şekil 3). Bu aralık, aşağıda kullanılan ve açıklanan QSP'lerin ve ACT1-CUP1 muhabirlerinin etkisinin tam olarak değerlendirilmesine izin verdiği için protokolde listelenenden daha küçüktür. Plakalar görüntülendi ve puanlandı (Şekil 3 ve Ek Tablo 3).
Bu temsili deney için, maya arka planı bozulmuş bir ADE2 geni içerir ve kolonilerin değişen kırmızı tonlarında olmasına neden olur (Şekil 3A, B). Adenosin üretim yolundaki bu yaygın maya bozulması, adenosin için kırmızı pigmentli bir öncünün birikmesine neden olur. Bu nedenle, kırmızı renk maya kolonisi olgunluğunun bir göstergesidir (yani, mevcut hücrelerin miktarı ve yaşı). Bir ACT1-CUP1 testinin amaçları doğrultusunda, kırmızı renk, beyaz veya sarı renkte ise mantar türlerini kirletici bir gösterge olarak hizmet edebilir. Renk, bakır toleransının ikincil bir teyidi olabilir, çünkü daha canlı koloniler daha derin bir kırmızı gölge olacaktır.
Bir pim çoğaltıcısı ile kaplanırken, birkaç yaygın sapma vardır. İlk olarak, eğer çoğaltıcı sola veya sağa hareket ederken yukarı kaldırılırsa oval şekilli koloniler oluşturmak mümkündür (Şekil 3B, turuncu ok). Ek olarak, mikrokoloniler, pin çoğaltıcısı bir açıyla getirilirse veya plakanın üzerinde çalkalanırsa, küçük hücre çözeltisi damlacıklarından da oluşabilir (Şekil 3B, kırmızı ok). Genellikle zararsız, bazen mikrokoloniler damgalı bir koloni ile karışabilir ve bu da o koloninin yorumlanmasını önler. Ek kaplama sorunları arasında, sterilizasyondan sonra çoğaltıcı pimlerin soğuması için yetersiz bekleme süresi ve plaka ile pimler arasında yetersiz temas bulunur, böylece kültür ortamının zayıf transferi gerçekleşir. Her iki durumda da, eğer varsa, vahşi tip muhabiri içeren kontrol suşları da dahil olmak üzere plakada çok az hücre büyüyecektir. Herhangi bir büyüme testinde olduğu gibi, kaplama yönteminden bağımsız olarak, sonuçların tutarlı ve tekrarlanabilir olduğunu doğrulamak için ACT1-CUP1'i üçlü olarak gerçekleştirmek önemlidir. İdeal olarak, bu farklı replikalar, tekrarlanabilirliği sağlamak için farklı zamanlarda hazırlanan bakır plakalar üzerinde yapılmalıdır.
Bu temsili deneyler için, A3c muhabiri, ek splisozom pertürbasyonlarının yokluğunda fikir birliği olmayan bir dizinin bakır toleransı üzerindeki etkisini vurgulamak için seçildi. A3c, splisozomun 5' SS15'i tanıma ve kullanma yeteneğini bozduğu için üretilen CUP1 mRNA miktarını önemli ölçüde azaltır. A3c muhabiri ile maya, 0.15 mM Cu2 + 'ya kadar hayatta kalırken, vahşi tip muhabir hücreleri, test edilen bakır konsantrasyonları aralığının sonuna kadar canlılığını korudu (Şekil 3C). Hücreleri içeren vahşi tip muhabir, canlılık üzerinde bir etkisi olmadan 2,5 mM Cu2 + 'ya kadar büyür (veriler gösterilmemiştir).
U6 snRNA, splisozomun önemli bir katalitik bileşenidir. Birçok çalışma, mutasyonların bu RNA 16,32,34 üzerindeki etkisini incelemek için ACT1-CUP1'i kullanmıştır. Bu çalışma için çoğaltılan üç U6 snRNA dizisi, yani vahşi tip dizi (WT), bir idrardan bir sitozine (U57c) ikame edilen pozisyon 57 ve bir idrardan bir adenosine (U57a) ikame edilen pozisyon 57 (Şekil 3 ve Şekil 4) incelenmiştir (Şekil 3 ve Şekil 4). Eklemedeki katalitik adımları etkileyen ACT1-CUP1 muhabirleri ile birleştiğinde, U57c'nin ilk katalitik adımı desteklediği ve U57a'nın ikinci adım 16,32'ye ilerlemeyi desteklediği belirlendi.
ACT1-CUP1 testine hazırlanmak için, U6 snRNA'nın genomik kopyası silinmiş ve U6 snRNA vahşi tip veya mutasyona uğramış dizileri plazmidlere dahil edilmiş bir suş oluşturuldu. U6 snRNA hücrenin önemli bir bileşeni olduğundan, hücre canlılığını korurken genomik U6 snRNA'yı ilk önce nakavt etmek, daha sonra plazmidler üzerinde mutasyona uğramış U6 snRNA'ları tanıtmak ve son olarak ACT1-CUP1 muhabirlerini eklemek için üç ayrı dönüşüm kullanıldı. İlk dönüşüm için, U6 snRNA'nın genomik kopyasının nakavtında bir cup1Δ maya suşu kullanıldı ve aynı anda canlılığı korumak için bir URA seçim belirteci plazmidine WT U6 snRNA eklendi. Daha sonraki bir dönüşüm, bir TRP seçim işaretleyicisi plazmidine vahşi tip veya mutasyona uğramış U6 snRNA ekledi ve 5-FOA seçimi yoluyla URA işaretleyicisine karşı seçim yaptı. Böylece, her biri U6 snRNA dizilerinden birine, yani WT, U57a ve U57c'ye sahip üç cup1Δ maya suşu üretildi. Her suş için son bir maya dönüşümü, bu deneyde kullanılacak üç farklı ACT1-CUP1 muhabir plazmidinden birini ekledi. Seçilen muhabirler, vahşi tip muhabir A3c ve dal bölgesi adenozininin guanine (BS-G) mutasyonuydu. Bu deney için, her biri bir U6 snRNA dizisi ve bir ACT1-CUP1 muhabiri içeren toplam dokuz suş üretildi (Ek Tablo 4 ve Ek Tablo 5).
Sonuçlar, U6 snRNA pozisyonu 57'deki farklı bazların, 5' SS veya BS mutasyonu ile kombinasyon halinde splisozom üzerinde benzersiz etkilere sahip olduğunu göstermiştir (Şekil 4). Hem A3c hem de BS-G muhabirleri, ilk katalitik adım konformasyonu 14,15'i stabilize ederek eklemeyi inhibe eder. Bu nedenle, U57c, bu muhabirlerden herhangi biriyle kombinasyon halinde bakır toleransını azaltan bir katkı mutasyonudur (Şekil 4B). Buna karşılık, U57a bakır toleransını arttırır çünkü ikinci adıma ilerlemeyi teşvik eder (Şekil 4B)16,32. BS-G muhabir suşunun U57a ile U6 snRNA WT'ye kıyasla azalan bakır toleransı, BS-G'nin16'yı eklemenin ikinci adımı üzerindeki olası ikincil etkisini vurgulamaktadır.
Bu sonuçlar aynı zamanda bu tahlilin nitel doğasını ve neden vahşi tip sorgu ve muhabir dizilerinin test edilmesi gerektiğini vurgulamaktadır. Artan veya azalan bakır toleransının genel paterni, vahşi tip U6 snRNA'ya kıyasla bu U6 snRNA mutasyonları için geçerli olsa da, hücrelerin hayatta kaldığı kesin bakır konsantrasyonu çalışmalar arasında farklılık gösterebilir (Tablo 1) ve bu temsili veriler ile diğer yayınlanmış sonuçlar arasında farklılık göstermiştir. Bu muhtemelen CUP1 delesyonunu içeren suşun arka planından kaynaklanmaktadır, ancak kaplamadan önce suşların genel sağlığından da kaynaklanabilir (yani, gerinimin üretilmesinden veya kriyodan restreak'ın üretilmesinden ne kadar kısa bir süre sonra tahlilin yapıldığı), plakaların nasıl hazırlandığı konusundaki farklılıklar ve farklı inkübatörler arasındaki değişkenlik. Benzer bir varyans Mayerle ve ark.'da da literatürdeki Prp8 sorgu mutasyonları için not edilmiştir43. Bu nedenle, farklı ACT1-CUP1 testleri için bakır tolerans eğilimlerinin karşılaştırılması yapılabilir, ancak bakır konsantrasyonlarının sayısal karşılaştırması yalnızca aynı laboratuarda ve bazen aynı bakır plaka seti ile yapılmalıdır.
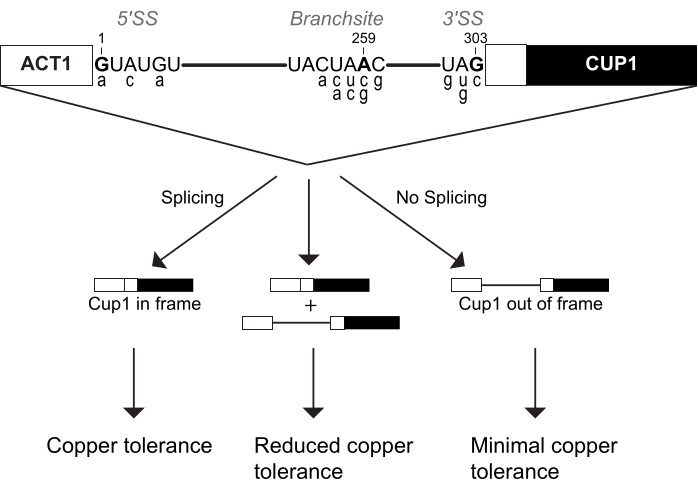
Resim 1: ACT1-CUP1 muhabir tasarımı. Eklenmiş muhabirin konsantrasyonu, maya bakır toleransı ile doğrudan ilişkilidir. Raporlayıcının diyagramı, 5' ekleme sitesinin (5' SS), dal-sitenin (BS) ve 3' ekleme sitesinin (3' SS) üç ekleme sitesini içerir. Bu bölgeler için maya konsensüs dizileri, bölünme için hedeflenenler kalın olarak gösterilir ve introndaki konumlarına göre numaralandırılır. Yaygın olarak kullanılan konsensüs dışı ACT1-CUP1 muhabir dizileri, karşılık gelen konsensüs dizisi konumlarının altında küçük harfle gösterilir ve Tablo 1'de listelenir. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.

Şekil 2: ACT1-CUP1 tahlil iş akışı. Bu test için, bir maya suşu cup1Δ leu2 olmalı ve istenen ACT1-CUP1 muhabir plazmidini ve şekilde Gen etiketli QSP genini içermelidir. QSP geni ya genomik olarak yerleştirilmeli ya da bir plazmid üzerine yerleştirilmelidir. Bir pin çoğaltıcısı kullanan protokol, maya hücrelerini hazırlamak için dört adımdan oluşur. Adım 1, hücreleri doygunluğa kadar büyütmektir. Adım 2, kültürün OD 600'ünü ölçmek ve 0.5'lik bir OD600'e seyreltmektir. Adım 3, 96 delikli bir plaka üzerine dağıtmaktır. Adım 4, artan konsantrasyonlarda bakır içeren plakalara plaka yapmaktır (artan mavi renkle gösterilir). Adım 1, adım 2 ve adım 4, elle pipetleme için aynı olacaktır. Kaplandıktan sonra, plakalar 30 ° C'de 3 gün boyunca inkübe edilir ve daha sonra canlılık için puanlanır. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.

Şekil 3: ACT1-CUP1 verilerinin temsili görünümleri. Bu deney için, maya splisozomlarına iki farklı U6 snRNA mutasyonu ile meydan okundu ve fikir birliği olmayan üç muhabirin varlığında test edildi. Bu tahlilin üç kopyası, gösterim amacıyla aynı plakalarda sunulmaktadır. Bu tahlilin ayrı plakalarda ve ayrı günlerde çoğaltma yapması önerilir. (A) 20 plaka üzerinde 0 mM ila 1,1 mM bakır gradyanı ile tamamlanmış bir tahlil gösterilir. Bakır konsantrasyonu arttıkça, daha düşük eklemeli suşlar, bakır konsantrasyonunun ölümcül hale geldiği noktaya kadar azalmış akıcılık gösterir. Maya arka planı ade2 idi ve bu nedenle olgun koloniler kırmızı renktedir. (B) Bir el kamerası ile dijital görüntüleme sistemi ile görüntülenen 0 mM ve 0,1 mM CuSO4'teki aynı plakaların karşılaştırılması. Bu, fikir birliği olmayan bazı muhabirlerin yan yana ve vahşi tip muhabirle nasıl karşılaştırılabileceğinin bir örneğidir. Plakalar üzerindeki yaygın gözlemler arasında, pim çoğaltıcısından (kırmızı ok) düşen sahte bir kültür ortamı damlası ve pimin plakanın yüzeyi boyunca kayması veya kültür damlası yeterince kurumadan önce plakanın hareketi (turuncu ok) nedeniyle kolonilerin hafif ovallanması sayılabilir. (C) A3c muhabirinin vahşi tip muhabire kıyasla hücre canlılığı üzerindeki etkisinin örneği. (B)'de gösterilenler gibi görüntüler, farklı bakır konsantrasyonlarındaki büyüme farklılıklarını vurgulamak için kırpılır ve hizalanır. A3c muhabir suşunun bakır toleransı, vahşi tip muhabir suşunun test edilen aralığın sonuna kadar yaşayabilirliğine kıyasla 0,15 mM Cu2 + 'ya düşer. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.
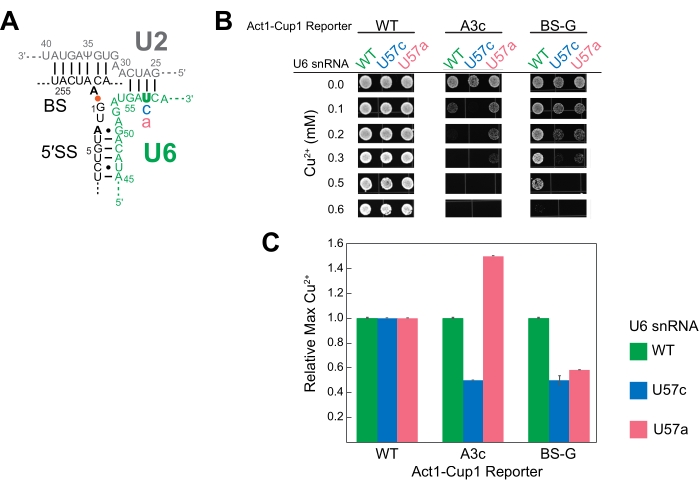
Şekil 4: Temsili ACT1-CUP1 sonuçları, ekleme bileşeni mutasyonları ile mayadaki eklemeyi izler . (A) İlk katalitik adımdan hemen sonra aktif bölgenin RNA bileşenlerinin şeması. U2 ve U6 snRNA'lar dublekse edilerek intron'un 5' SS ve BS'sini yakınlaştırır. A259 (BS) ve G1 (5' SS) arasındaki tronik bağ turuncu nokta ile gösterilir. Bu deneyde test edilen ACT1-CUP1 muhabirindeki fikir birliği olmayan dizi ikamelerinin yerleri koyu siyah renkle belirtilmiştir. U6 snRNA'daki (U57) mutasyona uğramış konum koyu yeşil renktedir ve ikame edilen bazlar mavi veya pembedir. (B) ACT1-CUP1 verilerinin bir yayında sunulması için bir olasılık, ilgili Cu2 + konsantrasyonlarından kolonilerin birkaç görüntüsünü içerir. WT muhabiri, sorgulanan üç U6 snRNA suşu için test edilen bakır konsantrasyonunu geçerek hayatta kaldı. (C) Muhabir başına ve U6 snRNA mutantı başına etkileri karşılaştıran bir çubuk grafik. Her ACT1-CUP1 muhabiri için normalleştirme, U6 snRNA WT'nin bakır toleransını 1'e ayarlayarak ve U57c ve U57a mutasyonlarının oranını hesaplayarak gerçekleştirilir. Hata çubukları, üç çoğaltmadan standart sapmayı temsil eder. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.
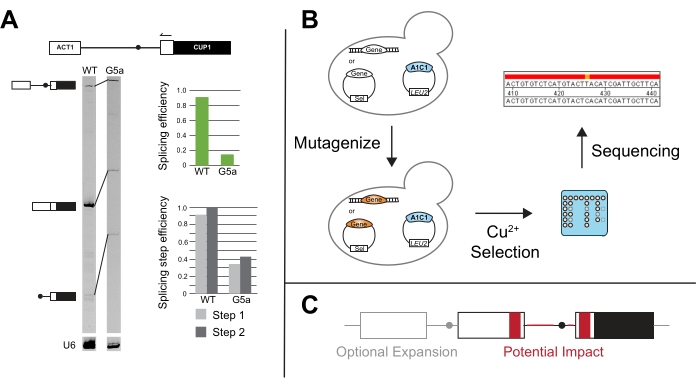
Şekil 5: ACT1-CUP1 sonuçlarını iltifat etmek için ek yöntemler. (A) Astar uzatması, 3' ACT1 ekzonunda bir astar tavlama ve daha sonra introna uzatılmış olarak gerçekleştirilir. Bu örnekte, astar IR700 boyası ile son etiketlenmiştir ve astar uzatması 20,21'de açıklandığı gibi gerçekleştirilmiştir. U6 snRNA'nın primer uzaması, yükleme kontrolü görevi görmek için aynı reaksiyonda gerçekleştirilir. % 7 19: 1 bis / akrilamid, denatüre jel, van der Feltz ve ark.22'de açıklandığı gibi yakın bir kızılötesi jel görüntüleme cihazı kullanarak primer uzatmadan sonra pre-mRNA, mRNA ve lariat ürünlerini çözer. Farklı bantların yoğunluğu, genel olarak ekleme verimliliğini ölçmek ve ImageJ44 veya başka bir jel bant ölçüm yazılımı ile ölçüldüğü gibi, birinci veya ikinci adımda meydana gelen ekleme farklılıklarını ayırt etmek için kullanılabilir. Hem ekleme verimliliği hem de ekleme adımı verimliliği, Query ve Konarska14'te açıklandığı gibi hesaplanır. (B) ACT1-CUP1 muhabirlerine sahip mutasyonel ekranlar, eklemeyi etkileyen mutantları tanımlamak için bakır seçimini kullanabilir. İlgilenilen gen (ler) daha sonra mutasyonun o gende meydana gelip gelmediğini belirlemek için ortaya çıkan suşlarda sıralanabilir. (C) İntron yapısı, ekzonik diziler, ekzon sayısı veya eklenmemiş RNA'nın nükleer ihracatı ile ilgili ekleme değişikliklerini izlemek için ekleme bölgelerinin dışındaki muhabire değişiklikler yapılabilir. Gri renkteki bölgeler, bir raportöre dahil edilecek isteğe bağlı genişleme bölgeleridir ve kırmızı renkteki alanlar, ACT1-CUP1 testi kullanılarak ekleme üzerindeki potansiyel etkileri açısından dizi ve yapısal değişikliklerin test edilebileceği bölgelerdir. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.
| Muhabirin adı | Intronic bölgesi | Sıra | Son uygulanabilir Cu2+ konsantrasyonu (mM) | |
| WT | 5' | GUAUGU | > 2.5 | |
| G1a | 5ʹ | a UAUGU | 0.0133 veya 0.0532 | |
| A3c | 5ʹ | GUcUGU | 0.15^,18 veya 0.216 | |
| G5a | 5ʹ | GUAUaU | 0.303 veya 0.259 | |
| WT | Şube-site | UACUAAC | > 2.5 | |
| C256a · | Şube-site | UAbirUAAC | 0.1526 veya 0.1832 | |
| U257c/a | Şube-site | UACc/aAAC | 0.226 veya 0.332 veya 0.545 | 0.059,32 |
| A258c/u | Şube-site | UACUc/uAC | 0.826 | 1.045 veya 1.646 |
| Lisans-C | Şube-site | UACUAcC | 0.153 veya 0.1832,56 veya 0.226 | |
| BS-G | Şube-site | UACUAgC | 0.0516,32 veya 0.625 veya 0.846 | |
| C260g | Şube-site | UACUAAg | 0.826 | |
| WT | 3' | UAG (UAG) | > 2.5 | |
| U301g | 3ʹ | g (Genel) AG | 0.1518 | |
| A302g/u | 3' | Ug/uG | 0.0139 | 0.07516 veya 0.1824 |
| G303c | 3ʹ | UAc | 0.0532 | |
Tablo 1: Ortak muhabirlerin listesi ve bildirilen Cu2+ konsantrasyon öldürücülüğü. Lesser ve Guthrie3'ün 100'den fazla alıntısı vardır. Bu tabloyu oluşturmak için bu alıntıların küçük bir kısmı kullanılmış olsa da, rapor edilen bakır canlılık konsantrasyonlarındaki çalışmalar arasındaki hafif ila orta dereceli farklılıkların genel eğilimini vurgulamaktadırlar. ACT1-CUP1'de, vahşi tip protein veya RNA'yı, yayınlanan konsantrasyonları bir rehber olarak kullanarak, ancak gözlemlenen konsantrasyonların farklı olabileceğini öngörerek, aynı maya suşu arka planına sahip mutantlarla karşılaştırmak önemlidir. Şekil 3'ten (^) ve aşağıdaki atıflarla ek açıklamalı birden fazla yayından toplanan veriler 3,9,16,18,24,25,26,32,45,46.
Ek Tablo 1: Tek bir bakır levhanın içeriği ve 1 M CuSO4 stokundan 0 mM'den 2,5 mM'ye kadar bakır seyreltmeleri elde etmek için yapılan hesaplamalara bir örnek. Bu tabloyu indirmek için lütfen tıklayınız.
Ek Tablo 2: 48 pimli çoğaltıcı için kaplama şeması örneği. Bu tabloyu indirmek için lütfen tıklayınız.
Ek Tablo 3: 30 ° C'de 3 gün boyunca inkübe edilen bakır plakalardan elde edilen canlılık örneği. Bu tabloyu indirmek için lütfen tıklayınız.
Ek Tablo 4: Temsili verileri oluşturmak için kullanılan maya suşlarının listesi. Bu tabloyu indirmek için lütfen tıklayınız.
Ek Tablo 5: Temsili verileri oluşturmak için kullanılan plazmidlerin listesi. U6 snRNA plazmidleri üretilmiş ve önceki araştırmalarda yayınlanmıştır 22,47. Bu tabloyu indirmek için lütfen tıklayınız.
Tartışmalar
ACT1-CUP1 bir büyüme testidir ve gözlemlenen büyüme farklılıklarının yalnızca ekleme kusurlarına atfedilebilmesini sağlamak için özen gösterilmelidir. Tüm suşlar, benzer uzunluk ve büyüme ve depolama koşullarına sahip olmak da dahil olmak üzere, kaplamadan önce benzer bir şekilde ele alınmalıdır. Sıcaklığa duyarlı suşlar kullanılıyorsa, ACT1-CUP1 testleri yalnızca bu suşların vahşi tiple karşılaştırılabilir şekilde büyüdüğü koşullar altında yapılmalıdır. İlgili olarak, QSP bileşeni için, sonuçların yorumlanmasını bulanıklaştırmamak için QSP genlerinin aynı maya arka planlarına ve ekspresyon seviyelerine sahip olması önerilir. Kullanılacak QSP'lerin ve muhabirlerin sayısı göz önüne alındığında, pin çoğaltıcı yöntemiyle bir seferde 30'dan fazla suşun tahlil edilmesi önerilmez. Her adımı gerçekleştirmek için ek süre ile, hücreler yerleşecek ve tahlil sonuçları, azalan hücre canlılığı nedeniyle tutarsız olacaktır.
ACT1-CUP1'in doğası gereği bir büyüme testi olarak sahip olduğu sınırlamalara ek olarak, bir QSP'nin ekleme üzerinde bu yöntemle çözülebileceğinden daha karmaşık bir etkisi olabilir. Ekleme çok adımlı bir işlem olduğundan ve faktörler geri dönüştürüldüğünden, gözlemlenen fenotip, birden fazla ekleme adımını etkileyen pertürbasyona neden olabilir. Bu, bazıları aşağıda açıklanan ACT1-CUP1'i takip edebilecek sonraki analizler için bile geçerlidir. Veriler, diğer adımlar ekleme faktörünün değiştirilmiş işlevinden etkilenebilse de, sürecin en tedirgin edici adımını vurgulayacaktır.
ACT1-CUP1 muhabirlerinin primer uzantısı ilk olarak Lesser ve Guthrie'nin orijinal makalesinde kullanılmıştır ve ACT1-CUP1 sonuçları bir büyüme kusuru3 gösteriyorsa sıklıkla gerçekleştirilir. Bu tahlil muhabiri hedefler ve mevcut eklenmemiş, kısmen eklenmiş ve tamamen eklenmiş muhabirin göreceli miktarlarını belirlemek için PCR ürünlerinin uzunluğunu kullanır (Şekil 5A). Genel ekleme verimliliği ve kusurun birinci veya ikinci katalitik adımı daha güçlü etkileyip etkilemediği, PCR ürün miktarlarının14 oranları alınarak hesaplanır. Örneğin, 5' SS muhabiri G5a, vahşi tip muhabire kıyasla eklemeyi azaltmıştır, ancak birinci ve ikinci adım verimlilikleri vahşi tipe benzer bir model izlemektedir (Şekil 5A). Bu, ilk katalitik adımdan önce, muhtemelen ekleme düzeneğinde bir kusura işaret eder, çünkü her iki adım da benzer şekilde etkilenir31.
Kanonik ACT1-CUP1 tahlilinden yeni tahliller geliştirilmiştir, örneğin diğer ekleme faktörü mutantlarının varlığında eklemeyi geliştiren mutantların taranması ve / veya konsensüs dışı ekleme dizileri (Şekil 5B). Örneğin, ACT1-CUP1 muhabirini içeren mayayı UV'ye maruz bırakmak ve daha sonra bakır varlığında seçmek, fikir birliği olmayan dizilerin 14,19'un eklenmesini geliştiren Prp8 ve Hsh155 mutantlarını verdi.
Ekleme bölgelerinin ve kurucu ekleme faktörlerinin etkisinin incelenmesini genişleten CUP1 büyüme bağımlılığı, çoklu intron ekleme, nükleer ihracat kontrolü ve UTR ve diğer periferik dizilerin ekleme üzerindeki etkisini incelemek için kullanılmıştır (Şekil 5C). Bu çalışmalardan bazıları, intronic ikincil yapı ve çoklu intron transkript ekleme 48,49,50,51,52 üzerindeki etkisini incelemek için daha karmaşık ekleme modellerine sahip olabilen CUP1 ve diğer intron içeren maya genlerine sahip muhabirler yaratmıştır. Ekleme ve nükleer ihracat arasındaki bağlantı,çerçeve 53,54'te CUP1'i kodlayan eklenmiş veya eklenmemiş transkriptlere sahip olarak incelenmiştir. Pirimidin iz uzunluğunun uzunluğu ve ekleme yeri seçiminin spesifik faktörlere bağlı mesafe bağımlılığı da test edilmiştir 20,55,56,57. Bu örnekler ve diğerleri, ACT1-CUP1 ve diğer CUP1 büyüme tahlillerinin çok yönlülüğünü vurgulamaktadır.
ACT1-CUP1 testi, pertürbasyonları geniş bir hassasiyet aralığına sahip basit bir büyüme fenotipi ile karmaşık bir reaksiyon döngüsüne bağlar. Bu eski tahlil, ekleme döngüsünün anlaşılmasının temelini atmak için birden fazla laboratuvar tarafından kullanılmıştır. Daha yakın zamanlarda, ACT1-CUP1, şu anda mevcut olan21,22,25 yapısal verilerin zenginliğinden kaynaklanan soruları cevaplamak için kullanılmıştır. Konsensüs dışı sekanslara bağlı splisozomların yapısal çalışmaları, değiştirilmiş yapı ve değiştirilmiş fonksiyonun nasıl ilişkili olduğunu yorumlamak için ACT1-CUP1 sonuçlarıyla eşleştirilebilir. ACT1-CUP1, daha karmaşık analizleri tamamlayabilecek mutasyonları eklemek için ideal bir ilk ekrandır.
Açıklamalar
Yazarın açıklayacak hiçbir şeyi yoktur.
Teşekkürler
Aaron Hoskins ve Wisconsin-Madison Üniversitesi'ndeki Hoskins laboratuvar üyelerine, şekil 3-5 neslinde maya suşlarının ve ekipmanlarının kullanımı için teşekkür ederiz. Harpreet Kaur ve Xingyang Fu'ya el yazması hakkındaki anlayışlı yorumları için teşekkür ederiz. Northwest University'deki destekleyici öğrencilere, personele ve fakülteye bu makalenin yazılması, düzenlenmesi ve filme alınması sırasında teşekkür ederiz. Bu yöntemin filme alınmasında yardım için Isabelle Marasigan'a teşekkür ederiz.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 1.5 mL sterile microcentrifuge tubes | Fisher Scientific | 05-408-129 | Or comparable item from a different manufacturer. |
| 2 mL sterile microcentrifuge tubes | Fisher Scientific | 05-408-138 | Or comparable item from a different manufacturer. |
| 50 mL sterile centrifuge tubes | Fisher Scientific | 07-201-332 | Or comparable item from a different manufacturer. |
| 96-well round bottom microplate | Fisher Scientific | 07-200-760 | Or comparable item from a different manufacturer. |
| 190 proof ethanol | Fisher Scientific | 22-032-600 | Or comparable item from a different manufacturer. |
| 500 mL Filter System (0.22 µm) | CellTreat Scientific Products | 229707 | Or comparable item from a different manufacturer. |
| Agar | Fisher Scientific | BP1423-500 | Any molecular grade agar will work. |
| Autoclave | Tuttnauer | 3870EA | Or comparable item from a different manufacturer. |
| Bunsen burner | Humboldt | PN6200.1 | Or comparable item from a different manufacturer. |
| Cell Density Meter | VWR | 490005-906 | Or other spectral device that can measure absorbance at 595 nm. |
| Copper sulfate Pentahydrate | Fisher Scientific | LC134051 | Or comparable item from a different manufacturer. |
| Digital imaging system | Cytiva | 29399481 | ImageQuant 4000 (used for Figure 3), Amersham ImageQuant 800, or comparable item from a different manufacturer. |
| Dropout mix (-Leu) | USBiological Life Sciences | D9525 | Use the appropriate drop out mix for your experiment. It is possible you will be using a yeast nutrient marker for your query perturbation also. In that case, the drop out mix should be for that marker and Leu |
| D-Glucose | Fisher Scientific | AAA1682836 | Or comparable item from a different manufacturer. |
| Gel band quantifying software | Cytiva | 29-0006-05 | ImageQuant TL v8.1 (used for figure 5A) or comparable item from a different manufacturer. |
| Hand held camera | Nikon | D3500 | Or comparable item from a different manufacturer. |
| Near infra-red gel imaging device | Cytiva | 29238583 | Amersham Typhoon NIR (used for Figure 5a) or comparable item from a different manufacturer. |
| Laboratory grade clamp | Fisher Scientific | 05-769-7Q | Or comparable item from a different manufacturer. |
| Laboratory grade stand and clamp | Fisher Scientific | 12-000-101 | Or comparable item from a different manufacturer. |
| Magnetic stir bars | Fisher Scientific | 14-513-51 | Or comparable item from a different manufacturer. |
| Pin replicator | VP Scientific | VP 407AH | |
| Semi-micro disposable cuvettes | VWR | 97000-590 | Or comparable item from a different manufacturer. |
| Shaker | JEIO Tech | IST-3075 | Or comparable item from a different manufacturer. |
| Spectrophotometer | Biowave | 80-3000-45 | Or any spectophotometer that can measure the absorbance at 600 nm. |
| Square plates | VWR | 102091-156 | Circular plates may also be used though are more challenging if using a pin replicator. |
| Stir plate | Fisher Scientific | 11-520-16S | Or comparable item from a different manufacturer. |
| Yeast nitrogen base | USBiological Life Sciences | Y2025 | Or comparable item from a different manufacturer. |
Referanslar
- Wahl, M. C., Will, C. L., Luhrmann, R. The spliceosome: Design principles of a dynamic RNP machine. Cell. 136 (4), 701-718 (2009).
- Wilkinson, M. E., Charenton, C., Nagai, K. RNA splicing by the spliceosome. Annual Review of Biochemistry. 89, 359-388 (2020).
- Lesser, C. F., Guthrie, C. Mutational analysis of pre-mRNA splicing in Saccharomyces cerevisiae using a sensitive new reporter gene, CUP1. Genetics. 133 (4), 851-863 (1993).
- Ng, R., Abelson, J. Isolation and sequence of the gene for actin in Saccharomyces cerevisiae. Proceedings of the National Academy of Sciences of the United States of America. 77 (7), 3912-3916 (1980).
- Gallwitz, D., Sures, I. Structure of a split yeast gene: Complete nucleotide sequence of the actin gene in I. Proceedings of the National Academy of Sciences of the United States of America. 77 (5), 2546-2550 (1980).
- Fogel, S., Welch, J. W., Cathala, G., Karin, M. Gene amplification in yeast: CUP1 copy number regulates copper resistance. Current Genetics. 7 (5), 347-355 (1983).
- Hamer, D. H., Thiele, D. J., Lemontt, J. E. Function and autoregulation of yeast copperthionein. Science. 228 (4700), 685-690 (1985).
- Winge, D. R., Nielson, K. B., Gray, W. R., Hamer, D. H. Yeast metallothionein. Sequence and metal-binding properties. Journal of Biological Chemistry. 260 (27), 14464-14470 (1985).
- Burgess, S. M., Guthrie, C. A mechanism to enhance mRNA splicing fidelity: The RNA-dependent ATPase Prp16 governs usage of a discard pathway for aberrant lariat intermediates. Cell. 73 (7), 1377-1391 (1993).
- Collins, C. A., Guthrie, C. Allele-specific genetic interactions between Prp8 and RNA active site residues suggest a function for Prp8 at the catalytic core of the spliceosome. Genes & Development. 13 (15), 1970-1982 (1999).
- Siatecka, M., Reyes, J. L., Konarska, M. M. Functional interactions of Prp8 with both splice sites at the spliceosomal catalytic center. Genes & Development. 13 (15), 1983-1993 (1999).
- Umen, J. G., Guthrie, C. Mutagenesis of the yeast gene PRP8 reveals domains governing the specificity and fidelity of 3' splice site selection. Genetics. 143 (2), 723-739 (1996).
- Grainger, R. J., Beggs, J. D. Prp8 protein: At the heart of the spliceosome. RNA. 11 (5), 533-557 (2005).
- Query, C. C., Konarska, M. M. Suppression of multiple substrate mutations by spliceosomal prp8 alleles suggests functional correlations with ribosomal ambiguity mutants. Molecular Cell. 14 (3), 343-354 (2004).
- Konarska, M. M., Vilardell, J., Query, C. C. Repositioning of the reaction intermediate within the catalytic center of the spliceosome. Molecular Cell. 21 (4), 543-553 (2006).
- Liu, L., Query, C. C., Konarska, M. M. Opposing classes of prp8 alleles modulate the transition between the catalytic steps of pre-mRNA splicing. Nature Structural and Molecular Biology. 14 (6), 519-526 (2007).
- MacRae, A. J., et al. Prp8 positioning of U5 snRNA is linked to 5' splice site recognition. RNA. 24 (6), 769-777 (2018).
- Query, C. C., Konarska, M. M. CEF1/CDC5 alleles modulate transitions between catalytic conformations of the spliceosome. RNA. 18 (5), 1001-1013 (2012).
- Tang, Q., et al. SF3B1/Hsh155 HEAT motif mutations affect interaction with the spliceosomal ATPase Prp5, resulting in altered branch site selectivity in pre-mRNA splicing. Genes & Development. 30 (24), 2710-2723 (2016).
- Carrocci, T. J., Zoerner, D. M., Paulson, J. C., Hoskins, A. A. SF3b1 mutations associated with myelodysplastic syndromes alter the fidelity of branchsite selection in yeast. Nucleic Acids Research. 45 (8), 4837-4852 (2017).
- Kaur, H., Groubert, B., Paulson, J. C., McMillan, S., Hoskins, A. A. Impact of cancer-associated mutations in Hsh155/SF3b1 HEAT repeats 9-12 on pre-mRNA splicing in Saccharomyces cerevisiae. PLoS One. 15 (4), 0229315(2020).
- vander Feltz, C., et al. Saccharomyces cerevisiae Ecm2 modulates the catalytic steps of pre-mRNA splicing. RNA. 27 (5), 591-603 (2021).
- Carrocci, T. J., Paulson, J. C., Hoskins, A. A. Functional analysis of Hsh155/SF3b1 interactions with the U2 snRNA/branch site duplex. RNA. 24 (8), 1028-1040 (2018).
- Hogg, R., de Almeida, R. A., Ruckshanthi, J. P., O'Keefe, R. T. Remodeling of U2-U6 snRNA helix I during pre-mRNA splicing by Prp16 and the NineTeen Complex protein Cwc2. Nucleic Acids Research. 42 (12), 8008-8023 (2014).
- Hansen, S. R., Nikolai, B. J., Spreacker, P. J., Carrocci, T. J., Hoskins, A. A. Chemical inhibition of pre-mRNA splicing in living Saccharomyces cerevisiae. Cell Chemical Biology. 26 (3), 443-448 (2019).
- Xu, Y. Z., Query, C. C. Competition between the ATPase Prp5 and branch region-U2 snRNA pairing modulates the fidelity of spliceosome assembly. Molecular Cell. 28 (5), 838-849 (2007).
- Staley, J. P., Guthrie, C. An RNA switch at the 5' splice site requires ATP and the DEAD box protein Prp28p. Molecular Cell. 3 (1), 55-64 (1999).
- Bousquet-Antonelli, C., Presutti, C., Tollervey, D. Identification of a regulated pathway for nuclear pre-mRNA turnover. Cell. 102 (6), 765-775 (2000).
- Villa, T., Guthrie, C. The Isy1p component of the NineTeen complex interacts with the ATPase Prp16p to regulate the fidelity of pre-mRNA splicing. Genes & Development. 19 (16), 1894-1904 (2005).
- Mayas, R. M., Maita, H., Staley, J. P. Exon ligation is proofread by the DExD/H-box ATPase Prp22p. Nature Structure and Molecular Biology. 13 (6), 482-490 (2006).
- Lesser, C. F., Guthrie, C. Mutations in U6 snRNA that alter splice site specificity: Implications for the active site. Science. 262 (5142), 1982-1988 (1993).
- McPheeters, D. S. Interactions of the yeast U6 RNA with the pre-mRNA branch site. RNA. 2 (11), 1110-1123 (1996).
- Perriman, R. J., Ares, M. Rearrangement of competing U2 RNA helices within the spliceosome promotes multiple steps in splicing. Genes & Development. 21 (7), 811-820 (2007).
- Mefford, M. A., Staley, J. P. Evidence that U2/U6 helix I promotes both catalytic steps of pre-mRNA splicing and rearranges in between these steps. RNA. 15 (7), 1386-1397 (2009).
- Hilliker, A. K., Mefford, M. A., Staley, J. P. U2 toggles iteratively between the stem IIa and stem IIc conformations to promote pre-mRNA splicing. Genes & Development. 21 (7), 821-834 (2007).
- Wu, G., et al. Pseudouridines in U2 snRNA stimulate the ATPase activity of Prp5 during spliceosome assembly. EMBO Journal. 35 (6), 654-667 (2016).
- Crotti, L. B., Bacikova, D., Horowitz, D. S. The Prp18 protein stabilizes the interaction of both exons with the U5 snRNA during the second step of pre-mRNA splicing. Genes & Development. 21 (10), 1204-1216 (2007).
- Fogel, S., Welch, J. W. Tandem gene amplification mediates copper resistance in yeast. Proceedings of the National Academy of Sciences of the United States of America. 79 (17), 5342-5346 (1982).
- Gardner, J. M., Jaspersen, S. L. Manipulating the yeast genome: Deletion, mutation, and tagging by PCR. Methods Molecular Biology. 1205, 45-78 (2014).
- JoVE. Yeast Transformation and Cloning. In Biology I: yeast, Drosophila and C. Elegant. JoVE Science Education Database. , Cambridge, MA. (2021).
- Gietz, R. D., Woods, R. A. Yeast transformation by the LiAc/SS Carrier DNA/PEG method. Methods Molecular Biology. 313, 107-120 (2006).
- Gietz, R. D., Woods, R. A. Genetic transformation of yeast. Biotechniques. 30 (4), 816(2001).
- Mayerle, M., et al. Structural toggle in the RNaseH domain of Prp8 helps balance splicing fidelity and catalytic efficiency. Proceedings of the National Academy of Sciences of the United States of America. 114 (18), 4739-4744 (2017).
- Schindelin, J., et al. Fiji: An open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Beier, D. H., et al. Dynamics of the DEAD-box ATPase Prp5 RecA-like domains provide a conformational switch during spliceosome assembly. Nucleic Acids Research. 47 (20), 10842-10851 (2019).
- vander Feltz, C., DeHaven, A. C., Hoskins, A. A. Stress-induced pseudouridylation alters the structural equilibrium of yeast U2 snRNA Stem II. Journal of Molecular Biology. 430 (4), 524-536 (2018).
- Rodgers, M. L., Didychuk, A. L., Butcher, S. E., Brow, D. A., Hoskins, A. A. A multi-step model for facilitated unwinding of the yeast U4/U6 RNA duplex. Nucleic Acids Research. 44 (22), 10912-10928 (2016).
- Stutz, F., Rosbash, M. A functional interaction between Rev and yeast pre-mRNA is related to splicing complex formation. EMBO Journal. 13 (17), 4096-4104 (1994).
- Libri, D., Lescure, A., Rosbash, M. Splicing enhancement in the yeast rp51b intron. RNA. 6 (3), 352-368 (2000).
- Libri, D., Stutz, F., McCarthy, T., Rosbash, M. RNA structural patterns and splicing: Molecular basis for an RNA-based enhancer. RNA. 1 (4), 425-436 (1995).
- Howe, K. J., Kane, C. M., Ares, M. Perturbation of transcription elongation influences the fidelity of internal exon inclusion in Saccharomyces cerevisiae. RNA. 9 (8), 993-1006 (2003).
- Cuenca-Bono, B., et al. SUS1 introns are required for efficient mRNA nuclear export in yeast. Nucleic Acids Research. 39 (19), 8599-8611 (2011).
- Scherrer, F. W., Spingola, M. A subset of Mer1p-dependent introns requires Bud13p for splicing activation and nuclear retention. RNA. 12 (7), 1361-1372 (2006).
- Hálová, M., et al. Nineteen complex-related factor Prp45 is required for the early stages of cotranscriptional spliceosome assembly. RNA. 23 (10), 1512-1524 (2017).
- Umen, J. G., Guthrie, C. A novel role for a U5 snRNP protein in 3' splice site selection. Genes & Development. 9 (7), 855-868 (1995).
- Crotti, L. B., Horowitz, D. S. Exon sequences at the splice junctions affect splicing fidelity and alternative splicing. Proceedings of the National Academy of Sciences of the United States of America. 106 (45), 18954-18959 (2009).
- Perriman, R., Ares, M. Invariant U2 snRNA nucleotides form a stem loop to recognize the intron early in splicing. Molecular Cell. 38 (3), 416-427 (2010).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır