Method Article
מבחני ACT1-CUP1 קובעים את הרגישויות הספציפיות למצע של מוטנטים שחבורים בשמרים ניצנים
In This Article
Summary
בדיקת ACT1-CUP1, בדיקת גידול נחושת, מספקת קריאה מהירה של שחבור RNA שליח מבשר (pre-mRNA) וההשפעה שיש לגורמי שחבור מוטנטיים על תפקוד השחבור השחבור. מחקר זה מספק פרוטוקול ומדגיש את ההתאמה האישית האפשרית כדי להתמודד עם שאלת השחבור המעניינת.
Abstract
מוטציות שהוכנסו בספליקוזום או במצע שלו תרמו באופן משמעותי להבנתנו את המורכבות של תפקוד השחבור. בין אם הן קשורות למחלה או נבחרו באופן פונקציונלי, רבות מהמוטציות הללו נחקרו באמצעות מבחני גדילה באורגניזם המודל Saccharomyces cerevisiae (שמרים). בדיקת צמיחת הנחושת הספציפית לשחבור, או בדיקת ACT1-CUP1, מספקת ניתוח מקיף של מוטציה ברמה הפנוטיפית. בדיקת ACT1-CUP1 משתמשת בעיתונאים המעניקים עמידות לנחושת כאשר הם מחוברים כהלכה. לפיכך, בנוכחות נחושת, שינויים בכדאיות השמרים מתואמים לשינויים בייצור mRNA באמצעות שחבור. בניסוי טיפוסי, שחבור השמרים מאותגר עם כתבי שחבור שונים שאינם בקונצנזוס ומוטציה של גורם שחבור מעניין כדי לזהות כל השפעה סינרגטית או אנטיתטית על השחבור. כאן ניתן תיאור מלא של הכנת לוחות נחושת, ציפוי של תאי שמרים והערכת נתונים. מתואר מבחר של ניסויים משלימים, המדגישים את הרבגוניות של כתבי ACT1-CUP1. בדיקת ACT1-CUP1 היא כלי שימושי בארגז הכלים של השחבור הודות לקריאה ישירה של אפקטים מוטציוניים והאפשרויות ההשוואתיות מהמשך השימוש בשטח.
Introduction
השחבור הוא מכונה ביולוגית גדולה המזרזת הסרה של אינטרונים, אזורים שאינם מקודדים ב-RNA שליח מבשר (pre-mRNA)1,2. אפיון ההשפעה של מוטציה נקודתית אחת ב-1 מתוך כמעט 100 חלבונים ו-5 רנ"א שאינם מקודדים הוא לעתים קרובות דו-משמעי כאשר חוקרים את החלבון או הרנ"א בבידוד. את השינוי בתפקוד הרכיב המוטנטי ניתן להעריך בצורה הטובה ביותר in vivo בהקשר של השחבור המלא והמתפקד.
בדיקת צמיחת הנחושת המתוארת כאן היא מדד מהיר של יעילות שחבור ב- Saccharomyces cerevisiae או שמרים ניצנים. בדיקה זו, שפותחה על ידי C.F. Lesser ו- C. Guthrie ופורסמה בשנת 1993, משלבת את קלות העבודה עם אורגניזם מודל פשוט ואת הקריאה הפשוטה של כדאיות התא3. הכדאיות מתואמת עם מידת היכולת של השחבורים בתאים אלה לזהות ולפצל את תעתיק הכתב.
בדיקת גידול נחושת זו נקראת בדרך כלל בדיקת ACT1-CUP1. השם ACT1-CUP1 מקורו בשני הגנים שהתמזגו ליצירת כתב של יעילות שחבור. ACT1 הוא גן האקטין של שמרים, אשר בא לידי ביטוי גבוה ויש לו אינטרוןשחבור יעיל 4,5. Cup1p הוא צ'לטור נחושת המסנן נחושת בתא כדי למנוע הפרעה לתפקודים תאיים סדירים 6,7,8. כתב ACT1-CUP1 מכיל את הגנים האלה ברצף כך ש-CUP1 נמצא במסגרת הקריאה הנכונה רק אם מתרחשת שחבור קדם-mRNA של האינטרון של ACT1 (איור 1). חלבון הפיוז'ן המתקבל מכיל את 21 חומצות האמינו הראשונות של אקטין ואת חלבון Cup1p באורך מלא, מה שמגדיל את כדאיות השמרים בסביבה עשירה בנחושת3. לפיכך, עלייה בכמות השחבור של הכתב גורמת לריכוז גבוה יותר של Cup1p ולהתנגדות נחושת גבוהה יותר (איור 1). בהשוואה לגנים מדווחים אחרים, CUP1 משפיע על כדאיות התאים גם ברמות נמוכות, יש לו טווח רגישות רחב, וניתן להשתמש בו כדי לבחור ישירות עבור שחבור מוטציות 3,6,7. בנוסף, CUP1 אינו חיוני לצמיחת שמרים סטנדרטית, ולכן הומאוסטזיס תאי אינו מושפע במהלך ההתקנה לבדיקה זו. ACT1-CUP1, המשלים את מבחני המחיקה או הצמיחה בטמפרטורה, מספק מידע על ההשפעות על שחבור בתנאי גידול שמרים אופטימליים אחרים.
השחבור מזהה את המצע שלו באמצעות שלושה רצפים אינטרוניים, כלומר אתר שחבור 5' (5' SS), אתר הסתעפות (BS) ואתר שחבור 3' (3' SS). באתרים אלה נוצרו מספר רב של כתבי ACT1-CUP1 המכילים רצפים שאינם בקונצנזוס. מבחר מהכתבים הנפוצים ביותר של ACT1-CUP1 מוצג באיור 1 ובטבלה 1. מכיוון שהשחבור מקיים אינטראקציה עם כל אתר שחבור באופן ייחודי בנקודות שונות במחזור השחבור, ניתן לבחון את חוסנו של השחבור בשלבים שונים על סמך איזה כתב שאינו קונצנזוס משמש. כתבים שאינם בקונצנזוס נקראים על שם העמדה שעברה מוטציה בתוך האינטרון והבסיס שאליו הוא עבר מוטציה. לדוגמה, A3c הוא כתב עם מוטציה ב-5' SS, במיוחד מיקום 3 מהקונצנזוס אדנוזין לציטוזין. כתב זה יקיים אינטראקציה חזקה עם מוטציות spliceosome המשפיעות על בחירת 5' SS ושימוש. במחקר הראשוני שלהם, לסר וגות'רי קבעו אילו מוטציות SS 5' מעכבות שחבור3. מאוחר יותר באותה שנה, כתבים שאינם בקונצנזוס בכל שלושת אתרי השחבור פורסמו על ידי ברג'ס וגות'רי במסך מדכא של מוטציות ב-ATPase Prp16p9. בהשוואה בין קונצנזוס לכתבים שאינם בקונצנזוס, מבחן ACT1-CUP1 היה מפתח חשוב להבנת החוסן והסלקטיביות של שחבור השמרים ולהסקת התפקוד של שחבורים אחרים של אאוקריוטים.
מכיוון שכתבי ACT1-CUP1 שאינם בקונצנזוס חושים את השחבור להפרעה נוספת, ניתן לאפיין את ההשפעה של מוטציה של גורם שחבור יחיד באמצעות הכתבים שהיא משפיעה עליהם באופן חיובי או שלילי. זה יושם על שחבור שאלות מחקר במגוון דרכים. ראשית, בדיקת ACT1-CUP1 יכולה לשמש כבדיקה גנטית למוטציות בגורמי שחבור. לדוגמה, Prp8p, חלבון השחבור הגדול ביותר, משמש כפלטפורמה שעליה ליבת הרנ"א של השחבור מזרזת את תגובת השחבור. זה הסיק, בין השאר, באמצעות האופן שבו מוטנטים של Prp8p שיפרו או הפחיתו את השחבור של כתבי ACT1-CUP1 שונים 10,11,12,13,14,15,16,17. רכיבי חלבון אחרים של השחבור נחקרו גם הם באמצעות ACT1-CUP1, כולל Hsh155p, Cwc2p, Cef1p ו-Ecm2p 18,19,20,21,22,23,24,25. הסף האנרגטי של Prp16p וארבעה ATPases אחרים המעורבים במעבר spliceosomal נחקרו גם הם באמצעות בדיקה זו 9,26,27,28,29,30. הרנ"א הגרעיניים הקטנים (snRNAs) נחקרו בהרחבה תוך שימוש ב-ACT1-CUP1 כדי לזהות את רצפי הקדם-mRNA שהם מתאמים ואת השינויים במבנה המשני שה-snRNAs עוברים במהלך שחבור 3,31,32,33,34,35,36,37.
בדיקת ACT1-CUP1 דורשת זן שמרים שבו כל העותקים של הגן CUP1 הודבקו. מכיוון של-CUP1 יכול להיות מספר עותק גבוה 6,38, הכנה של מאמץ נוק-אאוט מלא יכולה לדרוש סיבובים מרובים או סינון נרחב. כתוצאה מכך, זני שמרים cup1Δ חולקו לעתים קרובות בין המעבדות, וכך גם הכתבים.
אם מוטציות בפקטור שחבור נבדקות מעותק פלסמיד, יש לדפוק את הגן מסוג בר עבור גורם זה. בנוסף, רקע השמרים אמור לאפשר בחירה של לפחות שני פלסמידים, אחד המכיל כתב ACT1-CUP1, באופן היסטורי על פלסמיד לבחירת חומרים מזינים של לאוצין, ואחד המכיל מוטציה או הפרעה במנגנון השחבור שייחקרו (איור 2). בדרך כלל, בבדיקה אחת, זני שמרים מרובים, שכל אחד מהם נושא את השאילתה splicing perturbation (QSP) וכתב אחר, יבדקו את השפעת השאילתה על השחבור.
המשתנים הבלתי תלויים במבחן ACT1-CUP1 מאפשרים לחוקר להעריך את חומרת ה-QSP. משתנים בלתי תלויים אלה הם ריכוז הנחושת ובחירתם של כתבים רבים שאינם בקונצנזוס. ראשית, כאשר זני השמרים גדלים על לוחות המכילים מגוון ריכוזי נחושת (איור 2), הגדרת הבדיקה כוללת בחירת השיפוע של הריכוזים שבהם נעשה שימוש. מחקרים יכולים להשתמש בשיפוע ריכוז נחושת קורס כדי לקבל קריאה ראשונית של הכדאיות ולאחר מכן לחזור על הבדיקה עם שיפוע עדין יותר כדי לזהות הבדלים עדינים בכדאיות. המשתנה השני הוא המגוון הרחב של כתבי ACT1-CUP1 שניתן לבדוק (איור 1 וטבלה 1). אם ה-QSP משפיע באופן שונה על כדאיות השמרים בנוכחות כתב שאינו קונצנזוס לעומת סוג פראי, ניתן להסיק מסקנה שה-QSP משפיע על שלב בשחבור או על אזור של השחבור החשוב במהלך הזיהוי או העיבוד של אותו אזור של האינטרון.
ארגז הכלים של השמרים הוא נרחב, ובדיקת ACT1-CUP1 היא חלק בלתי נפרד ממחקר השחבור. בדיקת ACT1-CUP1 מבוצעת לעתים קרובות לצד ניתוח גנטי, מבני ו/או ביוכימי מעמיק יותר על ההשפעה של QSP. מכיוון שלמחקרים מפורטים יותר אלה יש בדרך כלל הליך ארוך יותר ו/או תג מחיר גבוה יותר, גישה שכיחה היא סינון מוטנטים מעניינים עם ACT1-CUP1 תחילה.
מסופק כאן פרוטוקול בדיקה ACT1-CUP1, כולל הכנת לוחות נחושת. בדיקה זו מספקת לחוקרים תשובה ראשונית להשפעת QSP על שחבור ואילו אזורים פנימיים מושפעים ביותר מההפרעה.
Protocol
1. בניית זן שמרים
- צור או קבל זן S. cerevisiae שהרקע שלו כולל leu2 ו - cup1Δ. כדי ליצור את הרקע הזה, השתמש בשיטת השמרים המבוססת היטב המשתמשת בליתיום אצטט ובדנ"אחד-גדילי 39.
הערה: זני שמרים הפלואידים עשויים להכיל עותק אחד, שניים או יותר של CUP1 6,38. עיין במידע גנומי עבור זן השמרים שנבחר בעת תכנון פריימרים נוק-אאוט כדי לאגף את מיקומי הגנים CUP1. - בצע טרנספורמציה של שמרים כדי לשלב את ה- QSP באמצעות שילוב גנומי או על פלסמיד. השתמש בפרוטוקול מבוסס היטב כמו אלה שתוארו במחקרים קודמים40,41,42.
- בצע טרנספורמציה של שמרים עם הזנים המתקבלים משלב 1.2. כדי להוסיף את פלסמיד הכתב הרצוי של ACT1-CUP1.
הערה: יש לשמור על התאים על צלחות ומדיה של נשירת לאוצין (-Leu) כדי להבטיח שימור של פלסמידים מדווחים ACT1-CUP1 לאחר שינוי זה. - בצע את שלבים 1.2. ו-1.3. עבור כל QSP וכל כתב ACT1-CUP1 פלסמיד להיבדק, כולל זני בקרה.
2. הכנת צלחת נחושת
- בחר טווח ריכוז נחושת המתאים לכתבים לבדיקה (ראה טבלה 1 לקטלניות של כתבים הנמצאים בשימוש תכוף).
הערה: דוגמה לטווח ריכוזי נחושת מקיף היא 30 ריכוזי נחושת שונים של 0 mM, 0.025 mM, 0.05 mM, 0.075 mM, 0.1 mM, 0.15 mM, 0.2 mM, 0.25 mM, 0.3 mM, 0.35 mM, 0.4 mM, 0.45 mM, 0.5 mM, 0.6 mM, 0.7 mM, 0.8 mM, 0.9 mM, 1.0 mM, 1.1 mM, 1.2 mM, 1.3 mM, 1.4 מ"מ, 1.5 מ"מ, 1.6 מ"מ, 1.7 מ"מ, 1.8 מ"מ, 1.9 מ"מ, 2.0 מ"מ, 2.25 מ"מ ו-2.5 מ"מ Cu2+. - צור תמיסת מלאי של 1 M CuSO4 ומסנן סטרילי באמצעות מסנן סטרילי PES (polyethersulfone) בגודל 0.22 מיקרומטר.
- לפי צלחת הנחושת הרצויה, הכינו דילול של 2 מ"ל של מלאי CuSO4 במים סטריליים.
הערה: מכיוון שהצלחת עם 0 mM Cu 2+ תמיד תנותח ותוצג כהפניה, מומלץ ליצור שתי צלחות 0 mM Cu2+, אחת בהתחלה ואחת בסוף שלב הציפוי (שלב 3.4.).- חישוב כמות המלאי עבור ריכוז הנחושת הרצוי הסופי ב-40 מ"ל מנפח הצלחת (טבלה משלימה 1).
- הוסף את הכמות המחושבת של מים סטריליים ומלאי 1 M CuSO4 לצינור סטרילי, 2 מ"ל.
- יוצקים צלחות לבדיקת ACT1-CUP1.
הערה: חלופה לפרוטוקול שלהלן היא לשלב בתחילה את המדיה והאגר במיכל גדול ועליקוט לאחר אוטוקלאבינג למכלים קטנים יותר כדי להשיג ריכוזי נחושת שונים עבור כל צלחת. לא משנה באיזו שיטה ננקטת, חשוב לוודא שריכוז המדיה עקבי בין כל הלוחות למרות שלכל אחד מהם יש ריכוז נחושת שונה.- סמן כל צלחת ריקה שיש למזוג עם ריכוז הנחושת הסופי שהיא תכיל. הכינו לפחות צלחת מרובעת אחת לכל ריכוז נחושת לבדיקה.
- תייג בקבוק של 100 מ"ל לכל ריכוז נחושת לבדיקה.
- לכל בקבוק, יש להוסיף 790 מ"ג אגר (2% עם אגר) וחטיף מוקפץ.
- בכוס גדולה, שלב את מצע הצמיחה -Leu כדי שכל לוחות הנחושת יישפכו. בכל צלחת שיש להכין, יש להמיס 265 מ"ג של בסיס חנקן שמרים (YNB) ו-64 מ"ג של תערובת נשירה פחות לאוצין (וכל חומר מזין אחר שעשוי להידרש כדי לשמור על פלסמיד QSP בתאים) ב-34 מ"ל של מים שעברו דה-יוניזציה.
- הוסיפו 34 מ"ל של תמיסת מדיית הגידול -Leu לכל בקבוק ופקק מוכן של 100 מ"ל עם רדיד אלומיניום. סמן את נייר הכסף בריכוז הנחושת המיועד.
- אוטוקלאב כדי לעקר ולהמיס את האגר באמצעות מחזור הנוזל המומלץ עבור האוטוקלב.
- בהקדם האפשרי, יש להוסיף 4 מ"ל של 20% גלוקוז (מסונן סטרילי) לכל בקבוק.
- התאימו את התוויות והוסיפו את הדילולים של 2 מ"ל של CuSO4 לבקבוק המיועד.
הערה: מכיוון שניתן לייצר עשרות לוחות נחושת בו זמנית, כל אחד עם ריכוז שונה, סימון כל הבקבוקים, הצינורות והצלחות בבירור עם ריכוז הנחושת המיועד ימנע בלבול במהלך מזיגת הצלחת. - השתמש בצלחת ערבוב כדי לערבב במשך ~ 30 שניות ולשפוך או פיפט 35 מ"ל לתוך הצלחת המסומנת, הימנעות בועות. יש להניח להתקרר לפני אחסון או שימוש.
הערה: לעתים קרובות, הצלחות מיוצרות יום אחד או יומיים לפני הבדיקה ומאוחסנות בטמפרטורה של 4 מעלות צלזיוס עד מספר שעות לפני השימוש. הצלחות צריכות להיות בטמפרטורת החדר (RT) לפני תחילת הציפוי (שלב 3.4).
3. בדיקת ACT1-CUP1
- פזרו את הזנים הרצויים על צלחות -Leu.
הערה: אם אתם עובדים ממלאי קריו, יש להקפיד על כך שהתאים יקומו לתחייה מספקת מהאחסון לפני הציפוי. הליך מומלץ לכך הוא לפסוע מהמלאי הקריוגני ולאפשר לו לגדול במשך 3-5 ימים ב 30 מעלות צלזיוס. לאחר מכן, פזרו דוגמית קטנה ואפשרו לה לגדול עוד 2-3 ימים בטמפרטורה של 30 מעלות צלזיוס. - לגדל תרבויות בן לילה ב 10 מ"ל של מדיה.
- הכן את מדיית הצמיחה של Leu באמצעות אותם יחסים כמתואר בשלב 2.4.2. לכל 10 מ"ל של מדיה, יש להוסיף 66 מ"ג של בסיס חנקן שמרים (YNB) ו-16 מ"ג של תערובת נשירה פחות לאוצין ל-9 מ"ל של מים שעברו דה-יוניזציה. יש לעבור דרך מסנן סטרילי PES בגודל 0.22 מיקרומטר.
- לכל זן שמרים, יש להוסיף 9 מ"ל של מדיית צמיחה -Leu ו-1 מ"ל של 20% w/v גלוקוז (מסונן סטרילי) לצינור חרוטי סטרילי של 50 מ"ל.
- בעזרת מקל סטרילי או קצה פיפט, אספו דוגמית קטנה (~1 מ"מ עגולה) של שמרים וחסנו את המדיה.
- נערו את כל תרביות הלילה ב-180 סל"ד וב-30 מעלות צלזיוס.
הערה: אם זמין, ניתן להשתמש בסיבובים במקום בשייקר.
- דלל את הזנים ל-OD600 0.5 ± 0.05 ב-10% גליצרול.
- לכל זן, יש להוסיף 100 μL של תרבית לקובטה המכילה 900 μL מים.
- מדוד את OD600 באמצעות ספקטרופוטומטר.
- חשב את הדילול הנדרש כדי להיות ב- OD600 של 0.5 בנפח סופי של 2 מ"ל.
- יש לדלל כל זן ל-OD600 0.5 ב-10% גליצרול (סטרילי).
- מדוד מחדש את OD600 כדי לוודא שצפיפות התאים נמצאת בטווח הרצוי של 0.5 ± 0.05.
- צלחת את הזנים על לוחות הנחושת.
הערה: ניתן להשתמש במגוון שיטות כדי לצלוח את הזנים, כולל פיפטר ידני בנפחים של 5-10 μL, שימוש בפיפטטור חוזר או רב-ערוצי, או הטבעה עם משכפל פינים. שיטה אחרונה זו מתוארת להלן, אם כי רוב השלבים יהיו דומים ללא קשר לשיטה.- הגדר מיקום עבודה סטרילי ומבער בונזן מואר.
- עבור משכפל 48 פינים, פיפט 200 μL של כל זן מדולל לתוך באר נפרדת של צלחת 96 באר. מלא את החללים הריקים ברשת 6 x 8 עם 200 μL של 10% גליצרול (סטרילי).
הערה: דוגמה לסכמת ציפוי עבור תשעה זני שמרים נמצאת בטבלה משלימה 2. - טובלים את המשכפל בצלחת רדודה של 95% (v/v) אתנול ולהבה כדי לעקר. תן לו להתקרר לפחות 2 דקות לאחר הלהבה כבה, כדי למנוע חום מזעזע את התאים.
- מניחים ארבע צלחות ליד המבער ומסירים את המכסים.
- טבלו את המשכפל בצלחת 96 הבארות והרימו אותו בתנועה מהירה אחת.
- מניחים בעדינות על הצלחת ומתנדנדים קלות קדימה ואחורה כדי להקל על העברה טובה.
- הרם בתנועה מהירה אחת והניח באותו כיוון בדיוק בלוח 96 הבאר.
- חזרו על הפעולה לקבלת עד שלוש צלחות נוספות. חזור על התהליך של טבילת המשכפל באתנול, בוער כדי לעקר, ומחכה להתקרר כל ארבע צלחות.
- לאחר שצלחת, נעים בתנועה חלקה לצד אך עדיין בתוך מטריית העיקור של הלהבה.
הערה: מומלץ לבצע את דילול השמרים וציפוי ליד להבה. הצלחות יכולות בקלות להזדהם בזמן הייבוש. - תנו לצלחות להתייבש לחלוטין לפני שאתם מניחים את המכסים, בדרך כלל 3-5 דקות.
- לדגור את הצלחות במשך 3 ימים ב 30 מעלות צלזיוס.
4. איסוף וניתוח נתונים
- הסר את הלוחות מהאינקובטור ובדוק אותם חזותית.
- הקלט את התמונות של הלוחות באמצעות מצלמה זמינה או מערכת הדמיה דיגיטלית אחרת.
- שיא (או ניקוד) עבור כל זן את ריכוז הנחושת האחרון נראה לעין צמיחה.
הערה: התאים מסוגלים לחבור ולהישאר בני קיימא עד לריכוז זה. לקבלת עקביות, השתמש תמיד באותה שיטה, בעין או מתמונות הצלחת, כדי להשיג את ריכוז הנחושת הישים האחרון. מושבות קטנות מאוד נראות לפעמים בעין אך לא בתמונה. ההבדל בין בדיקה חזותית ישירה או הקלטה מתמונות הוא קטן, בדרך כלל שלב בשיפוע. מכיוון שתמונות של המושבות משמשות לעתים קרובות בפרסומים, מומלץ להבקיע לפי התמונות. - שלב נתונים ממבחני ACT1-CUP1 מרובים עבור אותו זן כדי להסיק מסקנות לגבי האופן שבו ה-QSP משפיע על השחבור.
הערה: נתוני הפרסום נוהגים להציג תמונות של מושבות השמרים בריכוז 0 mM Cu2+ , ריכוז הנחושת האחרון בר קיימא, והריכוז שלאחר מכן שבו המושבה מתה. ניתן להציג נתונים גם כגרף עמודות עם קווי שגיאה עבור סטיית התקן בין עותקים משוכפלים. אין צורך לנרמל את הנתונים, אך ניתן לעשות זאת על ידי הגדרת הכדאיות של בקרת גורם השחבור WT ל-1 והשוואת ההשפעה של המוטציות(ות) שהוכנסו.
תוצאות
מבחני צמיחה, כמו ACT1-CUP1, דורשים הערכה חזותית והשוואתית של מושבות מרובות. כאן, כל זן גדל לרוויה בן לילה, מדוללל-OD 600 של 0.5, ומצופה על 20 לוחות המכילים טווח של ריכוזי נחושת מ-0 mM עד 1.1 mM CuSO4 (איור 3). טווח זה קטן יותר מזה המופיע בפרוטוקול מכיוון שהוא מאפשר הערכה מלאה של ההשפעה של כתבי QSPs ו- ACT1-CUP1 המשמשים ומתוארים להלן. הלוחות צולמו וקיבלו ניקוד (איור 3 וטבלה משלימה 3).
עבור הניסוי המייצג הזה, רקע השמרים כולל גן ADE2 משובש, וכתוצאה מכך המושבות הן בגוונים שונים של אדום (איור 3A,B). הפרעה שכיחה זו בשמרים במסלול ייצור האדנוזין גורמת להצטברות של מבשר אדום-פיגמנט לאדנוזין. לפיכך, הצבע האדום הוא אינדיקטור לבגרות מושבת השמרים (כלומר, כמות וגיל התאים הנוכחיים). לצורך בדיקת ACT1-CUP1, הצבע האדום יכול לשמש כאינדיקטור לזיהום מיני פטריות אם הם בצבע לבן או צהוב. הצבע יכול להיות אישור משני לסובלנות נחושת מכיוון שמושבות בנות קיימא יותר יהיו גוון אדום עמוק יותר.
בעת ציפוי עם משכפל פינים, ישנם מספר סטיות נפוצות. ראשית, אפשר ליצור מושבות בצורת אליפסה אם המשכפל מורם למעלה תוך כדי תנועה שמאלה או ימינה (איור 3B, חץ כתום). בנוסף, מיקרוקולוניות יכולות גם להיווצר מטיפות קטנות של תמיסת תאים אם משכפל הפינים מובא בזווית או אם הוא מזועזע מעל הצלחת (איור 3B, חץ אדום). לעתים קרובות מזיקים, לעתים, המיקרוקולונים יכולים להתערבב עם מושבה מוטבעת, וזה מונע פרשנות של אותה מושבה. בעיות ציפוי נוספות כוללות זמן המתנה לא מספיק לאחר העיקור כדי שסיכות המשכפל יתקררו ומגע לא מספיק בין הצלחת לפינים, כך שמתרחשת העברה לקויה של מדיית התרבות. בשני המקרים, מעט תאים, אם בכלל, יגדלו על הצלחת, כולל עבור זני הבקרה המכילים את הכתב מסוג בר. כמו בכל בדיקת גדילה, ללא קשר לשיטת הציפוי, חשוב לבצע את ACT1-CUP1 במשולש כדי לוודא שהתוצאות עקביות וניתנות לחזרה. באופן אידיאלי, אלה משוכפלים שונים צריך להתבצע על לוחות נחושת מוכן בזמנים שונים כדי להבטיח שכפול.
עבור ניסויים מייצגים אלה, כתב A3c נבחר כדי להדגיש את ההשפעה של רצף שאינו קונצנזוס על עמידות הנחושת בהיעדר הפרעות נוספות. A3c מפחית באופן משמעותי את כמות ה-CUP1 mRNA המיוצרת מכיוון שהוא מפריע ליכולתו של השחבור לזהות ולנצל את ה-SS15 5' שלו. שמרים עם כתב A3c שרדו עד 0.15 mM Cu2+, בעוד שתאי הכתב מסוג בר שמרו על כדאיות עד סוף טווח ריכוזי הנחושת שנבדקו (איור 3C). הכתב מסוג בר המכיל תאים גדל ל-2.5 mM Cu2+ ללא השפעה על הכדאיות (הנתונים לא מוצגים).
U6 snRNA הוא מרכיב קטליטי חיוני של השחבור. מחקרים רבים השתמשו ב-ACT1-CUP1 כדי לחקור את ההשפעה שיכולה להיות למוטציות על RNA זה 16,32,34. עבור מחקר זה נחקרו שלושה רצפי U6 snRNA, כלומר רצף מסוג בר (WT), מיקום 57 שהוחלף מאורידין לציטוזין (U57c), ומיקום 57 שהוחלף מאורידין לאדנוזין (U57a) (איור 3 ואיור 4). בשילוב עם כתבי ACT1-CUP1 המשפיעים על השלבים הקטליטיים בשחבור, נקבע כי U57c מעדיף את הצעד הקטליטי הראשון, ו- U57a מעדיף את ההתקדמות לשלב השני16,32.
כדי להתכונן לבדיקת ACT1-CUP1, נוצר זן כאשר העותק הגנומי של U6 snRNA נמחק והרצפים מסוג U6 snRNA מסוג פראי או מוטציה כלולים בפלסמידים. מכיוון ש-U6 snRNA הוא מרכיב חיוני בתא, נעשה שימוש בשלוש טרנספורמציות נפרדות כדי להפיל תחילה את ה-snRNA הגנומי של U6 תוך שמירה על כדאיות התא, ולאחר מכן להציג מוטציות של U6 snRNAs על פלסמידים, ולבסוף, להוסיף את כתבי ACT1-CUP1. לצורך הטרנספורמציה הראשונה, נעשה שימוש בזן שמרים cup1Δ בנוק-אאוט של העותק הגנומי של U6 snRNA ובמקביל הוספת WT U6 snRNA על פלסמיד סמן בחירה URA כדי לשמור על הכדאיות. טרנספורמציה מאוחרת יותר הוסיפה snRNA מסוג פרא או מוטציה של U6 על פלסמיד סמן בחירה TRP, ובחרה כנגד סמן URA באמצעות בחירת 5-FOA. כך נוצרו שלושה זני שמרים cup1Δ, כל אחד עם אחד מרצפי ה-snRNA של U6, כלומר WT, U57a ו-U57c. טרנספורמציה סופית של שמרים עבור כל זן הוסיפה אחד משלושת הפלסמידים השונים של ACT1-CUP1 שישמשו בניסוי זה. הכתבים שנבחרו היו כתב מסוג פראי, A3c, ומוטציה של אדנוזין באתר הענף לגואנין (BS-G). בסך הכל נוצרו תשעה זנים עבור ניסוי זה, שכל אחד מהם הכיל רצף U6 snRNA אחד וכתב ACT1-CUP1 אחד (טבלה משלימה 4 וטבלה משלימה 5).
התוצאות הראו שלבסיסים השונים במיקום 57 של U6 snRNA יש השפעות ייחודיות על השחבור בשילוב עם מוטציה של 5' SS או BS (איור 4). הן כתבי A3c והן BS-G מעכבים בעיקר שחבור על ידי ייצוב השלב הקטליטי הראשון קונפורמציה14,15. לפיכך, U57c היא מוטציה נוספת המפחיתה את עמידות הנחושת בשילוב עם כל אחד מהכתבים האלה (איור 4B). לעומת זאת, U57a מגביר את הסבילות לנחושת מכיוון שהוא מקדם התקדמות לשלב השני (איור 4B)16,32. הירידה בסבילות הנחושת של זן BS-G עם U57a בהשוואה ל-U6 snRNA WT מדגישה השפעה משנית סבירה של BS-G בשלב השני של שחבור16.
תוצאות אלה גם מדגישות את האופי האיכותי של בדיקה זו ומדוע יש לבדוק רצפי שאילתות וכתבים מסוג פראי. בעוד שהדפוס הכללי של עמידות מוגברת או מופחתת לנחושת נכון לגבי מוטציות U6 snRNA אלה בהשוואה ל-U6 snRNA מסוג פראי, הריכוז המדויק של נחושת שאליו שורדים התאים יכול להיות שונה בין מחקרים (טבלה 1) ואכן היה שונה בין נתונים מייצגים אלה לבין תוצאות אחרות שפורסמו. סביר להניח שהסיבה לכך היא הרקע של הזן המכיל את מחיקת CUP1 , אך יכול לנבוע גם מהבריאות הכללית של הזנים לפני הציפוי (כלומר, כמה זמן לאחר יצירת הזן או ה-restreak מהקריו בוצעה הבדיקה), הבדלים באופן הכנת הלוחות, ושונות בין אינקובטורים שונים. שונות דומה צוינה ב- Mayerle et al. עבור מוטציות שאילתה Prp8 בספרות43. לפיכך, השוואת מגמות סובלנות נחושת יכולה להתבצע עבור מבחני ACT1-CUP1 שונים, אך ההשוואה המספרית של ריכוזי הנחושת צריכה להיעשות רק באותה מעבדה, ולעתים עם אותה קבוצה של לוחות נחושת.
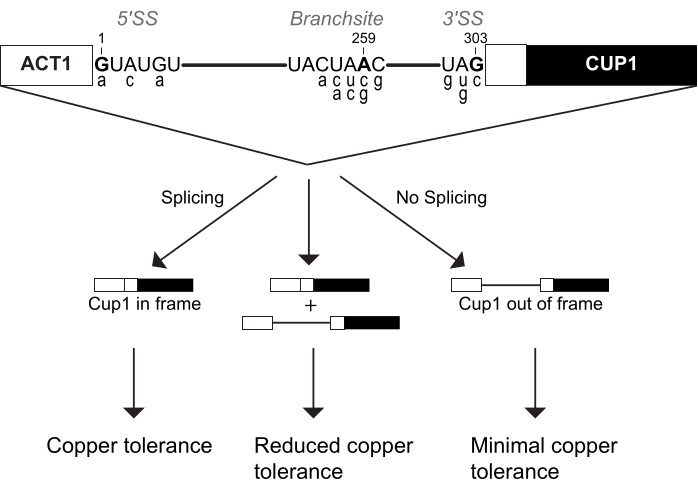
איור 1: עיצוב כתב ACT1-CUP1 . הריכוז של כתב שחבור נמצא בקורלציה ישירה עם סובלנות נחושת שמרים. הדיאגרמה של הכתב כוללת את שלושת אתרי השחבור של אתר השחבור 5' (5' SS), אתר הסניף (BS) ואתר השחבור 3' (3' SS). רצפי קונצנזוס השמרים עבור אתרים אלה מוצגים, כאשר אלה המיועדים למחשוף מסומנים בהדגשה וממוספרים על סמך מיקומם באינטרון. רצפי דיווח ACT1-CUP1 נפוצים שאינם בקונצנזוס מוצגים באותיות קטנות מתחת למיקומי רצף הקונצנזוס המתאימים שלהם ומפורטים בטבלה 1. אנא לחץ כאן כדי להציג גרסה גדולה יותר של נתון זה.

איור 2: זרימת עבודה של בדיקת ACT1-CUP1. לצורך בדיקה זו, זן שמרים חייב להיות cup1Δ leu2 ולהכיל את הפלסמיד הרצוי ACT1-CUP1 ואת הגן QSP, המסומן גן באיור. הגן QSP חייב להיות מוכנס גנומית או על פלסמיד. הפרוטוקול באמצעות משכפל פינים כולל ארבעה שלבים להכנת תאי השמרים. שלב 1 הוא לגדל את התאים לרוויה. שלב 2 הוא למדוד את OD 600 של התרבות ולדלל ל- OD600 של 0.5. שלב 3 הוא להפיץ על צלחת 96 באר. שלב 4 הוא צלחת על צלחות המכילות ריכוזים הולכים וגדלים של נחושת (מסומן בצבע כחול עולה). שלב 1, שלב 2 ושלב 4 יהיו זהים עבור פיפטינג ידני. לאחר הציפוי, הצלחות דוגרות במשך 3 ימים בטמפרטורה של 30 מעלות צלזיוס ולאחר מכן מקבלות ניקוד לכדאיות. אנא לחץ כאן כדי להציג גרסה גדולה יותר של נתון זה.

איור 3: תצוגות מייצגות של נתוני ACT1-CUP1. לצורך ניסוי זה, שחבורי שמרים מאותגרים עם שתי מוטציות שונות של U6 snRNA ונבדקים בנוכחות שלושה כתבים שאינם בקונצנזוס. שלושה שכפולים של בדיקה זו מוצגים על אותם לוחות למטרות הדגמה. מומלץ לבדיקה זו לעשות שכפולים על צלחות נפרדות ובימים נפרדים. (A) מוצגת בדיקה שהושלמה עם שיפוע נחושת של 0 mM עד 1.1 mM על פני 20 לוחות. ככל שריכוז הנחושת עולה, זנים עם שחבור נמוך יותר מראים ירידה במפגש עד לנקודה שבה ריכוז הנחושת הופך לקטלני. רקע השמרים היה ade2, ולכן מושבות בוגרות הן בצבע אדום. (B) השוואה של אותם לוחות ב-0 mM ו-0.1 mM CuSO4 בתמונה עם מצלמת כף יד לעומת מערכת הדמיה דיגיטלית. זוהי דוגמה לאופן שבו ניתן להשוות מספר כתבים שאינם בקונצנזוס זה לצד זה ועם הכתב הפרוע. תצפיות נפוצות על לוחות כוללות טיפה מטורפת של מדיה תרבותית שנפלה ממשכפל הסיכה (חץ אדום) והטלטלה קלה של המושבות עקב החלקה של הסיכה לאורך פני השטח של הצלחת או תנועה של הצלחת לפני שטיפת התרבית התייבשה מספיק (חץ כתום). (C) דוגמה להשפעתו של המדווח A3c על כדאיות התאים בהשוואה למדווח מסוג פראי. תמונות כגון אלה המוצגות ב-(B) נחתכות ומיושרות כדי להדגיש את הבדלי הצמיחה בריכוזי נחושת שונים. סבילות הנחושת של זן הכתב A3c יורדת ל-0.15 mM Cu2+ בהשוואה לכדאיות של זן המדווח מסוג פראי לסוף הטווח שנבדק. אנא לחץ כאן כדי להציג גרסה גדולה יותר של נתון זה.
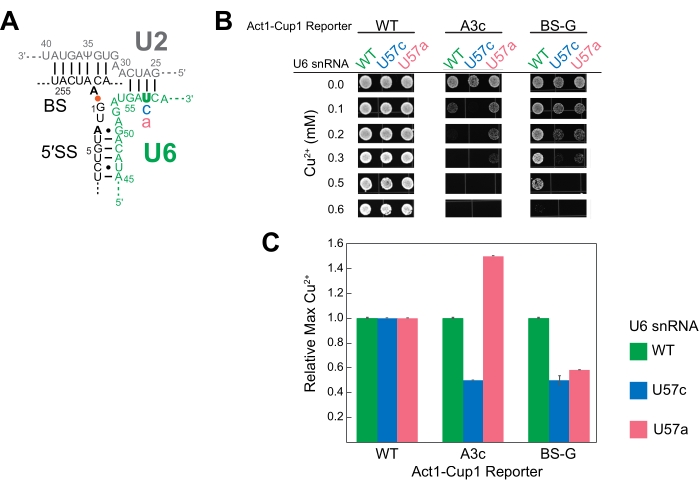
איור 4: תוצאות ACT1-CUP1 מייצגות המנטרות שחבור בשמרים עם מוטציות של רכיבי שחבור . (A) סכמת רכיבי ה-RNA של האתר הפעיל מיד לאחר הצעד הקטליטי הראשון. ה-SNRNAs U2 וה-U6 הם דו-צדדיים, ומביאים את ה-5' SS וה-BS של האינטרון בסמיכות. הקשר האינטרוני בין A259 (BS) ו- G1 (5' SS) מסומן על ידי הנקודה הכתומה. המיקומים של החלפות הרצף שאינן בקונצנזוס בכתב ACT1-CUP1 שנבדקו בניסוי זה מסומנים בשחור מודגש. המיקום המוטנטי ב-U6 snRNA (U57) הוא בצבע ירוק מודגש, והבסיסים המוחלפים הם בצבע כחול או ורוד. (ב) אפשרות אחת להצגת נתוני ACT1-CUP1 בפרסום כוללת מספר תמונות של מושבות מריכוזי Cu2+ רלוונטיים. כתב ה-WT שרד מעבר לריכוז הנחושת שנבדק עבור כל שלושת זני ה-snRNA של U6 שנשאלו. (C) גרף עמודות המשווה את ההשפעות לכל כתב ולכל מוטציה של U6 snRNA. הנורמליזציה מתבצעת עבור כל כתב ACT1-CUP1 על ידי הגדרת סבילות הנחושת של U6 snRNA WT ל-1 וחישוב היחס למוטציות U57c ו-U57a. קווי שגיאה מייצגים את סטיית התקן משלושה עותקים משוכפלים. אנא לחץ כאן כדי להציג גרסה גדולה יותר של נתון זה.
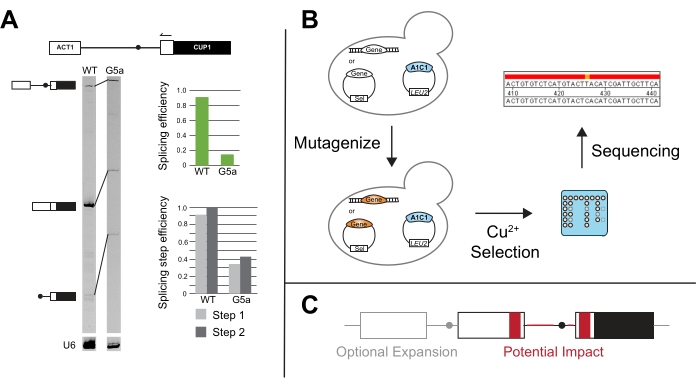
איור 5: שיטות נוספות להחמאת תוצאות ACT1-CUP1. (A) הארכת פריימר מתבצעת באמצעות חישול פריימר באקסון ACT1 3' ולאחר מכן התארכות לתוך האינטרון. בדוגמה זו, הפריימר מסומן סופית בצבע IR700, והרחבת הפריימר בוצעה כמתואר ב-20,21. הארכת פריימר של U6 snRNA מבוצעת באותה תגובה כדי לשמש כבקרת העמסה. 7% 19:1 bis/acrylamide, ג'ל דנטורינג פותר את תוצרי הקדם-mRNA, ה-mRNA והלריאט לאחר הארכת פריימר באמצעות מכשיר הדמיית ג'ל אינפרא-אדום כמתואר ב-van der Feltz et al.22. ניתן להשתמש בעוצמת הפסים השונים כדי למדוד את יעילות השחבור הכוללת וכן להבחין בהבדלי השחבור המתרחשים בשלב הראשון או השני, כפי שניתן לכמת באמצעות ImageJ44 או תוכנה אחרת לכימות פס ג'ל. הן יעילות השחבור והן יעילות שלב השחבור מחושבות כמתואר ב- Query וב- Konarska14. (B) מסכי מוטציה עם כתבי ACT1-CUP1 יכולים להשתמש בבחירת נחושת כדי לזהות מוטציות שמשפיעות על השחבור. לאחר מכן ניתן לרצף את הגנים המעניינים בזנים המתקבלים כדי לקבוע אם המוטציה התרחשה באותו גן. (C) ניתן לבצע שינויים לכתב מחוץ לאתרי השחבור כדי לעקוב אחר שינויים בשחבור ביחס למבנה האינטרון, רצפים אקסוניים, מספר אקסונים או ייצוא גרעיני של RNA לא מחובר. אזורים באפור הם אזורי הרחבה אופציונליים שיש לכלול במדווח, ואזורים באדום הם אזורים שבהם ניתן לבדוק את הרצף ואת השינויים המבניים על השפעתם הפוטנציאלית על שחבור באמצעות בדיקת ACT1-CUP1. אנא לחץ כאן כדי להציג גרסה גדולה יותר של נתון זה.
| שם הכתב | אזור אינטרוניק | רצף | ריכוז Cu2+ בר-קיימא אחרון (mM) | |
| WT | 5' | גואוגו | > 2.5 | |
| G1a | 5ʹ | א אואוגו | 0.0133 או 0.0532 | |
| A3c | 5ʹ | GUcUGU | 0.15^,18 או 0.216 | |
| ז5א | 5ʹ | GUAUaU | 0.303 או 0.259 | |
| WT | אתר הסניף | UACUAAC | > 2.5 | |
| C256a | אתר הסניף | UAaUAAC | 0.1526 או 0.1832 | |
| U257c/a | אתר הסניף | UACc/aAAC | 0.226 או 0.332 או 0.545 | 0.059,32 |
| A258c/u | אתר הסניף | UACUc/uAC | 0.826 | 1.045 או 1.646 |
| BS-C | אתר הסניף | UACUAcC | 0.153 או 0.1832,56 או 0.226 | |
| בס-ג | אתר הסניף | UACUAgC | 0.0516,32 או 0.625 או 0.846 | |
| C260g | אתר הסניף | UACUAAg | 0.826 | |
| WT | 3' | UAG | > 2.5 | |
| U301g | 3ʹ | ז א.ג. | 0.1518 | |
| A302g/u | 3' | Ug/uG | 0.0139 | 0.07516 או 0.1824 |
| G303c | 3ʹ | UAc | 0.0532 | |
טבלה 1: רשימת הכתבים הנפוצים ודיווח על קטלניות הריכוז Cu2+. ישנם מעל 100 ציטוטים של לסר וגות'רי3. בעוד שמבחר קטן של ציטוטים אלה שימש ליצירת טבלה זו, הם מדגישים את המגמה הכללית של הבדלים קלים עד בינוניים בין מחקרים בריכוזי הכדאיות המדווחים של נחושת. ב-ACT1-CUP1, חשוב להשוות חלבון או רנ"א מסוג בר למוטאנטים, כולם עם אותו רקע של זן שמרים, תוך שימוש בריכוזים שפורסמו כמדריך, אך מתוך ציפייה שהריכוזים הנצפים עשויים להיות שונים. הנתונים שנאספו מאיור 3 (^) ומפרסומים מרובים המבוארים על ידי הציטוטים הבאים 3,9,16,18,24,25,26,32,45,46.
טבלה משלימה 1: תכולה של לוח נחושת יחיד ודוגמה לחישובים שנעשו כדי להשיג דילולי נחושת מ-0 mM ל-2.5 mM ממלאי של 1 M CuSO4 . אנא לחץ כאן כדי להוריד טבלה זו.
טבלה משלימה 2: דוגמה לסכמת ציפוי עבור משכפל 48 פינים. אנא לחץ כאן כדי להוריד טבלה זו.
טבלה משלימה 3: דוגמה לכדאיות שהובקעה מלוחות נחושת שהודגמו במשך 3 ימים בטמפרטורה של 30 מעלות צלזיוס. אנא לחץ כאן כדי להוריד טבלה זו.
טבלה משלימה 4: רשימת זני השמרים המשמשים להפקת הנתונים המייצגים. אנא לחץ כאן כדי להוריד טבלה זו.
טבלה משלימה 5: רשימת הפלסמידים המשמשים להפקת הנתונים המייצגים. פלסמידים U6 snRNA שנוצרו ופורסמו במחקר קודם22,47. אנא לחץ כאן כדי להוריד טבלה זו.
Discussion
ACT1-CUP1 הוא מבחן גדילה, ויש לנקוט בזהירות כדי להבטיח שניתן לייחס הבדלי גדילה שנצפו רק לפגמים בשחבור. יש לטפל בכל הזנים באופן דומה לפני הציפוי, כולל אורך וסוג דומים של תנאי גידול ואחסון. אם משתמשים בזנים רגישים לטמפרטורה, יש לבצע בדיקות ACT1-CUP1 רק בתנאים שבהם זנים אלה גדלים באופן דומה לסוג בר. באופן דומה, עבור רכיב QSP, מומלץ שיהיו רקעים זהים של שמרים ורמות ביטוי זהות של גנים QSP כדי לא להעיב על הפרשנות של התוצאות. כאשר בוחנים את מספר ה- QSPs והכתבים לשימוש, לא מומלץ לבדוק יותר מ -30 זנים בכל פעם בשיטת משכפל הפינים. עם הזמן הנוסף לביצוע כל שלב, התאים ישקעו, ותוצאות הבדיקה לא יהיו עקביות עקב ירידה בכדאיות התא.
בנוסף למגבלות שיש ל-ACT1-CUP1 כבדיקת גדילה, ל-QSP עשויה להיות השפעה מורכבת יותר על השחבור מכפי שניתן לפתור בשיטה זו. מכיוון שהשחבור הוא תהליך רב-שלבי והגורמים ממוחזרים, הפנוטיפ שנצפה יכול לגרום להפרעה המשפיעה על יותר משלב שחבור אחד. זה נכון גם לגבי הניתוחים הבאים שיכולים לעקוב אחר ACT1-CUP1, שחלקם מתוארים להלן. הנתונים ידגישו את השלב המופרע ביותר בתהליך, למרות ששלבים אחרים עשויים להיות מושפעים מהתפקוד המשתנה של גורם השחבור.
הארכת פריימר של כתבי ACT1-CUP1 נוצלה לראשונה במאמרם המקורי של לסר וגאת'רי, והיא מבוצעת לעתים קרובות אם תוצאות ACT1-CUP1 מראות פגם בגדילה3. בדיקה זו מתמקדת במדווח ומשתמשת באורך של תוצרי ה-PCR כדי לקבוע את הכמויות היחסיות של כתב לא משוחב, שחבור חלקי ושחבור מלא נוכחים (איור 5A). יעילות השחבור הכוללת והאם הפגם משפיע בצורה חזקה יותר על השלב הקטליטי הראשון או השני מחושבים על ידי לקיחת יחסים של כמויות מוצר ה- PCR14. לדוגמה, כתב 5' SS G5a הפחית את השחבור בהשוואה לכתב מסוג פראי, אך יעילות הצעד הראשון והשני שלו עוקבת אחר דפוס דומה לכתב פראי (איור 5A). זה מצביע על פגם לפני הצעד הקטליטי הראשון, אולי בהרכבת שחבור, מכיוון ששני השלבים מושפעים באופן דומה31.
מבחנים חדשניים פותחו מהמבחן הקנוני ACT1-CUP1, כגון סינון למוטנטים המשפרים את השחבור בנוכחות מוטציות אחרות של גורמי שחבור ו/או רצפי שחבור שאינם בקונצנזוס (איור 5B). לדוגמה, חשיפת שמרים המכילים את כתב ACT1-CUP1 ל- UV ולאחר מכן בחירה בנוכחות נחושת הניבו מוטציות Prp8 ו- Hsh155 ששיפרו את השחבור של רצפים שאינם בקונצנזוס14,19.
מעבר לחקר ההשפעה של אתרי שחבור וגורמי שחבור מכוננים, נעשה שימוש בתלות בגדילה של CUP1 כדי לחקור שחבור אינטרון מרובים, בקרת ייצוא גרעיני וההשפעה של UTR ורצפים היקפיים אחרים על שחבור (איור 5C). חלק מהמחקרים האלה יצרו כתבים עם CUP1 וגנים אחרים של שמרים המכילים אינטרון שיכולים להיות בעלי תבניות שחבור מורכבות יותר כדי לחקור את ההשפעה על מבנה משני אינטרוני ושחבור תעתיק רב-אינטרוני 48,49,50,51,52. הקשר בין שחבור לייצוא גרעיני נחקר על ידי תעתיקים שחבורים או לא מחוברים המקודדים CUP1 במסגרת53,54. אורך המסלול הפירימידין ותלות המרחק של בחירת אתר השחבור עקב גורמים ספציפיים נבדקה גם היא 20,55,56,57. דוגמאות אלה ורבות אחרות מדגישות את הרבגוניות של ACT1-CUP1 ומבחני צמיחה אחרים של CUP1.
בדיקת ACT1-CUP1 מקשרת הפרעות למחזור תגובה מורכב עם פנוטיפ גדילה פשוט עם טווח רגישות רחב. מבחן מורשת זה שימש מעבדות רבות כדי להניח את היסודות להבנת מחזור השחבור. לאחרונה, ACT1-CUP1 שימש כדי לענות על שאלות הנובעות מעושר הנתונים המבניים הזמינים כעת21,22,25. מחקרים מבניים של שחבורים הקשורים לרצפים שאינם בקונצנזוס יכולים להיות משויכים לתוצאות ACT1-CUP1 כדי לפרש כיצד מבנה שונה ותפקוד שונה מתואמים. ACT1-CUP1 הוא מסך ראשון אידיאלי לשחבור מוטציות שיכולות להשלים אנליזה מורכבת יותר.
Disclosures
למחבר אין מה לחשוף.
Acknowledgements
תודה לאהרון הוסקינס ולחברי מעבדת הוסקינס באוניברסיטת ויסקונסין-מדיסון על השימוש בזני שמרים ובציוד בדור של איורים 3-5. תודה להרפרט קאור ושינגיאנג פו על הערותיהם התובנות על כתב היד. תודה לסטודנטים, לסגל ולסגל התומכים באוניברסיטת נורת'ווסט במהלך הכתיבה, העריכה והצילומים של מאמר זה. תודה לאיזבל מרסיגן על העזרה בצילום שיטה זו.
Materials
| Name | Company | Catalog Number | Comments |
| 1.5 mL sterile microcentrifuge tubes | Fisher Scientific | 05-408-129 | Or comparable item from a different manufacturer. |
| 2 mL sterile microcentrifuge tubes | Fisher Scientific | 05-408-138 | Or comparable item from a different manufacturer. |
| 50 mL sterile centrifuge tubes | Fisher Scientific | 07-201-332 | Or comparable item from a different manufacturer. |
| 96-well round bottom microplate | Fisher Scientific | 07-200-760 | Or comparable item from a different manufacturer. |
| 190 proof ethanol | Fisher Scientific | 22-032-600 | Or comparable item from a different manufacturer. |
| 500 mL Filter System (0.22 µm) | CellTreat Scientific Products | 229707 | Or comparable item from a different manufacturer. |
| Agar | Fisher Scientific | BP1423-500 | Any molecular grade agar will work. |
| Autoclave | Tuttnauer | 3870EA | Or comparable item from a different manufacturer. |
| Bunsen burner | Humboldt | PN6200.1 | Or comparable item from a different manufacturer. |
| Cell Density Meter | VWR | 490005-906 | Or other spectral device that can measure absorbance at 595 nm. |
| Copper sulfate Pentahydrate | Fisher Scientific | LC134051 | Or comparable item from a different manufacturer. |
| Digital imaging system | Cytiva | 29399481 | ImageQuant 4000 (used for Figure 3), Amersham ImageQuant 800, or comparable item from a different manufacturer. |
| Dropout mix (-Leu) | USBiological Life Sciences | D9525 | Use the appropriate drop out mix for your experiment. It is possible you will be using a yeast nutrient marker for your query perturbation also. In that case, the drop out mix should be for that marker and Leu |
| D-Glucose | Fisher Scientific | AAA1682836 | Or comparable item from a different manufacturer. |
| Gel band quantifying software | Cytiva | 29-0006-05 | ImageQuant TL v8.1 (used for figure 5A) or comparable item from a different manufacturer. |
| Hand held camera | Nikon | D3500 | Or comparable item from a different manufacturer. |
| Near infra-red gel imaging device | Cytiva | 29238583 | Amersham Typhoon NIR (used for Figure 5a) or comparable item from a different manufacturer. |
| Laboratory grade clamp | Fisher Scientific | 05-769-7Q | Or comparable item from a different manufacturer. |
| Laboratory grade stand and clamp | Fisher Scientific | 12-000-101 | Or comparable item from a different manufacturer. |
| Magnetic stir bars | Fisher Scientific | 14-513-51 | Or comparable item from a different manufacturer. |
| Pin replicator | VP Scientific | VP 407AH | |
| Semi-micro disposable cuvettes | VWR | 97000-590 | Or comparable item from a different manufacturer. |
| Shaker | JEIO Tech | IST-3075 | Or comparable item from a different manufacturer. |
| Spectrophotometer | Biowave | 80-3000-45 | Or any spectophotometer that can measure the absorbance at 600 nm. |
| Square plates | VWR | 102091-156 | Circular plates may also be used though are more challenging if using a pin replicator. |
| Stir plate | Fisher Scientific | 11-520-16S | Or comparable item from a different manufacturer. |
| Yeast nitrogen base | USBiological Life Sciences | Y2025 | Or comparable item from a different manufacturer. |
References
- Wahl, M. C., Will, C. L., Luhrmann, R. The spliceosome: Design principles of a dynamic RNP machine. Cell. 136 (4), 701-718 (2009).
- Wilkinson, M. E., Charenton, C., Nagai, K. RNA splicing by the spliceosome. Annual Review of Biochemistry. 89, 359-388 (2020).
- Lesser, C. F., Guthrie, C. Mutational analysis of pre-mRNA splicing in Saccharomyces cerevisiae using a sensitive new reporter gene, CUP1. Genetics. 133 (4), 851-863 (1993).
- Ng, R., Abelson, J. Isolation and sequence of the gene for actin in Saccharomyces cerevisiae. Proceedings of the National Academy of Sciences of the United States of America. 77 (7), 3912-3916 (1980).
- Gallwitz, D., Sures, I. Structure of a split yeast gene: Complete nucleotide sequence of the actin gene in I. Proceedings of the National Academy of Sciences of the United States of America. 77 (5), 2546-2550 (1980).
- Fogel, S., Welch, J. W., Cathala, G., Karin, M. Gene amplification in yeast: CUP1 copy number regulates copper resistance. Current Genetics. 7 (5), 347-355 (1983).
- Hamer, D. H., Thiele, D. J., Lemontt, J. E. Function and autoregulation of yeast copperthionein. Science. 228 (4700), 685-690 (1985).
- Winge, D. R., Nielson, K. B., Gray, W. R., Hamer, D. H. Yeast metallothionein. Sequence and metal-binding properties. Journal of Biological Chemistry. 260 (27), 14464-14470 (1985).
- Burgess, S. M., Guthrie, C. A mechanism to enhance mRNA splicing fidelity: The RNA-dependent ATPase Prp16 governs usage of a discard pathway for aberrant lariat intermediates. Cell. 73 (7), 1377-1391 (1993).
- Collins, C. A., Guthrie, C. Allele-specific genetic interactions between Prp8 and RNA active site residues suggest a function for Prp8 at the catalytic core of the spliceosome. Genes & Development. 13 (15), 1970-1982 (1999).
- Siatecka, M., Reyes, J. L., Konarska, M. M. Functional interactions of Prp8 with both splice sites at the spliceosomal catalytic center. Genes & Development. 13 (15), 1983-1993 (1999).
- Umen, J. G., Guthrie, C. Mutagenesis of the yeast gene PRP8 reveals domains governing the specificity and fidelity of 3' splice site selection. Genetics. 143 (2), 723-739 (1996).
- Grainger, R. J., Beggs, J. D. Prp8 protein: At the heart of the spliceosome. RNA. 11 (5), 533-557 (2005).
- Query, C. C., Konarska, M. M. Suppression of multiple substrate mutations by spliceosomal prp8 alleles suggests functional correlations with ribosomal ambiguity mutants. Molecular Cell. 14 (3), 343-354 (2004).
- Konarska, M. M., Vilardell, J., Query, C. C. Repositioning of the reaction intermediate within the catalytic center of the spliceosome. Molecular Cell. 21 (4), 543-553 (2006).
- Liu, L., Query, C. C., Konarska, M. M. Opposing classes of prp8 alleles modulate the transition between the catalytic steps of pre-mRNA splicing. Nature Structural and Molecular Biology. 14 (6), 519-526 (2007).
- MacRae, A. J., et al. Prp8 positioning of U5 snRNA is linked to 5' splice site recognition. RNA. 24 (6), 769-777 (2018).
- Query, C. C., Konarska, M. M. CEF1/CDC5 alleles modulate transitions between catalytic conformations of the spliceosome. RNA. 18 (5), 1001-1013 (2012).
- Tang, Q., et al. SF3B1/Hsh155 HEAT motif mutations affect interaction with the spliceosomal ATPase Prp5, resulting in altered branch site selectivity in pre-mRNA splicing. Genes & Development. 30 (24), 2710-2723 (2016).
- Carrocci, T. J., Zoerner, D. M., Paulson, J. C., Hoskins, A. A. SF3b1 mutations associated with myelodysplastic syndromes alter the fidelity of branchsite selection in yeast. Nucleic Acids Research. 45 (8), 4837-4852 (2017).
- Kaur, H., Groubert, B., Paulson, J. C., McMillan, S., Hoskins, A. A. Impact of cancer-associated mutations in Hsh155/SF3b1 HEAT repeats 9-12 on pre-mRNA splicing in Saccharomyces cerevisiae. PLoS One. 15 (4), 0229315(2020).
- vander Feltz, C., et al. Saccharomyces cerevisiae Ecm2 modulates the catalytic steps of pre-mRNA splicing. RNA. 27 (5), 591-603 (2021).
- Carrocci, T. J., Paulson, J. C., Hoskins, A. A. Functional analysis of Hsh155/SF3b1 interactions with the U2 snRNA/branch site duplex. RNA. 24 (8), 1028-1040 (2018).
- Hogg, R., de Almeida, R. A., Ruckshanthi, J. P., O'Keefe, R. T. Remodeling of U2-U6 snRNA helix I during pre-mRNA splicing by Prp16 and the NineTeen Complex protein Cwc2. Nucleic Acids Research. 42 (12), 8008-8023 (2014).
- Hansen, S. R., Nikolai, B. J., Spreacker, P. J., Carrocci, T. J., Hoskins, A. A. Chemical inhibition of pre-mRNA splicing in living Saccharomyces cerevisiae. Cell Chemical Biology. 26 (3), 443-448 (2019).
- Xu, Y. Z., Query, C. C. Competition between the ATPase Prp5 and branch region-U2 snRNA pairing modulates the fidelity of spliceosome assembly. Molecular Cell. 28 (5), 838-849 (2007).
- Staley, J. P., Guthrie, C. An RNA switch at the 5' splice site requires ATP and the DEAD box protein Prp28p. Molecular Cell. 3 (1), 55-64 (1999).
- Bousquet-Antonelli, C., Presutti, C., Tollervey, D. Identification of a regulated pathway for nuclear pre-mRNA turnover. Cell. 102 (6), 765-775 (2000).
- Villa, T., Guthrie, C. The Isy1p component of the NineTeen complex interacts with the ATPase Prp16p to regulate the fidelity of pre-mRNA splicing. Genes & Development. 19 (16), 1894-1904 (2005).
- Mayas, R. M., Maita, H., Staley, J. P. Exon ligation is proofread by the DExD/H-box ATPase Prp22p. Nature Structure and Molecular Biology. 13 (6), 482-490 (2006).
- Lesser, C. F., Guthrie, C. Mutations in U6 snRNA that alter splice site specificity: Implications for the active site. Science. 262 (5142), 1982-1988 (1993).
- McPheeters, D. S. Interactions of the yeast U6 RNA with the pre-mRNA branch site. RNA. 2 (11), 1110-1123 (1996).
- Perriman, R. J., Ares, M. Rearrangement of competing U2 RNA helices within the spliceosome promotes multiple steps in splicing. Genes & Development. 21 (7), 811-820 (2007).
- Mefford, M. A., Staley, J. P. Evidence that U2/U6 helix I promotes both catalytic steps of pre-mRNA splicing and rearranges in between these steps. RNA. 15 (7), 1386-1397 (2009).
- Hilliker, A. K., Mefford, M. A., Staley, J. P. U2 toggles iteratively between the stem IIa and stem IIc conformations to promote pre-mRNA splicing. Genes & Development. 21 (7), 821-834 (2007).
- Wu, G., et al. Pseudouridines in U2 snRNA stimulate the ATPase activity of Prp5 during spliceosome assembly. EMBO Journal. 35 (6), 654-667 (2016).
- Crotti, L. B., Bacikova, D., Horowitz, D. S. The Prp18 protein stabilizes the interaction of both exons with the U5 snRNA during the second step of pre-mRNA splicing. Genes & Development. 21 (10), 1204-1216 (2007).
- Fogel, S., Welch, J. W. Tandem gene amplification mediates copper resistance in yeast. Proceedings of the National Academy of Sciences of the United States of America. 79 (17), 5342-5346 (1982).
- Gardner, J. M., Jaspersen, S. L. Manipulating the yeast genome: Deletion, mutation, and tagging by PCR. Methods Molecular Biology. 1205, 45-78 (2014).
- JoVE. Yeast Transformation and Cloning. In Biology I: yeast, Drosophila and C. Elegant. JoVE Science Education Database. , Cambridge, MA. (2021).
- Gietz, R. D., Woods, R. A. Yeast transformation by the LiAc/SS Carrier DNA/PEG method. Methods Molecular Biology. 313, 107-120 (2006).
- Gietz, R. D., Woods, R. A. Genetic transformation of yeast. Biotechniques. 30 (4), 816(2001).
- Mayerle, M., et al. Structural toggle in the RNaseH domain of Prp8 helps balance splicing fidelity and catalytic efficiency. Proceedings of the National Academy of Sciences of the United States of America. 114 (18), 4739-4744 (2017).
- Schindelin, J., et al. Fiji: An open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Beier, D. H., et al. Dynamics of the DEAD-box ATPase Prp5 RecA-like domains provide a conformational switch during spliceosome assembly. Nucleic Acids Research. 47 (20), 10842-10851 (2019).
- vander Feltz, C., DeHaven, A. C., Hoskins, A. A. Stress-induced pseudouridylation alters the structural equilibrium of yeast U2 snRNA Stem II. Journal of Molecular Biology. 430 (4), 524-536 (2018).
- Rodgers, M. L., Didychuk, A. L., Butcher, S. E., Brow, D. A., Hoskins, A. A. A multi-step model for facilitated unwinding of the yeast U4/U6 RNA duplex. Nucleic Acids Research. 44 (22), 10912-10928 (2016).
- Stutz, F., Rosbash, M. A functional interaction between Rev and yeast pre-mRNA is related to splicing complex formation. EMBO Journal. 13 (17), 4096-4104 (1994).
- Libri, D., Lescure, A., Rosbash, M. Splicing enhancement in the yeast rp51b intron. RNA. 6 (3), 352-368 (2000).
- Libri, D., Stutz, F., McCarthy, T., Rosbash, M. RNA structural patterns and splicing: Molecular basis for an RNA-based enhancer. RNA. 1 (4), 425-436 (1995).
- Howe, K. J., Kane, C. M., Ares, M. Perturbation of transcription elongation influences the fidelity of internal exon inclusion in Saccharomyces cerevisiae. RNA. 9 (8), 993-1006 (2003).
- Cuenca-Bono, B., et al. SUS1 introns are required for efficient mRNA nuclear export in yeast. Nucleic Acids Research. 39 (19), 8599-8611 (2011).
- Scherrer, F. W., Spingola, M. A subset of Mer1p-dependent introns requires Bud13p for splicing activation and nuclear retention. RNA. 12 (7), 1361-1372 (2006).
- Hálová, M., et al. Nineteen complex-related factor Prp45 is required for the early stages of cotranscriptional spliceosome assembly. RNA. 23 (10), 1512-1524 (2017).
- Umen, J. G., Guthrie, C. A novel role for a U5 snRNP protein in 3' splice site selection. Genes & Development. 9 (7), 855-868 (1995).
- Crotti, L. B., Horowitz, D. S. Exon sequences at the splice junctions affect splicing fidelity and alternative splicing. Proceedings of the National Academy of Sciences of the United States of America. 106 (45), 18954-18959 (2009).
- Perriman, R., Ares, M. Invariant U2 snRNA nucleotides form a stem loop to recognize the intron early in splicing. Molecular Cell. 38 (3), 416-427 (2010).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved