室温以下の反応を実施
博士ダナ ラシュリー - 大学のウィリアムとメアリーのソース: 研究室
デモンストレーション: マット ・ スミス
化学反応の過程で新たな結合が形成される関係種 (原子または分子) 非常に近くに来るし、互いに衝突することが必要です。これらの種の衝突がより頻繁にかつ効果的なより高い速度では、これらの分子が移動します。アレニウス方程式1、約、10 K で温度を上げ状態にそのルーツを持って広く使用されているルールの親指、反応の速度を 2 倍し、20 K で温度を上げ、速度を 4 倍増します。
(1)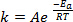
式 (1) しばしばその対数であります。
(2)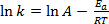
どこkは化学反応の速度、 (分子衝突の頻度に関連する) 頻度因子は、 E、反応に必要な活性化エネルギー、 Rは理想的な気体定数、 Tは温度で反応が行われています。
高い温度したがって、反応がはるかに速く完了を意味します。それにもかかわらず、いくつかのケースで、反応率の低下の効果にもかかわらず、低温で反応を行うことをお勧めします。いくつかのシナリオがこの点詳しくは、さらに以下。
それが室温以下の反応を実行するのに役に、化学者は特定の温度または温度範囲を維持するために冷却槽を使用します。反応は、適切な冷却槽内反応フラスコを配置することによって所望の温度に冷却です。反応試薬は、冷却槽での化学物質との直接接触してこない。冷却槽 (氷、ドライアイス、液体窒素など) 1 つのクライオ (冷却) コンポーネントから成るかもしれないまたは特定の溶媒および添加物塩と低温の成分の混合物があります。溶媒の目的は反応フラスコに冷却剤の温度を効果的に転送して、添加剤の目的は、混合物の凍結ポイントを下げる (または抑制)。(溶剤と添加剤をする物質のことであるに注意してください)。
ソリューションは、純粋な液体よりも低い温度でフリーズしたときこれは凝固点降下として知られている colligative プロパティによって引き起こされることを思い出してください。凍結ポイントを下げる効果は液体溶媒に追加される溶質 (添加物) の量に比例。この効果は、式 (3) で説明します。
(3) ΔDTf Tf (溶剤) − Tf (ソリューション)を = = Kf × m
ΔDTfは、凝固点降下で自体、添加剤/溶質と溶液の凍結溶媒の温度の違いによって記述されます。
Kfシステムの凍結ポイント不況定数、 mソリューションの重量モル濃度です。化学者は相対的な容易さと費用対効果の異なる温度の多様性を作成するのに彼らの利点にこの効果を使用します。
風呂の冷却温度が変動することができます。お風呂を監視する必要があり、調整が必要に応じて行われます。最高の結果を得るには、お風呂船自体がよく絶縁されて。利用可能な場合は、冷却槽のデュワー フラスコを使用ください。デュワー フラスコの不在 (アルミ箔またはタオルを使用) 可能な限り断熱容器で、ガラスやゴムの容器でお風呂を設定することが可能です。中古船は所望の温度で熱安定をする必要があり、ないをクラックする必要があります。
化学実験室の設定で室温以下で温度差の比較的経済的な達成のために多くの異なった浴室バリエーションが存在します。
- 少しだけ氷点下になる (しかし必要ならば - 55 ° C まで) の塩を別に添加して氷水浴となります。
- -78 ° c の温度、溶媒の異なるドライ氷浴を採用します。
- -196 ° c-78 ° C の下の温度は、液体窒素を使用して取得できます。
これらの冷却槽の設定は比較的簡単です、手順は、このドキュメントの最後に含まれています。
氷-水のお風呂
お風呂のこのタイプは非常に簡単にセットアップとすべての学部教育の実験室で利用できます。多くのお風呂、氷風呂が非常に低い温度に到達しないし、船を割れのリスクがないために、使用する容器の種類に柔軟性があります。
氷-水自体は 0 の ° C の温度が、NaCl、MgCl2または CaCl2など特定の塩添加による溶融点降下を実現できます。達成の最終温度変化し、氷の 100 g ごとに使用される添加剤の量によって調整することができます。共通の氷浴である NaCl を添加剤として氷の 100 g あたり塩化ナトリウム 33 g を追加する場所。この方法によって、達成最終的な温度は-20 ° C 前後氷水浴が達することができる最も冷たい温度は-55 ° C のまわり 143 g 氷 100 g 当たり CaCl2水和物の添加によって得られます。
ドライ氷風呂
ドライアイスは固体の二酸化炭素と気高く-78 ° C の温度でこれは、非常に安価な低温剤と多くの所ですぐに利用できます。この温度反応容器への効率的な熱伝達、溶媒が必要です下記-78 ° C の融点を持つ融点が高い、または (より良いという凝固点ここでは mp 溶剤も使用でき、結果、高いお風呂温度。
ドライの氷浴で頻繁に使用される溶剤はアセトン (mp =-95 ° C)、容易に入手可能で安価であります。アセトンでドライ氷浴は、絶縁の程度によりますが、時間の期間の-78 ° C の温度を維持します。最も一般的なドライ氷浴システムです。
高温ドライ-アイス-風呂、高い凍結ポイントで溶剤が使用されます。取得した浴温度は溶媒の凝固点を常に一致しません。別のシステムによって得られる温度は表 2を参照してください。
このタイプのお風呂まで低温、ドライアイスを取り扱う際は、低温保護手袋を着用常に必要があります。
ドライ氷浴の風呂船は、理想的に、デュワーです。デュワーを使用できない場合は、ガラス、ゴム、またはステンレスの容器を使用するが、断熱材は非常に最適なできないお風呂がより頻繁に調整する必要があることに注意してください。
| ドライアイス冷却浴温度 | |
| 混合物 | T (° C) |
| p-キシレン/ドライアイス | +13 |
| シクロヘキサン/ドライアイス | +6 |
| ベンゼン/ドライアイス | +5 |
| エチレング リコール/ドライアイス | -15 |
| 四塩化炭素/ドライアイス | -23 |
| 3-ヘプタノン/ドライアイス | -38 |
| Acetonenitrile/ドライアイス | -42 |
| Cylcohexanone/ドライアイス | -46 |
| ジエチル ブチルカルビトール/ドライアイス | -52 |
| クロロホルム/ドライ アイス | -61 |
| ブチルカルビトール アセテート/ドライアイス | -67 |
| エタノール/ドライアイス | -72 |
| ドライアイス/アセトン | -78 |
| イソプロパノール/ドライアイス | -78 |
表 2。異なるドライ氷水混合物の一覧です。
液体窒素風呂
液体窒素スラッシュ浴場は、ドライの氷浴のそれの下の非常に低い温度が必要な場合に使用されます。液体窒素は追加溶媒を使用しないときは、お風呂の温度-196 ° C の融点を持つ低温剤です。注意してください、ドライアイスと対照をなして N2は液体および均一な熱伝達の添加物の溶剤の使用は必要ではありません。-196 ° C より高い温度が必要な異なる温度、ドライ氷浴の場合と同様、その混合物の様々 な別の有機溶剤が使用されます。別のシステムによって得られる温度の表 3を参照してください。
リキッド N2風呂の非常に低温、デュワーにのみ風呂容器として使用する必要があります、この低温のエージェントを処理するとき、手袋を扱う常に。

表 3。液体窒素の一覧は、異なる溶媒を用いて風呂。2
冷却バス セットアップ
一般的なセットアップのため以下のとおり選択の冷却槽の準備、風呂 (図 1) に反応フラスコを浸します。すべての方法で、風呂の容器を記入しないが、反応フラスコの液浸のため許可する十分な部屋を去る。
注: 反応が湿気敏感な場合は、試薬をフラスコまたは (例えば滴下漏斗) 装置の他の部分に追加する場合非常に注意してください。ガラスが冷却浴に浸漬しながら開口部が生成される場合は、常温空気はすぐに中に流れてし、水分を 。
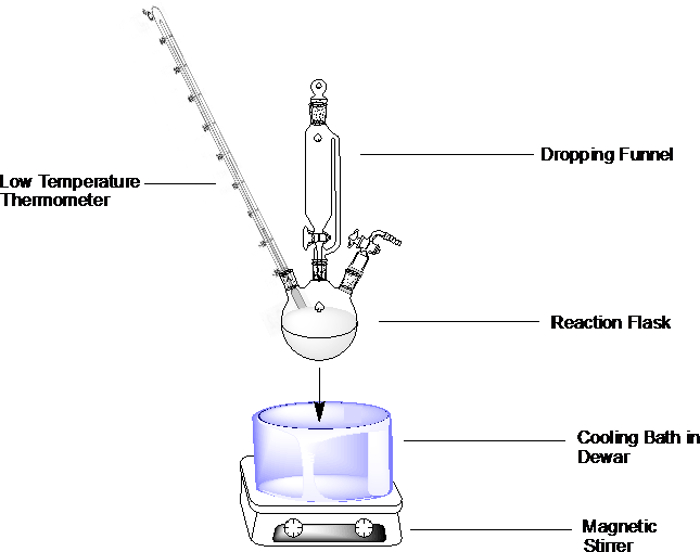
図 1。冷却バス セットアップには滴下漏斗で三首丸底フラスコ、不活性雰囲気下で温度計の例。
1. 氷水浴を作る
- 添加剤と水氷風呂、重量を量るし、好みの風呂船に氷の適切な量を追加します。デュワーは役立ちますが、必須ではありません。容器はプラスチック、ゴム (例えばバケツ)、または (例えば大きな結晶皿) ガラスになります。この実験では、1 L の容器に氷の 500 g を追加します。
- コンサルティング氷浴 (表 1) 添加剤の適切な量を比較検討し、添加物を氷に追加します。この実験のための重量を量るし、風呂容器に食塩の 165 g (= 5 x 33 g) を追加します。
- 風呂容器に少量の脱イオン水を加え、攪拌棒を使用して徹底的をかき混ぜます。すべての氷が覆われるまでは、だけで十分な水を追加します。
- 目的の温度に達していることを確認する温度計をチェックしてください。必要に応じて添加量を調整します。お風呂が非常に長いため、温度を維持しておらず、調整は 20-30 分毎についての頻繁な間隔で行われる必要があります。このお風呂の水の一部をピペットおよびより多くの氷と添加剤を追加する必要がある場合があります。
| 物質 | g/100 g H2O | 最終的な温度 (° C) |
| Na2CO3 | 20 | -2.0 |
| NH43 | 106 | -4.0 |
| NaC2H3O2 | 85 | -4.7 |
| NH4Cl | 30 | -5.1 |
| ナノ3 | 75 | -5.3 |
| ナ2S2O3 ● 5 H2O | 110 | -8.0 |
| CaCl2 ● 6 H2O | 41 | -9.0 |
| KCl | 30 | -10.9 |
| KI | 140 | -11.7 |
| NH43 | 60 | -13.6 |
| NH4Cl | 25 | -15.4 |
| NH43 | 45 | -16.8 |
| NH4SCN | 133 | -18.0 |
| 塩化ナトリウム | 33 | -21.3 |
| CaCl2 ● 6 H2O | 81 | -21.5 |
| H24 (66.2%) | 23 | -25 |
| NaBr | 66 | -28 |
| H24 (66.2%) | 40 | -30 |
| C2H5オハイオ (4°) | 105 | -30 |
| MgCl2 | 85 | -34 |
| H24 (66.2%) | 91 | -37 |
| CaCl2 ● 6 H2O | 123 | -40.3 |
| CaCl2 ● 6 H2O | 143 | -55 |
表 1。塩/氷、水または指定した量、特定の温度で氷と塩の混合によって得られる冷却の混合物。1
2. ドライアイス風呂を作る
- 低温保護手袋、安全ゴーグルを置きます。ドライアイスを取り扱う際にこれを常に練習し、肌を書き込むことができます急速に凍傷の原因となる素手でそれに触れることはありません。
- 約 1 リットルの容積を持つバス船、ドライアイス (~ 2 lb ブロックで通常利用可能) のブロックの約 1/3 を取るし、いくつかのより小さな部分に分割しています。
- お風呂容器にドライアイスの部分を追加します。
- ゆっくりとガラス棒で攪拌しながらドライアイスに有機溶剤 (アセトンなど) を追加します。CO2ガスの開発の結果として積極的な fizzing があります。
- ゆっくりと溶媒を追加し、均質なスラリー フォームおよびドライアイス溶解のほとんどになるまで炒め続けます。これは、反応フラスコへの熱伝達ができるだけ均一であることを確認することです。
- 所望の温度が達されることを確保するため風呂に低温温度計を挿入します。
- 一定の間隔でドライ氷浴を確認し、追加ドライアイス浴温の上昇のチャンクを気づいた。時間間隔は、断熱材の程度によって異なりますは通常約 45-60 分毎。
3. 液体窒素お風呂を作る
- 低温保護手袋、安全ゴーグルを置きます。皮膚組織と凍傷や永久的な目被害を引き起こす目流体を急速に書き込むことができますそれと液体窒素を処理するときにいつもこれを練習します。
- 添加物なしのバス、-196 ° C の温度を得るためデュワーに N2の適切な量を追加します。これは、所望の温度ステップ 3.3 に移動します。
- 添加剤とお風呂の最初に、デュワーに有機溶媒として選択 (右の溶媒を探して適切な温度の表 3を参照してください) を追加し、ゆっくりと、溶剤液 N2を追加します。
- 目的の温度に達していることを確保するため風呂に低温温度計を挿入します。他のお風呂とは対照的、デュワー内 N2浴は一度に数時間のための温度を維持します。
- お風呂で適切な間隔 (数時間) 以上の N2が必要なかどうか参照してくださいをチェックインします。
低温で反応を実行する役に立つはいつですか
この質問に答えるために私たちは 4 つの異なるアプリケーションを調査してみましょう。
アプリケーション 1.時々 反応があまりにも活発で、発熱し、流出を防ぐため、圧力ガスの開発のための上昇のために反応混合物を冷却する必要があります。発熱反応が反応混合物は急速に沸騰することができます、また安全上の問題になることができます (多くの有機溶剤は通常低沸点ポイントを持っている) が噴出して。この非常に一般的なアプリケーションは、焼入や水と残りの反応中間体と反応を反応してある最終製品の順序で最後に酸と反応し、反応当初行われる場所無水条件下で作業をステップ。たとえば、グリニャール反応、有機化学で非常に一般的な反応の最後に焼入の手順が必要になります、冷却にもかかわらず、0 ° C で氷水浴で十分です。
(4)
アプリケーション 2.冷却することができます反応の開始時に追加の手順の必要なときに発熱反応と有機溶剤から沸騰し、それ以外の場合。これは望ましい反応は、溶媒で遂行最高です。溶剤の損失を補うためにより多くの溶媒を追加することは無駄なと不経済なばかりも退屈な多くの反応の溶媒を必要と無水ようにステップを乾燥前。また、高温で熱分解する特定の試薬のため可能です。
発熱反応のこれらの発生を避けるためには、試薬はしばしば滴下シリンジまたは滴下漏斗でフラスコに加え攪拌、冷却しながら溶媒中で別の試薬を含みます。このように、追加を停止できますいつでも反応があまりにも積極的になった場合。多くの場合、反応は 0 ° C 以下も冷却する必要があります、氷水浴が十分ではありません。
これが必要な反応の例、ジイソプロピルアミン リチウムジイソプロピルアミド (LDA) を形成するために、強力な基本 n-ブチル リチウム (n-バリ) の追加です。
(5)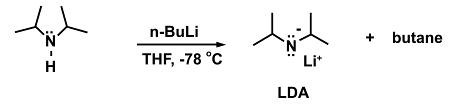
冷却槽の不在でより高い温度に達したとき、n バリは分解可能性があります。
(6)
アプリケーション 3.いくつかの化学反応で競合する反応経路から生じる 1 つ以上の可能な製品があります。1 つの製品より少ない活発化エネルギー (Ea1) を必要とするより安定した状態で経路の結果である、他の製品より多くの活性化エネルギー (Ea2) を必要があります全体的な安定はありませんが可能性があります。前者は、熱力学 (TD) 製品と称しながら運動の製品と呼ばれる (図 2のエネルギー図参照)。
反応温度を制御することでこれらの製品の 1 つの形成を制御できます。キネティックの製品より少ない活発化エネルギーを必要とするため低温で形成される製品です。しばしば低温で反応を行うと、熱力学的製品を運動製品の形成が保証されます。
エノラートの化学の領域で古典的な例 2-メチルシクロヘキサノン異なる反応条件下での異なるベースとの反応であります。反応液非対称ケトンは、したがっての α-水素の 2 種類を所有しています。水酸化ナトリウム脱プロトン化より高い置換の側より安定した、熱力学的エノラート (7) の結果でケトンなどの小さな拠点。基盤は、脱プロトン化の速度論的エノラート (8) の結果より少なく妨げ側ケトンを求めているより立体.キネティックのエノラートの形成だろう多くの収量室温に比べて-78 ° C で反応を行った場合エノラートの 2 つの形式は、以下に示す α-アルキル化製品を形成する適切な求電子体、methyiodide などと反応することができます。
(7)(8)
キネティック エノラートを取得に使用される立体厳しい基本 LDA、スキーム (5) に示したとおりのする準備がされます。熱力学的エノラートに平衡にキネティック エノラートを防ぐために-78 ° C に温度を制御することが重要です。(注: 以外の-78 ° C の温度にそれは簡単にアセトンでドライ氷浴によって得られる意義はありません)。
別に温度制御、追加注文と試薬の添加の方法が重要です。最良の結果は、速度論的エノラートを優遇、溶媒中で LDA ベースに滴下ケトン反応のソリューションが追加されます。LDA を反応に使用される無水溶媒は頻繁に THF です。例の反応は、スキーム (9) に表示されます。
(9)
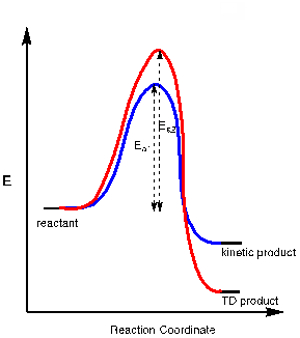
図 2。エネルギー ダイアグラムは、運動反応の熱力学的製品。
アプリケーション 4.いくつかのケースでは、温度と試薬の反応性を調整することが可能です。たとえば、エステル化を検討してください。強い水素還元剤リチウム アルミニウム水素化合物 (LAH) との反応は、それぞれ第一級アルコール (10) までのエステル化の結果します。ただし、それぞれのアルデヒド、エステルの還元のかさばる水素還元剤 diisobutylaluminum 水素化物 (DIBAL) の使用ができます。第一級アルコールを過剰減少を避けることができる、反応温度では限り、DIBAL-78 ° C (まだより良いダウン-90 ° c) の下で保たれたとだけに 1 つ化学量論的相当使用 (12)。-70 ° C の上の温度で DIBAL も反応となり、第一級アルコール (11) にエステルを削減します。
(10)-(12)
- Gordon, A. J., Ford, R. A. The Chemist's Companion - A Handbook of Practical Data, Techniques, and References. Chapter 11 (1973) ISBN: 978-0-471-31590-2.
- Rondeau, R. E. Slush baths. J. Chem. Eng. Data. 11, 124 (1966)
スキップ先...
このコレクションのビデオ:

Now Playing
室温以下の反応を実施
Organic Chemistry
70.3K 閲覧数

触媒入門
Organic Chemistry
34.1K 閲覧数

温水の化学反応のための還流システムの組み立て
Organic Chemistry
166.3K 閲覧数

Schlenk ライン溶剤伝
Organic Chemistry
41.5K 閲覧数

凍害ポンプ サイクリングで液体の脱気
Organic Chemistry
55.9K 閲覧数

無水試薬と機器の準備
Organic Chemistry
79.1K 閲覧数

再結晶により物質を浄化
Organic Chemistry
705.3K 閲覧数

沈殿物によって混合物の分離
Organic Chemistry
157.2K 閲覧数

固液抽出
Organic Chemistry
237.1K 閲覧数

溶媒を除去する回転蒸発
Organic Chemistry
212.3K 閲覧数

分別蒸留
Organic Chemistry
332.8K 閲覧数

X 線回折用結晶を成長
Organic Chemistry
32.3K 閲覧数

Performing 1D Thin Layer Chromatography
Organic Chemistry
288.4K 閲覧数

カラム ・ クロマトグラフィ
Organic Chemistry
358.4K 閲覧数

核磁気共鳴 (NMR) 分光法
Organic Chemistry
246.7K 閲覧数
Copyright © 2023 MyJoVE Corporation. All rights reserved