Galvanizzazione di pellicole sottili
Panoramica
Fonte: Logan G. Kiefer, Andrew R. Falkowski e Taylor D. Sparks,Dipartimento di Scienza e Ingegneria dei Materiali, Università dello Utah, Salt Lake City, UT
La galvanostegia è un processo che utilizza la corrente elettrica per ridurre i cationi metallici disciolti in modo che formino un rivestimento sottile su un elettrodo. Altre tecniche di deposizione a film sottile includono la deposizione chimica da vapore (CVD), il rivestimento spin, il rivestimento a immersione e la deposizione sputter, tra gli altri. CVD utilizza un precursore in fase gassosa dell'elemento da depositare. Il rivestimento di spin diffonde il precursore liquido centrifugamente. Il rivestimento a immersione è simile al rivestimento a spin, ma piuttosto che far girare il precursore liquido, il substrato è completamente immerso in esso. Sputtering utilizza il plasma per rimuovere il materiale desiderato da un bersaglio, che quindi piastre il substrato. Tecniche come CVD o sputtering producono film di altissima qualità, ma lo fanno molto lentamente e ad alto costo poiché queste tecniche richiedono in genere un'atmosfera sottovuoto e piccole dimensioni del campione. L'elettrodeposizione non si basa su un'atmosfera sottovuoto che riduce notevolmente i costi e aumenta la scalabilità. Inoltre, tassi di deposizione relativamente elevati possono essere raggiunti con l'elettrodeposizione.
Principi
Le celle galvaniche sono costituite da due metalli diversi collegati da un ponte salino o da una membrana porosa. Queste celle elettrochimiche hanno reazioni di ossidazione e riduzione delle semicelle che si verificano spontaneamente per ricavare energia. L'elettrodeposizione inverte la cella galvanica fornendo energia per guidare reazioni redox non spontanee per placcare un elettrodo con un film sottile. L'anodo è costituito dal metallo da placcare e viene ossidato alimentando corrente continua. Questa ossidazione all'anodo crea ioni che si dissolvono e fluiscono attraverso la soluzione elettrolitica, che contiene sali metallici e altri ioni per consentire il flusso di elettricità. Gli ioni disciolti vengono ridotti e placcati sul catodo. Le celle elettrocromiche cambiano il loro assorbimento ottico quando sottoposte a una tensione. Come per la galvanostea, l'azionamento delle reazioni redox elettrocromiche consente a questi materiali di passare tra stati sbiancati e colorati, come con il materiale rivestito blu di Prussia.
Il processo di galvanica richiede che entrambi i materiali utilizzati nel processo siano conduttivi, in quanto tali metalli e composti metallici sono principalmente utilizzati. Affinché la placcatura abbia successo, la superficie del materiale che verrà placcato deve essere completamente pulita. La pulizia della superficie è assicurata immergendo il materiale in un acido forte o collegando brevemente il circuito galvanico al contrario - se l'elettrodo è pulito, gli atomi del metallo di placcatura si legheranno ad esso in modo efficace. Anche se la superficie è pulita, può risultare una placcatura inefficace quando i componenti hanno geometrie complesse, che portano a una distribuzione irregolare dello spessore della placcatura. Lo spessore della placcatura può essere controllato variando la durata della corrente elettrica tra i metalli e la forza della corrente applicata tra i metalli. L'aumento di uno o entrambi questi aumenterà lo spessore della placcatura. Controllando lo spessore della placcatura, è possibile evitare problemi di placcatura derivanti da geometrie complesse.
L'obiettivo della tecnica proposta è quello di galvanizzare un sottile film di blu di Prussia su un foglio di PET rivestito ITO, e quindi misurare la capacità del film di assorbire e trasmettere luce utilizzando la spettroscopia UV-Vis. I dati UV-Vis del film sottile elettrocromico nello stato sbiancato e colorato quantificheranno le differenze di colore tra il film in questi due stati. Inoltre, i film elettrocromici più spessi raggiungeranno uno stato colorato più profondo e quindi assorbiranno relativamente più luce rispetto ai film più sottili. Pertanto, UV-Vis può essere utilizzato anche per effettuare confronti qualitativi dello spessore tra i film.
Procedura
- Preparare la soluzione di blu di Prussia mescolando 50 mL di acido cloridrico (HCl) 0,05 M), 100 mL di ferricianuro di potassio 0,05 M (K3[Fe(CN)6]) e 100 mL di cloruro di ferro (III) esaidrato (FeCl3,6H2O).
- Creare l'anodo avvolgendo circa 8 cm di filo di nicromo (NiCr) in una bobina stretta.
- Preparare il substrato catodico rimuovendo il rivestimento esterno che protegge il lato conduttivo di un foglio di 5X5 centimetri di PET rivestito ITO.
- Costruisci il circuito collegando il terminale positivo di una batteria da 9 volt (9V) in serie a un resistore da 30 ohm e quindi all'anodo NiCr usando una clip a coccodrillo. Collegare l'estremità negativa della batteria al substrato catodico ITO utilizzando una clip a coccodrillo. Assicurarsi che il catodo e l'anodo non si tocchino nella soluzione.
- Dopo aver preparato il circuito e la soluzione blu di Prussia, abbassare il catodo e l'anodo nella soluzione, facendo attenzione a non immergere nessuna delle due clip di alligatore. Tenere premuto per 2 minuti, quindi rimuovere e risciacquare sia il catodo che l'anodo in acqua DI. Questo passaggio può essere ripetuto con tempi di immersione variabili per variare lo spessore del rivestimento.
- Analizza il campione utilizzando lo spettrometro PERkin Elmer Lambda 950 UV-Vis, determinando la sua trasmittanza della luce visibile che varia in lunghezza d'onda da 750-400 nm. Assicurarsi di analizzare il livello di trasmittanza di fondo scansionando un campione PET rivestito ITO che non è stato rivestito con blu di Prussia.
- Dopo aver eseguito il campione di Blu di Prussia nell'UV-Vis, preparare una soluzione da 150 ml di cloruro di potassio (KCl) da 1,0 M.
- Utilizzare lo stesso circuito e l'anodo NiCr (utilizzando la batteria da 9 V in serie) e una clip alligatore aggiuntiva per collegare entrambi i lati dello strato blu di Prussia al circuito. Immergere l'anodo e il catodo nella soluzione KCl per 1,5 minuti, guidando la transizione elettrocromica da colorato a sbiancato.
- Quindi rimuovere e risciacquare sia il catodo che l'anodo in acqua DI come prima.
- Eseguire il campione sbiancato nell'UV-Vis, utilizzando i suddetti parametri scat di trasmittanza.
Risultati
Qualitativamente, l'ITO rivestito in blu di Prussia, diventerà trasparente quando verrà applicato un potenziale negativo, come mostrato nella Figura 1 di seguito. Questo cambiamento può essere invertito applicando una tensione positiva.

Figura 1: Blu di Prussia nei suoi stati colorati e sbiancati.
Più qualitativamente, lo spessore dello strato depositato può essere modificato e misurato in vari modi, anche modificando la tensione di elettrodeposizione o il tempo di elettrodeposizione. Per il blu di Prussia, gli spessori variabili dello strato influenzeranno la trasmissione percentuale della luce attraverso il campione. La relazione tra la quantità di Blu di Prussia depositata sull'ITO e il grado di opacità può essere misurata attraverso la spettrofotometria UV-Visibile ed è mostrata nelle Figure 2 e 3.
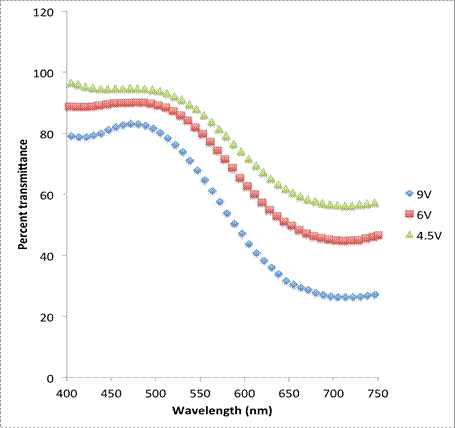
Figura 2: Spettroscopia UV-Vis del Blu di Prussia nel suo stato colorato per varie tensioni di deposizione elettrochimica.

Figura 3: Spettroscopia UV-Vis del Blu di Prussia allo stato colorato per vari tempi di deposizione elettrochimica.
Le pellicole depositate a una tensione più elevata hanno visto una trasmittanza percentuale inferiore rispetto a quelle depositate a una tensione inferiore. Ciò indica che gli strati sono più spessi a tensioni più elevate rispetto a tensioni più basse. Inoltre, i campioni elettrodepositati per tempi più lunghi hanno visto trasmittanze percentuali inferiori, indicando ancora una volta che i film sono più spessi a tempi di deposizione più lunghi.
Applicazione e Riepilogo
L'elettrodeposizione, come dimostrato in questo esperimento, consente la modifica delle proprietà superficiali di un materiale entro un minimo cambiamento di volume. Nel processo di elettrodeposizione, una corrente elettrica viene fatta passare attraverso una soluzione elettrolitica tra un anodo e un catodo. I cationi caricati positivamente nella soluzione elettrolitica sono attratti e depositati sul catodo caricato negativamente. Una volta depositati, gli atomi nello strato guadagnano elettroni attraverso il processo di riduzione.
La velocità e la quantità di elettrodeposizione dipendono dalla forza della corrente elettrica applicata tra il catodo e l'anodo nella soluzione elettrolitica. Inoltre, i metalli utilizzati nell'elettrodeposizione devono essere scelti con attenzione, poiché alcuni metalli si legheranno l'uno con l'altro; in questi casi, devono essere depositati più strati metallici.
Poiché i cationi sono legati chimicamente al substrato, l'elettrodeposizione presenta i vantaggi di un'espansione termica unificata, una migliore resistenza alla corrosione chimica e una maggiore durata fisica. Uno svantaggio della deposizione elettrochimica rispetto ad altri metodi di deposizione a film sottile è la necessità di una superficie conduttiva sul substrato prima della deposizione. Inoltre, il processo di elettrodeposizione non sempre produce una deposizione uniforme, il che causa incongruenze nel rivestimento del materiale.
L'elettrodeposizione ha molte applicazioni oltre al deposito del blu di Prussia. L'elettrodeposizione è ampiamente utilizzata nell'industria della gioielleria in quanto consente un alto grado di controllo sul processo di placcatura e consente varie modifiche estetiche. Un'ampia varietà di variazioni di colore può essere ottenuta depositando diversi metalli per formare leghe con aspetti unici. Inoltre, i metalli possono essere depositati in modo uniforme, il che riduce le incongruenze di colore e può nascondere le linee di saldatura e componenti. Utilizzando l'elettrodeposizione, i gioiellieri sono in grado di creare rivestimenti metallici funzionali e coerenti che sono esteticamente gradevoli.
L'elettrodeposizione è utilizzata anche nell'industria automobilistica. I veicoli sono costantemente soggetti a forze che usurano i componenti vitali. L'elettrodeposizione consente di modificare e migliorare le proprietà delle varie parti senza modificare il volume funzionale della parte. Il cromo depositato fornisce una protezione superiore all'usura e alla corrosione per i veicoli e consente alle auto di durare più a lungo con requisiti minimi per la manutenzione e la riparazione.
Nell'industria dei semiconduttori, l'elettrodeposizione offre notevoli vantaggi in termini di costi, affidabilità e ambiente rispetto alla classica tecnologia di evaporazione e può ospitare wafer di dimensioni molto diverse. Il processo di elettrodeposizione consente la deposizione su substrati fragili e consente anche un controllo avanzato della forma o nuove funzionalità. L'elettrodeposizione offre un mezzo per campioni unici a basso costo utilizzando una tecnologia prontamente adattata alla produzione industriale.
Tags
Vai a...
Video da questa raccolta:

Now Playing
Galvanizzazione di pellicole sottili
Materials Engineering
20.2K Visualizzazioni

Materialografia ottica parte1: preparazione del campione
Materials Engineering
15.6K Visualizzazioni

Materialografia ottica parte 2: analisi dell'immagine
Materials Engineering
11.2K Visualizzazioni

Spettroscopia fotoelettronica a raggi X
Materials Engineering
21.9K Visualizzazioni

Diffrazione dei raggi X
Materials Engineering
89.8K Visualizzazioni

Fasci ionici focalizzati
Materials Engineering
9.0K Visualizzazioni

Solidificazione direzionale e stabilizzazione di fase
Materials Engineering
6.7K Visualizzazioni

Calorimetria differenziale a scansione
Materials Engineering
38.7K Visualizzazioni

Diffusività termica e metodo del flash laser
Materials Engineering
13.4K Visualizzazioni

Analisi dell'espansione termica tramite dilatometria
Materials Engineering
16.0K Visualizzazioni

La spettroscopia di impedenza elettrochimica
Materials Engineering
23.4K Visualizzazioni

Materiali compositi a matrice ceramica e le loro proprietà di flessione
Materials Engineering
8.4K Visualizzazioni

Leghe nanocristalline e stabilità dimensionale dei nano-grani
Materials Engineering
5.2K Visualizzazioni

Sintesi di idrogel
Materials Engineering
23.9K Visualizzazioni