Method Article
Valutazione del Boro Doped Diamante elettrodi Qualità e applicazioni per
In questo articolo
Riepilogo
Un protocollo è descritto per la caratterizzazione dei parametri chiave elettrochimici di boro diamante drogato (BDD) elettrodo e la successiva domanda di esperimenti in situ generazione pH.
Abstract
Boron diamante drogato (BDD) elettrodi hanno dimostrato molto promettente come materiale degli elettrodi dove molte delle loro proprietà riportate come esteso finestra solvente, basse correnti di fondo, resistenza alla corrosione, ecc, derivano dalla natura cataliticamente inerte della superficie. Tuttavia, se durante il processo di crescita, non-diamante-carbonio (NDC) viene incorporato nella matrice elettrodi, le proprietà elettrochimiche cambiano mentre la superficie diventa più cataliticamente attivo. Come tale, è importante che la elettrochimico è consapevole della qualità e conseguente principali proprietà elettrochimiche dell'elettrodo BDD prima dell'uso. Questo articolo descrive una serie di fasi di caratterizzazione, tra cui la microscopia Raman, capacità, finestra solvente e redox elettrochimica, per accertare se l'elettrodo BDD contiene trascurabile NDC e quindi trascurabile sp 2 di carbonio. Un'applicazione è evidenziato che sfrutta il cataliticamente inertee la natura resistente alla corrosione di una superficie NDC privo cioè protoni locale stabile e quantificabile e la produzione di idrossido causa di elettrolisi dell'acqua ad un elettrodo di BDD. Un approccio per misurare la variazione del pH locale indotta mediante elettrolisi dell'acqua utilizzando ossido di iridio elettrodi rivestiti BDD è anche descritto in dettaglio.
Introduzione
Scelta del materiale degli elettrodi è di grande importanza per lo svolgimento di qualsiasi studio elettroanalitica. Negli ultimi anni, sp 3 del carbonio (diamante) drogato con boro sufficiente a rendere il materiale "metal-like" è diventato una scelta popolare per una vasta gamma di applicazioni elettroanalitiche grazie alla sua eccellente elettrochimica (e termiche e meccaniche) proprietà 1,2 , 3. Questi includono la resistenza alla corrosione sotto soluzione, temperatura e pressione estreme 4 finestre solvente ultra-larga e bassa sfondo correnti, e ridotto sporcamento, rispetto ad altri materiali elettrodici comunemente usati 5-7,3. Tuttavia, l'aumento non-diamante-carbonio (NDC: sp 2) Opere risultati in una finestra di solvente in diminuzione, l'aumento delle correnti di fondo 7,8, cambiamenti sia l'integrità strutturale e la sensibilità verso diverse specie redox sfera interiore, ad esempio. ossigeno 9-12.
Nota per cosìmi applicazioni, presenza NDC è visto come vantaggioso 13. Inoltre, se il materiale non contiene boro sufficiente si comporterà come p-tipo semiconduttore e mostra una ridotta sensibilità alle specie redox nella finestra potenziale riduttivo, dove il materiale è più impoverito di portatori di carica 7. Infine, la chimica superficiale del boro diamante drogato (BDD) può anche giocare un ruolo nella risposta elettrochimica osservata. Questo è particolarmente vero per le specie a sfera interna che sono sensibili alla superficie chimica e abbassare diamante drogato dove un idrogeno (H -) - superficie chiuso possa far apparire un elettrodo BDD semiconduttore "metal-like" 7.
Per sfruttare le proprietà superiori di BDD, è spesso necessario il materiale è sufficientemente drogato e contiene il meno possibile NDC. A seconda del metodo adottato per far crescere il BDD, le proprietà possono variare 14,15. Questo documento suggerisce primo un materiale e di un elettorochemical Guida protocollo di caratterizzazione per la valutazione BDD elettrodo idoneità prima dell'uso (cioè boro sufficiente, minimo NDC) e poi descrive una applicazione basata sul cambiamento localmente pH elettrochimica tramite l'elettrodo protocollo verificata. Questo processo sfrutta la resistenza superficiale del NDC-libera BDD verso corrosione o la dissoluzione sotto il controllo di potenziali estreme applicato (o correnti) per lunghi periodi di tempo. In particolare l'uso di un elettrodo BDD per generare protone stabile (H +) o idrossido (OH -) fondenti causa dell'elettrolisi (ossidazione o riduzione rispettivamente) di acqua in prossimità di un secondo (sensore) 16,17 è descritto qui.
In questo modo è possibile controllare l'ambiente pH del sensore in modo sistematico, ad esempio per esperimenti di titolazione pH, o per fissare il pH ad un valore in cui il processo elettrochimico è più sensibile. Quest'ultimo è particolarmente utile perapplicazioni in cui il sensore è posto alla fonte, ad esempio fiume, mare e il pH del sistema non è ottimale per la misura elettrochimica di interesse. Due esempi recenti comprendono: (i) generazione di un basso pH localizzata, in una soluzione a pH neutro, per l'elettrodeposizione e stripping di mercurio 17; notare BDD è un materiale preferito per elettrodeposizione di metalli grazie alla finestra catodica estesa 9,18,19. (ii) La quantificazione della forma elettrochimicamente rilevabile di solfuro di idrogeno, presente a pH elevato, aumentando localmente il pH da neutro a fortemente alcalina 16.
Protocollo
NOTA: elettrodi BDD sono più comunemente coltivate utilizzando tecniche di deposizione di vapore chimico, attaccato ad un substrato di crescita. Lasciano la camera di crescita H-terminato (idrofobico). Se coltivata abbastanza spessa BDD può essere rimosso dal substrato e si definisce indipendente. La superficie di crescita BDD freestanding è spesso lucidato per ridurre in modo significativo la rugosità superficiale. Pulizia del BDD nei risultati di acido in un ossigeno (O) di superficie -terminated.
1. Acido Pulizia BDD
- Posizionare un bicchiere di acido solforico concentrato (H 2 SO 4; ~ 2 ml o abbastanza in profondità per coprire il diamante) su un piatto caldo a temperatura ambiente e inserire il BDD.
- Aggiungere nitrato di potassio (KNO 3) fino dissolve non più (~ 0,5 g in 2 ml), poi coprire con un vetro d'orologio e calore a ~ 300 ° C, la soluzione diventa marrone come si riscalda e il nitrato di potassio si dissolverà.
ATTENZIONE Si deve prestare attenzione quando si maneggiano acido caldo!; guanti di gomma, di sicurezza glasses e camice da laboratorio dovrebbero essere indossati e questo processo dovrebbero essere condotte in una cappa aspirante. - Lasciare riscaldare per almeno 30 minuti o fino a quando non vi è più alcun colore marrone alla soluzione, quindi spegnere la piastra calda e lasciare la soluzione raffreddare a RT.
- Smaltire con cura dell'acido diluendo in acqua RT e sciacquare il BDD con acqua distillata.
- Misurare l'angolo di contatto di superficie, vedere la sezione 1.2. Idrofobo (H-terminato) 20,21 elettrodi hanno riportato angoli di contatto nell'intervallo 60-90 ° 3, che riduce significativamente la superficie è resa idrofila tramite O-terminazione.
- (metodo facoltativo alternativo) Per elettrodi a film molto sottili (attaccato al substrato di crescita ed evitare pellicola delaminazione utilizzando il trattamento di cui sopra), lavare una volta con 2-propanolo e due volte con acqua deionizzata in un bagno ad ultrasuoni. Poi, adotta uno dei tre seguenti procedure di pulizia (1) anodicamente polarizzare il diamante per 30 min a 10 mA cm -2 In 1 M di acido perclorico al 40 ° C 22; o (2) anodicamente polarizzare il diamante per 20 minuti a 10 mA cm -2 in 1 M di acido nitrico, successivamente catodicamente polarizzare a 10 mA cm -2 per altri 20 min nella stessa soluzione 23 o; (3) Ciclo diamante tra 2 V a 0,1 MH 2 SO 4 fino a quando un segnale elettrochimico stabile è raggiunto 7. Seguire questo con passo 1.4.
2. Angolo di contatto di misura
- Posizionare il diamante sul palco campione di un analizzatore di angolo di contatto, assicurando che sia piatta. Inserire una siringa da 1 ml nel posizionatore sopra la fase del campione, fissare un ago all'estremità. Riempire la siringa con acqua deionizzata.
- Utilizzare il controllore z per abbassare la siringa al campione, utilizzare il x - y - e controllori e la fotocamera / illuminatore per allineare la siringa sopra il centro del diamante.
- Utilizzando il software analizzatore di erogazione ripetere 1 ml volumes di acqua dalla siringa fino ad ottenere una gocciolina sulla punta dell'ago, visibili dell'immagine della telecamera (non più di 10 microlitri) su. Abbassare l'ago a depositare la goccia sulla superficie e regolare l'illuminazione per massimo contrasto.
- Raccogliere l'immagine e applicare rilasciare software di analisi forma, utilizzando il metodo conica. Fai clic su "trovare base" nel software, e quindi fare clic su "calcolo" seguito da "tangenti".
NOTA: questa procedura individua la linea di base e si inserisce un'equazione conica per la (ellittica) cadere forma; un angolo di contatto, θ, è tracciata tra la linea di base e la tangente nel punto di contatto trifase.
3. BDD Materiale Caratterizzazione
- Analisi Raman per sp 2 / sp 3 contenuti
- Eseguire Raman (vedi riferimento 14 per una guida pratica Raman Spectroscopy) in diverse aree diverse dell'elettrodo BDD, 24 utilizzo di un 514,5 nm o532 nm laser, che sottolinea sp 2 di contenuti, è sostenuto.
- Accendere lo spettrometro micro-Raman e consentire ~ 30 min per il rivelatore CCD raffreddare. Controllare l'obiettivo appropriato, reticolo di diffrazione e filtri sono in atto per l'uso con il laser di scelta.
- Calibrare il sistema utilizzando un campione di calibrazione di silicio (Si). Posizionare il substrato di Si nella camera di strumento e concentrarsi otticamente sul campione con il microscopio. Chiudi la porta alla camera. Passare alla visualizzazione del laser e controllare il punto laser è ben definito e circolare. Calibrare l'utilizzo del software, fare clic su "strumenti" seguito da "taratura" "calibrazione rapida" quindi quindi "ok".
- Rimuovere il substrato di Si dalla camera e sostituire con l'elettrodo BDD. Otticamente concentrarsi microscopio sulla zona di interesse, passare alla visualizzazione laser e aprire l'otturatore per verificare che il laser è focalizzato. Chiudere l'otturatore.
- Effettuare una misurazione Raman utilizzando il software; click "misura", allora "nuovo", quindi "acquisizione spettrale." impostare l'intervallo di misura numero d'onda per coprire le caratteristiche di interesse, per BDD questo è di 200 - 1.800 centimetri -1; impostare il tempo di acquisizione di scansione (<10 sec); impostare la potenza del laser di 100% (per BDD) e; impostare il numero di accumuli (scansioni ripetizione) a cinque (per BDD). Se lo spettro risultante è molto rumoroso più accumuli possono essere necessarie. Premere corsa e salvare lo spettro risultante per l'analisi. Scatta una foto della zona Raman è stata eseguita utilizzando il video in diretta. Salvare l'immagine come riferimento.
- Osservare i picchi ~ 1.332 cm -1 nello spettro che indica sp 3 diamante (figura 1); più ampio è il picco più difetti presenti 3,25.
- Osservare qualsiasi NDC - indicata da un picco ampio G centrato a 1.575 cm -1 26, negli spettri (Figura 1A e 1B), proveniente dalla stiramento sp accoppiato 2 siti; maggiore è l'intensità di picco più NDC presente.
NOTA: i legami ¸ formati da sp 2 C sono più polarizzabile di sp 3 σ obbligazioni e sono di risonanza arricchisce di laser visibili, portando a più ampio, più dominante, G picchi di 25. Si noti che il metodo esatto utilizzato per eseguire analisi può variare tra i diversi strumenti e software.
4. Caratterizzazione elettrochimica
- Preparazione contatti ohmici
- Freestanding BDD
- Usando tecniche standard per polverizzazione catodica (o evaporare) la parte posteriore del BDD con titanio (Ti) / oro (Au) 10 nm / 300 nm, utilizzando un sputterer / evaporatore a pressioni inferiori a 1 × 10 -5 mbar. Se una fonte di tre bersaglio è disponibile, più idealmente è Ti 10 nm / platino (Pt) 10 nm / Au 300 nm per evitare la diffusione di Ti in Au.
- Anneal per 5 ore a 400 ° C (pressione atmosferica) permettendo Ti formare carburo di titanio, CRUCial per la formazione di un contatto ohmico 27.
NOTA: se la superficie posteriore del BDD è molto lucido (~ nm rugosità), allora è preferibilmente irruvidire la superficie prima di polverizzazione catodica per garantire un rivestimento più robusto. Ciò può essere ottenuto, ad esempio, bassa potenza laser micromachining superficie (rimuovendo <30 micron di materiale).
- Sottile pellicola diamante cresciuto su un substrato conduzione
- Sputter / evaporare come sopra, ma per la faccia superiore, utilizzando una maschera ombra delicatamente posto sulla superficie superiore per evitare all'inizio contattando dell'intero elettrodo.
O - Scratch retro del substrato condurre utilizzando una penna con punta di diamante. Poi rivestire la zona graffiata di condurre Ag pasta o una vernice conduttiva da pittura su uno strato sottile con un pennello piccolo. Infine, collegare elettricamente allegando fili di rame con resina epossidica conduttivo.
NOTA: ci sono una varietà di modi per preparare il BDD dopo elettiRical contatto come descritto nel riferimento 4, ad esempio se il BDD può essere lavorato in strutture più piccole, un sigillo in vetro o resina epossidica, o se ancora attaccato al morsetto wafer / allegare una cella elettrochimica per la superficie superiore.
- Sputter / evaporare come sopra, ma per la faccia superiore, utilizzando una maschera ombra delicatamente posto sulla superficie superiore per evitare all'inizio contattando dell'intero elettrodo.
- Freestanding BDD
- Misure di capacità
- Preparare a 20 ml di 0,1 M KNO soluzione 3 pesando 0,20 g in acqua bidistillata (questa la qualità dell'acqua è raccomandato per tutto, resistività 18,2 M cm). Pulire l'elettrodo prima di utilizzare sia per la lucidatura allumina o elettrochimicamente bicicletta in acido diluito (vedi capitolo 1 NOTA) 16,23,28.
- Utilizzando un potenziostato eseguire voltammograms ciclici (CV) a 0,1 V sec-1 tra il -0,1 V e 0,1 V, a partire da 0 V, con il BDD come elettrodo di lavoro rispetto a un elettrodo di riferimento comune, per esempio argento / cloruro d'argento (Ag / AgCl ) o un elettrodo a calomelano (SCE), e un elettrodo di Pt contatore. Analizzare la seconda CV.
NOTA: Figura 2A Mostra una curva di capacità tipica registrato con un freestanding metallico drogato elettrodo BDD. - Misurare la grandezza corrente totale a 0 V dalla curva capacitanza registrata e dividere per 2, questo valore è "i". Determinare la capacità, C, utilizzando il valore per i, con l'equazione 1, normalizzare rispetto all'elettrodo zona (pari al rugosità della superficie, se del caso) e citare in uF cm -2. Alta qualità, "metal-like" BDD ha una capacità << 10 uF cm -2. Utilizzare i dati tramando software per presentare e analizzare i dati.
i = C (Vt -1) (1 eq.);
dove i è la corrente (A) e (V t -1) è la frequenza di scansione potenziale.
- Finestra di solventi
- Pulire l'elettrodo come al punto 4.2.1. Utilizzando un potenziostato eseguire un CV in 0.1 M KNO 3 a 0,1 V sec-1 da 0 V a -2 V poi tra -2 V e 2 V and torna a 0 V con il BDD come elettrodo di lavoro rispetto a un elettrodo di riferimento comune e controelettrodo Pt. Ripetere. Analizzare la seconda CV, un esempio CV è mostrato nella Figura 2B.
- Convertire la corrente di densità di corrente (mA cm -2), prendendo in considerazione rugosità superficiale, e citano la finestra solvente come la finestra potenziale definito da limiti di corrente di ± 0,4 mA cm -2 in entrambe le direzioni. 7,29 Utilizzare i dati plotting software per presentare e analizzare i dati.
- Osservare la prova di NDC (sp 2 di carbonio) nella finestra di solventi; la reazione di riduzione dell'ossigeno è favorita in NDC che è chiaramente evidente nella finestra riduttiva. Ossidazione di sp 2 contenenti gruppi comporta anche picchi caratteristici appena prima l'elettrolisi dell'acqua nella finestra anodica (Figura 2B).
NOTA: alta qualità "metallici" elettrodi BDD hanno finestre solventi >> 3 V, non supportano la reazione di riduzione dell'ossigenozione (ORR) in 0,1 M KNO3 (o ORR è fortemente cineticamente ritardato) e mostrano trascurabili firme ossidazione NDC.
- Redox Elettrochimica
- Pulire l'elettrodo come al punto 4.2.1.
- Utilizzando un record potenziostato CV in 1 mM rutenio hexaamine (Ru (NH 3) 6 3 +) e 0,1 M KNO3 tra 0,2 V e 0,8 V contro SCE, per i tassi di scansione della gamma 0,05 V sec -1 - 0,2 V sec -1.
NOTA: Questa coppia mostra trasferimento elettronico veloce ed è elettroattivi in una regione che sfida p-tipo semiconduttore BDD. sp 2 contenente BDD mostrerà anche ORR in questa regione, il segnale per il secondo è più evidente come la concentrazione di Ru (NH 3) 6 3+ viene diminuita. - Misurare la separazione tra la tensione anodica e catodica corrente di picco (Δ E p) dal CV registrati, e la temperatura come descritto 20.Per "metal-like" ohmicamente contattato ossigeno terminato BDD a 298 K, Δ E p <70 mV 30,31. Più grandi valori p Δ E sono sintomatici di un contatto ohmico scarsa o un boro inferiore, come mostrato nella Figura 2C per BDD elettrodi di densità droganti nell'intervallo 9.2 × 10 16 a 3 × 10 20 cm -3 B atomi.
- Misurare la corrente di picco della scansione in avanti, i p, e correlano con quello atteso dall'equazione Randles Sevcik 2 (quotato a 298 K) 3,30, assumendo l'elettrodo è in geometria e abbastanza grande a forma di disco (1 mm di diametro), che domina la diffusione lineare. Utilizzare i dati tramando software per presentare e analizzare i dati.
i p = 2.69 × 10 5 n 3/2 AD 1/2 cv 1/2 (eq 2)
dove nè il numero di elettroni trasferiti, A è l'area (cm 2), D è il coefficiente di diffusione (cm 2 sec -1), c è la concentrazione (mol cm -3) ev è velocità di scansione (V sec -1).
5. pH Generazione: Preparazione di elettrodi pH sensibile e pH Generation
- Iridium Oxide (pH sensibile) Soluzione Preparazione
- Preparare una soluzione di KNO 3 20 ml 0,1 M come nella sezione 5.4.1. Aggiungere 5 gocce di soluzione di fenolftaleina con una pipetta Pasteur e mescolare (questo è sufficiente per vedere una risposta ad occhio, ma per un colore più intenso, aggiungere più gocce). Posizionare l'elettrodo di lavoro e BDD controelettrodo Pt in soluzione.
- Regolare il pH della soluzione a 10,5 per aggiunta di sale cloruro di potassio anidro, agitando continuamente. Lasciare coperto e agitazione per 48 ore a RT per stabilizzare, in questa fase la soluzione si porta gradualmente dal giallo-verdeblu-viola. Conservare in frigorifero a 3 ° C.
- pH sensibile Iridium Ossido Deposizione Film
- Utilizzando un potenziostato eseguire un CV nella soluzione di ossido di iridio tra 0 V e V +1 contro SCE per determinare il potenziale a cui viene registrata la corrente massima. Questo è il potenziale di deposizione, dep E come mostrato in Figura 3A, tipicamente compresa tra 0,6 V ~ + - 0,85 V; esso può variare a seconda di vari fattori quali la temperatura, ecc materiale degli elettrodi 32, 33
- Utilizzando cronoamperometria con un potenziostato, passo il potenziale da 0 V ("iniziale E" e "basso E" nel software), dove avviene senza elettrolisi per E dep ("High E" nel software), per un periodo di tempo di 0,2 sec per passo, ripetere 100x.
- Eseguire un CV tra 0 V e V 1 in 0.1 MH 2 SO 4 per la IRO X depositato elettrodo. Il personaggioForma istic CV è mostrato in Figura 3B. Una densità di corrente nella gamma ~ 0,6 mA cm -2 - 0,7 mA cm -2 per il primo picco anodico (corrispondente ad uno spessore di film di media ~ 8 nm di 0,7 mA cm -2), indica una pellicola sensibile pH stabile 34, 35.
- Se la densità di corrente è inferiore a 0,6 mA cm -2 ripetere i punti 5.2.2 - 5.2.4 fino al raggiungimento di questo valore. Lasciare l'elettrodo nella soluzione tampone a pH 7 per 24 ore per idratare la risposta del film IRO x è idratazione-dipendente 33.
- Iro x Film pH Caratterizzazione
- Preparare una serie di soluzioni tampone che coprono l'intervallo di pH di interesse (pH 2 - pH 12), questi possono essere realizzati in casa (es Carmody 36) o acquistati commercialmente.
- Risciacquare l'elettrodo con acqua distillata. Posizionare l'elettrodo iro x ed elettrodo di riferimento nella soluzione tampone a pH basso. Utilizzando un potenziostatoregistrare il potenziale di circuito aperto (OCP) oltre 30 sec, con tre ripetizioni. Rimuovere l'elettrodo dalla soluzione, risciacquo e posto nel buffer successivo.
- Ripetere il passaggio 5.3.2 per ogni buffer, quindi ripetere la serie di almeno due volte. Trama pH vs OCP, il diagramma di taratura per la risposta pellicola. Un film IRO x presenta un pendio con una pendenza tra i 59 - 80 mV per decennio 37.
NOTA: La Figura 3C mostra una trama esempio di calibrazione per il successo sensore pH Iro x su BDD.
- Utilizzando un generatore pH e sistema di misura
NOTA: questo presuppone l'uso di un sistema a doppio elettrodo cui un elettrodo viene rivestita con il film iro x (es disco) e la seconda (es anello BDD) genererà H + o OH - galvanostaticamente da elettrolisi dell'acqua.- Preparare una soluzione di KNO 3 20 ml 0,1 M aggiungendo acqua deionizzata al sale. Collegare il iro x rivestitaElettrodo come elettrodo di lavoro in un sistema a due elettrodi, con il secondo elettrodo un elettrodo di riferimento stabile es SCE. Misurare la OCP usando un potenziostato, per stabilire il pH di partenza.
- Collegare l'elettrodo generatore di un sistema galvanostatico due elettrodi adatti con un contro-elettrodo, ad esempio un foglio di Pt, e ripetere il punto 5.4.1, ma dopo un periodo di tempo definito applicare una corrente all'elettrodo generatore.
NOTA: troviamo correnti nella gamma da 0 a ± 50 μA sono adatti ai nostri elettrodi BDD; correnti più elevate si traducono in sviluppo di gas apprezzabile. L'entità e la direzione della corrente dipende dal risultato desiderato; una corrente positiva si tradurrà in un passaggio a pH più acido e una corrente negativa a pH più alcalino, maggiore è la corrente maggiore è il cambiamento di pH. - Utilizzando il potenziostato, registrare la variazione di OCP in risposta alla corrente galvanostatico, attendere che la risposta si stabilizza. Quindi inserire il iro x elettrodo pH buffer di 7 per 10 minuti per riequilibrare il film iro x.
- Ripetere i passaggi da 5.4.2 a 5.4.3 con diverse correnti applicati, fino a quando tutti i dati richiesti sono stati raccolti. Tracciare i dati utilizzando la curva di calibrazione ottenuta nel paragrafo 5.3 per convertire OCP a pH, un set di dati esempio è mostrato in Figura 4A. Rimuovere la pellicola IRO x utilizzando lucidatura allumina o pulsare in 0.1 MH 2 SO 4 da 2 V a -2 V per 0,2 sec, × 100. Applicare al sistema di misura di interesse.
- Valutazione visiva di generazione del pH locale
- Preparare una soluzione di KNO 3 20 ml 0,1 M come nella sezione 5.4.1. Aggiungere 5 gocce di soluzione di fenolftaleina con una pipetta Pasteur e mescolare (questo è sufficiente per vedere una risposta ad occhio, ma per un colore più intenso, aggiungere più gocce). Posizionare l'elettrodo di lavoro e BDD controelettrodo Pt in soluzione.
- Applicare una corrente negativa all'elettrodo di lavoro utilizzandoun galvanostato come al punto 5.4.2 (es ~ -0.6 mA cm -2) tale che la soluzione cambia colore da incolore a rosa. Questo genera ora localmente una soluzione che è a pH ≥ 10,5.
- Ripetere il passaggio 5.5.1 con 5 gocce di soluzione di rosso metile invece di fenolftaleina e mescolate. Applicare sufficientemente positivo corrente (es ~ 6,6 mA cm -2) tale che la soluzione cambia colore dal giallo al rosso. Questo genera ora localmente una soluzione che è a pH 4,2 ≤ 38.
Risultati
Raman spettri ed elettrochimici caratteristiche sono state ottenute per rappresentativi elettrodi macrodisc BDD con diverse densità drogante, ed entrambi i livelli significativi e trascurabili di NDC, figure 1 e 2. Figure 1A e B mostrano dati tipici Raman per NDC contenenti film sottile microcristallina BDD e grano più grande autoportante BDD, drogato sopra della soglia metallica, rispettivamente. La presenza di NDC è identificabile per le grandi vette etichettati tra i 1.400 e 1.600 centimetri -1; non esiste alcun picco visibile in Figura 1C, che mostra la tipica firma Raman di NDC-libera, autoportante BDD. In tutti e tre gli spettri in Figura 1 è possibile osservare un forte picco a 1.332 cm -1, questo è il picco di firma sp 3 del carbonio (diamante); asimmetria della linea di base intorno questo picco è noto come "risonanza Fano"E, se presente, il campione è opportunamente drogato (10 B 20 atomi cm -3) per l'uso in studi elettrochimici. Questo è il caso per tutti i tre elettrodi mostrati qui.
Nella figura 2 i dati di esempio per studi elettrochimici (capacitanza, finestra solvente e CV registrati nel mediatore redox Ru (NH 3) 6 3+) sono presentate sia NDC contenenti NDC e privo BDD, drogato sopra della soglia metallico. Le curve di capacità in figura 2A indicano chiaramente che NDC contenenti BDD presenta una maggiore corrente capacitiva di NDC-libera BDD. Le capacità di ciascun è stato calcolato come descritto nel testo e sono quotate in Figura 2A come 10,8 uF cm -2 (NDC-contenenti) e 6,3 uF cm -2 (NDC-gratuito) BDD. Alta qualità, basso NDC-contenuto, elettrodi BDD sono tenuti ad avere una capacità << 10 uF cm -2. Allo stesso modo, figura 2B confronto le finestre solvente di esemplare NDC contenenti elettrodi e NDC-liberi BDD. Si può notare che per un elettrodo NDC contenente l'insorgenza di H 2 O ossidazione e riduzione è stata portata in modo significativo, restringendo la finestra solvente. Anche di nota è la comparsa di picchi anodici per l'ossidazione di NDC e un picco catodica causa ORR che viene catalizzata sul NDC ma non su sp 3 del carbonio. Per un BDD elettrodo ad alta qualità con trascurabile NDC finestra solvente dovrebbe essere >> 3 V in soluzione acquosa KNO 3. Nella Figura 2C risposta CV di elettrodi BDD con una varietà di livelli di drogaggio viene studiata utilizzando il mediatore redox Ru (NH 3) 6 3+. Per elettrodi BDD drogato sopra della soglia metallico, la separazione tra la tensione anodica e catodica picchi di corrente dovrebbe essere vicino a 59 mV, in conformità con l'equazione di Nernst; However, come il livello di drogante diminuisce il materiale si impoverisce di portatori di carica con conseguente aumento nel picco picco separazione.
Un macrodisc BDD, rivestito in IRO x, è stato utilizzato per registrare i dati in figura 3, mentre tutti diamante (BDD isolato in diamante) 39 doppi elettrodi e una resina epossidica sigillato BDD elettrodo disco anello sono stati utilizzati per gli esperimenti di generazione pH in Figura 4A. I dati nella figura 3 illustra il processo di deposizione e caratterizzazione di IRO sensibile x pellicola pH sulla BDD. Nella Figura 3A mostra il CV tipico registrata nella soluzione x deposizione IRO. Il potenziale impiegato per la successiva IRO x deposizione può essere identificato dalla posizione del picco di corrente ossidativo, come qui illustrato. Figura 3B è un CV esemplare in acido solforico di IRO x pellicola dell'elettrodepositoed il BDD. La forma del CV è caratteristica di un film depositato con successo con la densità di corrente di picco fornire informazioni dello spessore del film. Una densità di corrente più elevato indica una pellicola spessa. La stabilità del film dipende spessore; troppo sottile e la risposta pH deriva, troppo spessa e il tempo di risposta pellicola sarà lenta e la pellicola può sfaldarsi. Un valore di picco per densità di corrente ~ 0,7 mA cm -2 è stato dimostrato per indicare una pellicola stabile con una eccellente risposta pH. La risposta OCP dello strato IRO x su un elettrodo BDD verso diversi tamponi pH è mostrato in Figura 3C. La deriva tra le misurazioni è piccolo come dimostra la dimensione delle barre di errore e la pendenza è super-Nernst (> 59 mV) come previsto per questo tipo di film.
Infine, la Figura 4 illustra l'uso di un elettrodo per la generazione BDD pH. Nella figura 4A il pH cambia measured ad un IRO x rivestito elettrodo BDD è presentato per una gamma di correnti applicate alla generazione pH BDD elettrodo posto nelle vicinanze, sia in formato banda anello o, come illustrato nella figura 4. Per diverse correnti applicate, il pH può essere cambiata localmente e quantificabile da un valore iniziale (quasi neutro) a uno acide o alcaline. Questo processo può essere osservato visivamente, come illustrato in Figura 4B, dove una densità di corrente adatta viene applicata ad un elettrodo di BDD per passare da pH vicino alla neutralità a> 10.5. In presenza di fenolftaleina (indicatore pH) il risultato è la soluzione che va da incolore a rosa, in prossimità dell'elettrodo.
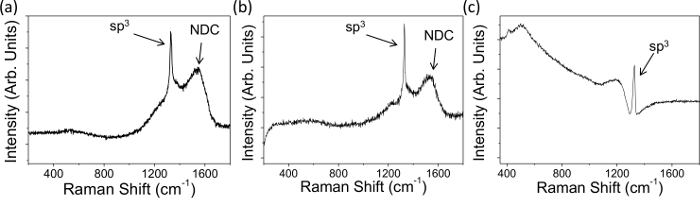
Figura 1. Dati tipici Raman registrati con un laser 514 nm su (A) NDC contenente sottile BDD pellicola microcristallino attaccato al substrato di crescita (dopdensità formica 1.9 × 10 20 atomi di boro cm -3) e (B, C) più grande di grano freestanding BDD, densità media drogante 1,9 × 10 20 e 3 × 10 20 B atomi cm -3, rispettivamente. NDC è evidente in (A) e (B) per la presenza dei picchi NDC etichettati tra 1.400 e 1.600 cm -1, (C) contiene trascurabili NDC. Tutti e tre gli elettrodi mostrano una "risonanza di Fano", e quindi sono opportunamente boro drogati per studi elettrochimici 7. Riprodotto in parte dal riferimento [4c] con il permesso. Cliccate qui per vedere una versione più grande di questa figura.
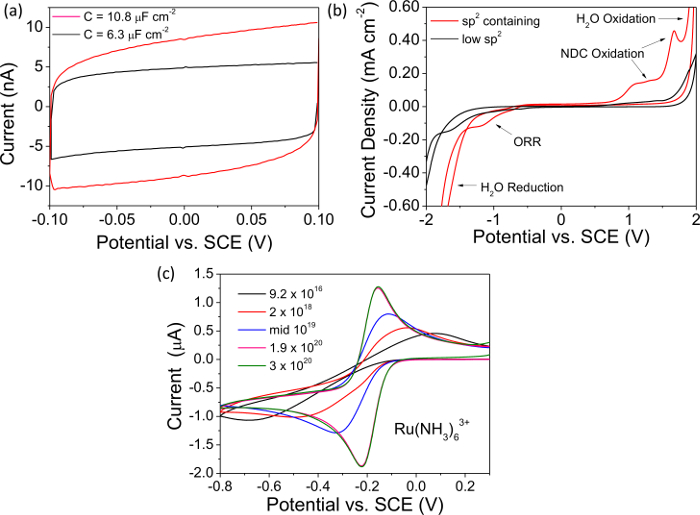
Figura 2. elettrochimica caratterizzazione. Tutti i dati rappresentativi a ( A, B) è stata registrata su isolante diamante incassato O-terminati elettrodi BDD drogati di sopra della soglia metallico cioè 10 20 B atomi cm -3 39. (A) le curve di capacità per NDC-gratis BDD dove C = 6,3 uF cm -2 (neri), e per la NDC contenenti BDD dove C = 10,8 cm uF -2 (rosso). (B) finestre solventi rappresentativi per NDC-gratis BDD, finestra solvente> 3,95 V (nero) e per NDC contenenti BDD, finestra solvente = 3.22 V (rosso). (C) CV registrate in 1 Ru mM (NH 3) 6 3+ a 0.1 V sec -1 per il vetro sigillato autoportante BDD elettrodi macrodisc di diversa densità boro droganti nell'intervallo 9.2 × 10 16 - 3 × 10 20 B atomi cm - 3. Riprodotto in parte dal riferimento [4c] con il permesso. Clicca qui per vedere una versione più grande di questa figura.

Figura 3. Caratterizzazione di IRO x deposizione di film su BDD e la risposta del pH. (A) CV in Iro soluzione x prima della deposizione. La corrente massima ossidazione fornisce un valore per il potenziale di deposizione, dep E, dove la formazione di pellicola è risultato essere più efficiente. Utilizzo dei potenziali> E par, si traduca in un film depositato instabile. (B) CV Caratteristica per un IRO x pellicola elettrolitica in 0.1 MH 2 SO 4 registrato a 0,1 V sec-1, i p, una è in genere ~ 0,7 mA cm -2. (C) Rappresentante pH CALIBRAZIOCurva n (R 2 = 0,997) per elettrodepositata IRO x su un elettrodo di BDD indipendente. La pendenza mostra una risposta super-Nernst (65,4 mV) a pH. Le piccole barre di errore (n = 3) indicano stabilità del film e riproducibilità nelle misure. Cliccate qui per vedere una versione più grande di questa figura.
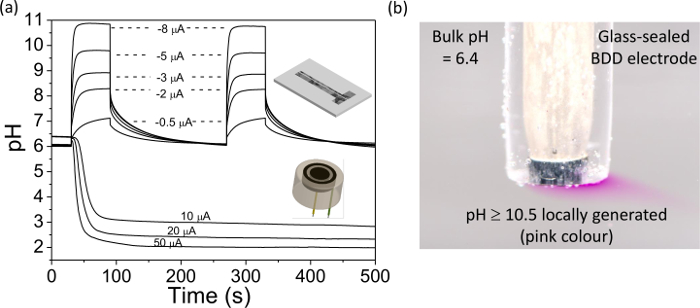
Figura 4. L'uso di un disco indipendente anello BDD ed elettrodi a doppia banda per in situ controllo del pH BDD elettrodo disco anello, diametro dei dischi = 0,922 millimetri, separazione = 0,262 millimetri e larghezza dell'anello = 0,150 millimetri.; BDD generatore elettrodo banda = 0.460 × 3 mm, sensore = 0,09 × 3 mm, e la separazione = 0.2 mm. (A) pH misurato sperimentalmente rispetto al profilo temporale nel corso degli elettrodi rivelatore come functisu di applicate galvanostatico correnti (+10 a +50 iA a all'elettrodo disco anello e -0.5 a -8 μA per l'elettrodo dual band). Notare il pH stabile generato per lunghi periodi di tempo. Riproduzione modificata di riferimenti [9a] e [9b]. (B) la visualizzazione semplice di generazione in situ pH utilizzando la soluzione fenolftaleina; una corrente di -4.55 (-0.58 mA μA cm -2) è stata applicata ad un vetro di diametro 1 mm sigillato BDD macroelectrode. Il colore rosa indica pH≥10.5, incolore indica pH≤8.4 38. Clicca qui per vedere una versione più grande di questa figura.
Discussione
Partendo da una superficie O-terminato è sostenuto perché la superficie H-terminato è elettrochimicamente instabile, soprattutto alle alte potenziali anodici 7,40,41. Cambiare terminazione superficie può influenzare la cinetica di trasferimento elettronico di coppie sfera interiore, come l'elettrolisi dell'acqua (qui utilizzato per modificare il pH della soluzione locale). Inoltre, se il BDD contiene significativa NDC al bordo dei grani è anche possibile che in seguito all'applicazione del estrema anodica / catodica potenziali sostenuto in questo articolo per generazione pH, incisione potrebbe verificarsi in questi punti deboli. Questo causerebbe il film di corrosione e per film sottili, alla fine delaminate, che si manifesta in un profilo instabile generazione pH, come si è visto con film sottile di Au e Pt elettrodi 17. Quindi un protocollo rigoroso per valutare la qualità dell'elettrodo prima dell'uso è adottato per valutare il contenuto NDC come discusso nelle figure 1 (Raman) e 2 (CapacitANCE e finestra solvente).
Altrettanto importante è il contenuto di boro. Se il materiale è drogato sotto della soglia metallico (<10 20 B atomi cm -3), sarà carica impoverito, a potenziali negativi del potenziale nastro piatto, con una conseguente diminuzione delle prestazioni elettrochimica 7,42. Il modo più semplice per valutare qualitativamente i livelli di drogaggio metallico è quello di cercare la presenza di una firma Fano che causa asimmetria nella sp 3 picco, negli spettri Raman, come mostrato nella Figura 1 (AC). Ciò è dovuto all'interferenza tra lo stato fononi discreto e il continuo elettronico ed è visto a livelli boro droganti> 10 20 cm -3 atomi B 43. Spettrometria di massa di ioni secondari (SIMS) quantifica in ultima analisi, il contenuto di boro ma è distruttivo e più intenso utilizzo. Nota come SIMS fornisce contenuto totale di boro non tiene conto di eventuali riduzioni del numero di liberamente dispone portatori di carica a causa di risarcimento o passivazione di boro accettori con donatori idonei, quali l'azoto rispettivamente 44 o idrogeno 45.
Elettrochimicamente, differenze di densità droganti possono essere visualizzati mediante impiego di una sfera esterna elettroni veloce coppia trasferimento redox cui potenziale giace all'interno della band-gap di formale O-terminati semiconduttore BDD, come Ru (NH 3) 6 3 + / 2 + 46. Ad esempio, come mostrato nella Figura 2C, come i livelli di drogaggio dell'aumento dell'elettrodo BDD, e il materiale si sposta da semi conduttore metallico per la corrente aumenta e il picco a picco separazione diminuisce trasferimento elettronico diventa più facile. A livelli droganti metalliche dell'elettrodo dovrebbe mostrare un comportamento simile a un elettrodo classica dove per un mediatore come Ru (NH 3) 6 3+, diffusione reversibile CV limitati sono iscritte ad un macroelectrode in solutio stazionarion. Nota, a livelli di boro droganti ~ 10 19 vicino al comportamento reversibile è stato registrato, ma solo per superfici H-terminati. Ciò è dovuto ad una interessante peculiarità di questa superficie dove H-terminati provoca i livelli di energia dei valenza e di conduzione bande in diamante da sollevare. Questo significa trasferimento di elettroni dalla banda di valenza alla H 3 O + è ora possibile, con conseguente trasferimento di superficie doping e una conduttività di superficie misurabile. Tuttavia, a causa dell'instabilità elettrochimica della superficie H-terminato, soprattutto in alti potenziali anodici, lavorando con elettrodi densità inferiore droganti H-terminati non è una soluzione valida a lungo termine 7,40,41.
La possibilità di modificare il pH locale dell'elettrodo di misura ha molte applicazioni diverse, ad esempio locali esperimenti di titolazione pH ora diventato possibile quando il pH può essere sistematicamente modificato e l'impatto sul sistema elettrochimicamente valutate in situ . Ioni metallici rilegati possono essere liberati diminuendo pH consentendo l'elettrodo sensore sia valutare il contenuto di metalli gratuito presso il pH naturale e il contenuto totale di metallo da localmente valori decrescenti a molto acide, in situ 47-50. Ciò è molto utile per le misurazioni di origine. Inoltre, specie possono essere commutati da non essere elettrochimicamente rilevabile rilevabile in virtù di cambiare il pH locale, ad es dissolto idrogeno solforato converte completamente alla forma solfuro elettrochimicamente rilevabile a pH> 9 16. Nell'esempio dato, per le geometrie di elettrodi impiegati , sono state dimostrate variazioni di pH superiori a 4 unità (da 6,4 a 2,0 e 6,0 a 10,8). Grandi cambiamenti sono possibili aumentando la corrente galvanostatico e cambiando le geometrie degli elettrodi. Ad esempio, riducendo la distanza tra il generatore e gli elettrodi del rivelatore e ridurre la dimensione relativa del rivelatore consentirà / valori pH superiori inferiori da raggiungere. L'impresadimensioni ure dell'elettrodo BDD sarà limitata dalla risoluzione della tecnica di fabbricazione utilizzata. Nota, c'è anche un limite superiore alla dimensione della corrente in grado di essere passato per la generazione pH stabile. Questo è dettato dalla corrente in cui viene osservato sviluppo di gas significativo e la formazione di bolle all'elettrodo generatore.
Divulgazioni
The authors declare that they have no competing financial interests.
Riconoscimenti
Vorremmo ringraziare il Dr. Jonathan Newland per la fotografia a figura 4B e per l'elaborazione di immagini al microscopio ottico per il video, la signorina Jennifer Webb per la consulenza e le immagini su misure di angolo di contatto, la signorina Sze-yin Tan per la finestra del solvente dati della figura 2B , il dottor Joseph Maxim per consigli sulla spettroscopia Raman, e anche i membri della Warwick Elettrochimica e interfacce Gruppo che hanno contribuito a sviluppare i protocolli descritti nel presente documento. Vorremmo anche ringraziare Max Joseph, Lingcong Meng, Zoe Ayres e Roy Meyler per la loro parte nella riprese del protocollo.
Materiali
| Name | Company | Catalog Number | Comments |
| Pt Wire | Counter Electrode | ||
| Saturated Calomel Electrode | IJ Cambria Scientific Ltd. | 2056 | Reference Electrode (alternatively use Ag|AgCl) |
| BDD Electrode | Working Electrode | ||
| Iridium Tetrachloride | VWR International Ltd | 12184.01 | |
| Hydrogen Peroxide | Sigma-Aldrich | H1009 | (30% w/w) Corrosive |
| Oxalic Acid | Sigma-Aldrich | 241172 | Harmful, Irritant |
| Anhydrous Potassium Chloride | Sigma-Aldrich | 451029 | |
| Sulphuric Acid | VWR International Ltd | 102765G | (98%) Corrosive |
| Potassium Nitrate | Sigma-Aldrich | 221295 | |
| Hexaamine Ruthenium Chloride | Strem Chemicals Inc. | 44-0620 | Irritant |
| Perchloric Acid | Sigma-Aldrich | 311421 | Oxidising, Corrosive |
| 2-Propanol | Sigma-Aldrich | 24137 | Flammable |
| Nitric Acid | Sigma-Aldrich | 695033 | Oxidising, Corrosive |
| Sputter/ Evapourator | With Ti & Au targets | ||
| Raman | 514.5 nm laser | ||
| Annealing Oven | Capable of 400 °C | ||
| Ag paste | Sigma-Aldrich | 735825 | or other conductive paint |
| Potentiostat | |||
| pH Buffer solutions | Sigma-Aldrich | 38740-38752 | Fixanal buffer concentrates |
| Phenolphthalein Indicator | VWR International Ltd | 210893Q | |
| Methyl Red Indicator | Sigma-Aldrich | 32654 |
Riferimenti
- Angus, J. C. Ch. 1, Synthetic Diamond Films: Preparation, Electrochemistry, Characterization and Applications. Electrochemistry on diamond: History and current status. Brillas, E., Huitle, C. A. M. , John Wiley & Sons, Inc. (2011).
- Fujishima, A. Diamond Electrochemistry. , BKC. (2005).
- Macpherson, J. V. A practical guide to using boron doped diamond in electrochemical research. Physical Chemistry Chemical Physics. 17 (5), 2935-2949 (2015).
- Balmer, R. S., et al. Chemical vapour deposition synthetic diamond: materials, technology and applications. Journal of Physics: Condensed Matter. 21 (36), 364221(2009).
- Swain, G. M., Ramesham, R. The electrochemical activity of boron-doped polycrystalline diamond thin film electrodes. Analytical Chemistry. 65 (4), 345-351 (1993).
- Luong, J. H. T., Male, K. B., Glennon, J. D. Boron-doped diamond electrode: synthesis, characterization, functionalization and analytical applications. Analyst. 134 (10), 1965-1979 (2009).
- Hutton, L. A., et al. Examination of the Factors Affecting the Electrochemical Performance of Oxygen-Terminated Polycrystalline Boron-Doped Diamond Electrodes. Analytical Chemistry. 85 (15), 7230-7240 (2013).
- Bennett, J. A., Wang, J., Show, Y., Swain, G. M. Effect of sp2-Bonded Nondiamond Carbon Impurity on the Response of Boron-Doped Polycrystalline Diamond Thin-Film Electrodes. Journal of The Electrochemical Society. 151 (9), E306-E313 (2004).
- Martin, H. B., Argoitia, A., Landau, U., Anderson, A. B., Angus, J. C. Hydrogen and Oxygen Evolution on Boron-Doped Diamond Electrodes. Journal of The Electrochemical Society. 143 (6), L133-L136 (1996).
- Panizza, M., Cerisola, G. Application of diamond electrodes to electrochemical processes. Electrochimica Acta. 51 (2), 191-199 (2005).
- Williams, O. A. Nanocrystalline diamond. Diamond and Related Materials. 20 (5-6), 5-6 (2011).
- Patel, A. N., Tan, S. -y, Miller, T. S., Macpherson, J. V., Unwin, P. R. Comparison and Reappraisal of Carbon Electrodes for the Voltammetric Detection of Dopamine. Analytical Chemistry. 85 (24), 11755-11764 (2013).
- Watanabe, T., Honda, Y., Kanda, K., Einaga, Y. Tailored design of boron-doped diamond electrodes for various electrochemical applications with boron-doping level and sp2-bonded carbon impurities. physica status solidi (a). 211 (12), 2709-2717 (2014).
- Poferl, D. J., Gardner, N. C., Angus, J. C. Growth of boron-doped diamond seed crystals by vapor deposition. Journal of Applied Physics. 44 (4), 1428-1434 (1973).
- Spitsyn, B. V., Bouilov, L. L., Derjaguin, B. V. Vapor growth of diamond on diamond and other surfaces. Journal of Crystal Growth. 52 (Pt 1), 219-226 (1981).
- Bitziou, E., et al. In Situ Optimization of pH for Parts-Per-Billion Electrochemical Detection of Dissolved Hydrogen Sulfide Using Boron Doped Diamond Flow Electrodes. Analytical Chemistry. 86 (21), 10834-10840 (2014).
- Read, T. L., Bitziou, E., Joseph, M. B., Macpherson, J. V. In Situ Control of Local pH Using a Boron Doped Diamond Ring Disk Electrode: Optimizing Heavy Metal (Mercury) Detection. Analytical Chemistry. 86 (1), 367-371 (2014).
- Manivannan, A., Tryk, D., Fujishima, A. Detection of Trace Lead at Boron-Doped Diamond Electrodes by Anodic Stripping Analysis. Electrochemical and solid-state letters. 2 (9), 455-456 (1999).
- Manivannan, A., Seehra, M. S., Tryk, D. A., Fujishima, A. Electrochemical detection of ionic mercury at boron-doped diamond electrodes. Analytical Letters. 35 (2), 355-368 (2002).
- Boukherroub, R., et al. Photochemical oxidation of hydrogenated boron-doped diamond surfaces. Electrochemistry Communications. 7 (9), 937-940 (2005).
- Yagi, I., Notsu, H., Kondo, T., Tryk, D. A., Fujishima, A. Electrochemical selectivity for redox systems at oxygen-terminated diamond electrodes. Journal of Electroanalytical Chemistry. 473 (1), 173-178 (1999).
- Duo, I., Levy-Clement, C., Fujishima, A., Comninellis, C. Electron Transfer Kinetics on Boron-Doped Diamond Part I: Influence of Anodic Treatment. Journal of Applied Electrochemistry. 34 (9), 935-943 (2004).
- Mahé, E., Devilliers, D., Comninellis, C. Electrochemical reactivity at graphitic micro-domains on polycrystalline boron doped diamond thin-films electrodes. Electrochimica Acta. 50 (11), 2263-2277 (2005).
- Vandenabeele, P. Practical Raman spectroscopy: an introduction. , John Wiley & Sons. (2013).
- Filik, J. Raman spectroscopy: a simple, non-destructive way to characterise diamond and diamond-like materials. Spectroscopy Europe. 17 (5), 10(2005).
- Tuinstra, F., Koenig, J. L. Raman Spectrum of Graphite. The Journal of Chemical Physics. 53 (3), 1126-1130 (1970).
- Tachibana, T., Williams, B., Glass, J. Correlation of the electrical properties of metal contacts on diamond films with the chemical nature of the metal-diamond interface. II. Titanium contacts: A carbide-forming metal. Physical Review B. 45 (20), 11975(1992).
- Zivcova, Z. V., et al. Electrochemistry and in situ Raman spectroelectrochemistry of low and high quality boron doped diamond layers in aqueous electrolyte solution. Electrochimica Acta. 87, 518-525 (2013).
- Granger, M. C., et al. Standard Electrochemical Behavior of High-Quality, Boron-Doped Polycrystalline Diamond Thin-Film Electrodes. Analytical Chemistry. 72 (16), 3793-3804 (2000).
- Bard, A. J., Faulkner, L. R. Electrochemical methods. Fundamentals and Applications. , 2nd ed, John Wiley and Sons. (2001).
- Simonov, A. N., et al. Inappropriate Use of the Quasi-Reversible Electrode Kinetic Model in Simulation-Experiment Comparisons of Voltammetric Processes That Approach the Reversible Limit. Analytical Chemistry. 86 (16), 8408-8417 (2014).
- Terashima, C., Rao, T. N., Sarada, B. V., Spataru, N., Fujishima, A. Electrodeposition of hydrous iridium oxide on conductive diamond electrodes for catalytic sensor applications. Journal of Electroanalytical Chemistry. 544, 65-74 (2003).
- Bitziou, E., O'Hare, D., Patel, B. A. Simultaneous Detection of pH Changes and Histamine Release from Oxyntic Glands in Isolated Stomach. Analytical Chemistry. 80 (22), 8733-8740 (2008).
- Pickup, P. G., Birss, V. I. The kinetics of charging and discharging of iridium oxide films in aqueous and non-aqueous media. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry. 240 (1-2), 185-199 (1988).
- Baur, J. E., Spaine, T. W. Electrochemical deposition of iridium (IV) oxide from alkaline solutions of iridium(III) oxide. Journal of Electroanalytical Chemistry. 443 (2), 208-216 (1998).
- Carmody, W. R. Easily prepared wide range buffer series. Journal of Chemical Education. 38 (11), 559(1961).
- Glab, S., Hulanicki, A., Edwall, G., Ingman, F. Metal-Metal Oxide and Metal Oxide Electrodes as pH Sensors. Critical Reviews in Analytical Chemistry. 21 (1), 29-47 (1989).
- Burgot, J. -L. Ionic equilibria in analytical chemistry. , Springer Science & Business Media. (2012).
- Joseph, M. B., et al. Fabrication Route for the Production of Coplanar Diamond Insulated, Boron Doped Diamond Macro- and Microelectrodes of any Geometry. Analytical Chemistry. 86 (11), 5238-5244 (2014).
- Vanhove, E., et al. Stability of H-terminated BDD electrodes: an insight into the influence of the surface preparation. physica status solidi (a). 204 (9), 2931-2939 (2007).
- Salazar-Banda, G. R., et al. On the changing electrochemical behaviour of boron-doped diamond surfaces with time after cathodic pre-treatments. Electrochimica Acta. 51 (22), 4612-4619 (2006).
- Gelderman, K., Lee, L., Donne, S. W. Flat-Band Potential of a Semiconductor: Using the Mott-Schottky Equation. Journal of Chemical Education. 84 (4), 685(2007).
- Ushizawa, K., et al. Boron concentration dependence of Raman spectra on {100} and {111} facets of B-doped CVD diamond. Diamond and Related Materials. 7 (11-12), 1719-1722 (1998).
- Chrenko, R. Boron, the dominant acceptor in semiconducting diamond. Physical Review B. 7 (10), 4560(1973).
- Uzan-Saguy, C., et al. Hydrogen diffusion in B-ion-implanted and B-doped homo-epitaxial diamond: passivation of defects vs passivation of B acceptors. Diamond and Related Materials. 10 (3-7), 453-458 (2001).
- Hammerich, O., Speiser, B. Organic Electrochemistry. , Fifth Edition, Taylor & Francis. (2015).
- Juang, R. -S., Wang, S. -W. Electrolytic recovery of binary metals and EDTA from strong complexed solutions. Water Research. 34 (12), 3179-3185 (2000).
- Byrne, R. H., Kump, L. R., Cantrell, K. J. The influence of temperature and pH on trace metal speciation in seawater. Marine Chemistry. 25 (2), 163-181 (1988).
- Schonberger, E., Pickering, W. The influence of pH and complex formation on the ASV peaks of Pb, Cu and Cd. Talanta. 27 (1), 11-18 (1980).
- Chau, Y., Lum-Shue-Chan, K. Determination of labile and strongly bound metals in lake water. Water Research. 8 (6), 383-388 (1974).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon