Method Article
Evaluación de dopado con boro Diamond Electrodo Calidad y Aplicación a
En este artículo
Resumen
Un protocolo se describe para la caracterización de los parámetros electroquímicos clave de un diamante dopado (BDD) electrodo de boro y solicitud ulterior de generación en los experimentos de pH situ.
Resumen
El boro de diamante dopado (BDD) electrodos han mostrado una promesa considerable como un material de electrodo, donde muchas de sus propiedades reportadas como ventana extendida disolvente, las corrientes de fondo bajo, resistencia a la corrosión, etc., surgen de la naturaleza catalíticamente inerte de la superficie. Sin embargo, si durante el proceso de crecimiento, sin diamantes-carbono (NDC) se incorpora en la matriz de electrodos, las propiedades electroquímicas cambiarán a medida que la superficie se vuelve más catalíticamente activo. Como tal, es importante que el electrochemist es consciente de la calidad y propiedades electroquímicas resultante clave del electrodo de BDD antes de su uso. En este trabajo se describe una serie de medidas de caracterización, incluyendo la microscopía Raman, capacitancia, ventana de disolvente y la electroquímica redox, para determinar si el electrodo BDD contiene insignificante NDC es decir insignificante sp 2 de carbono. Una aplicación se pone de relieve que se aprovecha de la catalíticamente inertey la naturaleza resistente a la corrosión de una superficie NDC-libre, es decir, protones locales estable y cuantificable y la producción de hidróxido debido a la electrólisis del agua en un electrodo de BDD. Un enfoque para medir el cambio local de pH inducido por la electrólisis del agua usando óxido de iridio electrodos recubiertos con TDC también se describe en detalle.
Introducción
Elección de material del electrodo es de gran importancia cuando se realiza cualquier estudio electroanalítica. En los últimos años, sp 3 de carbono (diamante) dopado con boro suficiente para hacer que el material "-metal como" se ha convertido en una opción popular para una amplia gama de aplicaciones electroanalíticas debido a su excelente electroquímica (y térmicas y mecánicas) 1,2 propiedades , 3. Estos incluyen resistencia a la corrosión bajo solución, temperatura y presión condiciones extremas 4 ventanas de disolvente ultra-anchas, corrientes de fondo bajos, y la reducción de ensuciamiento, en comparación con otros materiales de los electrodos usados comúnmente 5-7,3. Sin embargo, el aumento no diamantes carbono (NDC: sp 2) resultados de contenido en una ventana disolvente disminuyendo, aumentando las corrientes de fondo 7,8, cambios en la integridad estructural y la sensibilidad hacia las diferentes especies redox esfera interior, por ejemplo. oxígeno 9-12.
Nota para loMe aplicaciones, la presencia NDC es visto como una ventaja 13. Además, si el material no contiene suficiente de boro se comportará como una de tipo p semi-conductor y mostrar sensibilidad reducida a las especies redox en la ventana potencial reductor, donde el material es más agotado de portadores de carga 7. Por último, la química de la superficie de diamante dopado con boro (BDD) también puede desempeñar un papel en la respuesta electroquímica observada. Esto es especialmente cierto para las especies esfera interior que son sensibles a la química de superficie y bajar de diamante dopado donde un hidrógeno (H -) - superficie terminada puede hacer aparecer una BDD electrodo semiconductor "-metal como" 7.
Para tomar ventaja de las propiedades superiores de BDD, a menudo es esencial que el material se dopa suficientemente y contiene tan poco como sea posible NDC. Dependiendo del método adoptado para hacer crecer el TDC, las propiedades pueden variar 14,15. Este artículo primero sugiere un material y un elegidoguía de protocolo de caracterización rochemical para evaluar BDD idoneidad electrodo antes de su uso (es decir, el boro suficiente, mínimo NDC) y luego describe una aplicación basada en el cambio de pH localmente electroquímicamente utilizando el electrodo protocolo verificada. Este proceso se aprovecha de la resistencia superficial de NDC libre BDD hacia la corrosión o la disolución en virtud de la aplicación de los potenciales extremas aplicado (o corrientes) durante largos períodos de tiempo. En particular, el uso de un electrodo de BDD para generar protones estable (H +) o hidróxido (OH -) flujos debido a la electrólisis (oxidación o reducción, respectivamente) de agua en las proximidades de un segundo (sensor) 16,17 se describe en el presente documento.
De esta manera es posible controlar el entorno de pH del sensor de una manera sistemática, por ejemplo, para experimentos de titulación pH, o para fijar el pH en un valor donde el proceso electroquímico es más sensible. Este último es especialmente útil paraaplicaciones en las que el sensor se coloca en la fuente, por ejemplo, río, lago, el mar y el pH del sistema no es óptimo para la medición electroquímica de interés. Dos ejemplos recientes incluyen: (i) generación de un bajo pH localizado, en una solución de pH neutro, para la electrodeposición y extracción del mercurio 17; en cuenta BDD es un material preferido para la electrodeposición de metales debido a la ventana catódica extendida 9,18,19. (ii) La cuantificación de la forma electroquímicamente detectable de sulfuro de hidrógeno, presente a un pH alto, por aumentar localmente el pH de neutro a fuertemente alcalina 16.
Protocolo
NOTA: electrodos de BDD se cultivan más comúnmente usando técnicas de deposición química de vapor, que se adjunta a un sustrato de crecimiento. Salen de la cámara de crecimiento terminado-H (hidrofóbica). Si se cultiva lo suficientemente gruesa como la BDD se puede quitar desde el sustrato y se denomina independiente. La superficie de crecimiento BDD independiente es a menudo pulido para reducir significativamente la rugosidad superficial. Limpieza de la BDD en los resultados de ácido en un oxígeno (O) -terminated superficie.
1. Ácido Limpieza BDD
- Coloque un vaso de precipitados de ácido sulfúrico concentrado (H 2 SO 4; ~ 2 ml o lo suficientemente profundo para cubrir el diamante) en un plato caliente a temperatura ambiente y se insertan BDD.
- Añadir nitrato de potasio (KNO 3) hasta que se disuelva ya no (~ 0,5 g en 2 ml), a continuación, cubrir con un vidrio de reloj y se calienta hasta ~ 300 ° C, la solución se volverá de color marrón cuando se calienta y el nitrato de potasio se disolverá.
PRECAUCIÓN Se debe tener cuidado al manipular el ácido caliente!; guantes de goma, seguridad gmuchachas y bata de laboratorio se deben usar y este proceso debe llevarse a cabo en una campana de humos. - Deja que se caliente durante al menos 30 minutos o hasta que ya no hay ningún color marrón a la solución, a continuación, apague el plato caliente y dejar enfriar la solución a temperatura ambiente.
- Deseche con cuidado del ácido diluyendo en agua RT y enjuague la BDD con agua destilada.
- Mida el ángulo de contacto de la superficie, ver sección 1.2. Hidrofóbica (H-terminado) 20,21 electrodos han informado de ángulos de contacto en el intervalo de 60-90 ° 3, lo que reduce significativamente a medida que la superficie se vuelve hidrófilo a través de O-terminación.
- (método opcional alternativo) Para electrodos película muy delgada (adjunto al sustrato de crecimiento y para evitar la delaminación película usando el tratamiento anterior), se lava una vez con 2-propanol y dos veces con agua desionizada en un baño de ultrasonidos. A continuación, adoptar uno de los tres procedimientos de limpieza siguientes (1) anódicamente polarizar el diamante durante 30 minutos a 10 mA cm -2 En 1 M de ácido perclórico al 40 ° C 22; o (2) polarizar anódicamente el diamante durante 20 min a 10 mA cm -2 en ácido nítrico 1 M, a continuación, posteriormente polarizar catódicamente a 10 mA cm -2 durante otros 20 min en la misma solución o 23; (3) Ciclo de diamante entre 2 V en 0,1 MH 2 SO 4 hasta que una señal electroquímica estable se logra 7. Siga este con el paso 1.4.
Medida 2. Ángulo de contacto
- Coloque el diamante en la etapa de la muestra de un analizador de ángulo de contacto, asegurándose de que quede plana. Coloque una jeringa de 1 ml en el posicionador por encima de la etapa de la muestra, asegurar una aguja en el extremo. Llene la jeringa con agua desionizada.
- Utilice el controlador z para bajar la jeringa a la muestra, utilice el x - y y - controladores de la cámara y / iluminador para alinear la jeringa por encima del centro del diamante.
- Usando el software analizador de repetición de dispensación 1 l volumes de agua fuera de la jeringa hasta que se forme gotitas en la punta de la aguja, visibles en la imagen de la cámara (nunca más de 10 l). Baje la aguja para depositar la gota sobre la superficie y ajustar la iluminación para el máximo contraste.
- Reunir una imagen y aplicar caer software de análisis de la forma, utilizando el método de la sección cónica. Haga clic en "encontrar la línea de base" en el software y haga clic en "computación", seguido de "tangente".
NOTA: este procedimiento detecta la línea de base y se ajusta a una ecuación de la cónica (elíptica) gota forma; un ángulo de contacto, θ, se dibuja entre la línea de base y la tangente en el punto de contacto de tres fases.
3. BDD caracterización de Materiales
- Análisis Raman para sp 2 / sp 3 contenidos
- Realizar Raman (véase la referencia 14 para una guía de práctica Raman Spectroscopy) en varias áreas diferentes del electrodo de BDD, 24 uso de un 514,5 nm o532 nm láser, que hace hincapié en sp 2 de contenido, se defiende.
- Encienda el espectrómetro de micro-Raman y permitir ~ 30 min para el detector CCD se enfríe. Compruebe la lente adecuada, rejilla de difracción y los filtros están en su lugar para su uso con el láser de elección.
- Calibrar el sistema usando una de silicio (Si) muestra de calibración. Coloque el sustrato de Si en la cámara de instrumento y se centran ópticamente en la muestra con el microscopio. Cierra la puerta de la cámara. Cambiar a la vista con láser y comprobar el punto láser está bien definido y circular. Calibrar el uso del software, haga clic en "Herramientas", seguido de "calibración" "calibración rápida" y luego luego "ok".
- Retire el sustrato de Si de la cámara y vuelva a colocar con el electrodo de BDD. Ópticamente enfocar el microscopio en el área de interés, cambiar a la vista con láser y abrir el obturador para comprobar que el láser se enfoca. Cierre el obturador.
- Realice una medición Raman mediante el software; click "medición" y luego "Nuevo" y luego "adquisición espectral." establecer el rango de número de onda de medición para cubrir las características de interés, para BDD esto es 200 - 1800 cm -1; establecer el tiempo de adquisición de exploración (<10 segundos); ajustar la potencia del láser a 100% (para BDD) y; establecer el número de acumulaciones (repetición de exploraciones) a cinco (para BDD). Si el espectro resultante es muy ruidoso más acumulaciones pueden ser necesarios. Presione carrera y guardar el espectro resultante para el análisis. Tome una fotografía de la zona Raman se realizó en el uso del vídeo en directo. Guarda la imagen como referencia.
- Tenga en cuenta las máximas ~ 1.332 cm -1 en el espectro que indica sp 3 diamantes (Figura 1); el más amplio sea el pico de los más defectos presentes 3,25.
- Observe cualquier NDC - indicado por un pico ancho G centrada a 1.575 cm-1 26, en los espectros (Figura 1A y 1B), procedente de la estiramiento de sp emparejado 2 sitios; cuanto mayor es la intensidad del pico más NDC presentes.
NOTA: los bonos pi formados por sp 2 C son más polarizable que sp 3 σ bonos y están resonantemente reforzada por los láseres visibles, dando lugar a más amplia, más dominante, los picos G 25. Tenga en cuenta que el método exacto utilizado para realizar análisis puede variar entre diferentes instrumentos y software.
4. Caracterización electroquímica
- Preparación de contactos óhmicos
- Independiente BDD
- Usando técnicas estándar por bombardeo iónico (o evaporarse) la parte trasera del BDD con titanio (Ti) / oro (Au) 10 nm / 300 nm, utilizando un tartamudo / evaporador a presiones por debajo de 1 × 10 -5 mbar. Si una fuente de tres de destino está disponible, más idealmente es Ti 10 nm / platino (Pt) 10 nm / 300 nm Au para evitar la difusión de Ti en el Au.
- Recocido de 5 horas a 400 ° C (presión atmosférica) que permite el Ti para formar carburo de titanio, CRUCIAL para la formación de un contacto óhmico 27.
Nota: Si la superficie posterior de la BDD es muy pulido (~ nm rugosidad), entonces es preferentemente para hacer rugosa la superficie antes de la deposición por pulverización catódica para asegurar un recubrimiento más robusto. Esto se puede lograr mediante, por ejemplo, láser de baja potencia micromecanizado de la superficie (la eliminación de <30 micras de material).
- Diamantes de película delgada crecido sobre un sustrato conductor
- Pulverización catódica / evaporar el anterior, pero con la cara superior, usando una máscara de sombra colocar suavemente sobre la superficie superior para evitar contacto con la parte superior de todo el electrodo.
O - Raspe la parte posterior del substrato conductor usando una pluma con punta de diamante. Luego cubra el área rayada con la realización de pasta de Ag o una pintura conductora similares pintando en una capa delgada con un pequeño pincel. Finalmente, conectar eléctricamente conectando cables de cobre con epoxi conductor.
Nota: Hay una variedad de maneras de preparar la BDD después electorical contacto como se describe en la referencia 4, por ejemplo, si la BDD se puede mecanizar en estructuras más pequeñas, el precinto en vidrio o epoxi, o si todavía unido a la abrazadera de oblea / adjuntar una célula electroquímica a la superficie superior.
- Pulverización catódica / evaporar el anterior, pero con la cara superior, usando una máscara de sombra colocar suavemente sobre la superficie superior para evitar contacto con la parte superior de todo el electrodo.
- Independiente BDD
- Las mediciones de capacitancia
- Preparar a 20 ml de 0,1 M KNO solución 3 pesando 0,20 g en agua doblemente destilada (esto la calidad del agua se recomienda en todo, la resistividad 18,2 M cm). Limpie el electrodo antes de su uso, ya sea por el pulido de alúmina o electroquímicamente ciclismo en ácido diluido (véase la sección 1 NOTA) 16,23,28.
- El uso de un potenciostato ejecutar voltamogramas cíclicos (CV) a 0,1 V sec -1 entre -0,1 V y 0,1 V, a partir de 0 V, con el BDD como el electrodo de trabajo frente a un electrodo de referencia común, por ejemplo, plata / cloruro de plata (Ag / AgCl ) o un electrodo de calomelanos saturado (SCE), y un contador de electrodo de Pt. Analizar el segundo CV.
NOTA: La figura 2A Muestra una curva de capacitancia típica grabado con una estructura metálica autoportante dopado electrodos de BDD. - Medir la magnitud total de corriente a 0 V de la curva de capacitancia registrado y dividir por 2, este valor es "i". Determine la capacitancia, C, utilizando el valor de i, con la ecuación 1, normalizar con respecto al electrodo de área (que representa la rugosidad superficial en su caso) y la cotización en mF cm -2. De alta calidad, "-metal como" BDD tiene una capacitancia << 10 mF cm -2. Utilice los datos de trazado de software para presentar y analizar los datos.
i = C (Vt -1) (Ec. 1);
donde i es la corriente (A) y (V t -1) es la velocidad de barrido potencial.
- Solvente Ventana
- Limpie el electrodo como en el paso 4.2.1. El uso de un potenciostato ejecutar un CV en 0,1 M KNO 3 a 0,1 V sec -1 de 0 V a -2 V después entre -2 y 2 V V unand de nuevo a 0 V con el BDD como el electrodo de trabajo frente a un electrodo de referencia común y Pt contraelectrodo. Repetir. Analizar el segundo CV, un ejemplo CV se muestra en la Figura 2B.
- Convertir la corriente a la densidad de corriente (mA cm -2), teniendo en cuenta la rugosidad superficial, y citan la ventana solvente como la ventana de potencial definido por los límites actuales de ± 0,4 mA cm -2 en ambas direcciones. 7,29 Utilice los datos de trazado de software presentar y analizar los datos.
- Observe la evidencia de NDC (sp 2 de carbono) en la ventana de disolvente; la reacción de reducción de oxígeno se ve favorecida en NDC que es claramente evidente en la ventana reductora. La oxidación de la SP 2 grupos que contienen también resulta en picos característicos justo antes de la electrólisis del agua en la ventana anódica (Figura 2B).
NOTA: alta calidad "metálicos" electrodos TDC tienen ventanas solventes >> 3 V, no son compatibles con la reac reducción de oxígenoción (ORR) en 0,1 M KNO3 (o la ORR es fuertemente cinéticamente retraso) y mostrar las firmas de oxidación NDC insignificantes.
- Redox Electroquímica
- Limpie el electrodo como en el paso 4.2.1.
- El uso de un CV récord potenciostato en 1 mM de rutenio (Ru hexaamina (NH 3) 6 3+) y 0,1 M KNO3 entre 0,2 V y -0,8 V frente a SCE, para velocidades de barrido en el rango de 0,05 V s-1 - 0,2 V seg -1.
NOTA: Esta pareja demuestra la transferencia de electrones rápido y es electroactivo en una región que desafía tipo p semiconductor BDD. sp 2 que contiene BDD también mostrará la ORR en esta región, la señal para el último es más evidente a medida que la concentración de Ru (NH 3) 6 3+ disminuye. - Medir la separación entre la tensión anódica y catódica de corriente de pico (Δ E p) de la CV grabado, y la temperatura como se ha descrito 20.Para "metal-como" óhmicamente contactarse BDD terminado en oxígeno a 298 K, Δ E p <70 mV 30,31. Más grandes valores de p Δ E son sintomáticos de un pobre contacto óhmico o un contenido de boro inferior, como se muestra en la Figura 2C para electrodos de BDD de densidades de dopado en el rango de 9,2 × 10 16 × 10 3 20 B átomos cm -3.
- Mida la corriente de pico de la exploración hacia adelante, i p, y se correlacionan con la que se espera a partir de la ecuación Randles Sevcik 2 (citado a 298 K) 3,30, suponiendo que el electrodo está en la geometría y lo suficientemente grande en forma de disco (diámetro 1 mm) que la difusión lineal domina. Utilice los datos de trazado de software para presentar y analizar los datos.
i p = 2,69 × 10 5 n 3/2 AD 1/2 cv media (eq 2)
donde nes el número de electrones transferidos, A es el área (cm 2), D es el coeficiente de difusión (cm 2 seg -1), c es la concentración (mol cm -3) y V es velocidad de barrido (V seg -1).
5. pH Generación: Preparación del Electrodo de pH sensible y pH Generación
- Iridium óxido (sensible al pH) Preparación de la solución
- Preparar una solución de KNO3 20 ml 0,1 M como en la sección 5.4.1. Añadir 5 gotas de solución indicadora de fenolftaleína con una pipeta Pasteur y revolver (esto es suficiente para ver una respuesta a ojo, pero para un color más intenso, añadir más gotas). Coloque el electrodo de trabajo BDD y Pt contador de electrodo en la solución.
- Ajustar el pH de la solución a 10,5 por adición de sal de cloruro de potasio anhidro, se agita continuamente. Deja cubierta y agitar durante 48 h a RT a estabilizarse, en esta etapa la solución pasará gradualmente de color amarillo-verde paraazul púrpura. Almacenar en un refrigerador a 3 ° C.
- pH sensible Iridium Óxido de Cine de deposición
- El uso de un potenciostato ejecutar un CV en la solución de óxido de iridio entre 0 V y 1 V frente a SCE para determinar el potencial en el que se graba la corriente máxima. Este es el potencial de deposición, E dep como se muestra en la Figura 3A, por lo general se extiende entre ~ + 0,6 V - 0,85 V; puede variar dependiendo de un número de factores tales como la temperatura, etc. material de electrodo 32, 33
- Usando cronoamperometría con un potenciostato, paso el potencial de 0 V ("E inicial" y "Low E" en el software), donde no la electrólisis se produce a E dep ("High E" en el software), por un período de tiempo de 0,2 segundos por paso, repetir 100x.
- Ejecutar un CV entre 0 V y 1 V en 0,1 MH 2 SO 4 para la IRO x depositado electrodo. El carácterISTIC CV forma se muestra en la Figura 3B. Una densidad de corriente en el rango de ~ 0,6 mA cm -2 - 0,7 mA cm -2 para el primer pico anódico (correspondiente a un espesor de película promedio de ~ 8 nm para 0,7 mA cm -2), indica una película sensible al pH estable 34, 35.
- Si la densidad de corriente es menor que 0,6 mA cm -2 repita los pasos 5.2.2 - 5.2.4 hasta que se alcance este valor. Deje el electrodo en la solución tampón de pH 7 durante 24 horas para hidratar como la respuesta de la película IrO x es la hidratación dependiente 33.
- IrO x Film pH Caracterización
- Prepare una serie de soluciones tampón que cubren el intervalo de pH de interés (pH 2 - pH 12), estos pueden ser hechas en casa (por ejemplo Carmody 36) o comercialmente adquirida.
- Enjuagar el electrodo con agua destilada. Coloque la IRO x electrodo y electrodo de referencia en la solución tampón de pH bajo. El uso de un potenciostatoregistrar el potencial de circuito abierto (OCP) durante 30 s, con tres repeticiones. Retire el electrodo de la solución, enjuague y el lugar en el próximo buffer.
- Repita el paso 5.3.2 para cada buffer, luego repita la serie de al menos dos veces. Terreno pH vs. OCP, la curva de calibración para la respuesta de la película. Una película IrO x exhibe una pendiente con un gradiente entre 59 - 80 mV por década 37.
NOTA: La figura 3C muestra un gráfico ejemplo de calibración para un sensor de pH IrO x éxito en BDD.
- El uso de un generador de pH y sistema de medición
NOTA: esto supone el uso de un sistema de electrodos de doble donde un electrodo está recubierto con la película IrO x (por ejemplo, disco) y el segundo (por ejemplo, anillo de BDD) generará H + o OH - galvanostáticamente a partir de la electrólisis del agua.- Preparar una solución de KNO 3 20 ml 0,1 M mediante la adición de agua desionizada a la sal. Conecte la IRO x recubiertoelectrodo como el electrodo de trabajo en un sistema de dos electrodos, con el segundo electrodo de un electrodo de referencia estable por ejemplo, SCE. Medir la OCP usando un potenciostato, para establecer el pH de partida.
- Conecte el electrodo generador a un sistema adecuado galvanostático dos electrodos con un electrodo opuesto, por ejemplo, papel de Pt, y repita el paso 5.4.1, pero después de un período de tiempo definido aplicar una corriente al electrodo generador.
NOTA: encontramos corrientes en el rango de 0 a ± 50 mu son adecuadas con nuestros electrodos TDC; corrientes más grandes dan lugar a la evolución de gas apreciable. La magnitud y dirección de la corriente depende del resultado deseado; una corriente positiva dará como resultado un cambio a pH más ácido y una corriente negativa a pH más alcalino, cuanto mayor sea la corriente mayor será el cambio de pH. - Utilizando el potenciostato, registrar el cambio de OCP en respuesta a la corriente galvanostático, espere hasta que la respuesta se estabilice. A continuación, coloque la IRO x electrodo en tampón pH 7 durante 10 min para volver a equilibrar la película IrO x.
- Repita los pasos 5.4.2 al 5.4.3 con diferentes corrientes aplicadas, hasta que se han recogido todos los datos requeridos. Sinopsis de los datos utilizando la curva de calibración obtenida en el apartado 5.3 para convertir OCP al pH, un conjunto de datos ejemplo se muestra en la Figura 4A. Quite la película IrO x usando el pulido alúmina o pulsante en 0,1 MH 2 SO 4 de 2 V a -2 V de 0,2 seg, × 100. Aplicar sobre el sistema de medición de interés.
- Evaluación visual de la generación de pH local
- Preparar una solución de KNO3 20 ml 0,1 M como en la sección 5.4.1. Añadir 5 gotas de solución indicadora de fenolftaleína con una pipeta Pasteur y revolver (esto es suficiente para ver una respuesta a ojo, pero para un color más intenso, añadir más gotas). Coloque el electrodo de trabajo BDD y Pt contador de electrodo en la solución.
- Aplicar una corriente negativa al electrodo de trabajo utilizandoun galvanostato como en el paso 5.4.2 (por ejemplo ~ -0,6 mA cm -2) tal que la solución cambia de color desde incoloro a rosa. Esto ahora localmente genera una solución que es a pH ≥ 10,5.
- Repita el paso 5.5.1 con 5 gotas de solución de rojo de metilo en lugar de fenolftaleína y revuelva. Aplicar una corriente (por ejemplo, ~ 6,6 mA cm -2) suficientemente positivo tal que la solución cambia de color de amarillo a rojo. Esto ahora localmente genera una solución que es a pH 4,2 ≤ 38.
Resultados
Espectros y electroquímicos características Raman fueron obtenidos para representativas electrodos macrodisc BDD con diferentes densidades de dopado, y ambos niveles significativos y insignificantes de NDC, las Figuras 1 y 2. Las Figuras 1A y B muestran datos típicos Raman para NDC que contiene microcristalina película delgada BDD y grano más grande BDD independiente, dopado por encima del umbral metálico, respectivamente. La presencia de NDC es identificable por los picos anchos marcados entre 1400 y 1600 cm -1; no hay tal pico visible en la figura 1C, que muestra la típica firma de Raman-NDC libre, independiente BDD. En los tres espectros en la Figura 1 es posible observar un pico agudo a 1.332 cm -1, este es el pico de la firma del sp 3 de carbono (diamante); asimetría de la línea de base alrededor de este pico se conoce como una "resonancia Fano"Y si está presente indica que la muestra se dopa adecuadamente (10 B 20 átomos cm -3) para su uso en estudios electroquímicos. Este es el caso para los tres electrodos que se muestran aquí.
En la Figura 2 los datos de ejemplo para estudios electroquímicos (capacitancia, ventana de disolvente y los CV grabados en el mediador redox Ru (NH3) 6 3+) se presentan tanto para NDC-contener y NDC-libre de BDD, dopada por encima del umbral metálico. Las curvas de capacitancia en la figura 2A indican claramente que NDC contiene BDD exhibe una corriente capacitiva mayor que NDC libre BDD. Las capacidades de cada uno se ha calculado como se describe en el texto y se cotizan en la figura 2A como 10.8 mF cm -2 (NDC contienen) y 6,3 mF cm -2 (NDC gratis) TDC. Alta calidad, bajo NDC-contenido, se espera que los electrodos de BDD tener una capacitancia << 10 mF cm -2. Del mismo modo, la Figura 2B comparan las ventanas solventes de exemplar NDC contiene y NDC-gratis electrodos TDC. Se puede observar que para un electrodo NDC-que contiene el inicio de H 2 O oxidación y reducción que se ha traído en forma significativa, la reducción de la ventana de disolvente. También hay que resaltar la aparición de picos anódicos debido a la oxidación del NDC y un pico catódico, debido a la ORR que es catalizada en NDC pero no en sp 3 de carbono. Para un electrodo de alta calidad con BDD insignificante NDC se espera que la ventana de disolvente sea >> 3 V en una solución acuosa de KNO 3. En la figura 2C la respuesta CV de electrodos con TDC con una variedad de niveles de dopaje se investigó utilizando el mediador redox Ru (NH 3) 6 3+. Para electrodos con TDC dopados por encima del umbral metálico, se espera que la separación entre la tensión anódica y picos de corriente catódica para estar cerca de 59 mV, de acuerdo con la ecuación de Nernst; However, como el nivel de dopado disminuye el material se agota de portadores de carga que resulta en un aumento en el pico a pico de separación.
A macrodisc BDD, recubierto en IrO x, se utilizó para grabar los datos en la Figura 3, mientras que todos los diamantes (BDD aislado en el diamante) 39 electrodos duales y un epoxi sellado BDD electrodo de disco anillo se utilizaron para los experimentos de generación de pH en la figura 4A. Los datos en la Figura 3 ilustra el proceso de deposición y caracterización para un pH IrO sensible x película sobre BDD. En la figura 3A se muestra un CV típica registrada en la solución x deposición de la IRO. El potencial empleado para la posterior deposición IrO x puede ser identificado a partir de la posición del pico de corriente oxidativo, como se ilustra aquí. Figura 3B es una CV ejemplar en ácido sulfúrico de una IRO x electrodepósito de películaed en BDD. La forma de la CV es característico de una película depositada con éxito con la densidad de corriente pico de proporcionar información sobre espesor de la película. Una densidad de corriente más alta indica una película más gruesa. La estabilidad de la película es el espesor dependiente; demasiado delgada y la respuesta pH irá a la deriva, demasiado grueso y el tiempo de respuesta de la película será lenta y la película puede desprenderse. Se ha demostrado un valor para la densidad de corriente de pico ~ 0,7 mA cm -2 para indicar una película estable con una respuesta pH excelente. La respuesta OCP de la capa de IrO x sobre un electrodo de BDD hacia diferentes tampones de pH se muestra en la Figura 3C. La deriva entre las mediciones es pequeño como se evidencia por el tamaño de las barras de error y la pendiente es super-Nernst (> 59 mV) como se esperaba para este tipo de película.
Finalmente, la Figura 4 ilustra el uso de un electrodo de pH para la generación de BDD. En la Figura 4A, el pH me cambieelectrodo de BDD asured en una IRO x recubierta se presenta para una gama de corrientes aplicadas a la generación pH BDD electrodo colocado cerca, ya sea en formato de banda de anillo o, como se ilustra en la Figura 4. Para diferentes corrientes aplicadas, el pH se puede cambiar localmente y cuantificable, a partir de un valor inicial (casi neutro) para ya sea ácido o alcalino. Este proceso se puede observar visualmente como se ilustra en la figura 4B, donde se aplica una densidad de corriente adecuada a un electrodo de BDD para cambiar el pH de cerca de neutro a> 10.5. En presencia de fenolftaleína (indicador de pH) esto se traduce en la solución que va desde incoloro a rosa, en las proximidades del electrodo.
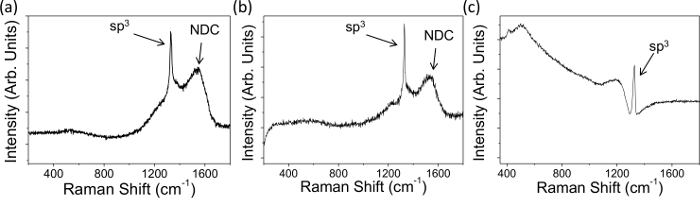
Figura 1. Los datos de Raman típicos grabados con un láser de 514 nm en (A) que contiene NDC delgada BDD microcristalina película unida al sustrato de crecimiento (dopdensidad hormiga 1,9 × 10 20 átomos de boro cm -3) y (B, C) de grano más grande autoportante BDD, la densidad media de dopante 1,9 × 10 20 × 10 y 3 20 B átomos cm -3, respectivamente. NDC es evidente en (A) y (B) debido a la presencia de los picos etiquetados NDC entre 1.400 y 1.600 cm -1, (C) contiene insignificante NDC. Los tres electrodos muestran una "resonancia Fano" y por lo tanto están adecuadamente boro dopados para estudios electroquímicos 7. Reproducido en parte de la referencia [4c] con permiso. Haga clic aquí para ver una versión más grande de esta figura.
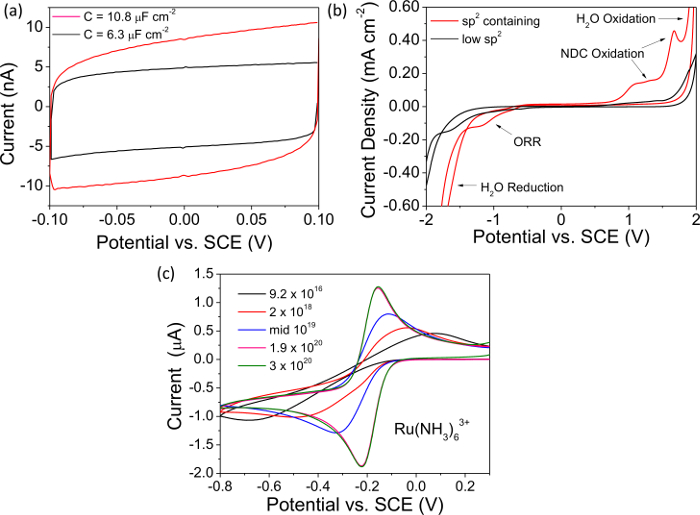
Figura 2. electroquímico caracterización. Todos los datos representativos en ( A, B) se grabó en aislante diamante encajonado O terminados en electrodos de BDD dopados por encima del umbral metálico es decir, 10 de 20 B átomos cm -3 39. (A) las curvas de capacitancia para NDC libre BDD donde C = 6.3 mF cm -2 (negro), y para NDC contiene BDD donde C = 10.8 mF cm -2 (rojo). (B) ventanas solventes representativos para NDC libre BDD, ventana de disolvente> 3,95 V (negro) y para NDC contiene BDD, ventana de disolvente = 3,22 V (rojo). (C) CV registran en 1 mM Ru (NH 3) 6 3+ a 0,1 V seg -1 para el vidrio sellada autoportante BDD electrodos macrodisc de diferentes densidades de dopado de boro en el intervalo de 9,2 × 10 16 - 3 × 10 cm 20 átomos de B - 3. Reproducido en parte de la referencia [4c] con permiso. Haga clic aquí para ver una versión más grande de esta figura.

Figura 3. Caracterización de IrO deposición x película sobre BDD y la respuesta de pH. (A) Currículum en IrO x solución antes de la deposición. La corriente máxima de oxidación proporciona un valor para el potencial de deposición, E dep, donde la formación de la película se encuentra para ser más eficiente. Uso de los potenciales> E dep, da como resultado una película depositada inestable. (B) CV Característica de una IRO x película electrodepositada en 0,1 MH 2 SO 4 registrados a 0,1 V s-1; i p, a es típicamente ~ 0,7 mA cm -2. (C) Calibració pH Representanten curva (R 2 = 0,997) para electrodepositada IrO x en una independiente BDD electrodo. La pendiente muestra una respuesta súper Nernstiana (65,4 mV) a pH. Las pequeñas barras de error (n = 3) indican estabilidad de la película y la reproducibilidad en las mediciones. Haga clic aquí para ver una versión más grande de esta figura.
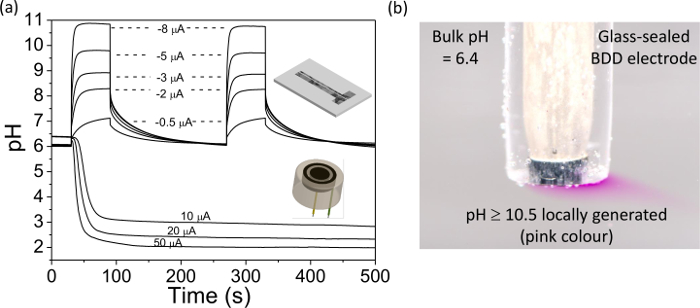
Figura 4. El uso de un disco independiente anillo de BDD y los electrodos de banda dual para el control de pH situ BDD electrodo de disco anular, diámetro del disco = 0.922 mm, separación = 0.262 mm, y la anchura del anillo = 0.150 mm.; BDD generador de electrodo de banda = 0,460 × 3 mm, detector = 0,09 × 3 mm, y la separación = 0,2 mm. (A) pH medido experimentalmente con respecto al tiempo en los electrodos detectores como functiel de aplicados galvanostáticas actuales (10 a 50 mu en el electrodo de disco y anillo de -0,5 a -8 mu para el electrodo de doble banda). Tenga en cuenta el pH estable generada durante largos períodos de tiempo. Reproducción de modificación de las referencias [9a] y [9b]. (B) la visualización simple de pH en la generación in situ utilizando solución indicadora de fenolftaleína; una corriente de -4.55 -0.58 mu (mA cm -2) se aplicó a un vaso de diámetro 1 mm sellados BDD macroelectrode. El color rosa indica pH≥10.5, solución incolora indica pH≤8.4 38. Haga clic aquí para ver una versión más grande de esta figura.
Discusión
Comenzando con una superficie de O-terminados se abogó porque la superficie H-terminado es electroquímicamente inestable, especialmente a altas potenciales anódicos 7,40,41. Cambio de la terminación de la superficie puede afectar a la cinética de transferencia de electrones de las parejas esfera interior, tales como la electrólisis del agua (usa en este documento para cambiar el pH de la solución local). Además, si el BDD contiene significativa NDC en los límites de grano es también posible que tras la aplicación de la extrema anódica / catódica potenciales preconizadas en la presente artículo para la generación de pH, grabado podría ocurrir en estos puntos débiles. Esto haría que la película se corroa y películas delgadas, con el tiempo delaminate, manifestándose en un perfil inestable generación de pH, como se ha visto con la película delgada de Au y Pt electrodos 17. Por lo tanto se adoptó un protocolo riguroso para evaluar la calidad del electrodo antes de su uso para evaluar el contenido de NDC como se discute en las Figuras 1 (Raman) y 2 (capacitANCE y la ventana de disolvente).
También de importancia es el contenido de boro. Si el material se dopa por debajo del umbral metálico (<10 20 B átomos cm -3), que será responsable empobrecido, a potenciales negativos del potencial planos a, resultando en una disminución en el rendimiento electroquímico 7,42. La forma más fácil para evaluar cualitativamente los niveles de dopaje metálico es buscar la presencia de una firma Fano que provoca asimetría en el pico sp 3, en los espectros Raman, tal como se muestra en la Figura 1 (AC). Esto es debido a la interferencia entre el estado de fonones discreto y el continuo electrónico y se observa a niveles de dopaje de boro> 10 20 B 43 átomos cm -3. Espectrometría de masas de iones secundarios (SIMS) en última instancia, cuantifica el contenido de boro, pero es destructivo y más intensivo de usar. Nota como SIMS proporciona contenido total de boro que no tiene en cuenta las posibles reducciones en el número de libremente availablcorreos portadores de carga debido a la compensación o pasivación del boro aceptadores con los donantes adecuados, como el nitrógeno o el hidrógeno 44 45 respectivamente.
Electroquímicamente, las diferencias de densidad de dopado pueden ser visualizados por el empleo de una esfera exterior de electrones rápida transferencia redox pareja cuyo formal de potenciales se encuentra dentro del intervalo de banda de O-terminados semiconductor BDD, como Ru (NH 3) 6 3 + / 2 + 46. Por ejemplo, como se muestra en la Figura 2C, como los niveles de dopaje del aumento electrodo BDD, y el material se mueve a partir de semi-conductor metálico a la corriente aumenta y el pico a pico de separación disminuye a medida que la transferencia de electrones se vuelve más fácil. A niveles dopantes metálicos del electrodo debe mostrar un comportamiento similar a un electrodo clásica donde por un mediador como Ru (NH 3) 6 3+, difusión reversible CV limitados se registran en una macroelectrode en solutio estacionarianorte. Tenga en cuenta, en los niveles de boro dopante ~ 10 19 cerca de comportamiento reversible ha sido registrado, pero sólo para las superficies terminadas-H. Esto es debido a una interesante peculiaridad de esta superficie donde terminan-H hace que los niveles de energía de las bandas de valencia y de conducción en diamante para ser planteadas. Esto significa la transferencia de electrones desde la banda de valencia a H 3 O + es ahora posible, lo que resulta en el dopaje de transferencia de superficie y una conductividad superficial medible. Sin embargo, debido a la inestabilidad electroquímica de la superficie H-terminado, especialmente a altos potenciales anódicos, trabajando con electrodos de menor densidad de dopado terminados-H no es un enfoque viable a largo plazo 7,40,41.
La capacidad de modificar el pH local del electrodo de medición tiene muchas aplicaciones diferentes, por ejemplo locales experimentos de titulación pH ahora convertido en posible cuando el pH puede ser modificado de manera sistemática y el impacto en el sistema electroquímico evaluó in situ . Iones metálicos enlazados pueden ser liberados por la disminución de pH que permite el electrodo sensor para evaluar tanto el contenido de metales gratis en el pH natural y el contenido total de metal al disminuir localmente valores muy ácidos, in situ 47-50. Esto es muy útil para las mediciones de origen. Además, las especies se pueden conmutar de no ser electroquímicamente detectable a detectable en virtud de cambiar el pH local, por ejemplo, sulfuro de hidrógeno disuelto convierte completamente a la forma de sulfuro electroquímicamente detectable a valores de pH> 9 16. En el ejemplo dado, por las geometrías de electrodos empleados , se demostraron cambios de pH más de 4 unidades (de 6,4 a 2,0 y 6,0 a 10,8). Cambios más grandes son posibles mediante el aumento de la corriente galvanostático y el cambio de las geometrías de electrodos. Por ejemplo, la disminución de la separación entre el generador y los electrodos detectores, y reducir el tamaño relativo del detector permitirá a valores de pH menor / mayor que deben alcanzarse. La hazañaure tamaño del electrodo BDD estará limitada por la resolución de la técnica de fabricación empleada. Nota, hay también un límite superior para el tamaño de la corriente capaz de ser pasado para la generación de pH estable. Esto es dictada por la corriente a la que se observa la evolución de gas significativa y formación de burbujas en el electrodo de generación.
Divulgaciones
The authors declare that they have no competing financial interests.
Agradecimientos
Nos gustaría agradecer al Dr. Jonathan Newland para la fotografía en la figura 4B y para el procesamiento de imágenes de microscopio óptico para el vídeo, la señorita Jennifer Webb para el asesoramiento y visuales en las mediciones del ángulo de contacto, Srta Sze-yin Tan para la ventana disolvente datos de la Figura 2B , el Dr. Joseph Maxim para el asesoramiento en la espectroscopia Raman, y también miembros de la Warwick Electroquímica y Interfaces de grupo que han ayudado a desarrollar los protocolos descritos en el presente documento. También nos gustaría dar las gracias a José máximo, Lingcong Meng, Zoe Ayres y Roy Meyler por su participación en el rodaje del protocolo.
Materiales
| Name | Company | Catalog Number | Comments |
| Pt Wire | Counter Electrode | ||
| Saturated Calomel Electrode | IJ Cambria Scientific Ltd. | 2056 | Reference Electrode (alternatively use Ag|AgCl) |
| BDD Electrode | Working Electrode | ||
| Iridium Tetrachloride | VWR International Ltd | 12184.01 | |
| Hydrogen Peroxide | Sigma-Aldrich | H1009 | (30% w/w) Corrosive |
| Oxalic Acid | Sigma-Aldrich | 241172 | Harmful, Irritant |
| Anhydrous Potassium Chloride | Sigma-Aldrich | 451029 | |
| Sulphuric Acid | VWR International Ltd | 102765G | (98%) Corrosive |
| Potassium Nitrate | Sigma-Aldrich | 221295 | |
| Hexaamine Ruthenium Chloride | Strem Chemicals Inc. | 44-0620 | Irritant |
| Perchloric Acid | Sigma-Aldrich | 311421 | Oxidising, Corrosive |
| 2-Propanol | Sigma-Aldrich | 24137 | Flammable |
| Nitric Acid | Sigma-Aldrich | 695033 | Oxidising, Corrosive |
| Sputter/ Evapourator | With Ti & Au targets | ||
| Raman | 514.5 nm laser | ||
| Annealing Oven | Capable of 400 °C | ||
| Ag paste | Sigma-Aldrich | 735825 | or other conductive paint |
| Potentiostat | |||
| pH Buffer solutions | Sigma-Aldrich | 38740-38752 | Fixanal buffer concentrates |
| Phenolphthalein Indicator | VWR International Ltd | 210893Q | |
| Methyl Red Indicator | Sigma-Aldrich | 32654 |
Referencias
- Angus, J. C. Ch. 1, Synthetic Diamond Films: Preparation, Electrochemistry, Characterization and Applications. Electrochemistry on diamond: History and current status. Brillas, E., Huitle, C. A. M. , John Wiley & Sons, Inc. (2011).
- Fujishima, A. Diamond Electrochemistry. , BKC. (2005).
- Macpherson, J. V. A practical guide to using boron doped diamond in electrochemical research. Physical Chemistry Chemical Physics. 17 (5), 2935-2949 (2015).
- Balmer, R. S., et al. Chemical vapour deposition synthetic diamond: materials, technology and applications. Journal of Physics: Condensed Matter. 21 (36), 364221(2009).
- Swain, G. M., Ramesham, R. The electrochemical activity of boron-doped polycrystalline diamond thin film electrodes. Analytical Chemistry. 65 (4), 345-351 (1993).
- Luong, J. H. T., Male, K. B., Glennon, J. D. Boron-doped diamond electrode: synthesis, characterization, functionalization and analytical applications. Analyst. 134 (10), 1965-1979 (2009).
- Hutton, L. A., et al. Examination of the Factors Affecting the Electrochemical Performance of Oxygen-Terminated Polycrystalline Boron-Doped Diamond Electrodes. Analytical Chemistry. 85 (15), 7230-7240 (2013).
- Bennett, J. A., Wang, J., Show, Y., Swain, G. M. Effect of sp2-Bonded Nondiamond Carbon Impurity on the Response of Boron-Doped Polycrystalline Diamond Thin-Film Electrodes. Journal of The Electrochemical Society. 151 (9), E306-E313 (2004).
- Martin, H. B., Argoitia, A., Landau, U., Anderson, A. B., Angus, J. C. Hydrogen and Oxygen Evolution on Boron-Doped Diamond Electrodes. Journal of The Electrochemical Society. 143 (6), L133-L136 (1996).
- Panizza, M., Cerisola, G. Application of diamond electrodes to electrochemical processes. Electrochimica Acta. 51 (2), 191-199 (2005).
- Williams, O. A. Nanocrystalline diamond. Diamond and Related Materials. 20 (5-6), 5-6 (2011).
- Patel, A. N., Tan, S. -y, Miller, T. S., Macpherson, J. V., Unwin, P. R. Comparison and Reappraisal of Carbon Electrodes for the Voltammetric Detection of Dopamine. Analytical Chemistry. 85 (24), 11755-11764 (2013).
- Watanabe, T., Honda, Y., Kanda, K., Einaga, Y. Tailored design of boron-doped diamond electrodes for various electrochemical applications with boron-doping level and sp2-bonded carbon impurities. physica status solidi (a). 211 (12), 2709-2717 (2014).
- Poferl, D. J., Gardner, N. C., Angus, J. C. Growth of boron-doped diamond seed crystals by vapor deposition. Journal of Applied Physics. 44 (4), 1428-1434 (1973).
- Spitsyn, B. V., Bouilov, L. L., Derjaguin, B. V. Vapor growth of diamond on diamond and other surfaces. Journal of Crystal Growth. 52 (Pt 1), 219-226 (1981).
- Bitziou, E., et al. In Situ Optimization of pH for Parts-Per-Billion Electrochemical Detection of Dissolved Hydrogen Sulfide Using Boron Doped Diamond Flow Electrodes. Analytical Chemistry. 86 (21), 10834-10840 (2014).
- Read, T. L., Bitziou, E., Joseph, M. B., Macpherson, J. V. In Situ Control of Local pH Using a Boron Doped Diamond Ring Disk Electrode: Optimizing Heavy Metal (Mercury) Detection. Analytical Chemistry. 86 (1), 367-371 (2014).
- Manivannan, A., Tryk, D., Fujishima, A. Detection of Trace Lead at Boron-Doped Diamond Electrodes by Anodic Stripping Analysis. Electrochemical and solid-state letters. 2 (9), 455-456 (1999).
- Manivannan, A., Seehra, M. S., Tryk, D. A., Fujishima, A. Electrochemical detection of ionic mercury at boron-doped diamond electrodes. Analytical Letters. 35 (2), 355-368 (2002).
- Boukherroub, R., et al. Photochemical oxidation of hydrogenated boron-doped diamond surfaces. Electrochemistry Communications. 7 (9), 937-940 (2005).
- Yagi, I., Notsu, H., Kondo, T., Tryk, D. A., Fujishima, A. Electrochemical selectivity for redox systems at oxygen-terminated diamond electrodes. Journal of Electroanalytical Chemistry. 473 (1), 173-178 (1999).
- Duo, I., Levy-Clement, C., Fujishima, A., Comninellis, C. Electron Transfer Kinetics on Boron-Doped Diamond Part I: Influence of Anodic Treatment. Journal of Applied Electrochemistry. 34 (9), 935-943 (2004).
- Mahé, E., Devilliers, D., Comninellis, C. Electrochemical reactivity at graphitic micro-domains on polycrystalline boron doped diamond thin-films electrodes. Electrochimica Acta. 50 (11), 2263-2277 (2005).
- Vandenabeele, P. Practical Raman spectroscopy: an introduction. , John Wiley & Sons. (2013).
- Filik, J. Raman spectroscopy: a simple, non-destructive way to characterise diamond and diamond-like materials. Spectroscopy Europe. 17 (5), 10(2005).
- Tuinstra, F., Koenig, J. L. Raman Spectrum of Graphite. The Journal of Chemical Physics. 53 (3), 1126-1130 (1970).
- Tachibana, T., Williams, B., Glass, J. Correlation of the electrical properties of metal contacts on diamond films with the chemical nature of the metal-diamond interface. II. Titanium contacts: A carbide-forming metal. Physical Review B. 45 (20), 11975(1992).
- Zivcova, Z. V., et al. Electrochemistry and in situ Raman spectroelectrochemistry of low and high quality boron doped diamond layers in aqueous electrolyte solution. Electrochimica Acta. 87, 518-525 (2013).
- Granger, M. C., et al. Standard Electrochemical Behavior of High-Quality, Boron-Doped Polycrystalline Diamond Thin-Film Electrodes. Analytical Chemistry. 72 (16), 3793-3804 (2000).
- Bard, A. J., Faulkner, L. R. Electrochemical methods. Fundamentals and Applications. , 2nd ed, John Wiley and Sons. (2001).
- Simonov, A. N., et al. Inappropriate Use of the Quasi-Reversible Electrode Kinetic Model in Simulation-Experiment Comparisons of Voltammetric Processes That Approach the Reversible Limit. Analytical Chemistry. 86 (16), 8408-8417 (2014).
- Terashima, C., Rao, T. N., Sarada, B. V., Spataru, N., Fujishima, A. Electrodeposition of hydrous iridium oxide on conductive diamond electrodes for catalytic sensor applications. Journal of Electroanalytical Chemistry. 544, 65-74 (2003).
- Bitziou, E., O'Hare, D., Patel, B. A. Simultaneous Detection of pH Changes and Histamine Release from Oxyntic Glands in Isolated Stomach. Analytical Chemistry. 80 (22), 8733-8740 (2008).
- Pickup, P. G., Birss, V. I. The kinetics of charging and discharging of iridium oxide films in aqueous and non-aqueous media. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry. 240 (1-2), 185-199 (1988).
- Baur, J. E., Spaine, T. W. Electrochemical deposition of iridium (IV) oxide from alkaline solutions of iridium(III) oxide. Journal of Electroanalytical Chemistry. 443 (2), 208-216 (1998).
- Carmody, W. R. Easily prepared wide range buffer series. Journal of Chemical Education. 38 (11), 559(1961).
- Glab, S., Hulanicki, A., Edwall, G., Ingman, F. Metal-Metal Oxide and Metal Oxide Electrodes as pH Sensors. Critical Reviews in Analytical Chemistry. 21 (1), 29-47 (1989).
- Burgot, J. -L. Ionic equilibria in analytical chemistry. , Springer Science & Business Media. (2012).
- Joseph, M. B., et al. Fabrication Route for the Production of Coplanar Diamond Insulated, Boron Doped Diamond Macro- and Microelectrodes of any Geometry. Analytical Chemistry. 86 (11), 5238-5244 (2014).
- Vanhove, E., et al. Stability of H-terminated BDD electrodes: an insight into the influence of the surface preparation. physica status solidi (a). 204 (9), 2931-2939 (2007).
- Salazar-Banda, G. R., et al. On the changing electrochemical behaviour of boron-doped diamond surfaces with time after cathodic pre-treatments. Electrochimica Acta. 51 (22), 4612-4619 (2006).
- Gelderman, K., Lee, L., Donne, S. W. Flat-Band Potential of a Semiconductor: Using the Mott-Schottky Equation. Journal of Chemical Education. 84 (4), 685(2007).
- Ushizawa, K., et al. Boron concentration dependence of Raman spectra on {100} and {111} facets of B-doped CVD diamond. Diamond and Related Materials. 7 (11-12), 1719-1722 (1998).
- Chrenko, R. Boron, the dominant acceptor in semiconducting diamond. Physical Review B. 7 (10), 4560(1973).
- Uzan-Saguy, C., et al. Hydrogen diffusion in B-ion-implanted and B-doped homo-epitaxial diamond: passivation of defects vs passivation of B acceptors. Diamond and Related Materials. 10 (3-7), 453-458 (2001).
- Hammerich, O., Speiser, B. Organic Electrochemistry. , Fifth Edition, Taylor & Francis. (2015).
- Juang, R. -S., Wang, S. -W. Electrolytic recovery of binary metals and EDTA from strong complexed solutions. Water Research. 34 (12), 3179-3185 (2000).
- Byrne, R. H., Kump, L. R., Cantrell, K. J. The influence of temperature and pH on trace metal speciation in seawater. Marine Chemistry. 25 (2), 163-181 (1988).
- Schonberger, E., Pickering, W. The influence of pH and complex formation on the ASV peaks of Pb, Cu and Cd. Talanta. 27 (1), 11-18 (1980).
- Chau, Y., Lum-Shue-Chan, K. Determination of labile and strongly bound metals in lake water. Water Research. 8 (6), 383-388 (1974).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados