Flüssigphasenreaktor: Inversion von Saccharose
Überblick
Quelle: Kerry M. Dooley und Michael G. Benton, Department of Chemical Engineering, Louisiana Landesuniversität, Baton Rouge, LA
Batch- und kontinuierliche Reaktoren werden in katalytischen Reaktionen verwendet. Gepackte Betten, die festen Katalysatoren und ein kontinuierlicher Strom verwenden, sind die häufigste Konfiguration. In Ermangelung einer umfangreichen Recycling-Stream werden solche verpackten Bett Reaktoren in der Regel modelliert, wie "plug-Flow". Am häufigsten kontinuierlichen Reaktors ist eine Rührbehälters, die angenommen wird, perfekt gemischt werden. 1 ein Grund für die Verbreitung von verpackten Bett Reaktoren ist, dass im Gegensatz zu den meisten Rührbehälters Designs eine große Wandfläche Reaktor-Volumen-Verhältnis mehr schnelle Wärmeübertragung fördert. Für fast alle Reaktoren muss Wärme entweder hinzugefügt oder zurückgezogen, um die Kontrolle der Temperatur für die gewünschte Reaktion stattfinden.
Die Kinetik der katalytischen Reaktionen sind oft komplexer als die einfache Bestellung 1St , 2Nd Ordnung, etc.-Kinetik in Lehrbüchern gefunden. Die Reaktionsgeschwindigkeiten können auch Preise der Stoffaustausch betroffen sein - Reaktion kann nicht schneller als die Rate, mit der Reaktanden geliefert werden, an die Oberfläche oder die mit der Produkte entfernt sind- und Wärmeübertragung stattfinden. Aus diesen Gründen ist fast immer Experimente Reaktionskinetik vor Gestaltung von Großgeräten festzulegen. In diesem Experiment erforschen wir, wie solche Experimente durchzuführen und wie sie zu interpretieren, indem du eine Reaktion Rate Ausdruck und eine scheinbare Geschwindigkeitskonstante.
Dieses Experiment untersucht die Verwendung eines verpackten Bett Reaktors die Kinetik der Saccharose-Inversion zu bestimmen. Diese Reaktion ist typisch für jene zeichnet sich durch eine solide Katalysator mit Flüssigphase Edukten und Produkten.
Saccharose → Glukose (Traubenzucker) + fructose(1)
Ein verpackte Bett Reaktor wird bei unterschiedlichen Strömungsgeschwindigkeiten, die Raum-Zeit zu kontrollieren, die Verweilzeit ist und ist analog zur verstrichenen Zeit in einem Batch-Reaktor betrieben werden. Der Katalysator, eine feste Säure wird zuerst vorbereitet werden, durch den Austausch von Protonen für alle anderen Kationen vorhanden. Der Reaktor wird dann auf die gewünschte Temperatur (Isotherme Betrieb) mit dem Fluss der Reaktanden beheizt werden. Wenn die Temperatur equilibriert hat, beginnt Produkt-Sampling. Durch ein Polarimeter, die optische Drehung misst, werden die Proben analysiert. Die Mischung optische Drehung kann zur Umwandlung von Saccharose, die dann im standard Kinetik Analysen verwendet werden kann, um die Reihenfolge der Reaktion in Bezug auf die Reaktanten Saccharose und die scheinbare Geschwindigkeitskonstante zusammenhängen. Die Auswirkungen der Strömungsmechanik - keine axiale Vermischung (Pfropfenströmung) vs. einige axiale mischen (gerührten Behälter in Serie) - auf die Kinetik werden auch analysiert werden.
Grundsätze
Im Vergleich zu kontinuierlichen Rührbehälters Reaktoren (CSTRs), sind Plug-Flow-Reaktoren (PFR) in der Regel besser geeignet für schnelle Reaktionen und großer Hitze Effekte. 2 jedoch können Druckabfall und die Entwicklung von "Hot Spots" problematisch sein. Daher Katalysator Partikelgrößen darf nicht zu klein sein und vorsichtig Startup-Prozeduren müssen befolgt werden.
Eine PFR ist mathematisch äquivalent zu einer Vielzahl von kleinen, gleich großen CSTRs in Serie, deren Gesamtgewicht Volumen oder Katalysator, der das System übereinstimmt. Wenn mischen in axialer Richtung auftritt, verringert die Anzahl der Tanks, N, musste Reaktorbetrieb zu beschreiben. Das Modell heißt "Tanks in Serie"-Modell. Die Parameter, die N und τ (Raum-Zeit) des Modells manchmal aus dem Mittelwert und der Varianz der Residenz ableiten lassen Zeit Vertrieb (E-Kurve) des Reaktors. Für eine PFR Mittelwert kann genau berechnet werden, und die Varianz ist null. Für einen echten Reaktor τ wird normalerweise geschätzt, und N ist aus dem Modell (Gleichung 2) zurückgebildet:
 (2)
(2)
wo "ich" ist der Reaktor Nummer CAo ist der feed Konzentration der begrenzende Reaktanten (in diesem Fall, Saccharose), ΔfAi ist die Veränderung der gebrochene Umwandlung von "A" in der ich die Rührbehälters und RAi ist die Rate der Reaktion in den Tank Ausfahrt Konzentrationen ausgewertet. Dieser Tarif muss positiv sein. Lösen der Massenbilanz für gleich große CSTRs in Serie auch verwendet werden, können um die Reihenfolge festzulegen Reaktion für "A" mit den Daten aus einem realen Reaktor und vorausgesetzt, die Temperatur können konstant gehalten werden vernünftig und, dass N bekannt.
Die Terminkurs Gleichung für eine katalytische Reaktion ist fast immer 1St Ordnung in Katalysatorkonzentration und einige positive Ordnung ≤2 in jeder Konzentration der Reaktionspartner. Produkte können manchmal hemmen den Katalysator, wodurch die Reaktanten Reihenfolge erscheinen weniger als es wirklich ist. Auch Edukte können den Katalysator, was Bestellungen für Reaktionspartner näher an Null hemmen. Aus diesen Gründen katalytische Reaktionen werden oft durch ein "Energie-Gesetz" Modell ausgedrückt:2
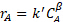 (3)
(3)
wo  ist die Konzentration der Begrenzung der Reaktanten, k' ist die scheinbare Rate konstant, und
ist die Konzentration der Begrenzung der Reaktanten, k' ist die scheinbare Rate konstant, und  ist die scheinbare Reaktionsordnung. Dieses Modell setzt voraus, dass der Katalysatorkonzentration konstant ist (es wird absorbiert in die wahre Geschwindigkeitskonstante geben k'). Im wirklichen Leben Katalysatoren oft deaktivieren, d. h., CKatze [in Mmol Säure Websites/Gcat] sinkt aufgrund der Ansammlung von Katalysatorgifte. Aus diesem Grund muss man entweder Konto für Deaktivierung (express CKatze als Funktion der Zeit Onstream) oder (vorzugsweise) sammeln Daten über einen bestimmten Zeitraum wo der Katalysator ist relativ stabil.
ist die scheinbare Reaktionsordnung. Dieses Modell setzt voraus, dass der Katalysatorkonzentration konstant ist (es wird absorbiert in die wahre Geschwindigkeitskonstante geben k'). Im wirklichen Leben Katalysatoren oft deaktivieren, d. h., CKatze [in Mmol Säure Websites/Gcat] sinkt aufgrund der Ansammlung von Katalysatorgifte. Aus diesem Grund muss man entweder Konto für Deaktivierung (express CKatze als Funktion der Zeit Onstream) oder (vorzugsweise) sammeln Daten über einen bestimmten Zeitraum wo der Katalysator ist relativ stabil.
Die Kinetik der Saccharose-Inversion finden meist erster Ordnung in Saccharose-Konzentration und erster Ordnung in der Konzentration des Katalysators Seiten sein. Lifshutz und Dranoff Berichten ein zweiter Ordnung Rate Konstante k ~0.029 ml / (Mmol Säure sites • min) für einen Katalysator ähnlich dem hier verwendeten bei 60 ° C mit einer Aktivierungsenergie von 77 kJ/Mol4 Gilliland Et Al. Berichten ~1.21 mL / (Mmol Säure sites • min) mit eine Aktivierungsenergie von 84 kJ/Mol für einen ähnlichen Katalysator zu diesen Konditionen. 4 die signifikanten Unterschiede in k können ergeben sich aus mehreren Faktoren: (a) Auswirkungen der Wärme- und Stoffübertragung auf die Kinetik; (b) schlechte Strömungsverteilung; (c) schlechte Temperaturregelung; und (d) unterschiedliche Zustände des Katalysator-Aktivierung.
Die Raum-Zeit für einen katalytischen Reaktor (analog Verweilzeit) ist in der Regel ausgedrückt als  = W/Q, wo W ist das Gewicht des Katalysators und Q ist die volumetrische Durchflussrate von Futtermitteln. Die Einheiten auf die Geschwindigkeitskonstante bereinigt um für die Einheiten auf Raum-Zeit (d. h. für eine 1St bestellen Reaktion der Einheiten auf k' wäre das gleiche wie bei 1 /
= W/Q, wo W ist das Gewicht des Katalysators und Q ist die volumetrische Durchflussrate von Futtermitteln. Die Einheiten auf die Geschwindigkeitskonstante bereinigt um für die Einheiten auf Raum-Zeit (d. h. für eine 1St bestellen Reaktion der Einheiten auf k' wäre das gleiche wie bei 1 / ). Abbildung 1 zeigt das Verhalten der Reaktionen der verschiedenen Kinetik Aufträge sowohl PFR und in einem Panzer in Serie-Modell, bestehend aus zwei Tanks. Beachten Sie, dass für positive Aufträge der PFR immer überlegen ist.
). Abbildung 1 zeigt das Verhalten der Reaktionen der verschiedenen Kinetik Aufträge sowohl PFR und in einem Panzer in Serie-Modell, bestehend aus zwei Tanks. Beachten Sie, dass für positive Aufträge der PFR immer überlegen ist.
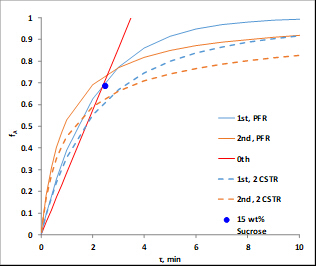
Abbildung 1. Berechnet gebrochene Konvertierungen (im Vergleich zu Raum-Zeit) von Saccharose mit Geschwindigkeitskonstanten abgeleitet aus den Daten für mehrere Saccharose Feeds bei 60 ° c
Um die Menge des Zuckers zu bestimmen, wird ein Polarimeter verwendet, die misst den Grad der Drehung des Lichts durch den Analyten zusammengesetzte polarisiert. Zucker sind Beispiele für Verbindungen mit Enantiomere, die durch ihre optische Aktivität, die Fähigkeit, Licht zu drehen unterschieden werden können. Ein Polarimeter eignet sich besonders zur Messung von Konzentrationen in diesem Experiment da die Reaktanten Saccharose dreht Licht nach rechts (positive optische Drehung), während die Produkte Glucose und Fructose nach links (negative optische Drehung) drehen.
Verfahren
Katalysator-Eigenschaften sind: Größe = 20-40 Maschen; Gewicht = 223 g; Wassergehalt = 30 wt. %; scheinbare (Schüttdichte) = 1,01 g/mL; Konzentration der Säure Website = 4,6 Mmol Säure Websites/g Trockengewicht; Fläche = 50 m2/g; Macroporosity (Makroporen-Volumen/Gesamt-Volumen von Kat.) = 0,34; durchschnittliche Makroporen-Größe = 80 nm. Eine P & ID-Abbildung des Gerätes ist in Abbildung 2dargestellt. Für dieses Experiment nur Bett #1, die Organics Tank, Pumpe und Rotameter verwendet. Proben werden auf den oberen Abfluss gesammelt. T505 ist der Temperaturregler.
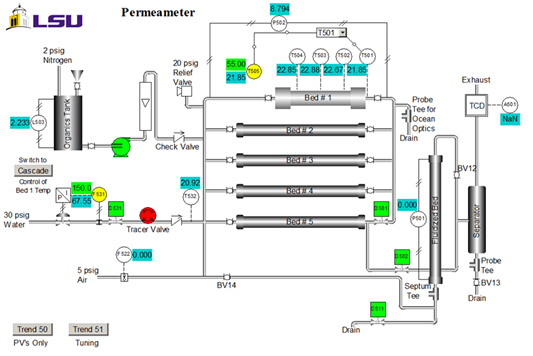
Abbildung 2 . P & ID-Darstellung des Apparates (System Steuerschnittstelle).
1. Inbetriebnahme des Reaktors
- Die dezentrale Steuerung-System-Schnittstelle zugreifen. Wählen Sie die Einheit Punkt im Menü Perm. Die Dauerwelle P & ID-Schema (Abbildung 2) erscheint. Alle Daten können in eine Excel-Tabelle erfasst werden. Klicken Sie auf "Trend 50" an der Schnittstelle zu die wichtigen Prozessvariablen in Bezug auf Zeit erhalten.
- Öffnen Sie die ein- und Ausfahrt Ventile zum katalytischen Reaktor Bett (Bett #1). Achten Sie darauf, dass die ein- und Ausfahrt Ventile zu den anderen Betten geschlossen sind, und dass das Regelventil (F531) und on / off-Ventil (D531) auf die Wasserversorgung der Stadt auch geschlossen sind.
- Fügen Sie verdünnten Säure (0,25 M H2SO4) zu den Vorlagebehälter (2 L).
- Einschalten der Förderpumpe zu einer konstanten Geschwindigkeit (mindestens 3 auf dem Zifferblatt), und der Rotameter, geben Sie die gewünschte Durchflussgeschwindigkeit (40-70 mL/min). Wenn der Rotameter Strömung in diesem Bereich kontrollieren kann, erhöhen Sie die Pumpendrehzahl zur nächsten höheren Einstellung.
- Sobald Säure zugeführt wurden, fügen Sie 200 mL oder mehr von DI-Wasser Vorlagebehälter hinzu. Die Säure, die Protonen austauschen werden, für was auch immer andere Ionen (Na+, Ca2 +) sind die Sulfonsäure Anionen beigefügt. Und zwar deshalb, weil auch DI Wasser Verunreinigungen und kommunale Wasserversorgung noch mehr enthält. Dies nennt man "Regeneration" des Katalysators.
- Bereiten Sie mindestens 10 L des feed-Lösung mit 15 wt % Saccharose in VE-Wasser. Bei der Vorbereitung der Saccharoselösung fügen Sie hinzu, die Saccharose langsam das Wasser unter ständigem Rühren bei Raumtemperatur. Verwenden Sie ein Magnetrührer und ein Paddel.
- Fügen Sie den Feed in den Organics-Tank.
(2) verpackte Bett Reaktorbetrieb
- Um Saccharose feed fließen beginnen, schalten Sie die Pumpe, und passen Sie fließen wie gewünscht mit der Pumpe Drehzahlregler und der Rotameter. Der Regler ist für grobe Anpassung während der Rotameter zur Feineinstellung ist.
- Programm des Sollwertes für T505 auf 50° C, und setzen Sie es auf AUTO. Das System ist so programmiert, die Heizungen abgeschnitten, wenn die Bett-Temperatur 90 ° C erreicht oder unterschreitet der Druckverlust gemessen an den d/p-Sender 1 Zoll auf der H2O Spalte Druck gibt an, dass es kein Futter.
- Eine typische für die Reaktion beträgt 60° C. Wenn die Reaktortemperatur zuerst 50 ° C übersteigt, bewegen Sie den Sollwert dazu Endtemperatur gewünscht. Ein Temperaturprofil kann über den Katalysator Abschnitt beobachten, die durch die Untersuchung von Thermoelementen T502 und T503 visualisiert werden können.
- Sammle 25 mL Proben von den Reaktionsprodukten am oberen Drain in Reagenzgläser oder Probenflaschen 10 Minuten auseinander. Sammeln Sie Proben nicht bis mindestens zwei Bett Verweilzeiten (das Bett offen Volumen ist ~1.2 L) bestanden haben.
3. Herunterfahren das System
- Stellen Sie die T-505, Bett #1 Temperaturregelung Ausgabe auf manuell auf Null ein.
- Fluss zum Ausschalten des Reaktors sobald die Temperatur beginnt zu sinken.
- Schließen Sie die Block-Ventile auf dem Bett #1.
4. Verwendung der Polarimeter
Analysieren Sie Reaktion Produktproben und die anfängliche füttern mit dem Polarimeter. Für ein 15 Gew.% % Saccharose ernähren sollte Umbauten im Bereich von 80 bis 120 mL/min reine Saccharose, Glukose und Fruktose sollte als die Kalibrierstandards verwendet werden. Finden Sie im Anhang für weitere Details auf Polarimetrie.
- Schalten Sie die Natriumlampe und lassen Sie es ca. 5 bis 10 Minuten aufwärmen. Ein gelbes Licht werden sichtbar.
- Überprüfen Sie die Nullstellung des Zifferblattes. Bei Null werden eine einheitliche Dunkelfeld mit keine hell/dunkel-Fransen, beachtet.
- Ein sauberes Röhrchen 25 mL der Ausgangslösung feed hinzufügen. Stellen Sie sicher, dass der Schlauch vollständig gefüllt ist. Verwenden Sie das gleiche Rohr für Kalibrierungen und Messungen, da die Lesung Weglänge abhängig ist.
- Legen Sie das Rohr in das Polarimeter. Das Rohr sollte nach oben eingeschlossene Luft aus der Visierlinie entfernen und die Lampe sollte in der Nähe des Okulars.
- Schließen Sie die Abdeckung. Wenn die Lösung polarisiertes Licht dreht, hell/dunkel Fransen durch die Linse zu beachten.
- Drehen Sie das Zifferblatt, bis die Ränder verschwinden und eine einheitliche Dunkelfeld beobachtet.
- Lesen Sie den Drehwinkel durch die Lupe mit dem Nonius-Skala. Die Zifferblatt-Abteilungen sind 1 Grad und jede Vernier Division ist 0,05 °. Um den Fokus einzustellen, drehen Sie das schwarze Zifferblatt befindet sich unterhalb des Okulars.
- Wiederholen Sie für jede Probe. Verwenden Sie VE-Wasser zur Reinigung der Röhre vor jeder Messung.
Ergebnisse
Das Polarimeter bestimmt die gebrochenen Konvertierungen von Saccharose nach der Reaktion in einem verpackten Bett-Reaktor. Eine vorherige Polarimeter-Kalibrierung für eine drei verschiedene Saccharose-Feeds ist in Abbildung 3dargestellt.
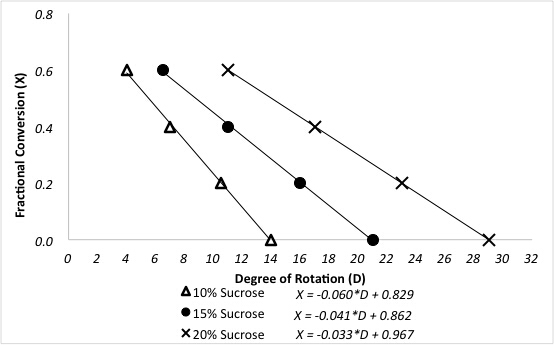
Abbildung 3 . Beziehung zwischen den Grad der Drehung und gebrochene Umstellung von Saccharose für unterschiedliche Futtermittel Konzentrationen.
Beispieldaten werden für die Reaktion bei 60 ° C bei unterschiedlichen Saccharose ernähren Konzentrationen in Abbildung 4 dargestellt. Gebrochene Konvertierungen wurden direkt aus der Eichkurve Polarimeter mit Hilfe der folgenden Gleichung, wo D ist der Grad der Drehung von der Polarimeter berechnet:
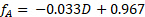 (4)
(4)
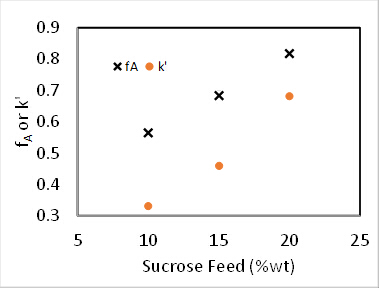
Abbildung 4 . Saccharose-Inversion-Reaktion bei 60° C, 100 mL/min Vorschub.
Bei 0th und 1St Bestellung Reaktionen erfolgt die Konvertierung in eine PFR unabhängig von feed Konzentration. 2 darüber hinaus k' Invarianten für 1St Auftrag Kinetik werden sollte. Vorausgesetzt, den Reaktor zu einem PFR, 2Nd Ordnung Geschwindigkeitskonstante, k2 (mL/Mmol Websites • min), wurde bestimmt durch Rechnungslegung für die 1St bestellen Abhängigkeit der Katalysator und die Geschwindigkeitskonstante Pseudo-1St bestellen k' () mL/gKatze • min) wurde durch das Ignorieren der 1St Bestellung Abhängigkeit des Katalysators ermittelt. Die Ergebnisse der Pseudo -k' Berechnungen werden in Abbildung 4dargestellt. Und der Wert von k2 wurde gefunden, indem man k' durch die Konzentration des Katalysators (Mmol Säure Websites/gKatze) zuvor gegeben.
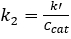 (5)
(5)
Um festzustellen, ob der Reaktionskinetik waren näher an 0, 0.5, 1, 1,5 oder 2Nd Ordnung in Saccharose, nicht-lineare Regression der Massenbilanz verwendet wurde, und die Summe der quadrierten Fehler für alle drei Läufe minimiert wurde. Um nicht-lineare Regression zu verwenden, wurde eine Zielfunktion formuliert, anhand der integrierten PFR Massenausgleich und die jeweiligen Reaktionsordnung. Im folgenden ist beispielsweise der Zielfunktion für eine 1,5 kinetische Ordnung in Saccharose-Konzentration:
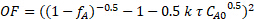 (6)
(6)
Andere Zielfunktionen können von PFR Massenbilanz Standardlösungen formuliert werden, die in allen Kinetik Lehrbüchern gefunden werden können. 2 Die experimentellen Daten in Abbildung 4 waren Fit, um die integrierte PFR Massenbilanzen für 1, 1,5 und 2 Aufträge in Bezug auf Saccharose. Die Summe der quadrierten Fehler für die drei Reaktion Aufträge waren entschlossen, 0,39, 0,16 und 1.3, betragen. Daher am besten geeignet erwies sich n = 1,5 Auftrag. Dies führt zu einem k' Wert von 35 (mL/gKatze • min).
Es war ursprünglich gedacht, dass die Kinetik 1St Ordnung in Bezug auf Saccharose waren. 2-3 mit dieser Annahme, kann man die Anzahl der gleichen Volumen CSTRs, N, in Serie bestimmen, die erforderlich sind, um dieses Reaktors zu modellieren. Wiederum die Summe der Quadrat Fehler in der Massenbilanz für alle drei Läufe minimiert wurden, um beide N zu bestimmen und k'. Die Daten wurden dem Panzer in Serie-Modell für 1St Bestellung Reaktionen passen:
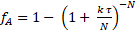 (7)
(7)
Es wurde festgestellt, dass N = 2,1 "Tanks" und k' = 0,62 mL/gKatze • min. Dies ist keine tolle Passform, da die Reaktionsordnung nicht genau 1 ist. Die Daten deuten darauf hin eine Saccharose Bestellung > 1. Die relativen Standardabweichungen von fA waren höchstens 2 %, was leicht durch die Variation der Temperatur (bis zu 9 ° C) berücksichtigt wird. Es gab keinen Beweis der Katalysator Deaktivierung. Die gebrochenen Konvertierungen für beide PFR und zwei CSTR Tanks in Serie wurde berechnet, mit der k aus nicht-lineare Regression und in Abbildung 1dargestellt. Für nullter Ordnung gab es keinen Unterschied zwischen einem PFR und CSTRs in Serie, da die Rate unabhängig von Saccharose-Konzentration ist. Wenn die Kurven für 6 oder mehr CSTRs geplant hatte, würde sie eng mit den PFR Kurven fiel haben. Die vorhergesagten gebrochenen Konvertierungen für zwei CSTR Tanks in Serie ist langsamer als ein PFR für alle Bestellungen der Reaktion. Die experimentellen Daten für 15 wt % Saccharose ist eigentlich näher an eine Reaktion erster Ordnung in PFR.
Der Fehler in k' abgeschätzt werden durch einen Vergleich der Unterschiede in der berechneten k' Werte an die durchschnittliche Temperaturabweichung (4,5 ° C) auf die Temperatur der Reaktion, 60 ° C, unter Verwendung der Arrhenius-Gleichung und Mittelung der beiden Literatur Aktivierungsenergien. Die geschätzte k "für 1,5 Ordnung Kinetik bei 64,5 ° C ist 52 (mL/Mol)0,5 mL • Gcat-1 • min-1, was fast 50 % höher als der Regression Wert 35 (mL/Mol)0,5 mL • Gcat-1 • min-1. Geringe Temperaturschwankungen beeinflussen die k' stark.
Anwendung und Zusammenfassung
Die Reaktion verhält nicht sich genau wie erwartet, da die scheinbare Ordnung n > 1 ist. Alle Phänomene, die solche Abweichungen verursachen können, in reale Reaktoren, werden Abweichungen vom idealen PFR Verhalten verursacht durch axiale mischen vorgeschlagen durch die Tatsache, dass passend zum Panzer im Serienmodell gibt nur eine kleine Anzahl von Panzer - für eine perfekte PFR N sollte mindestens 6 . Solche Abweichungen sind oft in relativ kurzen Betten gefunden, vor allem, wenn die Strömung mehrphasig (etwas Wasser ist verdampft im Reaktor). Eine weitere Ursache für die Abweichung ist jedoch weniger offensichtlich, aber wahrscheinlich noch wichtiger. Die Reaktion ist stark exotherm und wie bereits erwähnt, schwankte die Temperatur von weniger als 9° C (meist über den Sollwert). Die mehr Saccharose in das Futter, desto mehr Wärme, der generiert wird. Wie zu erwarten, waren die Schwingungen mit den 20 Gew.-% zu ernähren. Dies legt nahe, ein weiterer Grund für eine scheinbare Ordnung n > 1: mehr Wärme auf eine höhere Konzentration des Futters erhöht die Reaktortemperatur mehr, was wiederum erhöht die Geschwindigkeit der Reaktion, die wiederum einer abgeleiteten scheinbaren Ordnung > die tatsächliche Reihenfolge. Wenn die Temperatur nicht ausreichend kontrolliert wird, könnte die Reaktortemperatur auf den adiabatischen Grenzwert erhöhen. Abweichungen vom idealen PFR Verhalten im Durchfluss und Temperatur beeinflussen die scheinbare Kinetik, abgeleitet aus der tatsächlichen Reaktoren, setzen eine Prämie auf sorgfältige Reaktor Scale-Up auf Duplizieren Pilotanlage Bedingungen der Flüssigkeitsströmung und Wärmeübertragung.
Verpackten Bett Reaktoren haben viele Anwendungen in der chemischen Industrie. Schwefelsäure, eine Chemikalie, die verwendet, um Hunderte von verschiedenen Produkten ist häufig Teil mit verpackten Bett chemische Reaktoren in Serie hergestellt. Mehr als 200 Millionen Tonnen werden jährlich produziert. In dieser Reaktion von Schwefeldioxid und Luft sind durchlaufen Festbett Reaktoren in Serie (mit zwischengeschalteten Wärmetauscher für Wärmeabfuhr) mit unterstützten Vanadium Oxid Katalysator bei hohen Temperaturen. 4 die SO2 ist SO3, oxidiert, wenn im Wasser absorbiert, ist Schwefelsäure.
Eine neuere Anwendung für verpackte Bett Reaktoren ist in der Produktion von Biodiesel durch Transesterifying Triglyceride oder esterifying Fettsäuren mit Methanol. Während Biodiesel auf unterschiedliche Weise hergestellt wird, können verpackten Bett Reaktoren für eine kontinuierliche Produktion von Vorteil sein. Biodiesel ist eine erneuerbare Energiequelle in Betracht gezogen, weil es aus Algen oder Abfälle Lebensmittel hergestellt wird, und ist biologisch abbaubar und ungiftig. Unabhängig von der eingesetzten Katalysator muss es gründlich aus dem Produkt nach der Reaktion bereinigt werden, da auch kleine Mengen Kraftstoff unbrauchbar machen können. 5
ANHANG A – MIT DEM POLARIMETER
Polarimetrie misst das Ausmaß, zu dem ein Stoff interagiert mit Flugzeug polarisiertes Licht besteht aus Wellen, die nur in einer Ebene schwingen. Es kann polarisierte Licht nach links, rechts, oder überhaupt nicht drehen. Wenn es polarisiertes Licht nach links oder nach rechts dreht, ist es "optisch aktive". Wenn eine Verbindung eine chirale Zentrum nicht kennt, wird es nicht polarisiertes Licht drehen. Die Anzahl der Grad und die Drehrichtung werden gemessen, um die beobachteten Drehung zu geben. Die beobachteten Rotation wird für die Länge der Zelle verwendet und die Lösungskonzentration, unter Verwendung der folgenden Gleichung korrigiert: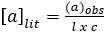 (A1)
(A1)
Wo: eine bestimmte Rotation (Grad) (Literaturwert) = l = Weglänge (dm) und c = Konzentration (g/mL).
Vergleicht man den korrigierten Drehung auf Literatur Werte beobachtet kann bei der Identifizierung einer unbekannten Verbindung unterstützen. Wenn die Verbindungen bekannt sind, ist es jedoch häufiger zur Vorbereitung Kalibrierstandards der unbekannten und korrelieren die beobachteten Drehung, Konzentration.
Referenzen
- J. Sauer, N. Dahmen and E. Henrich. "Chemical Reactor Types." Ullman's Encycylopedia of Industrial Chemistry (2015). Web. 15 Oct. 2016.
- H.S. Fogler, "Elements of Chemical Reaction Engineering," 4th Ed., Prentice-Hall, Upper Saddle River, NJ, 2006, Ch. 2-4; O. Levenspiel, "Chemical Reaction Engineering," 3rd Ed., John Wiley, New York, 1999, Ch. 4-6; C.G. Hill, Jr. and T.W. Root, "Introduction to Chemical Engineering Kinetics and Reactor Design," 2nd Ed., John Wiley, New York, 2014, Ch. 8.
- N. Lifshutz and J. S. Dranoff, Ind. Eng. Chem. Proc. Des. Dev., 7, 266-269 (1968).
- E.R. Gilliland, H. J. Bixler, and J. E. O'Connell, Ind. Eng. Chem. Fundam., 10, 185-191 (1971).
- "Sulfuric Acid." The Essential Chemical Industry. Univ. of York, 2016. http://www.essentialchemicalindustry.org/chemicals/sulfuric-acid.html. Accessed 10/20/16.
- E. Lotero, Y. Liu, D.E. Lopez, K. Suwannakarn, D.A. Bruce and J.G. Goodwin, Jr., Ind. Eng. Chem. Res.,44, 5353-5363 (2005); A. Buasri, N. Chaiyut, V. Loryuenyong, C. Rodklum, T. Chaikwan, and N. Kumphan, Appl. Sci.2, 641-653 (2012); doi:10.3390/app2030641.
pringen zu...
Videos aus dieser Sammlung:

Now Playing
Flüssigphasenreaktor: Inversion von Saccharose
Chemical Engineering
9.7K Ansichten

Prüfung der Wärmeübertragungseffizienz eines Rippenrohrwärmetauschers
Chemical Engineering
17.9K Ansichten

Ein Tablett mit Trockner, leitfähige und konvektive Wärmeübertragung zu untersuchen
Chemical Engineering
43.9K Ansichten

Viskosität von Propylenglykol-Lösungen
Chemical Engineering
32.7K Ansichten

Porosimetrie eines Aluminiumsilikatpulvers
Chemical Engineering
9.6K Ansichten

Demonstration des Potenzgesetzmodells durch Extrusion
Chemical Engineering
10.0K Ansichten

Gas-Absorber
Chemical Engineering
36.6K Ansichten

Dampf-Flüssigkeits-Gleichgewicht
Chemical Engineering
88.7K Ansichten

Der Einfluss des Rückflussverhältnisses auf die Effizienz der Tray-Destillation
Chemical Engineering
77.7K Ansichten

Effizienz der Flüssig-Flüssig-Extraktion
Chemical Engineering
48.4K Ansichten

Kristallisation von Salicylsäure durch chemische Modifikation
Chemical Engineering
24.2K Ansichten

Einphasen- und Zweiphasenströmung in einem Festbettreaktor
Chemical Engineering
18.9K Ansichten

Kinetik der Additionspolymerisation zu Polydimethylsiloxan
Chemical Engineering
16.1K Ansichten

Katalytischer Reaktor: Hydrierung von Ethylen
Chemical Engineering
30.4K Ansichten

Spin und Chill
Chemical Engineering
7.4K Ansichten
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten