Method Article
Epimedii Folyum koyun eti yağı işleme teknolojisinin optimizasyonu ve zebra balığı embriyonik gelişimi üzerindeki etkisinin test edilmesi
Bu Makalede
Özet
Bu protokolde, Epimedii folium'un (EF) koyun eti yağı işleme teknolojisi, bir Box-Behnken deneysel tasarım-tepki yüzey metodolojisi uygulanarak optimize edildi ve ham ve optimize edilmiş su ekstrakte edilen EF'nin zebra balığı embriyonik gelişimi üzerindeki etkisi önceden araştırıldı.
Özet
Geleneksel bir Çin tıbbı (TCM) olan Epimedii folium'un (EF), tıp ve gıdada > 2.000 yıllık bir geçmişi vardır. Klinik olarak, koyun eti yağı ile işlenmiş EF genellikle bir ilaç olarak kullanılır. Son yıllarda, EF'yi hammadde olarak kullanan ürünlerin güvenlik riskleri ve advers reaksiyonlarına ilişkin raporlar giderek artmıştır. İşleme, TCM'nin güvenliğini etkili bir şekilde artırabilir. TCM teorisine göre, koyun eti yağı işleme, EF'nin toksisitesini azaltabilir ve böbrekler üzerindeki tonlama etkisini artırabilir. Bununla birlikte, EF koyun eti yağı işleme teknolojisinin sistematik araştırma ve değerlendirme eksikliği vardır. Bu çalışmada, birden fazla bileşenin içeriğini değerlendirerek işleme teknolojisinin temel parametrelerini optimize etmek için Box-Behnken deneysel tasarım-tepki yüzey metodolojisini kullandık. Sonuçlar, EF'nin optimum koyun eti yağı işleme teknolojisinin şu şekilde olduğunu göstermiştir: koyun eti yağını 120 ° C'de 10 ° C'± ısıtmak, ham EF'yi eklemek, eşit derecede parlak olana kadar hafifçe 189 ° C'ye ± 10 ° C'ye kızartmak ve sonra çıkarmak ve soğutmak. Her 100 kg EF için 15 kg koyun eti yağı kullanılmalıdır. Sulu bir ham ve koyun eti yağı işlenmiş EF ekstraktının toksisiteleri ve teratojeniteleri, zebra balığı embriyo gelişim modelinde karşılaştırılmıştır. Sonuçlar, ham bitki grubunun zebra balığı deformitelerine neden olma olasılığının daha yüksek olduğunu ve yarı maksimal ölümcül EF konsantrasyonunun daha düşük olduğunu gösterdi. Sonuç olarak, optimize edilmiş koyun eti yağı işleme teknolojisi, iyi tekrarlanabilirlik ile istikrarlı ve güvenilirdi. Belirli bir dozda, EF'nin sulu ekstraktı zebra balığı embriyolarının gelişimi için toksikti ve toksisite, ham ilaç için işlenmiş ilaçtan daha güçlüydü. Sonuçlar, koyun eti yağı işlemenin ham EF'nin toksisitesini azalttığını göstermiştir. Bu bulgular, koyun eti yağı ile işlenmiş EF'nin kalitesini, homojenliğini ve klinik güvenliğini artırmak için kullanılabilir.
Giriş
Epimedii folium (EF), Epimedium brevicornu Maxim., Epimedium sagittatum'un (Sieb. et Zucc.) kurutulmuş yapraklarıdır. Maxim., Epimedium pubescens Maxim. veya Epimedium koreanum Nakai. EF, osteoporoz, menopoz sendromu, meme topakları, hipertansiyon, koroner kalp hastalığı ve diğer hastalıkların tedavisinde kullanılabilir1. Geleneksel bir Çin tıbbı (TCM) olarak EF, tıp ve gıda alanında 2.000 yıldan fazla bir geçmişe sahiptir. Düşük fiyatı ve böbrekleri tonlamanın dikkat çekici etkisi nedeniyle, ilaçlarda ve sağlık gıdalarında yaygın olarak kullanılmaktadır. EF, koyun eti yağı ile karıştırılarak kızartılarak işlenir, ilk olarak Liu Songdönemi 2'de Lei Xiao tarafından yazılan Lei Gong İşleme Teorisi'nde açıklanan bir işlemdir. Ham EF ve kızartılmış EF'nin etkinlikleri oldukça farklıdır. Ham EF esas olarak romatizmayı ortadan kaldırırken, kızartılmış EF, yang3'ü güçlendirmek için böbrekleri ısıtır. Şu anda, EF yaygın olarak ilaç ve sağlık gıdalarında hammadde olarak kullanılmaktadır; listelenen 399 Çin patentli ilaç, dokuz ithal sağlık gıdası ve EF'yi hammadde olarak kullanan 455 yerli sağlık gıdası bulunmaktadır4. Bu tıbbi malzeme büyük uygulama beklentilerine sahiptir. Bununla birlikte, son yıllarda, EF'yi hammadde olarak kullanan sağlık gıdaları ve Çin patentli ilaçların neden olduğu advers reaksiyonlar ve insan karaciğer hasarı raporları artmıştır ve ilgili toksisite çalışmaları 5,6,7, EF'nin bir hammadde olarak potansiyel güvenlik risklerine sahip olduğunu bildirmiştir.
Çin tıbbi işleme, toksisiteyi etkili bir şekilde azaltabilen veya ortadan kaldırabilen ve TCM'lerin güvenliğini artırabilen farmasötik teknikleri ifade eder. EF'nin geleneksel işleme yöntemi, EF'nin toksisitesini azaltan ve böbrekleri ısıtma ve yang8'i teşvik etme etkisini artıran koyun eti yağı ile kızartmadır. Bu işleme yöntemi, Çin Farmakopesine ve çeşitli işleme spesifikasyonlarına dahil edilmiştir1. EF işlemi sadece şu şekilde belirtilir: her 100 kg EF için, 20 kg amniyotik yağ (rafine edilmiş) eklenir ve düzgün ve parlak olana kadar hafif ateşlenir1. Yukarıdaki standartlarda katı EF işleme yöntemi parametreleri yoktur, bu nedenle yerel işleme spesifikasyonları tutarlılık sağlamak için birleştirilmemiştir. Bu nedenle, EF sürecinin sistematik bir çalışmasının yapılması yararlı olacaktır. Bu yazıda, EF'nin işleme teknolojisini optimize etmek için Box-Behnken deneysel tasarım-tepki yüzey yöntemi kullanılmıştır.
Box-Behnken deneysel tasarımı, tipik olarak bir süreçteki faktörleri optimize etmek için kullanılan bir yöntemdir. Ekstraksiyon parametreleri, çoklu regresyon denklemi uydurma faktörleri ile etki değerleri arasındaki fonksiyonel ilişki kurularak optimize edilebilir. Son zamanlarda, bu yöntem TCM ekstraksiyonu 5,6,7 ve işleme 9,10,11'i incelemek için yaygın olarak kullanılmaktadır. Çeşitli çalışmalar, tuzla işlenmiş Psoraleae fructus12, şarapla işlenmiş Cnidii fructus13 ve kavrulmuş Cinnamomi ramulus14 gibi bir Box-Behnken tasarımını takiben tuz işleme, şarap işleme ve kızartma içeren TCM hazırlama yöntemlerini bildirmiştir. Bu yöntem test süresini kısaltmış, yüksek test doğruluğuna sahiptir ve çok faktörlü ve çok seviyeli testler için uygundur. Yöntem, ortogonal tasarım test yönteminden daha basittir ve tek tip tasarım yönteminden daha kapsamlıdır15. Elde edilen ilişkiler, test aralığındaki herhangi bir test noktasının tahmin edilen değerini belirleyebilir, bu da büyük bir avantajdır. EF'nin işlemden sonra daha az toksik olup olmadığını test etmek için bir zebra balığı modeli kullanılabilir.
TCM toksisite çalışmalarında, zebra balığı modeli, hücre deneylerinin yüksek veriminin ve kemirgen deneyleriyle benzerliklerin ikili avantajlarına sahiptir16. Bu model küçük boyutu, yüksek yumurtlama oranı, kısa üreme döngüsü ve üreme kolaylığı ile karakterizedir. Model, hücre kültürü plakalarındaki büyük ölçekli senkron deneylerde kullanılabilir ve deneysel ilaç dozu küçüktür, deneysel döngü kısadır, maliyet düşüktür ve tüm deneysel sürecin gözlemlenmesi ve çalıştırılması kolaydır17. Zebra balığı embriyoları şeffaftır ve hızla gelişir. Bu nedenle, ilaçların farklı gelişim evrelerinde viseral dokular üzerindeki toksisitesi ve teratojenik etkileri mikroskop altında doğrudan gözlemlenebilir18. Zebra balığı ve insanlar arasındaki gen homolojisi %85 kadar yüksektir18. Zebra balıklarının sinyal iletim yolu, insanlarınkine benzer18. Zebra balıklarının biyolojik yapısı ve fizyolojik işlevi, memelilerinkine oldukça benzerdir18. Bu nedenle, uyuşturucu testi için bir zebra balığı modeli, insanlar için güvenilir ve tamamen uygulanabilir deney hayvanları sağlayabilir19.
Bu çalışmada, koyun eti yağı miktarını ve sıcaklığını ve EF işleme teknolojisinde kullanılan kızartma sıcaklığını optimize etmek için Box-Behnken tasarım-tepki yüzey metodolojisini kullandık ve değerlendirme indeksleri olarak icariin, epimedin A, epimedin B, epimedin C ve baohuoside I içerikleri kullanıldı. Zebra balığı modeli, bir EF su ekstraktının, işlemin EF üzerindeki zayıflama etkisini değerlendirmek için işlemden önce ve sonra zebra balığı embriyonik gelişimi üzerindeki etkisini önceden araştırmak için kullanılmıştır.
Protokol
Hayvanlarla ilgili tüm deneyler, TCM Chongqing Enstitüsü Deney Etik Komitesi'nin onayı ile gerçekleştirilmiştir (laboratuvar hayvanları etik inceleme sertifikası numarası: ZJS2022-03).
1. Biyoaktif bileşenlerin belirlenmesi
NOT: Bu araştırmada kullanılan türler Epimedium sagittatum idi ve örnekler Chongqing, Fengdu County'de toplandı. Örneklem, E. sagittatum'un (Sieb. et Zucc.) kuru bir toprak üstü kısmı olarak tanımlandı. Atasözü. Biyolojik Tıp Enstitüsü, Chongqing Geleneksel Çin Tıbbı Enstitüsü araştırmacıları tarafından.
- Elektronik analitik terazi kullanarak icariin, epimedin A (EA), epimedin B (EB), epimedin C (EC) ve baohuoside I (BI) olmak üzere her bir referans maddenin uygun miktarını doğru bir şekilde tartarak kontrol ürünü çözeltisini hazırlayın ve metanol içinde çözün. Bunları kullanarak 381,61 μg/mL icariin, 124,14 μg/mL EA, 110,24 μg/mL EB, 1091,75 μg/mL EC ve 184,98 μg/mL BI içeren karışık bir referans stok çözeltisi hazırlayın.
- EF'yi 3 numaralı bir elek ile ezerek test ürünü solüsyonunu hazırlayın. Yaklaşık 0,2 g (elektronik analitik terazi kullanarak) ezilmiş EF'yi tıpalı bir Erlenmeyer şişesine yerleştirin, 20 mL seyreltik etanol ekleyin ve ardından 1 saat boyunca 400 W güç ve 50 kHz frekansta ultrasonikat yapın. Test çözeltisini elde etmek için iyice çalkalayın ve 0,22 μm'lik bir membran filtresinden geçirin.
- Kromatografiyi aşağıdaki gibi yapın. 4,6 mm x 250 mm boyutlarında ve 5 μm iç çapa sahip C18 kolonlu yüksek performanslı sıvı kromatografisi (HPLC) kullanın. Mobil faz A olarak asetonitril ve mobil faz B olarak ultra saf su kullanın Aşağıdaki gradyan elüsyon parametrelerini kullanın: 0-30 dakika,% 24 A ila% 26 A; 30-31 dakika,% 26 A ila% 45 A; 31-45 dakika,% 45 A ila% 47 A. 220 nm'lik bir algılama dalga boyu kullanın (kullanılan dedektör için Malzeme Tablosuna bakınız). Kolon sıcaklığını 30 °C'de ve akım hızını 1,0 mL/dak'da tutun ve 10 μL'lik bir numune boyutu kullanın.
- Doğrusal ilişkiyi araştırmak için, adım 1.1'deki gibi icariin, EA, EB, EC ve BI için sırasıyla 2 kez, 4 kez, 8 kez, 16 kez ve 32 kez seyreltilmiş karma başvuru çözümünü kullanın. Asetonitril'i mobil faz A olarak ve ultra saf suyu mobil faz B olarak kullanın.
- Aşağıdaki gradyan elüsyon parametrelerini kullanın: 0-30 dakika,% 24 A ila% 26 A; 30-31 dakika,% 26 A ila% 45 A; 31-45 dakika,% 45 A ila% 47 A. 220 nm'lik bir algılama dalga boyu kullanın (kullanılan dedektör için Malzeme Tablosuna bakınız). Kolon sıcaklığını 30 °C'de ve akım hızını 1,0 mL/dak'da tutun ve 10 μL'lik bir numune boyutu kullanın. Son olarak, en yoğun alanları kaydedin. Doğrusal regresyonu, apsis olarak referans konsantrasyonu (x ekseni, μg / mL) ve tepe alanı (y ekseni) ordinat olarak profesyonel yazılım kullanarak çizin (bkz.
- Adım 1.3'te gösterilen kromatografik koşulları kullanarak HPLC tarafından karışık kontrol solüsyonunu art arda altı kez ölçerek hassasiyet testini gerçekleştirin. Her kimyasal bileşimin algılama süresini ve tepe alanlarını kaydedin ve aşağıdaki formülü kullanarak hassasiyeti (tekrarlanabilirlik) değerlendirmek için tepe alanlarının göreceli standart sapmalarını (RSD) hesaplayın:
RSD% = standart sapma (SD)/hesaplanan sonuçların aritmetik ortalaması (X) x %100 - Tekrarlanabilirlik testini gerçekleştirmek için EF tozunu doğru bir şekilde tartın ve adım 1.2'deki yönteme göre test ürünü çözeltisinin altı parçasını paralel olarak hazırlayın. Hazırlanan çözeltileri, adım 1.3'te sunulan kromatografik koşullar altında HPLC'ye tabi tutun. Her kimyasal bileşimin tutma sürelerini ve tepe alanlarını kaydedin ve her bileşiğin miktarlarını standart bir eğriden hesaplayın (pik alanlara karşı konsantrasyonlar). RSD% 'yi yukarıdaki gibi hesaplayın.
- Stabilite testini gerçekleştirmek için, test çözeltilerini oda sıcaklığında saklayın ve stabiliteyi değerlendirmek için hazırlandıktan sonra adım 1.3'te 0 saat, 2 saat, 4 saat, 8 saat, 12 saat ve 24 saatte açıklanan HPLC yöntemiyle içeriklerini ölçün. Her kimyasal bileşimin tutma sürelerini ve tepe alanlarını kaydedin ve tepe alanlarının RSD% 'sini yukarıdaki gibi hesaplayın.
- Numune geri kazanım testini gerçekleştirmek için, altı kopya için tıpalı bir Erlenmeyer şişesine 0,2 g EF tozu tartın. Uygun miktarda referans çözeltisi ekleyin (numuneye eklenen referans madde miktarı, numunenin bilinen içeriğinin% 100'üne eşdeğerdir) ve test çözeltisini adım 1.2'de sunulan yönteme göre hazırlayın.
- Numuneleri kromatografa enjekte edin ve adım 1.3'teki kromatografik koşullara göre analiz edin. Tepe alanlarını kaydedin ve ortalama kurtarma ve RSD% değerlerini aşağıdaki gibi hesaplayın:
Ani örnek kurtarma oranı = (çivili örnek içeriği − örnek içerik)/örnek miktarı x %100
2. Box-Behnken tasarım-tepki yüzey metodolojisi kullanılarak EF koyun eti yağı işleme teknolojisinin optimizasyonu
- EF işlemede koyun eti yağı miktarı (A; %15-%35), koyun eti yağı sıcaklığı (B; 50-120 °C) ve kızartma sıcaklığı (C; 80-300 °C) gibi temel parametreleri etkili faktörler olarak seçin. Değerlendirme dizinleri olarak icariin, EA, EB, EC ve BI içeriğinin kapsamlı puanlarını kullanın. Buradaki koyun eti yağı yüzdesi kütle yüzdesidir.
- Box-Behnken tepki yüzeyi deneylerini tasarlamak, ikinci dereceden tepki yüzeyini keşfetmek ve ikinci dereceden bir polinom modeli oluşturmak için yanıt yüzeyi analiz yazılımını (bkz. Yeni Box-Behnken Tasarımı'nı seçin ve Sayısal Faktörler seçeneğini 3 olarak ayarlayın; A, B ve C faktörlerini ayarlayın. Yanıtlar seçeneğini 1 olarak ayarlayın (kapsamlı puandır). Tasarımı tamamlamak için Devam'a tıklayın. Toplam 17 deney planlanmıştır (bakınız Tablo 1).
NOT: Bağımsız ve bağımlı değişkenler için, düşük, orta ve yüksek düzeyleriyle birlikte, bkz: Tablo 2. - EF'yi Tablo 1'deki belirli parametrelere göre işleyin; Örneğin, 1 numaralı sipariş için, rafine koyun eti yağını %15 V/V olarak tartın ve ardından eritmek için 50 °C'ye ısıtın. Ham EF'yi erimiş koyun etine ekleyin, eşit derecede parlak olana kadar hafif bir ateşte (190 ° C) karıştırın ve ardından çıkarın ve soğutun. 17 deneysel operasyon gerçekleştirdi. Bu çalışmada toplam 17 grup EF işlenmiş ürün elde edilmiştir.
NOT: Koyun eti yağı oda sıcaklığında (25 °C) katıdır ve ısıtıldığında sıvı halinde erir. Sıvı haldeki koyun eti yağı yardımcı madde olarak kullanılabilir. - İşlenmiş ürünlerin test çözeltilerini adım 1.2'de açıklanan yönteme göre hazırlayın. Ardından, adım 1.3'te açıklanan kromatografik koşullara göre HPLC kullanarak bunları analiz edin. Her kimyasal bileşimin tutma sürelerini ve tepe alanlarını kaydedin ve her bir test çözeltisindeki icariin, EA, EB, EC ve BI içeriğini harici bir standart eğriye göre hesaplayın. 17 deney grubunun kapsamlı puanlarını hesaplamak için aşağıdaki kapsamlı puan hesaplama formülünü kullanın:
Kapsamlı puan = Z/Z max × 0.5 + BI/BImax × 0.5
burada Z, icariin, EA, EB ve EC içeriklerinin toplamıdır; Zmax , 17 deney grubundaki icariin, EA, EB ve EC içeriklerinin toplamının maksimum değeridir; BI, BI içeriğidir; ve BImax , 17 deney grubundaki BI içeriğinin maksimum değeridir. - Deneysel verileri analiz etmek için 17 deney grubu için kapsamlı puanlama sonuçlarını veri analiz yazılımına aktarın (bkz. Değerlendirme öğeleri altında, ikinci dereceden işlem sırası seçeneğini ve polinom model türü seçeneğini belirleyin.
3. İşlemenin zebra balığı embriyonik gelişimi üzerindeki etkisinin test edilmesi
- Numune hazırlama
- Ham ve işlenmiş EF'yi 3 numaralı bir elek ile ezin (bkz. Her EF numunesinin 100 gramına 1.000 mL ultra saf su ekleyin. EF'yi 0,5 saat bekletin, suyu her biri 30 dakika boyunca iki kez kaynatın ve ardından filtre kağıdı ile filtreleyin.
- Filtratları birleştirin ve numuneyi ısıtarak konsantre edin. İşlenmiş EF (PEF, 1 g/mL) ve ham EF (CEF,1 g/mL) stok çözeltilerini elde etmek için 100 mL'lik son hacme ultra saf su ekleyin. Her stok çözeltisindeki ham ilaç miktarını ölçün.
- 10 mL volümetrik şişelere 1 mL, 1,5 mL, 2,5 mL, 5 mL ve 7,5 mL stok çözeltilerinin alikuatlarını yerleştirin ve ardından zebra balığı embriyotoksisitesi çalışması için 100 mg / mL, 150 mg / mL, 200 mg / mL, 250 mg / mL, 500 mg / mL ve 750 mg / mL konsantrasyonlarında test çözeltilerini hazırlamak için hacme ultra saf su ekleyin.
NOT: Test çözeltilerinin konsantrasyonları, ilgili literatüre 20,21 atıfta bulunularak ve normal toksikolojide kullanılan10 kat konsantrasyon gradyanını vermek için ön deneyler yapılarak hazırlanmıştır. CEF işlenmemiş bir numuneydi ve PEF, bölüm 2'de açıklanan en iyi işleme teknolojisi ile hazırlanmış bir numuneydi.
- Zebra balığı yetiştiriciliği ve embriyo tedavisi21
- Vahşi tip zebra balıklarını (Malzeme Tablosuna bakınız) 2 gün boyunca kontrollü bir sıcaklıkta uyarlayın, pH 7.0-7.4'te akan bir akvaryumda tutun ve günde iki kez besleyin.
NOT: Zebra balıklarında melanin oluşumunun inhibisyonu, vücutlarını morfolojik gözlem için şeffaf tutan kültür ortamına% 0.003'lük bir konsantrasyonda (kütle / hacim) 1-fenil-2-tiyoüre eklenerek elde edildi. - Akşamları yetişkin verimli vahşi tip zebra balıklarını seçin ve çiftleşme kutularında saptırıcılar kullanarak ayırın. Ertesi sabah bölmeleri çıkarın ve balığın 30 dakika yumurtlamasına izin verin. Döllenmiş yumurtaları her 15 dakikada bir damlalık ile topladı. Toplamda, 520 sağlıklı vahşi tip embriyo toplandı. Zebra balığı embriyolarını 24 saat boyunca 28.5 ° C'de bir inkübatörde tutun.
- Döllenme sonrası 24 saatte (hpf) sağlıklı embriyoları rastgele 13 gruba atayın ve bir kontrol grubuyla birlikte, bir kültür kabında aşağıdaki çözeltilerin her birinin 10 mL'sine ayrı ayrı batırın: PEF: 100 μg / mL, 150 μg / mL, 200 μg / mL, 250 μg / mL, 500 μg / mL, 750 μg / mL; CEF: 100 μg/mL, 150 μg/mL, 200 μg/mL, 250 μg/mL, 500 μg/mL, 750 μg/mL. Boş kontrol grubuna bir çözüm olarak ortam ile muamele edin. Bu çalışmada her grup 40 embriyo içeriyordu.
NOT: Orta bileşim 0,15 M NaCl, 5 mM KCl, 0,25 mM Na 2 HPO 4, 0,45 mM KH 2 PO 4, 1,3 mM CaCl 2,1,0 mM MgSO 4 ve4 mM NaHCO3'tür. - Zebra balıklarını 120 hpf'ye kadar sabit bir sıcaklık inkübatöründe kültürleyin. Her gün ölü larvaların sayısını sayın, her deney grubundaki larvaların ana organ morfolojisini stereomikroskop altında gözlemleyin (ölçek çubuğu = 500 μm, Malzeme Tablosuna bakınız) ve zebra balıklarının yarı ölüm konsantrasyonunu (LC50) veri analiz yazılımı kullanarak 72 hpf'de hesaplayın (bkz.
- Vahşi tip zebra balıklarını (Malzeme Tablosuna bakınız) 2 gün boyunca kontrollü bir sıcaklıkta uyarlayın, pH 7.0-7.4'te akan bir akvaryumda tutun ve günde iki kez besleyin.
Sonuçlar
Metodolojik araştırma sonuçları
Icariin, EA, EB, EC, BI konsantrasyonları ile kromatografik tepe alanları arasında doğrusal bir ilişki gözlenmiştir (bakınız Tablo 3). ICARIIN, EA, EB, EC ve BI'nın kromatografik tepe alanlarının RSD% değerleri (n = 6) sırasıyla% 0.28,% 1.22,% 0.65,% 1.67 ve% 1.06 idi ve HPLC ölçümlerinin hassasiyetinin iyi olduğunu gösterdi. ICARIIN, EA, EB, EC ve BI içeriklerinin RSD% değerleri (n = 6) sırasıyla %1.59, %1.46, %1.86, %2.29 ve %0.98 idi ve bu da yöntemin iyi tekrarlanabilirliğe sahip olduğunu gösteriyordu. Örneklerdeki icariin, EA, EB, EC ve BI'nın pik alanlarının RSD% değerleri (n = 6) sırasıyla% 1.49,% 1.96,% 1.42,% 0.96 ve% 0.81 idi ve bu da numune çözeltisinin 24 saat içinde kararlı olduğunu gösterdi. Icariin, EA, EB, EC ve BI'nin ortalama iyileşme oranları sırasıyla %99.98, %100.14, %100.09, %100.75 ve %100.94 ve RSD% değerleri sırasıyla %0.56, %0.78, %0.84, %1.10 ve %1.47 idi (bakınız Tablo 4). Bu sonuçlar, yöntemin doğruluğunun gereksinimleri karşıladığını göstermektedir.
Yukarıdaki deneysel sonuçlar, analitik yöntemin mükemmel hassasiyet, tekrarlanabilirlik ve doğruluğa sahip ve EF ile işlenmiş ürünlerin kalite analizi için kabul edilebilir sonuçlar sağladığını göstermiştir.
EF'nin koyun eti yağı işleme teknolojisinin Box-Behnken tasarım-tepki yüzey metodolojisi uygulanarak optimizasyonu
Aşağıdaki modeli elde etmek için yukarıdaki verilerin ikinci dereceden polinom regresyon uyumunu gerçekleştirdik: Y = 0.86 − 0.11 x A + 0.025 x B − 0.078 x C − 0.023 x A x B − 0.037 x A x C + 0.037 x B x C − 0.045 x A 2 + 2.5 x 10-3 x B 2 − 0.14 x C 2. Varyans analizi, modelin anlamlı olduğunu gösteren P < 0.01 değerini verdi. Uyum eksikliğinin P değeri P > 0.05 idi, bu da uyum eksikliğinin anlamlı olmadığını gösteriyordu. R2 değeri 0.9300 idi, bu da modelin uyumunun iyi olduğunu ve hatanın küçük olduğunu gösteriyordu. Bu modeli, koyun eti yağı ile kızartılmış EF'nin kimyasal bileşim içeriğinin etkisini analiz etmek ve tahmin etmek için kullanmak mümkündü. Ek olarak,A2 ve D2'nin işlenmiş ürünlerin içeriği üzerinde bir etkisi vardı ve fark istatistiksel olarak anlamlıydı (P < 0.01). Bir derecelik dönemin A ve C'sinin ve ikinci dereceden döneminC2'sinin kapsamlı puan üzerindeki etkileri anlamlıydı. Bir derecelik B terimi, ikinci dereceden A 2, B2 ve tüm etkileşim öğelerinin kapsamlı puan üzerinde anlamlı bir etkisi yoktu. P değerlerinin analizi, deneysel parametrelerden, koyun eti yağı miktarının (A) kapsamlı skor üzerinde en büyük etkiye sahip olduğunu, ardından kızartma sıcaklığının (C) ve ardından koyun eti yağı sıcaklığının (B) geldiğini göstermiştir. Yukarıdaki sonuçlar Tablo 5'te gösterilmiştir.
Yazılım, koyun eti yağı miktarını, koyun eti yağı sıcaklığını ve kızartma sıcaklığını medyanlara ayarlamak ve bir faktörün tek faktörlü bir etki diyagramını çizmek için kapsamlı puanı endeks olarak kullanmak için kullanıldı (Şekil 1). Kızartma sıcaklığının arttırılması önce kapsamlı skoru arttırmış, sonra düşürmüştür (Şekil 1). Koyun eti yağı sıcaklığı, kapsamlı skor üzerinde ihmal edilebilir bir etkiye sahipti. Koyun eti yağı miktarı, kapsamlı puandaki değişimi etkileyen ana önemli faktördü ve miktar arttıkça, içerik aşağı doğru eğilim gösterdi.
Sonuçların daha iyi anlaşılmasına yardımcı olmak için, tahmin edilen modeller Şekil 2'de 3B yanıt yüzeyi grafikleri olarak sunulmuştur. Tepki yüzeyinin eğimi açısından, faktörler arasındaki etkileşim etkisinin önemi ne kadar büyük olursa, eğim o kadar yumuşak ve etki o kadar az önemli olur. Kontur çizgisi şeklindeki bir elips, faktörler arasında güçlü bir etkileşimi gösterirken, bir daire bunun tersini gösterir. Koyun eti yağı miktarının ve kızartma sıcaklığının tepki yüzeyi, test edilen diğer faktörlere kıyasla daha dikti ve kontur çizgileri daha eliptik olma eğilimindeydi (bkz. Şekil 2C, D), bu iki faktör arasındaki etkileşimin daha anlamlı olduğunu göstermektedir; Buna karşılık, diğer faktörler arasındaki etkileşimler anlamlı değildi (bkz. Şekil 2A,B,E,F).
EF'nin optimal koyun eti yağı işleme teknolojisi şu şekilde seçilmiştir: koyun eti yağı miktarı% 15; 120 ° C'lik bir koyun eti yağı sıcaklığı; ve 189 °C'lik bir kızartma sıcaklığı. Gerçek çalışmada sıcaklığın çok doğru bir şekilde kontrol edilemediği göz önüne alındığında, sıcaklık değeri değişken ±10 ° C olarak belirtilir. Bu nedenle, nihai parametreler aşağıdaki gibidir:% 15'lik bir koyun eti yağı miktarı; 120 °C ± 10 °C koyun eti yağı sıcaklığı; ve 189 °C ± 10 °C kızartma sıcaklığı. En uygun işlem şu şekildeydi: koyun eti yağını 120 ° C'de 10 ° C'± ısıtmak, ham EF'yi eklemek, eşit derecede parlak olana kadar hafif bir ateşle (189 ° C ± 10 ° C) kızartmak ve çıkarmak ve soğutmak. Her 100 kg EF için 15 kg koyun eti yağı (rafine yağ) kullanılmalıdır. Bu koşullar kullanılarak, üç paralel deney yapıldı ve elde edilen puanlar, kararlı ve uygulanabilir koşulları gösteren 0.96, 0.97 ve 0.94 (RSD% =% 1.60) idi. EF'nin ham, işlenmiş ve karışık referans maddelerinin tipik HPLC kromatogramları Şekil 3'te gösterilmiştir.
İşlemenin zebra balıklarının embriyonik gelişimi üzerindeki etkisinin testi
Zebra balığı 72 hpf'de yavrulara yumurtadan çıktı. Her organın gelişimi temelde tamamlandı. Balık gövdeleri şeffaf kaldı ve onları cam slaytta yanlarına koymak kolaydı. Organların şekillerinin mikroskop altında bakıldığında gözlemlenmesi ve tanımlanması kolaydı. Boş kontrol grubu, uygulama süresi boyunca herhangi bir ölüm veya organ toksisitesi yaşamadı. Kontrol grubuyla karşılaştırıldığında, 100 μg / mL'lik bir ilaç konsantrasyonunda, ham EF grubunda (S) ve işlenmiş grupta (P) 72 hpf'de belirgin bir anormallik bulunmadı. 96 hpf ve sonrasında, yüzme mesane eksikliği ve yüzme mesanesinin kaybı, ham gruptaki yavru balıklarda daha yaygındı, ancak işlenmiş gruptaki yavru balıklarda nadirdi. 150 μg / mL'lik bir ilaç konsantrasyonunda, ham gruptaki yavru balıklarda 72 hpf'de belirgin omurga deformiteleri, vücut eğriliği deformiteleri, perikardiyal ödem ve karaciğer deformasyonu görüldü, ancak bu değişiklikler işlenmiş gruptaki yavru balıklarda nadirdi ve teratojenite derecesi ham grubunkinden daha zayıftı. 200 μg / mL'lik bir ilaç konsantrasyonunda, ham gruptaki tüm yavru balıklar öldü ve işlenmiş gruptaki yavru balıklarda belirgin teratojenite ortaya çıktı. 250 μg / mL'lik bir ilaç konsantrasyonunda, işlenmiş grupta az sayıda zebra balığı hayatta kalmıştır. Zebra balıklarının mikroskobik inceleme sonuçları Şekil 4'te gösterilmiştir.
Ham ve işlenmiş Epimedium bitki gruplarındaki zebra balığı ölüm oranları, uygulamanın konsantrasyonuna ve süresine bağlıydı. Zaman-doz-mortalite ilişkisi Şekil 5'te gösterilmiştir. Zebra balığı mortalite sonuçları, uygulamadan 24 saat sonra (48 hpf), 200 μg / mL'lik bir ilaç konsantrasyonunda, ham ilaç grubundaki tüm zebra balıklarının öldüğünü, oysa işlenmiş gruptaki mortalitenin sadece% 6.67 olduğunu göstermiştir. EF uygulamasından (72 hpf) 48 saat sonra, ham ilaç grubundaki tüm zebra balıklarının ölümüne neden olan konsantrasyon 200 μg / mL ve işlenmiş gruptaki tüm zebra balıklarının ölümüne neden olan konsantrasyon 500 μg / mL idi. İki deney grubunun 72 hpf'deki medyan ölümcül konsantrasyonu hesaplandı. Sonuçlar, LC50'nin (bkz. Şekil 6) ham grupta (S) 151.3 μg / mL ve işlenmiş grupta (P) 219.8 μg / mL olduğunu göstermiştir.

Şekil 1: Tek değişkenli analiz. Şekil tek faktörlü etki diyagramını göstermektedir. A, koyun eti (suet) yağı miktarının tek faktörlü sonucudur; B, koyun eti (suet) yağının sıcaklığının tek faktörlü sonucudur; ve C, kızartma sıcaklığının tek faktörlü sonucudur. Artan kızartma sıcaklığı ile kapsamlı skor önce artar ve sonra azalır. Koyun eti yağı sıcaklığının skor üzerinde çok az etkisi vardır. Koyun eti yağı miktarı, kapsamlı skordaki değişimi etkileyen ana önemli faktördü ve içerik, artan miktarda koyun eti yağı ile düşüş eğilimi gösterdi. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
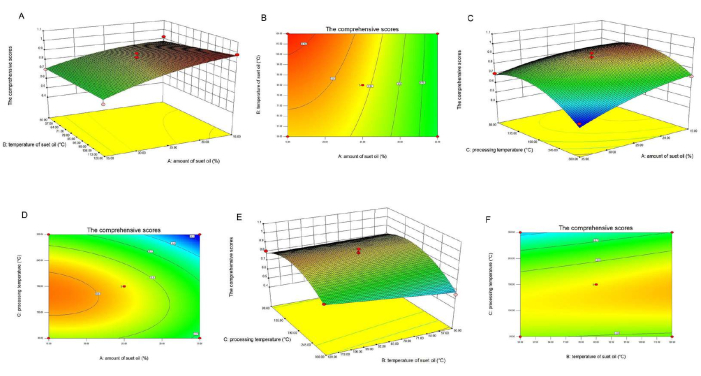
Şekil 2: Farklı faktör etkileşimlerinin kapsamlı skor üzerindeki etkisinin tepki yüzeyi ve kontur grafiği. (A) Bu şekil, koyun eti yağı miktarı ile sıcaklık arasındaki etkileşimin 3B tepki yüzeyi grafiğini göstermektedir. (B) Bu şekil, koyun eti yağı miktarı ile sıcaklık arasındaki etkileşimin kontur grafiğini göstermektedir. (C) Bu şekil, koyun eti yağı miktarı ile işleme sıcaklığı arasındaki etkileşimin 3B tepki yüzeyi grafiğini göstermektedir. (D) Bu şekil, koyun eti yağı dozajı ile işleme sıcaklığı arasındaki etkileşimin kontur grafiğini göstermektedir. (E) Bu şekil, koyun eti yağı miktarı ile işleme sıcaklığı arasındaki etkileşimin 3B tepki yüzey grafiğini göstermektedir. (F) Bu şekil, koyun eti yağı miktarı ile işleme sıcaklığı arasındaki etkileşimin kontur grafiğini göstermektedir. Sonuç, koyun eti yağı miktarının ve kızartma sıcaklığının tepki yüzeyinin test edilen diğer parametrelere göre dik olduğunu ve kontur çizgilerinin eliptik olma eğiliminde olduğunu göstermektedir (bakınız C,D), bu iki faktör arasındaki etkileşimin anlamlı olduğunu, diğer faktörler arasındaki etkileşimlerin ise anlamlı olmadığını göstermektedir (bkz. F). Şekilde kullanılan suet yağı terimi koyun eti yağını ifade eder. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
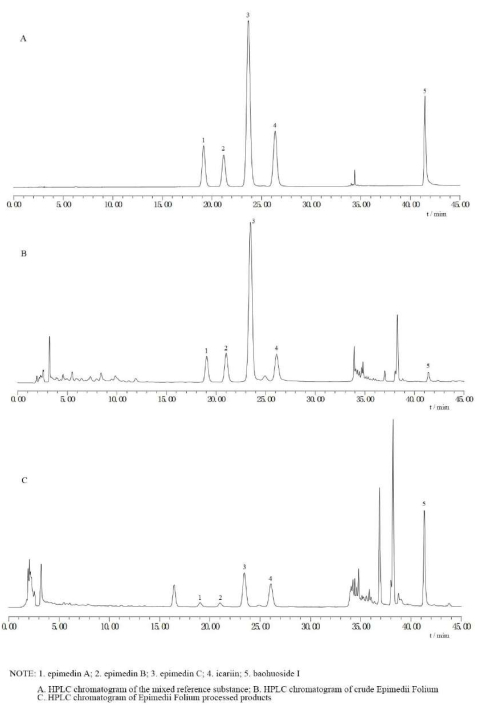
Şekil 3: EF'nin ham, işlenmiş ve karışık referans maddelerinin HPLC kromatogramları . (A) Bu şekil, karışık referans maddenin HPLC kromatogramını göstermektedir. (B) Bu şekil ham Epimedii folyumun HPLC kromatogramını göstermektedir. (C) Bu şekil, Epimedii foliyum işlenmiş ürünlerin HPLC kromatogramını göstermektedir. Bu üç resim, ham EF'deki BI içeriğinin düşük olduğunu, işlendikten sonra ise arttığını göstermektedir. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
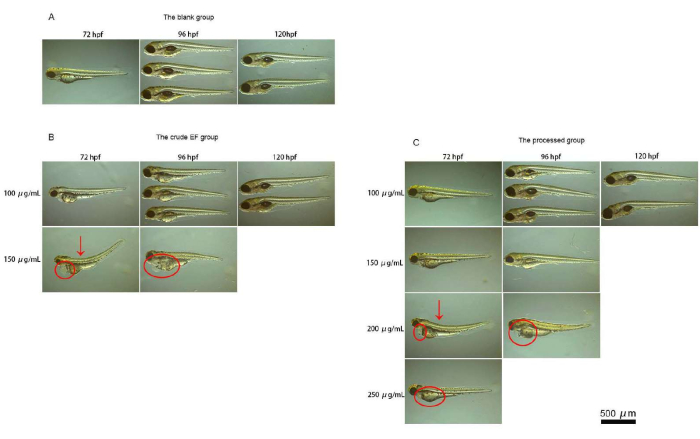
Resim 4: Zebra balığı mikrografları. Bu şekil zebra balıklarının mikrograflarını göstermektedir. (A) Bu şekil, zebra balıklarının boş grupta mikroskop altında gözlemlenmesinin sonuçlarını göstermektedir. (B) Bu şekil, ham gruptaki zebra balıklarının mikroskop altında gözlemlenmesinin sonuçlarını göstermektedir. (C) Bu şekil, zebra balıklarının işlenmiş grupta mikroskop altında gözlemlenmesinin sonuçlarını göstermektedir. Boş kontrol grubu, uygulama süresi boyunca herhangi bir ölüm veya organ toksisitesi yaşamadı. 150 μg / mL'lik bir EF ilaç konsantrasyonunda, ham gruptaki yavru balıklarda 72 hpf'de belirgin omurga deformiteleri, vücut eğriliği, perikardiyal ödem ve karaciğer deformasyonu görülürken, bu değişiklikler işlenmiş gruptaki yavru balıklarda nadirdi ve teratojenite derecesi ham gruptakinden daha zayıftı. 200 μg / mL'lik bir ilaç konsantrasyonunda, ham gruptaki tüm yavru balıklar öldü ve işlenmiş grupta belirgin teratojenite ortaya çıktı. 250 μg / mL'lik bir ilaç konsantrasyonunda, işlenmiş grupta sadece az sayıda zebra balığı hayatta kalmıştır. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.

Şekil 5: Dozlama süresi-doz-mortalite ilişkisi. Bu şekil dozlama süresi-doz-mortalite ilişkisini göstermektedir. (A) Bu şekil, ham grubun dozlama süresi-doz-mortalite ilişkisini göstermektedir. (B) Bu şekil, işlenen grubun dozlama süresi-doz-mortalite ilişkisini göstermektedir. n = 40. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
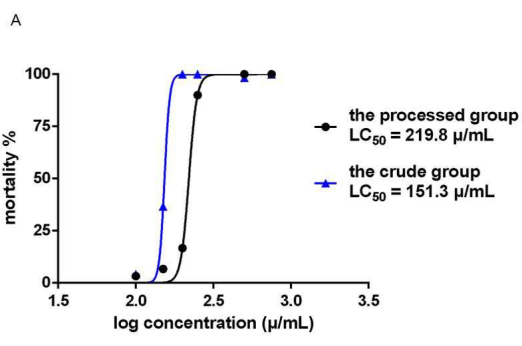
Resim 6: LC50 ham ve işlenmiş EF diyagramı. Ham ve işlenmiş EF'nin LC50 diyagramı gösterilmiştir. İki deney grubunun 72 hpf'deki medyan ölümcül konsantrasyonları hesaplandı. LC50 , ham grupta (S) 151.3 μg / mL ve işleme grubunda (P) 219.8 μg / mL idi. n = 40. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
Tablo 1: 17 deney grubunun deneysel tasarımı ve Box-Behnken tepki yüzeyi yöntemi sonuçları. Tablo 1 , Box-Behnken tasarım-tepki yüzey yöntemi ile tasarlanan 17 deney grubunu ve bunların kapsamlı puan sonuçlarını göstermektedir. Bu Tabloyu indirmek için lütfen tıklayınız.
Tablo 2: Box-Behnken tasarımında kullanılan değişkenler. Bağımsız ve bağımlı değişkenler burada düşük, orta ve yüksek düzeyleriyle birlikte listelenmiştir. Box-Behnken tasarımı, EF işlemede en etkili faktörlerin belirlenmesini sağladı; koyun eti yağı miktarı (A) (% 15 -% 35), koyun eti yağı sıcaklığı (B) (50 ° C-120 ° C) ve kızartma sıcaklığı (C) (80 ° C-300 ° C) etkileyen faktörler olarak. Bu Tabloyu indirmek için lütfen tıklayınız.
Tablo 3: EF'nin kimyasal bileşenlerinin regresyon denklemleri ve doğrusal aralıkları. Regresyon denkleminin ve EF kimyasal bileşiminin doğrusal aralığının sonuçları, icariin, EA, EB, EC ve BI konsantrasyonlarının her biri ile kromatografik tepe alanları arasında iyi bir doğrusallık olduğunu göstermektedir. Bu Tabloyu indirmek için lütfen tıklayınız.
Tablo 4: Örnek kurtarma testi hızları. ICARIIN, EA, EB, EC ve BI'nin ortalama iyileşme oranları sırasıyla% 99.98,% 100.14,% 100.09,% 100.75 ve% 100.94 idi ve RSD% değerleri sırasıyla% 0.56,% 0.78,% 0.84,% 1.10 ve% 1.47 idi. Sonuçlar, yöntemin doğruluğunun uygun olduğunu göstermektedir. Bu Tabloyu indirmek için lütfen tıklayınız.
Tablo 5: Tahmin edilen ikinci dereceden modelin regresyon katsayıları. Modelin P değeri P < 0.01 idi, bu da modelin anlamlı olduğunu gösteriyordu. Uyum eksikliğinin P değeri P > 0.05 idi, bu da uyum eksikliğinin anlamlı olmadığını gösteriyordu. R2 değeri, modelin uyumunun iyi olduğunu ve hatanın küçük olduğunu gösteren 0.9300 idi, bu nedenle model, koyun eti yağı ile kızartılmış EF'nin kimyasal bileşim içeriğinin etkisini analiz etmek ve tahmin etmek için uygundu. Ek olarak, A 2 ve D2'nin işlenmiş ürünlerin içeriği üzerinde önemli etkileri olmuştur (P < 0.01). Bir derecelik terimin A ve C'sinin ve ikinci dereceden terimin C2'sinin kapsamlı puan üzerindeki etkileri anlamlıydı. Bir derecelik B terimi, ikinci dereceden A 2, B2 ve tüm etkileşim öğelerinin kapsamlı puan üzerinde önemli bir etkisi yoktu. P değerinin analizi, deneysel parametrelerden, koyun eti yağı miktarının (A) kapsamlı skor üzerinde en büyük etkiye sahip olduğunu, ardından kızartma sıcaklığının (C) ve ardından koyun eti yağının sıcaklığının (B) geldiğini göstermiştir. Bu Tabloyu indirmek için lütfen tıklayınız.
Tartışmalar
Bağımsız değişkenler ve seviyelerinin belirlenmesi
EF işleme teknolojisi yalnızca Çin Farmakopesinin 2020 baskısında ve ülke genelinde 26 il, belediye ve özerk bölge tarafından yayınlanan yerel Çin tıbbı işleme spesifikasyonlarında açıklanmıştır1. Açıklama aşağıdaki adımları içerir: koyun eti yağı almak ve eritmek için ısıtmak, EF parçaları eklemek, düzgün ve parlak olana kadar yavaş bir ateşle kızartmak, çıkarmak ve soğumaya bırakmak. Ek olarak, her 100 kg Epimedium için 20 kg (% 20 olarak kısaltılır) koyun eti yağı (rafine edilmiş) kullanılır. Ancak, EF'nin işleme sürecinin parametreleri belirtilmemiştir. Bu deneydeki bağımsız değişkenler arasında, üretim sürecinde üç temel faktör ölçülebilir: koyun eti yağı dozajı, koyun eti yağı sıcaklığı ve kızartma sıcaklığı. Değer aralığı yukarıdaki açıklamaya göre ayarlanmalıdır. Ön testin sonuçlarından, koyun eti yağı miktarı% 15 olduğunda, EF yapraklarının koyun eti yağı ile eşit şekilde kaplanabileceği görülebilir. Dozaj% 35'i aştığında, çok fazla koyun eti yağı vardır. Son olarak, koyun eti yağı miktarının aralığı% 15 -% 35 olmalıdır. Sıcaklık 50 ° C'ye ulaştığında, koyun eti yağı erir. Sıcaklık >120 ° C'ye ulaştığında, koyun eti yağı sigara içmeye başlar ve sıcaklık çok yüksektir. Bu nedenle, koyun eti yağının sıcaklık aralığı 50 ° C -120 ° C olmalıdır. Çin Farmakopesi 2020 baskısı, EF'nin yavaş bir ateşle karıştırılarak kızartılmasını şart koşuyor. Yavaş ateş 200 ° C'yi geçmemeli ve kızartma sıcaklığı 80 ° C ile 300 ° C arasında değişmelidir.
Kapsamlı puanlama
Epimedium'un işlenmesi sırasında, glikosidik bağlar kırılır ve glikosidik bileşenler alt glikosidik bileşenlere dönüştürülür. Çin Farmakopesinin 2020 baskısında EF ile işlenmiş ürünlerin içeriğinin belirlenmesi, orijinal tıbbi malzemelerdeki toplam icariin, EA, EB ve EC içeriğinin belirlenmesine dayanmaktadır ve bir monoglikozit bileşeni olan BI, bir gösterge olarak ayrı ayrı listelenmiştir. Bu deneyde, işlenmiş EF'deki icariin, EA, EB ve EC'nin toplam ağırlığı% 50, BI'nın ağırlığı% 50 idi ve kapsamlı puan bu değerlere göre belirlendi.
Yanıt yüzeyi metodolojisi (RSM), optimum proses parametrelerini tanımlamak ve çok değişkenli problemleri çözmek için kullanılan istatistiksel bir tekniktir. Bu teknikte, deneyler yoluyla belirli verileri elde etmek için makul bir deneysel tasarım kullanılır ve faktörler ile yanıtlar arasında işlevsel bir ilişki elde etmek için çok değişkenli ikinci dereceden regresyon denklemi kullanılır22. Tek tip tasarım ve ortogonal tasarım süreci optimizasyonu yaygın olarak kullanılır, ancak test doğruluğu yüksek değildir ve matematiksel model çok öngörülebilir değildir. RSM'nin altında yatan matematiksel model oldukça öngörülebilirdir. RSM daha az deney ve daha kısa döngüler gerektirir, bu da sadece geleneksel matematiksel istatistiklerle ilişkili problemleri ortadan kaldırmakla kalmaz, aynı zamanda faktörler ve yanıtlar arasındaki ilişkileri de açıklığa kavuşturabilir23. RSM, sistemin tepkisini bir veya daha fazla faktörün bir fonksiyonu olarak kavramsallaştırır ve kullanıcının sezgisel görsel gözlemle deneysel tasarımdaki en uygun koşulları seçmesine yardımcı olmak için bu işlevsel ilişkiyi görüntülemek için grafik teknikler kullanır. Bu avantajlar, bu yöntemin kimya endüstrisinde24, biyoloji mühendisliğinde, gıda endüstrisinde25, ilaç endüstrisinde ve TCM preparatlarında yaygın olarak kullanılmasına yol açmıştır.
RSM, yanıtlar (araştırılacak indeksler) ve faktörler (bağımsız değişkenler) arasındaki işlevsel ilişkiyi tanımlayabilse de, yanıt ve faktörler arasında her zaman güçlü bir işlevsel ilişki olmadığından, tüm deneyler yanıt yüzeyi optimizasyonu için uygun değildir. RSM genellikle tüm faktörlerin sürekli değişkenler olmasını gerektiren sürekli işlev ilişkileri elde eder. Bununla birlikte, araştırılacak tüm faktörler sürekli değişkenler değildir veya deneysel tasarımın başlangıcındaki yanıt değerleri üzerinde önemli etkilere sahip değildir. Deney sayısını azaltmak ve yanıt yüzeyi modellemesinin doğruluğunu artırmak için, yanıt yüzeyi tasarım metodolojisini yürütmeden önce faktöriyel tasarım, tekdüze tasarım veya ortogonal tasarım yoluyla önemli faktörleri seçmek ve seviyelerini belirlemek için tarama gereklidir. Yanıt yüzeyi metodolojisinin en büyük avantajı, model doğru bir şekilde kurulduktan sonra, herhangi bir koşul kombinasyonu altındaki yanıt değerinin tahmin edilebilmesi ve işlevsel ilişkinin 3B yanıt yüzeyi aracılığıyla daha sezgisel ve görsel olarak görülebilmesidir. Bu görselleştirme, araştırmacılara en uygun işleme koşullarını bulmada çok yardımcı olur26.
Bu çalışmada, yanıt değeri olarak EF'nin kapsamlı kimyasal içerik skorunu kullanarak 17 kombine deney tasarlamak için RPM'nin Box-Behnken tasarım prensibi kullanılmıştır. Son olarak regresyon analizi ile en iyi süreç optimizasyonu sonuçları elde edilmiştir. İşleme teknolojisi şu şekilde optimize edildi: koyun eti yağını 120 ° C'de 10 ° C'± ısıtmak, ham EF'yi eklemek, eşit derecede parlak olana kadar hafif bir ateşle (189 ° C ± 10 ° C) kızartmak ve daha sonra çıkarmak ve soğutmak. Her 100 kg EF için 15 kg koyun eti yağı (rafine yağ) kullanılmalıdır. Sonuçlarımız, EF sürecinin kararlı, güvenilir ve tekrarlanabilir olduğunu gösterdi. Ek olarak, faktör etkileşimleri analiz edildi ve koyun eti yağı miktarı ile kızartma sıcaklığı arasındaki etkileşim, ancak diğer faktörler arasındaki etkileşimler değil, anlamlıydı. Bu çalışma, faktörler arasındaki etkileşimleri ve faktörler arasındaki ilişkileri ve tepki yüzey değerlerini analiz etmek için bir yöntem olarak tepki yüzeyi tasarımının, minimum sayıda deney ile kısa sürede işleme koşullarının optimizasyonunu sağladığını göstermiştir. Bu çalışmada seçilen faktörler, tek faktörlü tarama deneyinde tanımlanan anahtar faktörlerdi ve düzeyleri bir ön deneyde belirlendi. Test örnekleri, yanıt yüzeyi yönteminin özelliklerine uyuyordu, bu nedenle çalışma, öngörücü bir model oluşturmak için yanıt yüzeyi metodolojisini kullanabildi. Deneysel sonuçlar, işlenmiş EF'nin kalitesini ve homojenliğini geliştirmek için bir referans sağlayabilir.
Zebra balığı embriyoları, gelişimsel genetik alanında model organizmalar olarak kullanılır, çünkü şeffaftırlar, in vitro gelişirler ve gözlemlenmeleri kolaydır27. Gelişimsel toksisite çalışmalarında yaygın olarak kullanılan zebra balığı toksisite göstergeleri arasında embriyonik mortalite, embriyonik malformasyon hızı, yumurta sarısı-kese ödemi, pigment oluşumu, yumurta yoğunlaşması, kuyruk ekstansiyonu, kafa morfolojisi ve vücut segmenti oluşumu sayılabilir28. Memeli toksisitesi değerlendirme teknikleriyle karşılaştırıldığında, zebra balığı embriyolarının bileşik toksisite tespiti için özgüllüğü% 70 -% 80'dir ve duyarlılık% 80'i% 88'i aşmaktadır. Ton ve ark.29 , zebra balığı embriyoları ile teratojenik olmayan bileşiklerin gelişimsel toksisitesini değerlendirmenin doğruluğunun% 75 olduğunu bulmuşlardır. Teratojenik bileşikler burada %100 doğrulukla değerlendirildi. TCM, karmaşık bileşenlerin ve belirsiz hedef toksisite organlarının özelliklerine sahip olmasına rağmen, zebra balığı embriyoları, gelişimsel toksisitenin doğru ve hızlı bir şekilde değerlendirilmesi için deneysel bir hayvan modeli olarak hala kullanılabilir. O ve ark.30 , emodinin zebra balığı embriyolarının hayatta kalma ve kuluçka oranlarını etkilediğini, gövde bükülmesine ve yumurta sarısı kesesi ödemine neden olduğunu bulmuşlardır. Chen ve ark.31 , kaskoninin zebra balığı embriyo perikardiyal ödemi, spinal eğrilik ve yumurta sarısı-kese ödemine neden olduğunu bulmuşlardır. O ve ark.32 , Arnebiae Radix'in tüm gelişim aşamalarında zebra balığı üzerinde ölümcül etkilere sahip olduğunu ve 1.0 mg / L Arnebiae Radix'in embriyonik gelişimi inhibe ettiğini, bunun sonucunda zebra balığı embriyolarında somit sayısının, kuyruk deformitelerinin, vücut bükülmesinin ve melaninin azalmasının sağladığını bulmuşlardır.
Bu çalışmada ham ve işlenmiş EF'nin zebra balığı embriyo gelişimi üzerindeki etkilerini araştırmak amacıyla zebra balığı embriyo gelişimsel toksisite deneyi yapılmıştır. Veriler, LC50 değerlerinin ham grup (S) için 151.3 μg / mL ve işlenen grup (P) için 219.8 μg / mL olduğunu göstermiştir. Her deney grubundaki zebra balığı gövdelerini mikroskopla gözlemlemek, ham grupta belirgin bir zebra balığı teratojenite derecesi gösterdi. Balıkların çoğu, spinal deformite, vücut eğriliği deformitesi, perikardiyal ödem, yüzme mesane eksikliği veya karaciğer deformasyonu dahil olmak üzere değişen derecelerde teratojenite gösterdi ve bu gözlemler işlenmiş grupta nadirdi. Bu deneyler, EF'nin toksisitesinin işlemden sonra önemli ölçüde azaldığını göstermiştir, bu da işlemenin insanlarda ilaç toksisitesini azaltabileceğini düşündürmektedir. Deneysel sonuçlar, koyun eti yağı ile işlenmiş EF'nin klinik ilaç güvenliğini artırmak için bir referans sağlar.
Geleneksel Çin tıbbı, böbreğin işlevinin insan vücudunun büyümesi, gelişmesi ve çoğalması ile yakından ilişkili olduğunu göstermektedir33. Geleneksel Çin tıbbının eski kitapları, böbreğin vücudun kemik iliği olduğunu kaydeder. Böbrek özü depolar ve ilik kemiği beslemek için kemik boşluğunda bulunur. Böbrek özü eksik olduğunda, kemik iliği azalır34. Böbrek yang'ı tonlayan geleneksel Çin tıbbı, bel zayıflığını, osteoporozu, iktidarsızlığı, erken boşalmayı ve uterus soğuk infertilitesini tedavi edebilir35. EF, böbrek yangını tonlamak için temsili tıbbi malzemelerden biridir. Modern farmakolojik çalışmalar, EF'nin iskelet sistemi, bağışıklık sistemi, üreme sistemi, kardiyovasküler sistem ve sinir sistemi üzerinde belirgin etkileri olduğunu ve ayrıca anti-tümör etkilere sahip olduğunu göstermiştir36. İskelet sistemi üzerindeki aktivite açısından, icariin37 , yumurtalık ameliyathaneli sıçanlarda serumE2 seviyesini artırabilir ve yumurtalık ameliyathanesi yapılan sıçanların kemik dokusunda ERβ mRNA ekspresyonunu yukarı regüle edebilir. ERβ sentezi artar, böylece ER'nin biyolojik etkisi iyileştirilir, osteoklastların kemik rezorpsiyon aktivitesi zayıflatılır ve osteoblastların kemik oluşumu arttırılır. Kemik rezorpsiyonundaki değişiklikler, kemik metabolizmasının negatif dengesinden daha büyüktür. Epimedin A, osteoporoz model farelerde osteoklast oluşumunu, farklılaşmasını ve kemik rezorpsiyonunu inhibe ederek ve kemik korunmasında rol oynayarak kemik mikroyapısını ve serum kemik döngüsü belirteçlerini iyileştirebilir38. Epimedin C, esas olarak kemik kütlesini arttırmak ve sonuçta kemik gücünü arttırmak için trabeküler mikroyapıyı iyileştirmek açısından belirgin anti-osteoporoz aktivitesine sahiptir39. Diğer çalışmalar, epimedin B40 ve baohuoside I41'in anti-osteoporoz aktivitesine sahip olduğunu göstermiştir.
Açıklamalar
Yazarlar çıkar çatışması olmadığını beyan ederler.
Teşekkürler
Bu çalışma, Chongqing Geleneksel Çin Tıbbı Akademisi'nin Temel Bilimsel Araştırma İş Projesi (Proje Numarası: jbky20200013), Chongqing Bilimsel Araştırma Kurumlarının Performans Teşvik Rehberlik Projesi (Proje Numarası: cstc2021jxjl 130025) ve Çin Materia Medica İşleme Chongqing Belediye Sağlık Komisyonu Anahtar Disiplin İnşaat Projesi tarafından desteklenmektedir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Acetonitrile | Fisher | 197164 | |
Baohuoside 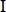 (B (B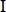 ) ) | Chengdu Manst Biotechnology Co., Ltd. | MUST-20042402 | |
| Chromatographic column | Waters Corporation | Symmetry C18 | |
| Design Expert software | Stat- Ease Inc., Minneapolis, MN | Trial Version8.0.6.1 | |
| Detector | Waters Corporation | 2998 | |
| Disintegrator | Hefei Rongshida Small Household Appliance Co., Ltd. | S-FS553 | |
| Electronic analytical balance | Mettler-Toledo International Inc. | MS205DU | |
| Epimedin A (EA) | Chengdu Manst Biotechnology Co., Ltd. | MUST-21112118 | |
| Epimedin B (EB) | Chengdu Manst Biotechnology Co., Ltd. | MUST-20080403 | |
| Epimedin C (EC) | Chengdu Manst Biotechnology Co., Ltd. | MUST-20080310 | |
| Ethanol | Chongqing Chuandong Chemical ( Group ) Co., Ltd. | 20180801 | |
| Graphpad software | GraphPad Software Inc., San Diego, CA, USA | 6.02 | |
| High Performance Liquid Chromatography (HPLC) | Waters Corporation | 2695 | |
| Icariin | Chengdu Glip Biotechnology Co., Ltd. | 21091401 | |
| Methanol | Chongqing Chuandong Chemical (Group) Co., Ltd. | 20171101 | |
| Microporous membrane | Tianjin Jinteng Experimental Equipment Co., Ltd. | 0.22μm | |
| Mutton oil | Kuoshan Zhiniu Fresh Food Store | 20211106 | |
| Office Excel office software | Microsoft | Office Excel 2021 | |
| Pharmacopoeia sieve | Shaoxing Shangyu Huafeng Hardware Instrument Co., Ltd. | R40/3 | |
| Pure water machine | Chongqing Andersen Environmental Protection Equipment Co., Ltd. | AT Sro 10A | |
| Qualitative filter paper | Shanghai Leigu Instrument Co., Ltd. | 18cm | |
| Stereomicroscope | Carl Zeiss, Oberkochen, Germany | Stemi 2000 | |
| Ultrasonic cleaner | Branson Ultrasonics (Shanghai) Co.,Ltd. | BUG25-12 | |
| Zebrafish | China Zebrafish Resource Center (CZRC) | The AB strain |
Referanslar
- Chinese Pharmacopoeia Commission. . Chinese Pharmacopoeia. Volume I. , (2020).
- Wang, X. T. . Collection of Traditional Chinese Medicine Processing Methods. , (1998).
- Chen, L. L., Jia, X. B., Jia, D. S. Advances in studies on processing mechanism of Epimedii Folium. Chinese Traditional and Herbal Drugs. 12 (12), 2108-2111 (2010).
- Zhao, W., et al. Optimized extraction of polysaccharides from corn silk by pulsed electric field and response surface quadratic design. Journal of The Science of Food and Agriculture. 91 (12), 2201-2209 (2011).
- Zhao, L. C., et al. The use of response surface methodology to optimize the ultrasound-assisted extraction of five anthraquinones from Rheum palmatum L. Molecules. 16 (7), 5928-5937 (2011).
- Mao, W. H., Han, L. J., Shi, B. Optimization of microwave assisted extraction of flavonoid from Radix Astragali using response surface methodology. Separation Science and Technology. 43 (12), 671-681 (2008).
- Liu, W., et al. Optimization of total flavonoid compound extraction from Gynura medica leaf using response surface methodology and chemical composition analysis. International Journal of Molecular Sciences. 11 (11), 4750-4763 (2010).
- Guo, G. L., et al. Research progress on processing mechanism of Epimedium fried with sheep fat oil based on warming kidney and promoting yang. Journal of Liaoning University of TCM. 22 (07), 1-5 (2020).
- Shen, X. J., Zhou, Q., Sun, L. -. L., Dai, Y. -. P., Yan, X. -. S. Optimization for cutting procedure of astragali radix with Box-Behnken design and response surface method. China Journal of Chinese Materia Medica. 39 (13), 2498-2503 (2014).
- Wang, L. H., et al. Optimization of processing technology of honey wheat bran based on Box-Behnken response surface methodology. Chinese Traditional and Herbal Drugs. 52 (12), 3538-3543 (2021).
- Zhang, J. B., et al. Study on integrated process of producing area and processing production for Paeoniae Radix Alba based on Box-Behnken response surface methodology. Chinese Traditional and Herbal Drugs. 53 (18), 5657-5662 (2022).
- Li, N., Zhang, X. M., Yao, Y. Y., Chen, Y. L., Fan, Q. Optimization of processing technology for Psoraleae Fructus by D-optimal response surface methodology with UHPLC. Chinese Traditional and Herbal Drugs. 39 (05), 42-44 (2022).
- Jia, Y. Q., et al. Optimization of processing technology with wine of Cnidii Fructus by AHP-entropy weight method combined with response surface method. Journal of Chinese Medicinal Materials. 10, 2338-2343 (2022).
- Chen, F. G., et al. Optimization of the baked drying technology of Cinnamomi Ramulus based on CRITIC combined with Box-Behnken response surface method. Journal of Chinese Medicinal Materials. 2022 (08), 1838-1842 (2022).
- Wang, W. D., et al. Optimization extraction of effective constituents from Epimedii Herba based on central composite design-response surface methodology and orthogonal experimental design. Lishizhen Medicine and Materia Medica. 21 (11), 2766-2768 (2010).
- Yang, L., et al. Zebrafish embryos as models for embryotoxic and teratological effects of chemicals. Reproductive Toxicology. 28 (2), 245-253 (2009).
- Kanungo, J., Cuevas, E., Ali, S. F., Paule, M. G. Zebrafish model in drug safety assessment. Current Pharmaceutical Design. 20 (34), 5416-5429 (2014).
- Jayasinghe, C. D., Jayawardena, U. A. Toxicity assessment of herbal medicine using zebrafish embryos: A systematic review. Evidence-Based Complementary and Alternative Medicine. 2019, 7272808 (2019).
- Scholz, S. Zebrafish embryos as an alternative model for screening of drug induced organ toxicity. Archives of Toxicology. 87 (5), 767-769 (2013).
- Ling, J., et al. Analysis of Folium Epimedium toxicity in combination with Radix Morindae Officinalis based on zebrafish toxicity/metabolism synchronization. Acta Pharmaceutica Sinica. 53 (1), 74 (2018).
- Wang, Y., et al. Tri-n-butyl phosphate delays tissue repair by dysregulating neutrophil function in zebrafish. Toxicology and Applied Pharmacology. 449, 116114 (2022).
- Sheng, Z. L., Li, J. C., Li, Y. H. Optimization of forsythoside extraction from Forsythia suspensa by Box-Behnken design. African Journal of Biotechnology. 10 (55), 11728-11737 (2011).
- Pang, X., et al. Prenylated flavonoids and dihydrophenanthrenes from the leaves of Epimedium brevicornu and their cytotoxicity against HepG2 cells. Natural Product Research. 32 (19), 2253-2259 (2018).
- Zhong, R., et al. The toxicity and metabolism properties of Herba Epimedii flavonoids on laval and adult zebrafish. Evidence-Based Complementary and Alternative Medicine. 2019, 3745051 (2019).
- Zhang, L., et al. Effect of 2" -O-rhamnosyl icariside II, baohuoside I and baohuoside II in Herba Epimedii on cytotoxicity indices in HL-7702 and HepG2 cells. Molecules. 24 (7), 1263 (2019).
- Chen, Y., Yang, R. J., Yu, M., Ding, S. L., Chen, R. Q. Application of response surface methodology in modern production process optimization. Science & Technology Vision. 2016 (19), 36-39 (2016).
- Zhang, Y., et al. Progress in using zebrafish as a toxicological model for traditional Chinese medicine. Journal of Ethnopharmacology. 282, 114638 (2022).
- Oliveira, R., Domingues, I., Grisolia, C. K., Soares, A. M. V. M. Effects of triclosan on zebrafish early-life stages and adults. Environmental Science and Pollution Research. 16 (6), 679-688 (2009).
- Ton, C., Lin, Y., Willett, C. Zebrafish as a model for developmental neurotoxicity testing. Birth Defects Research. Part A, Clinical and Molecular Teratology. 76 (7), 553-567 (2006).
- He, Q., et al. Toxicity induced by emodin on zebrafish embryos. Drug and Chemical Toxicology. 35 (2), 149-154 (2012).
- Chen, Y., et al. Developmental toxicity of muscone on zebrafish embryos. Chinese Journal of Pharmacology and Toxicology. (6), 267-273 (2014).
- He, Y. L., et al. Effects of shikonin on zebrafish's embryo and angiogenesis. Chinese Traditional Patent Medicine. 38 (2), 241-245 (2016).
- Zhou, Y. . The transformation research on the chemical compositions in the processing of Epimedium. , (2016).
- Xiao, Y. P., Zeng, J., Jiao, L. -. N., Xu, X. -. Y. Review for treatment effect and signaling pathway regulation of kidney-tonifying traditional Chinese medicine on osteoporosis. China Journal of Chinese Materia Medica. 43 (1), 21-30 (2018).
- Wang, R. H. Study on modern pharmacological effects of traditional Chinese medicine for tonifying kidney yang. Journal of Hubei University of Chinese Medicine. 13 (04), 63-66 (2011).
- Luo, L., et al. Advances in the chemical constituents and pharmacological studies of Epimedium. Asia-Pacific Traditional Medicine. 15 (6), 190-194 (2019).
- Liu, S., et al. Effects of icariin on ERβ gene expression and serum estradiol level in ovariectomized rats. Hunan Journal of Traditional Chinese Medicine. 32 (1), 150-152 (2016).
- Liu, Y., et al. Effects of epimedin A on osteoclasts and osteoporotic male mice. Chinese Journal of Veterinary Science. 41 (07), 1359-1364 (2021).
- Liu, Y. L., et al. Effects of icariin and epimedium C on microstructure of bone tissue in glucocorticoid osteoporosis model mice based on Micro-CT technique. Drug Evaluation Research. 43 (09), 1733-1739 (2020).
- Zhan, Y. Evaluation of antiosteoporotic activity for micro amount icariin and epimedin B based on the osteoporosis model using zebrafish. Chinese Pharmaceutical Journal. (24), 30-35 (2014).
- Zhan, Y., Wei, Y. -. J., Sun, E., Xu, F. -. J., Jia, X. -. B. Two-dimensional zebrafish model combined with hyphenated chromatographic techniques for evaluation anti-osteoporosis activity of epimendin A and its metabolite baohuoside I. Acta Pharmaceutica Sinica. 49 (06), 932-937 (2014).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır