Method Article
Síntese de nanopartículas luminescentes persistentes para displays regraváveis e aplicações de iluminação
Neste Artigo
Resumo
Um protocolo é apresentado para a síntese de nanomateriais luminescentes persistentes (PLNPs) e suas potenciais aplicações em displays regraváveis e processamento artístico utilizando o efeito afterglow sob irradiação de luz ultravioleta (365 nm).
Resumo
As nanopartículas luminescentes persistentes (PLNPs) possuem a capacidade de manter a longevidade prolongada e a emissão robusta mesmo após a cessação da excitação. Os PLNPs têm sido amplamente utilizados em vários domínios, incluindo exibições de informações, criptografia de dados, imagens biológicas e decoração artística com luminosidade sustentada e vívida, oferecendo possibilidades ilimitadas para uma variedade de tecnologias inovadoras e projetos artísticos. Este protocolo se concentra em um procedimento experimental para a síntese hidrotérmica de PLNPs. A síntese bem-sucedida de nanomateriais luminescentes duradouros com Mn2+ ou Cr3+ servindo como um centro luminescente em Zn2GeO4: Mn (ZGO: Mn) ou ZnGa2O4: Cr destaca a universalidade deste método sintético. Por outro lado, as propriedades ópticas do ZGO:Mn podem ser alteradas ajustando o pH das soluções precursoras, demonstrando a sintonia do protocolo. Quando carregados com ultravioleta (UV) em um comprimento de onda de 365 nm por 3 min e depois parados, os PLNPs exibem a notável capacidade de gerar brilho residual de forma eficiente e consistente, o que os torna ideais para fazer telas regraváveis bidimensionais e obras de arte luminosas e transparentes tridimensionais. Este protocolo descrito neste artigo fornece um método viável para a síntese de nanopartículas luminescentes persistentes para aplicações adicionais de iluminação e imagem, abrindo novas perspectivas para os campos da ciência e da arte.
Introdução
A luminescência persistente (PL) é um processo óptico exclusivo que pode armazenar energia de luz ultravioleta, luz visível, raios-X ou outras fontes de excitação e, em seguida, liberá-la na forma de emissão de fótons por segundos, minutos, horas ou até mesmo por dias1. A descoberta do fenômeno luminoso contínuo originou-se da dinastia Song na China antiga, há 1000 anos, quando um pintor descobriu acidentalmente uma pintura que brilhava no escuro. Mais tarde, descobriu-se que algumas matérias-primas e minerais naturais podem absorver a luz solar e depois brilhar no escuro e podem até ser transformados em fascinantes pérolas brilhantes2. No entanto, o primeiro registro adequado de fósforos persistentes precisava ser rastreado até a descoberta da emissão de PL da pedra de Bolonha no iníciodo século 17, que emitia um brilho residual amarelo a laranja no escuro 1,2,3,4. Mais tarde, descobriu-se que as impurezas naturais de+ em BaS desempenharam um papel importante nesse fenômeno de luminescência persistente 1,4. Até meados da década de 1990, a produção de fósforos persistentes era amplamente limitada a sulfetos5. Em 1996, Matsuzawa et al. relataram um novo óxido de óxido metálico (SrAl2O4: Eu2+, Dy3+) fósforo mostrando brilho residual extremamente brilhante, o que estimulou muito a expansão da pesquisa de luminescência persistente6.
As propriedades únicas dos materiais luminescentes persistentes são derivadas principalmente de dois tipos de centros ativos: centros de emissão e centros de armadilha 1,7,8. Entre eles, o primeiro determina o comprimento de onda de emissão, enquanto a intensidade e o tempo sustentados são determinados principalmente pelos centros de armadilha. Portanto, o projeto de materiais PL deve levar em consideração ambos os aspectos para atingir o comprimento de onda de emissão desejado e a luminescência de longa duração 9,10. Os centros de emissão podem ser íons lantanídeos com transições 5d para 4f ou 4f para 4f, íons metálicos de transição com transições d para d ou íons metálicos pós-transição com transições p para s 1,11,12,13. Por outro lado, os centros de armadilha são formados por defeitos de rede ou vários co-dopantes14,15, que geralmente não emitem radiação, mas armazenam a energia de excitação por um tempo e depois a liberam gradualmente para o centro emissor por meio de ativação térmica ou outra ativação física16,17. Muitos fósforos com diferentes hospedeiros e íons dopantes foram relatados. Até agora, descobriu-se que compostos metálicos inorgânicos18, estruturas metal-orgânicas8, certos compósitos orgânicos19 e polímeros20 têm propriedades PL. Nos últimos anos, materiais luminescentes persistentes de armadilha profunda com armazenamento de energia controlável e propriedades de liberação de fótons mostraram grandes aplicações potenciais no armazenamento de informações21, antifalsificação multicamada22 e monitores avançados23.
Com base na composição acima, PLNPs com várias matrizes foram projetados e sintetizados com sucesso, como BaZrSi3O97, Y2O2S24, Ca14Mg2(SiO4)825, CaAl2O426, SrAl2O426,27 e Sr2MgSi2O728 com centros luminescentes multidopados, nos quais os centros de luminescência dependem fortemente do efeito do campo cristalino da rede hospedeira, enquanto os defeitos gerados ou melhorados por diferentes dopagem servem como centros auxiliares para controlar a intensidade e duração do brilho residual. Além da codopagem, a emissão de longa duração também pode ser observada no caso de apenas um ativador, como PLNPs heterogêneos com a matriz de Y3Al2Ga3O1229, BaGa2O430, Ca2SnO431, CdSiO332 e Zn3Ga2Ge2O1033. Os óxidos ternários à base de geramato incluem Ca2, Ge7O16, Zn2, GeO4, BaGe4O9, etc., que são materiais semicondutores típicos de banda larga com emissão ajustável, luminescência reprodutível e estável, alto rendimento quântico, respeito ao meio ambiente e ampla disponibilidade 34,35,36. Essas vantagens o tornam um bom portador fotoluminescente do tipo ativador. Nos últimos anos, germanatos com várias microestruturas35,37, foram preparados por reações convencionais de estado sólido ou métodos de solução química, e essas características tornam o Zn2GeO4 útil na esterilização38, anti-falsificação39, catálise40, diodos de luz41, biossensores42, ânodos de bateria43, detectores44,45, etc.
Com o objetivo de expandir a aplicação de materiais PL, foi desenvolvida a síntese controlável de nanopartículas luminescentes uniformes e persistentes. Há uma década, os fósforos persistentes eram sintetizados por síntese em estado sólido46. No entanto, o longo tempo de reação e a alta temperatura de recozimento durante o processo de síntese resultaram em fósforos grandes e irregulares, o que limitou sua aplicação em outros campos, como a biomedicina. Em 2007, Chermont et al. usaram a abordagem sol-gel para sintetizar nanopartículas pela primeira vez e prepararam Ca0,2Zn0,9Mg0,9Si2O6: Eu2+, Dy3+, Mn2+, que abriu a era dos PLNPs47. No entanto, a estratégia de síntese de cima para baixo é acompanhada por problemas como tamanho e morfologia incontroláveis, de modo que os pesquisadores têm trabalhado muito no desenvolvimento de síntese controlável de baixo para cima de PLNPs. Desde 2015, vários métodos de síntese surgiram um após o outro, como o método de síntese de molde, método térmico hidrotérmico/solvente, método sol-gel e outros métodos de síntese química úmida para a síntese de PLNPs uniformes e controláveis 47,48,49,50. Entre eles, a síntese hidrotérmica é um dos métodos mais comumente usados para a preparação de nanomateriais, que pode fornecer um método sintético ajustável e suave para preparar compostos ou materiais com estruturas e propriedades especiais51.
Aqui, apresentamos um procedimento experimental detalhado para sintetizar Zn2GeO4: Mn PLNPs com morfologia de nanobastões 1D através do método hidrotérmico e fornecendo-lhes um ambiente rígido para futuras aplicações de iluminação. Verificou-se que as propriedades de luminescência dos PLNPs, incluindo comprimento de onda de emissão e curva de decaimento de brilho residual, podem ser alteradas ajustando o valor do pH do precursor. Por outro lado, para enfatizar a versatilidade deste método, também sintetizamos PLNPs com Cr como centro luminescente usando ZnGa2O4 como matriz (ZnGa2O4: Cr), que exibe emissão de brilho residual (697 nm) na região do infravermelho próximo após ser excitado por luz ultravioleta (365 nm). Este artigo se concentra principalmente em Zn2GeO4: Mn cujo valor de pH da solução precursora é 9,4 para produção e visualização de obras de arte bidimensionais e tridimensionais. Zn2GeO4: Mn é um tipo de nanomaterial com íons Mn como centro luminescente que obtém forte emissão de luz verde (~ 537 nm) sob a excitação de luz ultravioleta de 365 nm. Ao mesmo tempo, a luz verde contínua ainda pode ser vista após a interrupção da excitação. A fim de promover a polimerização de PLNPs em metacrilato de metila, ligantes (Polietilenoglicol) foram adicionados durante o processo de síntese hidrotérmica e, em seguida, os PLNPs foram polimerizados com metacrilato de metila (MMA) em um molde bidimensional ou tridimensional para que possa formar uma arte brilhante durante a desmoldagem suave.
Este protocolo fornece um método viável para a síntese hidrotérmica, reações de polimerização e aplicações luminescentes de PLNPs em reprodução avançada de cores. Quaisquer diferenças no pH, temperatura e reagentes químicos durante o crescimento dos nanocristais afetarão o tamanho e as propriedades ópticas das nanoestruturas PLNP. Este protocolo detalhado visa ajudar novos pesquisadores na área a melhorar a reprodutibilidade de PLNPs usando um método hidrotérmico para aplicações mais amplas.
Protocolo
1. Síntese de Zn2GeO4: Mn PLNPs
- Prepare a solução de hidróxido de sódio 2 M/L dissolvendo 10 mM de hidróxido de sódio em 5 mL de água deionizada.
- Prepare 0,4 M/L de solução de germanato de sódio adicionando 2 mM de óxido de germânio em 5 mL de solução de hidróxido de sódio e mexa em temperatura ambiente por cerca de 30 min.
- Adicione 4 mM de cloreto de zinco, 0,01 mM de nitrato de manganês e 600 μL de ácido nítrico (65%-68%, em peso) a um béquer pequeno de 100 mL contendo 22 mL de água deionizada.
CUIDADO: A adição de ácido nítrico deve ser rigorosamente realizada em um exaustor e garantir que não haja chamas abertas ou aquecimento ao redor. - Agitar vigorosamente até que a solução do passo 1.3 esteja completamente dissolvida.
- Adicione lentamente 2 mM de solução de germanato de sódio à solução da etapa 1.4. Adicione 1 ml de polietilenoglicol (PEG; 300, Mw) à solução.
- Coloque a sonda calibrada do medidor de pH na solução para monitorar o valor do pH do sistema de reação. Defina uma agitação relativamente suave para evitar respingos da solução e colisão entre a barra de agitação e a sonda.
- Adicione hidróxido de amônio com uma fração de massa de 25% a 28% à solução gota a gota e ajuste o pH da solução para 6,0, 8,0 ou 9,4, dependendo da propriedade de luminescência a ser estudada. Certifique-se de adicionar hidróxido de amônio lentamente e monitorar as mudanças de pH da solução em todos os momentos para evitar que o sistema seja muito ácido ou muito alcalino, de modo a não afetar a morfologia e as propriedades luminescentes dos nanomateriais.
- Cobrir o copo com película de fecho e agitar a solução à temperatura ambiente durante 1 h. Tente não expor o sistema ao ar para evitar que a poeira entre e cause volatilização do solvente, mexendo a uma velocidade constante para que o nível do líquido do sistema não respingue quando o sistema estiver totalmente misturado.
- Transferir a solução para um autoclave revestido de teflon e colocá-la num forno eléctrico de secagem termostática a 220 °C durante 4 h.
NOTA: A autoclave revestida de Teflon apropriada deve ser selecionada de acordo com o volume do sistema e o reator deve ser mantido limpo. O volume das matérias-primas adicionadas não deve exceder 1/3 do volume da autoclave. Ao mesmo tempo, certifique-se de que a autoclave esteja completamente fechada antes de colocá-la no forno elétrico de secagem termostático. - Desligue o forno elétrico de secagem termostática quando a reação estiver concluída e espere que o sistema esfrie até a temperatura ambiente para retirar o reator. Certifique-se de esperar até que o reator esteja completamente resfriado e a pressão seja reduzida a uma faixa segura antes de prosseguir para a próxima etapa para evitar o contato direto entre a alta temperatura e a pele.
- Abra lentamente o reator e transfira a solução de reação para dois tubos de centrífuga de 50 mL. Enxágue o reator com 40 mL de etanol e, em seguida, transfira a solução de etanol para os mesmos tubos de centrífuga.
- Vortex por 30 s para que a solução possa ser misturada uniformemente, depois centrifugue a amostra a 4000 x g por 15 min à temperatura ambiente e remova o sobrenadante.
- Adicione 10 mL de água deionizada a cada tubo de centrífuga e sonice por 5 min (240 W, 40 kHz) para redispersar o produto.
- Adicione 20 mL de etanol em cada tubo de centrífuga e vórtice por 30 s para misturar a solução uniformemente.
- Continue a centrifugar o produto de acordo com a configuração mencionada anteriormente (4000 x g, 15 min) à temperatura ambiente e descarte o sobrenadante.
- Ultrassonicate por 5 min para dispersar o produto em 2 mL de solução de metanol, selar a amostra com filme de vedação e armazená-la em um refrigerador a 4 °C para evitar a contaminação da amostra e a evaporação do solvente para futuras aplicações de iluminação.
2. Síntese de ZnGa2O4: Cr PLNPs
- Dissolver 12 mM de Ga(NO3)3.xH 2O, 7.2 mM de ZnCl2 e 0.024 mM de Cr(NO3)3.9H 2O em 30 mL de água deionizada.
- Adicione 1 mL de PEG (300, Mw) à solução. Adicione hidróxido de amônio (25% -28% em peso) à solução, mexa delicadamente para atingir um pH de 9,0-9,4. Certifique-se de controlar a velocidade de agitação para que a solução possa se misturar completamente sem respingar no medidor de pH.
- Cobrir o copo com uma película de fecho e agitar a solução à temperatura ambiente durante 1 h. Tente minimizar a exposição do sistema ao ar para evitar a entrada de poeira e a evaporação do solvente. Ao mesmo tempo, controle a velocidade de agitação para que o sistema não salpique enquanto mistura bem.
- Transferir a solução para um autoclave revestido de teflon e deixar funcionar a 220 °C durante 6 h. Retire o recipiente depois que a temperatura cair para a temperatura ambiente. Certifique-se de que o vaso de reação esfriou totalmente e a pressão caiu para uma faixa segura antes de prosseguir com as operações subsequentes, bem como evite o contato direto de altas temperaturas com a pele.
- Transferir a solução de reacção para dois tubos de centrifugação de 50 ml. Enxágue o reator com 40 mL de etanol e, em seguida, transfira a solução de etanol para os mesmos tubos de centrífuga.
- Agitar a solução durante 30 s e centrifugar a amostra a 4000 x g durante 15 minutos à temperatura ambiente e remover o sobrenadante.
- Adicione 10 mL de água deionizada a cada tubo de centrífuga e sonice por 5 min para redispersar o produto.
- Adicione 20 mL de etanol em cada tubo de centrífuga e vórtice por 30 s para misturar a solução uniformemente. Continue centrifugando o produto à temperatura ambiente conforme mencionado anteriormente (4000 x g, 15 min) e descarte o sobrenadante.
- Ultrassonicar por 5 min para dispersar o produto em 2 mL de água deionizada e selar a amostra com um filme de vedação para armazenamento.
3. Purificação de matérias-primas
- Purificar o metacrilato de metilo (MMA) por cromatografia em coluna, conforme descrito a seguir.
- Encha metade da coluna com óxido de alumínio alcalino (100-200 mesh) e compacte levemente com uma haste de vidro. Ao encher a coluna com óxido de alumínio, preste atenção à distribuição uniforme e compactação uniforme do enchimento para melhorar a eficiência da separação.
- Adicione uma pequena quantidade de MMA e abra o pistão do acelerador de PTFE abaixo. Assim que a camada de solvente umedecer todo o óxido de alumínio e o líquido fluir, adicione mais MMA e repita esse processo várias vezes. O tempo em que a razão de massa de todo o MMA adicionado ao óxido de alumínio básico é: 1:50 representa o fim do processo.
- Colocar a amostra final de MMA recolhida num frasco de vidro, fechá-la com uma película de fecho e conservar a 4 °C.
CUIDADO: Todo o processo deve ser realizado em capela devido à forte volatilidade do MMA. Ao mesmo tempo, os operadores devem usar máscaras e jalecos.
- Purificar a azobisisobutironitrila (AIBN) por recristalização, conforme descrito abaixo.
- Preparar 50 ml de solução misturada com uma proporção volumétrica de 7:3 de etanol e água destilada e aquecer a solução.
- Adicione 5 g de AIBN quando a solução estiver a ferver e mexa para misturar a solução uniformemente.
- Remova as impurezas insolúveis por filtração a quente, conforme descrito abaixo.
- Coloque o papel de filtro confortavelmente contra a parede interna do funil triangular e certifique-se de que o papel de filtro esteja abaixo da borda do funil.
- Coloque a haste de vidro contra a seção de três camadas do papel de filtro. Se a haste de vidro não for colocada contra a seção de três camadas do papel de filtro, ela pode perfurar o papel de filtro, levando a uma filtragem ineficiente.
- Coloque a ponta do copo que contém a solução perto da haste de vidro e despeje-a enquanto estiver quente. O objetivo desta etapa é evitar respingos de gotículas de líquido.
- Enxágue o béquer com 10 mL de água destilada fria e execute novamente o processo de filtração acima; repita 3x.
- A solução torna-se supersaturada devido à diminuição da solubilidade durante o resfriamento, resultando na precipitação de cristais. Colocar a solução recolhida num frigorífico a 4 °C para arrefecimento e cristalização. A amostra aparecerá no estado de cristais brancos em forma de agulha.
- Selar a amostra com papel alumínio e conservar a 4 °C.
CUIDADO Medidas de proteção devem ser tomadas durante a operação devido à toxicidade do AIBN, evitando também o contato com chamas abertas, altas temperaturas e agentes oxidantes.
4. Copolimerização de metacrilato de metila (MMA)
- Ajuste a temperatura do banho-maria para 80 °C.
NOTA: A temperatura da água tem uma influência severa na taxa de polimerização e, portanto, afeta a formação do produto final. Portanto, a temperatura do banho-maria deve ser estritamente garantida para não ser muito alta. - Pesar 20 g de MMA em um frasco de 100 mL em forma de berinjela. Mantenha o recipiente seco antes do experimento.
NOTA: A garrafa em forma de berinjela é escolhida para facilitar o aquecimento do banho-maria e a substituição do ar por nitrogênio no sistema. Tente pesar a amostra em um ambiente bem ventilado enquanto estiver usando uma máscara. - Adicione a solução de metanol pré-preparada de Zn2GeO4: Mn no recipiente de reação.
- Dissolva completamente a amostra em MMA com a ajuda de ultrassom por cerca de 10 min (240 W, 40 kHz) em temperatura ambiente. Mantenha o recipiente de reação selado para evitar a evaporação do solvente e evite temperaturas excessivamente altas durante o processo de ultrassom.
- Adicionar 0,012 g de AIBN à solução e misturar completamente a solução.
NOTA: O AIBN deve ser usado em condições anidras e garantir que não haja chama aberta ao redor da operação experimental. Certifique-se de usar equipamento de proteção. - Colocar o balão num banho-maria a 80 °C e purgar o ar do sistema de reacção com N2 durante cerca de 35 minutos. Quando a reação estiver prestes a terminar, agite suavemente o recipiente de reação. Se a solução não agitar vigorosamente, isso prova que a reação foi bem-sucedida.
NOTA: O tempo de reação mudará com a temperatura do banho-maria. Certifique-se de que a temperatura do banho-maria atinja 80 °C e comece a cronometrar por 35 min. - Após o término da reação, transfira rapidamente o vaso de reação para um banho de gelo para resfriá-lo rapidamente.
NOTA: Este processo deve ser o mais rápido possível para evitar a pré-polimerização excessiva do MMA, e o banho de gelo pode ser preparado com antecedência durante o intervalo de reação. - Despeje lentamente a solução em um molde bidimensional ou tridimensional, coloque o molde em um forno elétrico de secagem termostática a 40 ° C por 10 h, 70 ° C por 8 h e 100 ° C por mais 2 h para obter o material alvo.
- Feche o forno elétrico de secagem termostática após a interrupção da reação e deixe-o esfriar até a temperatura ambiente. Abra o forno elétrico de secagem termostática para retirar o molde depois que o sistema de reação estiver suficientemente resfriado para evitar queimaduras na pele causadas pelo contato direto entre a alta temperatura e o corpo.
- Remova cuidadosamente o molde e exponha a amostra de PMMA polimerizada (ZGO: Mn-PMMA) a uma lâmpada UV por cerca de 3 min. Por exemplo, ao expor um filme transparente ZGO: Mn-PMMA à luz ultravioleta através de um recorte de papelão preto na forma da letra H, obtém-se um padrão correspondente de emissão fosforescente verde. O padrão pode ser apagado após 5 min. Posteriormente, o processo pode ser repetido usando outro recorte de papelão preto em forma de letras diferentes, gerando novos padrões luminescentes.
Resultados
O diagrama de síntese de PLNPs de Zn2GeO4: Mn (ZGO: Mn) é mostrado na Figura 1. O polímero anfifílico Polietilenoglicol (PEG) é adicionado para modificar os nanobastões de Zn2GeO4: Mn (ZGO: Mn) livres de ligantes para melhor se dissolver em meio MMA. Primeiro, são coletadas as imagens de microscopia eletrônica de transmissão (TEM), microscopia eletrônica de transmissão de alta resolução (HRTEM) de ZGO: Mn cujo pH é 9,4 (Figura 1) e, em seguida, são coletados espalhamento dinâmico de luz (DLS), resultados de potencial zeta e difração de raios X (XRD) de ZGO: Mn (Figura 2). Os espectros de brilho residual e as curvas de decaimento dependentes do tempo de ZGO: Mn com pH diferente (pH = 6,0, 8,0, 9,4) em solução aquosa excitada a 365 nm por 3 min, juntamente com imagens de fotoluminescência e imagens de brilho residual são caracterizados (Figura 3). Obtém-se o TEM, o DRX, os espectros de brilho residual e a curva de atenuação do brilho residual de ZnGa2O4: Cr (Figura 4). O diagrama de copolimerização de ZGO: Mn cujo pH é 9,4 e MMA é mostrado na Figura 5. Os espectros de emissão de brilho residual e a intensidade do brilho residual em função do tempo para o material luminescente baseado em PMMA (ZGO: Mn-PMMA) podem ser obtidos após irradiar os alvos com 365 nm por 3 min e depois cessar a excitação. Materiais de processamento de arte regraváveis e que brilham no escuro em moldes 2D ou 3D podem ser capturados pela câmera após excitação com luz UV a 365 nm por 3 min (Figura 5), o que indica polimerização bem-sucedida de PLNPs em matriz PMMA para aplicações de iluminação.
Para a obtenção de imagens de microscopia eletrônica de transmissão (MET) de alta resolução, as medições foram realizadas em microscópio eletrônico de transmissão operado a uma tensão de aceleração de 200 kV. Um sistema XRD foi usado para caracterizar os dados de difração de raios X (XRD) de PLNPs. Os espectros de emissão de brilho residual e as curvas de decaimento da intensidade do brilho residual em função do tempo foram realizados usando espectrofluorômetro. Uma câmera digital foi usada para registrar imagens de fotoluminescência e luminescência persistente de PLNPs, materiais luminescentes 2D e 3D.
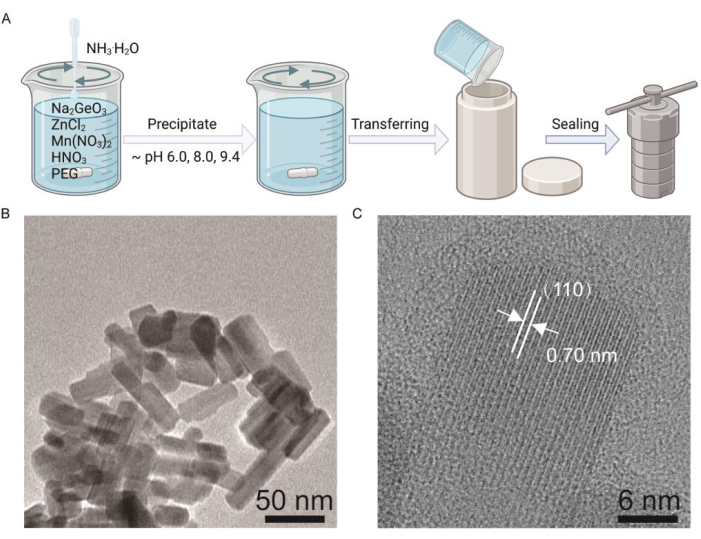
Figura 1: Síntese de Zn2GeO4: Mn (ZGO: Mn) PLNPs. (A) O diagrama de síntese de ZGO: nanobastões de Mn. (B) Microscopia eletrônica de transmissão (TEM) de ZGO: nanoestruturas de Mn cujo pH é 9,4. Barra de escala: 50 nm. (C) Imagem de microscopia eletrônica de transmissão de alta resolução (HRTEM) de ZGO: Mn cujo pH é 9,4. Barra de escala: 6 nm. Clique aqui para ver uma versão maior desta figura.

Figura 2: Síntese de nanoestruturas funcionais de Zn2GeO4: Mn. (A) Análise dinâmica de espalhamento de luz (DLS) de Zn2GeO4: Mn-Polietilenoglicol (ZGO: Mn-PEG) disperso em água deionizada e uma função log-normal ajustada para obter a distribuição de tamanho. (B) Resultados potenciais Zeta de ZGO: Mn-PEG. (C) Análise de difração de raios X (XRD) de Zn2GeO4: Mn. Clique aqui para ver uma versão maior desta figura.
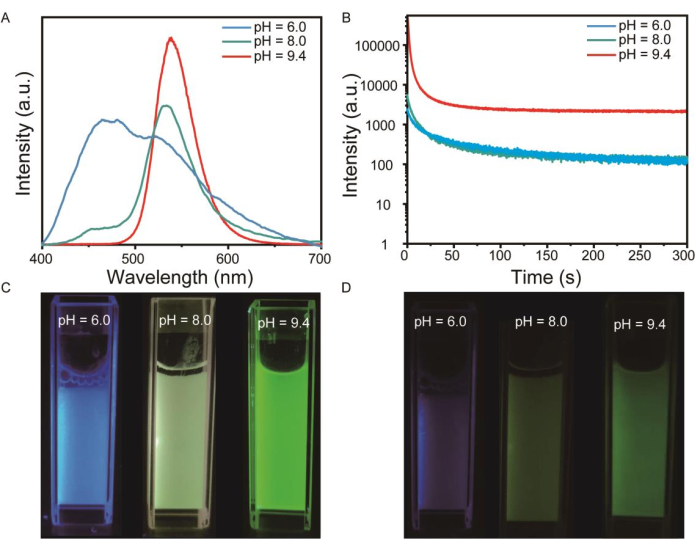
Figura 3: Caracterização de ZGO: Mn em solução aquosa. (A) Os espectros de emissão de brilho residual de ZGO: Mn-PEG com pH diferente (pH = 6,0, 8,0, 9,4) excitados por 365 nm por 3 min. (B) Curva de decaimento de brilho residual dependente do tempo de ZGO: Mn em água a 537 nm (excitado com luz UV de 365 nm por 3 min). (C) Imagens de fotoluminescência de ZGO: nanobastões de Mn. (D) Imagens de decaimento de luminescência de brilho residual de ZGO: Mn. Clique aqui para ver uma versão maior desta figura.
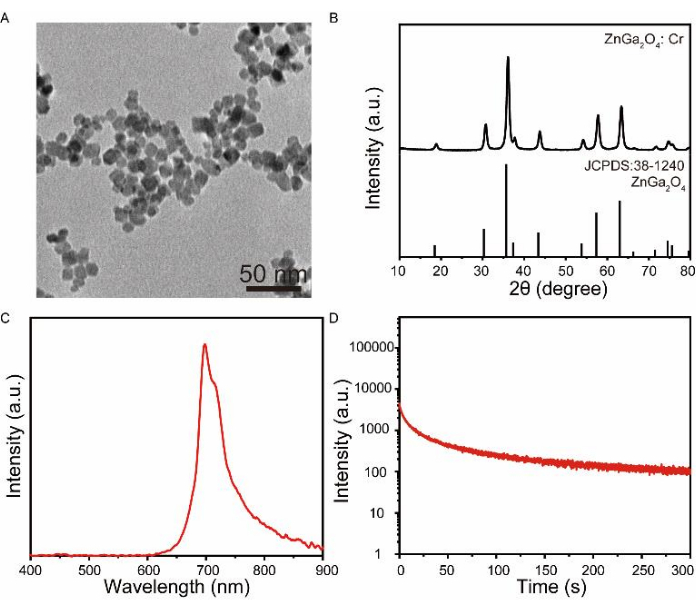
Figura 4: Caracterização de ZnGa2O4: Cr em solução aquosa. (A) Imagens TEM de ZnGa2O4: nanopartículas de Cr. Barra de escala: 50 nm. (B) Análise XRD de ZnGa2O4: Cr. (C) O espectro de emissão de brilho residual de ZnGa2O4: Cr após 3 min de excitação a 365 nm. (D) Curva de decaimento do brilho residual dependente do tempo de ZnGa2O4: Cr em água a 697 nm. Clique aqui para ver uma versão maior desta figura.

Figura 5: PLNPs para aplicações de exibição regravável e iluminação 3D. (A) Diagrama esquemático da reação de copolimerização entre ZGO: Mn cujo pH é 9,4 e metacrilato de metila (MMA). (B) O espectro de emissão de brilho residual de ZGO: Mn-PMMA excitado por 365 nm por 3 min. (C) A variação da intensidade do brilho residual ao longo do tempo de ZGO: Mn-PMMA a 537 nm (excitado com luz UV de 365 nm por 3 min). (D) Brilho residual fotoativado para exibição regravável e armazenamento de dados (gravado por irradiação UV). (E) Fotografias de luminescência de pato 3D transparente com ZGO: Mn-PMMA após irradiação UV. Clique aqui para ver uma versão maior desta figura.
Discussão
Este artigo apresenta um método de síntese para nanomateriais luminescentes persistentes e polimerização para aplicações de reprodução de cores. Os materiais mostraram propriedades ópticas extremamente estáveis e um brilho residual visível após a cessação da excitação da luz ultravioleta. Um nanomaterial luminescente persistente (Zn2GeO4: Mn) foi preparado usando um método hidrotérmico com pH diferente (Figura 1A). A imagem TEM mostrou que ZGO: Mn PLNPs cujo pH é 9,4 eram em forma de bastonete com um diâmetro médio de cerca de 65 nm (Figura 1B). As imagens MET de alta resolução mostraram boa cristalinidade dos nanomateriais, e o espaçamento das franjas de rede adjacentes paralelas à direção da haste foi de 0,70 nm, o que estava em boa concordância com o espaçamento plano (110) de Zn2GeO452, indicando que todo Zn2GeO4: Mn era altamente cristalino (Figura 1C).
Além disso, os dados de espalhamento dinâmico de luz (DLS) de ZGO: Mn em água deionizada ajustada por uma função log-normal mostraram que o tamanho hidrodinâmico calculado era de 63 nm de diâmetro e bem disperso (Figura 2A). Os resultados do potencial zeta também mostraram uma superfície negativa de ZGO:Mn (Figura 2B), indicando que os PLNPs apresentaram boa solubilidade e estabilidade em solução aquosa. O espectro XRD de ZGO: Mn pode ser atribuído à fase romboédrica de Zn2GeO4 (Figura 2C).
As propriedades ópticas dos PLNPs podem ser alteradas ajustando o pH da solução precursora. Os espectros de emissão visível de brilho residual da solução de ZGO: Mn excitada a 365 nm por 3 min mostraram que os PLNPs exibiram um desvio para o vermelho do pico de emissão principal quando a solução precursora mudou de ácida para alcalina (Figura 3A). A curva de decaimento da intensidade do afterglow ao longo do tempo também foi afetada pelo valor do pH, mas em qualquer caso, a intensidade da emissão ainda pode ser detectada quando o tempo de afterglow atingiu 300 s, o que verificou a síntese bem-sucedida de PLNPs com diferentes propriedades ópticas (Figura 3B). As imagens de fotoluminescência (Figura 3C) e imagens de brilho residual (Figura 3D) de PLNPs com diferentes níveis de pH foram capturadas pela câmera. Os resultados revelaram que a solução exibiu uma luminescência verde mais brilhante à medida que a alcalinidade da solução aumentava.
PLNPs com ZnGa2O4 como matriz e Cr como centro de luminescência (ZnGa2O4: Cr) foram sintetizados a fim de destacar a versatilidade deste método hidrotermal. A imagem TEM mostrou que ZnGa2O4: Cr era menor em tamanho e uniformemente disperso (Figura 4A). Os resultados do XRD indicaram que todos os picos de difração combinaram bem com os do espinélio cúbico ZnGa2O4 (Figura 4B). O espectro de emissão de brilho residual mostrou que ZnGa2O4: Cr exibiu emissão óbvia de infravermelho próximo após ser excitado por luz ultravioleta por 3 min (Figura 4C). A intensidade de emissão de ZnGa2O4: Cr a 697 nm foi monitorada ao longo do tempo, e os resultados mostraram que a emissão de brilho residual ainda pode ser coletada após 300 s (Figura 4D).
Existem várias etapas importantes na síntese hidrotermal de PLNPs. Primeiro, é necessário controlar rigorosamente o pH da solução aquosa durante a síntese de PLNPs. A acidez e a alcalinidade da solução podem ter um efeito dramático na persistência do arrebol e até mesmo na cor do resplendor. Em segundo lugar, ao monitorar o pH da solução, é importante ajustar a velocidade de agitação apropriada para garantir que o agitador não colida com a sonda de pH enquanto a solução está sendo misturada uniformemente. Finalmente, quando a solução for agitada por 1 h em um ambiente com pH alvo, mantenha o sistema de reação selado o máximo possível para evitar a influência da volatilização da água de amônia.
Além disso, obras de arte luminosas bidimensionais e tridimensionais são copolimerizadas por PLNPs e MMA para tornar os PLNPs mais funcionais (Figura 5A). Verificou-se que, seja um filme ou um pato tridimensional, o material apresenta boa capacidade de brilho residual (Figura 5B, C). Os materiais 2D e 3D exibem luminescência verde brilhante após a cessação da excitação da luz ultravioleta, e as imagens de brilho residual verde ainda podem ser vistas após 5s (Figura 4D, E), o que indica que os PLNPs podem gerar brilho residual eficaz sob a ativação da lâmpada UV.
Alguns processos precisam ser observados ao realizar a polimerização do MMA. Primeiro, as matérias-primas, ou seja, MMA e AIBN, precisam ser purificadas para não afetar a polimerização. A segunda, ao adicionar metanol disperso Zn2GeO4: Mn na solução de MMA, dispersa por ultrassom todo o sistema uniformemente. Terceiro, lembre-se de observar o estado da solução o tempo todo. Isso significa que a pré-polimerização é bem-sucedida se o balanço do frasco causar apenas uma leve agitação da solução. Quarto, o frasco deve ser banhado em gelo imediatamente após a pré-polimerização para evitar polimerização excessiva. Finalmente, a temperatura deve ser programada durante a reação de polimerização no forno de secagem termostático elétrico para formar uma matriz homogênea.
Em resumo, esperamos que este protocolo não apenas forneça um procedimento experimental detalhado para a síntese hidrotérmica de nanomateriais de emissão de longa duração, mas também introduza um método para a copolimerização de PLNPs e MMA para alcançar ainda mais aplicações regraváveis e luminescentes mediadas por UV. Mais importante, as propriedades ópticas dos PLNPs podem ser ajustadas para ter várias cores de brilho residual, ajustando diferentes defeitos, centros luminescentes e valores de pH com base neste método. Além disso, o método de copolimerização de PLNPs e polímeros pode ser usado na produção de arte. Essas vantagens tornam os PLNPs materiais ideais para aplicações de luminescência e imagem. Por outro lado, o método de síntese hidrotérmica pode limitar a aplicação de certos materiais, especialmente substâncias sensíveis à temperatura, uma vez que a reação requer temperaturas relativamente altas. Portanto, o método de síntese apropriado precisa ser selecionado com base em aplicações e requisitos específicos.
Divulgações
Não há nada a divulgar.
Agradecimentos
Os autores agradecem o financiamento da Fundação Nacional de Ciências Naturais da China (82001945), o Programa Shanghai Pujiang (20PJ1410700) e a concessão inicial da ShanghaiTech University. Os autores agradecem ao Centro de Microscopia Eletrônica de Alta Resolução (ChEM), Escola de Ciências Físicas e Tecnologia, Universidade ShanghaiTech (No. EM02161943) para o suporte à caracterização do material. Os autores agradecem ao Centro de Instrumentação Analítica (#SPST-AIC10112914), Escola de Ciências Físicas e Tecnologia, Universidade ShanghaiTech pelo suporte ao teste espectral e suporte ao teste XRD. Os autores também agradecem ao Prof. Jianfeng Li pela ajuda com as caracterizações do material.
Materiais
| Name | Company | Catalog Number | Comments |
| azobisisobutyronitrile (99%) | Macklin | A800354 | Further purification required |
| methyl methacrylate(99%) | Sigma-Aldrich | M55909 | Further purification required |
| deionized water | Merck | ZEQ7016T0C | Milli-Q Direct Water Purification System |
| alkaline aluminum oxide (100-200 mesh) | Macklin | A800033 | |
| ammonium hydroxide (25%-28%, wt) | Macklin | A801005 | |
| beaker | Synthware | B220100 | |
| chromium(III) nitrate nonahydrate (99.95%) | Aladdin | C116448 | |
| centrifuge | ThermoFisher Scientific | 75004250 | |
| column | Synthware | C184464CR | |
| digital camera | Canon | EOS M50 Mark II | |
| electric thermostaticdrying oven | Longyue | LDO-9036A | |
| ethanol (99.7%) | Greagent | 1158566 | |
| gallium nitrate hydrate(99.9%) | Aladdin | G109501 | |
| germanium oxide (99.99%) | Sinopharm Chemical ReagentCo., Ltd | 51009860 | |
| glass rod | Sinopharm Chemical ReagentCo., Ltd | 91229401 | |
| powder X-Ray Diffractometer | D2 PHASER DESKTOP XRD | BRUKER | |
| manganese nitrate (98%) | Macklin | M828399 | |
| methanol (99.5%) | Greagent | 1226426 | |
| nitric acid (65.0-68.0%, wt) | Sinopharm Chemical ReagentCo., Ltd | 10014508 | |
| pH meter | Shanghai Leici Sensor Technology Co., Ltd | PHS-3C | |
| polyethylene glycol (300, Mw) | Adamas | 01050882(41713A) | |
| sealing film | Parafilm | 2025722 | |
| sodium hydroxide (GR) | Sinopharm Chemical ReagentCo., Ltd | 10019764 | |
| spectrometer | Horiba | Fluorolog-3 | |
| transmission electron microscope | JEOL | JEM-1400 Plus | |
| transmission electron microscope | JEOL | 2100 Plus | |
| triangular funnel | Synthware | F181975 | |
| ultrasound machine | centrifuge | JP-040S | |
| zinc chloride (98%) | Greagent | 01113266/G81783A |
Referências
- Xu, J., Tanabe, S. Persistent luminescence instead of phosphorescence: History, mechanism, and perspective. J Luminesc. 205, 581-620 (2019).
- Harvey, E. N. A history of luminescence from the earliest times until 1900. , American Philosophical Society. Philadelphia, USA. (1957).
- Hölsä, J. Persistent luminescence beats the afterglow: 400 years of persistent luminescence. Electrochem Soc Interface. 18 (4), 42(2009).
- Lastusaari, M., et al. The Bologna stone: history's first persistent luminescent material. Euro J Mineral. 24 (5), 885-890 (2012).
- Liu, Y., Kuang, J., Lei, B., Shi, C. Color-control of long-lasting phosphorescence (LLP) through rare earth ion-doped cadmium metasilicate phosphors. J Mater Chem. 15 (37), 4025-4031 (2005).
- Matsuzawa, T., Aoki, Y., Takeuchi, N., Murayama, Y. A new long phosphorescent phosphor with high brightness, SrAl2O4:Eu2+, Dy3+. J Electrochem Soc. 143 (8), 2670(1996).
- Guo, H., et al. Cyan emissive super-persistent luminescence and thermoluminescence in BaZrSi3O9:Eu2+,Pr3+ phosphors. J Mater Chem C. 5 (11), 2844-2851 (2017).
- Yuan, J., Dong, J., Lei, S., Hu, W. Long afterglow MOFs: a frontier study on synthesis and applications. Mater Chem Front. 5 (18), 6824-6849 (2021).
- Fu, X., Zheng, S., Shi, J., Li, Y., Zhang, H. Long persistent luminescence property of a novel green emitting SrLaGaO4 : Tb3+ phosphor. J Luminesc. 184, 199-204 (2017).
- Zhuang, Y., Wang, L., Lv, Y., Zhou, T. L., Xie, R. J. Optical data storage and multicolor emission readout on flexible films using deep-trap persistent luminescence materials. Adv Func Mater. 28 (8), 1705769(2018).
- Singh, S. K. Red and near infrared persistent luminescence nano-probes for bioimaging and targeting applications. RSC Adv. 4 (102), 58674-58698 (2014).
- Matuszewska, C., Elzbieciak-Piecka, K., Marciniak, L. Transition metal ion-based nanocrystalline luminescent thermometry in SrTiO3:Ni2+,Er3+ nanocrystals operating in the second optical window of biological tissues. J Phys Chem C. 123 (30), 18646-18653 (2019).
- Zhuang, Y., Katayama, Y., Ueda, J., Tanabe, S. A brief review on red to near-infrared persistent luminescence in transition-metal-activated phosphors. Optic Mater. 36 (11), 1907-1912 (2014).
- Norrbo, I., et al. Lanthanide and heavy metal free long white persistent luminescence from Ti doped Li-hackmanite: A versatile, low-cost material. Adv Func Mater. 27 (17), 1606547(2017).
- Hoang, K. Defects and persistent luminescence in Eu-doped SrAl2O4. Phys Rev Appl. 19 (2), 024060(2023).
- Viana, B., et al. Long term in vivo imaging with Cr3+ doped spinel nanoparticles exhibiting persistent luminescence. J Luminesc. 170 (3), 879-887 (2016).
- Ding, Y., So, B., Cao, J., Langenhorst, F., Wondraczek, L. Light delivery, acoustic read-out, and optical thermometry using ultrasound-induced mechanoluminescence and the near-infrared persistent luminescence of CaZnOS:Nd3. Adv Optic Mater. 11 (17), 2300331(2023).
- Ge, S., et al. Realizing color-tunable and time-dependent ultralong afterglow emission in antimony-doped CsCdCl3 metal halide for advanced anti-counterfeiting and information encryption. Adv Optic Mater. 11 (14), 2300323(2023).
- Zhai, L., Ren, X. M., Xu, Q. Carbogenic π-conjugated domains as the origin of afterglow emissions in carbon dot-based organic composite films. Mater Chem Front. 5 (11), 4272-4279 (2021).
- Miao, Q., et al. Molecular afterglow imaging with bright, biodegradable polymer nanoparticles. Nat Biotechnol. 35 (11), 1102-1110 (2017).
- Zhou, B., Xiao, G., Yan, D. Boosting wide-range tunable long-afterglow in 1D metal-organic halide micro/nanocrystals for space/time-resolved information photonics. Adv Mater. 33 (16), e2007571(2021).
- Yang, H., et al. Highly flexible dual-mode anti-counterfeiting designs based on tunable multi-band emissions and afterglow from chromium-doped aluminates. J Mater Chem C. 8 (46), 16533-16541 (2020).
- Chen, Y., et al. Synaptic plasticity powering long-afterglow organic light-emitting transistors. Adv Mater. 33 (39), e2103369(2021).
- Qu, B., Wang, J., Liu, K., Zhou, R., Wang, L. A comprehensive study of the red persistent luminescence mechanism of Y2O2S:Eu,Ti,Mg. Phys Chem Chem Phys. 21 (45), 25118-25125 (2019).
- Zhang, J., Jiang, C. Luminescence properties of Ca14 Mg2(SiO4)8 :Eu2+ from various Eu2+ sites for white-light-emitting diodes. Mater Res Bull. 60, 467-473 (2014).
- Yamamoto, H., Matsuzawa, T. Mechanism of long phosphorescence of SrAl2O4: Eu2+, Dy3+ and CaAl2O4 Eu2+, Nd3+. J Luminesc. 72-74, 287-289 (1997).
- Rojas-Hernandez, R. E., Rubio-Marcos, F., Rodriguez, M. Á, Fernandez, J. F. Long lasting phosphors: SrAl2O4:Eu, Dy as the most studied material. Renew Sustain Ener Rev. 81 (2), 2759-2770 (2018).
- Lin, Y., Tang, Z., Zhang, Z., Wang, X., Zhang, J. Preparation of a new long afterglow blue-emitting Sr2MgSi2O7-based photoluminescent phosphor. J Mater Sci Lett. 20, 1505-1506 (2001).
- Katayama, Y., Viana, B., Gourier, D., Xu, J., Tanabe, S. Photostimulation induced persistent luminescence in Y3Al2Ga3O12:Cr3. Optic Mater Exp. 6 (4), 1405-1413 (2016).
- Li, H., et al. A strategy for developing thermal-quenching-resistant emission and super-long persistent luminescence in BaGa2O4:Bi3+. J Mater Chem C. 7 (42), 13088-13096 (2019).
- Lei, B., et al. Luminescent properties of orange-emitting long-lasting phosphorescence phosphor Ca2SnO4:Sm3. Solid State Sci. 13 (3), 525-528 (2011).
- Lei, B., Liu, Y., Ye, Z., Shi, C. Luminescence properties of CdSiO3:Mn2+ phosphor. J Luminesc. 109 (3-4), 215-219 (2004).
- Wu, Y., et al. Near-infrared long-persistent phosphor of Zn3Ga2Ge2O10: Cr3+ sintered in different atmosphere. Spectrochim Acta A Mol Biomol Spectrosc. 151, 385-389 (2015).
- Zhang, S., Hu, Y. Photoluminescence spectroscopies and temperature-dependent luminescence of Mn4+ in BaGe4O9 phosphor. J Luminesc. 177, 394-401 (2016).
- Wang, J., et al. One-dimensional luminous nanorods featuring tunable persistent luminescence for autofluorescence-free biosensing. ACS Nano. 11 (8), 8185-8191 (2017).
- Wang, T., Xu, X., Zhou, D., Qiu, J., Yu, X. Red phosphor Ca2Ge7O16:Eu3+ for potential application in field emission displays and white light-emitting diodes. Mater Res Bull. 60, 876-881 (2014).
- Ding, D., et al. X-ray-activated simultaneous near-infrared and short-wave infrared persistent luminescence imaging for long-term tracking of drug delivery. ACS Appl Mater Interfaces. 13 (14), 16166-16172 (2021).
- Zhao, X., Wei, X., Chen, L. J., Yan, X. P. Bacterial microenvironment-responsive dual-channel smart imaging-guided on-demand self-regulated photodynamic/chemodynamic synergistic sterilization and wound healing. Biomater Sci. 10 (11), 2907-2916 (2022).
- Huang, K., et al. Enhancing light and X-ray charging in persistent luminescence nanocrystals for orthogonal afterglow anti-counterfeiting. Adv Func Mater. 31 (22), 2009920(2021).
- Sun, L., Qi, Y., Jia, C. J., Jin, Z., Fan, W. Enhanced visible-light photocatalytic activity of g-C3N4/Zn2GeO4 heterojunctions with effective interfaces based on band match. Nanoscale. 6 (5), 2649-2659 (2014).
- Gupta, S. K., Sudarshan, K., Modak, B., Gupta, R. Interstitial zinc boosted light tunability, afterglow, and ultrabright white emission in zinc germanate (Zn2GeO4). ACS Appl Electron Mater. 5 (2), 1286-1294 (2023).
- Calderón-Olvera, R. M., et al. Persistent Luminescence Zn2GeO4:Mn2+ nanoparticles functionalized with polyacrylic acid: One-pot synthesis and biosensing applications. ACS Appl Mater Interfaces. 15 (17), 20613-20624 (2023).
- Li, Q., Miao, X., Wang, C., Yin, L. Three-dimensional Mn-doped Zn2GeO4 nanosheet array hierarchical nanostructures anchored on porous Ni foam as binder-free and carbon-free lithium-ion battery anodes with enhanced electrochemical performance. J Mater Chem A. 3 (42), 21328-21336 (2015).
- Lai, B., et al. A phosphorescence resonance energy transfer-based "off-on" long afterglow aptasensor for cadmium detection in food samples. Talanta. 232, 122409(2021).
- Chi, F., et al. Multimodal temperature sensing using Zn2GeO4:Mn2+ phosphor as highly sensitive luminescent thermometer. Sens Actuat B: Chem. 296, 126640(2019).
- Yin, S., Chen, D., Tang, W., Peng, Y. Synthesis of CaTiO3:Pr persistent phosphors by a modified solid-state reaction. Mater Sci Eng: B. 136 (2-3), 193-196 (2007).
- le Masne de Chermont, Q., et al. Nanoprobes with near-infrared persistent luminescence for in vivo imaging. Proc Natl Acad Sci U S A. 104 (22), 9266-9271 (2007).
- Li, Z., Shi, J., Zhang, H., Sun, M. Highly controllable synthesis of near-infrared persistent luminescence SiO2/CaMgSi2O6 composite nanospheres for imaging in vivo. Opt Express. 22 (9), 10509-10518 (2014).
- Sera, M., et al. Morphology control and synthesis of afterglow materials with a SrAl2O4 framework synthesized by Surfactant-Template and hydrothermal methods. Chem Phys Lett. 780, 138916(2021).
- Kim, J., Lee, C. K., Kim, Y. J. Low temperature synthesis of Lu3Al5-xGaxO12:Ce3+,Cr3+ powders using a sol-gel combustion process and its persistent luminescence properties. Optic Mat. 104, 109944(2020).
- Xu, Z., et al. Ln(3+) (Ln = Eu, Dy, Sm, and Er) ion-doped YVO(4) nano/microcrystals with multiform morphologies: hydrothermal synthesis, growing mechanism, and luminescent properties. Inorg Chem. 49 (4), 6706-6715 (2010).
- Wang, Y., et al. Zn2GeO4−x/ZnS heterojunctions fabricated via in situ etching sulfurization for Pt-free photocatalytic hydrogen evolution: interface roughness and defect engineering. Phys Chem Chem Phys. 22 (18), 10265-10277 (2020).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados