Method Article
Sintesi di nanoparticelle luminescenti persistenti per display riscrivibili e applicazioni di illuminazione
In questo articolo
Riepilogo
Viene presentato un protocollo per la sintesi di nanomateriali luminescenti persistenti (PLNP) e le loro potenziali applicazioni in display riscrivibili e processi artistici utilizzando l'effetto afterglow sotto irradiazione di luce ultravioletta (365 nm).
Abstract
Le nanoparticelle luminescenti persistenti (PLNP) possiedono la capacità di mantenere una longevità estesa e un'emissione robusta anche dopo che l'eccitazione è cessata. I PLNP sono stati ampiamente utilizzati in vari settori, tra cui la visualizzazione delle informazioni, la crittografia dei dati, l'imaging biologico e la decorazione artistica con una luminosità sostenuta e vivida, offrendo possibilità illimitate per una varietà di tecnologie innovative e progetti artistici. Questo protocollo si concentra su una procedura sperimentale per la sintesi idrotermale di PLNP. La riuscita sintesi di nanomateriali luminescenti duraturi con Mn2+ o Cr3+ che fungono da centro luminescente in Zn2GeO4: Mn (ZGO: Mn) o ZnGa2O4: Cr evidenzia l'universalità di questo metodo sintetico. D'altra parte, le proprietà ottiche di ZGO: Mn possono essere modificate regolando il pH delle soluzioni precursori, dimostrando la sintonizzabilità del protocollo. Quando vengono caricati con ultravioletti (UV) a una lunghezza d'onda di 365 nm per 3 minuti e poi fermati, i PLNP mostrano la notevole capacità di generare bagliore residuo in modo efficiente e coerente, il che li rende ideali per realizzare display riscrivibili bidimensionali e opere d'arte tridimensionali trasparenti e luminose. Questo protocollo delineato in questo articolo fornisce un metodo fattibile per la sintesi di nanoparticelle luminescenti persistenti per ulteriori applicazioni di illuminazione e imaging, aprendo nuove prospettive per i campi della scienza e dell'arte.
Introduzione
La luminescenza persistente (PL) è un processo ottico unico in grado di immagazzinare energia dalla luce ultravioletta, dalla luce visibile, dai raggi X o da altre fonti di eccitazione e quindi rilasciarla sotto forma di emissione di fotoni per secondi, minuti, ore o anche per giorni1. La scoperta del fenomeno luminoso continuo ha avuto origine durante la dinastia Song nell'antica Cina, 1000 anni fa, quando un pittore scoprì accidentalmente un dipinto che brillava al buio. In seguito si scoprì che alcune materie prime naturali e minerali potevano assorbire la luce solare e poi brillare al buio e potevano persino essere trasformati in affascinanti perle luminose2. Tuttavia, la prima registrazione adeguata di fosfori persistenti deve essere fatta risalire alla scoperta dell'emissione di PL dalla pietra di Bologna all'inizio del XVIIsecolo, che emetteva un bagliore residuo da giallo ad arancione al buio 1,2,3,4. Successivamente, si è scoperto che le impurità naturali del Cu+ nel BaS hanno svolto un ruolo importante in questo fenomeno di luminescenza persistente 1,4. Fino alla metà degli anni '90, la produzione di fosfori persistenti era in gran parte limitata ai solfuri5. Nel 1996, Matsuzawa et al. hanno riportato un nuovo fosforo di ossido di metallo (SrAl2O4:Eu2+, Dy3+) che mostra un bagliore residuo estremamente luminoso, che ha notevolmente stimolato l'espansione della ricerca sulla luminescenza persistente6.
Le proprietà uniche dei materiali luminescenti persistenti derivano principalmente da due tipi di centri attivi: centri di emissione e centri di trappola 1,7,8. Tra questi, il primo determina la lunghezza d'onda di emissione, mentre l'intensità e il tempo sostenuti sono determinati principalmente dai centri di trappola. Pertanto, la progettazione dei materiali PL dovrebbe prendere in considerazione entrambi gli aspetti al fine di ottenere la lunghezza d'onda di emissione desiderata e la luminescenza di lunga durata 9,10. I centri di emissione possono essere ioni lantanidi con transizioni da 5d a 4f o da 4f a 4f, ioni metalli di transizione con transizioni da d a d o ioni metallici post-transizione con transizioni da p a s 1,11,12,13. D'altra parte, i centri di trappola sono formati da difetti reticolari o vari co-droganti14,15, che di solito non emettono radiazioni ma invece immagazzinano l'energia di eccitazione per un po' e poi la rilasciano gradualmente al centro emittente attraverso l'attivazione termica o altra attivazione fisica16,17. Sono stati riportati molti fosfori con diversi ospiti e ioni droganti. Finora, è stato riscontrato che i composti metallici inorganici18, le strutture metallo-organiche8, alcuni compositi organici19 e i polimeri20 hanno proprietà PL. Negli ultimi anni, i materiali luminescenti persistenti a trappola profonda con proprietà controllabili di accumulo di energia e rilascio di fotoni hanno mostrato grandi applicazioni potenziali nell'archiviazione delle informazioni21, nell'anticontraffazione multistrato22 e nei display avanzati23.
Sulla base della composizione di cui sopra, sono stati progettati e sintetizzati con successo PLNP con varie matrici, come BaZrSi3O97, Y2O2S24, Ca14Mg2(SiO4)825, CaAl2O426, SrAl2O426,27 e Sr2MgSi2O728 con centri luminescenti multi-drogati, in cui i centri di luminescenza dipendono fortemente dall'effetto del campo cristallino del reticolo ospite, mentre i difetti generati o migliorati da diversi drogaggi fungono da centri ausiliari per controllare l'intensità e la durata dell'afterglow. Oltre al co-drogaggio, si possono osservare emissioni di lunga durata anche nel caso di un solo attivatore, come PLNP eterogenei con matrice di Y3Al2Ga3O1229, BaGa2O430, Ca2SnO431, CdSiO332 e Zn3Ga2Ge2O1033. Gli ossidi ternari a base di germaniato includono Ca2Ge7O16, Zn2GeO4, BaGe4O9, ecc., che sono tipici materiali semiconduttori a banda proibita larga con emissione regolabile, luminescenza riproducibile e stabile, elevata resa quantica, rispetto dell'ambiente e ampia disponibilità 34,35,36. Questi vantaggi lo rendono un buon vettore fotoluminescente di tipo attivatore. Negli ultimi anni, i germanati con varie microstrutture35,37, sono stati preparati mediante reazioni convenzionali allo stato solido o metodi di soluzione chimica, e queste caratteristiche rendono Zn2GeO4 utile nella sterilizzazione38, anticontraffazione39, catalisi40, diodi luminosi41, biorilevamento42, anodi batteria43, rivelatori44,45, ecc.
Al fine di espandere l'applicazione dei materiali PL, è stata sviluppata la sintesi controllabile di nanoparticelle luminescenti uniformi e persistenti. Un decennio fa, i fosfori persistenti sono stati sintetizzati mediante sintesi allo stato solido46. Tuttavia, il lungo tempo di reazione e l'elevata temperatura di ricottura durante il processo di sintesi hanno portato a fosfori grandi e irregolari, che ne hanno limitato l'applicazione in altri campi come la biomedicina. Nel 2007, Chermont et al. hanno utilizzato l'approccio sol-gel per sintetizzare nanoparticelle per la prima volta e hanno preparato Ca0,2Zn0,9Mg0,9Si2O6: Eu2+, Dy3+, Mn2+, che ha aperto l'era dei PLNP47. Tuttavia, la strategia di sintesi top-down è accompagnata da problemi come dimensioni e morfologia incontrollabili, quindi i ricercatori hanno svolto molto lavoro nello sviluppo di una sintesi controllabile dal basso verso l'alto dei PLNP. Dal 2015 sono emersi uno dopo l'altro vari metodi di sintesi, come il metodo di sintesi modello, il metodo termico idrotermale/solvente, il metodo sol-gel e altri metodi di sintesi chimica umida per la sintesi di PLNP uniformi e controllabili 47,48,49,50. Tra questi, la sintesi idrotermale è uno dei metodi più comunemente usati per la preparazione di nanomateriali, che può fornire un metodo sintetico regolabile e delicato per preparare composti o materiali con strutture e proprietà speciali51.
Qui, presentiamo una procedura sperimentale dettagliata per sintetizzare Zn2GeO4: Mn PLNP con morfologia a nanorod 1D tramite il metodo idrotermale e fornire loro un ambiente rigido per ulteriori applicazioni di illuminazione. È stato riscontrato che le proprietà di luminescenza dei PLNP, tra cui la lunghezza d'onda di emissione e la curva di decadimento dell'afterglow, possono essere modificate regolando il valore del pH del precursore. D'altra parte, per enfatizzare la versatilità di questo metodo, sintetizziamo anche PLNP con Cr come centro luminescente utilizzando ZnGa2O4 come matrice (ZnGa2O4: Cr), che mostra un'emissione di afterglow (697 nm) nella regione del vicino infrarosso dopo essere stata eccitata dalla luce ultravioletta (365 nm). Questo articolo si concentra principalmente su Zn2GeO4: Mn il cui valore di pH della soluzione precursore è 9,4 per la produzione e la visualizzazione di opere d'arte bidimensionali e tridimensionali. Zn2GeO4: Mn è un tipo di nanomateriale con ioni Mn come centro luminescente che ottiene una forte emissione di luce verde (~ 537 nm) sotto l'eccitazione di una luce ultravioletta di 365 nm. Allo stesso tempo, la luce verde continua può ancora essere vista dopo aver interrotto l'eccitazione. Al fine di promuovere la polimerizzazione dei PLNP in metacrilato di metile, durante il processo di sintesi idrotermale sono stati aggiunti leganti (glicole polietilenico) e quindi i PLNP sono stati polimerizzati con metacrilato di metile (MMA) in uno stampo bidimensionale o tridimensionale in modo che possa formare opere d'arte luminose mentre si sforma dolcemente.
Questo protocollo fornisce un metodo fattibile per la sintesi idrotermale, le reazioni di polimerizzazione e le applicazioni luminescenti dei PLNP nella resa cromatica avanzata. Eventuali differenze di pH, temperatura e reagenti chimici durante la crescita dei nanocristalli influenzeranno le dimensioni e le proprietà ottiche delle nanostrutture PLNP. Questo protocollo dettagliato mira ad aiutare i nuovi ricercatori del settore a migliorare la riproducibilità dei PLNP utilizzando un metodo idrotermale per ulteriori applicazioni più ampie.
Protocollo
1. Sintesi di Zn2GeO4: Mn PLNP
- Preparare 2 M/L di soluzione di idrossido di sodio sciogliendo 10 mM di idrossido di sodio in 5 mL di acqua deionizzata.
- Preparare 0,4 M/L di soluzione di germanato di sodio aggiungendo 2 mM di ossido di germanio in 5 mL di soluzione di idrossido di sodio, quindi mescolare a temperatura ambiente per circa 30 minuti.
- Aggiungere 4 mM di cloruro di zinco, 0,01 mM di nitrato di manganese e 600 μL di acido nitrico (65%-68%, in peso) a un becher piccolo da 100 mL contenente 22 mL di acqua deionizzata.
ATTENZIONE: L'aggiunta di acido nitrico deve essere eseguita rigorosamente in una cappa aspirante e assicurarsi che non vi siano fiamme libere o riscaldamento intorno. - Agitare energicamente fino a quando la soluzione del passaggio 1.3 è completamente sciolta.
- Aggiungere lentamente 2 mM di soluzione di germanato di sodio alla soluzione del passaggio 1.4. Aggiungere 1 mL di polietilenglicole (PEG; 300, Mw) alla soluzione.
- Inserire la sonda del pH calibrato nella soluzione per monitorare il valore del pH del sistema di reazione. Impostare un'agitazione relativamente delicata per evitare schizzi di soluzione e collisioni tra la barra di agitazione e la sonda.
- Aggiungere alla soluzione idrossido di ammonio con una frazione di massa del 25%-28% goccia per goccia e regolare il pH della soluzione a 6,0, 8,0 o 9,4 a seconda della proprietà di luminescenza da studiare. Assicurati di aggiungere lentamente l'idrossido di ammonio e monitora sempre le variazioni di pH della soluzione per evitare che il sistema sia troppo acido o troppo alcalino, in modo da non influenzare la morfologia e le proprietà luminescenti dei nanomateriali.
- Coprire il becher con pellicola sigillante e mescolare la soluzione a temperatura ambiente per 1 ora. Cercare di non esporre il sistema all'aria per evitare che la polvere entri e causi la volatilizzazione del solvente, mescolando a velocità costante in modo che il livello del liquido del sistema non schizzi quando il sistema è completamente miscelato.
- Trasferire la soluzione in un'autoclave rivestita in teflon e porla in un forno di essiccazione termostatico elettrico a 220 °C per 4 h.
NOTA: L'autoclave rivestita in teflon appropriata deve essere selezionata in base al volume del sistema e il reattore deve essere mantenuto pulito. Il volume delle materie prime aggiunte non deve superare 1/3 del volume dell'autoclave. Allo stesso tempo, assicurarsi che l'autoclave sia completamente chiusa prima di inserirla nella stufa di essiccazione termostatica elettrica. - Spegnere il forno di essiccazione termostatico elettrico quando la reazione è completata e attendere che il sistema si raffreddi a temperatura ambiente per estrarre il reattore. Assicurarsi di attendere che il reattore si sia completamente raffreddato e che la pressione sia ridotta a un intervallo di sicurezza prima di procedere alla fase successiva per evitare il contatto diretto tra l'alta temperatura e la pelle.
- Aprire lentamente il reattore e trasferire la soluzione di reazione in due provette da centrifuga da 50 mL. Sciacquare il reattore con 40 ml di etanolo e successivamente trasferire la soluzione di etanolo nelle stesse provette da centrifuga.
- Agitare per 30 s in modo che la soluzione possa essere miscelata in modo uniforme, quindi centrifugare il campione a 4000 x g per 15 minuti a temperatura ambiente e rimuovere il surnatante.
- Aggiungere 10 mL di acqua deionizzata a ciascuna provetta da centrifuga e sonicare per 5 minuti (240 W, 40 kHz) per disperdere nuovamente il prodotto.
- Aggiungere 20 mL di etanolo in ciascuna provetta da centrifuga e agitare per 30 s per miscelare la soluzione in modo uniforme.
- Continuare a centrifugare il prodotto secondo l'impostazione menzionata in precedenza (4000 x g, 15 min) a temperatura ambiente ed eliminare il surnatante.
- Ultrasuoni per 5 minuti per disperdere il prodotto in 2 mL di soluzione di metanolo, sigillare il campione con una pellicola sigillante e conservarlo in un frigorifero a 4 °C per prevenire la contaminazione del campione e l'evaporazione del solvente per future applicazioni di illuminazione.
2. Sintesi di ZnGa2O4: Cr PLNPs
- Sciogliere 12 mM di Ga(NO3)3.xH 2O, 7.2 mM di ZnCl2 e 0.024 mM di Cr(NO3)3.9H 2O in 30 mL di acqua deionizzata.
- Aggiungere 1 mL di PEG (300, Mw) alla soluzione. Aggiungere idrossido di ammonio (25%-28% in peso) alla soluzione, mescolare delicatamente per raggiungere un pH di 9,0-9,4. Assicurarsi di controllare la velocità di agitazione in modo che la soluzione possa mescolarsi accuratamente senza schizzi sul pHmetro.
- Coprire il becher con una pellicola sigillante e mescolare la soluzione a temperatura ambiente per 1 ora. Cercare di ridurre al minimo l'esposizione del sistema all'aria per evitare l'ingresso di polvere e l'evaporazione del solvente. Allo stesso tempo, controllare la velocità di agitazione in modo che il sistema non schizzi durante la miscelazione accurata.
- Trasferire la soluzione in un'autoclave rivestita di teflon e farla funzionare a 220 °C per 6 ore. Estrarre il contenitore dopo che la temperatura è scesa a temperatura ambiente. Assicurarsi che il recipiente di reazione si sia completamente raffreddato e che la pressione sia scesa a un intervallo di sicurezza prima di procedere con le operazioni successive, oltre a evitare il contatto diretto delle alte temperature con la pelle.
- Trasferire la soluzione di reazione in due provette da centrifuga da 50 mL. Sciacquare il reattore con 40 ml di etanolo, quindi trasferire la soluzione di etanolo nelle stesse provette da centrifuga.
- Agitare per 30 s per miscelare la soluzione e quindi centrifugare il campione a 4000 x g per 15 minuti a temperatura ambiente e rimuovere il surnatante.
- Aggiungere 10 mL di acqua deionizzata a ciascuna provetta da centrifuga e sonicare per 5 minuti per ridisperdere il prodotto.
- Aggiungere 20 mL di etanolo in ciascuna provetta da centrifuga e agitare per 30 s per miscelare la soluzione in modo uniforme. Continuare a centrifugare il prodotto a temperatura ambiente come accennato in precedenza (4000 x g, 15 min) ed eliminare il surnatante.
- Ultrasuoni per 5 minuti per disperdere il prodotto in 2 mL di acqua deionizzata e sigillare il campione con una pellicola sigillante per la conservazione.
3. Depurazione delle materie prime
- Purificare il metacrilato di metile (MMA) mediante cromatografia su colonna come descritto di seguito.
- Riempire metà della colonna con ossido di alluminio alcalino (100-200 mesh) e compattare leggermente con una bacchetta di vetro. Quando si riempie la colonna con ossido di alluminio, prestare attenzione alla distribuzione uniforme e alla compattazione uniforme della riempitrice per migliorare l'efficienza di separazione.
- Aggiungi una piccola quantità di MMA e apri il pistone dell'acceleratore in PTFE sottostante. Una volta che lo strato di solvente ha bagnato l'intero ossido di alluminio e il liquido fuoriesce, aggiungi altro MMA e ripeti questo processo più volte. Il tempo in cui il rapporto di massa dell'intero MMA aggiunto all'ossido di alluminio basico è: 1:50 rappresenta la fine del processo.
- Mettere il campione finale di MMA raccolto in una bottiglia di vetro, sigillarla con una pellicola sigillante e conservarla a 4 °C.
ATTENZIONE: L'intero processo deve essere eseguito in una cappa aspirante a causa della forte volatilità dell'MMA. Allo stesso tempo, gli operatori devono indossare maschere e camici da laboratorio.
- Purificare l'azobisisobutirronitrile (AIBN) mediante ricristallizzazione come descritto di seguito.
- Preparare 50 ml di soluzione miscelata con un rapporto in volume di 7:3 di etanolo e acqua distillata e riscaldare la soluzione.
- Aggiungere 5 g di AIBN quando la soluzione bolle e mescolare per mescolare uniformemente la soluzione.
- Rimuovere le impurità insolubili mediante filtrazione a caldo come descritto di seguito.
- Posizionare la carta da filtro ben aderente alla parete interna dell'imbuto triangolare e assicurarsi che la carta da filtro si trovi sotto il bordo dell'imbuto.
- Posizionare l'asta di vetro contro la sezione a tre strati della carta da filtro. Se l'asta di vetro non è posizionata contro la sezione a tre strati della carta da filtro, potrebbe forare la carta da filtro, causando una filtrazione inefficiente.
- Posizionare la punta del becher contenente la soluzione vicino alla bacchetta di vetro e versarla mentre è calda. Lo scopo di questo passaggio è prevenire la formazione di goccioline di liquido.
- Sciacquare il becher con 10 ml di acqua distillata fredda ed eseguire nuovamente il processo di filtrazione di cui sopra; Ripeti 3 volte.
- La soluzione diventa sovrasatura a causa della diminuzione della solubilità durante il raffreddamento, con conseguente precipitazione dei cristalli. Mettere la soluzione raccolta in frigorifero a 4 °C per il raffreddamento e la cristallizzazione. Il campione apparirà nello stato di cristalli aghiformi bianchi.
- Sigillare il campione con un foglio di alluminio e conservarlo a 4 °C.
ATTENZIONE Durante il funzionamento devono essere adottate misure di protezione a causa della tossicità dell'AIBN, evitando anche il contatto con fiamme libere, alte temperature e agenti ossidanti.
4. Copolimerizzazione del metacrilato di metile (MMA)
- Impostare la temperatura del bagnomaria a 80 °C.
NOTA: La temperatura dell'acqua ha una forte influenza sulla velocità di polimerizzazione e quindi influisce sulla formazione del prodotto finale. Pertanto, la temperatura del bagnomaria dovrebbe essere rigorosamente garantita per non essere troppo alta. - Pesare 20 g di MMA in una bottiglia da 100 ml a forma di melanzana. Mantenere il contenitore asciutto prima dell'esperimento.
NOTA: La bottiglia a forma di melanzana è stata scelta per facilitare il riscaldamento del bagnomaria e la sostituzione dell'aria con azoto nell'impianto. Provare a pesare il campione in un ambiente ben ventilato indossando una maschera. - Aggiungere la soluzione di metanolo pre-preparata di Zn2GeO4: Mn nel recipiente di reazione.
- Sciogliere accuratamente il campione in MMA con l'aiuto degli ultrasuoni per circa 10 minuti (240 W, 40 kHz) a temperatura ambiente. Mantenere il recipiente di reazione sigillato per evitare l'evaporazione del solvente ed evitare temperature eccessivamente elevate durante il processo di ultrasonicazione.
- Aggiungere 0,012 g di AIBN alla soluzione e mescolare completamente la soluzione.
NOTA: L'AIBN deve essere utilizzato in condizioni anidre e assicurarsi che non vi siano fiamme libere intorno all'operazione sperimentale. Assicurati di indossare indumenti protettivi. - Porre il matraccio in un bagno d'acqua a 80 °C e spurgare l'aria dal sistema di reazione con N2 per circa 35 minuti. Quando la reazione sta per terminare, agitare delicatamente il contenitore della reazione. Se la soluzione non agita vigorosamente, dimostra che la reazione ha avuto successo.
NOTA: Il tempo di reazione cambierà con la temperatura del bagnomaria. Assicurarsi che la temperatura del bagnomaria raggiunga gli 80 °C e iniziare a cronometrare per 35 minuti. - Al termine della reazione, trasferire rapidamente il recipiente di reazione in un bagno di ghiaccio per raffreddarlo rapidamente.
NOTA: Questo processo dovrebbe essere il più veloce possibile per evitare un'eccessiva pre-polimerizzazione dell'MMA e il bagno di ghiaccio può essere preparato in anticipo durante l'intervallo di reazione. - Versare lentamente la soluzione in uno stampo bidimensionale o tridimensionale, mettere lo stampo in un forno di essiccazione termostatico elettrico a 40 °C per 10 ore, 70 °C per 8 ore e 100 °C per altre 2 ore per ottenere il materiale target.
- Chiudere il forno di essiccazione termostatico elettrico dopo l'arresto della reazione e lasciarlo raffreddare a temperatura ambiente. Aprire il forno di essiccazione termostatico elettrico per estrarre lo stampo dopo che il sistema di reazione si è sufficientemente raffreddato per evitare ustioni cutanee causate dal contatto diretto tra l'alta temperatura e il corpo.
- Rimuovere con cautela lo stampo ed esporre il campione di PMMA polimerizzato (ZGO: Mn-PMMA) a una lampada UV per circa 3 minuti. Ad esempio, quando si espone una pellicola trasparente ZGO: Mn-PMMA alla luce ultravioletta attraverso un ritaglio di cartone nero a forma di lettera H, si ottiene un modello corrispondente di emissione fosforescente verde. Il motivo può essere cancellato dopo 5 minuti. Successivamente, il processo può essere ripetuto utilizzando un altro ritaglio di cartone nero a forma di lettere diverse, generando nuovi motivi luminescenti.
Risultati
Il diagramma di sintesi dei PLNP Zn2GeO4: Mn (ZGO: Mn) è mostrato nella Figura 1. Il polimero anfifilico polietilenglicole (PEG) viene aggiunto per modificare le nanobarre di Zn2GeO4: Mn (ZGO: Mn) prive di ligandi per dissolverle meglio nel mezzo MMA. In primo luogo, vengono raccolte le immagini della microscopia elettronica a trasmissione (TEM), della microscopia elettronica a trasmissione ad alta risoluzione (HRTEM) di ZGO: Mn il cui pH è 9,4 (Figura 1), quindi vengono eseguite la diffusione dinamica della luce (DLS), i risultati del potenziale zeta e la diffrazione di raggi X (XRD) di ZGO: Mn (Figura 2). Vengono caratterizzati gli spettri di afterglow e le curve di decadimento dipendenti dal tempo di ZGO: Mn con pH diverso (pH = 6,0, 8,0, 9,4) in soluzione acquosa eccitata a 365 nm per 3 min, insieme alle immagini di fotoluminescenza e alle immagini di afterglow (Figura 3). Si ottengono il TEM, l'XRD, gli spettri dell'afterglow e la curva di attenuazione dell'afterglow di ZnGa2O4: Cr (Figura 4). Il diagramma di copolimerizzazione di ZGO: Mn il cui pH è 9,4 e MMA è mostrato in Figura 5. Gli spettri di emissione dell'afterglow e l'intensità dell'afterglow in funzione del tempo per il materiale luminescente a base di PMMA (ZGO: Mn-PMMA) possono essere ottenuti dopo aver irradiato i bersagli con 365 nm per 3 minuti e quindi aver cessato l'eccitazione. I materiali per la lavorazione di display riscrivibili e opere d'arte fosforescenti in stampi 2D o 3D possono essere acquisiti dalla fotocamera dopo l'eccitazione con luce UV a 365 nm per 3 minuti (Figura 5), il che indica il successo della polimerizzazione dei PLNP in matrice di PMMA per applicazioni di illuminazione.
Per ottenere immagini ad alta risoluzione al microscopio elettronico a trasmissione (TEM), le misurazioni sono state eseguite su un microscopio elettronico a trasmissione azionato a una tensione di accelerazione di 200 kV. Un sistema XRD è stato utilizzato per caratterizzare i dati di diffrazione a raggi X (XRD) dei PLNP. Gli spettri di emissione dell'afterglow e le curve di decadimento dell'intensità dell'afterglow in funzione del tempo sono stati effettuati utilizzando lo spettrofluorimetro. Una fotocamera digitale è stata utilizzata per registrare immagini di fotoluminescenza e luminescenza persistente di PLNP, materiali luminescenti 2D e 3D.
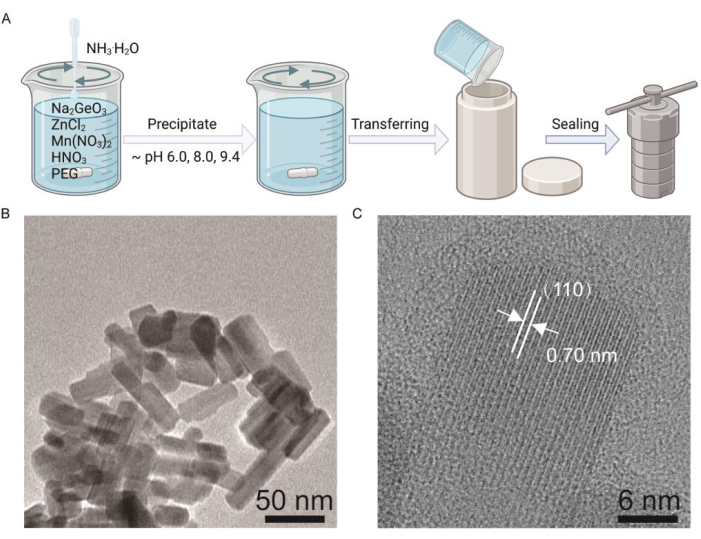
Figura 1: Sintesi di Zn2GeO4: Mn (ZGO: Mn) PLNPs. (A) Il diagramma di sintesi di ZGO: Mn nanorods. (B) Microscopia elettronica a trasmissione (TEM) di nanostrutture ZGO: Mn con pH 9.4. Barra di scala: 50 nm. (C) Immagine al microscopio elettronico a trasmissione ad alta risoluzione (HRTEM) di ZGO: Mn il cui pH è 9,4. Barra della scala: 6 nm. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 2: Sintesi di nanostrutture funzionali di Zn2GeO4: Mn. (A) Analisi di diffusione dinamica della luce (DLS) di Zn2GeO4: Mn-Polietilenglicole (ZGO: Mn-PEG) disperso in acqua deionizzata e adattamento della funzione log-normale per ottenere la distribuzione dimensionale. (B) Risultati potenziali Zeta di ZGO: Mn-PEG. (C) Analisi della diffrazione a raggi X (XRD) di Zn2GeO4: Mn. Fare clic qui per visualizzare una versione più ampia di questa figura.
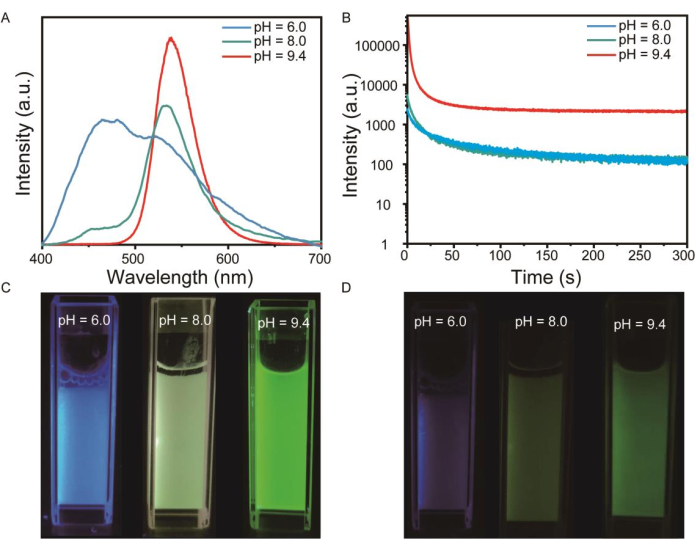
Figura 3: Caratterizzazione di ZGO: Mn in soluzione acquosa. (A) Gli spettri di emissione dell'afterglow di ZGO: Mn-PEG con pH diverso (pH = 6,0, 8,0, 9,4) eccitati da 365 nm per 3 min. (B) Curva di decadimento dell'afterglow dipendente dal tempo di ZGO: Mn in acqua a 537 nm (eccitati con luce UV a 365 nm per 3 min). (C) Immagini in fotoluminescenza di nanobarre ZGO: Mn. (D) Immagini del decadimento della luminescenza del bagliore residuo di ZGO: Mn. Clicca qui per visualizzare una versione più grande di questa figura.
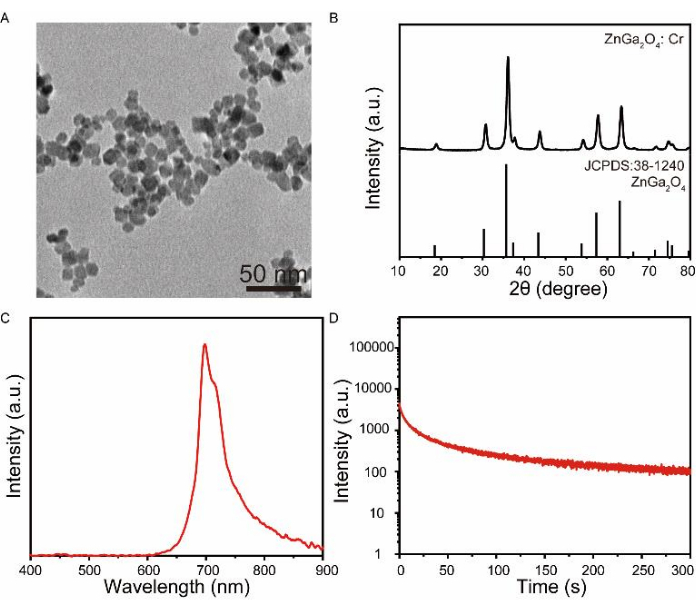
Figura 4: Caratterizzazione di ZnGa2O4: Cr in soluzione acquosa. (A) Immagini TEM di ZnGa2O4: nanoparticelle di Cr. Barra di scala: 50 nm. (B) Analisi XRD di ZnGa2O4: Cr. (C) Lo spettro di emissione afterglow di ZnGa2O4: Cr dopo 3 minuti di eccitazione a 365 nm. (D) Curva di decadimento dell'afterglow dipendente dal tempo di ZnGa2O4: Cr in acqua a 697 nm. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 5: PLNP per applicazioni di visualizzazione riscrivibile e illuminazione 3D. (A) Diagramma schematico della reazione di copolimerizzazione tra ZGO: Mn il cui pH è 9,4 e metacrilato di metile (MMA). (B) Lo spettro di emissione dell'afterglow di ZGO: Mn-PMMA eccitato da 365 nm per 3 min. (C) La variazione dell'intensità dell'afterglow nel tempo di ZGO: Mn-PMMA a 537 nm (eccitato con luce UV a 365 nm per 3 min). (D) Bagliore residuo fotoattivato per la visualizzazione riscrivibile e l'archiviazione dei dati (scritto mediante irradiazione UV). (E) Fotografie a luminescenza di anatra 3D trasparente con ZGO: Mn-PMMA dopo irradiazione UV. Clicca qui per visualizzare una versione più grande di questa figura.
Discussione
Questo articolo introduce un metodo di sintesi per nanomateriali luminescenti persistenti e polimerizzazione per applicazioni di resa cromatica. I materiali hanno mostrato proprietà ottiche estremamente stabili e un bagliore residuo visibile dopo aver cessato l'eccitazione della luce ultravioletta. Un nanomateriale luminescente persistente (Zn2GeO4: Mn) è stato preparato utilizzando un metodo idrotermale con pH diverso (Figura 1A). L'immagine TEM ha mostrato che i PLNP ZGO: Mn con pH 9,4 erano a forma di bastoncino con un diametro medio di circa 65 nm (Figura 1B). Le immagini TEM ad alta risoluzione hanno mostrato una buona cristallinità dei nanomateriali e la spaziatura delle frange reticolari adiacenti parallele alla direzione dell'asta era di 0,70 nm, che era in buon accordo con la spaziatura del piano (110) di Zn2GeO452, indicando che tutto Zn2GeO4: Mn era altamente cristallino (Figura 1C).
Inoltre, i dati di diffusione dinamica della luce (DLS) di ZGO: Mn in acqua deionizzata adattati da una funzione log-normale hanno mostrato che la dimensione idrodinamica calcolata era di 63 nm di diametro e ben dispersa (Figura 2A). I risultati del potenziale zeta hanno anche mostrato una superficie negativa di ZGO: Mn (Figura 2B), indicando che i PLNP avevano una buona solubilità e stabilità in soluzione acquosa. Lo spettro XRD di ZGO: Mn può essere assegnato alla fase romboedrica di Zn2GeO4 (Figura 2C).
Le proprietà ottiche dei PLNP potrebbero essere modificate regolando il pH della soluzione precursore. Gli spettri di emissione visibili del bagliore residuo della soluzione ZGO: Mn eccitata a 365 nm per 3 minuti hanno mostrato che i PLNP mostravano uno spostamento verso il rosso del picco di emissione principale quando la soluzione precursore cambiava da acida ad alcalina (Figura 3A). Anche la curva di decadimento dell'intensità dell'afterglow nel tempo è stata influenzata dal valore del pH, ma in ogni caso, l'intensità dell'emissione può ancora essere rilevata quando il tempo di afterglow ha raggiunto i 300 s, il che ha verificato il successo della sintesi di PLNP con diverse proprietà ottiche (Figura 3B). Le immagini a fotoluminescenza (Figura 3C) e le immagini di postluminescenza (Figura 3D) di PLNP con diversi livelli di pH sono state catturate dalla fotocamera. I risultati hanno rivelato che la soluzione mostrava una luminescenza verde più brillante all'aumentare dell'alcalinità della soluzione.
Sono stati sintetizzati PLNP con ZnGa2O4 come matrice e Cr come centro di luminescenza (ZnGa2O4: Cr) per evidenziare la versatilità di questo metodo idrotermale. L'immagine TEM ha mostrato che ZnGa2O4: Cr era di dimensioni più piccole e uniformemente disperso (Figura 4A). I risultati XRD hanno indicato che tutti i picchi di diffrazione corrispondevano bene con quelli dello spinello cubico ZnGa2O4 (Figura 4B). Lo spettro di emissione dell'afterglow ha mostrato che ZnGa2O4: Cr mostrava un'evidente emissione nel vicino infrarosso dopo essere stato eccitato dalla luce ultravioletta per 3 minuti (Figura 4C). L'intensità di emissione di ZnGa2O4: Cr a 697 nm è stata monitorata nel tempo e i risultati hanno mostrato che l'emissione di bagliore residuo poteva ancora essere raccolta dopo 300 s (Figura 4D).
Ci sono diversi passaggi chiave nella sintesi idrotermale dei PLNP. Innanzitutto, è necessario controllare rigorosamente il pH della soluzione acquosa durante la sintesi dei PLNP. L'acidità e l'alcalinità della soluzione possono avere un effetto drammatico sulla persistenza del bagliore residuo e persino sul colore del bagliore residuo. In secondo luogo, quando si monitora il pH della soluzione, è importante regolare la velocità di agitazione appropriata per garantire che l'agitatore non entri in collisione con la sonda di pH mentre la soluzione viene miscelata in modo uniforme. Infine, quando la soluzione viene agitata per 1 ora in un ambiente con un pH target, mantenere il sistema di reazione sigillato il più possibile per evitare l'influenza della volatilizzazione dell'acqua di ammoniaca.
Inoltre, le opere d'arte luminose bidimensionali e tridimensionali sono copolimerizzate da PLNP e MMA per rendere i PLNP più funzionali (Figura 5A). Si è scoperto che, sia che si tratti di una pellicola o di un'anatra tridimensionale, il materiale mostra una buona capacità di bagliore residuo (Figura 5B, C). I materiali 2D e 3D mostrano una luminescenza verde brillante dopo la cessazione dell'eccitazione della luce ultravioletta e le immagini del bagliore residuo verde possono ancora essere viste dopo 5 secondi (Figura 4D, E), il che indica che i PLNP possono generare un bagliore residuo efficace sotto l'attivazione della lampada UV.
Quando si esegue la polimerizzazione MMA, è necessario prestare attenzione ad alcuni processi. Innanzitutto, le materie prime, cioè MMA e AIBN, devono essere purificate in modo da non influire sulla polimerizzazione. Il secondo, quando si aggiunge metanolo disperso Zn2GeO4: Mn nella soluzione MMA, disperde ultrasonicamente l'intero sistema in modo uniforme. Terzo, ricordate di osservare sempre lo stato della soluzione. Significa che la pre-polimerizzazione ha successo se l'oscillazione del pallone provoca solo un leggero scuotimento della soluzione. In quarto luogo, il pallone deve essere bagnato con ghiaccio immediatamente dopo la pre-polimerizzazione per evitare un'eccessiva polimerizzazione. Infine, la temperatura deve essere programmata durante la reazione di polimerizzazione nel forno di essiccazione termostatico elettrico per formare una matrice omogenea.
In sintesi, ci aspettiamo che questo protocollo non solo fornisca una procedura sperimentale dettagliata per la sintesi idrotermale di nanomateriali a emissione di lunga durata, ma introduca anche un metodo per la copolimerizzazione di PLNP e MMA per ottenere ulteriori applicazioni riscrivibili e luminescenti mediate dai raggi UV. Ancora più importante, le proprietà ottiche dei PLNP possono essere ulteriormente regolate per avere vari colori di bagliore residuo regolando diversi difetti, centri luminescenti e valori di pH in base a questo metodo. Inoltre, il metodo di copolimerizzazione di PLNP e polimeri può essere ulteriormente utilizzato nella produzione artistica. Questi vantaggi rendono i PLNP materiali ideali per applicazioni di luminescenza e imaging. D'altra parte, il metodo di sintesi idrotermale può limitare l'applicazione di alcuni materiali, in particolare di sostanze sensibili alla temperatura, poiché la reazione richiede temperature relativamente elevate. Pertanto, è necessario selezionare il metodo di sintesi appropriato in base alle applicazioni e ai requisiti specifici.
Divulgazioni
Non c'è nulla da rivelare.
Riconoscimenti
Gli autori ringraziano il finanziamento della National Natural Science Foundation of China (82001945), lo Shanghai Pujiang Program (20PJ1410700) e la sovvenzione iniziale della ShanghaiTech University. Gli autori ringraziano il Centre for High-resolution Electron Microscopy (ChEM), School of Physical Science and Technology, ShanghaiTech University (No. EM02161943) per il supporto alla caratterizzazione del materiale. Gli autori ringraziano l'Analytical Instrumentation Center (#SPST-AIC10112914), la School of Physical Science and Technology, la ShanghaiTech University per il supporto ai test spettrali e XRD. Gli autori ringraziano anche il Prof. Jianfeng Li per l'aiuto con le caratterizzazioni dei materiali.
Materiali
| Name | Company | Catalog Number | Comments |
| azobisisobutyronitrile (99%) | Macklin | A800354 | Further purification required |
| methyl methacrylate(99%) | Sigma-Aldrich | M55909 | Further purification required |
| deionized water | Merck | ZEQ7016T0C | Milli-Q Direct Water Purification System |
| alkaline aluminum oxide (100-200 mesh) | Macklin | A800033 | |
| ammonium hydroxide (25%-28%, wt) | Macklin | A801005 | |
| beaker | Synthware | B220100 | |
| chromium(III) nitrate nonahydrate (99.95%) | Aladdin | C116448 | |
| centrifuge | ThermoFisher Scientific | 75004250 | |
| column | Synthware | C184464CR | |
| digital camera | Canon | EOS M50 Mark II | |
| electric thermostaticdrying oven | Longyue | LDO-9036A | |
| ethanol (99.7%) | Greagent | 1158566 | |
| gallium nitrate hydrate(99.9%) | Aladdin | G109501 | |
| germanium oxide (99.99%) | Sinopharm Chemical ReagentCo., Ltd | 51009860 | |
| glass rod | Sinopharm Chemical ReagentCo., Ltd | 91229401 | |
| powder X-Ray Diffractometer | D2 PHASER DESKTOP XRD | BRUKER | |
| manganese nitrate (98%) | Macklin | M828399 | |
| methanol (99.5%) | Greagent | 1226426 | |
| nitric acid (65.0-68.0%, wt) | Sinopharm Chemical ReagentCo., Ltd | 10014508 | |
| pH meter | Shanghai Leici Sensor Technology Co., Ltd | PHS-3C | |
| polyethylene glycol (300, Mw) | Adamas | 01050882(41713A) | |
| sealing film | Parafilm | 2025722 | |
| sodium hydroxide (GR) | Sinopharm Chemical ReagentCo., Ltd | 10019764 | |
| spectrometer | Horiba | Fluorolog-3 | |
| transmission electron microscope | JEOL | JEM-1400 Plus | |
| transmission electron microscope | JEOL | 2100 Plus | |
| triangular funnel | Synthware | F181975 | |
| ultrasound machine | centrifuge | JP-040S | |
| zinc chloride (98%) | Greagent | 01113266/G81783A |
Riferimenti
- Xu, J., Tanabe, S. Persistent luminescence instead of phosphorescence: History, mechanism, and perspective. J Luminesc. 205, 581-620 (2019).
- Harvey, E. N. A history of luminescence from the earliest times until 1900. , American Philosophical Society. Philadelphia, USA. (1957).
- Hölsä, J. Persistent luminescence beats the afterglow: 400 years of persistent luminescence. Electrochem Soc Interface. 18 (4), 42(2009).
- Lastusaari, M., et al. The Bologna stone: history's first persistent luminescent material. Euro J Mineral. 24 (5), 885-890 (2012).
- Liu, Y., Kuang, J., Lei, B., Shi, C. Color-control of long-lasting phosphorescence (LLP) through rare earth ion-doped cadmium metasilicate phosphors. J Mater Chem. 15 (37), 4025-4031 (2005).
- Matsuzawa, T., Aoki, Y., Takeuchi, N., Murayama, Y. A new long phosphorescent phosphor with high brightness, SrAl2O4:Eu2+, Dy3+. J Electrochem Soc. 143 (8), 2670(1996).
- Guo, H., et al. Cyan emissive super-persistent luminescence and thermoluminescence in BaZrSi3O9:Eu2+,Pr3+ phosphors. J Mater Chem C. 5 (11), 2844-2851 (2017).
- Yuan, J., Dong, J., Lei, S., Hu, W. Long afterglow MOFs: a frontier study on synthesis and applications. Mater Chem Front. 5 (18), 6824-6849 (2021).
- Fu, X., Zheng, S., Shi, J., Li, Y., Zhang, H. Long persistent luminescence property of a novel green emitting SrLaGaO4 : Tb3+ phosphor. J Luminesc. 184, 199-204 (2017).
- Zhuang, Y., Wang, L., Lv, Y., Zhou, T. L., Xie, R. J. Optical data storage and multicolor emission readout on flexible films using deep-trap persistent luminescence materials. Adv Func Mater. 28 (8), 1705769(2018).
- Singh, S. K. Red and near infrared persistent luminescence nano-probes for bioimaging and targeting applications. RSC Adv. 4 (102), 58674-58698 (2014).
- Matuszewska, C., Elzbieciak-Piecka, K., Marciniak, L. Transition metal ion-based nanocrystalline luminescent thermometry in SrTiO3:Ni2+,Er3+ nanocrystals operating in the second optical window of biological tissues. J Phys Chem C. 123 (30), 18646-18653 (2019).
- Zhuang, Y., Katayama, Y., Ueda, J., Tanabe, S. A brief review on red to near-infrared persistent luminescence in transition-metal-activated phosphors. Optic Mater. 36 (11), 1907-1912 (2014).
- Norrbo, I., et al. Lanthanide and heavy metal free long white persistent luminescence from Ti doped Li-hackmanite: A versatile, low-cost material. Adv Func Mater. 27 (17), 1606547(2017).
- Hoang, K. Defects and persistent luminescence in Eu-doped SrAl2O4. Phys Rev Appl. 19 (2), 024060(2023).
- Viana, B., et al. Long term in vivo imaging with Cr3+ doped spinel nanoparticles exhibiting persistent luminescence. J Luminesc. 170 (3), 879-887 (2016).
- Ding, Y., So, B., Cao, J., Langenhorst, F., Wondraczek, L. Light delivery, acoustic read-out, and optical thermometry using ultrasound-induced mechanoluminescence and the near-infrared persistent luminescence of CaZnOS:Nd3. Adv Optic Mater. 11 (17), 2300331(2023).
- Ge, S., et al. Realizing color-tunable and time-dependent ultralong afterglow emission in antimony-doped CsCdCl3 metal halide for advanced anti-counterfeiting and information encryption. Adv Optic Mater. 11 (14), 2300323(2023).
- Zhai, L., Ren, X. M., Xu, Q. Carbogenic π-conjugated domains as the origin of afterglow emissions in carbon dot-based organic composite films. Mater Chem Front. 5 (11), 4272-4279 (2021).
- Miao, Q., et al. Molecular afterglow imaging with bright, biodegradable polymer nanoparticles. Nat Biotechnol. 35 (11), 1102-1110 (2017).
- Zhou, B., Xiao, G., Yan, D. Boosting wide-range tunable long-afterglow in 1D metal-organic halide micro/nanocrystals for space/time-resolved information photonics. Adv Mater. 33 (16), e2007571(2021).
- Yang, H., et al. Highly flexible dual-mode anti-counterfeiting designs based on tunable multi-band emissions and afterglow from chromium-doped aluminates. J Mater Chem C. 8 (46), 16533-16541 (2020).
- Chen, Y., et al. Synaptic plasticity powering long-afterglow organic light-emitting transistors. Adv Mater. 33 (39), e2103369(2021).
- Qu, B., Wang, J., Liu, K., Zhou, R., Wang, L. A comprehensive study of the red persistent luminescence mechanism of Y2O2S:Eu,Ti,Mg. Phys Chem Chem Phys. 21 (45), 25118-25125 (2019).
- Zhang, J., Jiang, C. Luminescence properties of Ca14 Mg2(SiO4)8 :Eu2+ from various Eu2+ sites for white-light-emitting diodes. Mater Res Bull. 60, 467-473 (2014).
- Yamamoto, H., Matsuzawa, T. Mechanism of long phosphorescence of SrAl2O4: Eu2+, Dy3+ and CaAl2O4 Eu2+, Nd3+. J Luminesc. 72-74, 287-289 (1997).
- Rojas-Hernandez, R. E., Rubio-Marcos, F., Rodriguez, M. Á, Fernandez, J. F. Long lasting phosphors: SrAl2O4:Eu, Dy as the most studied material. Renew Sustain Ener Rev. 81 (2), 2759-2770 (2018).
- Lin, Y., Tang, Z., Zhang, Z., Wang, X., Zhang, J. Preparation of a new long afterglow blue-emitting Sr2MgSi2O7-based photoluminescent phosphor. J Mater Sci Lett. 20, 1505-1506 (2001).
- Katayama, Y., Viana, B., Gourier, D., Xu, J., Tanabe, S. Photostimulation induced persistent luminescence in Y3Al2Ga3O12:Cr3. Optic Mater Exp. 6 (4), 1405-1413 (2016).
- Li, H., et al. A strategy for developing thermal-quenching-resistant emission and super-long persistent luminescence in BaGa2O4:Bi3+. J Mater Chem C. 7 (42), 13088-13096 (2019).
- Lei, B., et al. Luminescent properties of orange-emitting long-lasting phosphorescence phosphor Ca2SnO4:Sm3. Solid State Sci. 13 (3), 525-528 (2011).
- Lei, B., Liu, Y., Ye, Z., Shi, C. Luminescence properties of CdSiO3:Mn2+ phosphor. J Luminesc. 109 (3-4), 215-219 (2004).
- Wu, Y., et al. Near-infrared long-persistent phosphor of Zn3Ga2Ge2O10: Cr3+ sintered in different atmosphere. Spectrochim Acta A Mol Biomol Spectrosc. 151, 385-389 (2015).
- Zhang, S., Hu, Y. Photoluminescence spectroscopies and temperature-dependent luminescence of Mn4+ in BaGe4O9 phosphor. J Luminesc. 177, 394-401 (2016).
- Wang, J., et al. One-dimensional luminous nanorods featuring tunable persistent luminescence for autofluorescence-free biosensing. ACS Nano. 11 (8), 8185-8191 (2017).
- Wang, T., Xu, X., Zhou, D., Qiu, J., Yu, X. Red phosphor Ca2Ge7O16:Eu3+ for potential application in field emission displays and white light-emitting diodes. Mater Res Bull. 60, 876-881 (2014).
- Ding, D., et al. X-ray-activated simultaneous near-infrared and short-wave infrared persistent luminescence imaging for long-term tracking of drug delivery. ACS Appl Mater Interfaces. 13 (14), 16166-16172 (2021).
- Zhao, X., Wei, X., Chen, L. J., Yan, X. P. Bacterial microenvironment-responsive dual-channel smart imaging-guided on-demand self-regulated photodynamic/chemodynamic synergistic sterilization and wound healing. Biomater Sci. 10 (11), 2907-2916 (2022).
- Huang, K., et al. Enhancing light and X-ray charging in persistent luminescence nanocrystals for orthogonal afterglow anti-counterfeiting. Adv Func Mater. 31 (22), 2009920(2021).
- Sun, L., Qi, Y., Jia, C. J., Jin, Z., Fan, W. Enhanced visible-light photocatalytic activity of g-C3N4/Zn2GeO4 heterojunctions with effective interfaces based on band match. Nanoscale. 6 (5), 2649-2659 (2014).
- Gupta, S. K., Sudarshan, K., Modak, B., Gupta, R. Interstitial zinc boosted light tunability, afterglow, and ultrabright white emission in zinc germanate (Zn2GeO4). ACS Appl Electron Mater. 5 (2), 1286-1294 (2023).
- Calderón-Olvera, R. M., et al. Persistent Luminescence Zn2GeO4:Mn2+ nanoparticles functionalized with polyacrylic acid: One-pot synthesis and biosensing applications. ACS Appl Mater Interfaces. 15 (17), 20613-20624 (2023).
- Li, Q., Miao, X., Wang, C., Yin, L. Three-dimensional Mn-doped Zn2GeO4 nanosheet array hierarchical nanostructures anchored on porous Ni foam as binder-free and carbon-free lithium-ion battery anodes with enhanced electrochemical performance. J Mater Chem A. 3 (42), 21328-21336 (2015).
- Lai, B., et al. A phosphorescence resonance energy transfer-based "off-on" long afterglow aptasensor for cadmium detection in food samples. Talanta. 232, 122409(2021).
- Chi, F., et al. Multimodal temperature sensing using Zn2GeO4:Mn2+ phosphor as highly sensitive luminescent thermometer. Sens Actuat B: Chem. 296, 126640(2019).
- Yin, S., Chen, D., Tang, W., Peng, Y. Synthesis of CaTiO3:Pr persistent phosphors by a modified solid-state reaction. Mater Sci Eng: B. 136 (2-3), 193-196 (2007).
- le Masne de Chermont, Q., et al. Nanoprobes with near-infrared persistent luminescence for in vivo imaging. Proc Natl Acad Sci U S A. 104 (22), 9266-9271 (2007).
- Li, Z., Shi, J., Zhang, H., Sun, M. Highly controllable synthesis of near-infrared persistent luminescence SiO2/CaMgSi2O6 composite nanospheres for imaging in vivo. Opt Express. 22 (9), 10509-10518 (2014).
- Sera, M., et al. Morphology control and synthesis of afterglow materials with a SrAl2O4 framework synthesized by Surfactant-Template and hydrothermal methods. Chem Phys Lett. 780, 138916(2021).
- Kim, J., Lee, C. K., Kim, Y. J. Low temperature synthesis of Lu3Al5-xGaxO12:Ce3+,Cr3+ powders using a sol-gel combustion process and its persistent luminescence properties. Optic Mat. 104, 109944(2020).
- Xu, Z., et al. Ln(3+) (Ln = Eu, Dy, Sm, and Er) ion-doped YVO(4) nano/microcrystals with multiform morphologies: hydrothermal synthesis, growing mechanism, and luminescent properties. Inorg Chem. 49 (4), 6706-6715 (2010).
- Wang, Y., et al. Zn2GeO4−x/ZnS heterojunctions fabricated via in situ etching sulfurization for Pt-free photocatalytic hydrogen evolution: interface roughness and defect engineering. Phys Chem Chem Phys. 22 (18), 10265-10277 (2020).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon