Method Article
Synthese von persistenten lumineszierenden Nanopartikeln für wiederbeschreibbare Displays und Beleuchtungsanwendungen
In diesem Artikel
Zusammenfassung
Es wird ein Protokoll für die Synthese von persistenten lumineszierenden Nanomaterialien (PLNPs) und ihre potenziellen Anwendungen in wiederbeschreibbaren Displays und künstlerischer Verarbeitung unter Ausnutzung des Nachleuchteffekts unter Bestrahlung mit ultraviolettem Licht (365 nm) vorgestellt.
Zusammenfassung
Persistente lumineszierende Nanopartikel (PLNPs) besitzen die Fähigkeit, auch nach Beendigung der Anregung eine längere Lebensdauer und eine robuste Emission aufrechtzuerhalten. PLNPs sind in verschiedenen Bereichen weit verbreitet, darunter Informationsdisplays, Datenverschlüsselung, biologische Bildgebung und künstlerische Dekoration mit anhaltender und lebendiger Leuchtkraft und bieten grenzenlose Möglichkeiten für eine Vielzahl innovativer Technologien und künstlerischer Projekte. Dieses Protokoll konzentriert sich auf ein experimentelles Verfahren zur hydrothermalen Synthese von PLNPs. Die erfolgreiche Synthese von dauerhaft lumineszierenden Nanomaterialien, wobei Mn2+ oder Cr3+ als Leuchtzentrum in Zn2GeO4: Mn (ZGO: Mn) oder ZnGa2O4: Cr dient, unterstreicht die Universalität dieses Syntheseverfahrens. Auf der anderen Seite können die optischen Eigenschaften von ZGO: Mn durch Einstellen des pH-Werts von Vorläuferlösungen verändert werden, was die Abstimmbarkeit des Protokolls demonstriert. Wenn PLNPs 3 Minuten lang mit Ultraviolett (UV) bei einer Wellenlänge von 365 nm aufgeladen und dann gestoppt werden, weisen sie die bemerkenswerte Fähigkeit auf, effizient und gleichmäßig Nachleuchten zu erzeugen, was sie ideal für die Herstellung von zweidimensionalen, wiederbeschreibbaren Displays und dreidimensionalen transparenten, leuchtenden Kunstwerken macht. Dieses Protokoll, das in diesem Artikel skizziert wird, bietet eine praktikable Methode für die Synthese von persistenten lumineszierenden Nanopartikeln für weitere Beleuchtungs- und Bildgebungsanwendungen und eröffnet neue Perspektiven für die Bereiche Wissenschaft und Kunst.
Einleitung
Persistente Lumineszenz (PL) ist ein einzigartiger optischer Prozess, der Energie aus ultraviolettem Licht, sichtbarem Licht, Röntgenstrahlen oder anderen Anregungsquellen speichern und dann in Form von Photonenemission für Sekunden, Minuten, Stunden oder sogar für Tage abgebenkann 1. Die Entdeckung des kontinuierlichen Leuchtphänomens stammt aus der Song-Dynastie im alten China vor 1000 Jahren, als ein Maler zufällig ein Gemälde entdeckte, das im Dunkeln leuchtete. Später stellte sich heraus, dass einige natürliche Rohstoffe und Mineralien Sonnenlicht absorbieren und dann im Dunkeln leuchten und sogar zu faszinierenden Leuchtperlen verarbeitet werden können2. Der erste adäquate Nachweis persistenter Leuchtstoffe musste jedoch auf die Entdeckung der PL-Emission aus dem Bologna-Stein im frühen 17. Jahrhundert zurückgeführt werden, die im Dunkeln ein gelbes bis orangefarbenes Nachleuchten abgab 1,2,3,4. Später wurde entdeckt, dass die natürlichen Verunreinigungen von Cu+ in BaS eine wichtige Rolle bei diesem anhaltenden Lumineszenzphänomen spielten 1,4. Bis Mitte der 1990er Jahre beschränkte sich die Produktion von persistenten Leuchtstoffen weitgehend auf die Sulfide5. Im Jahr 1996 berichteten Matsuzawa et al. über einen neuen Metalloxid-Leuchtstoff (SrAl2O4:Eu2+, Dy3+), der ein extrem helles Nachleuchten zeigte, was die Expansion der persistenten Lumineszenzforschung stark stimulierte6.
Die einzigartigen Eigenschaften persistenter lumineszierender Materialien ergeben sich hauptsächlich aus zwei Arten von aktiven Zentren: Emissionszentren und Fallenzentren 1,7,8. Unter ihnen bestimmt erstere die Emissionswellenlänge, während die anhaltende Intensität und Zeit hauptsächlich durch die Fallenzentren bestimmt werden. Daher sollten bei der Konstruktion von PL-Materialien beide Aspekte berücksichtigt werden, um die gewünschte Emissionswellenlänge und eine lang anhaltende Lumineszenz 9,10 zu erreichen. Bei den Emissionszentren kann es sich um Lanthanoid-Ionen mit 5d-zu-4f- oder 4f-zu-4f-Übergängen, Übergangsmetallionen mit d-zu-d-Übergängen oder Nachübergangs-Metallionen mit p-zu-s-Übergängen 1,11,12,13 handeln. Auf der anderen Seite werden Fallenzentren durch Gitterdefekte oder verschiedene Co-Dotierstoffegebildet 14,15, die in der Regel keine Strahlung emittieren, sondern die Anregungsenergie für eine Weile speichern und dann durch thermische oder andere physikalische Aktivierung allmählich an das emittierende Zentrum abgeben16,17. Es wurde über viele Leuchtstoffe mit unterschiedlichen Wirten und Dotationen berichtet. Bisher wurde festgestellt, dass anorganische Metallverbindungen18, metallorganische Gerüstverbindungen8, bestimmte organische Komposite19 und Polymere20 PL-Eigenschaften aufweisen. In den letzten Jahren haben persistente Lumineszenzmaterialien mit kontrollierbarer Energiespeicherung und Photonenfreisetzung große potenzielle Anwendungen in der Informationsspeicherung21, der Mehrschichtfälschungssicherheit22 und fortschrittlichen Displays23 gezeigt.
Basierend auf der obigen Zusammensetzung wurden PLNPs mit verschiedenen Matrizen erfolgreich entworfen und synthetisiert, wie z. B. BaZrSi3O97, Y2O2S24, Ca14Mg2(SiO4)825, CaAl2O426, SrAl2O426,27 und Sr2MgSi2O728 mit mehrfach dotierten Lumineszenzzentren, bei denen die Lumineszenzzentren stark vom Kristallfeldeffekt des Wirtsgitters abhängen, während die durch unterschiedliche Dotierung erzeugten oder verbesserten Defekte als Hilfszentren dienen, um die Intensität und Dauer des Nachleuchtens zu steuern. Neben der Co-Dotierung kann eine lang anhaltende Emission auch bei nur einem Aktivator beobachtet werden, wie z. B. bei heterogenen PLNPs mit der Matrix von Y3Al2Ga3O1229, BaGa2O430, Ca2SnO431, CdSiO332 und Zn3Ga2Ge2O1033. Zu den ternären Oxiden auf Germanatbasis gehörenCa2 Ge7O16, Zn2GeO4, BaGe4O9 usw., bei denen es sich um typische Halbleitermaterialien mit breiter Bandlücke mit einstellbarer Emission, reproduzierbarer und stabiler Lumineszenz, hoher Quantenausbeute, Umweltfreundlichkeit und breiter Verfügbarkeithandelt 34,35,36. Diese Vorteile machen es zu einem guten photolumineszierenden Träger vom Aktivator-Typ. In den letzten Jahren wurden Germanate mit verschiedenen Mikrostrukturen35, 37 durch konventionelle Festkörperreaktionen oder chemische Lösungsverfahren hergestellt, und diese Eigenschaften machen Zn2GeO4 nützlich bei der Sterilisation38, der Fälschungssicherheit39, der Katalyse40, den Leuchtdioden41, der Biosensorik42, den Batterieanoden43, den Detektoren44, 45 usw.
Um die Anwendung von PL-Materialien zu erweitern, wurde die kontrollierbare Synthese von gleichmäßigen und persistenten lumineszierenden Nanopartikeln entwickelt. Vor einem Jahrzehnt wurden persistente Leuchtstoffe durch Festkörpersynthese synthetisiert46. Die lange Reaktionszeit und die hohe Glühtemperatur während des Syntheseprozesses führten jedoch zu großen und unregelmäßigen Leuchtstoffen, was ihre Anwendung in anderen Bereichen wie der Biomedizin einschränkte. Im Jahr 2007 verwendeten Chermont et al. zum ersten Mal den Sol-Gel-Ansatz, um Nanopartikel zu synthetisieren, und stellten Ca0,2Zn0,9Mg0,9Si2O6: Eu2+, Dy3+, Mn2+ her, was die Ära der PLNPs47 eröffnete. Die Top-down-Synthesestrategie geht jedoch mit Problemen wie unkontrollierbarer Größe und Morphologie einher, so dass die Forscher viel Arbeit in die Entwicklung einer kontrollierbaren Bottom-up-Synthese von PLNPs gesteckt haben. Seit 2015 sind nacheinander verschiedene Synthesemethoden entstanden, wie z. B. die Template-Synthesemethode, die hydrothermale/lösungsmittelthermische Methode, die Sol-Gel-Methode und andere nasschemische Synthesemethoden zur Synthese von gleichmäßigen und kontrollierbaren PLNPs 47,48,49,50. Unter ihnen ist die hydrothermale Synthese eines der am häufigsten verwendeten Verfahren zur Herstellung von Nanomaterialien, das ein einstellbares und mildes Syntheseverfahren zur Herstellung von Verbindungen oder Materialien mit besonderen Strukturen und Eigenschaften bietenkann 51.
In dieser Arbeit stellen wir ein detailliertes experimentelles Verfahren vor, um Zn2GeO 4: Mn PLNPs mit der Morphologie von 1D-Nanostäbchen über die hydrothermale Methode zu synthetisieren und ihnen eine starre Umgebung für weitere Beleuchtungsanwendungen zur Verfügung zu stellen. Es wurde festgestellt, dass die Lumineszenzeigenschaften von PLNPs, einschließlich der Emissionswellenlänge und der Nachleuchtabklingkurve, durch Anpassen des pH-Wertes des Vorläufers verändert werden können. Um die Vielseitigkeit dieser Methode zu unterstreichen, synthetisieren wir auch PLNPs mit Cr als Lumineszenzzentrum unter Verwendung von ZnGa2O4 als Matrix (ZnGa2O4: Cr), das nach Anregung durch ultraviolettes Licht (365 nm) im nahen Infrarotbereich eine Nachleuchtemission (697 nm) aufweist. Dieser Artikel konzentriert sich hauptsächlich auf Zn2GeO4: Mn, dessen pH-Wert der Vorläuferlösung 9,4 für die Herstellung und Visualisierung von zwei- und dreidimensionalen Kunstwerken beträgt. Zn2GeO4: Mn ist eine Art Nanomaterial mit Mn-Ionen als Lumineszenzzentrum, das unter Anregung von 365 nm ultraviolettem Licht eine starke grüne Lichtemission (~ 537 nm) erzielt. Gleichzeitig ist das durchgehend grüne Licht auch nach Beendigung der Anregung noch zu sehen. Um die Polymerisation von PLNPs in Methylmethacrylat zu fördern, wurden während des hydrothermalen Syntheseprozesses Liganden (Polyethylenglykol) zugesetzt, und dann wurden PLNPs mit Methylmethacrylat (MMA) in einer zweidimensionalen oder dreidimensionalen Form polymerisiert, so dass es ein leuchtendes Kunstwerk bilden kann, während es sich sanft entformt.
Dieses Protokoll bietet eine praktikable Methode für die hydrothermale Synthese, Polymerisationsreaktionen und lumineszierende Anwendungen von PLNPs in der fortschrittlichen Farbwiedergabe. Unterschiede in pH-Wert, Temperatur und chemischen Reagenzien während des Nanokristallwachstums wirken sich auf die Größe und die optischen Eigenschaften der PLNP-Nanostrukturen aus. Dieses detaillierte Protokoll soll neuen Forschern auf diesem Gebiet helfen, die Reproduzierbarkeit von PLNPs mit einer hydrothermalen Methode für weitere breitere Anwendungen zu verbessern.
Protokoll
1. Synthese von Zn2GeO 4: Mio PLNPs
- Bereiten Sie 2 m/l Natriumhydroxidlösung vor, indem Sie 10 mM Natriumhydroxid in 5 mL entionisiertem Wasser auflösen.
- Bereiten Sie 0,4 m/l Natriumgermanatlösung vor, indem Sie 2 mM Germaniumoxid in 5 mL Natriumhydroxidlösung geben und dann etwa 30 Minuten lang bei Raumtemperatur rühren.
- Geben Sie 4 mM Zinkchlorid, 0,01 mM Mangannitrat und 600 μl Salpetersäure (65 %-68 Gew.-%) in ein 100 mL kleines Becherglas mit 22 mL deionisiertem Wasser.
ACHTUNG: Die Zugabe von Salpetersäure sollte streng in einem Abzug erfolgen und darauf achten, dass sich keine offenen Flammen oder Erwärmung in der Nähe befinden. - Kräftig rühren, bis sich die Lösung aus Schritt 1.3 vollständig aufgelöst hat.
- 2 mM Natriumgermanatlösung werden langsam zu der Lösung in Schritt 1.4 gegeben. Geben Sie 1 ml Polyethylenglykol (PEG; 300, Mw) in die Lösung.
- Setzen Sie die kalibrierte pH-Messsonde in die Lösung ein, um den pH-Wert des Reaktionssystems zu überwachen. Stellen Sie ein relativ sanftes Rühren ein, um ein Spritzen der Lösung und eine Kollision zwischen dem Rührstab und der Sonde zu vermeiden.
- Geben Sie der Lösung Tropfen für Tropfen Ammoniumhydroxid mit einem Massenanteil von 25 % bis 28 % hinzu und stellen Sie den pH-Wert der Lösung auf 6,0, 8,0 oder 9,4 ein, abhängig von der zu untersuchenden Lumineszenzeigenschaft. Achten Sie darauf, Ammoniumhydroxid langsam hinzuzufügen und überwachen Sie jederzeit die pH-Änderungen der Lösung, um zu verhindern, dass das System zu sauer oder zu alkalisch wird, um die Morphologie und die lumineszierenden Eigenschaften von Nanomaterialien nicht zu beeinträchtigen.
- Das Becherglas mit Siegelfolie abdecken und die Lösung 1 h bei Raumtemperatur rühren. Versuchen Sie, das System nicht der Luft auszusetzen, um zu verhindern, dass Staub eindringt und eine Lösungsmittelverflüchtigung verursacht, während Sie mit konstanter Geschwindigkeit rühren, damit der Flüssigkeitsstand des Systems nicht spritzt, wenn das System vollständig gemischt ist.
- Füllen Sie die Lösung in einen mit Teflon ausgekleideten Autoklaven und stellen Sie sie für 4 Stunden bei 220 °C in einen elektrischen thermostatischen Trockenofen.
HINWEIS: Der geeignete mit Teflon ausgekleidete Autoklav sollte entsprechend dem Volumen des Systems ausgewählt werden, und der Reaktor sollte sauber gehalten werden. Das Volumen der zugesetzten Rohstoffe sollte 1/3 des Volumens des Autoklaven nicht überschreiten. Stellen Sie gleichzeitig sicher, dass der Autoklav vollständig geschlossen ist, bevor Sie ihn in den elektrischen thermostatischen Trockenschrank stellen. - Schalten Sie den elektrischen thermostatischen Trockenschrank aus, wenn die Reaktion abgeschlossen ist, und warten Sie, bis das System auf Raumtemperatur abgekühlt ist, um den Reaktor abzuschalten. Warten Sie, bis der Reaktor vollständig abgekühlt und der Druck auf einen sicheren Bereich reduziert ist, bevor Sie mit dem nächsten Schritt fortfahren, um einen direkten Kontakt zwischen hohen Temperaturen und Haut zu vermeiden.
- Öffnen Sie langsam den Reaktor und geben Sie die Reaktionslösung in zwei 50-ml-Zentrifugenröhrchen. Spülen Sie den Reaktor mit 40 mL Ethanol und geben Sie anschließend die Ethanollösung in dieselben Zentrifugenröhrchen.
- 30 s lang vortexen, damit die Lösung gleichmäßig gemischt werden kann, dann die Probe bei 4000 x g für 15 min bei Raumtemperatur zentrifugieren und den Überstand entfernen.
- Geben Sie 10 mL deionisiertes Wasser in jedes Zentrifugenröhrchen und beschallen Sie es 5 Minuten lang (240 W, 40 kHz), um das Produkt wieder zu dispergieren.
- Geben Sie 20 ml Ethanol in jedes Zentrifugenröhrchen und wirbeln Sie es 30 s lang, um die Lösung gleichmäßig zu mischen.
- Zentrifugieren Sie das Produkt weiterhin gemäß der oben genannten Einstellung (4000 x g, 15 min) bei Raumtemperatur und entsorgen Sie den Überstand.
- 5 Minuten lang mit Ultraschall beschallen, um das Produkt in 2 mL Methanollösung zu dispergieren, die Probe mit einer Siegelfolie zu versiegeln und in einem 4 °C-Kühlschrank zu lagern, um eine Kontamination der Probe und eine Verdunstung des Lösungsmittels für zukünftige Beleuchtungsanwendungen zu verhindern.
2. Synthese von ZnGa2O4: Cr PLNPs
- 12 mM Ga(NO3)3.xH 2O, 7,2 mM ZnCl2 und 0,024 mM Cr(NO3)3,9H 2O werden in 30 mL deionisiertem Wasser gelöst.
- Geben Sie 1 ml PEG (300, Mw) in die Lösung. Fügen Sie der Lösung Ammoniumhydroxid (25%-28 Gew.-%) hinzu und rühren Sie vorsichtig um, um einen pH-Wert von 9,0-9,4 zu erreichen. Achten Sie darauf, die Rührgeschwindigkeit so zu steuern, dass sich die Lösung gründlich mischen kann, ohne auf das pH-Messgerät zu spritzen.
- Das Becherglas mit einer Siegelfolie abdecken und die Lösung bei Raumtemperatur 1 h lang umrühren. Versuchen Sie, die Exposition des Systems gegenüber Luft zu minimieren, um das Eindringen von Staub und die Verdunstung von Lösungsmitteln zu verhindern. Kontrollieren Sie gleichzeitig die Rührgeschwindigkeit, damit das System beim gründlichen Mischen nicht spritzt.
- Übertragen Sie die Lösung in einen mit Teflon ausgekleideten Autoklaven und lassen Sie sie 6 Stunden lang bei 220 °C laufen. Nehmen Sie den Behälter heraus, nachdem die Temperatur auf Raumtemperatur gesunken ist. Stellen Sie sicher, dass das Reaktionsgefäß vollständig abgekühlt ist und der Druck auf einen sicheren Bereich gesunken ist, bevor Sie mit nachfolgenden Operationen fortfahren, und vermeiden Sie den direkten Kontakt hoher Temperaturen mit der Haut.
- Die Reaktionslösung wird in zwei 50-ml-Zentrifugenröhrchen überführt. Spülen Sie den Reaktor mit 40 ml Ethanol und geben Sie dann die Ethanollösung in dieselben Zentrifugenröhrchen.
- 30 s vortexen, um die Lösung zu mischen, und dann die Probe bei 4000 x g für 15 min bei Raumtemperatur zentrifugieren und den Überstand entfernen.
- Geben Sie 10 mL deionisiertes Wasser in jedes Zentrifugenröhrchen und beschallen Sie es 5 Minuten lang, um das Produkt zu redispergieren.
- Geben Sie 20 ml Ethanol in jedes Zentrifugenröhrchen und wirbeln Sie es 30 s lang, um die Lösung gleichmäßig zu mischen. Das Produkt wird wie zuvor erwähnt bei Raumtemperatur (4000 x g, 15 min) weiter zentrifugiert und der Überstand wird verworfen.
- 5 Minuten lang mit Ultraschall beschallen, um das Produkt in 2 mL deionisiertem Wasser zu dispergieren, und versiegeln Sie die Probe zur Lagerung mit einer Siegelfolie.
3. Reinigung von Rohstoffen
- Reinigen Sie Methylmethacrylat (MMA) durch Säulenchromatographie wie unten beschrieben.
- Die Hälfte der Säule mit alkalischem Aluminiumoxid (100-200 mesh) füllen und mit einem Glasstab leicht verdichten. Achten Sie bei der Befüllung der Säule mit Aluminiumoxid auf eine gleichmäßige Verteilung und gleichmäßige Verdichtung des Füllstoffs, um die Abscheideleistung zu verbessern.
- Fügen Sie eine kleine Menge MMA hinzu und öffnen Sie den PTFE-Gaskolben unten. Sobald die Lösungsmittelschicht das gesamte Aluminiumoxid benetzt hat und die Flüssigkeit herausfließt, fügen Sie mehr MMA hinzu und wiederholen Sie diesen Vorgang mehrmals. Der Zeitpunkt, zu dem das Massenverhältnis des gesamten MMA zum basischen Aluminiumoxid hinzugefügt wird: 1:50 stellt das Ende des Prozesses dar.
- Die fertig gesammelte MMA-Probe in eine Glasflasche geben, mit einer Siegelfolie verschließen und bei 4 °C lagern.
ACHTUNG: Der gesamte Prozess sollte aufgrund der starken Flüchtigkeit von MMA in einem Abzug durchgeführt werden. Gleichzeitig sollten die Bediener Masken und Laborkittel tragen.
- Reinigen Sie Azobisisobutyronitril (AIBN) durch Rekristallisation wie unten beschrieben.
- Bereiten Sie eine 50 ml gemischte Lösung mit einem Volumenverhältnis von 7:3 aus Ethanol und destilliertem Wasser vor und erhitzen Sie die Lösung.
- Fügen Sie 5 g AIBN hinzu, wenn die Lösung kocht, und rühren Sie um, um die Lösung gleichmäßig zu vermischen.
- Entfernen Sie unlösliche Verunreinigungen durch Heißfiltration wie unten beschrieben.
- Legen Sie das Filterpapier eng an die Innenwand des dreieckigen Trichters und achten Sie darauf, dass sich das Filterpapier unter dem Rand des Trichters befindet.
- Legen Sie den Glasstab gegen den dreilagigen Teil des Filterpapiers. Wenn der Glasstab nicht gegen den dreischichtigen Abschnitt des Filterpapiers gelegt wird, kann er das Filterpapier durchstechen, was zu einer ineffizienten Filtration führt.
- Platzieren Sie die Spitze des Becherglases mit der Lösung in der Nähe des Glasstabes und gießen Sie es heiß ein. Der Zweck dieses Schritts besteht darin, das Spritzen von Flüssigkeitströpfchen zu verhindern.
- Spülen Sie das Becherglas mit 10 ml kaltem destilliertem Wasser und führen Sie den obigen Filtrationsprozess erneut durch. 3x wiederholen.
- Die Lösung wird durch die Abnahme der Löslichkeit während des Abkühlens übersättigt, was zur Ausfällung von Kristallen führt. Die gesammelte Lösung zum Abkühlen und Kristallisieren bei 4 °C in einen Kühlschrank stellen. Die Probe erscheint im Zustand von weißen, nadelartigen Kristallen.
- Die Probe mit Alufolie verschließen und bei 4 °C lagern.
VORSICHT Aufgrund der Toxizität von AIBN sollten während des Betriebs Schutzmaßnahmen ergriffen werden, wobei auch der Kontakt mit offenen Flammen, hohen Temperaturen und Oxidationsmitteln zu vermeiden ist.
4. Copolymerisation von Methylmethacrylat (MMA)
- Stellen Sie die Temperatur des Wasserbads auf 80 °C ein.
HINWEIS: Die Temperatur des Wassers hat einen starken Einfluss auf die Polymerisationsgeschwindigkeit und damit auf die Bildung des Endprodukts. Daher sollte streng sichergestellt werden, dass die Temperatur des Wasserbades nicht zu hoch ist. - Wiegen Sie 20 g MMA in eine 100-ml-Flasche in Auberginenform. Halten Sie den Behälter vor dem Experiment trocken.
HINWEIS: Die auberginenförmige Flasche wurde gewählt, um die Erwärmung des Wasserbades und den Ersatz von Luft durch Stickstoff im System zu erleichtern. Versuchen Sie, die Probe in einer gut belüfteten Umgebung zu wiegen, während Sie eine Maske tragen. - Die vorbereitete Methanollösung von Zn2GeO4: Mn wird in das Reaktionsgefäß gegeben.
- Die Probe mit Hilfe von Ultraschall ca. 10 min (240 W, 40 kHz) bei Raumtemperatur gründlich in MMA auflösen. Halten Sie das Reaktionsgefäß verschlossen, um eine Verdunstung des Lösungsmittels zu verhindern und zu hohe Temperaturen während des Ultraschallprozesses zu vermeiden.
- Geben Sie 0,012 g AIBN in die Lösung und mischen Sie die Lösung vollständig.
HINWEIS: AIBN sollte unter wasserfreien Bedingungen verwendet werden und sicherstellen, dass sich keine offene Flamme um den Versuchsbetrieb herum befindet. Achten Sie darauf, Schutzausrüstung zu tragen. - Den Kolben in ein 80 °C heißes Wasserbad stellen und die Luft mit N2 ca. 35 min lang aus dem Reaktionssystem spülen. Wenn die Reaktion kurz vor dem Ende steht, schütteln Sie den Reaktionsbehälter vorsichtig. Wenn die Lösung nicht kräftig schüttelt, beweist dies, dass die Reaktion erfolgreich war.
HINWEIS: Die Reaktionszeit ändert sich mit der Temperatur des Wasserbads. Stellen Sie sicher, dass die Temperatur des Wasserbades 80 °C erreicht, und beginnen Sie mit der Zeitmessung für 35 Minuten. - Nachdem die Reaktion beendet ist, stellen Sie das Reaktionsgefäß schnell in ein Eisbad, um es schnell abzukühlen.
HINWEIS: Dieser Prozess sollte so schnell wie möglich ablaufen, um eine übermäßige Vorpolymerisation von MMA zu vermeiden, und das Eisbad kann während des Reaktionsintervalls im Voraus vorbereitet werden. - Gießen Sie die Lösung langsam in eine zweidimensionale oder dreidimensionale Form, stellen Sie die Form 10 h lang bei 40 °C, 8 h bei 70 °C und weitere 2 h bei 100 °C in einen elektrischen thermostatischen Trockenofen, um das Zielmaterial zu erhalten.
- Schließen Sie den elektrischen thermostatischen Trockenschrank nach Beendigung der Reaktion und lassen Sie ihn auf Raumtemperatur abkühlen. Öffnen Sie den elektrischen thermostatischen Trockenschrank, um die Form zu entfernen, nachdem das Reaktionssystem ausreichend abgekühlt ist, um Hautverbrennungen durch direkten Kontakt zwischen hoher Temperatur und Körper zu vermeiden.
- Entfernen Sie vorsichtig die Form und setzen Sie die polymerisierte PMMA-Probe (ZGO: Mn-PMMA) für ca. 3 min einer UV-Lampe aus. Wenn beispielsweise eine transparente ZGO:Mn-PMMA-Folie durch einen schwarzen Pappausschnitt in Form des Buchstabens H ultraviolettem Licht ausgesetzt wird, erhält man ein entsprechendes Muster grüner phosphoreszierender Emission. Das Muster kann nach 5 min gelöscht werden. Anschließend kann der Vorgang wiederholt werden, indem ein weiterer schwarzer Pappaufsteller in Form verschiedener Buchstaben verwendet wird, wodurch neue Leuchtmuster erzeugt werden.
Ergebnisse
Das Synthesediagramm von Zn2GeO4: Mn (ZGO: Mn) PLNPs ist in Abbildung 1 dargestellt. Das amphiphile Polymer Polyethylenglykol (PEG) wird zugesetzt, um die ligandenfreien Zn2GeO4: Mn (ZGO: Mn) Nanostäbchen so zu modifizieren, dass sie sich besser in MMA-Medium auflösen. Zuerst werden die Transmissionselektronenmikroskopie (TEM), hochauflösende Transmissionselektronenmikroskopie-Bilder (HRTEM) von ZGO: Mn mit einem pH-Wert von 9,4 gesammelt (Abbildung 1), dann die dynamische Lichtstreuung (DLS), die Ergebnisse des Zetapotenzials und die Röntgenbeugung (XRD) von ZGO: Mn durchgeführt (Abbildung 2). Die Nachleuchtspektren und die zeitabhängigen Zerfallskurven von ZGO: Mn mit unterschiedlichem pH-Wert (pH = 6,0, 8,0, 9,4) in wässriger Lösung, angeregt bei 365 nm für 3 min, zusammen mit Photolumineszenzbildern und Nachleuchtbildern sind charakterisiert (Abbildung 3). Es werden die TEM-, XRD-, Nachleuchtspektren und Nachleuchtdämpfungskurve von ZnGa2O4: Cr erhalten (Abbildung 4). Das Copolymerisationsdiagramm von ZGO: Mn mit einem pH-Wert von 9,4 und MMA ist in Abbildung 5 dargestellt. Die Nachleuchtemissionsspektren und die Nachleuchtintensität als Funktion der Zeit für das auf PMMA (ZGO: Mn-PMMA) basierende Lumineszenzmaterial können erhalten werden, nachdem die Targets 3 min lang mit 365 nm bestrahlt und dann die Anregung eingestellt wurde. Wiederbeschreibbare Displays und im Dunkeln leuchtende Kunstverarbeitungsmaterialien in 2D- oder 3D-Formen können von der Kamera erfasst werden, wenn sie 3 Minuten lang mit UV-Licht bei 365 nm angeregt werden (Abbildung 5), was auf eine erfolgreiche Polymerisation von PLNPs in PMMA-Matrix für Beleuchtungsanwendungen hinweist.
Um hochauflösende Bilder der Transmissionselektronenmikroskopie (TEM) zu erhalten, wurden Messungen an einem Transmissionselektronenmikroskop durchgeführt, das bei einer Beschleunigungsspannung von 200 kV betrieben wurde. Ein XRD-System wurde verwendet, um die Röntgenbeugungsdaten (XRD) von PLNPs zu charakterisieren. Die Nachglühemissionsspektren und die Nachglühintensitäts-Abklingkurven in Abhängigkeit von der Zeit wurden mit Hilfe eines Spektrofluorometers durchgeführt. Eine Digitalkamera wurde verwendet, um Photolumineszenz- und persistente Lumineszenzbilder von PLNPs, 2D- und 3D-Leuchtmaterialien aufzunehmen.
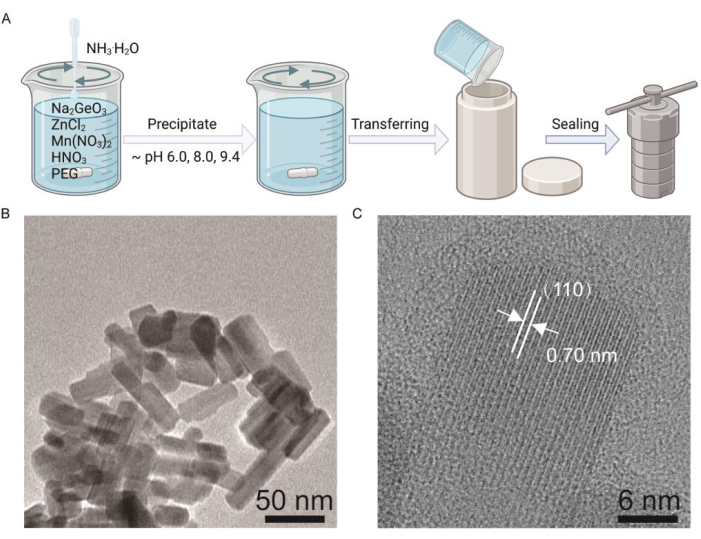
Abbildung 1: Synthese von Zn2GeO4: Mn (ZGO: Mn) PLNPs. (A) Das Synthesediagramm von ZGO: Mn Nanostäbchen. (B) Transmissionselektronenmikroskopie (TEM) von ZGO: Mn-Nanostrukturen mit einem pH-Wert von 9,4. Maßstab: 50 nm. (C) Hochauflösende Transmissionselektronenmikroskopie-Aufnahme (HRTEM) von ZGO: Mn mit einem pH-Wert von 9,4. Maßstab: 6 nm. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 2: Synthese von funktionellen Zn2GeO4: Mn Nanostrukturen. (A) Analyse der dynamischen Lichtstreuung (DLS) von Zn2GeO4: Mn-Polyethylenglykol (ZGO: Mn-PEG) dispergiert in deionisiertem Wasser und eine logarithmisch-normale Funktionsanpassung zur Erzielung der Größenverteilung. (B) Zeta-mögliche Ergebnisse von ZGO: Mn-PEG. (C) Röntgenbeugungsanalyse (XRD) von Zn2GeO4: Mn. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
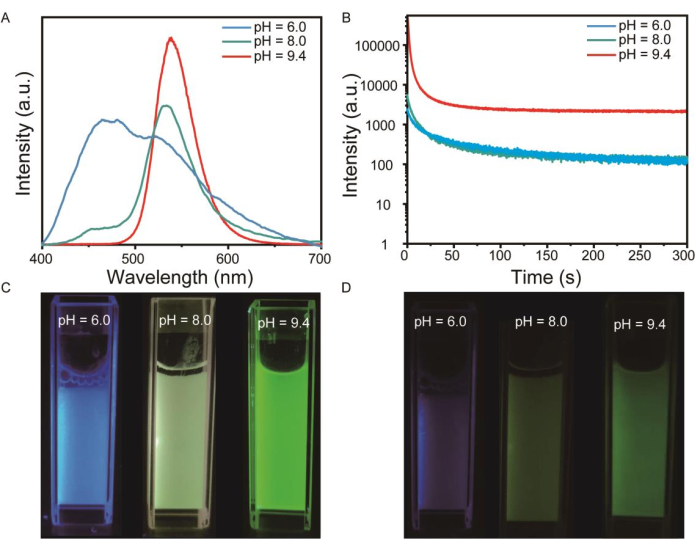
Abbildung 3: Charakterisierung von ZGO: Mn in wässriger Lösung. (A) Die Nachglühemissionsspektren von ZGO: Mn-PEG mit unterschiedlichem pH-Wert (pH = 6,0, 8,0, 9,4) angeregt um 365 nm für 3 min. (B) Zeitabhängige Nachglühabklingkurve von ZGO: Mn in Wasser bei 537 nm (angeregt mit 365 nm UV-Licht für 3 min). (C) Photolumineszenzbilder von ZGO:Mn-Nanostäbchen. (D) Bilder des Nachglühen-Lumineszenz-Zerfalls von ZGO: Mn. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
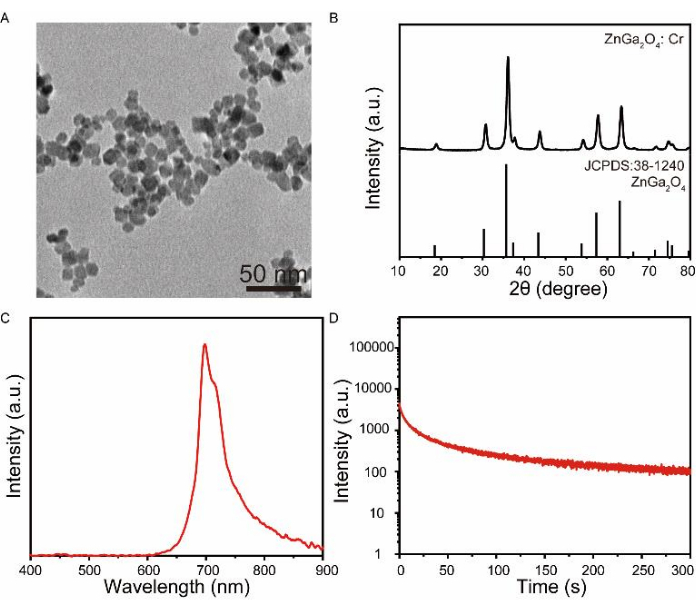
Abbildung 4: Charakterisierung von ZnGa2O4: Cr in wässriger Lösung. (A) TEM-Bilder von ZnGa2O4: Cr Nanopartikeln. Maßstab: 50 nm. (B) XRD-Analyse von ZnGa2O4: Cr. (C) Das Nachleuchtemissionsspektrum von ZnGa2O4: Cr nach 3 min Anregung bei 365 nm. (D) Zeitabhängige Nachleucht-Zerfallskurve von ZnGa2O4: Cr in Wasser bei 697 nm. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 5: PLNPs für wiederbeschreibbare Displays und 3D-Beleuchtungsanwendungen. (A) Schematische Darstellung der Copolymerisationsreaktion zwischen ZGO: Mn mit einem pH-Wert von 9,4 und Methylmethacrylat (MMA). (B) Das Nachleuchten-Emissionsspektrum von ZGO: Mn-PMMA wird 3 min lang um 365 nm angeregt. (C) Die zeitliche Variation von ZGO: Mn-PMMA bei 537 nm (3 min lang mit 365 nm UV-Licht angeregt). (D) Photoaktiviertes Nachleuchten für wiederbeschreibbare Anzeige und Datenspeicherung (geschrieben durch UV-Strahlung). (E) Lumineszenzaufnahmen einer transparenten 3D-Ente mit ZGO: Mn-PMMA nach UV-Bestrahlung. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Diskussion
In diesem Artikel wird eine Synthesemethode für persistente lumineszierende Nanomaterialien und die Polymerisation für Farbwiedergabeanwendungen vorgestellt. Die Materialien zeigten extrem stabile optische Eigenschaften und ein sichtbares Nachleuchten nach Beendigung der Anregung durch ultraviolettes Licht. Ein persistentes lumineszierendes Nanomaterial (Zn2GeO4: Mn) wurde mit einem hydrothermalen Verfahren mit unterschiedlichem pH-Wert hergestellt (Abbildung 1A). Das TEM-Bild zeigte, dass ZGO:Mn PLNPs mit einem pH-Wert von 9,4 stäbchenförmig waren und einen durchschnittlichen Durchmesser von etwa 65 nm aufwiesen (Abbildung 1B). Die hochauflösenden TEM-Bilder zeigten eine gute Kristallinität von Nanomaterialien, und der Abstand der angrenzenden Gitterstreifen parallel zur Stäbchenrichtung betrug 0,70 nm, was in guter Übereinstimmung mit dem (110) ebenen Abstand von Zn2GeO 4 52 war, was darauf hindeutet, dass alle Zn2GeO4: Mn hochkristallin waren (Abbildung 1C).
Darüber hinaus zeigten dynamische Lichtstreuungsdaten (DLS) von ZGO: Mn in deionisiertem Wasser, angepasst an eine logarithmisch-normale Funktion, dass die berechnete hydrodynamische Größe einen Durchmesser von 63 nm hatte und gut dispergiert war (Abbildung 2A). Die Ergebnisse des Zetapotenzials zeigten auch eine negative Oberfläche von ZGO: Mn (Abbildung 2B), was darauf hindeutet, dass die PLNPs in wässriger Lösung eine gute Löslichkeit und Stabilität aufwiesen. Das XRD-Spektrum von ZGO:Mn kann der rhomboedrischen Phase von Zn2GeO4 zugeordnet werden (Abbildung 2C).
Die optischen Eigenschaften von PLNPs könnten durch Einstellen des pH-Werts der Vorläuferlösung verändert werden. Die sichtbaren Emissionsspektren von ZGO: Mn-Lösung, die 3 min lang bei 365 nm angeregt wurde, zeigten, dass die PLNPs eine rote Verschiebung des Hauptemissionspeaks zeigten, wenn die Vorläuferlösung von sauer zu alkalisch wechselte (Abbildung 3A). Die Abklingkurve der Nachleuchtintensität über die Zeit wurde ebenfalls durch den pH-Wert beeinflusst, aber in jedem Fall kann die Emissionsintensität immer noch detektiert werden, wenn die Nachleuchtzeit 300 s erreicht, was die erfolgreiche Synthese von PLNPs mit unterschiedlichen optischen Eigenschaften bestätigt (Abbildung 3B). Die Photolumineszenzbilder (Abbildung 3C) und Nachleuchtbilder (Abbildung 3D) von PLNPs mit unterschiedlichen pH-Werten wurden von der Kamera aufgenommen. Die Ergebnisse zeigten, dass die Lösung eine hellere grüne Lumineszenz aufwies, wenn die Alkalität der Lösung zunahm.
PLNPs mit ZnGa2O4 als Matrix und Cr als Lumineszenzzentrum (ZnGa2O4: Cr) wurden synthetisiert, um die Vielseitigkeit dieses hydrothermalen Verfahrens hervorzuheben. Das TEM-Bild zeigte, dass ZnGa2O4: Cr kleiner und gleichmäßig dispergiert war (Abbildung 4A). Die XRD-Ergebnisse zeigten, dass alle Beugungspeaks gut mit denen des kubischen Spinells ZnGa2O4 übereinstimmten (Abbildung 4B). Das Nachleuchtemissionsspektrum zeigte, dass ZnGa2O4: Cr eine offensichtliche Nahinfrarotemission zeigte, nachdem es 3 Minuten lang durch ultraviolettes Licht angeregt wurde (Abbildung 4C). Die Emissionsintensität von ZnGa2O4: Cr bei 697 nm wurde über die Zeit überwacht, und die Ergebnisse zeigten, dass die Nachleuchtemission auch nach 300 s noch gesammelt werden konnte (Abbildung 4D).
Bei der hydrothermalen Synthese von PLNPs gibt es mehrere wichtige Schritte. Zunächst ist es notwendig, den pH-Wert der wässrigen Lösung während der Synthese von PLNPs streng zu kontrollieren. Der Säuregehalt und die Alkalität der Lösung können einen dramatischen Einfluss auf die Persistenz des Nachglühens und sogar auf die Farbe des Nachglühens haben. Zweitens ist es bei der Überwachung des pH-Werts der Lösung wichtig, die entsprechende Rührgeschwindigkeit einzustellen, um sicherzustellen, dass der Rührer nicht mit der pH-Sonde kollidiert, während die Lösung gleichmäßig gemischt wird. Wenn die Lösung schließlich 1 h lang in einer Umgebung mit einem Ziel-pH-Wert gerührt wird, halten Sie das Reaktionssystem so weit wie möglich verschlossen, um den Einfluss der Verflüchtigung von Ammoniakwasser zu vermeiden.
Darüber hinaus werden zweidimensionale und dreidimensionale Leuchtwerke durch PLNPs und MMA copolymerisiert, um PLNPs funktionaler zu machen (Abbildung 5A). Es wurde festgestellt, dass das Material, egal ob es sich um einen Film oder eine dreidimensionale Ente handelt, eine gute Nachleuchtfähigkeit aufweist (Abbildung 5B, C). Die 2D- und 3D-Materialien zeigen eine hellgrüne Lumineszenz nach Beendigung der Anregung durch ultraviolettes Licht, und die grünen Nachleuchtbilder sind nach 5 s immer noch zu sehen (Abbildung 4D,E), was darauf hindeutet, dass PLNPs unter der Aktivierung der UV-Lampe ein effektives Nachleuchten erzeugen können.
Bei der Durchführung der MMA-Polymerisation müssen einige Prozesse beachtet werden. Zunächst müssen die Rohstoffe, d.h. MMA und AIBN, gereinigt werden, um die Polymerisation nicht zu beeinträchtigen. Die zweite, bei Zugabe von Methanol dispergiert Zn2GeO4: Mn in die MMA-Lösung, dispergiert das gesamte System gleichmäßig mit Ultraschall. Drittens, denken Sie daran, den Zustand der Lösung die ganze Zeit zu beobachten. Das bedeutet, dass die Vorpolymerisation erfolgreich ist, wenn das Schwanken des Kolbens nur ein leichtes Schütteln der Lösung verursacht. Viertens sollte der Kolben unmittelbar nach der Vorpolymerisation in Eis gebadet werden, um eine übermäßige Polymerisation zu verhindern. Abschließend sollte die Temperatur während der Polymerisationsreaktion im elektrischen thermostatischen Trockenschrank so programmiert werden, dass eine homogene Matrix gebildet wird.
Zusammenfassend erwarten wir, dass dieses Protokoll nicht nur ein detailliertes experimentelles Verfahren für die hydrothermale Synthese von langlebigen Emissionsnanomaterialien bietet, sondern auch eine Methode zur Copolymerisation von PLNPs und MMA einführt, um weitere UV-vermittelte wiederbeschreibbare und lumineszierende Anwendungen zu erreichen. Noch wichtiger ist, dass die optischen Eigenschaften von PLNPs weiter abgestimmt werden können, um verschiedene Nachleuchtfarben zu haben, indem verschiedene Defekte, Lumineszenzzentren und pH-Werte auf der Grundlage dieser Methode angepasst werden. Darüber hinaus kann das Verfahren der Copolymerisation von PLNPs und Polymeren in der Kunstproduktion weiter verwendet werden. Diese Vorteile machen PLNPs zu idealen Materialien für Lumineszenz- und Bildgebungsanwendungen. Andererseits kann die hydrothermale Synthesemethode die Anwendung bestimmter Materialien, insbesondere temperaturempfindlicher Substanzen, einschränken, da die Reaktion relativ hohe Temperaturen erfordert. Daher muss die geeignete Synthesemethode auf der Grundlage spezifischer Anwendungen und Anforderungen ausgewählt werden.
Offenlegungen
Es gibt nichts offenzulegen.
Danksagungen
Die Autoren danken der National Natural Science Foundation of China (82001945), dem Shanghai Pujiang Program (20PJ1410700) und dem Starting Grant der ShanghaiTech University. Die Autoren danken dem Centre for High-resolution Electron Microscopy (ChEM), School of Physical Science and Technology, ShanghaiTech University (No. EM02161943) für die Unterstützung der Materialcharakterisierung. Die Autoren danken dem Analytical Instrumentation Center (#SPST-AIC10112914), der School of Physical Science and Technology der ShanghaiTech University für die Unterstützung bei Spektraltests und XRD-Tests. Die Autoren danken auch Prof. Jianfeng Li für die Hilfe bei den Materialcharakterisierungen.
Materialien
| Name | Company | Catalog Number | Comments |
| azobisisobutyronitrile (99%) | Macklin | A800354 | Further purification required |
| methyl methacrylate(99%) | Sigma-Aldrich | M55909 | Further purification required |
| deionized water | Merck | ZEQ7016T0C | Milli-Q Direct Water Purification System |
| alkaline aluminum oxide (100-200 mesh) | Macklin | A800033 | |
| ammonium hydroxide (25%-28%, wt) | Macklin | A801005 | |
| beaker | Synthware | B220100 | |
| chromium(III) nitrate nonahydrate (99.95%) | Aladdin | C116448 | |
| centrifuge | ThermoFisher Scientific | 75004250 | |
| column | Synthware | C184464CR | |
| digital camera | Canon | EOS M50 Mark II | |
| electric thermostaticdrying oven | Longyue | LDO-9036A | |
| ethanol (99.7%) | Greagent | 1158566 | |
| gallium nitrate hydrate(99.9%) | Aladdin | G109501 | |
| germanium oxide (99.99%) | Sinopharm Chemical ReagentCo., Ltd | 51009860 | |
| glass rod | Sinopharm Chemical ReagentCo., Ltd | 91229401 | |
| powder X-Ray Diffractometer | D2 PHASER DESKTOP XRD | BRUKER | |
| manganese nitrate (98%) | Macklin | M828399 | |
| methanol (99.5%) | Greagent | 1226426 | |
| nitric acid (65.0-68.0%, wt) | Sinopharm Chemical ReagentCo., Ltd | 10014508 | |
| pH meter | Shanghai Leici Sensor Technology Co., Ltd | PHS-3C | |
| polyethylene glycol (300, Mw) | Adamas | 01050882(41713A) | |
| sealing film | Parafilm | 2025722 | |
| sodium hydroxide (GR) | Sinopharm Chemical ReagentCo., Ltd | 10019764 | |
| spectrometer | Horiba | Fluorolog-3 | |
| transmission electron microscope | JEOL | JEM-1400 Plus | |
| transmission electron microscope | JEOL | 2100 Plus | |
| triangular funnel | Synthware | F181975 | |
| ultrasound machine | centrifuge | JP-040S | |
| zinc chloride (98%) | Greagent | 01113266/G81783A |
Referenzen
- Xu, J., Tanabe, S. Persistent luminescence instead of phosphorescence: History, mechanism, and perspective. J Luminesc. 205, 581-620 (2019).
- Harvey, E. N. A history of luminescence from the earliest times until 1900. , American Philosophical Society. Philadelphia, USA. (1957).
- Hölsä, J. Persistent luminescence beats the afterglow: 400 years of persistent luminescence. Electrochem Soc Interface. 18 (4), 42(2009).
- Lastusaari, M., et al. The Bologna stone: history's first persistent luminescent material. Euro J Mineral. 24 (5), 885-890 (2012).
- Liu, Y., Kuang, J., Lei, B., Shi, C. Color-control of long-lasting phosphorescence (LLP) through rare earth ion-doped cadmium metasilicate phosphors. J Mater Chem. 15 (37), 4025-4031 (2005).
- Matsuzawa, T., Aoki, Y., Takeuchi, N., Murayama, Y. A new long phosphorescent phosphor with high brightness, SrAl2O4:Eu2+, Dy3+. J Electrochem Soc. 143 (8), 2670(1996).
- Guo, H., et al. Cyan emissive super-persistent luminescence and thermoluminescence in BaZrSi3O9:Eu2+,Pr3+ phosphors. J Mater Chem C. 5 (11), 2844-2851 (2017).
- Yuan, J., Dong, J., Lei, S., Hu, W. Long afterglow MOFs: a frontier study on synthesis and applications. Mater Chem Front. 5 (18), 6824-6849 (2021).
- Fu, X., Zheng, S., Shi, J., Li, Y., Zhang, H. Long persistent luminescence property of a novel green emitting SrLaGaO4 : Tb3+ phosphor. J Luminesc. 184, 199-204 (2017).
- Zhuang, Y., Wang, L., Lv, Y., Zhou, T. L., Xie, R. J. Optical data storage and multicolor emission readout on flexible films using deep-trap persistent luminescence materials. Adv Func Mater. 28 (8), 1705769(2018).
- Singh, S. K. Red and near infrared persistent luminescence nano-probes for bioimaging and targeting applications. RSC Adv. 4 (102), 58674-58698 (2014).
- Matuszewska, C., Elzbieciak-Piecka, K., Marciniak, L. Transition metal ion-based nanocrystalline luminescent thermometry in SrTiO3:Ni2+,Er3+ nanocrystals operating in the second optical window of biological tissues. J Phys Chem C. 123 (30), 18646-18653 (2019).
- Zhuang, Y., Katayama, Y., Ueda, J., Tanabe, S. A brief review on red to near-infrared persistent luminescence in transition-metal-activated phosphors. Optic Mater. 36 (11), 1907-1912 (2014).
- Norrbo, I., et al. Lanthanide and heavy metal free long white persistent luminescence from Ti doped Li-hackmanite: A versatile, low-cost material. Adv Func Mater. 27 (17), 1606547(2017).
- Hoang, K. Defects and persistent luminescence in Eu-doped SrAl2O4. Phys Rev Appl. 19 (2), 024060(2023).
- Viana, B., et al. Long term in vivo imaging with Cr3+ doped spinel nanoparticles exhibiting persistent luminescence. J Luminesc. 170 (3), 879-887 (2016).
- Ding, Y., So, B., Cao, J., Langenhorst, F., Wondraczek, L. Light delivery, acoustic read-out, and optical thermometry using ultrasound-induced mechanoluminescence and the near-infrared persistent luminescence of CaZnOS:Nd3. Adv Optic Mater. 11 (17), 2300331(2023).
- Ge, S., et al. Realizing color-tunable and time-dependent ultralong afterglow emission in antimony-doped CsCdCl3 metal halide for advanced anti-counterfeiting and information encryption. Adv Optic Mater. 11 (14), 2300323(2023).
- Zhai, L., Ren, X. M., Xu, Q. Carbogenic π-conjugated domains as the origin of afterglow emissions in carbon dot-based organic composite films. Mater Chem Front. 5 (11), 4272-4279 (2021).
- Miao, Q., et al. Molecular afterglow imaging with bright, biodegradable polymer nanoparticles. Nat Biotechnol. 35 (11), 1102-1110 (2017).
- Zhou, B., Xiao, G., Yan, D. Boosting wide-range tunable long-afterglow in 1D metal-organic halide micro/nanocrystals for space/time-resolved information photonics. Adv Mater. 33 (16), e2007571(2021).
- Yang, H., et al. Highly flexible dual-mode anti-counterfeiting designs based on tunable multi-band emissions and afterglow from chromium-doped aluminates. J Mater Chem C. 8 (46), 16533-16541 (2020).
- Chen, Y., et al. Synaptic plasticity powering long-afterglow organic light-emitting transistors. Adv Mater. 33 (39), e2103369(2021).
- Qu, B., Wang, J., Liu, K., Zhou, R., Wang, L. A comprehensive study of the red persistent luminescence mechanism of Y2O2S:Eu,Ti,Mg. Phys Chem Chem Phys. 21 (45), 25118-25125 (2019).
- Zhang, J., Jiang, C. Luminescence properties of Ca14 Mg2(SiO4)8 :Eu2+ from various Eu2+ sites for white-light-emitting diodes. Mater Res Bull. 60, 467-473 (2014).
- Yamamoto, H., Matsuzawa, T. Mechanism of long phosphorescence of SrAl2O4: Eu2+, Dy3+ and CaAl2O4 Eu2+, Nd3+. J Luminesc. 72-74, 287-289 (1997).
- Rojas-Hernandez, R. E., Rubio-Marcos, F., Rodriguez, M. Á, Fernandez, J. F. Long lasting phosphors: SrAl2O4:Eu, Dy as the most studied material. Renew Sustain Ener Rev. 81 (2), 2759-2770 (2018).
- Lin, Y., Tang, Z., Zhang, Z., Wang, X., Zhang, J. Preparation of a new long afterglow blue-emitting Sr2MgSi2O7-based photoluminescent phosphor. J Mater Sci Lett. 20, 1505-1506 (2001).
- Katayama, Y., Viana, B., Gourier, D., Xu, J., Tanabe, S. Photostimulation induced persistent luminescence in Y3Al2Ga3O12:Cr3. Optic Mater Exp. 6 (4), 1405-1413 (2016).
- Li, H., et al. A strategy for developing thermal-quenching-resistant emission and super-long persistent luminescence in BaGa2O4:Bi3+. J Mater Chem C. 7 (42), 13088-13096 (2019).
- Lei, B., et al. Luminescent properties of orange-emitting long-lasting phosphorescence phosphor Ca2SnO4:Sm3. Solid State Sci. 13 (3), 525-528 (2011).
- Lei, B., Liu, Y., Ye, Z., Shi, C. Luminescence properties of CdSiO3:Mn2+ phosphor. J Luminesc. 109 (3-4), 215-219 (2004).
- Wu, Y., et al. Near-infrared long-persistent phosphor of Zn3Ga2Ge2O10: Cr3+ sintered in different atmosphere. Spectrochim Acta A Mol Biomol Spectrosc. 151, 385-389 (2015).
- Zhang, S., Hu, Y. Photoluminescence spectroscopies and temperature-dependent luminescence of Mn4+ in BaGe4O9 phosphor. J Luminesc. 177, 394-401 (2016).
- Wang, J., et al. One-dimensional luminous nanorods featuring tunable persistent luminescence for autofluorescence-free biosensing. ACS Nano. 11 (8), 8185-8191 (2017).
- Wang, T., Xu, X., Zhou, D., Qiu, J., Yu, X. Red phosphor Ca2Ge7O16:Eu3+ for potential application in field emission displays and white light-emitting diodes. Mater Res Bull. 60, 876-881 (2014).
- Ding, D., et al. X-ray-activated simultaneous near-infrared and short-wave infrared persistent luminescence imaging for long-term tracking of drug delivery. ACS Appl Mater Interfaces. 13 (14), 16166-16172 (2021).
- Zhao, X., Wei, X., Chen, L. J., Yan, X. P. Bacterial microenvironment-responsive dual-channel smart imaging-guided on-demand self-regulated photodynamic/chemodynamic synergistic sterilization and wound healing. Biomater Sci. 10 (11), 2907-2916 (2022).
- Huang, K., et al. Enhancing light and X-ray charging in persistent luminescence nanocrystals for orthogonal afterglow anti-counterfeiting. Adv Func Mater. 31 (22), 2009920(2021).
- Sun, L., Qi, Y., Jia, C. J., Jin, Z., Fan, W. Enhanced visible-light photocatalytic activity of g-C3N4/Zn2GeO4 heterojunctions with effective interfaces based on band match. Nanoscale. 6 (5), 2649-2659 (2014).
- Gupta, S. K., Sudarshan, K., Modak, B., Gupta, R. Interstitial zinc boosted light tunability, afterglow, and ultrabright white emission in zinc germanate (Zn2GeO4). ACS Appl Electron Mater. 5 (2), 1286-1294 (2023).
- Calderón-Olvera, R. M., et al. Persistent Luminescence Zn2GeO4:Mn2+ nanoparticles functionalized with polyacrylic acid: One-pot synthesis and biosensing applications. ACS Appl Mater Interfaces. 15 (17), 20613-20624 (2023).
- Li, Q., Miao, X., Wang, C., Yin, L. Three-dimensional Mn-doped Zn2GeO4 nanosheet array hierarchical nanostructures anchored on porous Ni foam as binder-free and carbon-free lithium-ion battery anodes with enhanced electrochemical performance. J Mater Chem A. 3 (42), 21328-21336 (2015).
- Lai, B., et al. A phosphorescence resonance energy transfer-based "off-on" long afterglow aptasensor for cadmium detection in food samples. Talanta. 232, 122409(2021).
- Chi, F., et al. Multimodal temperature sensing using Zn2GeO4:Mn2+ phosphor as highly sensitive luminescent thermometer. Sens Actuat B: Chem. 296, 126640(2019).
- Yin, S., Chen, D., Tang, W., Peng, Y. Synthesis of CaTiO3:Pr persistent phosphors by a modified solid-state reaction. Mater Sci Eng: B. 136 (2-3), 193-196 (2007).
- le Masne de Chermont, Q., et al. Nanoprobes with near-infrared persistent luminescence for in vivo imaging. Proc Natl Acad Sci U S A. 104 (22), 9266-9271 (2007).
- Li, Z., Shi, J., Zhang, H., Sun, M. Highly controllable synthesis of near-infrared persistent luminescence SiO2/CaMgSi2O6 composite nanospheres for imaging in vivo. Opt Express. 22 (9), 10509-10518 (2014).
- Sera, M., et al. Morphology control and synthesis of afterglow materials with a SrAl2O4 framework synthesized by Surfactant-Template and hydrothermal methods. Chem Phys Lett. 780, 138916(2021).
- Kim, J., Lee, C. K., Kim, Y. J. Low temperature synthesis of Lu3Al5-xGaxO12:Ce3+,Cr3+ powders using a sol-gel combustion process and its persistent luminescence properties. Optic Mat. 104, 109944(2020).
- Xu, Z., et al. Ln(3+) (Ln = Eu, Dy, Sm, and Er) ion-doped YVO(4) nano/microcrystals with multiform morphologies: hydrothermal synthesis, growing mechanism, and luminescent properties. Inorg Chem. 49 (4), 6706-6715 (2010).
- Wang, Y., et al. Zn2GeO4−x/ZnS heterojunctions fabricated via in situ etching sulfurization for Pt-free photocatalytic hydrogen evolution: interface roughness and defect engineering. Phys Chem Chem Phys. 22 (18), 10265-10277 (2020).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten