Method Article
標的新生児心エコー検査を用いた新生児集中治療室における血行動態の精度
要約
ここに提示されるのは、新生児集中治療室で訓練を受けた新生児科医による包括的な新生児心エコー検査を実施するためのプロトコルです。訓練を受けた個人は、相談の役割で心臓機能、全身および肺の血行動態の縦断的評価を提供します。この原稿には、完全に訓練された新生児血行動態の専門家になるための要件も記載されています。
要約
標的新生児心エコー検査(TnECHO)とは、包括的な心エコー検査評価と生理学的データを使用して、病気の新生児の発達血行動態に関する正確で信頼性の高いリアルタイムの情報を取得することを指します。包括的な評価は、個々の測定の信頼性の問題を克服し、心血管系の障害を早期に認識し、診断精度の向上とタイムリーな管理を促進するマルチパラメトリックアプローチに基づいています。TnECHO主導の研究は、病気のメカニズムの理解を深め、リスクのある集団を特定するための予測モデルの開発につながりました。この情報は、診断印象を定式化し、心血管治療の選択のための個別のガイダンスを提供するために使用できます。TnECHOは、新生児血行動態の高度なトレーニングを受けた新生児科医が包括的で標準化されたTnECHO評価を行う専門家コンサルティングモデルに基づいています。限定的で短時間の1回限りの評価を提供するポイントオブケア超音波検査(POCUS)との違いは重要です。新生児血行動態トレーニングは、画像取得、測定分析、および血行動態の知識(生理学、薬物療法)を最適化して、心血管の意思決定をサポートするように設計された1年間の構造化されたプログラムです。血行動態の専門知識を持つ新生児科医は、正常な解剖学的構造からの逸脱を認識し、構造異常の可能性の症例を適切に参照するように訓練されています。新生児の血行動態トレーニングの概要、標準化されたTnECHOイメージングプロトコル、および血行動態的に重要な動脈管開存症における代表的なエコー所見の例を提供します。
概要
標的新生児心エコー検査 (TnECHO) とは、心筋機能、全身血流、肺血流、心臓内シャントと心外シャントを縦断的に評価するための心エコー検査のベッドサイド使用を指します1。TnECHOを臨床所見と統合すると、診断、治療介入のガイダンス、および治療に対する反応の動的モニタリングに不可欠な情報を提供できます2。TnECHOは、訓練を受けた新生児科医が特定の臨床的質問に応じて頻繁に実施し、患者の臨床状態を補完および提供する生理学的洞察を補完および提供できる血行動態情報を取得し、正確な心血管ケアを実現します3。過去10〜15年間で、TnECHOサービスは、オーストラリア、ニュージーランド、ヨーロッパ、および北米の複数の三次新生児集中治療室(NICU)に組み込まれており、特に複雑な重症度の高い症例の管理に組み込まれています4,5,6,7,8。現在までに、米国には8つのセンターがあり、訓練を受けた開業医がTnECHOサービスを提供しており、新生児の血行動態研究に関与するセンターの数は増え続けています。さらに、米国心エコー学会(ASE)に新生児血行動態およびTnECHO特別利益グループ(SIG)が設立されたことは、小児心臓病学との学術的協力を強化し、この分野でのさらなる成長のための強力な政治的プラットフォームを作成します9。
新生児血行動態トレーニングは、トレーニングを受けた個人が高レベルのイメージングを達成し、包括的な心血管の意思決定を提供できるように設計されています。2011年には、ヨーロッパと北米の専門機関によって承認されたTnECHOのトレーニング推奨事項が発表されました3。現在、50人以上の北米の新生児科医がTnECHOの正式なトレーニングを修了しています。注目すべきは、血行動態の臨床医の50%以上が、この分野の新たな学術的リーダーと見なされており、これは予期せぬことですが、正式なトレーニングの非常に必要な利点です。 図1 は、血行動態のトレーニングと認定をまとめたものです。
TnECHOサービスの重要な要素には、専用の心エコー装置へのアクセスが含まれます。これにより、画像取得を即座に利用でき、縦断的なフォローアップが可能になります(図2および図3)。データベース/画像アーカイブには、心エコー検査検査所認定のための社会委員会10の推奨事項に従って、ビデオの劣化、標準化されたレポート、および長期保存なしで即時再生を提供する機能が含まれている必要があります。標準的なTnECHOには、新生児期の複雑な心血管生理学を包括的に評価できる主要な測定値が含まれています。これには、左心室(LV)機能、右心室(RV)機能、心臓内シャント(心房レベルシャントおよび乳管レベルシャント)、動脈管開存症(PDA)の血行動態効果、右心室収縮期血圧(RVSp)/肺動脈(PA)圧、全身および肺血流、心嚢液の存在、血栓、および中心線の位置が含まれます。表1は、これらの測定データの一部を取得するために一般的に使用される心エコー検査用語を示しています。評価は、症状に基づく適応症と疾患に基づく適応症の両方に対して実施できます。補足ファイル1および表2は、出生後7日間の正期産新生児の推奨測定値、解釈、および参照範囲を含む包括的な新生児心エコー検査評価の概要を示しています。
LV収縮期機能の評価は、重症新生児の病因の描写と血行動態の不安定性の管理に役立つため、重要な要素です。定性的評価は観察者間および観察者内の変動性が生じやすいため、定量的評価が推奨されます11。シンプソン複葉機法や面積長法などの多面法を用いた駆出率の計算は、局所的な壁運動異常を見逃す可能性があり、中隔平坦化の存在下では不正確であるMモード推定よりも優れている12。LV拡張期機能障害は、新生児の血行動態における新しい概念です。但し、データは限られた13に残る。
RVは移行循環における優勢な心室であり、多くの新生児疾患は右心臓の病状と関連しているため、RV機能の評価は新生児の生活において非常に重要です。同様の理由で、LV収縮期機能の評価では、主観的な評価は避けるべきです14。しかし、RVの特殊な形状、高度に軌跡のある表面、およびLVに巻き付けられた位置により、RV機能の測定はより困難になります。それにもかかわらず、いくつかの信頼できる定量的パラメータが研究され、規範的なデータが公開されています15,16。フラクショナル・エリア・チェンジ(FAC)と三尖弁環状平面収縮期エクスカーション(TAPSE)は、使用される推奨される定量的測定値の2つです17。
心臓内シャント(心房および乳管レベル)は、包括的な新生児心エコー検査評価のもう一つの重要な側面です。ほとんどの場合、左心房圧は右心房圧(RA)に比べて高く、左から右へのシャントになります。ただし、新生児期には、双方向シャントが正常である可能性があります。心房レベルで右から左へのシャントがある場合は、特に肺高血圧症(PH)に関連する右側の充填圧力の上昇を考慮する必要がありますが、心室コンプライアンス/圧力の変動も心周期のさまざまな時点で心房圧に影響を与える可能性があるため、これを単独で使用するべきではありません。.
動脈管開存症(PDA)の評価には、治療の決定を支援するために使用される乳管シャント方向の決定と乳管圧勾配の測定を含める必要があります。弓側性評価も重要であり、特に外科的PDA結紮を検討する場合には重要です。PDAシャントの方向は、大動脈圧とPA圧の差、および肺循環と全身循環の相対抵抗を反映しています。血行動態の重要性を判断するために使用される1つの要因は、下行する胸部または腹部の大動脈における全拡張期逆行性の流れの存在です18。血行動態の重要性は、包括的な測定によって体積過負荷の程度を定量化することによってさらに評価することができる19。アイオワPDAスコアなど、心臓への容積負荷およびPDAシャントに関連する全身性低灌流の代理的結果を評価するスコアリングシステムが公開されています(表3)19,20,21アイオワPDAスコアは、PDAシャントの血行動態の重要性を決定する際の客観性を高めるために、アイオワ大学で臨床的に採用されています。6を超えるスコアは、血行動態的に有意な動脈管開存症(hsPDA)を示唆しています19。
肺血行動態の評価では、RVSpの絶対値は三尖弁逆流(TR)勾配の測定によって推定されます。連続波ドップラーは、三尖弁を通る最大三尖弁逆流速度を測定するために使用され、三尖弁逆流ピーク速度と呼ばれます。通常、5 mmHgのRA圧力を想定して計算します。次に、RVSpは、簡略化されたベルヌーイ式22を使用して計算されます。
RVSp = 4 × (三尖弁逆流ピーク速度 [m/s])2 + RA 圧
時折、代替として、PDAを横切るドップラー由来の圧力勾配が、PA(肺動脈)圧の計算に使用される23。ただし、TRジェットは慢性PH24、25、26の患者の約50%にのみ存在します。このような状況では、LV真円度の尺度である収縮末期偏心指数(sEI)などの測定値は、心室間の相対圧力を示している可能性があります。全身性高血圧症の患者では、LV拡張末期血圧の上昇により軽度の疾患が検出されない可能性があるため、この測定値は注意して解釈する必要があります。. 図4 は、肺高血圧症のアルゴリズムと包括的な新生児心エコー検査評価ガイドラインの例を示しています。
LVストローク量の評価では、大動脈弁の高さで頂端の5チャンバービューでパルスドップラートレースを測定して、時間速度積分(TVI)を取得します。これは、胸骨傍長軸ビューでの大動脈弁輪径の測定と組み合わされます。次の式による計算を使用して、LV出力27を推定します。
LV出力(mL / min / kg)=(TVI [cm] × π x [D / 2] 2 [cm2] ×心拍数)/体重。
ただし、PDAの存在下では、LV出力測定値は、PDAレベル3でのシャントに続発する全身血流を反映していません。腹腔動脈、上腸間膜動脈、および中大脳動脈のドップラー尋問による末梢臓器への拡張期の流れは、PDAによる全身の盗みを示すことができますが、代わりに、臓器の抵抗を反映している可能性があり、高抵抗の設定では拡張期の流れが低いか存在しないことが見られます。
TnECHOは、心臓内血栓、心嚢液の存在、およびその血行動態の重要性の検出、心嚢穿刺のガイド、ならびに末梢動脈ライン、末梢に挿入された中心カテーテル、および臍帯静脈カテーテルの配置の支援にも利用することができる28。ここでは、TnECHOと血行動態情報を取得するための包括的なアプローチを示すために、イメージングプロトコルとTnECHOサービスの要素について説明します(図3)。
プロトコル
このプロトコルは、施設のヒト研究倫理委員会によって承認され、手順の前に患者から書面による同意が得られました。
1. 事前準備
- 画像取得には、2次元(2D)、Mモード、フルドップラー機能、および心電図の同時トレース表示機能を備えた超音波システムを使用します。
- 5〜6 MHz(乳児>2 kg)および8〜12 MHz(乳児< 2 kg)の多周波プローブが、適切なサイズの乳児で使用できることを確認してください。一般的に使用される心エコー検査の用語は、プローブの配置例と対応する代表的な心エコー図図を示す補足ファイル1の表1に記載されています。
注:最初の心エコー検査研究には、米国心エコー学会(ASE)ガイドライン11に従って、セグメントアプローチを使用した心臓の解剖学的および生理学の完全な形態学的および血行動態学的評価が含まれます。
2.心エコー検査評価のための患者の準備
- 患者への感染予防のために、施設の特定の感染管理予防ガイドラインに従ってください。
- 赤ちゃんの胸部と上腹部をほどいて露出させ、邪魔になる可能性のあるリードを慎重に動かし、皮膚の完全性に特に注意を払います。
- インキュベーターの開口部を最小限にすることで、患者の体温と中性の熱環境を維持します。
- スキャン中は、心肺の継続的なモニタリングを確保してください。
3. プローブと画像の取得
- 心エコー検査装置を接続し、心電図コードを取り付け、機械が起動するのを待っている間、超音波ジェルを102°Fに温めます。
- 画像が適切な患者カルテにリンクされるように、患者識別子を確認します。
- 患者様のサイズに適したプローブをお選びください(患者様≥2kg)には6S-D心臓セクター超音波トランスデューサ、患者様<2kg)には12S-D心臓セクター超音波トランスデューサをお選びください。
注:このプロトコルでは、12S-Dトランスデューサを使用する場合について説明します。 - 画像の奥行きと明るさを調整します。
- 以下に概説する各手順の後に、保存する画像 ストア をクリックします。
注意: 最低3回の心周期を取得する必要があります。
4. 画像取得
- 頂端ビュー
- まずは、頂端の4室ビューから。位置マーカー(ノッチ)を左肩に向かって傾けて、プローブを頂点に置きます( 補足を参照 file 1)。 [2D ] をクリックして、最初の画像を開始します。インタラクティブタッチスクリーンの上 /下 ボタンをクリックして、画面下部の心臓の頂点を方向付けます。
注:慢性肺疾患が進行している乳児では、このビューはより外側に、場合によってはより内側に得られます。幅リセットボタンを時計回りに回すことにより、両側心室壁を完全に視覚化できるように、セクター幅を広げる必要がある場合があります。 - 取得した画像は、心臓の4つの部屋を示しています。最適なビューが得られたら、ゲイン、深度、グレースケールを調整して画質を最適化します。コンソールの 奥行き つまみを回して奥行きを調整し、奥行きを3.5cmまで伸ばし、心房と心室の視覚化を完成させます。 画像ストア をクリックして、2D 画像を保存します。
- コンソールの [色 ] をクリックします。トラックボールを使用して、三尖弁の上にカラーボックスを置きます。 速度リセット を70〜80 cm / sのカラースケールに調整します。
注:収縮期中に三尖弁を通る青い逆流ジェットは、三尖弁逆流の証拠です。 - カーソルをクリックし、トラックボールを使用してサンプルゲートを三尖弁の上に配置します。CWボタンをクリックして、三尖弁逆流のピーク速度を取得します。[画像ストア>フリーズ] をクリックします。
- [ 2D ] をクリックして画面をリセットします。 カラーボタン>同時 ボタンをクリックして、カラードップラーをアクティブにします。トラックボールを使用して、カラーボックスを肺静脈の上に置きます。
- 速度を調整し、カラードップラーを50〜60cm / sに下げます。カーソルをクリックし、サンプルゲートを肺静脈の上に置き、PWをクリックしてパルス波を取得します。保存するには、[画像ストア>フリーズ] をクリックします。
注:ドップラー心エコー検査で記録された肺静脈流速のトレースは、収縮期成分(S)、拡張期成分(D)の3つの成分で記述されることが多く、場合によっては心房収縮中に流れが逆転することがあります(A)。 - [ 2D ] をクリックして画像をリセットします。 カーソル をクリックし、開いた僧帽弁の先端にサンプルゲートを配置します。 PW をクリックして僧帽弁E/Aを取得します。 freeze > image storeをクリックします。
- [2D]をクリックして画面をリセットし、[カラー>同時]をクリックしてカラードップラーをアクティブにします。僧帽弁のすぐ上から頂点まで覆うようにカラーボックスを増やします。手順4.1.3と同様に設定を行います。[イメージ ストア] をクリックします。
- プローブを時計回りに回転させて開き、左心室流出路を視覚化します。 カーソル をクリックし、僧帽弁の流入と流出の接合部にサンプルゲートを配置し、 PW をクリックしてパルス波を取得します。[ 画像ストア>固定 ] をクリックして、画像を保存します。
- 2Dをクリックして、左心室流出路(LVOT)が開いた状態で画像をリセットします。サンプルゲートを大動脈弁に置き、手順4.1.9を繰り返して画像を取得します。
注:等量緩和時間(IVRT)の測定を行うときは、収縮期の終わりと拡張期の始まりの間の間隔が見られるように掃引速度(25〜50 mm / s)を下げるのが最適です。 - LVOTに焦点を合わせるには、 幅 ボタンを回してセクター幅を狭くし、ヒンジポイントの高さで大動脈弁の上にサンプルゲートを配置し、手順4.1.9を繰り返します。
注意: LVOTを最適に位置合わせするには、時計回りに回転したり、左股関節に向かって移動したりする必要がある場合があります。左心室出力を正確に測定するには、共鳴線がLVOTに平行であることが不可欠です。速度時間積分(VTI)の計算には、エンベロープのトレースが必要です。
- まずは、頂端の4室ビューから。位置マーカー(ノッチ)を左肩に向かって傾けて、プローブを頂点に置きます( 補足を参照 file 1)。 [2D ] をクリックして、最初の画像を開始します。インタラクティブタッチスクリーンの上 /下 ボタンをクリックして、画面下部の心臓の頂点を方向付けます。
- アピカル4チャンバービューからの組織ドップラーイメージング
- [ 2D ] をクリックして画像をリセットします。 [画像ストア ] をクリックして、2D 画像を保存します。
- コンソールの TVI ボタンをクリックして、組織ドップラーイメージングをアクティブにします。 [イメージ ストア ] をクリックして、イメージの頂点をベースに保存します。
- 幅ボタンを回してセクター幅を狭くし、>200フレーム/秒(fps)の目標フレームレートでセプタムに問い合わせます。中隔壁の僧帽弁輪の下にサンプルゲートを置き、ステップ4.1.9を繰り返します。
注:これは、収縮期に正の速度、拡張期に負の速度を持つ弁輪からの組織速度曲線を提供します。収縮期のピーク速度はS'、初期拡張期はE'、心房収縮期の後期拡張期はA'である。すべての組織ドップラー画像(TDI)心筋速度について、測定された速度が心室頂点から心室の基部への移動になるように、カーソルを心室壁に合わせるようにしてください。. - インタラクティブタッチスクリーンで [2D ]をクリックし、[ チルト ]をクリックしてセクターを移動し、左心室の側壁に焦点を合わせ、フレームレートを>200fpsに維持します。壁の僧帽弁輪のすぐ下にサンプルゲートを置き、手順4.1.9を繰り返します。
- セクターを移動して、RV の側面の壁に焦点を合わせます。 インタラクティブ タッチ スクリーンで[ 2D ]をクリックします。 [傾き]をクリックし、サンプル ゲートを RV の側壁に配置して、手順 4.1.9 を繰り返します。
- 組織ドップラーモードのまま、 カーソル をクリックし、トラックボールを使用して、三尖弁の自由な壁ヒンジ点に垂直な三尖弁環に共鳴線を配置します。三尖弁環状平面収縮期エクスカーション(TAPSE)のコンソールの Mモード ボタンをクリックし、手順4.1.9を繰り返します。これは、TDI マップの有無にかかわらず測定されます。
- コンソールの [2D ] をクリックして、イメージをリセットします。プローブを反時計回りに回転させて頂端の2チャンバービュー(約1時)に移行し、2D画像の 画像保存 をクリックします。「 TVI >イメージ・ストア 」をクリックして、TDI イメージを取得します。
- 頂端の3チャンバーLVの場合 view、プローブを反時計回り(約11時)に回し、画像保存をクリックします。画像ストア>TVIボタンをクリックします。手順4.1.9を繰り返します。
- 幅ボタンを回し、セクターを前壁に狭くして、手順4.1.9を繰り返します。
- アピカル 3 チャンバー RV ビュー
注:頂端の3室RVビューは、ノッチが左腋窩を向いている状態で、第4肋間腔の左胸骨境界にプローブを配置することによって得られます。RVの入口と流出路を示すように画像を調整するために、胸骨境界に沿った動きが必要になる場合があります。- 2Dボタンをクリックして画像をリセットし、幅ボタンを回してRVの側壁を完全に視覚化し、画像ストアをクリックして画像を保存し、色をクリックします。トラックボールを使用して、三尖弁の上にカラーボックスを配置します。青いジェットが観察される三尖弁の上にサンプルゲートを置き、手順4.1.4を繰り返します。
- トラックボールを使用して、カラーボックスを肺動脈の上に移動します。 カーソル をクリックし、サンプルゲートを肺動脈弁の上に置きます。 PW と CW をクリックして、右心室流出のパルス波および連続波ドップラーを取得します。[ 画像ストア>フリーズ] をクリックします。
- 胸骨傍長軸図
注意: 最適な胸骨傍長軸を得るには view 胸骨のすぐ左側にある3番目または4番目の肋間スペースにプローブをまっすぐ下に置き、ノッチを右肩に向けます。プローブを反時計回りまたは時計回りに回転させて、左心室、僧帽弁、大動脈弁、および右心室の全長を取得してください。- 2Dとインタラクティブコントロールの上下タブをクリックして、右心室を画面上部に向けます。カーソル>画像ストアをクリックします。僧帽弁尖の先端に左心室を通る軲滅線を配置し、線が心室中隔に対して垂直であり、左心室が短縮されていないことを確認します。[M モード] をクリックして>イメージ ストア>フリーズします。
注:Mモードトレースは、僧帽弁の二相性開閉、および収縮期と拡張期の両方で、心室中隔、左心室腔、および右心室と左心室の後壁の寸法を示します。この画像は、駆出率および分数短縮29の計算に使用される。 - [ 2D ] をクリックして画像をリセットします。 幅 ボタンを回して、大動脈弁に焦点を合わせます。 深度 ノブを回して奥行き(2.5〜3 cm)を調整するか、コンソールの ズーム ボタンを回して大動脈輪を表示します。両方のリーフレットが、直径が測定可能になるように視覚化してください。
- カーソルをクリックし、大動脈弁輪と左心房を通る共鳴線を左心房と大動脈の寸法(ヒンジポイント)に配置します。[M-mode] をクリックして>イメージ ストア>フリーズします。
- [2D]をクリックし、プローブを左肩に向けて角度を付け、肺動脈に焦点を合わせます。カラー>を同時にクリックして、右心室流出路の画像を取得します。
- サンプルゲートを肺弁のヒンジポイントの上に置き、手順4.1.9を繰り返します。サンプルゲートを三尖弁の上に置き、手順4.1.4を繰り返します。
注意: 右心室腔を伸ばすには、左肩に向かってわずかに移動する必要がある場合があります。右心室の他のビューと同様に、三尖弁逆流がある場合は、連続波ドップラーを取得してTRを計算します。
- 2Dとインタラクティブコントロールの上下タブをクリックして、右心室を画面上部に向けます。カーソル>画像ストアをクリックします。僧帽弁尖の先端に左心室を通る軲滅線を配置し、線が心室中隔に対して垂直であり、左心室が短縮されていないことを確認します。[M モード] をクリックして>イメージ ストア>フリーズします。
- 胸骨傍短軸図
注意: 胸骨のすぐ左側にある第3または第4肋間腔の矢状位置にプローブを配置し、ノッチが左肩を向いており、3つの弁(大動脈弁、肺弁、および三尖弁)がすべて開いている状態で、胸骨傍短軸図を取得します。右心室の流入と流出の2D画像を取得します。- ステップ4.1.5のようにカラードップラーをアクティブにします。手順4.1.3の設定を行います。青いジェットが観察される三尖弁の上にサンプルゲートを置き、手順4.1.4を繰り返します。サンプルゲートを肺弁のヒンジポイントに置き、手順4.1.9を繰り返します。
- [ フリーズ ] をクリックして、イメージのフリーズを解除します。 カーソル をクリックし、肺動脈弁の逆流ジェット(赤い色)の上に共鳴線を置きます。 [CW ] をクリックし、手順 4.1.9 を繰り返します。
- [ 2D ] をクリックして画像をリセットします。僧帽弁の魚の口の外観が視覚化されるまで、プローブを左側面に向けて角度付け続けます。僧帽弁を通るインソネーションラインを僧帽弁尖の高さに配置し、手順4.4.3を繰り返します。このビューは、駆出率と分数短縮の計算にも使用されます。
- コンソールの [2D ] をクリックし、画像をリセットします。左心室の頂点にある左脇腹に向かって2Dスイープ(25〜50 mm / s)を続けます。乳頭筋(偏心指数の計算に使用)と頂点のレベルで2D画像を取得します。[ 画像ストア>フリーズ] をクリックします。
- 高い胸骨傍ビュー
注意: 乳児の頭が左肩の方を向いた状態で、矢状面からわずかに時計回りに回転させ、マーカーを頭に向けながら、胸骨の右上の境界に沿ってプローブを配置します。- ステップ4.1.5のようにカラードップラーをアクティブにします。手順4.1.3の設定を行います。 画像ストア をクリックして、大動脈の3つの近位枝が見えるようにしながら、2D画像とカラー画像を同時に取得します。
- サンプルゲートを腭管前大動脈弓に置き、共鳴線が流れと平行であることを確認し、次に導管のレベルより下の腱後弓に、共鳴線が流れと平行であることを確認し、ステップ4.1.9を繰り返します。
- PDAのカラースイープでダクトビューを取得するには、 フリーズ ボタンを2回クリックします。プローブを右脇腹に向けて傾けて、大動脈弓から肺動脈に向かって角度をつけてプローブを動かします。 [フリーズ] をクリックして>すべての>イメージ ストアを選択します。
- 動脈管開存症(PDA)の存在下で、 カーソルをクリックし、PDAの最も狭い点にサンプルボリュームを置き、ステップ4.1.9を繰り返します。
- 枝肺動脈ビュー
注:この図は、胸骨の左側の上部2/3に沿って3時の位置にプローブを配置することによって得られます。プローブマーカーは患者の左側に向けられます。特に慢性換気などの頂端性肺過膨満症の患者では、音響が悪い窓をナビゲートするために頭に向かって移動する必要がある場合があります。- プローブを患者の頭部に向けて角度をつけ、大動脈弓ビューと同じ設定の画面で枝肺動脈を明らかにします。サンプル量を右肺動脈(RPA)に通し、共鳴線が流れと平行になるようにし、ステップ4.1.9を繰り返します。最高収縮期速度が>1.5 m/sの場合は、4.1.4を繰り返します。
注:これは、末梢肺狭窄症(PPS)を評価するために実行されます。 - 左肺動脈(LPA)でも同じ手順を繰り返します。
- プローブを患者の頭部に向けて角度をつけ、大動脈弓ビューと同じ設定の画面で枝肺動脈を明らかにします。サンプル量を右肺動脈(RPA)に通し、共鳴線が流れと平行になるようにし、ステップ4.1.9を繰り返します。最高収縮期速度が>1.5 m/sの場合は、4.1.4を繰り返します。
- 肺静脈ビュー:カニビュー
注:この図は、矢状面に垂直な胸骨上ノッチにプローブを配置することによって得られます。マーカーを患者の左側に向けて、プローブを患者の頭に向けて角度を付け、肺静脈を明らかにします。- 幅ボタンを時計回りに回してセクター幅を広げてから、速度ノブを反時計回りに回してカラードップラーゲインを30〜50cm / sに調整し、[画像ストア]をクリックして画像を取得します。各肺静脈をカラーフロードップラーで調べ、サンプルゲートを肺静脈に配置し、手順4.1.9を繰り返します。すべての肺静脈が調べられるまで、この手順を繰り返します。
- 肋骨下ビュー
注:肋骨下図は、プローブを腹部の上腹部領域に配置することによって得られます。プローブマーカーが乳児の左側を向いている状態で、プローブを患者の腹部に向けて角度を付けます。右心房と左心房の両方の視覚化が得られたら、このビューを最適化するために、画像の少なくとも1/3が肝臓のものであることを確認してください。- インタラクティブ画面で 2D > up/down をクリックします。右のアトリウムが画面の下部に向けられていることを確認します。 幅 ボタンを回します。 [色] > [同時] をクリックします。 速度 ノブを回して、カラーゲインを40〜50cm / sに調整します。卵円孔が特許を取得している場合は、サンプルゲートを欠損箇所に置き、手順4.1.9を繰り返します。
- 上大静脈(SVC)を視覚化するには、プローブを時計回りに回転させます。 カーソル をクリックし、サンプルボリュームをSVC内に約1cm配置し、共鳴線が流れと平行になるようにします。[ 画像ストア>フリーズ] をクリックします。
- インタラクティブ画面を 上下 にクリックすると、ハートが画面の右側に配置されるように画面の向きが変わります。ノッチが患者の頭部を向くようにして、プローブを矢状面に配置します。プローブを患者の左側に傾けて、IVCと肝静脈を視覚化します。サンプルゲートを肝静脈に置き、手順4.1.9を繰り返します。
- 臍帯静脈カテーテル(UVC)または下肢末梢に挿入された中央カテーテル(PICC)の位置を表示するには、カテーテルが画像セクターに表示されるまで、プローブを胸部の中央に向かって上にスライドさせます。カテーテルのコースを見るには、右または左からのスイープまたは反時計回りの回転が必要です。 画像ストア をクリックして、中央カテーテルの適切なビューが視覚化されたら画像を取得します。
- 切欠きが頭部を向いている状態で、剣状下領域の臍に向かってプローブをスライドさせることにより、腹部大動脈の矢状面図に移行します。カラーゲインを70〜80cm / sに調整します。サンプルゲートを腹腔動脈の上に置き、手順4.1.9を繰り返します。上腸間膜動脈(SMA)についても同じ手順を繰り返します。
結果
以下の代表的な結果は、臨床現場でのTnECHOの使用例として、血行動態的に有意な動脈管開存症(hsPDA)の評価の概要を示しています。前述したように、血行動態の重要性を判断するために、複数の測定による包括的な評価が行われます。アイオワPDAスコア(表3)は、PDAシャントに関連する体積負荷と全身性低灌流の結果を定量化するのに役立つため、臨床使用に採用されているスコアリングシステムの1つです。
評価は、肺静脈の D 波速度、僧帽弁 E 波速度、および IVRT が得られる頂端の 4 室ビューで構成されます。僧帽弁E波と肺静脈D波の速度の上昇は、左心容積過負荷の証拠とIVRTの短縮を示しています。速度はセンチメートル/秒(cm/s)で記録されます。時間測定はミリ秒(ms)単位で記録されます。その後、左心室流出が評価されます。左心室出量の増加は、左心室容積負荷の増加も示唆しています。.次に、胸骨傍長軸図では、左心房/大動脈比(LA:Ao比)が評価されます。LA:Ao比の上昇は、左心房拡張を示しており、左心拍容積過負荷と一致しています。.高い胸骨傍ビューにより、PDAのサイズ、方向性、シャントパターン、および下行大動脈に供給する血流に対するシャント効果を評価できます。次に、全身性低灌流は、腹腔動脈、上腸間膜動脈 (SMA)、および中大脳動脈 (MCA) のドップラー画像によって評価されます。
次に、 表 3 に示すように、心エコー検査の結果は、アイオワ PDA スコアなどの評価システムを使用して評価されます。次に、スコアリングシステムは、PDAの血行動態の重要性の定量的評価を可能にし、6を超えるアイオワPDAスコアは、血行動態的に有意なPDAを示唆しています。
以下は、このプロトコルを使用して実施される心エコー検査を説明するための症例ビネットです。
男性の未熟児は在胎週数29週で生まれました。彼は、PDAの血行動態の重要性を評価するために、生後2日目にTnECHO評価を受けました。TnECHOの測定値は 表4に以下の結果を示し、アイオワPDAスコアは8であり、血行動態的に有意なPDAを示唆した。
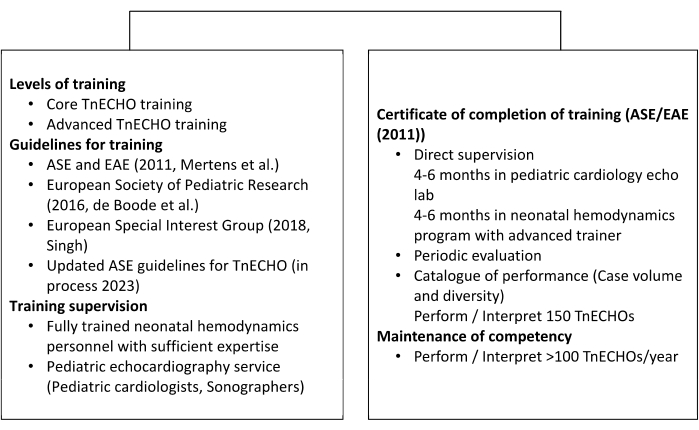
図1:新生児の血行動態のトレーニングと認定の概要。 北米、米国を対象とした新生児心エコー検査と新生児血行動態トレーニングの簡単な概要。この図は 3 から修正し、許可を得て公開しています。 この図の拡大版をご覧になるには、ここをクリックしてください。
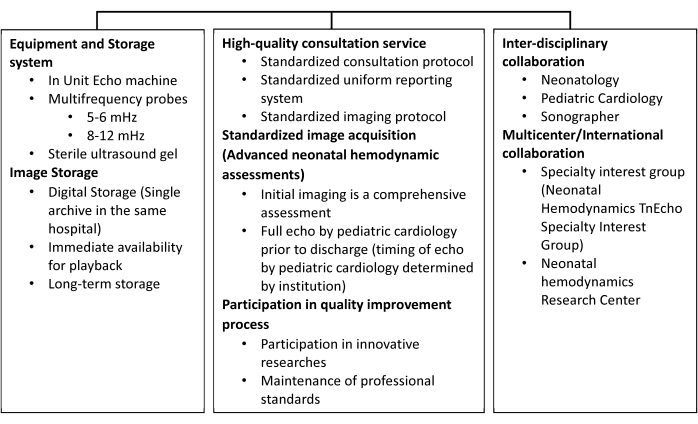
図2:新生児血行動態相談サービスの要素。新生児血行動態サービスの機器と保管システム、および学際的なコラボレーションを詳述する概要。この数字は 30 から修正され、許可を得て再掲載されています。 この図の拡大版をご覧になるには、ここをクリックしてください。

図3:新生児血行動態の診察の適応。 症状および疾患に基づく適応症の概要。 この数字は 30 から修正され、許可を得て再掲載されています。 この図の拡大版をご覧になるには、ここをクリックしてください。

図4:肺高血圧症のTnECHO評価ガイドライン。 肺高血圧症のアルゴリズムとTnECHO評価ガイドラインの例。 この図の拡大版をご覧になるには、ここをクリックしてください。
表1:一般的に使用される超音波モダリティ/用語の定義。 このリストは、このプロトコルに記載されている超音波モダリティの定義を提供します。 この表をダウンロードするには、ここをクリックしてください。
表2:正期産新生児の推奨測定値、解釈、および参照範囲を含む、標準的な標的新生児心エコー検査評価。 対象を絞った新生児心エコー検査評価の概要と、推奨される測定値、解釈、および参照範囲。略語:CW =連続波。LA =左心房;LVOT = 左心室流出路;MV = 僧帽弁;PW = パルス波;RVOT右心室流出路;3D = 3次元。この図は 3 から修正し、許可を得て公開しています。 この表をダウンロードするには、ここをクリックしてください。
表3:アイオワ州PDAスコアを決定するために評価された心エコーマーカー。 このスコアリングシステムは、心臓への体積負荷と動脈管開存シャントに関連する全身性低灌流の代理的影響を評価します。合計スコア = (合計ポイント) + (心エコー検査での PDA 直径 [mm]/体重 [kg])。この図は 平成19年度 から修正し、許可を得て掲載しています。 この表をダウンロードするには、ここをクリックしてください。
表4:プロトコルとアイオワPDAスコアを使用して実施された心エコー検査を示すための症例ビネットの代表的な結果。 TnECHOから取得した測定値を使用して、アイオワ州PDAスコアに基づいてスコアリングします。その結果、アイオワPDAスコアは8となり、血行動態的に有意なPDAが示唆された。 この表をダウンロードするには、ここをクリックしてください。
補足ファイル 1: プローブ配置による標準的な標的新生児心エコー測定。 この表は、プローブの配置、代表的なエコー画像、および測定されたパラメーターを使用して、対象となる新生児心エコー検査評価の概要を示しています。略語:LPA =左肺動脈;LVO = 左心室出量;PDA = 動脈管開存症;RV = 右心室;VSD = 心室中隔欠損症。 このファイルをダウンロードするには、ここをクリックしてください。
ディスカッション
TnECHOガイド下ケアは、新生児科医による乳児の血行動態不安定性の臨床評価の補助として、多くの新生児集中治療室で採用されています4。認定トレーニングプログラムは、2011 ASE3に従って開発されており、トレーニングへの能力ベースのアプローチに重点を置いています。未熟な心血管系の独特の脆弱性と出生後の移行中の心血管適応の複雑さは、血行動態の安定性の重要な決定要因であり、包括的で正確な連続TnECHO評価の重要性を強調しています7,31。
最初の心エコー検査研究は、米国心エコー学会 (ASE) のガイドラインに従って、セグメント的アプローチを使用した心臓の解剖学的および生理学の完全な形態学的および血行動態学的評価で構成されていることに注意することが重要です。小児心臓専門医による修正も、正常な心臓解剖学的構造を確認するために12時間以内に実行する必要があります。.その後の心エコー検査の評価は、この記事で前述した標準化されたプロトコルに従います。さらに、臨床(病歴と検査)情報の抽象化は、診断印象と治療の推奨事項を策定するために体系的であるべきです。主観的評価の限界を浮き彫りにする最近の証拠14では、マルチパラメトリック血行動態アプローチの使用により、定量的分析が可能になり、臨床的意思決定の洗練度が高まります32。
急性代償不全患者の設定では、修正された画像プロトコルが必要な場合があります(例、体外式膜型酸素化前の状態)。この設定では、緊急の血行動態救助を容易にするために、最も重要な画像(例えば、左心室および右心室出力、RVおよびLV機能、大動脈弓、PDAおよび卵円孔開存[PFO]の開存性と方向)を迅速に取得する必要があります。既存の注意点は、TnECHOが非侵襲的ツールとして使用されていることを認識して、血行動態が不安定な乳児の根底にある心血管病態生理学に関する追加情報を提供し、治療への反応を監視することです。したがって、TnECHOは、資格のある小児心臓専門医による心エコー図による先天性心疾患の評価に代わるものでも同等物でもないことを理解することが重要です。同様に、心膜タンポナーデの検出や中心カテーテル位置の評価などの特定の適応症に対して適応となる限定的な1回限りの評価である心臓ポイントオブケア超音波(心臓POCUS)の適用にも注意が必要です。
ここ数年、技術の進歩により、新生児の血行動態の分野が急速に成長し、変形分析や血斑画像診断などのより高度な心エコー評価が可能になり、新生児での使用の可能性を秘めています。標的新生児心エコー検査と新生児血行動態におけるこれらの継続的な進歩、特に方法の精度、実現可能性、信頼性、および限界の理解において、 将来、最も脆弱な患者のケアに大幅な臨床的改善をもたらす可能性があります7,27。
開示事項
著者は開示するものは何もなく、利益相反もありません。
謝辞
内容は著者の責任であり、必ずしも米国国立衛生研究所の公式見解を表すものではありません。M.M.は、米国国立衛生研究所(NIH)のマイノリティの健康と健康格差に関する国立研究所(National Institute on Minority Health and Health Disparities)の助成金第R25MD011564号で支援を受けています。
図、基準値、およびトレーニングの推奨事項のリソースは、Ruoss et al.30、TnECHO教育マニュアル47、新生児血行動態研究センター(NHRC)48、およびターゲット新生児心エコー検査アプリケーション49から採用しました。
資料
| Name | Company | Catalog Number | Comments |
| DICOM VIEWER EP | GEHealthcare | H45581CC | DICOM Viewer on MediaThis option provides the ability to export DICOM images including a DICOM viewer to storage media (USB, DVD), for easy access to patient images on offline computers. |
| 2D Strain | GEHealthcare | H45561WF | Automated 2D EF Measurement tool based upon 2D-Speckle tracking algorithm. |
| EchoPAC* Software Only v203 | GEHealthcare | H8018PF | |
| EchoPAC* Advanced Bundle Package | GEHealthcare | H8018PG | Advanced QScan provides dedicated parametric imaging applications for quantitative display of regional wall deformation. |
| Multi-Link 3-lead ECG Care cable neonatal DIN, AHA (3.6 m/12 feet) | GEHealthcare | H45571RD | Multi-Link 3-lead ECG Care cable neonatal DIN, AHA (3.6 m/12 feet) Used together with neonatal leads H45571RJ |
| Myocardial Work | H45591AG | Myocardial Work adjusts the AFI (strain) results using the systolic and diastolic blood pressure measured immediately prior to the echo exam. Using the Myocardial Work feature helps achieve a less load dependent strain/ pressure curve and work efficiency index | |
| 12S-D Phased Array Probe | GEHealthcare | H45021RT | |
| 6S-D Phased Array Probe | GEHealthcare | H45021RR | |
| Sterile ultrasound gel | Parker labs | PM-010-0002D | sterile water solubel single packet ultrasound transmission gel |
| Ultrasound gel warmer | Parker Labs | SKU 83-20 | ultrasound gel warmer for single gel package. |
| Wireless USB adapter | H45591HS | Wireless external G type USB adapter with extension cable and hardware for mounting on the rear panel. | |
| Vivid* E90 v203 Console Package | GEHealthcare | H8018EB | Vivid E90 w/OLED monitor v203 Console |
参考文献
- Shah, D. M., Kluckow, M. Early functional echocardiogram and inhaled nitric oxide: Usefulness in managing neonates born following extreme preterm premature rupture of membranes (PPROM). Journal of Paediatrics and Child Health. 47 (6), 340-345 (2011).
- El-Khuffash, A., McNamara, P. J. Hemodynamic assessment and monitoring of premature infants. Clinics in Perinatology. 44 (2), 377-393 (2017).
- Mertens, L., et al. Targeted neonatal echocardiography in the neonatal intensive care unit: Practice guidelines and recommendations for training. Writing Group of the American Society of Echocardiography (ASE) in collaboration with the European Association of Echocardiography (EAE) and the Association for European Pediatric Cardiologists (AEPC). Journal of the American Society of Echocardiography. 24 (10), 1057-1078 (2011).
- Papadhima, I., et al. Targeted neonatal echocardiography (TNE) consult service in a large tertiary perinatal center in Canada. Journal of Perinatology. 38 (8), 1039-1045 (2018).
- Sehgal, A., McNamara, P. J. Does point-of-care functional echocardiography enhance cardiovascular care in the NICU. Journal of Perinatology. 28 (11), 729-735 (2008).
- El-Khuffash, A., Herbozo, C., Jain, A., Lapointe, A., McNamara, P. J. Targeted neonatal echocardiography (TnECHO) service in a Canadian neonatal intensive care unit: A 4-year experience. Journal of Perinatology. 33 (9), 687-690 (2013).
- Harabor, A., Soraisham, A. S. Utility of targeted neonatal echocardiography in the management of neonatal illness. Journal of Ultrasound in Medicine. 34 (7), 1259-1263 (2015).
- Evans, N. Echocardiography on neonatal intensive care units in Australia and New Zealand. Journal of Paediatric and Child Health. 36 (2), 169-171 (2000).
- McNamara, P., Lai, W. Growth of neonatal hemodynamics programs and targeted neonatal echocardiography performed by neonatologists. Journal of the American Society of Echocardiography. 33 (10), 15-16 (2020).
- Frommelt, P., et al. Digital imaging, archiving, and structured reporting in pediatric echocardiography: Impact on laboratory efficiency and physician communication. Journal of the American Society of Echocardiography. 21 (8), 935-940 (2008).
- De Geer, L., Oscarsson, A., Engvall, J. Variability in echocardiographic measurements of left ventricular function in septic shock patients. Cardiovasc Ultrasound. 13, 19(2015).
- Margossian, R., et al. The reproducibility and absolute values of echocardiographic measurements of left ventricular size and function in children are algorithm dependent. Journal of the American Society of Echocardiography. 28 (5), 549-558 (2015).
- Harada, K., Takahashi, Y., Tamura, M., Orino, T., Takada, G. Serial echocardiographic and Doppler evaluation of left ventricular systolic performance and diastolic filling in premature infants. Early Hum Development. 54 (2), 169-180 (1999).
- Smith, A., et al. Accuracy and reliability of qualitative echocardiography assessment of right ventricular size and function in neonates. Echocardiography. 36 (7), 1346-1352 (2019).
- Koestenberger, M., et al. Systolic right ventricular function in preterm and term neonates: Reference values of the tricuspid annular plane systolic excursion (TAPSE) in 258 patients and calculation of Z-score values. Neonatology. 100 (1), 85-92 (2011).
- Jain, A., et al. A comprehensive echocardiographic protocol for assessing neonatal right ventricular dimensions and function in the transitional period: normative data and z scores. Journal of the American Society of Echocardiography. 27 (12), 1293-1304 (2014).
- Koestenberger, M., et al. Right ventricular function in infants, children and adolescents: Reference values of the tricuspid annular plane systolic excursion (TAPSE) in 640 healthy patients and calculation of z score values. Journal of the American Society of Echocardiography. 22 (6), 715-719 (2009).
- Groves, A. M., Kuschel, C. A., Knight, D. B., Skinner, J. R. Does retrograde diastolic flow in the descending aorta signify impaired systemic perfusion in preterm infants. Pediatric Research. 63 (1), 89-94 (2008).
- Rios, D. R., et al. Early role of the atrial-level communication in premature infants with patent ductus arteriosus. Journal of the American Society of Echocardiography. 34 (4), 423-432 (2021).
- de Freitas Martins, F., et al. Relationship of patent ductus arteriosus size to echocardiographic markers of shunt volume. The Journal of Pediatrics. 202, 50-55 (2018).
- Martins, F. F., et al. Relationship of patent ductus arteriosus echocardiographic markers with descending aorta diastolic flow. Journal of Ultrasound in Medicine. 40 (8), 1505-1514 (2021).
- Waggoner, A. D. Quantitative echocardiography. Journal of Diagnostic Medical Sonography. 21 (6), 464-470 (2005).
- Masuyama, T., et al. Continuous-wave Doppler echocardiographic detection of pulmonary regurgitation and its application to noninvasive estimation of pulmonary artery pressure. Circulation. 74 (3), 484-492 (1986).
- Mourani, P. M., Sontag, M. K., Younoszai, A., Ivy, D. D., Abman, S. H. Clinical utility of echocardiography for the diagnosis and management of pulmonary vascular disease in young children with chronic lung disease. Pediatrics. 121 (2), 317-325 (2008).
- Fisher, M. R., et al. Accuracy of Doppler echocardiography in the hemodynamic assessment of pulmonary hypertension. American Journal of Respiratory and Critical Care Medicine. 179 (7), 615-621 (2009).
- Krishnan, U., et al. Evaluation and management of pulmonary hypertension in children with bronchopulmonary dysplasia. The Journal of Pediatrics. 188, 24-34 (2017).
- Huntsman, L. L., et al. Noninvasive Doppler determination of cardiac output in man. Clinical validation. Circulation. 67 (3), 593-602 (1983).
- Weisz, D. E., Poon, W. B., James, A., McNamara, P. J. Low cardiac output secondary to a malpositioned umbilical venous catheter: Value of targeted neonatal echocardiography. AJP Reports. 4 (1), 23-28 (2014).
- Quinones, M. A., et al. A new, simplified and accurate method for determining ejection fraction with two-dimensional echocardiography. Circulation. 64 (4), 744-753 (1981).
- Ruoss, J. L., et al. The evolution of neonatal hemodynamics and the role of ASE in cultivating growth within the field. ECHO. 11 (4), 16-19 (2022).
- Bensley, J. G., De Matteo, R., Harding, R., Black, M. J. The effects of preterm birth and its antecedents on the cardiovascular system. Acta Obstetricia et Gynecologica Scandinavica. 95 (6), 652-663 (2016).
- Sehgal, A., Mehta, S., Evans, N., McNamara, P. J. Cardiac sonography by the neonatologist: Clinical usefulness and educational perspective. Journal of Ultrasound in Medicine. 33 (8), 1401-1406 (2014).
- Zecca, E., et al. Left ventricle dimensions in preterm infants during the first month of life. European Journal of Pediatrics. 160 (4), 227-230 (2001).
- Jain, A., et al. Left ventricular function in healthy term neonates during the transitional period. The Journal of Pediatrics. 182, 197-203 (2017).
- Nagasawa, H. Novel regression equations of left ventricular dimensions in infants less than 1 year of age and premature neonates obtained from echocardiographic examination. Cardiology in the Young. 20 (5), 526-531 (2010).
- Skelton, R., Gill, A. B., Parsons, J. M. Reference ranges for cardiac dimensions and blood flow velocity in preterm infants. Heart. 80 (3), 281-285 (1998).
- Kampmann, C., et al. Normal values of M mode echocardiographic measurements of more than 2000 healthy infants and children in central Europe. Heart. 83 (6), 667-672 (2000).
- Overbeek, L. I. H., et al. New reference values for echocardiographic dimensions of healthy Dutch children. European Journal of Echocardiography. 7 (2), 113-121 (2006).
- Riggs, T. W., Rodriguez, R., Snider, A. R., Batton, D. Doppler echocardiographic evaluation of right and left ventricular diastolic function in normal neonates. Journal of the American College of Cardiology. 13 (3), 700-705 (1989).
- Schmitz, L., Koch, H., Bein, G., Brockmeier, K. Left ventricular diastolic function in infants, children, and adolescents. Reference values and analysis of morphologic and physiologic determinants of echocardiographic Doppler flow signals during growth and maturation. Journal of the American College of Cardiology. 32 (5), 1441-1448 (1998).
- Schmitz, L., et al. Doppler-derived parameters of diastolic left ventricular function in preterm infants with a birth weight <1500 g: Reference values and differences to term infants. Early Human Development. 76 (2), 101-114 (2004).
- Ito, T., Harada, K., Takada, G. Changes in pulmonary venous flow patterns in patients with ventricular septal defect. Pediatric Cardiology. 23 (5), 491-495 (2002).
- Mori, K., et al. Pulsed wave Doppler tissue echocardiography assessment of the long axis function of the right and left ventricles during the early neonatal period. Heart. 90 (2), 175-180 (2004).
- Galiè, N., et al. Guidelines on diagnosis and treatment of pulmonary arterial hypertension. The Task Force on Diagnosis and Treatment of Pulmonary Arterial Hypertension of the European Society of Cardiology. European Heart Journal. 25 (24), 2243-2278 (2004).
- Shiraishi, H., Yanagisawa, M. Pulsed Doppler echocardiographic evaluation of neonatal circulatory changes. Heart. 57 (2), 161-167 (1987).
- Howard, L. S., et al. Echocardiographic assessment of pulmonary hypertension: Standard operating procedure. European Respiratory Review. 21 (125), 239-248 (2012).
- El-Khuffash, A., et al. Neonatologist Performed Echocardiography. Teaching Manual. , Available from: https://neonatalhemodynamics.com/PDF/NPE%20Teaching%20Manual%20El-Khuffash%20-%202019.pdf (2019).
- Neonatal Hemodynamics Research Center. , Available from: https://neonatalhemodynamics.com/ (2022).
- Targeted neonatal echocardiography application. , Available from: https://itunes.apple.com/i.e./app/tnecho (2022).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved