Method Article
3Dプリントガイドとリングスタッキング法を用いたエンジニア血管移植片のスケーリング
要約
スケーラブルな設計された血管は、臨床適用性を改善するであろう。簡単にかなりの3Dプリントガイドを使用して、血管平滑筋のリングは、血管移植片を形成し、筒状に作成して積層しました。移植片は、単純に、3Dプリントガイドサイズを変更することによってヒト冠状動脈寸法の範囲を満たすような大きさにすることができます。
要約
冠動脈疾患は、数百万人のアメリカ人に影響を与え、死の主要な原因です。利用可能な自家血管移植片の不足により、人工移植片は、患者の治療のための大きな可能性を提供します。しかし、操作された血管移植片は、一般に容易に拡張されない時間がかかり、高価な練習を構成する、異なるサイズをカスタマイズするためにカスタムモールドまたはポリマーチューブの製造を必要とします。人間の動脈は、約2.0〜38ミリメートルから約0.5〜2.5ミリメートルから壁の厚さで内腔直径の範囲です。我々は、血管平滑筋細胞(SMC)とここに実証所望の細胞型の組織の可変サイズのリングは、内腔の直径を制御するために、中央ポストのガイドを使用して作成することができる」は、環スタッキング法」と呼ばれるメソッドを作成しましたそして、外殻は、血管壁の厚さを決定します。これらの組織のリングは、その後、血管の自然な形状を模倣、管状構造物を作成するために積層されています。容器の長さがbのことができますeは、単に必要な長さを構成するのに必要な環の数を積層して合わせ。私達の技術を用いて、血管に類似した管状の形態の組織は、容易に診療所および患者のニーズを満たすために寸法および長さの多様で製造することができます。
概要
冠動脈疾患(CAD)の処置において、患者自身の血管バイパス手術用移植材料として回収します。しかし、多くの場合、病気の患者は、自分自身に寄付する実行可能な船を持っていない、と彼らが行う場合には、ドナー部位は、かなりの追加的な害を引き起こし、感染の重大なリスクがあります。 1操作された血管移植片は、この必要性を満たすことができます。スケーラビリティは、患者の血管のサイズ要件の広い範囲を満たすために、エンジニアリング船の最も重要です。しかし、エンジニアリング船舶のための本方法は、容易に拡張されず、一般的に複雑な金型またはポリマー足場の再製造を必要とします。ほとんどの操作された移植片血管線維芽細胞、平滑筋、または内皮細胞を播種されたポリマー管状足場を利用してのいずれか。または組織管を作成するために、マンドレルの周りに細胞シートをロール。臨床試験における二工学血管移植片は、脱細胞化に基づいていますDポリマー-ECMプラットフォーム。血管の修復に使用できる2、3、4ポリマー移植片は、既に持続ポリマーの存在とグラフトの長期適用の主な課題として生じる可能性が開存性の問題を有することが知られています。管状の型は様々なサイズで血管を生成するためにカスタムモールドのための追加の設計及びツールの製造を必要とする手順、完全に細胞容器を製造するために使用される5、6、7、8、9、10、11、12、13れています。
本明細書に記載される方法は、容易に拡張操作血管を作成するための新規な技術を包含しますカスタマイズ可能な3Dプリント挿入と伝統的な培養プレートを使用して移植片。 14細胞は、中央ポストと外殻のインサートを有するプレートに播種します。ポストコントロールは直径ルーメンと自己集合組織のリングにに細胞単層を可能にします。リングの外殻を制御する厚さ、および最終的な容器のこのように壁の厚さ。完成した組織のリングは、その後、管状血管移植片を形成するように積層されています。この方法の利点は、「リングスタッキング法」と呼ばれる任意の接着細胞タイプは、単に修正ガイドを挿入することによって生成することができるプレートの設定および組織環または所望の用途に必要な任意のサイズの管に播種することができることです。組織のリングを作成する組織工学における比較技術は、15、スケールに難しいまま各所望の大きさのために金型の再製造を必要とする16。さらに、この方法を用いて作製血管グラフトを生産することができ2-3週間でdは、数週間では速く、他の操作された容器に比べて。 図6は、診療所では、この時間のずれが悪化している患者の治療に有意な差を作ることができます。
プロトコル
1.細胞培養の準備
- 商業的に購入したヒト大動脈平滑筋細胞を利用します。
- 88.6%とからなる平滑筋細胞増殖培地中で細胞を維持する231培地、0.1%の組換えヒトインスリン(RH-インスリン)、組換えヒト線維芽細胞増殖因子(RH-FGF)、組換えヒト上皮細胞増殖因子(RH-FGF)の各々アスコルビン酸; 5%ウシ胎児血清(FBS)およびL-グルタミンの各;そして、1%抗生物質/抗真菌剤。
注:各増殖因子、FBSおよびL-グルタミンは、血管メディア増殖キットとして購入されます。 - 細胞が約90%コンフルエントと組織播種のための準備が整うまで、メディアごとに48時間を変更します。
- 拡張のためのメディアの変化との間でインキュベーター中で細胞を保管してください。
3Dプリント挿入とカスタムシリコーン成形プレートの調製
- 3Dは、プレートインサートを印刷するための市販の3Dプリンタ( 例えば 、レプリケータミニ)を使用します。
- オペアンプを使用してください印刷された外殻とポストの3Dモデルを作成するために、このようなブレンダーとしてソースの3D設計ソフトウェアアン。
- 3Dプリンタのソフトウェアへの移植を可能に.STLフォーマットを経由して、モデルのドライバファイルをエクスポートします。
- 3Dプリンターにロードされたポリ(乳酸)フィラメント(PLA)を使用して印刷柱と外殻を生成します。
- 次の印刷、30分を行う各インサートを滅菌するために、70%-100%のエタノール溶液に浸します。
- ポリ(ジメチルシロキサン)(PDMS)のシリコーンポリマーのポリマー混合物をベースと室温で10分間脱気し、混合物を可能に1:10の硬化剤を準備します。
- 、(35ミリメートル)小さい(60ミリメートル)、中間、および大規模(100ミリメートル)として使用シャーレのサイズを定義します。
- 2 mLを、4 mLおよびそれぞれ、小中間および大プレートに未硬化のシリコーンの6 mLを加え、シャーレの底面全体を横断薄層を作成します。
- PDMSを注ぐことにより、小さなプレートのための投稿を作成します。7mm高さの100mmプレートとは、約2~3時間、60℃のホットプレート上で硬化させます。次に、円筒状の支柱をパンチアウトするために5ミリメートル生検パンチを使用します。各PDMSシリンダーを確保し、各小板の中央にするために、未硬化PDMSの少量を使用してください。
- プレートの底にPDMSの硬化を完了する前に、中間および大規模なプレートについては、3Dはそれぞれ、各中間および大型プレートに集中直径ポスト10ミリメートルと20ミリメートルを印刷置きます。大規模なプレートの場合は、さらに3Dプリント外殻をポストから直径等距離では約66.7ミリメートルを置きます。
- 各皿は、ポリマーの脱ガスのための18時間を可能にする、約2〜3時間、60℃のホットプレート上で大気中で硬化させます。 図1に見られるように、適切な領域と向きでプレートに印刷されたコンポーネントを修正しました。
- すべてのPLAの内部に30分間、30%の蒸留水で70%エタノール溶液を添加その後、滅菌のためのTESと各プレートをカバーしています。
- 慎重に各プレートからのエタノールを吸引空気乾燥させ。
- その蓋、フェイスアップの隣に生物学的安全キャビネット(BSC)内の各プレートを配置します。滅菌を完了するために30分間BSCの下でUV光にプレートし、蓋を公開します。滅菌技術は、UV曝露後のすべての工程を用いて行われます。
平滑筋細胞とプレートのメンテナンスで播種フィブリンハイドロゲルの調製、
- それぞれ、小中間および大型プレートサイズの0.5 mLを、1.1 mLおよび1.81ミリリットルの量の成長培地+ 0.01%のTGF-β1を含むフィブリンゲル溶液を混ぜます。
- それぞれ、100 U / mLのストックから、それぞれ、小中間および大型プレートのメディアに、40μL、88.4μLとトロンビンの145μLを追加します。ゆっくりとそのトロンビンが均等にメディア内で混合されていることを確認するために手で各プレートを旋回させます。
- 次に、160を追加1; L、354μLおよび580μLのフィブリノゲンは、20 mg / mlでの在庫から、滴下円それぞれ、小中間および大プレートにトロンビンメディア混合物に、それぞれ。ゆっくりでも層に混入し、ヒドロゲルの分布を確認するために手で旋回。
- ヒドロゲルは、室温で10〜15分間硬化させます。
- 標準的なプロトコルに従って、平滑筋の150mm細胞培養プレート中で増殖する細胞と遠心分離をトリプシン処理。 231培地、1%FBSおよび1%抗生物質/抗真菌 - 得られたペレットを98%からなる分化培地3mLに再懸濁されるべきです。
- 積極的に任意の細胞塊を破壊するために2 mLのピペットで上下に滴定により細胞を混ぜます。血球計数器を用いて細胞をカウントし、/ mLで、小中間および大型プレート用、それぞれ2×10 6細胞/ mL、1.0×10 7細胞/ mLおよび1.4×10 7細胞の細胞懸濁液を作成します。
- 各細胞懸濁液intの1 mLを加え50 mLコニカルに対応するOAは、小さな中間および大型の標識。希望するそれぞれの追加の組織のリングのために、このように、追加の50 mLコニカルを設定します。
- それぞれ、各小中間および大血管のための2 mLを、4 mLおよび5 mLの最終播種量を得るために、各円錐形に分化培地を追加します。その後、慎重に滴ずつそれぞれ対応するプレートで準備ヒドロゲルの上に細胞溶液をピペット。
- 37℃インキュベーターで5%CO 2に代えプレート。
- 分化培地を各プレート毎に48〜72時間を変更します。より大きな板の場合には、大細胞播種密度を補償することごとに48から24時間を変更した後、24時間後に最初にメディアを変更します。
- リングが完全にポストに向かって収縮していますように2〜4日後に、それぞれ、各小中間および大きいリングに10μL、20μLおよびTGF-β1の35μLを追加します。 TGF-βへの曝露後; 1、少なくとも24時間、リングを扱うことする準備が整いました。
血管構築とメンテナンスの4アセンブリ
- 最終的な血管構造物の製造前に、特殊な容器が完成容器を保持するために作成されます。
- 小血管のために、50mLのポリカーボネートコニカルチューブの上から2インチのセクションを切断することにより、リングの積み重ねのための背の高い板を作成し、PDMS 35ミリメートルプレートにカットエッジを接着。プレートの蓋として円錐形の蓋を使用してください。
- プレートを積み重ね、中間および大血管背の高いリングのために、背の高い板壁として機能するように縦方向に2.5インチのセクションに1.75インチの直径のポリカーボネートチューブをカット。背の高いプレート底部は、2インチ直径の円形片に0.125インチ厚のポリカーボネートシートを切断します。アクリル溶剤セメントを使用して、円形の切断片をポリカーボネート管部分に結合します。背の高い板用の蓋として60ミリメートルのペトリ皿から蓋を使用してください。
- 3DのpRINTポスト5、直径10から20mm、長さ50mm。
- 各コンテナに未硬化のシリコーンの10ミリリットルを追加します。 PDMSの完全な硬化に先立ち、中央にそれぞれ、小さな中間、および大規模な容器にステップ4.1.3で作成した各ポストを配置します。
- 2-3時間、60℃にホットプレートセットに硬化させます。
- 30分間、30%蒸留水で70%エタノール溶液で滅菌します。
- 慎重に各容器からエタノールを吸引した後、BSCで空気乾燥させ。次に、その蓋、フェイスアップの隣に配置、各プレートとフード内のコンテナを配置します。さらに滅菌のための追加の30分間BSCの下でUV光にコンテナを公開します。 UV照射後のすべてのステップで滅菌技術を使用してください。
- 非常に微細な鉗子を使用して、慎重にそのポストから各きつく巻か平滑筋ヒドロゲルリングを削除し、背の高いポストとその対応するより大きな容器に移します。
- のペアを使用しますそれぞれの手で鉗子とは、ポストからリングの片側を持ち上げ、その後、他の。内腔を保護し、維持するために注意してください。
- 背の高いポストに最初の1辺、リングのもう一方の側をスライドさせる、この両手方式で転送を実行します。穏やかな、緩やかな動きを使用して、円周方向に働いて、ゆっくりと背の高いポストの上にリングを押し下げます。所望の血管の長さは、各リングが完了構築物の長さの約1〜ミリ加えると、得られるまで、続いて組織リングスタック。
- ポストは、作業面と平行になるように背の高い3Dプリントポスト上に位置決めリングのスタックを使用すると、プレートを回します。
- マイクロピペットを用いて、それぞれ、各小中間および大血管の外表面に軽く100 U / mLの濃度でトロンビンの40、80および160μLを追加します。トロンビンを添加しながら、ゆっくりと構築物の全ての表面の均一な被覆を確実にするためにプレートを回転させます。これは、構築後の初期日にリングスタック構造体を固定するために利用フィブリン糊のベースになります。
- 次に、迅速に構築体を回転させながらマイクロピペットを用いて、それぞれ、各小中間、および大規模な構築物の20mg / mLの濃度でフィブリノゲンの40、80および160μLを追加します。トロンビンおよびフィブリノーゲンはすぐに一度混合固いゲルに設定してください。短い硬化時間に、可能な限り迅速かつ均等にフィブリノゲンを適用します。
- 構築物を保持する各コンテナに分化培地の20 mLを加え。 37℃のインキュベーターに置き容器が必要になるまで。 3〜5日毎のメディアを変更します。
結果
ここで実証されたリングスタッキング法(RSM)がスケーラブルであることを示し、3つの異なる工学血管移植片の大きさ( 図1)の製造です。適用性を証明するために、3つの異なる容器のサイズは、動脈左前のため、実際の人間の血管サイズに相関を選択した(小;直径ルーメン= 4ミリメートル)17、(中間;直径ルーメン= 10ミリメートル)大動脈降順と上行大動脈(大規模;直径= 20ミリメートル)18ルーメン 。壁の厚さは約500μmの小さなリングのため、約1500ミクロンの両方の中間と大きなリングのです。実証された各容器は、小さな容器では約6ミリメートルと中間と大型船舶のための9ミリメートルの長さに等しくする、6リングを積み重ねることによって構築されています。長さは、個々のリングの壁の厚さに基づいています。
組織学的分析は、明らかにしましたすべてのリングサイズで高い細胞充実性( 図2)。レッド材料は、フィブリンゲルを画定します。小さなリングでは、残留フィブリンゲルの少量は、リングの外縁に見られます。大きなリングでは、一部のフィブリンゲルは、細胞内容が点在しました。マッソントリクローム染色では、(青でマークされた)コラーゲン産生の指標は中間と大きなリングで見ることができます。
環形成後の細胞の表現型を決定するために、組織のリングは、α-平滑する筋アクチン(SMA)およびトロポミオシン( 図3)抗体について免疫蛍光を用いて分析しました。全ての環の大きさは、平滑筋の表現型が維持されたことを確認し、両方の抗体について陽性でした。
引張試験は、それらの機械的特性( 図4)を決定するために、異なるサイズのリングを行いました。 U-ストレッチ、mechaniインストロン引張試験大型リングと容器に使用しながら、校正試験装置は、試験小さな中間リングと血管を引張するために使用されました。弾性率(E)、極限引張強さ(UTS)および破壊強度(FS)データを収集しました。一貫した傾向は増加し、リングと容器のサイズに相関する強度の増加に伴って観察されました。
様々なサイズのリングを作成するために必要な数の細胞播種は、播種面積( 図5)とほぼ直線的に増加しました。より大きなリングを作成するためには、少なくとも1400万細胞は、腹部大動脈サイズのリングを作成するために必要でした。
六リングスタック、または容器は、流れに耐えるそれらの能力について試験しました。構築物は、特注の灌流システム( 図6)に装填し、100〜417 ml /分の流速で最大5分間流れに供しました。船舶でした流れに耐えることができます。軽微な漏れは、潅流システムにコネクタにおいて、容器の端部で観察されました。
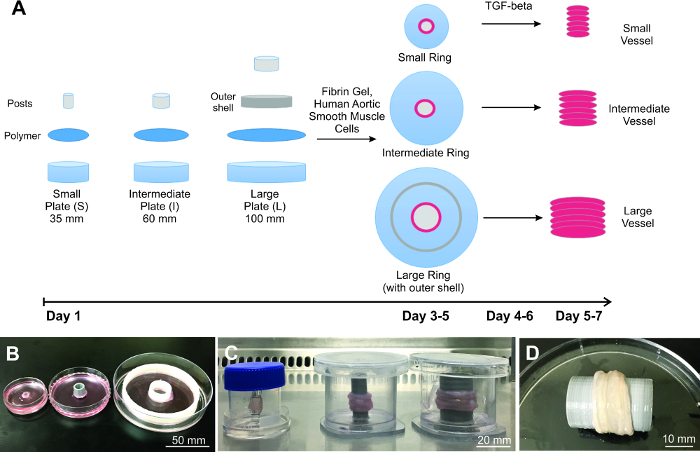
図1: スケーリング工学血管の構築。 A)工学血管をスケーリングするプロセスの図は、プレートの準備、細胞播種と血管建物から始まります。 3異なるサイズのB)リングおよびC)血管が実証されています。 D)代表大血管が完全に生物学的で、自然な組織に似ています。 この図の拡大版をご覧になるにはこちらをクリックしてください。
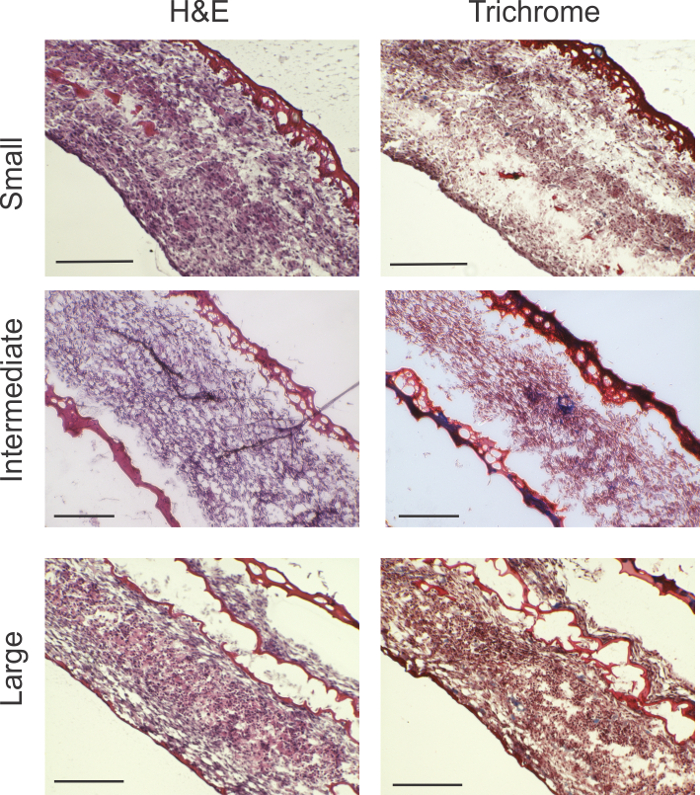
図2:組織学的分析。 > H&E栄とマッソントリクローム染色は、すべてのリングサイズのためのリング厚さ全体にわたって生存可能な細胞充実性を示しています。トリクローム染色はブルー(青矢印)で示されるコラーゲン産生の領域を明らかにしました。大きなリングが原因細胞シートの比較的大きな表面積の折りたたみの可能性、フィブリンゲルが散在示しました。スケールバー:小さなリング= 200ミクロン;中間リング= 200ミクロン;そして、大きなリング= 0.5ミリメートル。 この図の拡大版をご覧になるにはこちらをクリックしてください。
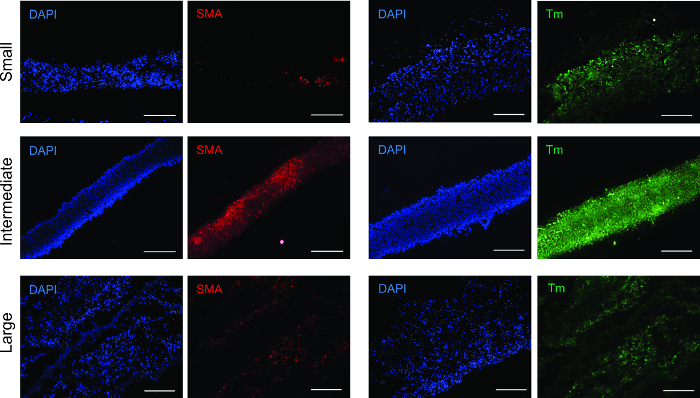
図3:平滑筋マーカーのための免疫蛍光分析。すべてのリングサイズは、平滑筋収縮タンパク質α平滑筋アクチン(SMA)およびトロポミオシン(Tm)が陽性でした。スケールバー=200μmです。ロード/ 55322 / 55322fig3large.jpg "ターゲット=" _空白 ">この図の拡大版をご覧になるにはこちらをクリックしてください。
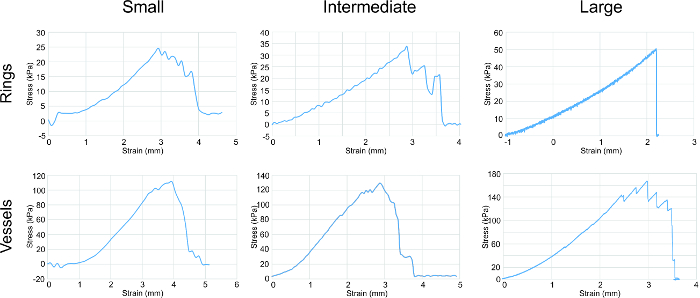
図4:引張試験分析。リングと容器のすべてのサイズの応力 - ひずみ曲線は、リング/血管のサイズの増大と相関する強度の増加の一般的な傾向を示しました。指輪や血管を円周方向に延伸されました。グラフから評価パラメータは、弾性率、極限引張強さ及び破壊強度( 表1に記載)でした。 この図の拡大版をご覧になるにはこちらをクリックしてください。

図5:細胞が播種サーフィンを数相関を播種エースエリア。ヒト大動脈平滑筋細胞に基づきます。表面積は、センターポストとプレート壁または外殻との間の環形成プレート内の領域として定義されます。 この図の拡大版をご覧になるにはこちらをクリックしてください。
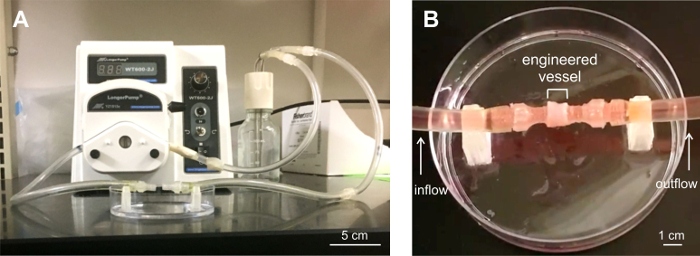
図6:潅流分析に供シックスリング容器。流動試験用A)カスタム構築された灌流システム。 B)灌流システムにロードされた容器を開発しました。三つ血管灌流流動条件下で最大5分間、漏れについて試験しました。容器は、システム配管に取り付けられた容器のエンドコネクタでマイナー漏れて、流れの下で安定していました。 ご覧になるにはこちらをクリックしてください。この図の拡大版。

アニメーション図1:工学血管を通る潅流のデモンストレーション。 このビデオを見るにはこちらをクリックしてください。 (ダウンロードするには、右クリックします。)
| 小さい | 中間体 | 大 | |||||
| リング | 弾性率(kPaで) | 13.6±2.25 | (N = 6) | 14.5±1.2 | (n = 3)を | 17.2±2.2 | (N = 4) |
| 極限引張強さ(Kペンシルベニア州) | 34.5±10.2 | 39.6±2.98 | 50.9±10.6 | ||||
| 破壊強度(キロパスカル) | 34.5±10.2 | 39.6±2.98 | 50.9±10.6 | ||||
| 船舶 | 弾性率(kPaで) | 49.7±2.80 | (n = 3)を | 59.8±3.90 | (N = 2) | 79.8±10.1 | (N = 2) |
| 極限引張強さ(キロパスカル) | 115±6.90 | 137±12.0 | 192±86.9 | ||||
| 破壊強度(キロパスカル) | 96.2±12.2 | 60.7±12.1 | 173±92.2 | ||||
表1:スケーリングリングと容器の引張特性。
ディスカッション
リングスタッキングメソッド現在の血管組織工学構築物の技術上の複数の利点を提供します。 RSMは、単にポストと外殻寸法をカスタマイズすることによって、任意の大きさの人間の血管を生成するように適合され得ます。私たちの方法は、ヒトの細胞でのみ構成されるポリマーフリー工学血管の開発を可能にし、迅速に身体の自然な創傷治癒過程で見つかった支持体材料を劣化させます。ポリマーグラフトは、診療所に再狭窄を引き起こすことが知られており、操作された移植片に含まれている場合に問題となる可能性があります。細胞播種数は、それぞれ異なるサイズの組織のリングのために変更する必要があります。播種数は近似および/または推定することが可能なシード表面積に対する細胞数のグラフは、図5に示されています。なお、ここで使用される細胞型は、ヒト大動脈平滑筋細胞であることに留意すべきです。異なる細胞型にRSMを適合させるために、セルの大きさおよび増殖速度が取り込まれる必要があります考慮し、最適な播種密度を決定しました。例えば、我々はまた、RSMを用いて、ヒト線維芽細胞のリングを作成している、少なくとも細胞の数を約2倍の平滑筋細胞と比較して必要とされることを見出しました。容器の任意の所望の長さは、リングの添加によって構築することができます。リングスタックは最大2ヶ月間培養し、安定的に推移してきました。中級、大きなリングは、両方のは、彼らがそれぞれ100ミリメートルプレート内の外殻の配置によって、それぞれ、60ミリメートルと100ミリメートルプレートで構成されていても、適切な1500μmの壁の厚さに保たれています。これは、所与の容器に適した壁の厚さを制御し、取得するための外殻の有用性を示しています。コラーゲン産生19を刺激することが知られており、リングの締め付けの観察された効果を有しているので、ステップ3.3.1においては、TGF-β1を添加しました。リングは完全に巻かれた後、TGF-β1の1用量は、最終工程で添加され、そしてリングは後で使用する1日の準備ができています。 TGF-β1は、トリクローム画像( 図2)に見られるように、リング内のコラーゲン産生を増強し。
2より大きいサイズで、外側の縁に沿って細胞が組織エッジや他の整列細胞と一緒に整列の度合いを表示するのに対し、小環中の細胞は、より丸くコンパクトです。後者は、より大きなリングでより高い細胞コンテンツから進化した細胞の成熟の後の段階を、示している可能性があり、したがって、細胞間シグナル伝達の大きい程度は成熟を促進します。より大きなリングでフィブリンゲル散在は、より大きな細胞シートは、彼らが転がるようにわずかに折り畳むする傾向があることを示すことができます。この現象を示す組織学的画像がアップしたがって、完全なリングロール、文化の中で分解するために2週間かかりフィブリンゲルは、依然として存在するであろうことは理解され、次の1日に採取しました。少なくとも2週間のリングを培養し、完全な細胞構造物を残し、フィブリンゲルを低下させる必要があります。
NT ">アルファ平滑筋アクチン(SMA)が収縮し、トロポミオシンは、収縮性タンパク質である容易に細いフィラメントを構成している。20、21 SMAおよびトロポミオシンの両方が中間で最強、最も均等に分配された信号で、すべてのサイズのリングに存在しましたリングは、この現象は、収縮operandi開発の増加を刺激し、細胞密度および組織の高度に起因し得ます。弾性率は、リングの弾性を示し、小から大環の増加Eは、コラーゲンとエラスチン産生の増加を示唆しています。極限引張強度は、破断することなくリングによって耐え最高強度です。破壊強度は、組織障害点です。リングのために、UTSはFSに等しいです。船の場合、UTSは、容器の最終的な強度はすべてのリングから機械的貢献の組み合わせに起因していることを示している、FSよりも大きいです容器に、故障箇所は最も弱い環によるものです。
天然ヒト血管がMPaの範囲内に強みを持っているのに対し、私たちの工学血管の強さは、kPaの範囲にありました。ネイティブ血管のことに向かって私たちの血管を強化するために、我々はすなわち、そのコラーゲンとエラスチンの、細胞外マトリックス産生を増加させるための技術を調査しています。コラーゲンとエラスチンの生産を促進する成長因子は、現在、引張特性が増加するかどうかを調査するために私達のリングに適用されています。
機械的特性に加えて、筋肉収縮の機能的な対策は、血管のパフォーマンスに関連します。例えばアセチルコリンおよびエピネフリンなどの因子による筋刺激と収縮は、筋収縮力をテストするために使用することができます。このような実験は、当社の将来の研究のために検討されています。
全体として、我々の結果は、リングスタッキング方法を簡単にスケーリングすることができることを示しています操作された血管組織のサイズの範囲を実現しています。このような直径の大動脈内腔40ミリメートルとして最大の人間の血管にスケーリング、おそらく私たちの研究室が現在開発している脈管の脈管、大型船舶内に自然に存在する微小血管系の開発が必要となります。また、メディア層の内腔は、容器内の適切な血行動態の確立のために重要である、典型的にはライン内皮細胞層( すなわち 、内膜)。私たちの研究室では、現在、ヒト血管内皮細胞を用いて、私たちのSMCリングスタックに内膜の作成に取り組んでいます。これらの組み合わせの技術により、人工血管は、診療所に大きな適用性を持っているでしょう。
開示事項
著者らは、開示することは何もありません。
謝辞
著者らは、組織学、細胞培養液の一部との親切な援助のために私たちの仲間のラムラボの同僚アマルChishtiとBijalパテルに感謝したいと思います。資金はスタートアップ資金と心臓血管研究所のシード・グラント(MTL)、ウェイン州立大学ナノメディシンフェローシップ(CBP)によって提供されました。
資料
| Name | Company | Catalog Number | Comments |
| Human Aortic Smooth Muscle Cells | ATCC | PCS-100-012 | vascular smooth muscle cells |
| Medium 231 | Gibco (Life Technologies | M-231-500 | media specific to vascular smooth muscle cells |
| Human Aortic Smooth Muscle Cell Growth Kit | ATCC | PSC-100-042 | growth factors for maintaining vascular smooth muscle cell viability |
| Replicator Mini 3D printer | MakerBot | N/A | 3D printer |
| Poly(lactic acid) 3D ink (PLA) | MakerBot | N/A | 3D printer filament |
| Poly(dimethlysiloxane) (PDMS) | Ellworth Adhesives | 3097358-1004 | polymer for gluing plate parts |
| Fibrinogen | Hyclone Labratories, Inc. | SH30256.01 | fibrin gel component |
| Thrombin | Sigma Life Sciences | F3879-5G | fibrin gel component |
| Tranforming Growth Factor-Beta 1 | PeproTech | 100-21 | growth factor for stimulating collagen production |
| Hemocytometer | Hausser Scientific Co. | 3200 | for cell counting |
| Polycarbonate tubing | US Plastics | PCTUB1.750X1.625 | material for making tall, ring stacking plates |
| Polycarbonate sheet | Home Depot | 409497 | material for making tall, ring stacking plates |
| Adhesive polymer solvent | SCIGRIP | 10799 | material for making tall, ring stacking plates |
| Instron 5940 | Instron | N/A | tensile testing machine |
| U-Stretch | Cell Scale | N/A | tensile testing machine |
| Smooth Muscle Actin | MA5-11547 | Thermo Fisher | antibody |
| Tropomyosin | MA5-11783 | Thermo Fisher | antibody |
参考文献
- Luciani, G. B., et al. Operative risk and outcome of surgery in adults with congenital valve disease. ASAIO J. 54 (5), 458-462 (2008).
- Lawson, J. H., et al. Bioengineered human acellular vessels for dialysis access in patients with end-stage renal disease: two phase 2 single-arm trials. Lancet. 14 (387), 2026-2034 (2016).
- McAllister, T. N., et al. Effectiveness of haemodialysis access with an autologous tissue-engineered vascular graft: a multicentre cohort study. Lancet. 373 (9673), 1440-1446 (2009).
- Wystrychowski, W., et al. First human use of an allogeneic tissue-engineered vascular graft for hemodialysis access. J Vasc Surg. 60 (5), 1353-1357 (2014).
- Konig, G., et al. Mechanical properties of completely autologous human tissue engineered blood vessels compared to human saphenous vein and mammary artery. Biomaterials. 30 (8), 1542-1550 (2009).
- Gui, L., et al. Construction of tissue-engineered small-diameter vascular grafts in fibrin scaffolds in 30 days. Tissue Eng Part A. 20 (9-10), 1499-1507 (2014).
- Sundaram, S., Echter, A., Sivarapatna, A., Qiu, C., Niklason, L. Small-diameter vascular graft engineered using human embryonic stem cell-derived mesenchymal cells. Tissue Eng Part A. 20 (3-4), 740-750 (2014).
- Quint, C., Arief, M., Muto, A., Dardik, A., Niklason, L. E. Allogeneic human tissue-engineered blood vessel. J Vasc Surg. 55 (3), 790-798 (2012).
- Quint, C., et al. Decellularized tissue-engineered blood vessel as an arterial conduit. Proc Natl Acad Sci U S A. 31 (108), 9214-9219 (2011).
- Dahl, S. L., et al. Readily available tissue-engineered vascular grafts. Sci Transl Med. 2 (68), (2011).
- Syedain, Z. H., Meier, L. A., Lahti, M. T., Johnson, S. L., Tranquillo, R. T. Implantation of completely biological engineered grafts following decellularization into the sheep femoral artery. Tissue Eng Part A. 20 (11-12), 1726-1734 (2014).
- Syedain, Z. H., Meier, L. A., Bjork, J. W., Lee, A., Tranquillo, R. T. Implantable arterial grafts from human fibroblasts and fibrin using a multi-graft pulsed flow-stretch bioreactor with noninvasive strength monitoring. Biomaterials. 32 (3), 714-722 (2011).
- Meier, L. A., et al. Blood outgrowth endothelial cells alter remodeling of completely biological engineered grafts implanted into the sheep femoral artery. J Cardiovasc Transl Res. 7 (2), 242-249 (2014).
- Pinnock, C. B., Meier, E. M., Joshi, N. N., Wu, B., Lam, M. T. Customizable engineered blood vessels using 3D printed inserts. Methods. S1046-2023 (15), 30184-30185 (2015).
- Blakely, A. M., Manning, K. L., Tripathi, A., Morgan, J. R. Bio-Pick, Place,and Perfuse: A New Instrument for Three-Dimensional Tissue Engineering. Tissue Eng Part C Methods. 21 (7), 737-746 (2015).
- Gwyther, T. A., et al. Engineered vascular tissue fabricated from aggregated smooth muscle cells. Cells Tissues Organs. 194 (1), 13-24 (2011).
- Fearon, W. F., et al. Changes in coronary arterial dimensions early after cardiac transplantation. Transplantation. 27 (6), 700-705 (2007).
- Erbel, R., Eggebrecht, H. Aortic dimensions and the risk of dissection. Heart. 92 (1), 137-142 (2006).
- Ha, D. M., et al. Transforming growth factor-beta 1 produced by vascular smooth muscle cells predicts fibrosis in the gastrocnemius of patients with peripheral artery disease. J Transl Med. 14, 39(2016).
- Skalli, O., et al. Alpha-smooth muscle actin, a differentiation marker of smooth muscle cells, is present in microfilamentous bundles of pericytes. J Histochem Cytochem. 37 (3), 315-321 (1989).
- von der Ecken, J., et al. Structure of the F-actin-tropomyosin complex. Nature. 519 (7541), 114-117 (2015).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved