Extraction solide-liquide
Vue d'ensemble
Source : Laboratoire de Dr. Jay Deiner — City University of New York
L’extraction est une étape cruciale dans des analyses plus chimiques. Il s’agit d’éliminer de l’analyte de sa matrice de l’échantillon et en le passant dans la phase a besoin pour la quantification et identification spectroscopique ou par chromatographie en phase. Lorsque l’échantillon est un solide et la phase nécessaire pour l’analyse est un liquide, le processus est appelé extraction solide-liquide. Une forme simple et largement applicable d’extraction solide-liquide implique combinant le solide avec un solvant dans lequel l’analyte est soluble. Par agitation, les partitions de l’analyte dans la phase liquide, qui peut ensuite être séparé du solide par l’intermédiaire de filtration. Le choix du solvant convient basé sur la solubilité de l’analyte cible et sur le solde du coût et de sécurité, les préoccupations environnementales.
Principles
Extraction utilise la propriété de solubilité pour transférer un soluté d’une phase à une autre phase. Afin d’effectuer une extraction, soluté doit avoir une solubilité plus élevée dans la deuxième phase que dans la première phase. En extraction liquide-liquide, un soluté est séparé entre deux phases liquides, généralement une phase aqueuse et une phase organique. Dans le cas le plus simple, trois composantes sont impliqués : le soluté, le liquide du transporteur et du solvant. Le mélange initial, contenant le soluté dissous dans le liquide de transporteur, est mélangé avec le solvant. Après mélange, le soluté est transféré depuis le liquide porteur au solvant. La solution plus dense se dépose au fond. L’emplacement du soluté dépendra des propriétés des liquides et le soluté.
Extraction solide-liquide est semblable à une extraction liquide-liquide, sauf que le soluté est dispersé dans une matrice solide, plutôt que dans un liquide porteur. La phase solide, contenant le soluté, est dispersée dans le solvant et mixtes. Le soluté est extraite de la phase solide au solvant, et la phase solide est ensuite éliminée par filtration.
Dans cette vidéo, un exemple de la technique d’extraction solide-liquide est illustré en montrant l’extraction des résidus organochlorés dans le sol. L’extraction solide-liquide illustrée implique la combinaison de l’échantillon avec n-hexanes suivies d’agitation ultrasonique, filtration, l’élimination des eaux résiduelles par séchage sur CaCl2et préconcentration sous courant d’azote. L’échantillon préparé comme est alors prêt pour l’analyse d’un éventail de méthodes chromatographiques et spectroscopiques.
Procédure
1. extraction de produits organiques adsorbés dans le sol
- Placer 20 g de terre dans un plat en Pyrex de large-bouche propre et sec dans un four à 50 ° C et sécher pendant au moins 12 h. Après séchage, retirer le sol le plat en Pyrex et broyer en une poudre homogène à l’aide d’un mortier et un pilon. Peser 5,00 g du sol et placez-le dans un ballon à fond rond (100 mL en taille) propre et sec. Dans le ballon, ajouter 15 mL de n-hexane. Placer la fiole dans un bain ultrasonique et laisser agir pendant 60 min.
2. séparation de l’extrait et le sol
- Préparer un entonnoir Büchner analytique de papier filtre. Mouiller le papier filtre avec 1 mL de n-hexane et commencer la filtration sous vide. Versez lentement le contenu du ballon à fond rond sur le papier filtre. Le flacon de Büchner contient maintenant le n-hexane avec les matières organiques extraites du sol. Le filtre retient les solides du sol dénudé.
3. nettoyer haut et préconcentration
- Si le n-hexane solution est nuageuse, il y a l’eau résiduelle. Sécher le n-solution d’hexane, ajouter une petite spatule de CaCl2. Agiter la solution et d’observer pendant au moins 15 min. Si la solution est encore trouble et/ou toutes les CaCl2 est groupé en masse compacte, il n’y a encore l’eau restante, et étape 3.1 doit être répété. Si la solution est translucide et le CaCl2 est fluide, puis de ne pas répéter étape 3.1. Une fois une solution claire a été atteint, séparer les hexanes CaCl2 , à l’aide de filtration de la gravité. Si la concentration de l’extrait est suffisante pour la détection, les hexanes filtrés peuvent être transférées à un flacon propre et sec pour le stockage et l’analyse ultérieure. Si la concentration de l’extrait est faible par rapport à la limite de détection, transférer les hexanes filtrées dans un propre et sec à col trois ballon à fond rond, 100 mL en taille. Placez un bouchon en caoutchouc dans le goulot du centre de la fiole et un septum en caoutchouc sur l’un des autres cous. Laissez le troisième col ouvert. Percer le bouchon de caoutchouc et d’introduire un courant d’azote par le biais de la fiole. L’azote doit être coulant dans l’espace situé au-dessus de la solution, ne pas de propagation via la solution. L’extrait peut maintenant être pré concentré par coulant azote pour évaporer l’excès de solvant. L’échantillon est maintenant prêt pour l’analyse.
Résultats
Un échantillon de sol a été prélevé d’une friche industrielle semblable à celle à Sewickley en Pennsylvanie, comme indiqué dans Figure 1. Friches industrielles, telles que définies par les États-Unis États Environmental Protection Agency (U.s. EPA), sont des biens réels, où l’expansion, le réaménagement ou la réutilisation peut être compliquée en raison de la présence potentielle de contaminants dangereux. Le sol a été prélevé de la friche industrielle à l’aide d’un échantillonneur de sol, comme le montre Figure 2.
Les polluants d’intérêt dans cette expérience était l’atrazine (Figure 3) ; un herbicide courant des organochlorés. Une fois que les composants organiques du sol ont été extraites et concentrés, ils ont été analysés par chromatographie en phase gazeuse avec un détecteur à ionisation de flamme (GC-FID). L’analyse de GC a été réalisée à l’aide d’un GC de Shimadzu 14 a (détecteur : FID) équipé d’un injecteur split/splitless et une colonne capillaire de CBP-10 (30 m × 0,22 mm d.i.). La température de la colonne a été d’abord fixée à 150 ° C et ensuite programmée de 150 à 230 ° C, à raison de 5 ° C / min. La température de l’injecteur a 250 ° C et la température du détecteur 260 ° C. Les injections ont été réalisées avec le mode splitless. Gaz vecteur hélium a été utilisé à un débit constant de 1 mL/min. La concentration de l’atrazine a été calculée en utilisant des concentrations d’atrazine standard, comme illustré à la Figure 4. Dans ce cas, la concentration approximative de l’atrazine dans la friche a étudié était de 2 mg d’atrazine par kg de sol.

La figure 1. Friche industrielle à Sewickley, PA.

La figure 2. Le sol prélevé à l’aide d’un échantillonneur de sol contaminé.

La figure 3. Structure chimique de l’atrazine organochlorés.
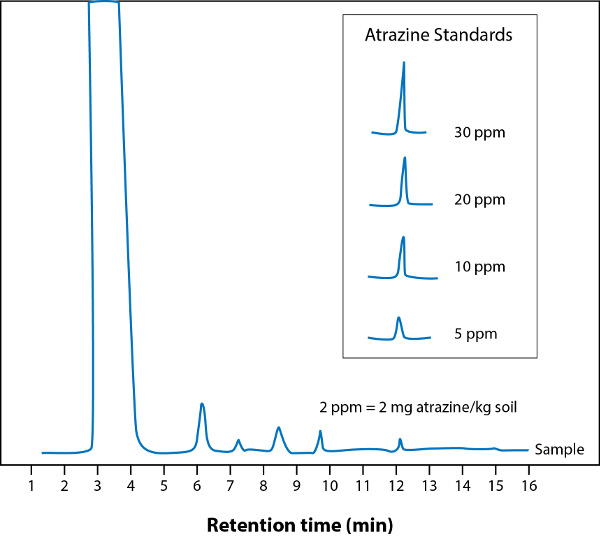
La figure 4. Chromatogramme de gaz de l’échantillon de sol avec l’atrazine. Médaillon : normes atrazine.
Applications et Résumé
La procédure générale extraction solide-liquide s’applique à un éventail de domaines de surveillance de l’environnement (montrée dans cette vidéo) aux cosmétiques et la transformation des aliments. La question cruciale est de choisir un solvant dissout efficacement l’analyte. Avec des changements minimes dans le solvant, le procédé de préparation d’échantillon dans cette vidéo peut servir à extraire tout d’un large éventail de contaminants environnementaux semi-volatils cette partition principalement sur les sols et les boues.
Exemples de ces semivolatiles de nombreux polluants nocifs tels que pesticides, hydrocarbures aromatiques polycycliques (HAP) et les polychlorobiphényles (PCB). En raison de l’ampleur de la santé les effets de ces molécules, l’identification et la quantification de ces espèces est d’un intérêt théorique et aussi largement pratiquée dans l’industrie environnementale et dans les organismes gouvernementaux. L’EPA maintient les recueils des méthodes approuvées d’analyses et d’échantillonnage pour identifier et quantifier les polluants possibles. La méthode présentée dans cette vidéo illustre les principes de base contenus dans la méthode EPA 3550C, qui décrit l’extraction ultrasonique de semivolatiles et nonvolatiles des solides. 1 méthode EPA 3550 C est une des méthodes d’extraction référencées dans la méthode EPA 8081B, qui décrit l’analyse de GC de pesticides organochlorés. 2 la plupart des fichiers méthode approuvé par l’EPA sont écrits avec l’hypothèse que l’analyste a une formation préalable. Gagnant ainsi, connaissant les caractéristiques de base du sida préparation échantillon en suivant les méthodes de l’EPA.
L’utilisation d’un appareil de Soxhlet peut aider à l’extraction des solutés qui sont peu solubles dans les solvants. L’installation se compose d’un ballon à fond rond, un appareil d’extraction Soxhlet et un réfrigérant à reflux. Cette technique est démontrée par l’élimination des PCB des poissons afin d’examiner le transfert des toxines entre les poissons prédateurs et proies des poissons. 3 en outre, cette technique peut servir à mesurer la teneur en cires en peaux de fruits afin de comprendre la composition et la dégradation des fruits indigènes et d’ingénierie. 4 Enfin, l’extraction des hydrates de carbone de la lignocellulose, ou la matière végétale sèche, peut se faire par extraction liquide solide. 5 lorsque les glucides sont extraites, la lignine est laissée. Les deux composants puis peuvent être utilisés que pour des applications de biocarburant.
Divulgations
Passer à...
Vidéos de cette collection:

Now Playing
Extraction solide-liquide
Organic Chemistry
238.4K Vues

Introduction à la catalyse
Organic Chemistry
34.7K Vues

Montage d'un chauffage à reflux
Organic Chemistry
168.6K Vues

Réaliser des réactions en dessous de la température ambiante
Organic Chemistry
70.8K Vues

Transfert de solvants via une rampe à vide (ligne Schlenk)
Organic Chemistry
41.7K Vues

Dégazage des liquides par la technique "cycle geler-pomper-dégeler"
Organic Chemistry
56.4K Vues

Préparation de réactifs anhydres et équipement
Organic Chemistry
79.5K Vues

Purification des composés par recristallisation
Organic Chemistry
711.0K Vues

Séparation des mélanges par précipitation
Organic Chemistry
158.2K Vues

Utilisation d'un évaporateur rotatif (ou Rotovap) pour éliminer un solvant
Organic Chemistry
213.1K Vues

Distillation fractionnée
Organic Chemistry
335.1K Vues

Préparation de cristaux pour analyse par diffraction des rayons X
Organic Chemistry
32.9K Vues

Performing 1D Thin Layer Chromatography
Organic Chemistry
290.3K Vues

Chromatographie sur colonne
Organic Chemistry
361.6K Vues

Spectroscopie à résonance magnétique nucléaire (RMN)
Organic Chemistry
249.2K Vues