Method Article
Imagerie tissulaire hautement multiplexée avec des colorants Raman
Dans cet article
Résumé
L’imagerie électronique par diffusion Raman stimulée par pré-résonance (epr-SRS) de colorants Raman de type arc-en-ciel est une nouvelle plate-forme pour l’imagerie de protéines à base d’épitopes hautement multiplexées. Ici, nous présentons un guide pratique comprenant la préparation des anticorps, la coloration des échantillons de tissus, l’assemblage du microscope SRS et l’imagerie tissulaire epr-SRS.
Résumé
La visualisation d’un vaste éventail de biomarqueurs spécifiques dans les tissus joue un rôle essentiel dans l’exploration des organisations complexes de systèmes biologiques complexes. Par conséquent, les technologies d’imagerie hautement multiplexées ont été de plus en plus appréciées. Nous décrivons ici une plate-forme émergente d’imagerie vibratoire hautement multiplexée de protéines spécifiques avec une sensibilité comparable à l’immunofluorescence standard via l’imagerie électronique par diffusion Raman stimulée par pré-résonance (epr-SRS) de colorants Raman de type arc-en-ciel. Cette méthode contourne la limite des canaux résolvables spectralement dans l’immunofluorescence conventionnelle et fournit une approche optique unique pour interroger plusieurs marqueurs dans les tissus avec une résolution subcellulaire. Il est généralement compatible avec les préparations tissulaires standard, y compris les tissus fixés au paraformaldéhyde, les tissus congelés et les tissus humains incorporés dans de la paraffine fixée au formol (FFPE). Nous envisageons que cette plate-forme fournira une image plus complète des interactions protéiques des spécimens biologiques, en particulier pour les tissus épais intacts. Ce protocole fournit le flux de travail de la préparation des anticorps à la coloration des échantillons de tissus, à l’assemblage du microscope SRS, à l’imagerie tissulaire epr-SRS.
Introduction
Les systèmes tissulaires complexes sont composés de sous-populations cellulaires distinctes dont les emplacements spatiaux et les réseaux d’interaction sont profondément liés à leurs fonctions et à leurs dysfonctionnements 1,2. Pour révéler l’architecture tissulaire et interroger sa complexité, la connaissance des emplacements spatiaux des protéines à résolution unicellulaire est essentielle. Par conséquent, les technologies d’imagerie protéique hautement multiplexées ont été de plus en plus appréciées et pourraient devenir une pierre angulaire pour l’étude de la biologie tissulaire 3,4,5. Les méthodes courantes actuelles d’imagerie des protéines multiplexées peuvent être classées en deux catégories principales. L’un est l’imagerie par immunofluorescence en série reposant sur plusieurs cycles de coloration tissulaire et d’imagerie, et l’autre est l’imagerie par cytométrie de masse couplée àdes anticorps marqués par des métaux lourds 6,7,8,9,10,11,12.
Ici, une stratégie alternative pour l’imagerie des protéines multiplexées à base d’anticorps est introduite. Contrairement à la modalité d’imagerie par fluorescence répandue, qui ne peut visualiser que 4 à 5 canaux simultanément en raison des larges spectres d’excitation et d’émission (pleine largeur à la moitié maximale (FWHM) ~ 500 cm-1), la microscopie Raman présente une largeur de ligne spectrale beaucoup plus étroite (FWHM ~ 10 cm-1) et fournit donc une multiplexité évolutive. Récemment, en exploitant le spectre étroit, un nouveau schéma de microscopie Raman nommé microscopie électronique à diffusion Raman stimulée par pré-résonance (epr-SRS) a été développé, fournissant une stratégie puissante pour l’imagerie multiplexée13. En sondant les modes vibratoires couplés électroniquement des colorants Raman, epr-SRS obtient un effet d’amélioration drastique de10 13 fois sur les sections transversales Raman et surmonte le goulot d’étranglement de sensibilité de la microscopie Raman conventionnelle (Figure 1A)13,14,15. En conséquence, la limite de détection de l’epr-SRS a été repoussée à moins de μM, ce qui permet la détection Raman de marqueurs moléculaires intéressants tels que des protéines et des organites spécifiques à l’intérieur des cellules13,16. En particulier, en utilisant des anticorps conjugués au colorant Raman, l’imagerie epr-SRS de protéines spécifiques dans les cellules et les tissus (appelée immuno-eprSRS) a été démontrée avec une sensibilité comparable à l’immunofluorescence standard (Figure 1B)13,17. En réglant la longueur d’onde de la pompe de seulement 2 nm, le signal epr-SRS sera complètement désactivé (Figure 1B), ce qui présente un contraste vibratoire élevé.
Du côté de la sonde, un ensemble de sondes Raman de type arc-en-ciel appelées colorants de diffusion Raman Manhattan (MARS) a été développé pour la conjugaison des anticorps 13,18,19,20. Cette palette Raman unique se compose de nouveaux colorants portant des liaisons triples conjuguées π (matériau supplémentaire), chacun affichant un pic epr-SRS unique et étroit dans la gamme spectrale Raman bioorthogonale (Figure 1C). En modifiant la structure du chromophore central et en éditant isotopiquement les deux atomes de la triple liaison (matériau supplémentaire), des sondes Raman séparées spectralement ont été développées. Tirant parti de la multiplexité évolutive, la microscopie epr-SRS associée à la palette de colorants MARS offre une stratégie optique pour l’imagerie des protéines multiplex en un seul coup dans les cellules et les tissus.
Immuno-eprSRS fournit une stratégie alternative aux méthodes actuelles d’imagerie des protéines multiplexes avec des forces uniques. Par rapport aux approches de fluorescence avec coloration cyclique, imagerie et élimination du signal, cette plate-forme basée sur Raman assure une coloration et une imagerie à un tour. Par conséquent, il contourne la complexité pratique des procédures cycliques et simplifie largement le protocole, ouvrant ainsi de nouveaux territoires d’imagerie des protéines multiplexées. Par exemple, en exploitant un protocole de nettoyage des tissus adapté aux colorants Raman, l’immuno-eprSRS a été étendue à trois dimensions pour la cartographie des protéines hautement multiplexées dans les tissus intacts épais17. Plus de 10 cibles protéiques ont été visualisées le long de tissus cérébraux de souris d’une épaisseur millimétrique17. Plus récemment, le couplage de l’immuno-eprSRS avec un protocole optimisé de microscopie à expansion de rétention de biomolécules (ExM)21, l’imagerie nanométrique à un coup de plusieurs cibles a également été démontré22. Comparé à la spectroscopie de masse d’imagerie 4,9, epr-SRS est non destructif et a une capacité de sectionnement intrinsèquement optique. De plus, epr-SRS est plus rapide sur le balayage des tissus. En règle générale, une région tissulaire de 0,25 mm2 avec une taille de pixel de 0,5 μm ne prend que quelques minutes à imager pour un seul canal epr-SRS. Par exemple, le temps total d’imagerie de quatre canaux SRS plus quatre canaux de fluorescence dans la figure 4 est d’environ 10 min.
Protocole
Le protocole a été mené conformément au protocole expérimental animal (AC-AABD1552) approuvé par le Comité institutionnel de soins et d’utilisation des animaux de l’Université Columbia.
1. Préparation d’anticorps conjugués Raman-dye
- Préparer le tampon de conjugaison comme ~0,1 M NaHCO3 dans un tampon PBS, pH = 8,3, conserver à 4 °C.
- Préparer la solution de sonde MARS fonctionnant sous forme d’ester (matériau supplémentaire) de N-hydroxysuccinimidy (NHS) sous forme de 3 mM dans du DMSO anhydre. La synthèse des sondes MARS peut être renvoyée aux rapports antérieurs 13,17,18.
REMARQUE: À des fins de stockage, la solution d’ester NHS doit être protégée de la lumière et maintenue à -20 ° C. - Dissoudre les solides d’anticorps dans le tampon de conjugaison à une concentration de 2 mg/mL. Pour les anticorps qui sont dissous dans d’autres tampons, échangez-les dans le tampon de conjugaison à une concentration de 1-2 mg / mL avec des filtres centrifuges.
REMARQUE: Les anticorps secondaires hautement adsorbés par croisement sont préférés pour la coloration multiplex afin de minimiser la réactivité inter-espèces. Les anticorps secondaires utilisés sont énumérés dans le tableau 1 et le tableau des matériaux. - Effectuer la réaction de conjugaison.
- Pour les anticorps secondaires, ajouter 15 fois l’excès molaire de solution de colorant à la solution d’anticorps dans un flacon en verre lentement en remuant. Par exemple, dans une solution d’anticorps de 0,5 mL 2 mg/mL, ajouter 35 μL 3 mM de solution de colorant.
- Incuber le mélange réactionnel à température ambiante (RT) sous agitation pendant 1 h. Protégez la réaction de la lumière.
- Purification.
- Préparer la boue de résine de filtration en gel (Table des matériaux) dans un tampon PBS, en suivant les étapes 1.5.2-1.5.4.
- Ajouter 10 mL de poudre de résine de filtration de gel dans 40 mL de tampon PBS à l’intérieur d’un tube de 50 mL.
- Conserver la solution au bain-marie à 90 °C pendant 1 h.
- Décantez le surnageant et rajoutez le PBS à 40 mL. Conserver la bouillie à 4 °C.
- Emballez la colonne d’exclusion de taille (diamètre de 1 cm, colonnes à écoulement par gravité) avec la solution de boue à la hauteur de 10-15 cm.
- Rincez et lavez la colonne avec environ 10 mL de tampon PBS pour emballer davantage la résine.
- Pipeter le mélange réactionnel de conjugaison (~0,5 mL) à la colonne. Ajouter immédiatement 1 mL de tampon PBS comme tampon d’élution lorsque tout le mélange réactionnel est chargé. Rechargez constamment le tampon d’élution (PBS) dans la colonne.
- Recueillir l’éluat de la solution conjuguée en regardant la couleur sur la colonne (les colorants MARS ont des couleurs vert clair à bleu) ou en mesurant l’absorbance à 280 nm (A280).
- Concentrer la solution collectée à 1-2 mg/mL avec un filtre centrifuge.
- Déterminer la concentration et le degré moyen de marquage (DOL, rapport colorant-protéine) en mesurant le spectre ultraviolet-visible (UV-Vis) de la solution conjuguée à l’aide d’un lecteur de nanoplaques.
REMARQUE: Le matériau supplémentaire fournit les propriétés des esters NHS de colorant MARS pour le calcul. Le DOL normal pour l’anticorps secondaire est d’environ 3.
2. Préparation d’échantillons de tissus
- Paraformaldéhyde fixe les tissus cérébraux de souris.
- Anesthésier les souris (C57BL/6J, Femelle, 25 d postnatale) avec de l’isoflurane. Évaluez la bonne anesthésie avec un test de pincement des orteils.
- Tuez les souris par déplacement cervical. Perfuser immédiatement les souris avec 4% de paraformaldéhyde (PFA) dans pbS de manière transcardique.
- Recueillir le cerveau de la souris, en suivant les étapes 2.1.4-2.1.5
- Couper vers le haut à partir du tronc cérébral le long de la suture sagittale. Pelez les deux moitiés du crâne sur le côté et retirez le cerveau avec une pince.
- Fixer le cerveau collecté dans 4% de PFA dans pbS à 4 °C pendant 24 h. Ensuite, lavez le cerveau dans un tampon PBS à 4 °C pendant 24 h pour éliminer l’excès de PFA.
- Placer l’agarose solide dans l’eau jusqu’à une concentration finale de 7% (p / v) dans un bécher, avec un couvercle lâche. Remuer la solution avec une tige d’agitation en verre. Chauffer la boue au micro-ondes jusqu’à ce que la solution soit claire.
- Laisser refroidir l’agarose à 45-55 °C.
- Versez l’agarose liquide dans une petite chambre, puis transférez le cerveau du PBS à l’agarose liquide et orientez-le avec une spatule pour intégrer le cerveau. Attendez que le bloc tissu-agarose durcisse.
- Découper l’agrose tissulaire en tranches coronales de 40 μm d’épaisseur à l’aide d’un vibratome.
- Transférer le tissu dans une plaque à 4 puits pour la coloration suivante. Retirez l’agarose avec une pince à épiler. Lavez le mouchoir avec 1 mL de PBS, trois fois.
- Tissus pancréatiques de souris congelés fixes.
- Fixer le pancréata de la souris dans 4% de PFA dans pbS à 4 ° C avec un basculement pendant 16-20 h.
- Lavez l’échantillon dans 1 mL de PBS (4 °C) trois fois pour éliminer le PFA.
- Incorporer l’échantillon (~0,3-0,5 cm) dans des blocs composés à température de coupe optimale (OCT). Mettez 2 gouttes d’OCT dans un cryomoulage en plastique. Placez le tissu dans la bonne orientation et versez l’OCT sur les tissus jusqu’à ce qu’aucun tissu ne reste exposé.
- Coupez le pancréas en tranches de 8 μm d’épaisseur et immobilisez-les sur une lame de verre de liaison tissulaire, stockez-les à -80 °C.
- Avant de tacher, équilibrez l’échantillon en RT. Lavez le tissu avec du PBS pour enlever les blocs OCT.
- Échantillons FFPE.
- Cuire la lame de tissu FFPE à 60 °C pendant 10 min.
- Déparaffinisation et réhydratation: Placer les échantillons séquentiellement dans les solutions suivantes dans un tube de 50 mL à RT pendant 3 minutes à chaque fois avec une légère agitation:
xylène deux fois,
éthanol deux fois,
95% (vol/vol) d’éthanol dans de l’eau désionisée deux fois,
70% (vol/vol) d’éthanol dans de l’eau désionisée deux fois,
50% (vol/vol) d’éthanol dans de l’eau désionisée une fois,
eau désionisée une fois. - Transférer l’échantillon dans du citrate de sodium de 20 mM (pH 8,0) à 100 °C dans un bocal en verre. Assurez-vous que les tissus sont immergés dans la solution.
- Mettez le pot au bain-marie à 60 °C pendant 45 min.
- Laver l’échantillon avec de l’eau désionisée à TA pendant 5 min.
3. Coloration immuno-eprSRS tissulaire
- Utilisez un stylo hydrophobe pour tracer une limite autour des sections de tissu sur la diapositive.
REMARQUE: Un pot de coloration à glissière est utilisé pour suivre les étapes d’incubation du tissu sur la lame. Les tissus flottants (sections cérébrales de souris de 40 μm d’épaisseur) sont colorés dans des plaques de puits. - Incuber les tissus avec 0,3-0,5% de PBST (Triton X-100 dans PBS) pendant 10 min.
- Incuber les tissus avec un tampon bloquant (5% de sérum d’âne, 0,5% de Triton X-100 dans du PBS) pendant 30 min.
- Préparer la solution de coloration primaire: ajouter tous les anticorps primaires à 200-500 μL de tampon de coloration (2% de sérum d’âne, 0,5% de Triton X-100 dans PBS) aux concentrations souhaitées. Centrifuger la solution de coloration primaire à 13 000 x g pendant 5 min. N’utilisez le surnageant que si les précipités se forment.
- Incuber le tissu dans la solution d’anticorps primaire à 4 °C pendant 1-2 jours.
REMARQUE: Pour les sections de tissu de coloration sur la diapositive, mettez l’échantillon dans une boîte de coloration avec une lingette humide pour maintenir l’humidité. - Lavez les lames trois fois avec 0,3-0,5% PBST à RT pendant 5 minutes chacune. Utilisez 1 mL de PBST pour les tissus flottants. Pour les mouchoirs sur la lame, lavez les lames dans un pot de coloration à glissière et assurez-vous que les tissus sont tous immergés dans la solution.
- Incuber le tissu dans 200-500 μL de tampon bloquant pendant 30 min.
- Préparer la solution de coloration secondaire : ajouter tous les anticorps secondaires (et les lectines si nécessaire) à 200-500 μL de tampon de coloration avec les concentrations souhaitées (normalement 10 μg/mL). Centrifuger la solution de coloration secondaire à 13 000 x g pendant 5 min. N’utilisez le surnageant que si les précipités se forment.
- Incuber les tissus dans 200-500 μL de solution d’anticorps secondaire à 4 °C pendant 1-2 jours.
- Lavez les lames deux fois avec 0,3-0,5% PBST à RT pendant 5 min chacune.
- Incuber avec 200-500 μL de solution de DAPI pendant 30 min.
- Lavez les diapositives trois fois avec PBS à RT pendant 5 minutes chacune.
- Pour les coupes de tissus flottants, transférez-les sur des lames de verre avec une pipette à goutte de verre. Étalez le mouchoir avec une brosse à mouchoirs et nettoyez l’environnement avec des lingettes si nécessaire.
- Montez le tissu dans une goutte de réactifs antifade avec un couvercle en verre et fixez-le avec du vernis à ongles.
4. Assemblage de microscope SRS
REMARQUE: Un système de fluorescence confocale commercial est utilisé dans l’imagerie par fluorescence SRS en tandem. D’autres descriptions peuvent être trouvées dans un rapport antérieur17. Ce protocole se concentrera sur le côté imagerie SRS en utilisant l’excitation à bande étroite.
- Préparez une table optique isolée des vibrations dans une pièce avec contrôle de la température.
- Placez un système double laser synchronisé (pompe et Stokes) sur la table optique (Figure 2A) avec un refroidisseur connecté.
REMARQUE: Le laser fondamental du système à double laser fournit un train d’impulsions de sortie à 1064 nm avec une largeur d’impulsion de 6 ps et un taux de répétition de 80 MHz. Le faisceau de Stokes provient du laser fondamental. L’intensité du faisceau de Stokes a été modulée sinusoïdalement par un modulateur d’amplitude électro-optique (EOM) intégré à 8 MHz avec une profondeur de modulation de plus de 90%. L’autre partie du laser fondamental est doublée de fréquence à 532 nm, qui est ensuite utilisée pour ensemencer de manière synchrone un oscillateur paramétrique optique picoseconde (OPO) afin de produire un train d’impulsions à mode verrouillé avec une largeur d’impulsion de 5 à 6 ps (le faisceau inactif de l’OPO est bloqué par un filtre interférométrique). La longueur d’onde de sortie de l’OPO est accordable de 720 à 950 nm, qui sert de faisceau de pompe. - Montez les miroirs (gamme de longueurs d’onde: 750-1100 nm), les séparateurs de faisceau dichroïque (DBS, filtre passe-long de 980 nm, rectangulaire) et la lentille (achromatique, revêtement AR pour 650-1050 nm) sur leurs montures respectives. Utilisez des supports de miroir très stables pour les miroirs et les séparateurs de faisceaux dichroïques.
- Mesurez la hauteur de la sortie laser et la taille des faisceaux de la pompe et des faisceaux de Stokes. Ajustez la hauteur des miroirs et des lentilles pour vous assurer que la lumière atteindra le centre de tous les éléments optiques.
- Placez le miroir M1 sur la table optique et faites-le ~45° à la sortie laser (Figure 2B). Utilisez les boutons du support cinématique pour effectuer des réglages de pointe et d’inclinaison. Assurez-vous que la lumière se déplace à la même hauteur le long de la table et en ligne droite par rapport à la table.
- Placez et alignez les séparateurs de faisceaux dichroïques (filtres passe-long de 980 nm) et les miroirs pour diviser la pompe et les faisceaux de Stokes (Figure 2A-B).
- Placez et alignez les paires de lentilles (L1, L2 et L3, L4) sur chacun des chemins de faisceau pour collimater les faisceaux et élargir les diamètres du faisceau pour correspondre à la pupille arrière de l’objectif (Figure 2A-B).
- Utilisez les miroirs M7 et M8 pour aligner les faisceaux laser combinés dans le microscope (Figure 2C). Alignez d’abord un faisceau dans le microscope et utilisez les paires de miroirs sur l’autre faisceau pour assurer le chevauchement spatial des deux faisceaux.
- Configurez la partie détection.
- Mettez un condenseur d’huile revêtu d’infrarouge (1,4-NA) pour recueillir la pompe avant et les faisceaux de Stokes après avoir traversé les échantillons (Figure 2C).
- Montez une photodiode Si de grande surface sur un boîtier blindé avec des connecteurs BNC (Figure 2E). Ajoutez une alimentation 64 V CC à la photodiode montée pour augmenter son seuil de saturation et sa bande passante de réponse.
- Réfléchissez la lumière vers l’avant avec un miroir de 2 pouces. Recentrez la lumière sur la photodiode après un filtre optique pour bloquer le faisceau de Stokes modulant (Figure 2D).
- Envoyez le courant de sortie de la photodiode à un amplificateur à verrouillage rapide terminé par 50 pour la démodulation du signal. Envoyez un déclencheur de 8 MHz à l’amplificateur de verrouillage comme signal de référence.
- Envoyez le composant X en phase de l’amplificateur de verrouillage dans le boîtier d’interface analogique du microscope.
- Optimisez le chevauchement temporel avec l’étage de retard motorisé intégré en mesurant le signal SRS du liquide D2O pur au microscope.
5. Acquisition et analyse d’images
- Effectuez une imagerie epr-SRS multicanal avec réglage séquentiel de la longueur d’onde de la pompe.
- Réglez la puissance laser sur la pompe P = 10-40 mW et PStokes = 40-80 mW sur le panneau de commande laser.
- Réglez le temps de séjour des pixels à 2-4 μs et utilisez plusieurs images avec une moyenne de 10-20 images sur le logiciel de microscopie.
REMARQUE: Évitez l’utilisation combinatoire d’une puissance laser élevée (pompe P> 40 mW, PStokes> 80 mW) et d’une petite taille de pixel (<0,2 μm), ce qui provoque probablement un « effet de blanchiment » des colorants Raman en raison de l’excitation multiphotonique. - Réglez les constantes de temps de l’amplificateur de verrouillage sur la moitié du temps de séjour des pixels.
- Démélange spectral linéaire.
NOTE: epr-SRS suit une stricte dépendance linéaire signal-concentration sur toute la plage de concentration; ainsi, le démélange spectral linéaire est efficace pour éliminer toutes les diaphonies potentielles entre les canaux. Pour la mesure epr-SRS à canal N avec des sondes N MARS, les signaux mesurés (S) peuvent être exprimés en S = MC, où C est les concentrations de la sonde MARS, et M est une matrice N x N déterminée par des sections raman des sondes MARS.- Mesurez la matrice M sur des échantillons immuno-eprSRS monochromes marqués avec différentes sondes MARS.
- Utilisez l’équation C = M−1· S pour déterminer la matrice de concentration de la sonde MARS avec mesure du signal d’échantillon multiplex S.
Résultats
La figure 3 montre des exemples d’images d’epr-SRS dans différents échantillons, y compris des cellules fixes (figure 3A), des tissus de souris fixés au paraformaldéhyde (PFA) (figure 3B) et des échantillons humains incorporés à de la paraffine fixée au formol (FFPE) (figure 3C). La résolution spatiale de la microscopie SRS est limitée par diffraction, la résolution latérale typique est d’environ 300 nm et la résolution axiale est de 1 à 2 μm en utilisant la lumière proche infrarouge pour l’excitation. En conséquence, de fines structures subcellulaires telles que les microtubules dans les cellules HeLa ont été fidèlement révélées avec l’imagerie immuno-eprSRS de la α-tubuline (Figure 3A). De plus, l’epr-SRS est généralement compatible avec les tissus FFPE (Figure 3C), qui est une forme courante d’échantillons de biopsie pour le diagnostic clinique et la recherche en pathologie. Semblable à la microscopie à fluorescence à deux photons, en tant que processus non linéaire, epr-SRS a une capacité de sectionnement optique pour visualiser des motifs tridimensionnels avec une résolution subcellulaire (Figure 3D-E).
Nous avons d’abord présenté l’utilité d’imagerie des protéines multiplexes de l’epr-SRS sur des échantillons de tissus congelés fixes d’îlots de souris de Langerhans dans le pancréas. Plusieurs cibles intéressées sont sélectionnées, y compris l’expression hormonale (p. ex., insuline, agoniste du glucose (glucagon), polypeptide pancréatique (PP) et somatostatine) pour la classification de type cellulaire (cellules β et non-cellules β (cellules α, δ)) et les facteurs de transcription qui sont connus pour être liés à l’hétérogénéité β cellules23. Il est à noter que puisque la détection de fluorescence est orthogonale à la détection SRS, epr-SRS est entièrement compatible avec la fluorescence confocale et la fluorescence à deux photons. En tant que preuve de concept, l’imagerie en tandem SRS-fluorescence 7 couleurs sur un seul îlot a été facilement réalisée (Figure 4) avec un bon contraste et des motifs corrects. Les cibles à faible expression telles que le facteur de transcription Pdx1 ont été imagées avec un contraste suffisant.
Nous avons également démontré une imagerie en tandem SRS-fluorescence à huit couleurs dans des tissus de cervelet de souris fixés par PFA (Figure 5). Grâce à des biomarqueurs établis, différents types de cellules, tels que les neurones granulaires cérébelleux (NeuN), les neurones de Purkinje (Calbindin), les astrocytes (GFAP), les oligodendrocytes (MBP) et les neurones GABAergiques (récepteur GABA B2 ) peuvent être identifiés.

Figure 1 : Microscopie Epr-SRS pour l’imagerie des protéines hautement multiplexées. (A) Diagramme d’énergie pour raman spontané, SRS non résonant et SRS pré-résonant électronique (epr-SRS). Le taux de transition vibratoire des chromophores sera multiplié par10 dans l’epr-SRS. (B) L’immuno-imagerie à base d’épitope de la α-tubuline a été démontrée dans des cellules COS-7 colorées par ATTO740 avec un contraste vibratoire élevé par epr-SRS. Le signal epr-SRS disparaît complètement lorsque la longueur d’onde laser de la pompe est hors résonance de seulement 2 nm (à droite). Barres d’échelle, 20 μm. (C) Spectres Epr-SRS des sondes MARS conjuguées à l’ester du NHS, telles qu’énumérées dans Matériel supplémentaire. Veuillez cliquer ici pour voir une version agrandie de cette figure.
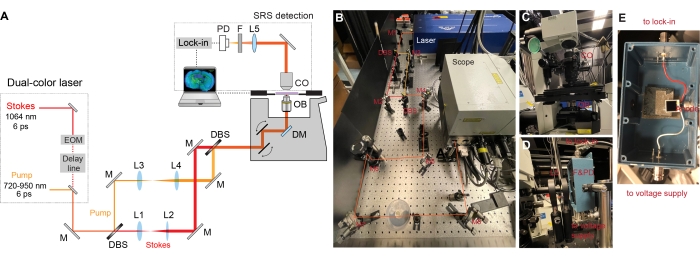
Figure 2: Conception de la configuration du microscope SRS. (A) Diagramme schématique de la configuration SRS. EOM = modulateur électro-optique, M = miroir, L = lentille, DBS = séparateur de faisceau dichroïque, DM = miroir dichroïque, OB = lentille d’objectif, CO = condensateur, F = filtre, = photodiode. (B) Ce panneau montre la partie d’excitation laser. Le faisceau bicolore de la sortie laser est d’abord séparé, chaque faisceau étant collimé et étendu, puis combiné et dirigé dans le corps du microscope. (C) Ce panneau montre la collection transmise à l’aide d’un condenseur. (D) Ce panneau montre la partie détection SRS. La photodiode et le filtre sont montés sur une boîte blindée avec deux connecteurs femelles BNC. Le connecteur BNC inférieur est pour la tension de polarisation inverse, et le connecteur BNC supérieur est pour la sortie du signal de courant vers l’amplificateur de verrouillage terminé par 50 Ω. (E) Ce panneau montre comment la photodiode Si est montée à l’intérieur de la boîte blindée. Veuillez cliquer ici pour voir une version agrandie de cette figure.

Figure 3 : Imagerie par colorant Raman de marqueurs protéiques distincts par immunomarquage. (A) Imagerie immuno-eprSRS de α-tubuline dans les cellules HeLa. (B) Imagerie immuno-eprSRS de NeuN dans le cortex cérébral de souris fixé PFA. (C) Imagerie immuno-eprSRS de Vimentin dans le tissu FFPE du rein humain. (D) Image rendue en volume du GFAP coloré par MARTIN2145 dans un tissu cérébral de souris de 100 μm d’épaisseur. La taille de l’étape en z était de 2 μm. (E) Image rendue en volume de NEUN coloré par MARS2228 dans un tissu cérébral de souris de 40 μm d’épaisseur. La taille du pas en z était de 1 μm. Barres d’échelle, 20 μm in (A), 50 μm in (B-C), 30 μm in (D-E). Veuillez cliquer ici pour voir une version agrandie de cette figure.

Figure 4 : Résultats représentatifs de l’imagerie en tandem 7 couleurs des hormones et des facteurs de transcription sur le tissu d’îlots de souris congelés. Epr-SRS: Insuline (détectée par Cy5, marqueur β cellules, vert), Pdx1 (détectée par MARS2228, facteur de transcription, rouge), Glucagon (détecté par MARS2216, marqueur α cellules, jaune), PP (détecté par MARS2147, marqueur de cellules PP, bleu). Fluorescence: Somatostatine (Alexa488, marqueur δ cellules, orange), Nkx2.2 (Cy3, facteur de transcription, magenta), DAPI (noyau, bleu foncé). Barre d’échelle, 20 μm. Veuillez cliquer ici pour voir une version plus grande de cette figure.
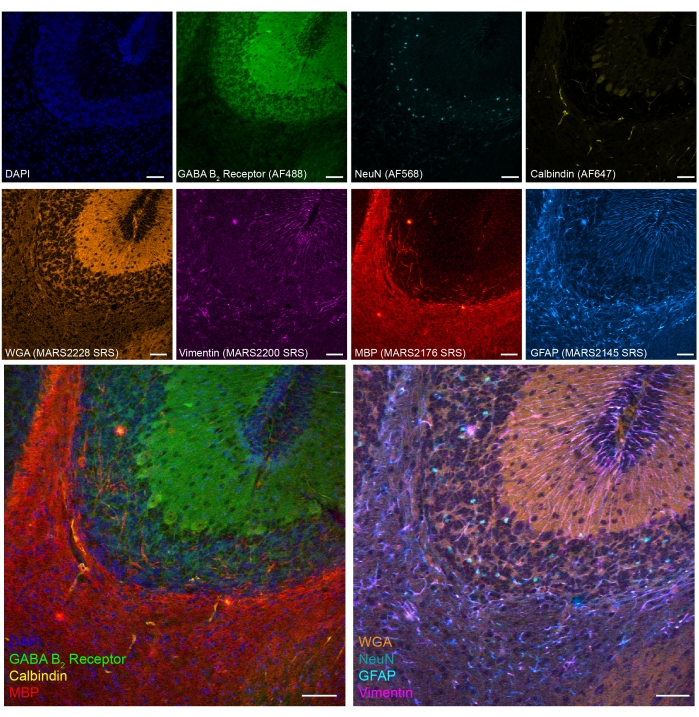
Figure 5 : Résultats représentatifs de l’imagerie en tandem 8 couleurs de marqueurs de type cellulaire sur une section de cerveau de souris fixée par PFA. Fluorescence : ADN (DAPI), GABA (acide γ-aminobutyrique), récepteur B 2 (neurones GABAergiques, Alexa Fluor 488), noyaux neuronaux (NeuN ; neurones, Alexa Fluor 568) et Calbindine (neurones purkinje, Alexa Fluor 647) ; epr-SRS: agglutinine de germe de blé (WGA; MARS2228), Vimentine (MARS2200), protéine basique de myéline (MBP; oligodendrocytes, MARS2176) et GFAP (astrocytes et cellules souches neurales, MARS2145). Barre d’échelle, 50 μm. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Tableau 1 : Anticorps validés pour l’immuno-eprSRS. Reportez-vous à la Table des matériaux pour plus de détails. Veuillez cliquer ici pour télécharger ce tableau.
Matériel supplémentaire: Propriétés de 8 sondes MARS fonctionnalisées par l’ester NHS utilisées. Lesabs λ et les coefficients d’excitation des colorants MARS ont été mesurés en solution de DMSO sur spectromètre UV-Vis en utilisant une cuvette en verre de 1 cm comme récipient. Les sections Raman absolues des colorants MARS ont été déterminées dans le DMSO en comparant le signal epr-SRS des colorants MARS avec le mode d’étirement C−O standard (1030 cm-1) du méthanol. La section Raman absolue pour le mode d’étirement C−O standard (1030 cm-1) du méthanol a été rapportée comme 2,1 x 10-30 cm2 à 785 nm. Une section transversale de 0,9 x 10-30 cm2 a été estimée sous une longueur d’onde de pompe de 860 nm par extrapolation. Veuillez cliquer ici pour télécharger ce fichier.
Discussion
Ici, nous présentons le protocole immuno-eprSRS qui est largement applicable aux types de tissus courants, y compris les tissus de souris fraîchement conservés, les tissus humains FFPE et les tissus de souris congelés. Immuno-eprSRS a été validé pour un panel d’épitopes dans les cellules et les tissus, comme indiqué dans le tableau 1. Cette plate-forme one-shot est particulièrement adaptée aux applications où les stratégies cycliques ne fonctionnent pas bien. Par exemple, la fluorescence cyclique est exigeante pour les tissus épais car plusieurs cycles d’immunomarquage 3D sont peu pratiqueset longs 17. Il est également très probable d’introduire des erreurs d’enregistrement dues à des changements histologiques 3D nonlinéaires 11,17. Immuno-eprSRS surmonte les barrières pratiques de la fluorescence cyclique dans un tel scénario et apporte des opportunités pour révéler des réseaux d’interaction protéique sur un grand volume17.
La multiplexité actuelle est principalement limitée par la disponibilité d’anticorps secondaires. Dans ce protocole, nous nous sommes concentrés sur l’immunomarquage indirect, dans lequel les sondes MARS sont conjuguées à des anticorps secondaires, l’immunomarquage direct et la coloration à la lectine sont réalisables17. Après plus de validation d’anticorps primaires avec des colorants Raman, 20 canaux sont attendus avec les colorants Raman actuellement développés 13,18,24. De plus, l’imagerie de cibles à très faible abondance pourrait être difficile pour l’epr-SRS en raison de sa sensibilité légèrement compromise par rapport au système de fluorescence confocale. À cet égard, nous recommandons d’attribuer des cibles relativement peu abondantes aux colorants MARS plus brillants et des cibles à faible expression aux canaux de fluorescence.
Un aspect critique du protocole est l’accessibilité des instruments et des sondes. Du point de vue de l’instrumentation, un microscope SRS est généralement composé d’une source laser bicolore avec un modulateur optique, un microscope, un détecteur de photodiode et un amplificateur de verrouillage pour la démodulation25. Chaque composant est disponible dans le commerce avec un coût total légèrement plus élevé qu’un microscope à fluorescence à balayage laser à deux photons. Un microscope de recherche SRS/fluorescence multimodal entièrement intégré a été commercialisé26 en utilisant un laser picoseconde similaire à celui d’ici pour l’excitation SRS et les ensembles de lasers à ondes continues (CW) pour la fluorescence. Ce système est facilement applicable à l’imagerie vibratoire multiplex dans la recherche biologique quotidienne. En ce qui concerne les sondes, les sondes MARS n’ont pas encore été commercialisées et nécessitent certaines capacités de synthèse. Alternativement, de nombreux fluorophores rouge lointain commerciaux (voir le tableau de données étendues 1 dans L. Wei et al. Nature 201713) peuvent être utilisés pour epr-SRS. Pourtant, la multiplexité pourrait être compromise. De plus, puisque les sondes MARS sont par nature de petites molécules organiques, l’immuno-eprSRS est similaire à l’immunofluorescence en termes de coloration tissulaire. Par conséquent, l’archive des réactifs d’affinité validés tels que les anticorps en immunofluorescence peut être facilement transférée dans des applications immuno-eprSRS.
Déclarations de divulgation
Les auteurs n’ont rien à divulguer.
Remerciements
Nous remercions Ruth A. Singer et Richard K.P. Benninger d’avoir fourni des tissus pancréatiques de souris. W.M. reconnaît le soutien des NIH R01 (GM128214), R01 (GM132860), R01 (EB029523) et de l’armée américaine (W911NF-19-1-0214).
matériels
| Name | Company | Catalog Number | Comments |
| 16% Paraformaldehyde, EM Grade | Electron Microscopy Sciences | 15710 | |
| α-tubulin | Abcam | ab18251 | Primary antibodies |
| α-tubulin | BioLegend | 625902 | Primary antibodies |
| β-III-tubulin | BioLegend | 657402 | Primary antibodies |
| β-III-tubulin | Abcam | ab41489 | Primary antibodies |
| β-tubulin | Abcam | ab131205 | Primary antibodies |
| Agarose, low gellling temperature | Sigma Aldrich | A9414 | For brain embedding |
| Anti-a-tubulin antibody produced in rabbit (α-tubulin) | Abcam | ab52866 | Primary antibodies |
| Anti-Calbindin antibody produced in mouse (Calbindin) | Abcam | ab82812 | Primary antibodies |
| Anti-GABA B receptor R2 antibody produced in guinea pig (GABA B receptor R2) | Millipore Sigma | AB2255 | Primary antibodies |
| Anti-GFAP antibody produced in goat (GFAP) | Thermo Scientific | PA5-18598 | Primary antibodies |
| Anti-Glucagon antibody produced in mouse (Glucagon) | Santa Cruz Biotechnology | sc-514592 | Primary antibodies |
| Anti-insulin antibody produced in guinea pig (insulin) | DAKO | IR00261-2 | Primary antibodies |
| Anti-MBP antibody produced in rat (MBP) | Abcam | ab7349 | Primary antibodies |
| Anti-NeuN antibody produced in rabbit (NeuN) | Thermo Scientific | PA5-78639 | Primary antibodies |
| Anti-Pancreatic polypeptide (PP) antibody produced in goat- Pancreatic polypeptide (PP) | Sigma Aldrich | SAB2500747 | Primary antibodies |
| Anti-Pdx1 antibody produced in rabbit (Pdx1) | Milipore | 06-1379 | Primary antibodies |
| Anti-Somatostatin antibody produced in rat (Somatostatin) | Abcam | ab30788 | Primary antibodies |
| Anti-Vimentin antibody produced in chicken (Vimentin) | Abcam | ab24525 | Primary antibodies |
| Band-pass filter | KR Electronics | KR2724 | 8 MHz |
| BNC 50 Ohm Terminator | Mini Circuits | STRM-50 | |
| BNC cable | Thorlabs | 2249-C | Coaxial Cable, BNC Male / Male |
| Broadband dielectric mirror | Thorlabs | BB1-E03 | 750 - 1100 nm |
| C57BL/6J mice | Jackson Laboratory | 000664 | |
| Centrifuge | |||
| Condenser | Olympus | oil immersion, 1.4 N.A. | |
| Cytokeratin 18 | Abcam | ab7797 | Primary antibodies |
| Cytokeratin 18 | Abcam | ab24561 | Primary antibodies |
| DC power supply | TopWard | 6302D | Bias voltage is 64 V |
| Dichroic mount | Thorlabs | KM100CL | Kinematic Mount for up to 1.3" (33 mm) Tall Rectangular Optics, Left Handed |
| Donkey anti-Chicken IgY (H+L) | Jackson ImmunoResearch | 703-005-155 | Secondary antibodies for MARS conjugation |
| Donkey anti-Goat IgG (H+L) | Jackson ImmunoResearch | 705-005-147 | Secondary antibodies for MARS conjugation |
| Donkey anti-Guinea Pig IgG (H+L) | Jackson ImmunoResearch | 706-005-148 | Secondary antibodies for MARS conjugation |
| Donkey anti-Mouse IgG (H+L) | Jackson ImmunoResearch | 715-005-151 | Secondary antibodies for MARS conjugation |
| Donkey anti-Rabbit IgG (H+L) | Jackson ImmunoResearch | 711-005-152 | Secondary antibodies for MARS conjugation |
| Donkey anti-Rat IgG (H+L) | Jackson ImmunoResearch | 712-005-153 | Secondary antibodies for MARS conjugation |
| Donkey anti-Sheep IgG (H+L) | Jackson ImmunoResearch | 713-005-147 | Secondary antibodies for MARS conjugation |
| DPBS | Fisher Scientific | 14-190-250 | |
| EpCAM | Abcam | ab71916 | Primary antibodies |
| Ethanol | Sigma Aldrich | 443611 | |
| Fast-speed look-in amplifier | Zurich Instruments | HF2LI | DC - 50 MHz |
| FFPE Kidney Sample | USBiomax | HuFPT072 | |
| Fibrillarin | Abcam | ab5821 | Primary antibodies |
| Giantin | Abcam | ab24586 | Primary antibodies |
| Glucagon | Santa Cruz Biotechnology | sc-514592 | Primary antibodies |
| H2B | Abcam | ab1790 | Primary antibodies |
| HeLa | ATCC | ATCC CCL-2 | |
| High O.D. bandpass filter | Chroma Technology | ET890/220m | Filter the Stokes beam and transmit the pump beam |
| Hydrophobic pen | Fisher Scientific | NC1384846 | |
| Insulin | ThermoFisher | 701265 | Primary antibodies |
| Integrated SRS laser system | Applied Physics & Electronics, Inc. | picoEMERALD | picoEMERALD provides an output pulse train at 1,064 nm with 6-ps pulse width and 80-MHz repetition rate, which serves as the Stokes beam. The frequency doubled beam at 532 nm is used to synchronously seed a picosecond optical parametric oscillator (OPO) to produce a mode-locked pulse train with five~6 ps pulse width (the idler beam of the OPO is blocked with an interferometric filter). The output wavelength of the OPO is tunable from 720–950 nm, which serves as the pump beam. The intensity of the 1,064-nm Stokes beam is modulated sinusoidally by a built-in EOM at 8 MHz with a modulation depth of more than 90%. The pump beam is spatially overlapped with the Stokes beam by using a dichroic mirror inside picoEMERALD. The temporal overlap between pump and Stokes pulse trains is achieved with a built-in delay stage and optimized by the SRS signal of pure D2O at the microscope. |
| Inverted laser-scanning microscope | Olympus | FV1200MPE | |
| Kinematic mirror mount | Thorlabs | POLARIS-K1-2AH | 2 Low-Profile Hex Adjusters |
| Lectin from Triticum vulgaris (wheat) | Sigma Aldrich | L0636-5 mg | |
| Long-pass dichroic beam splitter | Semrock | Di02-R980-25x36 | 980 nm laser BrightLine single-edge laser-flat dichroic beamsplitter |
| MAP2 | BioLegend | 801810 | Primary antibodies |
| Microscopy imaging software | Olympus | FluoView | |
| NanoQuant Plate | Tecan | For absorbance-based, small volume analyses in a plate reader. | |
| Normal donkey serum | Jackson ImmunoResearch | 017-000-121 | |
| NucBlue Fixed Cell ReadyProbes Reagent (DAPI) | Thermo Scientific | R37606 | |
| Nunc 4-Well Dishes | Fisher Scientific | 12-566-300 | |
| Objective lens | Olympus | XLPlan N | x25, 1.05-NA, MP, working distance = 2 mm |
| Paint brush | |||
| Periscope assembly | Thorlabs | RS99 | includes the top and bottom units, Ø1" post, and clamping fork. |
| pH meter | |||
| Plate reader | Tecan | Infinite 200 PRO | An easy-to-use multimode plate reader. Absorbance measurement capabilities over a spectral range of 230–1000 nm. |
| ProLong Gold antifade reagent | Thermo Scientific | P36930 | |
| PSD95 | Invitrogen | 51-6900 | Primary antibodies |
| Sephadex G-25 Medium | GE Life Sciences | 17-0033-01 | gel filtration resin for desalting and buffer exchange |
| Shielded box with BNC connectors | Pomona Electronics | 2902 | Aluminum Box With Cover, BNC Female/Female |
| Si photodiode | Thorlabs | FDS1010 | 350–1100 nm, 10 mm x 10 mm Active Area |
| Synapsin 2 | ThermoFisher | OSS00073G | Primary antibodies |
| Tissue Path Superfrost Plus Gold Slides | Fisher Scientific | 22-035813 | Adhesive slide to attract and chemically bond fresh or formalin-fixed tissue sections firmly to the slide surface (tiisue bindling glass slides) |
| Triton X-100 | Fisher Scientific | BP151-500 | |
| Vibratome | Leica | VT1000 | |
| Vimentin | Abcam | ab8069 | Primary antibodies |
| Xylenes | Sigma Aldrich | 214736 |
Références
- Goltsev, Y., et al. Deep profiling of mouse splenic architecture with CODEX multiplexed imaging. Cell. 174 (4), 968-981 (2018).
- Taube, J. M., et al. The Society for Immunotherapy of Cancer statement on best practices for multiplex immunohistochemistry (IHC) and immunofluorescence (IF) staining and validation. Journal for Immunotherapy of Cancer. 8 (1), 000155 (2020).
- Lewis, S. M., et al. Spatial omics and multiplexed imaging to explore cancer biology. Nature Methods. 18 (9), 997-1012 (2021).
- Bodenmiller, B. Multiplexed epitope-based tissue imaging for discovery and healthcare applications. Cell Systems. 2 (4), 225-238 (2016).
- Hickey, J. W., et al. Spatial mapping of protein composition and tissue organization: a primer for multiplexed antibody-based imaging. Nature Methods. , (2021).
- Lin, J. -. R., et al. Highly multiplexed immunofluorescence imaging of human tissues and tumors using t-CyCIF and conventional optical microscopes. eLife. 7, 31657 (2018).
- Black, S., et al. CODEX multiplexed tissue imaging with DNA-conjugated antibodies. Nature Protocols. 16 (8), 3802-3835 (2021).
- Giesen, C., et al. Highly multiplexed imaging of tumor tissues with subcellular resolution by mass cytometry. Nature Methods. 11 (4), 417-422 (2014).
- Keren, L., et al. MIBI-TOF: A multiplexed imaging platform relates cellular phenotypes and tissue structure. Science Advances. 5 (10), 5851 (2019).
- Gerdes, M. J., et al. Highly multiplexed single-cell analysis of formalin-fixed, paraffin-embedded cancer tissue. Proceedings of the National Academy of Sciences of the United States of America. 110 (29), 11982 (2013).
- Angelo, M., et al. Multiplexed ion beam imaging of human breast tumors. Nature Medicine. 20 (4), 436-442 (2014).
- Radtke, A. J., et al. IBEX: A versatile multiplex optical imaging approach for deep phenotyping and spatial analysis of cells in complex tissues. Proceedings of the National Academy of Sciences of the United States of America. 117 (52), 33455 (2020).
- Wei, L., et al. Super-multiplex vibrational imaging. Nature. 544, 465 (2017).
- Wei, L., Min, W. Electronic preresonance stimulated Raman scattering microscopy. The Journal of Physical Chemistry Letters. 9 (15), 4294-4301 (2018).
- Shi, L., et al. Electronic resonant stimulated Raman scattering micro-spectroscopy. The Journal of Physical Chemistry B. 122 (39), 9218-9224 (2018).
- Fujioka, H., et al. Multicolor activatable Raman probes for simultaneous detection of plural enzyme activities. Journal of the American Chemical Society. 142 (49), 20701-20707 (2020).
- Shi, L., et al. Highly-multiplexed volumetric mapping with Raman dye imaging and tissue clearing. Nature Biotechnology. , (2021).
- Miao, Y., Qian, N., Shi, L., Hu, F., Min, W. 9-Cyanopyronin probe palette for super-multiplexed vibrational imaging. Nature Communications. 12 (1), 4518 (2021).
- Miao, Y., Shi, L., Hu, F., Min, W. Probe design for super-multiplexed vibrational imaging. Physical Biology. 16 (4), 041003 (2019).
- Qian, N., Min, W. Super-multiplexed vibrational probes: Being colorful makes a difference. Current Opinion in Chemical Biology. 67, 102115 (2022).
- Klimas, A., et al. Nanoscale imaging of biomolecules using molecule anchorable gel-enabled nanoscale in-situ fluorescence microscopy. Nature Portfolio. , (2021).
- Shi, L., et al. Super-resolution vibrational imaging using expansion stimulated Raman scattering microscopy. bioRxiv. , (2021).
- Benninger, R. K. P., Hodson, D. J. New understanding of β-cell heterogeneity and in situ islet function. Diabetes. 67 (4), 537 (2018).
- Hu, F., et al. Supermultiplexed optical imaging and barcoding with engineered polyynes. Nature Methods. 15 (3), 194-200 (2018).
- Hu, F., Shi, L., Min, W. Biological imaging of chemical bonds by stimulated Raman scattering microscopy. Nature Methods. 16 (9), 830-842 (2019).
- . Coherent Raman Scattering Microscope Available from: https://www.leica-microsystems.com/products/confocal-microscopes/p/leica-tcs-sp8-cars/ (2022)
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon