Anwendung der Gruppentheorie auf die IR-Spektroskopie
Überblick
Quelle: Tamara M. Powers, Department of Chemistry, Texas A & M Universität
Metal Carbonyl-komplexe werden als Metall Vorläufer für die Synthese von metallorganischen komplexe sowie Katalysatoren verwendet. Infrarotspektroskopie (IR) ist einer der eingesetzten und informative Charakterisierungsmethoden Co, Verbindungen enthalten. Gruppentheorie oder die Verwendung von Mathematik, die Symmetrie eines Moleküls zu beschreiben bietet eine Methode, um die Anzahl der IR aktiven C-O-Schwingungs-Modi innerhalb eines Moleküls Vorhersagen. Experimentell beobachtet, dass die Anzahl der C-O in der IR erstreckt, ist eine direkte Methode, die Geometrie und Struktur der Metal Carbonyl Komplex zu etablieren.
In diesem Video werden wir die Molybdän Carbonyl Komplex Mo(CO)4[P(OPh)3]2, synthetisieren, das in den Cis- und Trans -Formen (Abbildung 1) vorhanden sein können. Wir werden Gruppentheorie und IR-Spektroskopie verwenden, um festzustellen, welche Isomer isoliert ist.
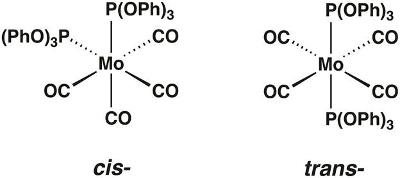
Abbildung 1. Der Cis- und Trans-Isomere von Mo(CO)4[P(OPh)3]2.
Grundsätze
Auswahlregeln:
Auswahlregeln bestimmen die Anzahl der elektronischen Übergänge von einem Quantum Zustand zu einem anderen, für ein gegebenes Molekül möglich sind. IR-Spektroskopie-Sonden Schwingungs Übergänge vom Grundzustand des Moleküls, V = 0, um den ersten angeregten Zustand, V = 1. Die Anzahl der Freiheitsgrade Schwingungs (Normalschwingungen Vibration) für lineare und nicht lineare Moleküle kann mit Gleichung 1 und Gleichung 2, bzw. berechnet werden.
3N - 5 (1)
3N - 6 (2)
wo N = Anzahl der Atome im Molekül
Normalen Modus der Schwingung IR aktiv zu sein muss das Molekül Dipol ändern. Daher sind Normalschwingungen Vibration, wo eine Änderung der Dipol tritt nicht auf, IR inaktiv. Die Anzahl der aktiven IR-Modi kann durch Gruppentheorie bestimmt werden.
Gruppentheorie:
Chemiker benutzen Gruppe Theorie um zu verstehen, die Beziehung zwischen die Symmetrie und die physikalischen Eigenschaften eines Moleküls. Während der Bereich der Gruppentheorie zu breit um rigoros in diesem Video zu decken ist, stellen wir die notwendigen Werkzeuge benötigt, um einfache Koordination komplexe Gruppentheorie zuweisen und zeigen, wie es verwendet werden, um die Anzahl der aktiven Schwingungs Modi IR Vorhersagen. Um zu demonstrieren, werden wir durch die Anwendung der Gruppentheorie, das Molekül Cis -Mo(CO)4[P(OPh)3]2laufen.
Zuerst müssen wir die Punktgruppe des Moleküls zu ermitteln. Punktgruppen werden verwendet, um die Symmetrie-Elemente, die in einem bestimmten Molekül zu beschreiben. Um die Punktgruppe des Cis -Mo(CO)4[P(OPh)3]2zu ermitteln, nutzen wir ein Flussdiagramm genannt einen Symmetrie-Baum, der eine Reihe von Fragen über die Symmetrie Elemente im Molekül (Abbildung 2) fragt. Tabelle 1 enthält eine Zusammenfassung aller Symmetrie Elemente in der Symmetrie-Baum enthalten. Mit der Symmetrie-Baum, und vorausgesetzt, dass die Liganden P(OPh)3 Punkt Liganden (unter Missachtung der Symmetrie dieser Liganden), finden wir, dass GUS -Mo(CO)4[P(OPh)3]2 in die Punktgruppe C ist 2v.

Abbildung 2. Symmetrie-Baum für Punkt Gruppenentscheidung verwendet.
Tabelle 1. Symmetrie-Elemente verwendet in Punkt Gruppenentscheidung.
| Symmetrie-element | Symbol verwendet | Beispiel * |
| Identität | E |  |
| Drehachse (Drehung von 360 ° / n) |
C n |  |
| Horizontale Spiegelebene (Reflexion über die Xy-Ebene) |
Σ h | 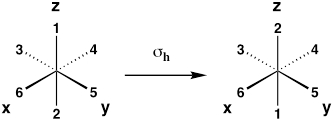 |
| Vertikale Spiegelebene (Reflexion über Xz oder Yz-Ebene) |
Σ v | 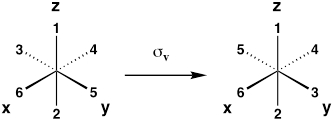 |
| Diagonale Spiegelebene (Reflexion zwischen Xz und Yz-Ebenen) |
Σ d | 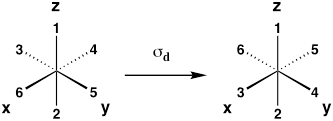 |
| Inversion Center | Ich | 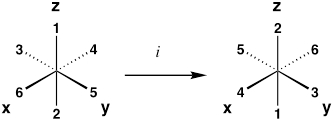 |
| Unsachgemäße Drehachse (Drehung von 360 ° / n gefolgt von Reflexion senkrecht zur Drehachse) |
S n |  |
| * Beispiele sind für einem oktaedrischen Komplex, wo Liganden 1–6 gleichwertig sind. Auf die Operation, sollte das resultierende Molekül von seiner ursprünglichen Konfiguration zu unterscheiden. | ||
Wir müssen für den nächsten Schritt Zeichentabellen, einzuführen, die alle die Symmetrie vorhanden innerhalb einer bestimmten Gruppe zu beschreiben. Die Zeichentabelle für die Punkt-Gruppe- C-2v ist unten dargestellt.
| C 2v | E | C 2 | Σ v (Xz) | Σ v ' (Yz) | ||
| A 1 | 1 | 1 | 1 | 1 | z | x2, y2, Z2 |
| A 2 | 1 | 1 | −1 | −1 | R-z | XY |
| B 1 | 1 | −1 | 1 | −1 | X, Ry | XZ |
| B 2 | 1 | −1 | −1 | 1 | y, Rx | YZ |
Die Punktgruppe wird in der oberen linken Ecke der Zeichentabelle angezeigt. Auf der rechten Seite der Punktgruppe sind alle Symmetrie Vorgänge in dieser Punktgruppe aufgeführt.Die nachfolgenden Zeilen auflisten aller Symmetrie Darstellungen (irreduziblen Darstellungen, vertreten durch Mulliken-Symbole, i.e.,A1) in dieser Punktgruppe, zusammen mit der Symmetrie von Funktionen, die erzählen von der Symmetrie der enthaltenen atomaren orbitale sowie lineare Bewegung entlang der x-, y- und z-Achse.
Mit der Zeichentabelle für die Punkt-Gruppe- C-2v, erzeugen wir eine reduzierbar (Γrot) Darstellung der C-O stretching Modi in das Molekül Cis -Mo(CO)4[P(OPh)3]2 (Abbildung 3 ). Die reduzierbar Darstellung oder die Linearkombination der irreduziblen Darstellungen können durch Anwendung jeder der Symmetrie Vorgänge innerhalb der Zeichentabelle auf die Schwingungen im Molekül und aufzeichnen, die Anzahl der C-O-Schwingungen erzeugt werden, die bleiben Sie unverändert (in der gleichen Position im Raum). Z. B. auf die C-O-Schwingungen in Cis -Mo(CO)4[P(OPh)3]2das Identity-Symmetrie-Element zuweisen, bleiben alle vier der Schwingungs Pfeile in der gleichen Position. Daher ist der erste Wert in unserer reduzierbar Darstellung 4. Wenn wir diese Übung weiter, generieren wir die reduzierbar Darstellung unten gezeigt.
| C 2v | E | C 2 | Σ v (Xz) | Σ v ' (Yz) |
| Γ rot | 4 | 0 | 2 | 2 |
Als Nächstes verwenden wir die C-2v -Zeichentabelle Linearkombination der irreduziblen Darstellungen zu finden, die Γrot für die C-O-Schwingungen im Cis -Mo(CO)-4[P(OPh)3]2erzeugt. Reduktion der reduzierbaren Darstellung kann mit der Reduzierung der Formel in Gleichung 3erreicht werden.
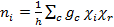 (3)
(3)
Wo:
nich mehrmals die irreduzible Darstellung ich in der reduzierbaren Darstellung tritt =
h = Ordnung der Gruppe (Gesamtzahl der Symmetrie Operationen)
c = die Klasse der Betrieb
gc = Anzahl der Vorgänge in der Klasse
Χ Ich = Zeichen der irreduziblen Darstellung für den Betrieb der Klasse
Χ R = Zeichen der reduzierbaren Darstellung für den Betrieb der Klasse
Mit Gleichung 3 für jede der irreduziblen Darstellungen in der Zeichentabelle C2v, finden wir, dass Γrot = 2A1 + B1 + B2. Alle drei beteiligten irreduziblen Darstellungen, A1, B1und B2, sind IR aktiv, weil sie zu, wie die x-, y- oder z-Achse verwandeln (siehe die Symmetrie von Funktionen in der Zeichentabelle). Daher erwarten wir, dass GUS -Mo(CO)4[P(OPh)3]2 4 C-O stretching Modi in seinem IR-Spektrum aufweisen wird.
Zusammenfassend lässt sich sagen, sind folgende Schritte notwendig, um die Anzahl der IR aktiven Schwingungs-Modi in einem Molekül zu ermitteln:
1. bestimmen der Punktgruppe des Moleküls.
(2) erzeugen Sie eine reduzierbar Darstellung der C-O stretching Vibrationen innerhalb des Moleküls.
3. reduzieren Sie die reduzierbar Darstellung mit Gleichung 3.
4. ermitteln Sie die Anzahl der translationalen irreduziblen Darstellungen in die verkleinerte Darstellung von Schritt 3 vorhanden.
Wenn wir diese 4 mit Trans -Mo(CO)4[P(OPh)3]2 Schritte, finden wir, dass das Molekül nur 1 aktive C-O-Schwingungen-Modus besitzt.

Abbildung 3. CO Schwingungs erstreckt sich in GUS-Mo(CO)4[P(OPh)3]2.
Verfahren
1. Setup der Schlenk-Linie (für eine genauere Verfahren, lesen Sie bitte die "Schlenk Linien übertragen von Lösungsmittel" Video der Serie Essentials of Organic Chemistry ). Schlenk Linie Sicherheit sollte überprüft werden, vor der Durchführung dieses Experiments. Gläser sollten für Sterne Risse vor Gebrauch überprüft werden. Darauf sollte geachtet werden, um sicherzustellen, dass O2 ist nicht in der Schlenk Linie Falle kondensiert, wenn Flüssigkeit N2verwenden. Bei N2 Flüssigkeitstemperatur O2 kondensiert und explosiv in Anwesenheit von organischen Lösungsmitteln. Wenn der Verdacht besteht, dass O2 verdichtet worden oder eine blaue Flüssigkeit in die Kühlfalle eingehalten wird, lassen Sie die Falle unter dynamischen Vakuum kalt. Entfernen Sie die Flüssigkeit N2 Falle nicht oder schalten Sie die Vakuumpumpe. Im Laufe der Zeit wird die Flüssigkeit O2 in die Pumpe erhaben; Es ist nur sicher, die flüssige N2 Falle zu entfernen, sobald alle O2 hat sublimiert.
- Schließen Sie das Überdruckventil.
- Aktivieren Sie das N2 Gas und die Vakuumpumpe.
- Als die Schlenk Linie Vakuum erreicht seine Mindestdruck, bereiten die Kühlfalle mit Flüssigkeit N2 oder Trockeneis/Aceton.
- Montieren Sie die Kühlfalle.
(2) Synthese von Mo(CO)4[P(OPh)3]2 (Abbildung 4)1
Hinweis: Verwenden Sie standard Schlenk-Linie-Techniken für die Synthese von Mo(CO)4[P(OPh)3]2 (siehe Video "Synthese einer Ti(III) Metallocen-Katalysatoren mit Schlenk Linie Technik"). Metal Carbonyl-komplexe sind eine Quelle für kostenlose CO, das ist hochgiftig. Kohlenmonoxid-Vergiftung tritt auf, wenn CO an Hämoglobin bindet, wodurch deutliche Reduzierung der Sauerstoffversorgung des Körpers. Daher ist es äußerst wichtig, entsprechende Schutzmaßnahmen beim Umgang mit und arbeiten mit Metall Carbonyl-komplexe. Reaktionen, die kostenlose CO generieren müssen in einem gut gelüfteten Abzug zur Vermeidung der Exposition mit dem giftigen Gas durchgeführt werden.
- Fügen Sie 1,6 g (4,92 Mmol) Mo(CO)4(Nbd) (Nbd = 2,5-Norbornadiene) und 1,6 mL (9.84 Mmol) Triphenyl gefährdeten (P(OPh)3) in einem 100 mL-Schlenk-Kolben und die Kanüle Übertragung des Lösungsmittels Schlenk-Kolben vorbereiten.
Hinweis: Mo(CO)4(Nbd) ((Bicyclo[2.2.1]hepta-2,5-diene)tetracarbonylmolybdenum(0)) von Sigma-Aldrich erworben werden können oder mit Literatur Methoden synthetisiert. 2 - Schlenk-Kolben per Kanüle 20 mL entgast Dichlormethan hinzufügen.
- Rühren Sie das Reaktionsgemisch für 4 h bei Raumtemperatur unter N2.
- Entfernen Sie die flüchtigen Bestandteile unter Vakuum und die daraus resultierenden waschen mit kaltem Hexanes Niederschlag (zwei wäscht jede mit 10 mL, −78 ° C).
- Trocknen Sie das feste Produkt unter Vakuum für 15 min.
- IR-Spektrum des Produkts in einer Lösung von Hexanes zu messen.
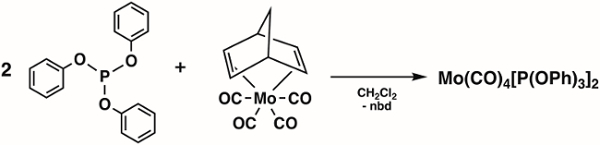
Abbildung 4. Synthese von Mo(CO)4[P(OPh)3]2.
Ergebnisse

Abbildung 5. IR Mo(CO)4[P(OPh)3]2.
Lösung IR in gesättigten Kohlenwasserstoff (cm-1): 2046 (s), 1958 (s), 1942 (Vs).
Die vierte Resonanz kann nur hoch auflösende Bedingungen gesehen werden. Daher ist es möglich, da in diesem Fall, dass nur 3 der 4 Resonanzen eingehalten werden.
Basierend auf den erhaltenen IR, können wir daraus schließen, dass Cis-Isomer des Mo(CO)4[P(OPh)3]2 wurde isoliert.
Anwendung und Zusammenfassung
In diesem Video haben wir gelernt, wie Gruppentheorie verwenden, um die Anzahl der IR aktiven Schwingungs-Modi in einem Molekül Vorhersagen. Wir das Molekül Mo(CO)4[P(OPh)3]2 synthetisiert und IR verwendet, um festzustellen, welche Isomer isoliert wurde. Wir beobachteten, dass das Produkt hatte drei C-O-Schwingungen in ihrer IR-Spektrum, die im Einklang mit dem Cis-Isomer.
Gruppentheorie ist ein leistungsfähiges Werkzeug, das von Chemikern nicht nur IR aktiv Schwingungs-Modi, Vorhersagen verwendet aber auch Schwingungs, Rotations- und anderen Niederfrequenz-Modi in der Raman-Spektroskopie zu beobachten. Darüber hinaus ist Gruppentheorie theoretisch molekularen orbital (MO) implementiert, das am weitesten verbreitete Modell Verklebung in Übergang Metall komplexe zu beschreiben ist. MO-Diagramme von organischen und anorganischen Chemie, verwendet können Vorhersagen und beobachteten Reaktivität eines Moleküls zu erklären.
1St, 2Ndund 3rd Reihe Metal Carbonyl-komplexe sind in anorganische Synthese als Metall Vorläufer für komplexere metallorganischen Verbindungen verbreitet. Die häufigsten Arten von Reaktionen mit Metal Carbonyl-komplexe Beispiele für CO Liganden Substitution, Redox an das Metallzentrum und nukleophilen Angriff an der CO-Einheit. Metal Carbonyl-komplexe selbst sind weit verbreitet in der Katalyse. Zum Beispiel ist Hydroformylierung, die industrielle Herstellung von Aldehyden aus Alkenen, durch das Metall Carbonyl Komplex HCo(CO)3 (Abbildung 6) katalysiert.
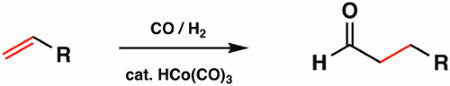
Abbildung 6. Hydroformylierung von Metal Carbonyl Komplex HCo(CO)3.
Referenzen
- Fukumoto, K., Nakazawa, H. Geometrical isomerization of fac/mer-Mo(CO)3(phosphite)3 and cis/trans-Mo(CO)4(phosphite)2 catalyzed by Me3SiOSO2CF3. J Organomet Chem. 693(11), 1968-1974 (2008).
- Darensbourg, M. Y., Magdalena, P., Houliston, S. A., Kidwell, K. P., Spencer, D., Chojnacki, S. S., Reibenspies, J. H. Stereochemical nonrigidity in heterobimetallic complexes containing the bent metallocene-thiolate fragment. Inorg Chem. 31(8), 1487-1493 (1992).
- Darensbourg, M. Y., Darensbourg, D. J. Infrared Determination of Stereochemistry in Metal Complexes. J Chem Ed. 47(1), 33-35 (1970).
pringen zu...
Videos aus dieser Sammlung:

Now Playing
Anwendung der Gruppentheorie auf die IR-Spektroskopie
Inorganic Chemistry
45.3K Ansichten

Synthese eines Ti(III)-Metallocen-Katalysators mittels Schlenk-Technik
Inorganic Chemistry
31.6K Ansichten

Handschuhbox und Verunreinigungssensoren
Inorganic Chemistry
18.6K Ansichten

Reinigung von Ferrocen durch Sublimation
Inorganic Chemistry
54.7K Ansichten

Die Evans-Methode
Inorganic Chemistry
68.6K Ansichten

Einkristall- und Pulverröntgendiffraktometrie
Inorganic Chemistry
104.6K Ansichten

Elektronenparamagnetische Rezonanzspektroskopie (EPR-Spektroskopie)
Inorganic Chemistry
25.5K Ansichten

Mößbauerspektroskopie
Inorganic Chemistry
22.0K Ansichten

Lewis-Säure-Base-Wechselwirkungen in Ph3P-BH3
Inorganic Chemistry
38.9K Ansichten

Struktur von Ferrocen
Inorganic Chemistry
79.6K Ansichten

Molekülorbital (MO)-Theorie
Inorganic Chemistry
35.4K Ansichten

Vierfach-metallgeklebte Schaufelräder
Inorganic Chemistry
15.3K Ansichten

Farbstoffsensibilisierte Solarzellen
Inorganic Chemistry
15.8K Ansichten

Synthese eines Sauerstoff-transportierenden Cobalt(II) - Komplex
Inorganic Chemistry
51.7K Ansichten

Photochemische Initiierung von radikalischen Polymerisationsreaktionen
Inorganic Chemistry
16.8K Ansichten
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten