Method Article
تطبيق الموجات فوق الصوتية بالمنظار في خياطة الصفراو الأولية أثناء الجراحة المشتركة ذات العدستين
In This Article
Summary
هنا ، نقوم بتطوير وتقديم تقنية خالية من الدعامات الصفراوية وأنبوب T باستخدام تصور العدسة المزدوجة (عبر منظار البطن ومنظار الصفراو) جنبا إلى جنب مع التصوير بالموجات فوق الصوتية بالمنظار (LUS) لإجراء خياطة صفراوية أولية.
Abstract
تعتبر حصوات المرارة جنبا إلى جنب مع حصوات القناة الصفراوية الشائعة مرضا سريريا شائعا. تشمل العلاجات طفيفة التوغل استئصال المرارة بالمنظار + استكشاف القناة الصفراوية المشتركة بالمنظار (LC + LCBDE) وتصوير البنكرياس والقنوات الصفراوية بالمنظار + استئصال المرارة بالمنظار (ERCP + LC). يمكن أن يحل LCBDE مشكلتين في إجراء واحد ، بينما يتطلب ERCP + LC نهجا من خطوتين. كما أظهرت المزيد من الدراسات ، فإن استكشاف القناة الصفراوية المشتركة مع استخراج الحصوات متبوعا بالإغلاق الأولي قد يؤدي إلى تعافي أسرع وتحسين نوعية الحياة للمرضى.
من المعروف أن الاختلافات التشريحية في القنوات الصفراوية والأوعية الدموية شائعة. الموجات فوق الصوتية بالمنظار (LUS) مفيدة في توضيح الهياكل التشريحية لمنطقة البوابة الكبدية ، وتحديد اتجاه القناة الصفراوية ، وتحديد العلاقات المكانية بين القنوات الصفراوية ، والشرايين الكبدية ، والأوردة البابية ، وتقليل مخاطر الإصابة الصفراوية.
يتم توضيح الإجراء هنا من خلال وصف مفصل للحالة. بعد إعطاء التخدير العام ، تم إنشاء نهج بالمنظار بشكل روتيني لفحص تجويف البطن وتقييم الآفات. تم استخدام الموجات فوق الصوتية بالمنظار لتقييم مثلث المرارة داخل منطقة البوابة الكبدية ، بما في ذلك تشريح القنوات الصفراوية والأوعية. تم تشريح مثلث المرارة ، متبوعا بشق إبرة 5-0 في جدار القناة الصفراوية. تم إجراء تنظير الصفراو لاستخراج الحصوات ، مع تأكيد وظيفة الحليمة الطبيعية للاثني عشر. تم تحقيق خياطة مستمرة لجدار القناة الصفراوية باستخدام مادة خياطة الشعيرات الأحادية 5-0 بولي ديوكسانون. في الوقت نفسه ، تحققت الموجات فوق الصوتية بالمنظار من إزالة الحصوات الكاملة وتقييم سلامة الخياطة.
Introduction
تحص المرارة هو مرض سريري شائع ، حيث يعاني ما يقرب من 10-20٪ من المرضى الذين يصابون بتحص صفراوي ثانوي1،2. تعتبر حصوات المرارة جنبا إلى جنب مع حصوات القناة الصفراوية الشائعة حالة سريرية متكررة. قد يؤدي انسداد القناة الصفراوية إلى آلام في البطن واليرقان والتهابات القناة الصفراوية وحتى الصدمة الشديدة. العلاج الأمثل يتضمن تخفيف الانسداد وإزالة الآفات.
تشمل الأساليب العلاجية الحالية لحصوات المرارة مع حصوات القناة الصفراوية الشائعة استئصال المرارة المفتوح + استكشاف القناة الصفراوية المشتركة المفتوحة (OC + OCBDE) ، وتصوير البنكرياس والقنوات الصفراوية بالمنظار + استئصال المرارة بالمنظار (ERCP + LC) ، واستئصال المرارة بالمنظار + استكشاف القناة الصفراوية المشتركة بالمنظار (LC + LCBDE) 3،4.
ترتبط الجراحة المفتوحة بصدمة كبيرة وتعافي طويل الأمد ، وعادة ما تكون مخصصة للحالات التي لا تكون فيها التقنيات طفيفة التوغل ممكنة. تعتبر ERCP + LC و LC + LCBDE بدائل طفيفة التوغل. ومع ذلك ، يتطلب ERCP + LC إجراءين منفصلين ويحمل مخاطر حدوث مضاعفات مثل النزيف والتهاب البنكرياس وانثقاب الاثني عشر وضعف وظيفة العضلة العاصرة Oddi. في المقابل ، تم إثبات LC + LCBDE كطريقة جراحية آمنة وفعالة نظرا للحد الأدنى من التوغل ، والتعافي السريع ، والإقامة القصيرة في المستشفى ، والفعالية المواتية من حيث التكلفة5،6،7. بالإضافة إلى ذلك ، يشار إلى LCBDE للمرضى الذين يعانون من فشل ERCP أو التهاب الأقنية الصفراوية الحاد أو التهاب البنكرياس الحاد أو تاريخ جراحة تحويل الجهاز الهضمي7.
يشمل LCBDE تقنيتين أساسيتين: الإغلاق الأولي وتصريف الأنبوب T. تشير البينات الناشئة إلى أن الإغلاق الأولي يوفر مزايا على تصريف الأنبوب T ، بما في ذلك فترات الجراحة والاستشفاء الأقصر ، بالإضافة إلى تقليل مضاعفات ما بعد الجراحة والقنواتالصفراوية 8.
يمكن إجراء الإغلاق الأولي ل LCBDE مع أو بدون دعامات داخلية. تشير الدراسات إلى أن الإغلاق الأولي الخالي من الدعامات آمن وموثوق به ، ويتجنب المضاعفات المحتملة مثل ترحيل الدعامة أو الحاجة إلى إجراءات إزالة الدعامةاللاحقة 9.
يظهر الجهاز الصفراوي اختلافات تشريحية كبيرة10،11 ، مع معدل تباين تم الإبلاغ عنه يبلغ 42.3٪ 12. أثناء الجراحة بالمنظار ، يزيد عدم القدرة على جس الهياكل التشريحية ، جنبا إلى جنب مع وذمة الأنسجة أو المعالم الغامضة بصريا ، من خطر إصابات القناة الصفراوية والأوعية الدموية. يعالج التصوير بالموجات فوق الصوتية بالمنظار (LUS) هذه التحديات من خلال تمكين التقييم في الوقت الفعلي لمنطقة البوابة الكبدية ، وتوفير تصور ديناميكي للقنوات الصفراوية والأوعية الدموية والأنسجة المحيطة ، والتعويض عن نقص التغذية الراجعة عن طريق اللمس ، وتعزيز السلامة الجراحية13،14. بينما تظل الموجات فوق الصوتية عبر البطن طريقة تصوير قياسية لتشخيص حصوات المرارة ، فإن دقتها محدودة بعوامل مثل سمك جدار البطن والدهون الحشوية وتداخل الغازات المعدية المعوية. يتغلب LUS على هذه القيود من خلال الجمع بين فوائد الموجات فوق الصوتية التقليدية والتصوير عالي التردد وعالي الدقة والقرب المباشر من الأعضاء والتوجيه أثناء الجراحة في الوقت الفعلي.
Protocol
يتبع هذا البروتوكول المبادئ التوجيهية الأخلاقية للأبحاث البشرية في مستشفى دونغقوان تونغواه. وقع المريض على نموذج الموافقة المستنيرة ذي الصلة.
ملاحظة: تم إدخال مريض ذكر يبلغ من العمر 78 عاما مع تاريخ من آلام البطن لمدة 3 أيام. كشف الفحص المقطعي المحوسب عن تحص المرارة جنبا إلى جنب مع تحص الصفراو ، بقطر القناة الصفراوية المشتركة (CBD) يبلغ حوالي 10 مم (انظر الشكل 1). لم يظهر التقييم قبل الجراحة أي موانع جراحية. الأدوات والمعدات المستخدمة مفصلة في جدول المواد.
1. فحص ما قبل الجراحة
- اختبارات الدم: إجراء اختبارات وظائف الكبد واختبارات وظائف الكلى ، بالإضافة إلى تعداد الدم الكامل ، وملف التخثر ، وفصيلة الدم ، والتطابق المتبادل.
- التصوير التشخيصي والتقييمات: إجراء مخطط كهربية القلب ، والأشعة السينية للصدر ، وتقييم القلب والأوعية الدموية ، والموجات فوق الصوتية دوبلر الملونة للكبد والجهاز الصفراوي ، والتصوير المقطعي المحوسب (CT) للجزء العلوي من البطن.
2. الإجراء الجراحي
- إجراء التنبيب الرغامي ووضع المريض في وضع ضعيف. تنفيذ التطهير الروتيني باستخدام محلول بوفيدون اليود.
ملاحظة: تم إعطاء التخدير العام وفقا للبروتوكولات المعتمدة من المؤسسة. - قم بإجراء تقنية قياسية رباعية المنافذ لاستئصال المرارة بالمنظار (انظر الشكل 2).
- قم بإنشاء شق رأسي 10 مم تحت السرة ، وأدخل غاز ثاني أكسيد الكربون باستخدام إبرة Veress لإنشاء التهاب الرئة الصفاق عند 12 مم زئبق.
- ثم ضع المبزل مقاس 10 مم ومنظار البطن تحت الأرض. تحت التصور المباشر الذي يوفره منظار البطن ، ضع منفذا تحت الخسج (10 مم) ، ومنفذ منتصف الترقوة الأيمن (5 مم) ، والمنفذ الإبطي الأمامي الأيمن (5 مم).
- الخطوات الجراحية (انظر الشكل 3 والشكل 4)
ملاحظة: يتم إجراء العملية الجراحية من قبل جراح بمساعدة مساعد.- قم بإجراء استكشاف بالمنظار لتجويف البطن باتباع هذا التسلسل: من أعلى إلى أسفل ، والأعضاء الصلبة أولا ، ثم الأعضاء المجوفة ، وتجويف البطن أولا ، ثم تجويف الحوض ، لتقييم آفات البطن بشكل منهجي (انظر الشكل 3 أ).
- استخدم LUS لاستكشاف منطقة البوابة الكبدية ، ووضع المسبار بالمنظار في منطقة التهاب الكبد الوبائي من خلال منفذ تحت الخرسانة (10 مم) ، وحرك المسبار لأعلى ولأسفل. يميز القنوات الصفراوية والأوعية الدموية عبر إشارات تدفق الدم وتقييم توزيع الحصوات (انظر الشكل 3 ب والشكل 4 أ ، ب).
- رفع قاع المرارة باستخدام ملقط غير رضحي (مساعد). سحب وتوسيع مثلث Calot لتحسين التعرض (الجراح). قم بتشريح طبقة مثلث Calot تلو الأخرى باستخدام خطاف كهربائي أو مشرط بالموجات فوق الصوتية (انظر الشكل 3C).
- استخدم LUS لتأكيد موقع اتفاقية التنوع البيولوجي. قم بتصويب إبرة مستديرة 5-0 بحامل إبرة واربط خياطة حريرية رقم 4 بذيلها لمنع الخسارة العرضية.
- أمسك نقطة منتصف الإبرة باستخدام ملقط بالمنظار متصل بالكي الكهربائي (20 واط). قم بعمل شق طولي بطول 1 سم على جدار CBD الأمامي (انظر الشكل 3 د).
- أدخل منظار الصفراوات من خلال منفذ تحت الوحجن في اتفاقية التنوع البيولوجي. تصور واسترداد حساب التفاضل والتكامل باستخدام سلة استرجاع الحجر (انظر الشكل 3E).
- افحص القنوات الصفراوية القريبة والبعيدة بحثا عن الحصوات المتبقية. تأكيد كفاءة العضلة العاصرة الحليمية الاثني عشر. أغلق بضع الصفراو بخياطة بولي ديوكسانون 5-0 (PDS) باستخدام خيوط مستمرة أو متقطعة (تباعد 1-2 مم) (انظر الشكل 3F ، G).
- ضع شاشا معقما على اتفاقية التنوع البيولوجي للكشف عن تسرب الصفراء. أكمل استئصال المرارة باستخدام المقصات بالموجات فوق الصوتية أو الكي الكهربائي.
- استخرج المرارة عبر المنفذ تحت الوحرة. إجراء المسح بالموجات فوق الصوتية بالمنظار (LUS) على طول محور القناة الصفراوية خارج الكبد في النقير الكبدي. تأكد من عدم وجود حساب التفاضل والتكامل المتبقي وتأكد من سالكية مفاغرة القناة الصفراوية دون تضيق (انظر الشكل 3H).
- أدخل أنبوب تصريف في الثقبة تحت الكبدية (ثقبة وينسلو) من خلال المنفذ الأمامي الأمامي الأيمن 5 مم (انظر الشكل 3I).
3. رعاية ما بعد الجراحة
- راقب باستمرار معدل ضربات القلب وضغط الدم ومعدل التنفس ودرجة حرارة الجسم.
- إدارة السوائل الوريدية للحفاظ على الترطيب وتوازن الكهارل والتوازن الحمضي القاعدي. تطبيق المضادات الحيوية الوريدية والعوامل الواقية من الكبد بعد الجراحة.
- بدء تناول الماء عن طريق الفم بعد 6 ساعات من الجراحة. تشجيع التعبئة المبكرة بجانب السرير لتعزيز التعافي.
- الحفاظ على سالكية أنابيب الصرف. مراقبة علامات تسرب الصفراء (على سبيل المثال، تصريف مصفر وانتفاخ البطن).
النتائج
استمر الإجراء 110 دقائق مع فقدان دم أثناء الجراحة بمقدار 10 مل. تمت إزالة أنبوب التصريف في اليوم 4 بعد الجراحة (POD4) ، وتم إخراج المريض دون أحداث على POD5. تم استخدام الموجات فوق الصوتية بالمنظار أثناء الجراحة (LUS) لتحديد القناة الكيسية والقناة الصفراوية المشتركة وتشريح الأوعية الدموية بوضوح وحجم وكمية وموقع حصوات القناة الصفراوية الشائعة (انظر الشكل 4) ، مما يتيح التوجيه أثناء الجراحة في الوقت الفعلي. لم يلاحظ أي مضاعفات حول الجراحة - بما في ذلك تسرب الصفراء أو النزيف أو الحصوات المتبقية أو تضيق القناة الصفراوية. خلال المتابعة التي استمرت 3 سنوات بعد الجراحة ، لم يتم تحديد أي مضاعفات كبيرة مرتبطة بالجراحة. كل هذه التفاصيل معروضة في الجدول 1.

الشكل 1: صور التصوير المقطعي المحوسب. (أ ، ب) تظهر الصور تحص المرارة جنبا إلى جنب مع تحص القنوات الدوارة. يمثل السهم الأصفر المرارة وتحص المرارة ، ويمثل السهم الأحمر القناة الصفراوية المشتركة وتحص القنوات الصفراوية. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
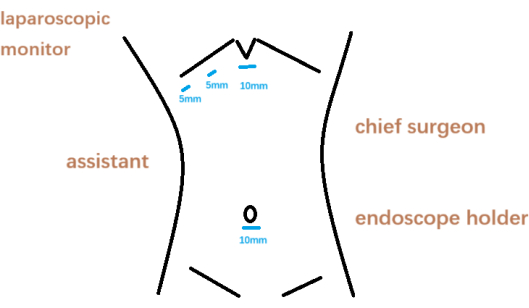
الشكل 2: وضع الجراح وموقع البزل. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
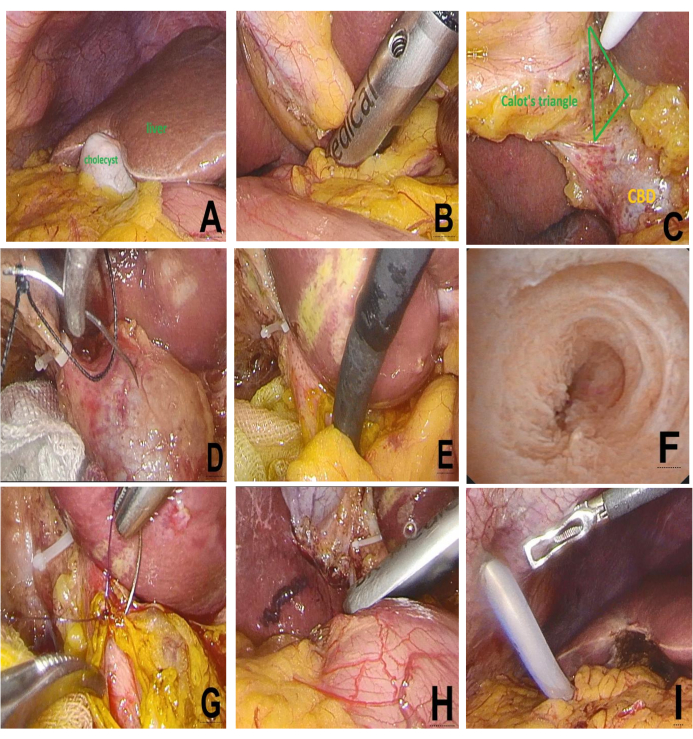
الشكل 3: خطوات LCBDE أثناء الجراحة: (أ) الاستكشاف بالمنظار. (ب) تقييم جامعة ليسانس اللون. (ج) تشريح مثلث كالوت. (د) شق الكي الكهربائي CBD. (ه) استخراج الحصوات بالمنظار الصفراوي. (و) ما بعد بضع الحصوات اتفاقية التنوع البيولوجي والحليمة. (ز) إغلاق اتفاقية التنوع البيولوجي الأساسي. (ح) إعادة تقييم جامعة المحيط الهادئ. (ط) وضع الصرف. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
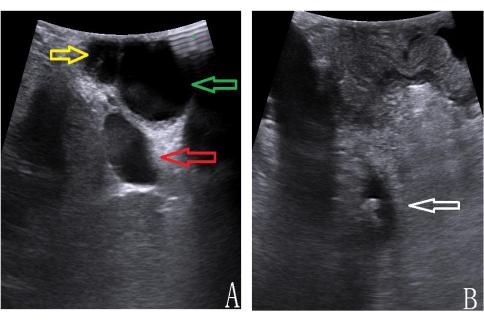
الشكل 4: تصوير LUS لتشريح البابات الكبدية. (أ) القناة الكيسية [صفر] ، اتفاقية التنوع البيولوجي [أخضر] ، الوريد البابي [أحمر]). (ب) أحجار اتفاقية التنوع البيولوجي [السهم الأبيض]. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
| البارامترات | النتائج |
| وقت العملية | 110 دقيقة |
| فقدان الدم | 10 مل |
| وقت إزالة أنبوب الصرف | 4 أيام |
| وقت الخروج بعد الجراحة | 5 أيام |
| تسرب الصفراء | لا |
| الحجر المحتجز | لا |
| تضيق القناة الصفراوية | لا |
| وقت المتابعة | 3 سنوات |
| تكرار أحجار CBD | لا |
الجدول 1: النتائج الجراحية.
Discussion
LC + LCBDE و ERCP + LC هي الأساليب الأساسية طفيفة التوغل لحصوات المرارة مع حصوات القناة الصفراوية الشائعة. بالمقارنة مع ERCP ، يوفر LCBDE مزايا في إدارة الأحجار الكبيرة ، والحفاظ على الوظيفة الحليمية ، وتجنب الإجراءات المرحلية15،16.
لا يزال دور تصريف الأنبوب T بعد LCBDE موضع نقاش. في حين أن هناك ما يبرره في حالات ارتفاع ضغط الدم الصفراوي أو الحصوات المتبقية أو التضيقات أو التهاب الأقنية الصفراوية الحاد ، يوصى بالإغلاق الأولي عندما يكون الالتهاب الصفراوي خفيفا ، وإزالة الحصوات كاملة ، وتكون وظيفة الحليمة سليمة17،18. يتجنب مركزنا الدعامات الصفراوية الروتينية لمنع هجرة الدعامة والتكاليف الإضافية وإجراءات الإزالة الثانوية.
تحد الجراحة بالمنظار من ردود الفعل اللمسية ، مما يزيد من مخاطر الإصابة في الأنسجة الوذمية أو المتغيرات التشريحية. يتغلب التصوير بالموجات فوق الصوتية بالمنظار (LUS) على ذلك من خلال توفير تصوير عالي الدقة في الوقت الفعلي للقنوات الصفراوية والأوعية الدموية. على عكس الموجات فوق الصوتية عبر البطن ، لا يتأثر LUS بسماكة جدار البطن أو غاز الأمعاء. بالمقارنة مع تصوير الأقنية الصفراوية أثناء الجراحة ، فإن LUS خال من الإشعاع وفعال من حيث الوقت ، مع حساسية تم الإبلاغ عنها بنسبة 96٪ وخصوصية 100٪ 19،20.
في هذه الدراسة ، أجرينا استكشاف القناة الصفراوية المشتركة بالمنظار (LCBDE) وتأكدنا من إزالة القناة مع الإغلاق الأولي لاتفاقية التنوع البيولوجي باستخدام تنظير الصفراو بالمنظار والموجات فوق الصوتية بالمنظار (LUS). تم استخدام LUS لاستكشاف المثلث الكيسي ، وتحديد موضع القناة الصفراوية خارج الكبد ، والشريان الكبدي ، والوريد البابي ، وتقييم موقع الحصوات وحجمها وعددها. كما قدمت إرشادات أثناء الجراحة.
حاليا ، تشمل الطرق الشائعة لشق القناة الصفراوية المشتركة (CBD) المقص والشفرات والخطافات الكهربائية. القطع بالمقص أو الشفرات عرضة للنزيف ويتطلب إرقاء إضافيا ، بينما قد تتسبب الخطافات الكهربائية في إصابة حرارية لجدار القناة الصفراوية بسبب التوصيل الحراري. في نهجنا ، تم استخدام إبرة جراحية كهربائية 5-0 لشق اتفاقية التنوع البيولوجي. قللت هذه التقنية من الضرر الذي لحق بجدار القناة الصفراوية ومنعت النزيف بشكل فعال. ثم تم استخدام منظار الصفراو لاستكشاف القناة الصفراوية وإزالة الحصوات. إذا أكد الفحص بالمنظار الصفراوي عدم وجود حصوات متبقية ووظيفة حليمة الاثني عشر الطبيعية ، فقد تم إغلاق اتفاقية التنوع البيولوجي بخيطة قابلة للامتصاص أحادية الشعيرات 5-0 باستخدام خيوط مستمرة أو متقطعة بسماكة كاملة (تباعد الغرز 1-2 مم ، هامش 1-2 مم) ، مما يضمن إغلاقا موحدا وخاليا من التوتر. تم تطبيق إسفنج شاش معقم جاف لاختبار تسرب الصفراء. تم استخدام الموجات فوق الصوتية بالمنظار (LUS) أيضا لتقييم الحصوات المتبقية وتقييم القناة الصفراوية المخيطة بحثا عن التضيقات. تم وضع أنابيب التصريف تحت الكبد بشكل روتيني للكشف عن تسرب الصفراء على الفور وضمان الصرف الكافي. في الحالة الموضحة هنا ، تمت إزالة أنبوب الصرف في اليوم 4 بعد الجراحة ، وتم إخراج المريض في اليوم 5. لم يلاحظ أي مضاعفات ، مثل تسرب الصفراء أو النزيف أو الحصوات المتبقية أو تضيق القناة الصفراوية.
ومع ذلك ، عند تنفيذ العملية ، من الضروري فهم المؤشرات بدقة لتحقيق أقصى قدر من فوائد المرضى. لقد قمنا بتلخيص التجربة السريرية وتقارير الأدبيات ذات الصلة21،22،23. هناك 4 مؤشرات للخياطة الصفراوية الأولية: (ط) قطر القناة الصفراوية ≥ 6 مم. يمكن أن يدخل منظار القنوات الصفراوية إلى القناة الصفراوية ، والتي لا يمكنها إزالة الحصوات فحسب ، بل تقلل أيضا من تضيق القناة الصفراوية بعد الجراحة. (ثانيا) بالنسبة لحصوات القناة الصفراوية خارج الكبد البسيطة ، يمكن إجراء خياطة أولية إذا تم ضمان إزالة الحصوات. ومع ذلك ، من الصعب عموما ضمان إزالة الحصوات بالكامل للحالات التي تحتوي على حصوات القناة الصفراوية داخل الكبد ، ولا ينصح بالخياطة الأولية. (ثالثا) حليمة الاثني عشر لها وظيفة فتح وإغلاق جيدة ولا يوجد تضيق في القناة الصفراوية. (رابعا)يتم خياطة جدار القناة الصفراوية المشتركة بالتساوي وبدقة وموثوقية دون تسرب الصفراء أو تضيقها.
ومع ذلك ، فإن الموجات فوق الصوتية بالمنظار لها أيضا حدودها. عادة ما يكون مسبار الموجات فوق الصوتية بالمنظار صغيرا في الحجم ، مما يجعل من الصعب مراقبة مساحة كبيرة من الأنسجة بشكل شامل في وقت واحد. فقط من خلال الخبرة العملية المتراكمة في العمليات الجراحية بالمنظار وتقنيات الفحص بالموجات فوق الصوتية يمكن للمرء أن يتقن حقا تقنية الموجات فوق الصوتية بالمنظار. تعتبر معدات الموجات فوق الصوتية بالمنظار باهظة الثمن نسبيا ، مما يحد من التطبيق الواسع لهذه التكنولوجيا في بعض المناطق المحدودة الموارد.
في الختام ، يمكن أن يضمن تطبيق LUS جنبا إلى جنب مع منظار الصفراو في الجراحة بالمنظار فعالية وسلامة الإغلاق الأولي لاتفاقية التنوع البيولوجي.
Disclosures
أفاد المؤلفون بعدم وجود تضارب في المصالح.
Acknowledgements
نشكر أطباء التخدير وممرضات غرفة العمليات الذين ساعدوا في العملية.
Materials
| Name | Company | Catalog Number | Comments |
| Basket catheter | Guangzhou Manya Medical Technology Co., Ltd | WL-F65-115M | |
| Cholangioscope | Olympus | CHF-V | |
| Disposable laparoscopic trocar | Mindray | CW-Z346 | |
| Electrocautery hook | Visionstar | HV300B | |
| Laparoscopic system | KARL STORZ | 26003AA | |
| Laparoscopic ultrasound | BK Medical | 8666-RF | |
| Polydioxanone suture | ETHICON | Z303H | |
| Ultrasonic dissector | ETHICON | ACE+7 |
References
- Marilee-L, F., Robert-L, B., Andrew-J, D. Choledocholithiasis: Evolving standards for diagnosis and management. World J Gastroenterol. 12 (20), 3162-3167 (2006).
- Costi, R., Gnocchi, A., Di Mario, F., Sarli, L. Diagnosis and management of choledocholithiasis in the golden age of imaging, endoscopy and laparoscopy. World J. Gastroenterol. 20 (37), 13382-13401 (2014).
- Shojaiefard, A., Esmaeilzadeh, M., Ghafouri, A., Mehrabi, A. Various techniques for the surgical treatment of common bile duct stones: a meta review. Gastroenterol Res Pract. 2009, 840208 (2009).
- Naotaka, F., et al. Evidence-based clinical practice guidelines for cholelithiasis. J Gastroenterol. 58 (9), 801-833 (2023).
- Chen, C. C., et al. The fading role of T-tube in laparoscopic choledochotomy: primary choledochorrhaphy and over pigtail j and endonasobiliary drainage tubes. J Laparoendosc Adv Surg Tech A. 20 (10), 807-811 (2000).
- Zhang, H. W., Chen, Y. J., Wu, C. H., Li, W. D. Laparoscopic common bile duct exploration with primary closure for management of choledocholithiasis: A retrospective analysis and comparison with conventional T-tube drainage. Am Surg. 80 (2), 178-181 (2014).
- Podda, M., et al. Systematic review with meta-analysis of studies comparing primary duct closure and T-tube drainage after laparoscopic common bile duct exploration for choledocholithiasis. Surg Endosc. 30 (3), 845-861 (2016).
- Kurinchi, S. G., Rahul, K. T-tube drainage versus primary closure after laparoscopic common bile duct exploration. Cochrane Database Syst Rev. 21 (6), CD005641 (2013).
- Yan, Y. The safety and efficacy of primary duct closure without endoscopic nasobiliary drainage after laparoscopic common bile duct exploration. Gastrointest Tumors. 7 (4), 117-124 (2020).
- Brent, T. X. Biliary anatomy and variations. Surg Clin North A. 104 (6), 1137-1144 (2024).
- Onofrio, A. C., et al. Vascular and biliary variants in the liver: implications for liver surgery. Radiographics. 28 (2), 359-378 (2008).
- Wu, J. S., Peng, C., Mao, X. -. H., Lv, P. Bile duct injuries associated with laparoscopic and open cholecystectomy: sixteen-year experience. World J Gastroenterol. 13 (16), 2374-2378 (2007).
- Jamal, K. N., et al. Meta-analysis of the diagnostic accuracy of laparoscopic ultrasonography and intraoperative cholangiography in detection of common bile duct stones. Ann R Coll Surg Engl. 98 (4), 244-249 (2016).
- Omer, A., et al. Laparoscopic ultrasonography versus intra-operative cholangiogram for the detection of common bile duct stones during laparoscopic cholecystectomy: a meta-analysis of diagnostic accuracy. Int J Surg. 12 (7), 712-719 (2014).
- Rogers, S. J., et al. Prospective randomized trial of LC+LCBDE vs ERCP/S+LC for common bile duct stone disease. Arch Surg. 145 (1), 28-33 (2010).
- Salminen, P., Laine, S., Gullichsen, R. Severe and fatal complications after ERCP: Analysis of 2555 procedures in a single experienced center. Surg Endosc. 22 (9), 1965-1970 (2008).
- Jiang, C., Zhao, X. H., Cheng, S. T-tube use after laparoscopic common bile duct exploration. JSLS. 23 (1), e2018.00077 (2019).
- Xie, W., et al. Is T-tube drainage no longer needed for laparoscopic common bile duct exploration? A retrospective analysis and literature review. Videosurgery. 18 (1), 99-107 (2023).
- Atstupens, K., Mukans, M., Plaudis, H., Pupelis, G. The role of laparoscopic ultrasonography in the evaluation of suspected choledocholithiasis. A single-center experience. Medicina. 56 (5), 246-260 (2020).
- Maple, J. T., et al. The role of endoscopy in the evaluation of suspected choledocholithiasis. Gastrointest Endosc. 71 (1), 1-9 (2010).
- Estellés, V. N., et al. Eleven years of primary closure of common bile duct after choledochotomy for choledocholithiasis. Surg Endosc. 30 (5), 1975-1982 (2016).
- Guan, H., Jiang, G., Mao, X. Primary duct closure combined with transcystic drainage versus T-tube drainage after laparoscopic choledochotomy. ANZ J Surg. 89 (7-8), 885-888 (2019).
- Khaled, Y. S., et al. Laparoscopic bile duct exploration via choledochotomy followed by primary duct closure is feasible and safe for the treatment of choledocholithiasis. Surg Endosc. 27 (11), 4164-4170 (2013).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved