Method Article
الحماية فعالية والرئوي الاستجابة المناعية بعد تحت الجلد والطريق الأنفي BCG الإدارة في الفئران
In This Article
Summary
We herein detail the methodology followed to compare protective efficacy and lung immune response induced by intranasal and subcutaneous immunization with BCG in mouse model. Our results show the benefits of pulmonary vaccination and suggest a role for IL17-mediated response in vaccine-induced protection.
Abstract
Despite global coverage of intradermal BCG vaccination, tuberculosis remains one of the most prevalent infectious diseases in the world. Preclinical data have encouraged pulmonary tuberculosis vaccines as a promising strategy to prevent pulmonary disease, which is responsible for transmission. In this work, we describe the methodology used to demonstrate in the mouse model the benefits of intranasal BCG vaccination when compared to subcutaneous. Our data revealed greater protective efficacy following intranasal BCG administration. In addition, our results indicate that pulmonary vaccination triggers a higher immune response in lungs, including Th1 and Th17 responses, as well as an increase of immunoglobulin A (IgA) concentration in respiratory airways. Our data show correlation between protective efficacy and the presence of IL17-producing cells in lungs post-Mycobacterium tuberculosis challenge, suggesting a role for this cytokine in the protective response conferred by pulmonary vaccination. Finally, we detail the global workflow we have developed to study respiratory vaccination in the mouse model, which could be extrapolated to other tuberculosis vaccines, apart from BCG, targeting the mucosal response or other pulmonary routes of administration such as the intratracheal or aerosol.
Introduction
السل (TB) هو واحد من الأمراض المعدية الرائدة تسبب المزيد من الوفيات المرتبطة من فيروس نقص المناعة البشرية في العالم، وجنبا إلى جنب مع ارتفاع الزيادة من أدوية المتعددة السلالات المقاومة يجعل السل مشكلة صحية عالمية تنذر بالخطر 1. أدوات جديدة للتشخيص والمخدرات أكثر فعالية وأقل سمية، واللقاحات السل آمنة وفعالة جديدة هي حاجة ملحة، خاصة في العالم النامي.
تعيش الموهن عصيات كالميت غيران (BCG) حاليا لقاح مرخص الوحيد ضد السل، الذي تديره الأدمة عند الولادة منذ 1970s في جميع أنحاء العالم. ويعتبر السل فعالة في الوقاية من أشكال حادة من المرض (التهاب السحايا والسل الدخني) في الأطفال، ولكن أظهرت فعالية تتعارض ضد السل الرئوي المسؤول عن انتقال المرض 2.
التطعيم الرئوي، الذي يحاكي الطريق الطبيعي لعدوى السل، يمثل نهجا جذابا للفتيلة المضيف المحلي الاستجابة المناعيةالصورة. وفي هذا الصدد، أظهرت أعمال مختلفة قبل السريرية في نماذج السل حيوانية مختلفة ذات الصلة أكبر فعالية لقاح التالية التحصين الرئوي مقارنة تحت الجلد أو داخل الأدمة الطريق 3-6. ومع ذلك، فإن آليات الحماية الناجمة عن التطعيم الرئوي ليست مفهومة جيدا. في السنوات الأخيرة، وقد أشار العديد من الأعمال من أجل الاستجابة بوساطة IL17 باعتبارها عاملا مهما من الاستجابة المناعية المخاطية-TB معين، كما في نماذج الفئران ناقصة لIL17 المخاطية فعالية الحماية التي يسببها اللقاح تضعف 7،8.
نحن في الآونة الأخيرة أظهرت لأول مرة أن الأنف إدارة BCG باي DBA / 2 الفئران، سلالة الماوس تتميز انعدام الحماية بعد التطعيم ضد مرض السل تحت الجلد 9. وتشير هذه النتائج إلى أن تطعيم السل التنفسي يمكن أن تكون أكثر فعالية في الحد من نسبة السل في البلدان الموبوءة، حيث يعتبر BCG داخل الأدمة غير فعالة ضد pulmonالسل آرى.
Protocol
وظلت كل الفئران تحت ظروف خاضعة للرقابة وملاحظة أي علامة على المرض. أجري العمل التجريبي في اتفاق مع التوجيهات الأوروبية والوطنية لحماية حيوانات التجارب وبموافقة من لجان الأخلاقيات المحلية المختصة.
1. إعداد الأرصدة كمية لالجلسرين من BCG الدنماركية وH37Rv المتفطرة السلية
وقد أجريت جميع البروتوكولات المذكورة في ظل ظروف BSL3: ملاحظة.
- أسهم الجلسرين المجمدة ذوبان الجليد من BCG الدنماركية أو سلالات H37Rv وتطعيم 100 ميكرولتر في 10 مل من 7H9 المتوسط 10 تستكمل مع توين-80 بنسبة 0.05٪ (ت / ت) وشركة تطوير العقبة (الزلال، سكر العنب، الكاتلاز) 10٪ (ت / ت).
- احتضان في ظل ظروف ثابتة لمدة أسبوع واحد على 37 درجة مئوية حتى الثقافة هي في نمو السجل المرحلة.
- رفع مستوى الثقافة البكتيرية عن طريق نقل ثقافة 10 مل إلى 200 مل من المتوسط الطازجة. احتضان لمدة 20 إضافيةأيام في ظل ظروف ثابتة.
- نقل إلى أنابيب الطرد المركزي 50 مل وأجهزة الطرد المركزي لمدة 15 دقيقة في 2500 ز س.
- تجاهل supernatants و resuspend بيليه البكتيرية في حجم المتبقية. إضافة إلى كل أنبوب العقيمة الخرز الزجاجي 3 ملم قطرها (10-15 في أنبوب).
- دوامة بقوة خلال 1 دقيقة من أجل فصل كتل البكتيرية. resuspend كل بيليه في 10 مل من برنامج تلفزيوني مع توين-80 بنسبة 0.05٪ (ت / ت).
- ترك الأنابيب لمدة 10 دقيقة مما يتيح أكبر قدر من المجاميع البكتيرية والخرز الزجاجي ليستقر.
- استرداد 9.5 مل من طاف من كل من 4 أنابيب تحتوي على كتل صغيرة والبكتيريا واحدة وأحجام نقل إلى أدنى أنبوب الطرد المركزي 50 مل واحد (الحجم النهائي تعافى 38 مل). أجهزة الطرد المركزي لمدة 10 دقيقة على 400 ز س.
- استرداد 35 مل من طاف (التي تحتوي على البكتيريا بشكل رئيسي واحد) في جديدة أنبوب الطرد المركزي 50 مل واحد وإضافة 15 مل من برنامج تلفزيوني مع الجلسرين 50٪ (ت / ت)، والحصول على تركيز الجلسرين النهائية 15٪ (ت / ت).
- المزيج بلطفوتوزيعها في قسامات 1 مل في أنابيب مناسبة لتجميد. مخزن في -80 درجة مئوية (قطعة واحدة يوفر ما يقرب من 50 قسامات الأسهم الجلسرين).
- لقياس الأسهم الجلسرين، ذوبان الجليد والجلسرين اليوم بعد تجميد وتنفيذ سبعة التخفيفات المسلسل عشرة أضعاف في منفصلة أنابيب 1.5 مل تحتوي على 900 ميكرولتر من برنامج تلفزيوني.
- لوحة 100 ميكرولتر من كل تخفيف في 7H10 المتوسطة الصلبة أجار 10 تستكمل مع شركة تطوير العقبة 10٪ (ت / ت) التي أعدت في 55 مم أطباق بتري.
- بعناية إضافة 3 حبات الزجاج ملم قطرها (حوالي 10 في لوحة) ويهز بلطف لوحة لتوزيع بالتساوي حجم فوق لوحة أجار. تجاهل الخرز وختم لوحة أجار مع بارافيلم.
- احتضان لمدة 21 يوما في 37 درجة مئوية، وتحديد تركيز البكتيريا عن طريق عد الوحدات المكونة للمستعمرة (كفو) في التخفيفات حيث المستعمرات واحد يمكن تمييزها بدقة.
2. ماوس التطعيم
- ذوبان الجليد في BCG الجلسرين كميا قبل وتمييع في برنامج تلفزيوني لالإعداديةهما تعليق. حساب الحجم النهائي النظر في جرعة لكل حيوان هو 100 ميكرولتر للإدارة تحت الجلد (10 7 كفو لكل مل للتطعيم تحت الجلد) و 40 ميكرولتر لإدارة الأنف (2.5 × 10 7 كفو للتطعيم داخل الأنف).
- استخدام محطة عمل التخدير المتخصصة للقوارض لتخدير الفئران مع خليط من الأيزوفلورين والأكسجين. استخدام الأيزوفلورين 5٪ للحث على التخدير و 2٪ للحفاظ على الفئران في غرفة التخدير. (ويمكن استخدام غيرها من طريقة التخدير مقبول).
- لإعطاء اللقاح تحت الجلد ملء حقنة 1 مل مع إبرة 26 G مع 1 مل من تعليق البكتيرية (10 7 خلية / مل). إزالة فقاعات الهواء.
- وضع الماوس تخدير على سطح مستو في موقف المعرضة داخل غطاء تدفق الصفحي وتطعيم تحت الجلد 100 ميكرولتر (10 6 كفو / جرعة) من اللقاح في الجهة من الماوس مرة أخرى. عودة الماوس إلى القفص ومراقبة لضمان propeRLY يتعافى من التخدير.
- تغيير إبرة حقنة بين كل إدارة الماوس. إزالة فقاعات الهواء كما هو موضح أعلاه.
- لإدارة الأنف، وضع الماوس تخدير في موقف ضعيف داخل غطاء محرك السيارة.
- مع micropipette يستغرق 20 ميكرولتر من تعليق مع 2.5 × 10 7 خلية / مل. وضع اللقاح قطرة تلو قطرة بين فتحتي الأنف حتى يتم إيداع مجلدا كاملا، وترك الوقت بين قطرات للسماح الماوس التنفس وحدة التخزين في ملاحظة: يمكن أن الفئران تعاني من ضيق في التنفس أثناء هذا الإجراء ولذلك يجب أن تترك لل استيعاب كل قطرة مسبق لادارة المرحلة التالية لمنع ذلك قدر الإمكان.
- إعادة ملء micropipette مع 20 ميكرولتر آخر وكرر العملية. إذا بدأ الفأر أن يستيقظ من التخدير بعد التلقيح الأول، وضعه في غرفة التخدير قبل ثانية واحدة. عودة الماوس إلى القفص، وضمان أنه يتعافى بشكل صحيحمن التخدير.
3. ماوس الطعن في الأنف مع H37Rv الانفعال
- ذوبان الجليد في H37Rv الجلسرين كميا قبل وتمييع في برنامج تلفزيوني لإعداد تعليق البكتيرية من 2500 كفو لكل مل. حساب الحجم النهائي النظر في جرعة لكل حيوان هو 40 ميكرولتر.
- وتلقيح H37Rv الأنف كما هو موضح في 2،5-2،7. جرعة التحدي النهائية في الماوس هو 10 2 كفو / 40 ميكرولتر.
4. تحليل المستحثة الاستجابة المناعية في الرئتين
- الرئة تعليق الخلوي
ملاحظة: تقييم الاستجابة المناعية التكيفية التي يسببها اللقاح في الرئتين يتطلب توليد تعليق خلية واحدة. لهذا الغرض، ونحن نستخدم dissociator الأنسجة مثل GentleMACS.- التضحية الماوس عن طريق خلع عنق الرحم (أو غيرها من منهجية الإنسانية المقبولة) وضمان الفأر هو ميت لمس مقلة العين لتأكيد غائبة منعكس طرفة.
- داخل غطاء تدفق الصفحي، استخراج لترungs باستخدام مقص العقيمة وملقط ووضعها على سطح نظيف. الرئتين نظيفة إزالة القصبة الهوائية والنسيج الضام، ونقل الرئتين إلى أنبوب 1.5 مل مع برنامج تلفزيوني (الحفاظ على الجليد حتى التجهيز).
- لتوليد تعليق الخلوية، وضع الرئتين في أنبوب المناسب لتفكك الجهاز (أنبوب C-dissociator) تحتوي على 5 مل من 10 ملي HEPES-هيدروكسيد الصوديوم 7.4 درجة الحموضة، 150 مم كلوريد الصوديوم، 5 مم بوكل، 1 ملم MgCl 2 و 1.8 ملي CaCl 2 العازلة.
- إضافة 100 ميكرولتر من كولاجيناز D 100 ملغ / مل (2 ملغ / مل تركيز النهائي)، و 40 ميكرولتر من أنا الدناز 20000 وحدة دولية / مل (160 وحدة دولية / مل تركيز النهائي.
ملاحظة: الحلول المالية من كولاجيناز D أو DNaseI يتم إعداد حل الانزيمات مجفف بالتجميد في برنامج تلفزيوني أو الجلسرين 50٪ (ت / ت)، 20 ملي تريس، حمض الهيدروكلوريك 7.5 درجة الحموضة ذ MgCl 2 1 ملم، على التوالي. - وضع أنبوب في dissociator الأنسجة واستخدام m_lung_01 برنامج محدد مسبقا لتجزئة الرئة. احتضان الأنبوب عند 37 درجة مئوية في حمام مائي لمدة 30 دقيقة.
- المركز الرابعأنبوب الإلكترونية في dissociator واستخدام m_lung_02 البرنامج مسبقا لتجانس الرئة الكامل إلى تعليق الخلوي واحد.
- تمرير تعليق الخلوي من خلال 70 ميكرون خلية النايلون مصفاة لتركيب أنبوب الطرد المركزي 50 مل. غسل مصفاة مع 10 مل من المتوسط 1640 RPMI.
- خلايا الطرد المركزي لمدة 5 دقائق في 400 x ج وتجاهل طاف.
- إضافة 1 مل من الكريات الحمراء الناشر العازلة، مزيج من قبل vortexing واحتضان لمدة 1 دقيقة في درجة حرارة الغرفة.
- إضافة 10 مل من RPMI 1640 الخلايا المتوسطة وأجهزة الطرد المركزي لمدة 5 دقائق في 400 ز س.
- Resuspend الخلايا في 0.5 مل من اكتمال المتوسط 1640 RPMI تستكمل مع المعطل للحرارة بنسبة 10٪ الجنين العجل المصل (FCS)، 2 مم L-Glutamin، 100 ميكروغرام / مل الستربتوميسين، و 100 وحدة دولية / مل البنسلين و 50 ميكرومتر 2-المركابتويثانول.
ملاحظة: يتم المعطل FCS من الحضانة عند 56 درجة مئوية لمدة 30 دقيقة. - عد الخلايا وإضافة RPMI كاملة 1640 المتوسطة للوصول إلى الكثافة الخلوية النهائية من 10 7 خلية / مل.
ملاحظة: للحصول على عدد خلايا، ونحن نستخدم مكافحة خلية الآلي. - توزيع 100 ميكرولتر من تعليق الخلوية في U-أسفل لوحة 96-جيدا العقيمة (10 6 خلايا / جيد).
- إضافة 50 ميكرولتر / بئر الكامل المتوسط 1640 RPMI مع 15 ميكروغرام / مل من H37Rv التجاري البروتين النقي المشتق (PPD) (5 ميكروغرام / مل تركيز النهائي).
- جمع طاف لتحديد خلوى بواسطة ELISA
- احتضان لوحة من 4.1.14 لمدة 48 ساعة على 37 درجة مئوية و 5٪ CO 2.
- لوحة أجهزة الطرد المركزي لمدة 5 دقائق في 400 x ج واسترداد 100 ميكرولتر من طاف.
- تخزين في -80 درجة مئوية.
- تمييع supernatants 1/10 و 1/2 في المخزن فحص لIFNγ وتقرير IL17A، على التوالي. تحديد تركيزات خلوى مع مجموعات ELISA التجارية، وفقا لتعليمات الشركة الصانعة (مجموعات التنمية ELISA).
- تلطيخ الخلايا لتحديد خلوى-producing CD4 + الخلايا عن طريق التدفق الخلوي
- احتضان لوحة من 4.1.14 لمدة 18 ساعة على 37 درجة مئوية و 5٪ CO 2.
- إضافة 1.5 ميكرولتر من Brefeldin A 1 ملغ / مل (الأسهم الذائبة في DMSO) لكل (تركيز النهائي 10 ميكروغرام / مل) جيدا واحتضان لمدة ست ساعات إضافية.
- أجهزة الطرد المركزي لوحة من 4.3.2 لمدة 1 دقيقة في 3200 x ج وتجاهل طاف.
- Resuspend الخلايا في 50 ميكرولتر من مكافحة فأر CD4-FITC المخفف في RPMI 1640 مع 10٪ FCS (1/500)، واحتضان لمدة 10 دقيقة على 4 درجات مئوية.
- أجهزة الطرد المركزي لوحة من 4.3.4 لمدة 1 دقيقة في 3200 x ج، تجاهل طاف وإضافة 100 ميكرولتر / بئر حل التثبيت. احتضان عند 4 درجة مئوية لمدة 20 دقيقة.
- غسل الخلايا مرتين مع 150 ميكرولتر / غسل من حل permeabilization.
ملاحظة: يتم تخفيف 10X الأسهم تتركز في الماء منزوع الأيونات لإعداد محلول العمل 1X. - Resuspend الخلايا في 50 ميكرولتر من مكافحة فأر IFNγ-APC ومكافحة فأر IL17A-APC.Cy7 مخففة في permeabilحل سعودة (1/250 كل من الأجسام المضادة).
- احتضان لمدة 1 ساعة على RT.
- غسل الخلايا مرتين مع 150 ميكرولتر / غسل من حل permeabilization.
- Resuspend الخلايا في 200 ميكرولتر من برنامج تلفزيوني لاكتساب التدفق الخلوي.
5. تحليل المناعية في القصبات الغسل (نال)
- حصولهم العينات BAL
- التضحية الماوس عن طريق خلع عنق الرحم (أو غيرها من منهجية الإنسانية المقبولة) وضمان الفأر هو ميت لمس مقلة العين لتأكيد غائبة منعكس طرفة.
- فضح القصبة الهوائية باستخدام المناسبة الدقة ملقط معقم والمقص وإجراء قطع صغير في القصبة الهوائية، والتأكد من عدم استئصال تماما. الحرص على عدم تسبب النزيف التي يمكن أن تلوث العينة بال.
- ندخل في القصبة الهوائية قنية متصلة معقمة حقنة 1-مل مع 800 ميكرولتر من الجليد الباردة برنامج تلفزيوني.
- تطعيم ببطء برنامج تلفزيوني في الرئتين ومن ثم صإيكوفر حجم بال الانسحاب مكبس الحقنة ببطء للغاية من أجل تجنب انهيار الرئة.
ملاحظة: استرداد 500 و 600 ميكرولتر غير مرضية. - نقل حجم بال في أنبوب 1.5 مل وتأكيد يبقى بال uncoloured، مشيرا إلى أن لا تكون ملوثة بالدم (الحفاظ على الجليد حتى التجهيز).
- الطرد المركزي عينات بال لمدة 5 دقائق في 400 x ج، ونقل طاف لأنبوب جديد.
- متجر supernatants في -80 درجة مئوية.
- تقرير من إعتلال في بال supernatants
ملاحظة: جميع الكواشف المستخدمة في RT.- معطف نسبة عالية من البروتين البوليسترين ملزم أسفل شقة لوحات 96-جيدا مع 100 ميكرولتر من PPD مخففة في برنامج تلفزيوني (10 ميكروغرام / مل) لم. السل -specific تقرير ايغا، أو مع 100 ميكرولتر من BAL طاف المخفف 10 مرات في برنامج تلفزيوني لمجموع تقرير ايغا.
- احتضان بين عشية وضحاها في 4 درجات مئوية.
- تجاهل طاف والاستفادة من لوحة على منشفة ورقية لدراي. يغسل مع 200 ميكرولتر / جيد من برنامج تلفزيوني.
- منع مع 200 ميكرولتر / بئر من زلال المصل البقري (BSA) 1٪ (ث / ت) في برنامج تلفزيوني-توين-80 بنسبة 0.05٪ (ت / ت) (عازلة حجب).
- احتضان 1 ساعة على RT.
- يغسل مرة واحدة مع 200 ميكرولتر / بئر برنامج تلفزيوني توين-80 بنسبة 0.05٪ (ت ت /) (عازلة الغسل).
- إضافة 100 ميكرولتر من طاف بال مخفف في الآبار المغلفة PPD. احتضان ساعتين في درجة حرارة الغرفة.
ملاحظة: إذا تم الكلي تقرير ايغا بالتوازي مع PPD محددة ايغا، وترك مجموع الآبار ايغا مع غسل العازلة 100 ميكرولتر خلال هذه الحضانة. - يغسل ثلاث مرات مع 200 ميكرولتر / بئر غسل buffer.0170004
- إضافة 100 ميكرولتر من الفجل البيروكسيداز (HRP) -conjugated مكافحة فأر ايغا المخفف في عرقلة العازلة (1/10000).
- احتضان 1 ساعة RT.
- غسل خمس مرات مع 200 ميكرولتر / بئر غسل العازلة.
- إضافة 100 ميكرولتر / بئر 3،3 '، 5،5'-Tetramethylbenzidine (TMB). احتضان 20 دقيقة في درجة حرارة الغرفة في تيكان الظلام.
- إضافة 100 ميكرولتر / بئر H 2 SO 4 0.5N. قراءة لوحة في معمل عند طول موجي 450 نانومتر.
6. الجرثومي تقرير الحمل في الرئتين
- الرئة التجانس والطلاء
- بعد أربعة أسابيع التحدي، تضحية الماوس بواسطة الخلع عنق الرحم (أو غيرها من منهجية الإنسانية المقبولة) وضمان الفأر هو ميت لمس مقلة العين لتأكيد غائبة منعكس طرفة.
- ضع الماوس في موقف ضعيف ثابتة على سطح مستو وتطهيرها داخل غطاء تدفق الصفحي.
- إجراء شق وإزالة الجلد من منطقة الصدر لترك مرئية منطقة الصدر.
- قطع الأضلاع وحصاد الرئتين والقلب باستخدام مقص العقيمة وملقط. وضع الأجهزة على سطح نظيف.
- تنظيف الرئتين عن طريق إزالة القلب والقصبة الهوائية والأنسجة الضامة ونقل الرئتين إلى أنبوب 1.5 مل مع 1 مل من الماء منزوع الأيونات(الحفاظ على الجليد حتى معالجة).
- استخدام ملقط معقم لنقل الرئتين من كل فأر في أنبوب المناسب لتجانس جهاز (M - أنبوب dissociator)، التي تحتوي على 1 مل من الماء منزوع الأيونات.
- وضع أنبوب في dissociator الأنسجة واستخدام RNA_1 برنامج محدد مسبقا لالتجانس الرئتين.
- جعل خمسة التخفيفات المسلسل عشرة أضعاف في أنابيب 1.5 مل، بدءا من 100 ميكرولتر من جناسة الرئة مخففة في 900 ميكرولتر.
- التخفيفات لوحة كما هو موضح في 1،11-1،14.
- التمايز بين BCG وH37Rv بواسطة PCR
ملاحظة: في لوحات من 6.1.6 الموافق المجموعة التي تم تلقيحها مع BCG بالطريق الأنف، قمنا بتحليل عدد تمثيلي من المستعمرات قبل PCR المميزين بين BCG وH37Rv للتأكد من أن كفو تعتبر لتقييم فعالية يتفق واقية الممنوحة لقاح فريد لH37Rv. هذه الأهداف PCR التضخيم من RD9، وهي منطقة الجينومية مختلفة في مجموعة بوسطن الاستشارية وم توberculosis، وإعطاء جزء من 2618 سنة مضت لH37Rv، و 465 نقطة أساس لقاح بي سي جي 11.- إعداد المخزون مزيج الرئيسي لجميع العينات مع وحدات التخزين في عينة كما هو مبين، ومن ثم توزيعها في أنابيب PCR (9 ميكرولتر / العينة).
ملاحظة: المخزن المؤقت 5X: 2 ميكرولتر. التمهيدي إلى الأمام 25 ميكرومتر (GTGTAGGTCAGCCCCATCC): 0.32 ميكرولتر، عكس التمهيدي 25 ميكرومتر (GCCCAACAGCTCGACATC): 0.32 ميكرولتر، طق البلمرة 5 وحدات / ميكرولتر: 0.04 ميكرولتر، منزوع الأيونات H 2 O: 6.32 ميكرولتر. - المس مستعمرة مع المسواك العقيمة وتزج مسواك مع العينة في أنبوب PCR التي تحتوي على مزيج الرئيسي.
- تشغيل PCR مع البرنامج التالي: 10 دقيقة 95 درجة مئوية (هذه الخطوة لتحريك تعطل البكتيري)، 10 دقيقة 95 درجة مئوية (هذه الخطوة لتحريك تعطل البكتيري)، 35 دورات (30 ثانية في 95 درجة مئوية، 1 دقيقة في 58 درجة مئوية و 4 دقائق عند 72 درجة مئوية).
- تحميل عينات PCR في هلام الاغاروز 1٪ مع عينات بروميد إيثيديوم وتشغيل لتصور شظايا.
- إعداد المخزون مزيج الرئيسي لجميع العينات مع وحدات التخزين في عينة كما هو مبين، ومن ثم توزيعها في أنابيب PCR (9 ميكرولتر / العينة).
النتائج
يصف هذا العمل المقارنة بين طريقين من إدارة BCG: تحت الجلد وداخل الأنف. الطريق تحت الجلد هو مشابه إلى الأدمة، الذي هو الطريق السريرية الحالية لمجموعة بوسطن الاستشارية في جميع أنحاء العالم. ويهدف طريق الأنف التطعيم لتقليد الطريق الطبيعي لعدوى م. السل، بهدف تحريض استجابة مناعية مباشرة في الرئتين، والجهاز الهدف الرئيسي لهذا العامل الممرض.
يوضح الشكل رقم (1) وسير العمل المتبعة. ثمانية لDBA أنثى عمرها أسابيع عشر / يتم تطعيم 2 الفئران مع 10 6 كفو من BCG الدنماركية بالطريق تحت الجلد أو الأنف الإدارة. وبعد ثمانية أسابيع، تم التضحية مجموعة من الفئران لتحليل الرئة الاستجابة المناعية الناتجة عن التطعيم. يتم الحصول على عينات بال أولا ثم نحن حصاد الرئتين. من أجل دراسة فعالية واقية الممنوحة لقاح، فإننا تطعيم احمجموعة الشمالي من الفئران مع الطعن في الأنف جرعة منخفضة من م. السل H37Rv سلالة. بعد شهر واحد، ونحن نضحي الحيوانات والرئتين الحصاد. في هذه الحالة، لكل حيوان نستخدم الرئة اليسرى لتحديد الحمولة الجرثومية والرئة اليمنى لتقييم يسببها اللقاح الاستجابة المناعية بعد التحدي. والهدف هو توليد الحمولة الجرثومية والبيانات الاستجابة المناعية في الرئتين لكل حيوان من أجل دراسة يرتبط المحتملة للحماية.
كما هو مبين في الشكل 2، تم فصلها الرئتين للحصول إما جناسة الجهاز أو تعليق الخلوية. كانت مطلية الرئتين المتجانس على وسط أجار الصلبة لتحديد الحمولة الجرثومية أربعة أسابيع بعد التحدي. تم الحصول على تعليق الخلوي لدراسة الاستجابة المناعية التي يسببها اللقاح التالية الرئة الأنزيمية الهضم مع كولاجيناز D وDNaseI.
نتائجنا تشير بوضوح إلى أن، تي مقارنةس الطريق تحت الجلد، والطريق الأنف التطعيم يمنح وفعالية وقائية أكبر بكثير في الرئتين أربعة أسابيع بعد التحدي (الشكل 3A). وبالإضافة إلى ذلك، أكدنا أن الحمل البكتيري في الرئتين من مجموعة BCG-لقاح الأنف تتوافق مع H37Rv وليس لقاح BCG. تحقيقا لهذه الغاية، قمنا بتحليل عدد تمثيلي من المستعمرات من هذه المجموعة من قبل PCR محددة للمنطقة الجينوم RD9، مما يزيد شظايا طول مختلفة في مجموعة بوسطن الاستشارية وم. السل (الشكل 3B). أظهر الرقم بوضوح أن جميع المستعمرات تحليلها توفير جزء من 0.4 KBP، وهو ما يعادل H37Rv.
وكشفت البيانات المتوفرة لدينا ارتباط بين فعالية الحماية التي يمنحها الأنف قاح BCG والاستجابة المناعية التي يسببها اللقاح في الرئتين السابقة للتحدي. أثار الأنف BCG بوضوح أعلى IL17 والإنتاج IFNγ في الرئتين، ويقاس بواسطة ELISA (الشكل4A). وتأكدت هذه البيانات عن طريق تلطيخ الخلايا (ICS) والتدفق الخلوي (لا تظهر البيانات). وبالإضافة إلى ذلك، وجدنا أيضا على تركيز أعلى من كل من إجمالي وPPD محددة تركيز ايغا في عينات بال (الشكل 4B)، مشيرا إلى أن لقاح BCG الرئوي يدفع إنتاج ايغا والنبات إلى الشعب الهوائية في الجهاز التنفسي.
وأخيرا، درسنا الاستجابة المناعية BCG-يتسبب في الرئتين بعد التحدي (الشكل 5). وكشفت البيانات المتوفرة لدينا خلافات بين IL17 وIFNγ. تم الكشف عن CD4 الخلايا المنتجة للIL17A + فقط في المجموعة BCG داخل الأنف، في حين تم العثور على خلايا IFNγ المنتجة في جميع الفئات المصابة H37Rv بغض النظر عن التطعيم. أظهر تمثيل البيانات من كل حيوان الموافق الخلايا المنتجة للIL17 والحمولة الجرثومية وجود علاقة ذات دلالة إحصائية بين وجود IL17 والرئة البكتيري الحد من الحمل، والذي لم يكن لوحظ في حالة IFNγ.
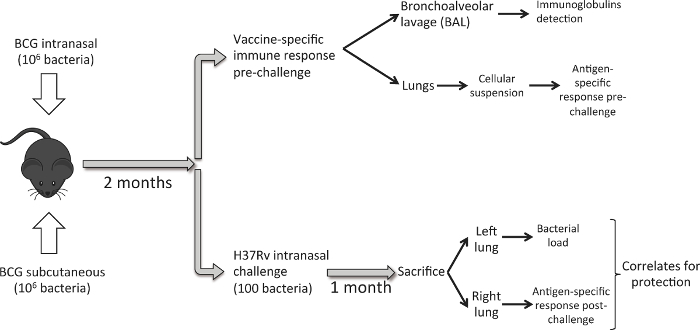
الشكل 1. سير العمل إلى قارن الطريق الأنفي وتحت الجلد الطريق من BCG التطعيم ثمانية أسابيع بعد التطعيم ضد مرض السل، ومجموعة من الفئران (6 في المجموعة التجريبية) يستخدم لحصاد الرئتين وإجراء بال، وتحليل الاستجابة المناعية الرئوية الناجمة عن التطعيم. مجموعة أخرى من الفئران (6 / مجموعة)، وتلقيح مع الطعن في الأنف جرعة منخفضة من م. السل H37Rv سلالة (100 كفو). وبعد شهر، والتضحية الحيوانات ويتم تحليل الحمل البكتيري في الرئة اليسرى والاستجابة المناعية PPD محددة في الرئة اليمنى. الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
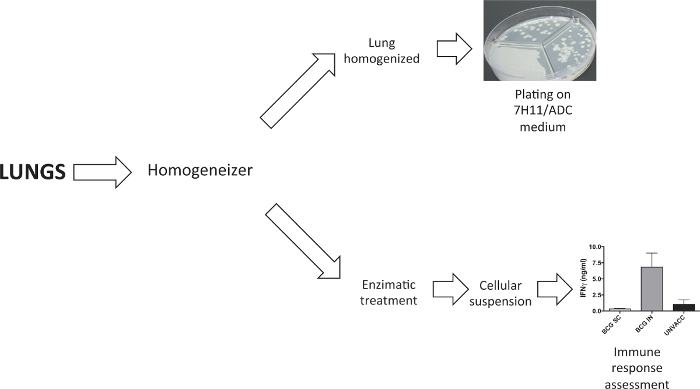
الشكل 2. تجهيز العينات الرئة. تم استخدام dissociator الأنسجة لمعالجة الرئتين. في التجارب لتحديد الحمولة الجرثومية، ومتجانسة الرئتين قبل لوحة منها في المتوسط أجار الصلبة. في التجارب التي تتطلب تعليق الخلوي الرئة، تم إنشاء هذا التالية الهضم الأنزيمي مع كولاجيناز D وDNaseI. الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.

الرقم 3. واقية فعالية تمنحها BCG التحصين. المجموعات من 6 ديسيبل / تم تطعيم 2 الفئران التي تحت الجلد (BCG الشوري)، الأنف (BCG في) الطريق، أو غير تطعيم (Unvacc) بلقاح BCG الدنماركية 10 6 كفو. في شهرين بعد التطعيم، تم تلقيح الفئران الأنف بجرعة منخفضة (100تم تحديد كفو) التحدي H37Rv، وشهر واحد عبء البكتيرية في وقت لاحق في الرئتين. ويرد تجربة تمثيلية من اثنين من المستقلين. (A) البيانات في الرسوم البيانية يتم تمثيل كما يعني + SD. وقد أجريت في اتجاه واحد أنوفا اختبار مع تحليل آخر بونفيروني لحساب دلالة إحصائية. (ب) عدد تمثيلي من تم تحليلها من قبل PCR محددة لمنطقة RD9 (مختلفة في مجموعة بوسطن الاستشارية وH37Rv الجينوم) المستعمرات واحد من مجموعة الأنف BCG لتبين BCG و المستعمرات H37Rv. (نشرت في السابق 9). الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.

الرقم 4. لقاح محدد الرئوي الاستجابة المناعية تحليلها قبل التحدي مع H37Rv. كانت المجموعات من 6 ديسيبل 2 الفئران /التحصين من تحت الجلد (BCG الشوري) أو الأنف (BCG في) الطريق، أو غير تطعيم (Unvacc) بلقاح BCG الدنماركية 10 6 كفو. (A) في شهرين بعد التطعيم، تم الحصول على تعليق الخلوي من الرئتين المقطوع. وقد حفز الخلايا مع PPD كما هو موضح في قسم الأساليب وIL17A (اللوحة اليسرى) وIFNγ (اللوحة اليمنى) وقد تم تحليل الإنتاج عن طريق ELISA. (ب) إجمالي ايغا، و م. وقد تم تحليل السل (MTB) -specific ايغا من العينات BAL بواسطة ELISA. وأظهرت البيانات المجمعة من تجربتين مستقلة. يتم تمثيل البيانات في الرسوم البيانية كما يعني + SD. (نشرت في السابق 9). الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
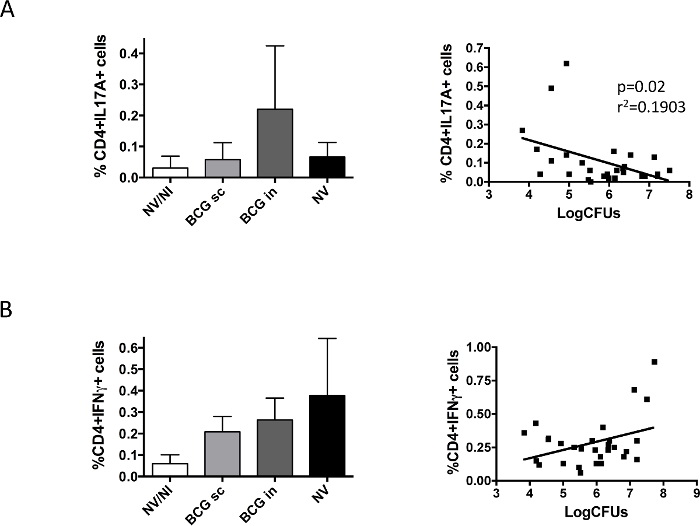
الرقم 5. لقاح محددةالاستجابة المناعية الرئوية تحليلها قبل التحدي مع H37Rv. المجموعات من 6 ديسيبل / تم تطعيم 2 الفئران التي تحت الجلد (BCG الشوري) أو الأنف (BCG في) الطريق، أو يطعموا (NV) بلقاح BCG الدنماركية 10 6 كفو. أدرج مجموعة مراقبة من يطعموا الفئران، غير مصاب أيضا (نيفادا / NI). في شهرين بعد التطعيم، وقد تم الطعن الفئران الأنف بجرعة H37Rv منخفضة (100 كفو)، وبعد شهر واحد الموت الرحيم كانت الحيوانات. اليسار واستخدمت الرئتين اليمنى من نفس الحيوان لتحديد الحمولة الجرثومية وIL17A- (A) أو IFNγ- (ب) إنتاج خلايا CD4 +، على التوالي. بيانات في لوحات اليسرى تتوافق مع النسبة المئوية للخلايا المنتجة للخلوى قياس التدفق الخلوي، وتمثل كما يعني + SD. وتمثل لوحات اليمين البيانات من الحمل البكتيري وcytokine- إنتاج خلايا CD4 + التي تم الحصول عليها لكل الماوس. تم حساب الانحدار الخطي ويظهر القيمة ص التي تم الحصول عليها في كل حالة في حالة IL17A. المجمعةوأظهرت بيانات من تجربتين مستقلة في الشكل. (نشرت في السابق 9). الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
Discussion
Although current vaccine against tuberculosis, BCG, is the most widely administered vaccine in history, tuberculosis remains one of the leading causes of death and morbidity from infectious diseases worldwide. This paradox is explained by the lack of protection of this vaccine against pulmonary tuberculosis, the responsible form of transmission. New vaccination approaches effective against pulmonary forms of the disease are urgently needed, as they would have the greatest impact on disease transmission globally.
Our data clearly show that a change in the route of administration of BCG to mimic the natural route of infection could be a successful strategy to prevent pulmonary tuberculosis. Our results are in accordance with other authors showing equivalent data in different animal models, including guinea pigs and non-human primates (NHP) 6,9,12.
Remarkably, our unpublished data indicated that the volume of administration by the intranasal route is a critical step of the protocol. These results revealed that following intranasal delivery of 100 H37Rv bacteria resuspended in 10 μl (instead of 40 μl), we only recovered lung CFUs from around 20% of the animals (data not shown.
Importantly, one of the possible limitations of intranasal administration as a vaccine delivery route in clinic could be its proximity with the central nervous system13,14. In this regard, aerosol immunization might be safer as delivery route for pulmonary tuberculosis vaccines in humans.
This protocol describes a standardized methodology that can be adapted to other studies, as comparison of pulmonary vaccines, or different routes of pulmonary immunization, including aerosol.
Our data suggest that the analysis in parallel of protective efficacy and immune response, using lung samples from the same animal, could be a useful tool to identify biomarkers of protection. In this regard, our results reveal that lung IL17, but not IFNγ, seems to correlate with a better vaccine protective efficacy. These data highlight a possible role of IL17 in the protective response induced by intranasal BCG, which is in accordance with data reported by other authors using mucosal subunit TB vaccines 7,15. Our data also indicate that presence of IgA (both total and MTB-specific) in BAL samples correlates with protection conferred by intranasal BCG. Importantly, we described previously, in agreement with other works, that IL17 contributes to traslocation of IgA to respiratory airways and gut lumen.9,16,17
Disclosures
The authors have nothing to disclose.
Acknowledgements
This work was supported by "Spanish Ministry of Economy and Competitiveness" [grant number BIO2014-5258P], "European Commission" by the H2020 programs [grant numbers TBVAC2020 643381].
Materials
| Name | Company | Catalog Number | Comments |
| Middlebrook 7H9 broth | BD | 271310 | |
| Middlebrook ADC Enrichment | BD | 211887 | |
| Tween 80 | Scharlau | TW00800250 | |
| 3-mm diameter Glass Beads | Scharlau | 038-138003 | |
| Middlebrook 7H10 Agar | BD | 262710 | |
| 1-ml syringe 26GA 0.45x10 mm | BD | 301358 | |
| GentleMACS dissociator | Miltenyi Biotec | 130-093-235 | |
| C tubes | Miltenyi Biotec | 130-093-237 | |
| M tubes | Miltenyi Biotec | 130-093-236 | |
| Collagenase D | Roche | 11088882001 | |
| DNaseI | Applichem | A3778,0100 | |
| Falcon 70µm Cell Strainer | Corning | 352350 | |
| RPMI 1640 | Sigma | R0883 | |
| Red Blood Cell Lysing Buffer | Sigma | R7757 | |
| GlutaMAX Supplement | Gibco | 35050-061 | 100X concentrated |
| Penicillin-Streptomycin Solution | Sigma | P4333 | 100X concentrated |
| Fetal Calf Serum | Biological Industries | 04-001-1A | |
| 2-Mercaptoethanol | Sigma | M3148-25ML | |
| Scepter 2.0 Handheld Automated Cell Counter | Millipore | PHCC20040 | |
| Scepter Cell Counter Sensors, 40 µm | Millipore | PHCC40050 | |
| Mycobacterium Tuberculosis - Tuberculin PPD | Statens Serum Institut (SSI) | 2390 | |
| Mouse IFN-γ ELISA development kit | Mabtech | 3321-1H | |
| Mouse IL17A ELISA development kit | Mabtech | 3521-1H | |
| Brefeldin A | Sigma | B7651 | |
| FITC Rat Anti-Mouse CD4 | BD | 553047 | |
| BD Cytofix/Cytoperm Kit | BD | 555028 | |
| APC-Cy7 Rat Anti-mouse IL-17A | BD | 560821 | |
| APC Mouse Anti-mouse IFNg | BD | 554413 | |
| LACHRYMAL OLIVE LUER LOCK 0.60 x 30 mm. 23G x 1 1/4” | UNIMED | 27.134 | Used as trachea cannula for BAL |
| high-protein binding polystyrene flat-bottom 96-well plates MAXISORP | NUNC | 430341 | |
| Albumin, from bovine serum | Sigma | A4503 | |
| Goat Anti-Mouse IgA (α-chain specific)−Peroxidase antibody | Sigma | A4789 | |
| 3,3′,5,5′-Tetramethylbenzidine (TMB) | Sigma | T0440 | |
| MyTaq DNA Polymerase | Bioline | BIO-21107 | The kit Includes Buffer 5x |
References
- Zumla, A., et al. The WHO 2014 global tuberculosis report--further to go. Lancet Glob Health. 3 (1), e10-e12 (2015).
- Mangtani, P., et al. Protection by BCG vaccine against tuberculosis: a systematic review of randomized controlled trials. Clin Infect Dis. 58 (4), 470-480 (2014).
- Aguilo, N., et al. Pulmonary Mycobacterium bovis BCG vaccination confers dose-dependent superior protection compared to that of subcutaneous vaccination. Clin Vaccine Immunol. 21 (4), 594-597 (2014).
- Chen, L., Wang, J., Zganiacz, A., Xing, Z. Single intranasal mucosal Mycobacterium bovis BCG vaccination confers improved protection compared to subcutaneous vaccination against pulmonary tuberculosis. Infect Immun. 72 (1), 238-246 (2004).
- Giri, P. K., Verma, I., Khuller, G. K. Protective efficacy of intranasal vaccination with Mycobacterium bovis BCG against airway Mycobacterium tuberculosis challenge in mice. J Infect. 53 (5), 350-356 (2006).
- Lagranderie, M., et al. BCG-induced protection in guinea pigs vaccinated and challenged via the respiratory route. Tuber Lung Dis. 74 (1), 38-46 (1993).
- Gopal, R., et al. Interleukin-17-dependent CXCL13 mediates mucosal vaccine-induced immunity against tuberculosis. Mucosal Immunol. 6 (5), 972-984 (2013).
- Khader, S. A., et al. IL-23 and IL-17 in the establishment of protective pulmonary CD4+ T cell responses after vaccination and during Mycobacterium tuberculosis challenge. Nat Immunol. 8 (4), 369-377 (2007).
- Aguilo, N., et al. Pulmonary but Not Subcutaneous Delivery of BCG Vaccine Confers Protection to Tuberculosis-Susceptible Mice by an Interleukin 17-Dependent Mechanism. J Infect Dis. , (2015).
- Middlebrook, G., Cohn, M. L. Bacteriology of tuberculosis: laboratory methods. Am J Public Health Nations Health. 48 (7), 844-853 (1958).
- Brosch, R., et al. A new evolutionary scenario for the Mycobacterium tuberculosis complex. Proc Natl Acad Sci U S A. 99 (6), 3684-3689 (2002).
- Kaushal, D., et al. Mucosal vaccination with attenuated Mycobacterium tuberculosis induces strong central memory responses and protects against tuberculosis. Nat Commun. 6, 8533 (2015).
- Lochhead, J. J., Thorne, R. G. Intranasal delivery of biologics to the central nervous system. Adv Drug Deliv Rev. 64 (7), 614-628 (2012).
- Lochhead, J. J., Wolak, D. J., Pizzo, M. E., Thorne, R. G. Rapid transport within cerebral perivascular spaces underlies widespread tracer distribution in the brain after intranasal administration. J Cereb Blood Flow Metab. 35 (3), 371-381 (2015).
- Griffiths, K. L., et al. Cholera toxin enhances vaccine-induced protection against Mycobacterium tuberculosis challenge in mice. PLoS One. 8 (10), e78312 (2013).
- Hirota, K., et al. Plasticity of Th17 cells in Peyer's patches is responsible for the induction of T cell-dependent IgA responses. Nat Immunol. 14 (4), 372-379 (2013).
- Jaffar, Z., Ferrini, M. E., Herritt, L. A., Roberts, K. Cutting edge: lung mucosal Th17-mediated responses induce polymeric Ig receptor expression by the airway epithelium and elevate secretory IgA levels. J Immunol. 182 (8), 4507-4511 (2009).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved