Method Article
زرع الليفين جل في الرئة ماوس لدراسة الأوعية الدموية الرئة محددة
In This Article
Summary
Recapitulation of the organ-specific microenvironment, which stimulates local angiogenesis, is indispensable for successful regeneration of damaged tissues. This report demonstrates a novel method to implant fibrin gels on the lung surface of living mouse in order to explore how the lung-specific microenvironment modulates angiogenesis and alveolar regeneration in adult mouse.
Abstract
جعلت تقدما كبيرا مؤخرا في تقنيات أبحاث الخلايا الجذعية والهندسة الحيوية تقدما كبيرا في استخدام المواد الحيوية لتجديد وإصلاح الأضرار في أنسجة بسيطة في مجالات تقويم العظام واللثة. ومع ذلك، فإن محاولات لتجديد هياكل ومهام أكثر تعقيدا ثلاثية الأبعاد (3D) أجهزة مثل الرئتين لم تكن ناجحة جدا لأن العمليات البيولوجية للتجديد الجهاز لم يتم استكشافها بشكل جيد. لقد أصبح من الواضح أن الأوعية الدموية، وتشكيل الأوعية الدموية الجديدة، ويلعب دورا رئيسيا في تجديد الجهاز. شكلت حديثا vasculatures تقديم ليس فقط الأكسجين والمغذيات ومكونات الخلية المختلفة المطلوبة لتجديد الجهاز ولكن أيضا توفير إشارات مفيدة إلى الأنسجة المحلية تجديد. لذلك، لتجديد الرئتين في البالغين بنجاح، فمن الضروري أن ألخص في microenvironments الرئة المحددة التي الأوعية الدموية محركات تجديد أنسجة الرئة المحلية. وإن كانت المشاركةnventional في الجسم الحي المقايسات الأوعية الدموية، مثل زرع تحت الجلد من المصفوفة خارج الخلية (ECM) الغنية الهلاميات المائية (على سبيل المثال، الفيبرين أو الكولاجين والمواد الهلامية أو Matrigel - خليط من البروتين ECM يفرز من قبل خلايا Engelbreth-هولم-سرب الماوس ساركوما)، وتستخدم على نطاق واسع لاستكشاف الآليات العامة من الأوعية الدموية، الأوعية الدموية في الرئة محددة لم تميزت جيدا لأن طرق لزرع مثلي من المواد الحيوية في الرئة لم راسخة. والهدف من هذا البروتوكول هو إدخال طريقة فريدة من نوعها لزرع هلام الليفين على سطح الرئة المعيشة الماوس الكبار، والسماح لخلاصة الناجح لاستضافة المستمدة الرئة الأوعية الدموية داخل الجل. هذا النهج يمكن الباحثين لاستكشاف الآليات التي المكروية الرئة محددة تسيطر الأوعية الدموية وتجديد السنخية في كل الظروف العادية والمرضية. ومنذ إطلاق المواد الحيوية مزروع وتوريد إشارات الفيزيائية والكيميائية إلى l المجاورالأنسجة اونغ، زرع هذه المواد الحيوية على الرئة المريضة يمكن أن يحتمل تطبيع الأنسجة المريضة المجاورة، وتمكين الباحثين لتطوير مناهج علاجية جديدة لأنواع مختلفة من أمراض الرئة.
Introduction
ويتمثل الهدف العام من هذا البروتوكول هو تقديم طريقة لزرع هلام الليفين على سطح الرئة من الماوس الكبار، والذي يسمح للباحثين لتوصيف الآليات الجزيئية من الأوعية الدموية في الرئة والتنمية السنخية، وللاستفادة من هذه المعرفة من أجل تطوير مواد قادرة بيوميمتيك من تلخص الفسيولوجية الأوعية الدموية في الرئة وتشكيل السنخية لعلاج أمراض الرئة المختلفة.
أكثر من 35 مليون أميركي يعانون من أمراض الرئة المزمنة بما فيها مرض الانسداد الرئوي المزمن والتليف الرئوي. هذه المرضى الذين لديهم طويلة الأمد أعراض تنفسية مزمنة مثل ضيق في التنفس، وضيق الصدر، والسعال المزعجة، والتعب، التي تعوق بشكل كبير الحياة اليومية 1-3. وعلى الرغم من كمية كبيرة من الجهد لتطوير علاجات فعالة لهذه الأمراض الرئة، وحاليا لا يوجد علاج. وبالتالي، ونوعية الحياة لهؤلاء المرضى والفقراء والاقتصادية والتكاليف البشرية ومرحباGH 4-7. حاليا، زرع الرئة هو السبيل الوحيد لإنقاذ المرضى الذين يعانون من أمراض الرئة المزمنة في نهاية المرحلة. ومع ذلك، بسبب نقص المتبرعين زرع، وارتفاع تكلفة، ومضاعفات خطيرة، وانخفاض معدل البقاء على قيد الحياة 8-11، زرع ليس النهج الأمثل. وقد مكن التقدم السريع الذي حدث مؤخرا في تقنيات هندسة الأنسجة الباحثون إلى مهندس بيولوجي الرئة التي تزرع في الجسم عن طريق إعادة إسكانها الرئة كلها decellularized مع أنواع مختلفة من الخلايا الاصلية أو الجذعية المحفزة (آي بي إس) خلايا 12،13. ومع ذلك، فإن هذه الرئتين الهندسة البيولوجية وظيفية في الحيوانات المضيفة فقط لعدة ساعات بعد زرع 12،14،15. استخدام المواد الحيوية لتجديد الهياكل وظائف معقدة من الرئتين كما تم ناجحة إلى حد ما. قد يكون هذا بسبب العمليات البيولوجية الرئيسية التي تحكم الكبار تجديد الرئة لم تستكشف جيدا. في الرئة، وتشكيل نظام الأوعية الدموية هي واحدة من أقدم وأهم الأحداث الدوريتطوير نانوغرام وتجديد 16-21. شكلت حديثا vasculatures في الرئة يتم تسليم سوى الأكسجين والمغذيات ومكونات الخلية المختلفة اللازمة لتشكيل الجهاز، ولكن أيضا توفير إشارات التنظيمية مفيدة للخلايا المحيطة 22-25. وهكذا، الأوعية الدموية يلعب الأدوار الرئيسية في alveolarization التجدد في الرئتين الكبار 24،26،27. وبالإضافة إلى ذلك، يساهم الأوعية الدموية حررت لأمراض الرئة المزمنة مثل مرض الانسداد الرئوي المزمن (COPD) 28، وخلل التنسج القصبي الرئوي (برميل يوميا) 21-23، والتليف الرئوي 29. وهكذا، لوضع استراتيجيات أكثر فعالية لهندسة الرئتين أو علاج أمراض الرئة المزمنة، فمن الضروري لفهم الآليات الأساسية لتكوين الأوعية الدموية في الرئة محددة.
يعرض كل جهاز الخواص الميكانيكية والكيميائية فريدة من نوعها، والتي قد تختلف بين الظروف الفسيولوجية والمرضية 30-33. هذه microenviron جهاز محددالإدلاء بالبيانات تنظم السلوكيات خلية البطانية والانسجام في تشكيل شبكة الأوعية الدموية في الجهاز بطريقة محددة 24،34-36. وهكذا، لوضع استراتيجيات أكثر كفاءة لتجديد الرئة، والآلية الكامنة وراء تكوين الأوعية الدموية في الرئة محددة يجب أن يكون مفهوما. بينما التقليدية في الجسم الحي المقايسات الأوعية الدموية تحت الجلد مثل هيدروجيل غرس وقد استخدمت على نطاق واسع للأبحاث الأوعية الدموية 37-39، وتلك الأساليب لا ألخص الأوعية الدموية جهاز معين. مؤخرا، تم تطوير طريقة رواية لزرع Matrigel في قالب مرن على الرئة الماوس وأظهرت لتجنيد بنجاح الأوعية الدموية والخلايا الظهارية الرئة في المواد الهلامية 22. وهذا النهج الفريد تسمح للباحثين لاستكشاف آلية تكوين الأوعية الدموية في الرئة محددة وكذلك التفاعلات بين الأوعية الدموية وخلايا الرئة غير الوعائية في الظروف الفسيولوجية والمرضية. منذ 1) Matrigel ليست مناسبة للالتطبيق السريري. 2) هالعفن lastic المستخدمة للادلاء الجل قد تؤثر على التفاعلات بين الهلاميات المائية وأنسجة الرئة المضيفة و3) قالب مرن على الرئة يحتمل أن يسبب ضعف وظيفة الرئة وألم أثناء التنفس، كنهج ذات الصلة أكثر سريريا، والفيبرين مصفوفة 3D التي تحتوي على العوامل المولدة للأوعية (عامل نمو بطانة الأوعية الدموية (VEGF) / الأساسية عامل نمو الخلايا الليفية (bFGF)) تم زرعها على الرئة الماوس دون الصب في قالب مرن، وقد لخص بنجاح المضيف المستمدة الرئة الأوعية الدموية. هلام الليفين، الألياف البوليمر المتولدة من-المشقوق ثرومبين الفيبرينوجين، ومن المعروف إلى اعتراض مجموعة متنوعة من العوامل عائية مثل bFGF وVEGF لتسريع تكوين الأوعية الدموية في الجسم الحي 40،41. بسبب قدرته على التجدد والطبيعة القابلة للتحلل 42، ويستخدم على نطاق واسع جل الليفين في مجال هندسة الأنسجة.
يقدم هذا المقال رواية ونهجا فريدا لزرع هلام الليفين على سطح الرئة من أدول الذين يعيشونيوضح ر الماوس والتي تستضيف المستمدة الرئة الأوعية الدموية وتلخيصها داخل المواد الهلامية في الجسم الحي. هذه الطريقة، والتي تمكن الباحثين لدراسة الأوعية الدموية في الرئة محددة، من المرجح أن يؤدي إلى تطوير طرق علاجية جديدة لأنواع مختلفة من أمراض الرئة ودفع كثيرا من جهود لتجديد الرئة الكبار بنجاح.
Protocol
ملاحظة: تم تنفيذ في الجسم الحي دراسة أجريت على الحيوانات وفقا صارم مع التوصيات الواردة في دليل لرعاية واستخدام الحيوانات المختبرية من المعاهد الوطنية للصحة. وجرى استعراض البروتوكول والموافقة عليها من قبل لجنة رعاية الحيوان واستخدام مستشفى بوسطن للأطفال (أرقام البروتوكول: 13-10-2526R، 14-02-2568R). جميع الأدوية المستخدمة في هذا البروتوكول هي الصف الصيدلانية وأعدت هذه الأدوية تحت ظروف معقمة.
1. إعداد الليفين جل
- تحضير هلام الليفين الذي يحتوي VEGF وbFGF.
- حلول الأسهم ذوبان الجليد من الفيبرينوجين والثرومبين التي يتم تخزينها في -80 درجة مئوية إلى درجة حرارة الغرفة (25 درجة مئوية).
- إضافة الثرومبين (تركيز النهائي: 2.5 U / مل)، CaCl 2 (تركيز النهائي: 45 مم)، VEGF (تركيز النهائي: 0-100 نانوغرام / مل)، وbFGF (تركيز النهائي: 0-100 نانوغرام / مل) إلى الفيبرينوجين الحل (تركيز النهائي: 12.5 ملغ / مل في 0.9٪ sodiuم محلول كلوريد 43-45) في أنبوب 1.5 مل.
- مزيج من قبل pipetting بلطف.
- ماصة بلطف 200 ميكرولتر من الخليط على طبق بلاستيكية معقمة بطريقة الإفلات من الحكمة استخدام P200 ماصة.
- احتضان قطرات عند 37 درجة مئوية لمدة 30-60 دقيقة حتى يصلب.
ملاحظة: يمكن الاحتفاظ هلام طدت في طبق من البلاستيك مختوم في درجة حرارة الغرفة (25 درجة مئوية) لعدة ساعات قبل الزرع (الشكل 1A).
- تقليم هلام الليفين إلى حوالي 3 × 3 × 3 مم باستخدام مكعبات مقص جراحي صغيرة قبل الزرع.
2. إعداد ماوس
- تخدير الماوس الكبار (8-12 أسابيع) من قبل داخل الصفاق (IP) حقن الكيتامين (100 ملغ / كلغ) وزيلازين (10 ملغ / كلغ) وتأكيد أن الفأر هو تخدير بشكل كاف عن طريق معسر إصبع القدم من الفأرة.
- استخدام البيطري مرهم على العينين من الماوس لمنع جفاف أثناء التجربة.
- حلاقة فوص على الجانب الأيسر من القفص الصدري من الفأرة.
- أداء التنبيب داخل الرغامى من الفأرة.
- ضع الماوس على التنبيب يقف الزاوية عند 70 درجة وعقد الماوس في المكان التي ربط القواطع العلوية على الشريط المطاطي صغيرة تقع في الجزء العلوي من هذا الموقف.
- التراجع بلطف اللسان لجانب واحد باستخدام ملقط حادة.
- تصور الحنجرة بمساعدة المجهر معقوفة إضاءة الألياف الضوئية.
- إدراج القصبة الهوائية قسطرة مرنة (21 G) في القصبة الهوائية.
- تأكد من أن الماوس يتنفس من تلقاء أنفسهم بطريقة سلسة (العادية 100-150 الأنفاس / دقيقة، لا تنفس متناقض أو الضحلة).
- ضع الماوس في موقف المعرضة تحت المجهر تشريح.
- ميكانيكيا تهوية الماوس باستخدام جهاز التنفس الصناعي القوارض (150 الأنفاس / دقيقة و 7 مل / كغ حجم المد والجزر).
- عدد الأضلاع لتحديد مساحة وربي بين ال 4 و 5 ال الصدري.
- إنشاء حقل معقمة على المنطقة بذ محو بدقة أسفل مع الكحول وبوفيدون اليود. تغطية الجراحي الميداني على نحو كاف مع ثنى الجراحية المعقمة.
3. جراحة ماوس
- بعد حقن المحلي من 0.25٪ بوبيفاكايين (200 ميكرولتر) في الجلد، وجعل شق الجلد عرضية (حوالي 1 سم طول) عبر الفضاء وربي باستخدام مقص تشريح.
- بعد حقن 0.25٪ بوبيفاكايين (200 ميكرولتر) في العضلات الوربية، وجعل شق العضلات بين ال 4 و 5 عشر ضلع باستخدام مقص صغير غرامة.
- إدراج ضام تشريح بين الأضلاع لتصور كامل الرئة اليسرى.
- كشط منطقة صغيرة (1 × 1 مم مربع) من غشاء الجنب الحشوية من مركز الرئة اليسرى باستخدام ملقط غرامة.
- تطبيق ضغط لطيف على المنطقة باستخدام قطعة من القطن المعقمة حتى يتم التحكم تماما نزيف وتسرب الهواء.
- ضع كمية صغيرة من خليط جديد من الفيبرينوجين / الثرومبين (الليفين الغراء) (الخطوة 1.1.2 20 & #181؛ ل) على المنطقة باستخدام P200 ماصة.
- وضع بلطف واحدة هلام الليفين (الخطوة 1.2) باستخدام ملقط صغير فوق المنطقة (الشكل 1B).
- تأكيد أن الجل هو ثابت بشكل جيد على المنطقة خلال الحركات التنفسية في الرئة.
- تأكد من أن هناك لا تسرب الهواء هائل ولا نزيف من الرئة.
- شقوق وثيقة (العضلات وطبقات الجلد) مع خياطة للامتصاص، والتي لا بد من إزالتها.
- نضح التجويف الصدري باستخدام إبرة 27 G و 1 مل حقنة لمنع استرواح الصدر.
- إنهاء التهوية الميكانيكية.
4. ماوس الانتعاش
- تأكد من أن الماوس يتنفس من تلقاء أنفسهم بطريقة سلسة (100-150 الأنفاس العادية / دقيقة، لا تنفس متناقض أو الضحلة).
- IP حقن 1 مل من قبل تحسنت بنسبة 0.9٪ كلوريد الصوديوم لمنع الجفاف.
- السماح الماوس لاستعادة على تعميم سادة المياه الدافئة.
- إزالة endotracheآل أنبوب بعد التأكد من أن الفأر لديه مستقر التنفس.
- حقن ميلوكسيكام (5 ملغ / كغ، والحقن تحت الجلد (SC)، لمدة 3 أيام كما مسكن بعد العملية الجراحية.
- رصد تحركات الماوس بعناية في ما لا يقل عن 15 دقيقة فترات حتى يتم القصية (قادرة على لفة على المعدة، وتبقى في وضع مستقيم) واعية.
- بعد الشفاء، والعودة الماوس إلى قفص جديد المعزولة من الفئران من دون جراحة.
- رصد موقع الجراحية لعلامات العدوى (احمرار، تورم والتفريغ)، وظائف البيولوجية الأساسية الحيوان (الغذاء والماء المدخول، والتبول، التبرز، الزيادة في وزن الجسم)، وكذلك العلامات السريرية الشدة (انتصاب الشعر، وانخفاض تنقل) يوميا بعد إجراء العمليات الجراحية.
5. حصاد الرئة
- بعد 7 إلى 30 يوما الزرع، الموت ببطء الماوس باستخدام CO 2 عبر مصدر للغاز المضغوط.
- إجراء شق بين غيض من عملية سيفي الشكل والقصيةالشق (القص متوسط) والحصاد الرئة كاملة مع هلام المزروع للتحليل النسيجي والبيوكيميائية عن طريق قطع القصبة الهوائية وتشريح كافة الاتصالات إلى القلب والرئتين والقصبة الهوائية.
- إصلاح هلام المزروع مع الرئة مع 4٪ محلول بارافورمالدهيد بين عشية وضحاها في 4 درجة مئوية، تضمين في أكتوبر المجمع، واتخاذ خطوة أقسام المسلسل من 30 ميكرون سمك.
- أداء النسيجية (الهيماتوكسيلين ويوزين تلطيخ) والتحاليل المناعية (علامة البطانية: CD31، علامة الظهارية: aquaporin (AQP) 5 والسطحي البروتين (SP) -B) باستخدام متحد البؤر المجهر 22،37،40.
- تجميع أكوام من المقاطع البصرية (30 ميكرون سميكة) لتشكيل صور ثلاثية الأبعاد للالبطانية الرئة والخلايا الظهارية باستخدام صورة 3D تحليل البرمجيات 37.
- تحديد المناطق المتوقع من الأوعية الدموية التي شكلت حديثا باستخدام صورة برامج التحليل 46.
النتائج
لفحص ما إذا كان لخص المضيف المستمدة الرئة تشكيل الأوعية الدموية داخل الحيوية وزرع على الرئة، والمواد الهلامية الليفين تستكمل مع رئيسي عائية العوامل VEGF وbFGF (0، 10 و 100 نانوغرام / مل لكل منهما) تم زرعها على سطح يعيشون الرئتين الماوس كما وذكرت باستخدام Matrigel 22. ملفقة المواد الهلامية الليفين 47 التي تحتوي على هذه عوامل النمو عائية كما هو مبين في الشكل 1A. بعد بضع الصدر، تم كشط مساحة صغيرة من سطح الرئة اليسرى باستخدام ملقط وكان مزروع هلام الليفين ملفقة على الرئة من الفأرة الكبار باستخدام كمية صغيرة من الغراء الليفين، وهو FDA المعتمدة والمستخدمة على نطاق واسع باعتبارها تسرب فعالة لوقف تسرب الهواء والحد من نزيف في جراحة الرئة 48،49 (الشكل 1B). تعافت معظم الفئران دون أعراض تنفسية شديدة (على سبيل المثال، استرواح الصدر، ضيق في التنفس). بعد سبعة أيام الزرع، والموت الرحيم الفئران وكانت الرئتين harveSTED. تأسست زرع هلام الليفين في الرئة المضيف بعد 7 أيام زرع (الشكل 1C). وقد أظهرت إعادة الإعمار 3D من الصور مضان مبائر أن المستمدة المضيف CD31 إيجابي الخلايا البطانية تشكيل شبكات الأوعية الدموية داخل الهلام بعد 7 أيام غرس في VEGF / bFGF تعتمد على الجرعة الطريقة (الشكل 2A، ج). تم تجنيدهم من النوع الأول (AQP5 إيجابي) والنوع الثاني (SP-B الإيجابية) خلايا الظهارية الرئة أيضا على طول الأوعية الدموية التي شكلت حديثا داخل المواد الهلامية التي تستكمل مع تركيزات أعلى من VEGF وbFGF (كل 100 نانوغرام / مل) (الشكل 2A) . كشفت H & E تلطيخ أقسام النسيجية أن أنواع أخرى من الخلايا المضيفة هاجر أيضا إلى هلام 7 أيام بعد زرع (الشكل 2B). وتشير هذه النتائج إلى أن المضيف المستمدة الرئة شبكات الأوعية الدموية التجدد هي التي شيدت بنجاح داخل المواد الهلامية الليفين التي تستكمل مع العوامل المولدة للأوعية وزرعها على سطح مذكرة التفاهم الكبارحد ذاته الرئة.
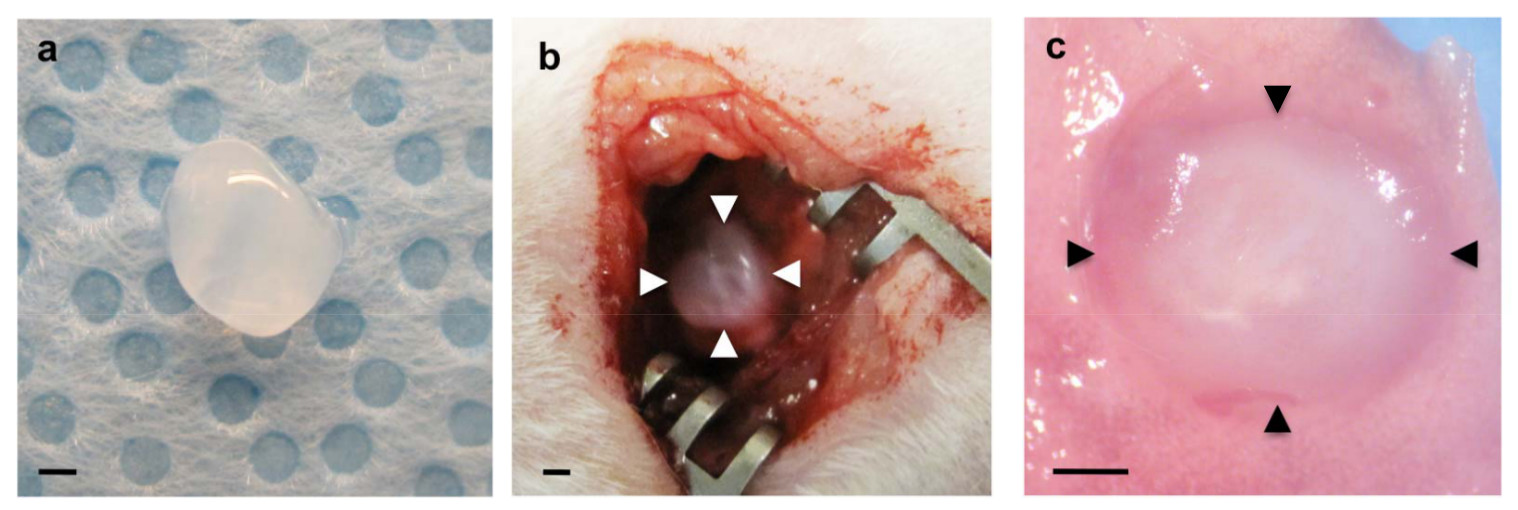
الشكل (1): (أ) هلام الليفين أعدت قبل الزرع (ب) هلام الليفين زرعها على غشاء الجنب الحشوية كشط من الرئة اليسرى (السهام) (ج) مزروع هلام الليفين (السهام) دمجها في الرئة المضيف بعد 7 أيام الزرع. الحانات مقياس 1 مم.
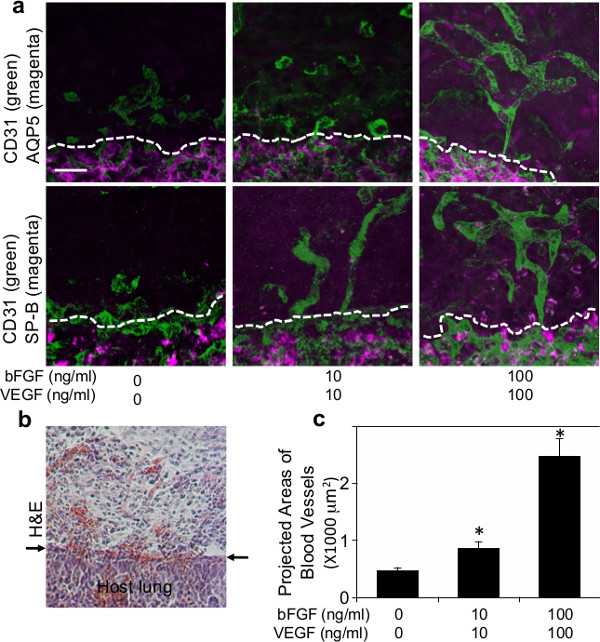
الشكل 2: (أ) الميكروسكوب الإسفار يظهر تشكيل شبكات الأوعية الدموية (CD31 إيجابية؛ الأخضر) ونوع تجنيد I (AQP5-إيجابية؛ أرجواني) أو من النوع الثاني (SP-B إيجابية؛ أرجواني) خلايا الظهارية الرئة داخل هلام الليفين تستكمل مع تركيزات مختلفة من VEGF وbFGF (0، 10 و 100 نانوغرام / مل لكل منهما) بعد 7 أيام الزرع. الخطوط المتقطعة تشير إلى واجهة بين زرع هلام الليفين والرئة المضيف. شريط مقياس: 20 ميكرون (ب) صورة مجهرية الخفيفة من H & E تلطيخ تظهر تسلل الخلايا المضيفة في هلام الليفين بعد 7 أيام الزرع. السهام تشير إلى واجهة بين جل والرئة المضيف. شريط مقياس: 20 ميكرون (ج) رسم بياني يبين المناطق المتوقعة من الأوعية الدموية التي شكلت حديثا في المواد الهلامية الليفين التي تستكمل مع تركيزات مختلفة من VEGF وbFGF (0، 10 و 100 نانوغرام / مل لكل منهما) بعد 7 أيام الزرع.
Discussion
يقدم هذا المقال طريقة جديدة لزرع المواد الحيوية على سطح الرئة المعيشة الماوس الكبار. مع هذا النظام، ولخص الأوعية الدموية المستمدة الرئة في استضافة بنجاح داخل المادة. هذا النظام يسمح للباحثين لاستكشاف الحديث المتبادل بين الخلايا البطانية، وخلايا أخرى (على سبيل المثال، الخلايا الظهارية، خلايا اللحمة المتوسطة، الخلايا المناعية) ومختلف مكونات ECM المطلوبة لتكوين الأوعية الدموية المحلي 50-53 وتجديد السنخية 24،54. وعلى الرغم التقليدي في الجسم الحي هيدروجيل تحت الجلد غرس وقد استخدم على نطاق واسع للأبحاث الأوعية الدموية 37-39، وتلك الأساليب لا ألخص الأوعية الدموية جهاز معين. هذا النظام، الذي هو مزروع هيدروجيل مباشرة على سطح الرئة، سيمكن الباحثين لاستكشاف أدوار المكروية الرئة محددة في الأوعية الدموية وتجديد السنخية في الرئة الماوس الكبار. يمكن أن تكون ملفقة هذه المواد الهلامية من مختلف-ECM الغنية biomateريال (على سبيل المثال، الكولاجين، fibrins) التي يمكن أن تستكمل مع عوامل مختلفة الكيميائية (مثل، والعوامل المولدة للأوعية، وعوامل النمو) 55،56، الخلايا الاصلية و / أو خلايا الجذع. بالإضافة إلى العوامل الكيميائية، القوى الميكانيكية أيضا التحكم في الأوعية الدموية 23،37. صلابة من التغييرات هلام الليفين في الفيبرينوجين تعتمد على التركيز نحو 57 والتلاعب تركيز الفيبرينوجين قد تؤثر على الأوعية الدموية ليس فقط من خلال إشارات كيميائية ولكن أيضا من خلال العظة المادية 58،59. لذلك، قد يحتاج الخصائص الفيزيائية من المواد الهلامية الليفين إلى أن يكون الأمثل بعناية لألخص الفسيولوجية الأوعية الدموية جهاز محدد في المستقبل. التئام الجروح بعد كشط غشاء الجنب الحشوية أيضا ينتج جلطة الفيبرين الذاتية، والتي تشمل أنواع مختلفة من الخلايا المضيفة ويعزز عملية الشفاء وتجديد الأنسجة. هذه الجلطة الطبيعية قد تتفاعل مع هلام الليفين مزروع خارجيا، وبالتالي السيطرة على القسطرةنشأة في هلام المزروع. Fluorescently الفيبرينوجين المسمى قد تمكن الباحثين على التمييز بين جلطة الفيبرين الطبيعية وزرع هلام الليفين واستكشاف هذه الآليات. على الرغم من أن هذا هو وسيلة قوية لتوصيف الأوعية الدموية في الرئتين الماوس الكبار، وتطبيق لدراسة نمو الرئة وأمراض في الفئران حديثي الولادة من شأنه التحديات التقنية الحالية على الأرجح.
والهدف النهائي من هذه الدراسة هو لتجنيد الأوعية الدموية وظيفية في المواد الهلامية الليفين وزرع على الرئتين المريضة واستخدام مصفوفة كجهاز طبي لاستعادة الهياكل الرئة وظيفية. ينبغي استكشاف الاتصالات الممكنة بين الخلايا المضيفة والأوعية الدموية والهياكل السنخية داخل المواد الهلامية، وكذلك وظيفة من هذه الهياكل في التجارب المستقبلية. منذ انخفاض مستويات VEGF في الرئتين في المرضى الذين يعانون برميل يوميا 60 وانتفاخ الرئة 61، مضيفا VEGF إلى مصفوفة قد يحسن توظيف الأوعية الدموية في impl مصفوفةanted على هذه الرئتين المريضة. تختلف الخواص الميكانيكية أيضا بين الرئتين السليمة والمريضة 23،62. على سبيل المثال، التعبير عن مصفوفة metalloproteinases والليزيل أوكسيديز، التي تتحكم في تدهور ويشابك من الكولاجين، على التوالي، يتم تغيير في أمراض الرئة المختلفة بما في ذلك مرض الانسداد الرئوي المزمن والتليف الرئوي 63-67. في الرئتين المريضة، تنضب الأنساب معينة من الأسلاف لالبطانية الرئة والخلايا الظهارية 68. وهكذا، والتلاعب هذه العوامل (عوامل عائية، موبينيل، ECM صلابة) أو زرع المواد الهلامية الليفين تستكمل مع الخلايا الاصلية و69 المرجح أن تؤدي إلى تشكيل الأوعية الدموية وظيفية داخل المصفوفة واستعادة وظيفة الرئة في مختلف الحالات المرضية. منذ العوامل الكيميائية يمكن أن تستكمل داخل المواد الهلامية الليفين لتعديل تكوين الأوعية الدموية المحلية، وهذا النظام يمكن أيضا أن تستخدم استكشاف العظة البيئية المحددة التي قد تطبيع الرئتين المريضة في أمراض الرئة المزمنة.
وباختصار، يقدم هذا المقالة طريقة لزرع الفيبرين هيدروجيل على سطح الرئة من الماوس الحية، التي تمكن الباحثين من تحديد خصائص الأوعية الدموية في الرئة محددة في الجسم الحي. تعديل عوامل مختلفة (على سبيل المثال، بالطبع الوقت، وتركيزات ومجموعات من العوامل المولدة للأوعية، وأنواع مختلفة من الهلاميات المائية، والخصائص الفيزيائية من الهلاميات المائية) في هذا النظام، وسوف تكشف النقاب عن آليات الأوعية الدموية وتجديد في الرئة. وبالتالي، فإن هذا النظام تتقدم بشكل ملحوظ المعرفة العلمية لعلم الأحياء الأوعية الدموية الأساسي، وهندسة الأنسجة، وكذلك الطب الرئوي.
Disclosures
The authors declare that they have no competing financial interests.
Acknowledgements
وأيد هذا العمل من جانب صناديق من جمعية القلب الأمريكية (AM)، وزارة الدفاع الأمريكية (BC074986)، ومستشفى كلية زمالة التطوير الوظيفي بوسطن للطفولة (TM، AM). الكتاب أشكر أماندا جيانغ جيانغ واليزابيث للحصول على المساعدة الفنية.
Materials
| Name | Company | Catalog Number | Comments |
| Fibrinogen from human placenta | Sigma | F4883 | For fabrication of fibrin gel |
| Thrombin from bovine plasma | Sigma | T9549 | For fabrication of fibrin gel |
| Recombinant mouse VEGF 164 | R&D | 493-MV | For supplementation to fibrin gel |
| Recombinant mouse bFGF | R&D | 3139-FB | For supplementation to fibrin gel |
| Rodent Intubation Stand | Braintree Scientific INC | RIS 100 | For intubation |
| Fiber-Optic Light Source | Fisher Scientific | 12-565-35 | For intubation |
| 21 G Elastic catheter | B.Braun | 4251652-02 | For intubation |
| MiniVent Ventilator | Harvard Apparatus | CGS-8009 | For ventilation |
| Stemi DV4 Steromicroscope | Fisher Scientific | 12-070-515 | For surgey |
| Absobable suture | Ethicon | PDP304 | Surgical suture |
| Antibody against CD31 | BD Biosciences | 553370 | Immunohistochemistry |
| Antibody against AQP5 | Abcam | AB78486 | Immunohistochemistry |
| Antibody against SP-B | Abcam | AB40876 | Immunohistochemistry |
References
- Donaldson, G. C., Seemungal, T. A., Bhowmik, A., Wedzicha, J. A. Relationship between exacerbation frequency and lung function decline in chronic obstructive pulmonary disease. Thorax. 57, 847-852 (2002).
- Lopez-Campos, J. L., Calero, C., Quintana-Gallego, E. Symptom variability in COPD: a narrative review. Int J Chron Obstruct Pulmon Dis. 8, 231-238 (2013).
- Ley, B., Collard, H. R., King, T. E. Clinical course and prediction of survival in idiopathic pulmonary fibrosis. Am J Respir Crit Care Med. 183, 431-440 (2011).
- Ferrer, M., et al. Chronic obstructive pulmonary disease stage and health-related quality of life. The Quality of Life of Chronic Obstructive Pulmonary Disease Study Group. Ann Intern Med. 127, 1072-1079 (1997).
- Reardon, J. Z., Lareau, S. C., ZuWallack, R. Functional status and quality of life in chronic obstructive pulmonary disease. Am J Med. 119, 32-37 (2006).
- De Vries, J., Kessels, B. L., Drent, M. Quality of life of idiopathic pulmonary fibrosis patients. Eur Respir J. 17, 954-961 (2001).
- Sullivan, S. D., Ramsey, S. D., Lee, T. A. The economic burden of COPD. Chest. 117, 5S-9S (2000).
- Orens, J. B., Garrity, E. R. General overview of lung transplantation and review of organ allocation. Proc Am Thorac Soc. 6, 13-19 (2009).
- Benden, C. Specific aspects of children and adolescents undergoing lung transplantation. Curr Opin Organ Transplant. 17, 509-514 (2012).
- Lyu, D. M., Zamora, M. R. Medical complications of lung transplantation. Proc Am Thorac Soc. 6, 101-107 (2009).
- Trulock, E. P., et al. Registry of the International Society for Heart and Lung Transplantation: twenty-fourth official adult lung and heart-lung transplantation report-2007. J Heart Lung Transplant. 26, 782-795 (2007).
- Weiss, D. J. Current status of stem cells and regenerative medicine in lung biology and diseases. Stem Cells. 32, 16-25 (2013).
- Ghaedi, M., et al. Human iPS cell-derived alveolar epithelium repopulates lung extracellular matrix. J Clin Invest. 123, 4950-4962 (2013).
- Ott, H. C., et al. Regeneration and orthotopic transplantation of a bioartificial lung. Nat Med. 16, 927-933 (2010).
- Petersen, T. H., et al. Tissue-engineered lungs for in vivo implantation. Science. 329, 538-541 (2010).
- Tuyl, M., et al. Angiogenic factors stimulate tubular branching morphogenesis of sonic hedgehog-deficient lungs. Dev Biol. 303, 514-526 (2007).
- Galambos, C., deMello, D. E. Molecular mechanisms of pulmonary vascular development. Pediatr Dev Pathol. 10, 1-17 (2007).
- McGrath-Morrow, S. A., et al. Vascular endothelial growth factor receptor 2 blockade disrupts postnatal lung development. Am J Respir Cell Mol Biol. 32, 420-427 (2005).
- White, A. C., Lavine, K. J., Ornitz, D. M. FGF9 and SHH regulate mesenchymal Vegfa expression and development of the pulmonary capillary network. Development. 134, 3743-3752 (2007).
- Zhao, L., Wang, K., Ferrara, N., Vu, T. H. Vascular endothelial growth factor co-ordinates proper development of lung epithelium and vasculature. Mech Dev. 122, 877-886 (2005).
- Stenmark, K. R., Abman, S. H. Lung vascular development: implications for the pathogenesis of bronchopulmonary dysplasia. Annu Rev Physiol. 67, 623-661 (2005).
- Mammoto, T., et al. LRP5 Regulates Development of Lung Microvessels and Alveoli through the Angiopoietin-Tie2 Pathway. PLoS ONE. 7, e41596(2012).
- Mammoto, T., Jiang, E., Jiang, A., Mammoto, A. ECM structure and tissue stiffness control postnatal lung development through the LRP5-Tie2 signaling system. American Journal of Respiratory Cell and Molecular Biology. 49, 1009-1018 (2013).
- Ding, B. S., et al. Endothelial-derived angiocrine signals induce and sustain regenerative lung alveolarization. Cell. 147, 539-553 (2011).
- Crivellato, E. The role of angiogenic growth factors in organogenesis. Int J Dev Biol. 55, 365-375 (2011).
- Sakurai, M. K., et al. Vascular endothelial growth factor accelerates compensatory lung growth after unilateral pneumonectomy. Am J Physiol Lung Cell Mol Physiol. 292, 742-747 (2007).
- Panigrahy, D., et al. Epoxyeicosanoids promote organ and tissue regeneration. Proc Natl Acad Sci U S A. 110, 13528-13533 (2013).
- Voelkel, N. F., Douglas, I. S., Nicolls, M. Angiogenesis in chronic lung disease. Chest. 131, 874-879 (2007).
- Hanumegowda, C., Farkas, L., Kolb, M. Angiogenesis in pulmonary fibrosis: too much or not enough. Chest. 142, 200-207 (2012).
- Levental, K. R., et al. Matrix crosslinking forces tumor progression by enhancing integrin signaling. Cell. 139, 891-906 (2009).
- Mammoto, A., Mammoto, T., Ingber, D. E. Mechanosensitive mechanisms in transcriptional regulation. J Cell Sci. 125, 3061-3073 (2012).
- Westermann, D., et al. Role of left ventricular stiffness in heart failure with normal ejection fraction. Circulation. 117, 2051-2060 (2008).
- Merchante, N., et al. Liver stiffness predicts clinical outcome in human immunodeficiency virus/hepatitis C virus-coinfected patients with compensated liver cirrhosis. Hepatology. 56, 228-238 (2012).
- Ding, B. S., et al. Inductive angiocrine signals from sinusoidal endothelium are required for liver regeneration. Nature. 468, 310-315 (2010).
- Fidler, I. J. Angiogenic heterogeneity: regulation of neoplastic angiogenesis by the organ microenvironment. J Natl Cancer Inst. 93, 1040-1041 (2001).
- Folkman, J. How is blood vessel growth regulated in normal and neoplastic tissue? G.H.A. Clowes memorial Award lecture. Cancer Res. 46, 467-473 (1986).
- Mammoto, A., et al. A mechanosensitive transcriptional mechanism that controls angiogenesis. Nature. 457, 1103-1108 (2009).
- Malinda, K. M. In vivo matrigel migration and angiogenesis assay. Methods Mol Biol. 467, 287-294 (2009).
- Norrby, K. In vivo models of angiogenesis. J Cell Mol Med. 10, 588-612 (2006).
- Mammoto, T., Jiang, A., Jiang, E., Mammoto, A. Platelet rich plasma extract promotes angiogenesis through the angiopoietin1-Tie2 pathway. Microvasc Res. 89, 15-24 (2013).
- Mosesson, M. W. Fibrinogen and fibrin structure and functions. J Thromb Haemost. 3, 1894-1904 (2005).
- Bensaid, W., et al. A biodegradable fibrin scaffold for mesenchymal stem cell transplantation. Biomaterials. 24, 2497-2502 (2003).
- Teichert-Kuliszewska, K., et al. Biological action of angiopoietin-2 in a fibrin matrix model of angiogenesis is associated with activation of Tie2. Cardiovasc Res. 49, 659-670 (2001).
- Lafleur, M. A., Handsley, M. M., Knauper, V., Murphy, G., Edwards, D. R. Endothelial tubulogenesis within fibrin gels specifically requires the activity of membrane-type-matrix metalloproteinases (MT-MMPs). J Cell Sci. 115, 3427-3438 (2002).
- Collen, A., et al. Aberrant fibrin formation and cross-linking of fibrinogen Nieuwegein, a variant with a shortened Aalpha-chain, alters endothelial capillary tube formation. Blood. 97, 973-980 (2001).
- Mammoto, T., et al. Mechanochemical Control of Mesenchymal Condensation and Embryonic Tooth Organ Formation. Dev Cell. 21, 758-769 (2011).
- Murphy, K. C., Leach, J. K. A reproducible, high throughput method for fabricating fibrin gels. BMC Res Notes. 5, 423(2012).
- Matar, A. F., Hill, J. G., Duncan, W., Orfanakis, N., Law, I. Use of biological glue to control pulmonary air leaks. Thorax. 45, 670-674 (1990).
- Thetter, O. Fibrin adhesive and its application in thoracic surgery. Thorac Cardiovasc Surg. 29, 290-292 (1981).
- Rahbarghazi, R., et al. Juxtacrine and paracrine interactions of rat marrow-derived mesenchymal stem cells, muscle-derived satellite cells, and neonatal cardiomyocytes with endothelial cells in angiogenesis dynamics. Stem Cells Dev. 22, 855-865 (2013).
- Nucera, S., Biziato, D., De Palma, M. The interplay between macrophages and angiogenesis in development, tissue injury and regeneration. Int J Dev Biol. 55, 495-503 (2011).
- Joensuu, K., et al. Interaction between marrow-derived human mesenchymal stem cells and peripheral blood mononuclear cells in endothelial cell differentiation. Scand J Surg. 100, 216-222 (2011).
- Takakura, N. Role of intimate interactions between endothelial cells and the surrounding accessory cells in the maturation of blood vessels. J Thromb Haemost. 9 Suppl 1, 144-150 (2011).
- Plantier, L., Boczkowski, J., Crestani, B. Defect of alveolar regeneration in pulmonary emphysema: role of lung fibroblasts. Int J Chron Obstruct Pulmon Dis. 2, 463-469 (2007).
- Belair, D. G., Murphy, W. L. Specific VEGF sequestering to biomaterials: influence of serum stability. Acta Biomater. 9, 8823-8831 (2013).
- Wong, C., Inman, E., Spaethe, R., Helgerson, S. Fibrin-based biomaterials to deliver human growth factors. Thromb Haemost. 89, 573-582 (2003).
- Stolzing, A., Colley, H., Scutt, A. Effect of age and diabetes on the response of mesenchymal progenitor cells to fibrin matrices. Int J Biomater. 2011, 378034(2011).
- Vailhe, B., Ronot, X., Tracqui, P., Usson, Y., Tranqui, L. In vitro angiogenesis is modulated by the mechanical properties of fibrin gels and is related to alpha(v)beta3 integrin localization. In Vitro Cell Dev Biol Anim. 33, 763-773 (1997).
- Kniazeva, E., Kachgal, S., Putnam, A. J. Effects of extracellular matrix density and mesenchymal stem cells on neovascularization in vivo. Tissue Eng Part A. 17, 905-914 (2011).
- Angio, C. T., Maniscalco, W. M. The role of vascular growth factors in hyperoxia-induced injury to the developing lung. Front Biosci. 7, 1609-1623 (2002).
- Kasahara, Y., et al. Inhibition of VEGF receptors causes lung cell apoptosis and emphysema. J Clin Invest. 106, 1311-1319 (2000).
- Owen, C. A. Roles for proteinases in the pathogenesis of chronic obstructive pulmonary disease. Int J Chron Obstruct Pulmon Dis. 3, 253-268 (2008).
- Demedts, I. K., et al. Elevated MMP-12 protein levels in induced sputum from patients with COPD. Thorax. 61, 196-201 (2006).
- Haq, I., et al. Association of MMP-2 polymorphisms with severe and very severe COPD: a case control study of MMPs-1, 9 and 12 in a European population. BMC Med Genet. 11, 7(2010).
- Mercer, P. F., et al. MMP-9, TIMP-1 and inflammatory cells in sputum from COPD patients during exacerbation. Respir Res. 6, 151(2005).
- Matute-Bello, G., et al. Essential role of MMP-12 in Fas-induced lung fibrosis. Am J Respir Cell Mol Biol. 37, 210-221 (2007).
- Sivakumar, P., Gupta, S., Sarkar, S., Sen, S. Upregulation of lysyl oxidase and MMPs during cardiac remodeling in human dilated cardiomyopathy. Mol Cell Biochem. 307, 159-167 (2008).
- Gomperts, B. N., Strieter, R. M. Stem cells and chronic lung disease. Annu Rev Med. 58, 285-298 (2007).
- Lau, A. N., Goodwin, M., Kim, C. F., Weiss, D. J. Stem cells and regenerative medicine in lung biology and diseases. Mol Ther. 20, 1116-1130 (2012).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved