Method Article
Tavşanlarda Lomber Disk Dejenerasyonu Modellemesi için Transperitoneal Retroperitoneal Erişim ve Perkütan Ponksiyonun Karşılaştırılması
* Bu yazarlar eşit katkıda bulunmuştur
Bu Makalede
Özet
Bu protokol, bir tavşan intervertebral disk dejenerasyonu (IVDD) modelinde perkütan ve trans-retroperitoneal ponksiyonları karşılaştırdı. Her iki yöntem de IVDD'yi indükledi; Bununla birlikte, trans-retroperitoneal yaklaşım daha kapsamlı değişiklikler ve daha düşük mortalite ile sonuçlanmıştır.
Özet
Bu çalışma, tavşanlarda intervertebral disk dejenerasyonunu (IVDD) indüklemek için iki yöntemin etkinliğini karşılaştırmaktadır: annulus fibrosusun perkütan ve trans-retroperitoneal ponksiyonu. On beş sağlıklı erkek Yeni Zelanda Beyaz tavşanı rastgele üç gruba ayrıldı: sahte, perkütan ponksiyon ve trans-retroperitoneal ponksiyon. İki yöntem arasında doğru ve ayrıntılı bir karşılaştırma sağlamak için mortalite oranları, morfolojik ve histolojik değerlendirmeler, radyolojik görüntüleme ve biyobelirteç analizi dahil olmak üzere kapsamlı bir değerlendirme yapıldı. Sonuçlar, her iki delme tekniğinin de tavşan modelinde IVDD'yi başarılı bir şekilde indüklediğini göstermektedir. Bununla birlikte, trans-retroperitoneal yaklaşım, perkütan yönteme kıyasla önemli ölçüde daha düşük bir mortalite oranını korurken, intervertebral disklerde daha belirgin dejeneratif değişikliklere neden oldu. Bu bulgular, IVDD modellemesinde trans-retroperitoneal yaklaşımın avantajlarını vurgulamaktadır. Bu çalışma, IVDD modellerinin oluşturulmasına ilişkin değerli bilgiler sağlamakta ve bel ağrısı için etkili tedavi stratejilerine yönelik gelecekteki araştırmalar için bir temel oluşturmakta ve sonuçta hasta sonuçlarını iyileştirmektedir.
Giriş
Son birkaç on yılda, bel ağrısı (LBP) yaşam kalitesini etkileyen en önemli kas-iskelet sistemi bozukluğu olarak ortaya çıkmıştır1. LBP, giderek daha önemli bir halk sağlığı sorunu haline gelmiş, işgücü kaybı ve ek tıbbi harcamalar nedeniyle topluma önemli bir ekonomik yük getirmiştir 2,3. Yalnızca Amerika Birleşik Devletleri'nde, LBP ile ilişkili doğrudan ve dolaylı maliyetler, tıbbi harcamalar, gelir kayıpları ve işgücü kayıpları dahil olmak üzere yıllık 100 milyar doları aşmaktadır4. LBP'ye genellikle intervertebral disk dejenerasyonu (IVDD) neden olur5,6,7,8. LBP'nin yüksek prevalansı ve ekonomik etkisi göz önüne alındığında, IVDD'nin doğru bir şekilde modellenmesi tedavi stratejilerini keşfetmek için çok önemlidir.
IVDD'nin patofizyolojisini anlamak ve tedavi stratejilerini değerlendirmek için çeşitli preklinik in vivo hayvan modelleri geliştirilmiş ve kullanılmıştır9. Bu modellerde disk dejenerasyonunu indüklemek için cerrahi veya kimyasal disk yaralanması, non-invaziv mekanik stres, genetik modifikasyon ve doğal oluşum dahil olmak üzere birçok yöntem kullanılmıştır10. Bu yöntemler arasında cerrahi yaralanma, IVDD indüksiyonunun %64,9'unu oluşturur ve iğne delme birincil cerrahi tekniktir11. İğne delme modeli, kurulum kolaylığı ve deney hayvanlarına minimum zarar vermesi ile karakterize edilir. Yaygın iğne ponksiyon yaklaşımları arasında lomber disk boşluğuna açık retroperitoneal erişim ve perkütan posterolateral ponksiyon yer alır. Yerleştirme derinliği, radyografik izleme veya iğne uzunluğu kullanılarak belirlenebilir. Özellikle, perkütan yaklaşım, açık cerrahi yöntemlere kıyasla iyatrojenik doku hasarını azaltabilirken, retroperitoneal erişim, önceki literatürde kantitatif olarak karşılaştırılmamış olan doğrudan görselleştirme özelliklerinin yararını sağlar. Çalışmalar, farklı çaplarda iğnelerin12 kullanılmasının ve farklı disklerindelinmesinin 10 IVDD indüksiyonu üzerindeki etkilerini araştırmış olsa da, farklı iğne delme yaklaşımlarına odaklanan karşılaştırmalı çalışmalar sınırlı kalmaktadır. Seçilen tavşan modeli, insan disklerine anatomik benzerliği ve boyut ve yapı açısından kemirgen modellerine göre avantajları göz önüne alındığında, sık görüntüleme değerlendirmeleri ile uygun maliyetli uzunlamasına çalışmalara ihtiyaç duyan araştırmacılar için özel bir fayda sunmaktadır13.
Bu çalışmada, lomber disk boşluğunu delmek için açık retroperitoneal erişim ve perkütan posterolateral ponksiyon olmak üzere iki yöntem kullanılarak lomber IVDD'nin tavşan modelleri oluşturulmuştur. Morfolojik, histolojik ve radyolojik değişiklikler dahil olmak üzere kapsamlı bir sonuç ölçütleri seti analiz edildi.
Protokol
Hayvan deney prosedürleri, Ulusal Sağlık Enstitüleri tarafından yayınlanan Laboratuvar Hayvanlarının Bakımı ve Kullanımı Kılavuzu'na sıkı sıkıya bağlı kaldı ve Chengdu Geleneksel Çin Tıbbı Üniversitesi Deney Hayvanları Etik Kurulu tarafından onaylandı (Etik Onay Numarası: 2021-23). Yedi erkek ve sekiz dişi olmak üzere on beş sağlıklı, 4 aylık, temiz dereceli Yeni Zelanda Beyaz tavşanı (2.25 kg ± 0.25 kg) kullanıldı. Hayvanlar, bir haftalık adaptasyon için 23 °C ila 3 °C oda sıcaklığına ± yaklaşık %60 ± %10 nem oranına sahip, su ve yiyeceğe ücretsiz erişimi olan bir ortamda barındırıldı. Deneyden önce, 15 tavşan rastgele üç gruptan birine atandı: sahte grup (Grup A), perkütan annulus fibrosus ponksiyon grubu (Grup B) ve trans-retroperitoneal boşluk annulus fibrosus ponksiyon grubu (Grup C), her grupta beş tavşan ile. Bu çalışmada kullanılan reaktiflerin ve ekipmanların detayları Malzeme Tablosunda listelenmiştir.
1. Perkütan annulus fibrosus ponksiyonu ile tavşan IVDD modelinin kurulması
NOT: Tavşan IVDD modeli, perkütan annulus fibrosus ponksiyon yöntemi kullanılarak kurulmuştur. Prosedür, Luo TD ve ark.14 tarafından tarif edilen delinme modelleme yöntemini takip etti ve X-ışını rehberliğinde gerçekleştirildi (Şekil 1).
- Tavşanı hazırla.
- Ameliyattan önce tavşanları 24 saat oruç tutun ve suya erişim sağlayın.
- Kulak damarına intravenöz %3 pentobarbital sodyum (1.3 mL / kg) enjeksiyonu yoluyla anestezi uygulayın (kurumsal olarak onaylanmış protokolleri izleyerek).
- Hareketsizlik, gevşemiş kaslar, kornea refleksi eksikliği ve ağrı tepkisi yokluğunu kontrol ederek başarılı anesteziyi onaylayın.
- Tavşanı konumlandırın ve işaretleyin.
- Tavşanı bir sabitleme tahtası üzerine yüzüstü pozisyonda sabitleyin.
- Cerrahi alanı tıraş edin ve hazırlayın, ardından kemik işaretlerini palpe edin.
- Tavşanın bel sırtındaki kemikli yer işaretlerini palpe edin. Tavşan üzerinde, tipik olarak L1 spinöz sürecinin hemen üzerindeki omurlara karşılık gelen en düşük kaburgayı bulun.
- L1 dikenli sürecini belirlemek için bu omurun hemen altındaki dikenli süreci tanımlayın.
- İlyak tepelerin en yüksek noktalarını, yaklaşık olarak L6 omuru ile aynı seviyede bulun.
- Her bir dikenli süreci L7'ye kadar sırayla tanımlamak için L1 dikenli süreçten aşağı doğru izleyin.
- L1 dikenli işlemi tavşanın sırtında net bir şekilde işaretlemek için bir işaretleme kalemi kullanın.
- Bir sonraki dikenli işleme geçin ve L2 olarak işaretleyin.
- Sonraki her dikenli işlemi L3, L4, L5, L6 ve L7 olarak işaretlemeye devam edin. Net tanımlama için her işaretin farklı ve sıralı sırada olduğundan emin olun.
- Delinme bölgesini bulun ve işaretleyin.
- Enine süreçleri palpe edin ve L5 ve L6'nın distal uçları arasındaki orta noktayı bulun.
- Bu noktayı işaretleyin ve delme iğnesini yaklaşık 1 cm yukarıya sokmaya hazırlanın.
- Delme iğnesini yerleştirin.
- Delme iğnesini yatay olarak tutun ve cildi kırarak yere doğru sokun.
- L4 omur gövdesine ulaşmak için iğneyi ilerletin ve X-ışını rehberliğinde doğru konumlandırmayı doğrulayın.
- İğneyi L4-5 intervertebral diske doğru yaklaşık 20°'lik bir açıyla hafifçe sefalik olarak eğin. Diski delin ve X-ışını muayenesi altında delinmenin doğruluğunu onaylayın.
- Disk ponksiyonları yapın.
- Gerekirse X-ışını kılavuzluğunu kullanarak annulus fibrosusu hassas bir şekilde delin.
- L2-3 ve L3-4 intervertebral diskler için delme işlemini tekrarlayın ve her birini bir kez delin.
- Her disk için 5 s'lik bir bekleme süresi ile yaklaşık 5 mm'lik bir delme derinliğini koruyun.
- İşlem sonrası bakım
- Delinme bölgesini dezenfekte edin ve bandajlayın.
- Penisilini 3 gün boyunca tavşan başına günde 40.000 U'luk bir dozda gluteus maximus'a intramüsküler olarak enjekte edin.
NOT: İğne sert dokuyla karşılaşırsa yaklaşımı ayarlayın. Hassas delme için X-ışını kılavuzunu kullanın. Tavşanın iyileşmesini izleyin ve uygun bakımı sağlayın.
2. Trans-retroperitoneal boşluk annulus fibrosus ponksiyonu ile tavşan IVDD modelinin kurulması
NOT: Tavşan IVDD modeli, trans-retroperitoneal boşluk anulus fibrosus ponksiyon yöntemi12 kullanılarak kurulmuştur (Şekil 2).
- Ameliyattan önce tavşanları 24 saat oruç tutun ve suya erişim sağlayın.
- Kulak damarına intravenöz olarak %3 pentobarbital sodyum (1.3 mL/kg) enjekte ederek tavşanı uyuşturun (kurumsal olarak onaylanmış protokolleri izleyerek).
- Başarılı anesteziyi doğrulamak için tavşanın hareketsiz olduğundan, kasları gevşediğinden, kornea refleksi olmadığından ve basınca ağrı tepkisi olmadığından emin olun.
- Tavşanı bir sabitleme tahtası üzerine yüzüstü pozisyonda sabitleyin.
- Ameliyat bölgesini tıraş edin ve hazırlayın.
- Tavşanın bel sırtındaki L1-L7 lomber spinöz süreçlerini bir işaretleme kalemi ile işaretleyerek kemik işaretlerini palpe edin.
- Cerrahi insizyon yerini belirlemek için tavşanın enine işlemlerini yeniden palpe edin.
- Steril bir örtü yerleştirin ve aseptik koşulları sağlamak için yerel cildi dezenfekte edin.
- Lomber intervertebral diskin lateral yönünü ortaya çıkararak fasyayı ve kasları katman katman incelemek için posterior retroperitoneal bir yaklaşım kullanın.
- Anulus fibrosusu bir delme iğnesi ile yaklaşık 5 mm derinliğe ve 5 s'lik bir bekleme süresine kadar delin.
- L3-4, L4-5 ve L5-6 intervertebral diskleri sırayla delin ve her diskin yalnızca bir kez delinmesini sağlayın.
- 0,25 mm çapında bir dikiş ipliği kullanarak dokuları katman katman dikin.
- Modellemeden sonra delinme bölgesini dezenfekte edin ve bandajlayın.
- Art arda üç gün boyunca tavşan başına 40.000 U'luk bir dozda günlük olarak tavşanın gluteus maximus'una intramüsküler olarak penisilin enjekte edin.
NOT: 800.000 birim / flakon spesifikasyonu ve Veteriner İlaç 140051251 onay numarası ile penisilin kullanın.
3. IVDD modellerinin seçimi ve sonuç değerlendirmesi
- Tavşanların mortalite ve genel durum değerlendirmesi
- Hayatta kalmayı belirlemek ve zihinsel durum, aktivite modelleri, yiyecek ve su alımının yanı sıra dışkı ve idrar çıkışı dahil olmak üzere genel durumu kaydetmek için tavşanları haftalık olarak gözlemleyin.
- Gözlemleri doğru bir şekilde kaydedin ve durumdaki değişiklikleri not edin.
- Tavşanların kilo takibi
- Model oluşturulmadan önce ve sonra ve ayrıca doku toplamadan önce tavşanların vücut ağırlığını kaydedin.
- Ağırlığın doğru bir şekilde kaydedildiğinden emin olun ve önemli değişiklikleri not edin.
- Radyolojik değerlendirme
- Model oluşturulmadan önce ve 4 hafta sonra her beyaz tavşanın tüm lomber vertebral eksplant dizisinin sagital 1.5T T2 ağırlıklı manyetik rezonans görüntülemesini elde edin.
- İntervertebral disk dejenerasyonunun derecesini gözlemleyin.
- Griffith ve ark.15 tarafından önerilen modifiye Pfirrmann derecelendirme sistemini kullanarak intervertebral disk dejenerasyonunun kantitatif bir değerlendirmesini yapın. Üç bağımsız kör radyoloğun T2 ağırlıklı MRI dizilerini belirlenen kriterlere göre değerlendirmesini sağlayın: disk yüksekliği, nükleus pulpozus sinyal yoğunluğu ve annulus fibrosus bütünlüğü.
- Tutarsızlıklar bir sınıf seviyesini aştığında final notlarını fikir birliği yoluyla belirleyin. Tüm değerlendirmeleri, kalibre edilmiş ekran ayarlarına sahip standartlaştırılmış DICOM görüntüleme yazılımını kullanarak gerçekleştirin.
- Histopatolojik değerlendirme ve skorlama
- İntravenöz aşırı dozda pentobarbital sodyum kullanarak modellemeden 4 hafta sonra tavşanlara ötenazi yapın (kurumsal olarak onaylanmış protokolleri izleyerek), ardından L2-L3, L3-L4 ve L4-L5 intervertebral diskleri buz15 üzerinde hızla hasat edin.
- L2-L3 disklerini %4 paraformaldehit içinde sabitleyin ve kalan numuneleri -80 °C'de saklayın.
- Sabit diskleri% 10 EDTA gibi kireç çözücü bir çözeltiye daldırın ve tamamen daldırın. Etkinliği korumak için kireç çözücü solüsyonu her 2-3 günde bir değiştirin.
- Disk boyutuna ve kalınlığına bağlı olarak birkaç gün ila bir hafta sürebilen tam kireç çözme elde edilene kadar kireç çözme işlemini düzenli olarak izleyin.
- Kireç çözücü solüsyonun kalıntılarını gidermek için kireçten arındırılmış diskleri akan su ile iyice durulayın.
- Diskleri, %70 etanol ile başlayan ve kademeli olarak %100 etanole yükselen bir dizi kademeli etanol çözeltisine daldırarak kurutun. Her dehidrasyon adımını sınıf başına 1-2 saat boyunca gerçekleştirin.
- Susuz kalmış disklere parafin mumu (erime noktası 56-58 °C) ile en az 2 saat boyunca sızın ve tam sızmayı sağlayın.
- Sızan diskleri bir balmumu bloğuna gömün ve bölümlere ayırmak için konumlandırın. Balmumu bloğunun soğumasını ve tamamen katılaşmasını bekleyin.
- Gömülü diskleri bir mikrotom kullanarak ince, düzgün dilimler (5-10 μm) halinde bölümlere ayırın. Histolojik boyama veya immünohistokimya gibi daha ileri analizler için bölümleri cam slaytlara monte edin12,13.
- Hematoksilen ve eozin (HE) boyaması yapın, optik mikroskop altında görüntü yakalayın ve IVD histopatolojik derecelendirme ölçeği12'yi kullanarak HE boyama skorları atayın.
- TUNEL testi
- İntervertebral disk doku kesitlerini dewax ve rehidre edin, ardından antijen alımı ve membran permeabilizasyonu gerçekleştirin.
- 1:9 oranında reaktif 1 (TdT) ve reaktif 2 (dUTP) karışımı ekleyin ve nemlendirilmiş bir odada inkübe edin.
- Bölümleri PBS tamponu ile yıkayın, DAPI boyası uygulayın ve karanlıkta oda sıcaklığında 10 dakika inkübe edin.
- Tam otomatik bir panoramik tarayıcı ve işleme yazılımı kullanarak görüntü yakalayın.
- Sitokin tespiti
- Deney tavşanlarına ötenazi yapın (adım 3.4.1) ve abdominal aorttan kan örnekleri alın.
- Serumu kan hücrelerinden ayırmak için tavşan kanı örneklerini 2000 × g'da 25 ° C'de 10 dakika santrifüjleyin. Süpernatanı (serum) dikkatlice toplayın ve hücresel kalıntı içermediğinden emin olun.
- Serum örneklerinde TGF-β ekspresyonunu tespit etmek için ELISA kitinde verilen talimatları izleyin.
- ELISA kitinde belirtildiği gibi reaktifleri ve standartları hazırlayın.
- Serum örneklerini ELISA plakasındaki uygun kuyucuklara ekleyin.
- Plakayı kit talimatlarına göre önerilen sıcaklık ve sürede inkübe edin.
- Bağlanmamış reaktifleri çıkarmak için plakayı talimatlara göre yıkayın.
- Kitin protokolünü takip ederek tespit antikorunu ve diğer gerekli reaktifleri ekleyin.
- Plakayı belirtilen süre ve sıcaklık için tekrar inkübe edin.
- Fazla reaktifleri çıkarmak için plakayı iyice yıkayın.
- Alt tabaka çözeltisini kuyucuklara ekleyin ve renk gelişimine izin vermek için önerilen süre boyunca inkübe edin.
- Kit talimatlarında belirtilen dalga boyunda bir spektrofotometre kullanarak optik yoğunluğu (OD) ölçün.
- OD değerlerini sağlanan denkleme koyarak veya standartların bilinen konsantrasyonlarından oluşturulan standart eğriyi kullanarak numune konsantrasyonlarını hesaplayın.
4. İstatistiksel analiz
- Piyasada bulunan yazılımı kullanarak istatistiksel analiz yapın.
- Sürekli değişkenleri ortalama ± standart sapma olarak ifade edin.
- Gruplar arasındaki farkları test etmek için tek yönlü ANOVA kullanın.
- İkili karşılaştırmalar için LSD testlerini uygulayın.
- Tekrarlanan ölçümleri analiz etmek için ANOVA'yı kullanın.
- Değişkenler arasındaki korelasyonu değerlendirmek için Spearman korelasyon analizi yapın.
- Anlamlılık düzeyini α = 0,05 olarak ayarlayın ve 0,05'ten küçük P değerlerini istatistiksel olarak anlamlı olarak kabul edin.
Sonuçlar
Cerrahi işlemler komplikasyonsuz gerçekleştirildi. Grup B'den (perkütan ponksiyon grubu) bir tavşan işlem sonrası öldü. Diğer tüm hayvanlar ameliyat sonrası normal beslenme ve aktivite modellerine devam etti ve deney süresi boyunca hayatta kaldı. Ameliyat bölgelerinde uzun süreli kanama veya enfeksiyon gözlenmedi.
Mortalite ve genel durum değerlendirmesi
Mortalite oranı hem Grup A'da hem de Grup C'de %0 iken, Grup B'de %20 idi (Tablo 1). A grubundaki tavşanların genel durumları normaldi. Modellemeden önce, B Grubu'ndaki tavşanlar, sahte gruptakilere benzer koşullar sergiledi. Bununla birlikte, modellemeden sonraki ikinci günde, Grup B'deki tavşanlar azalmış canlılık, azalmış aktivite, kafeslerinin köşelerinde toplanma tercihi, önemli ölçüde azalmış gıda alımı, nispeten değişmemiş su alımı, daha donuk kürk, artan dışkı çıkışı ve gevşek dışkı gösterdi. Zamanla, B Grubundan bir tavşan öldü, kalan tavşanlar ise yavaş yavaş besin alımlarını modelleme öncesi seviyelere geri kazandı. Bununla birlikte, canlılıkları, aktiviteleri, kürk durumları ve dışkı kıvamları, modelleme öncesi seviyelerden daha düşük kaldı. Buna karşılık, Grup C'deki tavşanlar, modellemeden sonraki ikinci haftadan başlayarak Grup B'dekilere kıyasla daha iyi canlılık, aktivite, gıda alımı, kürk parlaklığı ve dışkı kıvamı sergiledi.
Vücut ağırlığı değerlendirmesi
Tavşanların vücut ağırlığı, modellemeden önce tüm gruplarda benzerdi. Bununla birlikte, örneklemeden önce, Grup B'deki tavşanlar, Grup A ve C'dekilerden daha ağırdı (Şekil 3).
İntervertebral disklerin radyolojik değerlendirilmesi
Grup B ve C'de ameliyat sonrası bir hafta sonra başlayarak intervertebral disk (IVD) yüksekliğinde azalma gözlendi (Şekil 4). Pfirrmann derecelendirmesi gruplar arası anlamlı farklılıklar gösterdi (p < 0.001, Kruskal-Wallis testi ve Dunn'ın post hoc analizi). Sahte grup (Grup A), tüm örneklerde tek tip derece 1 skorları ile bozulmamış disk morfolojisini korudu (medyan [aralık]: 1 [1-1]). Perkütan ponksiyon grubu (Grup B) orta-şiddetli dejenerasyon (medyan [aralık]: 6 [5-6]), retroperitoneal yaklaşım grubu (Grup C) karşılaştırılabilir derecede dejenerasyon gösterirken (medyan [aralık]: 5 [5-6]). İkili karşılaştırmalar arasında önemli farklılıklar ortaya çıktı: (1) Grup A vs. B Grubu (p = 0.0039); (2) A Grubu vs. C Grubu (p = 0.0039); (3) B Grubu vs. C Grubu (p = 0.206). Değerlendiriciler arası güvenilirlik mükemmel kalmıştır (Krippendorff'un α = 0.87) (Tablo 2).
Histopatolojik değerlendirme ve skorlama
Kalitatif histolojik analizde Grup A, B ve C arasında ultrayapı, vasküler infiltrasyon ve granülasyon dokusu birikiminde farklılıklar görüldü (Şekil 5). Patolojik skorlamada Grup B ve C'de Grup A'ya göre anlamlı derecede yüksek skorlar bulunurken, Grup C'de Grup B'ye göre daha yüksek skor görüldü (Tablo 3).
TUNEL tahlil sonuçları
Grup A'da belirgin yeşil punktat apoptotik hücre veya nükleus pulposus hücre apoptozu gözlenmedi. Buna karşılık, Grup B ve C, Grup A'ya kıyasla çok sayıda yeşil punktat apoptotik hücre ve ciddi nükleus pulpozus hücre apoptozu sergiledi. Bununla birlikte, Grup B, Grup C'ye göre nispeten daha az yeşil punktat apoptotik hücre ve daha az nükleus pulposus hücre apoptozu gösterdi (Şekil 6).
TGF-β algılama sonuçları
TGF-β düzeylerinin kantitatif analizinde gruplar arası anlamlı farklılıklar saptandı (tek yönlü ANOVA, F(2,12) = 87.3, p < 0.0001). Sham grubu (Grup A) başlangıç TGF-β konsantrasyonları gösterirken (ortalama ± SD: 1944.6 pg / mL ± 182.3 pg / mL), perkütan ponksiyon grubu (Grup B) orta derecede bir yükselme gösterdi (2635.4 pg / mL ± 136.7 pg / mL). Özellikle, retroperitoneal yaklaşım grubu (Grup C), Grup B seviyelerini %57.2 oranında aşarak önemli TGF-β upregülasyonu (4143.7 pg/mL ± 353.7 pg/mL) sergiledi (Tukey'in post hoc: p < 0.0001). Bireysel biyolojik varyasyonlar grup ortalamalarının %15'i içinde kalmıştır (varyasyon katsayısı aralığı: %5.2-%8.5) (Şekil 7, Tablo 4).

Şekil 1: X-ışını kılavuzluğunda perkütan anulus fibrosus ponksiyon modellemesi. Anulus fibrosusun hassas bir şekilde delinmesini sağlamak için X-ışını görüntüleme kullanıldı. Şekil, disk penetrasyonundan önce X-ışını altında lokalize edilen delme iğnesini göstermektedir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
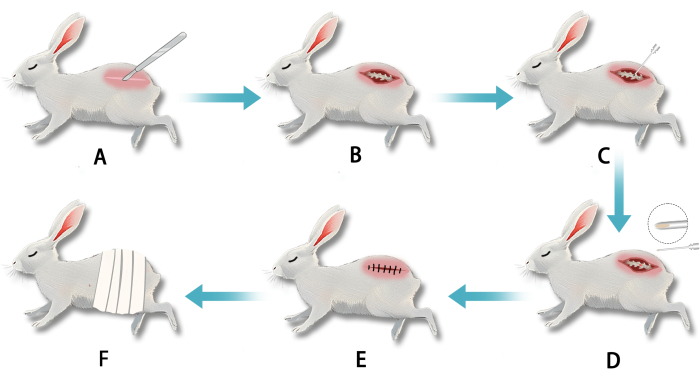
Şekil 2: Anulus fibrosusun transperitoneal retroperitoneal boşluk ponksiyonu kullanılarak intervertebral disk dejenerasyonunun (IVDD) beyaz tavşan modelinin oluşturulması. (A) Anestezi sonrası lomber vertebral segmentte bir kesi yapıldı. (B) Künt diseksiyon lomber annulus fibrousu ortaya çıkardı. (C) Nukleus pulpozusu bozmak için annulus fibrosus bir iğne ile delinmiştir. (D) Çekildikten sonra iğne ucunda beyaz, jöle benzeri nükleus pulpozus dokusu görüldü. (E) Kesi, ponksiyon tamamlandıktan sonra dikildi. (F) Yara ameliyat sonrası pansuman yapıldı. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 3: Modelleme ve örneklemeden önce her gruptaki beyaz tavşanların ortalama vücut ağırlıkları. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 4: Modelleme öncesi ve sonrası tavşan intervertebral disklerinin MRG görüntüleri. Modelleme sonrası Grup B ve C'de önemli boy kaybı gözlenirken, Grup C'de Grup B'ye göre daha fazla kayıp gözlendi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 5: Tavşan intervertebral disklerinin histolojik görüntüleri. (A) Grup A, düzenli bir nükleus pulpozus şekli, bol hücre dağılımı, jelatinimsi matriksteki vakuoller (siyah oklar) ve organize fibrokartilajinöz plakalar (sarı oklar) sergiledi. (B) Grup B'de düzensiz çekirdek pulpozus şekli, azalmış hücre sayısı, kümelenmiş matris dağılımı, büyük boşluklar (mavi oklar) ve çekirdek pulpozustan ayrılmış fibrokartilajinöz plakalar (yeşil oklar) bozulmuştur. (C) Grup C'de düzensiz çekirdek pulpozus şekli, belirgin hücre kaybı (mor oklar), kümelenmiş matris dağılımı, düzensiz şekiller ve bozulmuş fibrokartilajinöz plakalar (kırmızı oklar) görüldü. Ölçek çubuğu: 200 μm (tüm paneller için geçerlidir). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
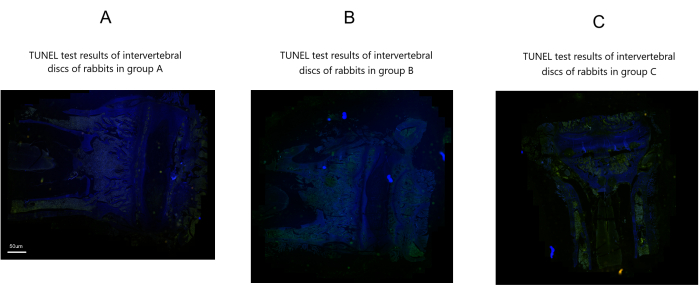
Şekil 6: Üç grupta tavşan intervertebral disklerinin modelleme sonrası TUNEL test sonuçları. Ölçek çubuğu: 50 μm (tüm paneller için geçerlidir). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
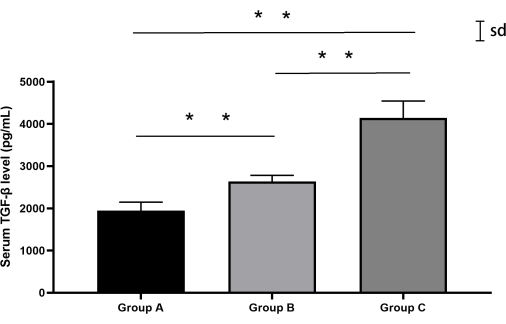
Şekil 7: Her gruptan tavşanlarda serum TGF-β seviyeleri. Hem Grup B hem de C, Grup A'ya kıyasla daha yüksek TGF-β seviyeleri sergilerken, Grup C en yüksek seviyeleri gösterdi. Hata çubukları ortalama ± standart sapmayı (SD) temsil eder. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
| Grup | A | B | C |
| Ölümlülük | 0 | 20% | 0 |
Tablo 1: Tavşan gruplarında modelleme sonrası ölüm oranı.
| n | Pfirrmann Sınıf Dağılımı | Medyan [Aralık] | Gruplar Arası Karşılaştırma (p değeri) |
| 5 | 1 (100%) | 1 [1-1] | A ve B: 0.0039 |
| 5 | 5 (40%), 6 (60%) | 6 [5-6] | A ve C: 0.0039 |
| 5 | 5 (60%), 6 (40%) | 5 [5-6] | B'ye karşı C: 0.206 |
Tablo 2: Modifiye edilmiş Pfirrmann derecelendirme sistemi kullanılarak intervertebral disk dejenerasyonunun karşılaştırmalı analizi.
| Grup | A | B | C |
| Patoloji skoru | 4 | 10 | 11 |
Tablo 3: Her gruptaki tavşanların ortalama patolojik skorları.
| Grup | n | Ortalama ± SD (pg/mL) | Medyan [Aralık] (pg/mL) | İkili Karşılaştırmalar (Tukey'in HSD'si) |
| A | 5 | 1944.6 ± 182.3 | 2054.5 [1709.1-2126.6] | A ve B: p = 0.0012 |
| B | 5 | 2635.4 ± 136.7 | 2544.6 [2526.6-2889.6] | A'ya karşı C: p < 0.0001 |
| C | 5 | 4143.7 ± 353.7 | 4090.3 [3694.9-4595.5] | B'ye karşı C: p < 0.0001 |
| Tüm değerler toplam protein içeriğine (μg/mg doku) normalize edilmiştir ANOVA varsayımları doğrulandı (Levene'nin testi p = 0.18, Shapiro-Wilk p > 0.15) Efekt büyüklükleri: Cohen's f = 2.16 (büyük efekt)* |
Tablo 4: Deney gruplarında TGF-β konsantrasyon profilleri.
Tartışmalar
Bu çalışmanın bulguları, tavşan modellerinde intervertebral disk dejenerasyonunu (IVDD) indüklemede hem perkütan hem de trans-retroperitoneal ponksiyon yaklaşımlarının etkili olduğunu göstermektedir. Özellikle, genel durum, mortalite, histopatolojik değerlendirme, TUNEL testi ve serum TGF-β seviyelerinin kapsamlı bir değerlendirmesine dayanarak, trans-retroperitoneal ponksiyon modeli, daha düşük bir mortalite oranını korurken intervertebral disklerde daha kapsamlı dejeneratif değişikliklere neden oldu.
Cerrahi yaralanma, IVDD modellerinin oluşturulmasında en sık kullanılan yöntemdir. Lipson ve Muir (1981) tavşanlarda cerrahi neşter annulotomi16 kullanarak başarılı bir şekilde bir IVDD modeli geliştirdiğinden, iğne delme 12,14,17, annulus fibrosus eksizyonu 18, total diskektomi, parsiyel ve total nükleotomi19, nükleus pulpozus aspirasyonu 20,21,22 ve matkap yaralanması 23,24 dahil olmak üzere çeşitli yaralanma teknikleri ortaya çıkmıştır. 26. Bu cerrahi yöntemler, hayvanlara farklı fizyolojik yükler getirir ve bu da değişen derecelerde IVDD indüksiyonuna yol açar. Neşter yaralanması modelleriyle karşılaştırıldığında, iğne delme modelleri disk dejenerasyonunun yavaş ve ilerleyici doğasını daha iyi taklit eder14.
Masuda ve ark.12 trans-retroperitoneal ponksiyon tekniğini tanıtmış olsa da, bu açık cerrahi yaklaşım daha uzun ameliyat süresi, daha fazla cerrahi beceri ve daha geniş cerrahi kaynaklar gerektirir. Ek olarak, açık cerrahi sırasında oluşturulan kesi, deney hayvanlarında enfeksiyon, ameliyat sonrası ağrı ve mortalite riskini artırabilir. Buna karşılık, Luo ve ark.14 tarafından önerilen perkütan posterolateral ponksiyon tekniği daha basit ve uygulanabilirdir. Bu çalışmanın sonuçları, trans-retroperitoneal ponksiyon modelinin, daha düşük bir mortalite oranını korurken intervertebral disklerde daha kapsamlı dejeneratif değişikliklere neden olduğunu doğrulamaktadır.
İğne delme modellerinde, intervertebral diskteki dejeneratif değişikliklerin kapsamı ve doğası, zamanla değişen çoklu mekanik ve biyolojik faktörlerden etkilenir27,28. Bu faktörler disk dejenerasyonuna iyi bilinen patolojik katkıda bulunurlar. İğne delinmesi annulus fibrosusun bütünlüğünü bozar, nükleus pulpozusun elastikiyetini azaltır, nükleus pulpozus hücre apoptozunu teşvik eder ve omurga içindeki mekanik stres dağılımını değiştirir29. Ek olarak, yaralanan bölge, dış annulus fibrosusunda kılcal proliferasyon ve granülasyon ve fibrotik dokuların birikmesi dahil olmak üzere enflamatuar ve erken onarım yanıtlarını ortaya çıkarır. Bu patolojik reaksiyonlar, disk dejenerasyonunun çok sayıda hayvan modelinde30,31 tanımlanmıştır ve ayrıca insan lomber disk herniasyonunda da gözlenir.
Bu çalışmada, bu patolojik yanıtlar her iki modelde de belirgindi. Perkütan ponksiyon ile karşılaştırıldığında, trans-retroperitoneal ponksiyon daha net bir ponksiyon görünümü sunarak annulus fibrosusun daha hassas bir şekilde bozulmasını kolaylaştırır ve yaralanma bölgesinde daha fazla iltihaplanmaya yol açar. Bu, trans-retroperitoneal ponksiyon modelinin intervertebral disklerde neden daha kapsamlı dejeneratif değişikliklere neden olduğunu açıklayabilir. Tersine, perkütan ponksiyondaki sınırlı görünürlük, omuriliğin veya diğer yapıların yanlış delinme olasılığını arttırır ve potansiyel olarak bu çalışmada gözlenen daha yüksek mortalite oranını açıklar.
Disk dejenerasyonu için iğne delme modelleri, sıçanlar ve fareler32 gibi küçük hayvanlarda ve ayrıca tavşanlarda 12,14,16 yaygın olarak kullanılmaktadır. Bununla birlikte, bu teknik, IVDD model geliştirme için köpekler33, koyun34, sığır35 ve rhesus maymunları36 dahil olmak üzere daha büyük hayvanlara da uygulanabilir. Dört ayaklı hayvan modelleri ile iki ayaklı insan omurgası arasındaki farklarla ilgili endişeler olmasına rağmen, biyomekanik çalışmalar, dört ayaklı omurgaların öncelikle insan omurgalarına benzer şekilde eksenel kompresyon yaşadığını göstermektedir37,38. Dört ayaklı omurgalara etki eden yoğun eğilme ve burulma kuvvetleri, uzun eksen38 boyunca önemli gerilme kuvvetleri oluşturan paraspinal kaslar ve bağlar tarafından dengelenir. Etik ve pratik kısıtlamalar göz önüne alındığında, daha büyük dört ayaklıların elde edilmesi maliyetli ve zordur, bu da tavşanları IVDD araştırması için ideal bir model haline getirir. Ayrıca, tavşan ve insan intervertebral diskleri arasındaki anatomik homoloji - özellikle faset eklemlerin, paraspinal kasların ve bağların varlığı - tavşanların bu araştırma için uygunluğunu daha da desteklemektedir13,39.
Bununla birlikte, bu hayvan modelleri ile insan intervertebral diskleri arasında, bu çalışmanın bir sınırlamasını temsil eden önemli farklılıklar vardır. Bu farklılıklar arasında disk boyutundaki varyasyonlar, anatomik özellikler, notokordal hücrelerin varlığı ve deneysel sonuçların çevrilebilirliği yer alır. Sonuç olarak, bu çalışma bazı zorluklarla karşı karşıyadır. Ek olarak, klinik uygulamada, hastalar sıklıkla intervertebral diskte önceden var olan dejeneratif değişikliklerle başvururlar ve bu da sonuçta disk herniasyonuna ve nöral kompresyona yol açabilir. Buna karşılık, bu çalışmadaki hayvan modelleri, sağlıklı disklere zarar vererek dejenerasyona neden oldu. Dejenere diskler, yaralanmadan sonra kendi kendini onarma ve rejeneratif yetenekleri azalmış olabilir veya bu deneyde incelenen sağlıklı disklere kıyasla daha ciddi dejenerasyon sergileyebilir. İntervertebral disk dejenerasyonunun hayvan modelleri üzerine gelecekteki araştırmalar bu faktörleri tam olarak dikkate almalıdır.
Hem perkütan hem de trans-retroperitoneal ponksiyon yaklaşımları, tavşanlarda intervertebral disk dejenerasyon modellerinin oluşturulmasında etkilidir. Bununla birlikte, trans-retroperitoneal ponksiyon tekniği, daha düşük bir mortalite oranı ile ilişkilendirilirken daha kapsamlı dejeneratif değişikliklere neden olur.
Açıklamalar
Hiç kimse.
Teşekkürler
Bu proje, Çin Ulusal Doğa Bilimleri Vakfı (No. 82004497), Çin Doktora Sonrası Bilim Vakfı (No. 2021M693788), Çin Ulusal Doğa Bilimleri Vakfı (No. 82105043) ve Sichuan Eyaleti Doğa Bilimleri Vakfı (No. 2023NSFSC1814) tarafından desteklenmiştir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 0.3 T Veterinary Maenetic Resonance lmaging(MRI) | NINGBO CHUANSHANJIA | CSJ-MR | |
| Alcohol medical | LIRCON | 20230107 | |
| Benzylpenicillin potassium | Jiangxi Keda Animal Pharmaceutical | 140051251 | |
| Haemostatic forceps | SHINVA | 20211239 | |
| Injection syringe | CONPUVON | 20153151307 | |
| Knife blades | Hons Medincal | 20210615 | |
| Medical absorbent cotton ball | Cofoe | 20210006 | |
| Medical suture needle | Shanghai Xiaoyi Medical Devices | 20192020430 | |
| Medullo-puncture needle | Yangzhou Jiangzhou Medical Devices | 20190902 | Used to puncture lumbar disc |
| Physiological saline | NeilMed | C1210504D2 | |
| Povidone iodine solution | Sichuan IJIS Medical Technology | 20221209 | |
| Quasi-microbalance | Explorer | ||
| Rabbit dissection operating table | Zhenhua Biomedical | ZH-BXT-3Z | |
| Shaver | AUX | ||
| Statistical analysis softeare | IBM | SPSS | |
| Sterile gauze | Cofoe | 20202140675 | |
| Surgical gloves | DR.LERSH | 20172140028 | |
| Surgical knife | Hons Medinca | 20210019 | |
| Surgical tweezers | SHINVA | 20210233 | |
| USB-C data transmission line | KINI | ||
| White light photography microscope | Nikon | Eclipse Ci-L |
Referanslar
- Vos, T., et al. Years lived with disability (YLDS) for 1160 sequelae of 289 diseases and injuries 1990-2010: A systematic analysis for the global burden of disease study 2010. Lancet. 380 (9859), 2163-2196 (2012).
- Daly, C., Ghosh, P., Jenkin, G., Oehme, D., Goldschlager, T. A review of animal models of intervertebral disc degeneration: Pathophysiology, regeneration, and translation to the clinic. Biomed Res Int. 2016, 5952165 (2016).
- Risbud, M. V., Shapiro, I. M. Role of cytokines in intervertebral disc degeneration: Pain and disc content. Nat Rev Rheumatol. 10 (1), 44-56 (2014).
- Katz, J. N. Lumbar disc disorders and low-back pain: Socioeconomic factors and consequences. J Bone Joint Surg Am. 88 (Suppl 2), 21-24 (2006).
- Cheung, K. M. The relationship between disc degeneration, low back pain, and human pain genetics. Spine J. 10 (11), 958-960 (2010).
- Knezevic, N. N., Candido, K. D., Vlaeyen, J. W. S., Van Zundert, J., Cohen, S. P. Low back pain. Lancet. 398 (10294), 78-92 (2021).
- Livshits, G., et al. Lumbar disc degeneration and genetic factors are the main risk factors for low back pain in women: The UK twin spine study. Ann Rheum Dis. 70 (10), 1740-1745 (2011).
- Takatalo, J., et al. Does lumbar disc degeneration on magnetic resonance imaging associate with low back symptom severity in young finnish adults. Spine (Phila Pa 1976). 36 (25), 2180-2189 (2011).
- Singh, K., Masuda, K., An, H. S. Animal models for human disc degeneration. Spine J. 5 (6 Suppl), 267s-279s (2005).
- Liang, T., et al. Constructing intervertebral disc degeneration animal model: A review of current models. Front Surg. 9, 1089244 (2022).
- Poletto, D. L., Crowley, J. D., Tanglay, O., Walsh, W. R., Pelletier, M. H. Preclinical in vivo animal models of intervertebral disc degeneration. Part 1: A systematic review. JOR Spine. 6 (1), e1234 (2023).
- Masuda, K., et al. A novel rabbit model of mild, reproducible disc degeneration by an anulus needle puncture: Correlation between the degree of disc injury and radiological and histological appearances of disc degeneration. Spine (Phila Pa 1976). 30 (1), 5-14 (2005).
- Kroeber, M. W., et al. New in vivo animal model to create intervertebral disc degeneration and to investigate the effects of therapeutic strategies to stimulate disc regeneration. Spine (Phila Pa 1976). 27 (23), 2684-2690 (2002).
- Luo, T. D., et al. A percutaneous, minimally invasive annulus fibrosus needle puncture model of intervertebral disc degeneration in rabbits. J Orthop Surg (Hong Kong). 26 (3), 2309499018792715 (2018).
- Griffith, J. F., et al. Modified Pfirrmann grading system for lumbar intervertebral disc degeneration. Spine (Phila Pa 1976). 32 (24), E708-E712 (2007).
- Lipson, S. J., Muir, H. Experimental intervertebral disc degeneration: Morphologic and proteoglycan changes over time. Arthritis Rheum. 24 (1), 12-21 (1981).
- Wang, Y., Wu, Y., Deng, M., Kong, Q. Establishment of a rabbit intervertebral disc degeneration model by percutaneous posterolateral puncturing of lumbar discs under local anesthesia. World Neurosurg. 154, e830-e837 (2021).
- Gruber, H. E., et al. A new small animal model for the study of spine fusion in the sand rat: Pilot studies. Lab Anim. 43 (3), 272-277 (2009).
- Alini, M., et al. Are animal models useful for studying human disc disorders/degeneration. Eur Spine J. 17 (1), 2-19 (2008).
- Gandhi, S. D., et al. Intradiscal delivery of anabolic growth factors and a metalloproteinase inhibitor in a rabbit acute lumbar disc injury model. Int J Spine Surg. 14 (4), 585-593 (2020).
- Omlor, G. W., et al. A new porcine in vivo animal model of disc degeneration: Response of anulus fibrosus cells, chondrocyte-like nucleus pulposus cells, and notochordal nucleus pulposus cells to partial nucleotomy. Spine (Phila Pa 1976). 34 (25), 2730-2739 (2009).
- Serigano, K., et al. Effect of cell number on mesenchymal stem cell transplantation in a canine disc degeneration model. J Orthop Res. 28 (10), 1267-1275 (2010).
- Daly, C. D., et al. A comparison of two ovine lumbar intervertebral disc injury models for the evaluation and development of novel regenerative therapies. Global Spine J. 8 (8), 847-859 (2018).
- Kim, J. S., et al. The rat intervertebral disk degeneration pain model: Relationships between biological and structural alterations and pain. Arthritis Res Ther. 13 (5), R165 (2011).
- Lim, K. Z., et al. Ovine lumbar intervertebral disc degeneration model utilizing a lateral retroperitoneal drill bit injury. J Vis Exp. (123), e55753 (2017).
- Zhang, Y., et al. Histological features of the degenerating intervertebral disc in a goat disc-injury model. Spine (Phila Pa 1976). 36 (19), 1519-1527 (2011).
- Freemont, A. J. The cellular pathobiology of the degenerate intervertebral disc and discogenic back pain. Rheumatology (Oxford). 48 (1), 5-10 (2009).
- Vergroesen, P. P., et al. Mechanics and biology in intervertebral disc degeneration: A vicious circle. Osteoarthritis Cartilage. 23 (7), 1057-1070 (2015).
- Natarajan, R. N., Andersson, G. B., Patwardhan, A. G., Verma, S. Effect of annular incision type on the change in biomechanical properties in a herniated lumbar intervertebral disc. J Biomech Eng. 124 (2), 229-236 (2002).
- Hoogendoorn, R. J., Wuisman, P. I., Smit, T. H., Everts, V. E., Helder, M. N. Experimental intervertebral disc degeneration induced by chondroitinase ABC in the goat. Spine (Phila Pa 1976). 32 (17), 1816-1825 (2007).
- Melrose, J., Roberts, S., Smith, S., Menage, J., Ghosh, P. Increased nerve and blood vessel ingrowth associated with proteoglycan depletion in an ovine annular lesion model of experimental disc degeneration. Spine (Phila Pa 1976). 27 (12), 1278-1285 (2002).
- Elmounedi, N., et al. Impact of needle size on the onset and the progression of disc degeneration in rats. Pain Physician. 25 (6), 509-517 (2022).
- Tellegen, A. R., et al. Intradiscal delivery of celecoxib-loaded microspheres restores intervertebral disc integrity in a preclinical canine model. J Control Release. 286, 439-450 (2018).
- Vadalà, G., et al. The transpedicular approach as an alternative route for intervertebral disc regeneration. Spine. 38 (6), E319-E324 (2013).
- Yang, J. J., Li, F., Hung, K. C., Hsu, S. H., Wang, J. L. Intervertebral disc needle puncture injury can be repaired using a gelatin-poly (γ-glutamic acid) hydrogel: An in vitro bovine biomechanical validation. Eur Spine J. 27 (10), 2631-2638 (2018).
- Xi, Y., et al. Minimally invasive induction of an early lumbar disc degeneration model in rhesus monkeys. Spine (Phila Pa 1976). 38 (10), E579-E586 (2013).
- Elliott, D. M., Sarver, J. J. Young investigator award winner: Validation of the mouse and rat disc as mechanical models of the human lumbar disc. Spine (Phila Pa 1976). 29 (7), 713-722 (2004).
- Smit, T. H. The use of a quadruped as an in vivo model for the study of the spine - biomechanical considerations. Eur Spine J. 11 (2), 137-144 (2002).
- Romaniyanto, F. N. U., et al. Effectivity of puncture method for intervertebral disc degeneration animal models: Review article. Annals Med Surg. 85 (7), 3501-3505 (2023).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır