Method Article
Anjiogenik potansiyelinin In vivo çalışması için Işlenmiş tümör ilişkili Nötroflelerin tümör taşıyan fareler içine aktarılması
Bu Makalede
Özet
Burada, tümör taşıyan farelere transferinden sonra anti-anjiyojenik tümör ilişkili nötrofiller terapötik potansiyelini gösteriyoruz. Bu protokol, nötrofil aktivitesini ex vivo olarak işlemek ve daha sonra tümörlerin geliştirilmesinde in vivo olarak işlevselliğini değerlendirmek için kullanılabilir. Potansiyel nötrofil bazlı immünoterapileri incelemek için uygun bir modeldir.
Özet
Nötrofiller, tümörijenezde düzenlenmesi katkısı artan dikkat çekiyor. Bu hücreler heterojen ve tümör ortama bağlı olarak yanlısı veya anti-tümör kapasitesine sahip olabilir. Tümör bağlamında nötrofil fonksiyonlarını düzenleyen önemli sitokinlerden biri ben interferonlar türüdür. İnterferonlar varlığında, nötrofil anti-tümör özellikleri kazanmak, sitotoksisite veya bağışıklık sisteminin stimülasyon dahil. Bunun tersi olarak, bir interferon sinyalinin eksikliği, tümör anjiyogenezinin güçlü stimülasyon ile karakterize belirgin Pro-tümör aktivitesinde sonuçlanır. Son zamanlarda, nötrofiller yanlısı anjiyojenik özelliklerinin bu hücrelerdeki nikotinamid phosphoribosyltransferase (NAMPT) sinyalizasyon yolunun aktivasyonuna bağlı olduğunu gösterebiliriz. Tümör ilişkili nötrofiller bu yolun inhibisyonu onların güçlü anti-anjiyojenik fenotipi yol açar. Burada, yeni kurulan modelimizi, manipüle tümör ilişkili nötrofiller (Tans) ' nın tümörojenik potansiyelinin in vivo olarak değerlendirilmesine olanak tanıyarak gösteriyoruz. Kısa bir süre, Pro-anjiyojenik tümör ilişkili nötrofiller tümör taşıyan interferon-eksikliği fareler izole edilebilir ve NAMPT sinyalizasyon bloke ederek Anti-anjiyojenik fenotipi içine repolarize. Bu hücrelerin anjiyojenik aktivite daha sonra bir aort halka tahlil kullanılarak değerlendirilebilir. Anti-anjiyojenik TANs tümör taşıyan vahşi tip alıcılara aktarılabilir ve tümör büyümesi 14 gün boyunca izlenmelidir. Günde 14 fare feda edilir, tümör kaldırıldı ve vazkülarizasyon ile kesilmiş değerlendirildi. Genel olarak, protokollerimiz, yapay nötrofil hücre hattı modellerini kullanmaya gerek kalmadan, tümör ilişkili nötrofiller gibi primer hücrelerin anjiyojenik kapasitesini değerlendirmek için yeni bir araç sağlar. Vc
Giriş
Tip ı Interferonlar (ıfns) neoplasias ana tepkiler stimülasyon önemli bir rol oynar, tip ı ıFN eksikliği önemli ölçüde yüksek tümör büyümesi sonuçları sinyal1. Bu süreçte yer alan mekanizmalardan biri, koloniye uyarıcı faktör 3 reseptör (CSF3R) aşağı sinyal2ile kontrol edilen tümör ilişkili nötrofiller, tümör-genetik aktivitesinin düzenlenmesi. Koloniye uyarıcı faktör 3 (CSF3) veya granülosit kolonisi uyarıcı faktör, nikotinamid phosphoribosyltransferase (nampt)3,4içeren sinyalizasyon etkinleşmeye gösterilmiştir. NAMPT, glikoliz geliştirir ve DNA onarımı, gen ifadesi ve stres tepkisi kanser hücrelerinin hayatta kalma ve proliferasyon teşvik düzenleyen nikotinamide adenin dinükleotit sentezini için bir oran sınırlayıcı enzimdir5. NAMPT, kolorektal, ovaryalı, meme, mide, prostat kanseri ve gliomas6dahil olmak üzere birden fazla kanser tipinde aşırı ifade edilir. NAMPT sadece tümör hücreleri için değil, aynı zamanda miyeloid hücreler gibi tümörlerde bulunan diğer hücre türlerinin geniş bir çeşitliliği için de önemlidir-onların farklılaşma4Sürücüler, apoptozis inhibe ve çoklu sitokinlerin ifade teşvik veya makrofajlar içinde matris-aşağılayıcı enzimler7.
Tümör ilişkili nötrofiller tümör büyümesinin önemli modülatörlerini temsil eder. BRONZLAŞMA fonksiyonları nötrofiller bu sitokinler Prime anti-tümör aktivitesi olarak, türü ı ıFN kullanılabilirlik güçlü bağlıdır. Aksine, ıfns yokluğunda bu hücrelerin tümör aktivasyonunu destekler, özellikle kendi yanlısı anjiyojenik özellikleri. Bununla anlaşmada, INS eksikliği fareler önemli ölçüde daha büyük ve daha iyi vaskülarize tümörlerin geliştirmek, hangi güçlü yanlısı tümörü ile sızan/Pro-anjiyojenik nötrofiller1,2,8, 9,10. Daha da önemlisi, bu tür Pro-anjiyojenik TANs NAMPT yüksek aktivite göstermek, nötrofiller Pro-tümör polarizasyon temel rolünü düşündürmektedir.
Nötrofiller Ly6G antikor veya göç inhibisyonu kullanarak tükenmesi (CXCR2 antikor) azalmış tümör anjiyogenez sonuçları, büyüme, ve metasjen1,8. Yine de, oluşturulan monoklonal antikorlar immunogenic, ve onların yönetimi yaşam tehdit yan etkileri bir dizi ile ilişkilidir11. Nötrofil tumoriogenicity modüle nampt inhibitörü FK866 gibi küçük moleküller ile tedavi, bu tür komplikasyonları önlemek için yardımcı olabilir. Ne yazık ki, NAMPT farmakolojik sistemik inhibisyonu, tümör büyümesi üzerinde terapötik etkisi yanında, gastrointestinal toksisite ve trombositopeni de dahil olmak üzere şiddetli yan etkilere yol açar. Bu nedenle, nampt inhibitörlerinin sistemik uygulanması mümkün değildir12,13,14.
Bu nedenle, burada NAMPT aktivitesinin doğrudan yalıtılmış TANs 'de engellendiği bir protokol öneriyoruz. Bu tür anti-tümör nötrofiller sonra adoptively bir tümör taşıyan ev sahibi aktarılır. Bu protokol, bileşiklerin sistemik toksik yan etkilerini önlemeye yardımcı olur, ancak hedef hücreler üzerindeki etkisi sürdürülecektir.
Protokol
Hayvan konuları dahil tüm prosedürler düzenleyici yetkililer tarafından onaylanmıştır: LANUV (Landesamt für Natur, Umwelt und Verbraucherschutz NRW) ve Regierungspräsidium Tübingen, Almanya. Tüm manipülasyonlar steril reaktifler ve aletler (şırıngalar, makas, forseps, tek kullanımlık neşter, Petri Yemekleri) kullanılarak steril koşullarda (laminar akış kaputu altında) yapılmalıdır.
Not: protokol genel şeması Şekil 1' de gösterilir.
1. B16F10 melanom hücre hattının hazırlanması
- Tam Iscove 'un değiştirilmiş Dulbecco 'nun ortamında (ımdmc: ımdm + 10% fetal sığır serumu (FBS) +% 1 penisilin-streptomisin) içinde% 90 ' lik confluent Tek tabakalı (yaklaşık 10 x 106 hücre/T75 Flask) olarak yetiştirilen Mycoplasma-negatif hücreleri hazırlayın.
- Orta çıkarın ve fosfat tamponlu tuz (PBS) ile hücreleri durulayın. Proteolitik ve kolajagenolitik enzimler içeren 6 mL 'Lik bir hücre dekolmanı çözeltisi uygulayın ( malzeme tablosunabakın) ve 37 °c ' de 2 dakika boyunca Inküye yapın.
- Alttan kalan yapışkıcı hücreleri seferber etmek için yavaşça Flask Knock. Hücre süspansiyonunu 15 mL tüpte toplayın ve 300 x g 'de 7 dakika ve 20 °c ' de santrifüjün.
- Supernatant kaldırmak ve PBS 1 ml Pelet iyi pelletini. 14 mL PBS ve Santrifüjü (300 x g ve 20 °c için 7 dk) ekleyin.
- Süpernatant çıkarın ve 1 ml PBS içinde Pelet pelletini.
- Hücreleri saymak ve onları 3 x 106/ml PBS (adım 2 için) veya 6 x 106/ml PBS (adım 6 için) enjeksiyon için konsantrasyonuna pelletini. Hücreleri buz üzerinde en fazla 30 dakika tutun.
2. farelerde Allogenik tümör modeli
- Belirli-patojen içermeyen (SPF) koşullarda tutulan 10 kadın Ifnar1-/- Mice 8-12 hafta eski kullanın.
Not: kadın fareler tümör büyümesi bir subkutan modelinde tercih edilir, çünkü erkekler daha agresif ve böylece tümör alanı ihlalleri için eğilimli, hangi tümör büyümesini etkiler. - Bir elektrikli tıraş makinesi ile kanat üzerindeki fare cildi tıraş ve% 70 etanol ile ıslak doku ile cildi dezenfekte.
- Hazırlanan B16F10 Melanom hücrelerini 3 x 106/ml PBS konsantrasyonunda topla (1. adıma bakın) 1 ml şırınga ve 0,4 x 19 mm iğne. 100 mL süspansiyon subkutan enjekte.
- Her enjeksiyondan önce hücreleri iyi karıştırın. Tümör hücrelerini rahatsız etmemek için çapı 0,4 mm 'den az olmayan iğneler kullanın.
- Bir kafeste 5 fareye kadar yerleştirin ve 14 gün boyunca bir Kaliper ile tümör boyutunu (uzunluk, genişlik ve derinlik) kontrol etme.
Not: hayvan yönetmeliklerine göre, tümör büyüklüğü 15 mm çapını geçmemelidir, daha büyük veya nekrotik/açık tümörlü fareler önceden feda edilmelidir. - 14. gün, CO2 odasında fareler feda.
- % 70 etanol ile cilt dezenfekte ve steril bir petri tabak makas ve forseps ile tümörleri çıkarın. Tam Dulbecco modifiye kartal orta 50 mL tüp tümörleri tutun (DMEMc: DMEM + 10% FBS + 1% penisilin-streptomicin) buz üzerinde.
3. TAN yalıtımı
- Tümörler steril 6-kuyu plakaları, iyi başına 5 tümör yerleştirin. Steril makas ile 2-3 mm parçaları içine tümörler keser.
- 1 mL dispaz/collagenase D/DNase ı çözeltisi ile Özet (0,2 mg/0.2 mg/100 mg DMEMc 1 mL) tümör başına. 37 °C, 5% CO2 ' de nemli bir inkübatör içinde kuluçat ve her 15 dk 3 kez bir iğne olmadan 10 ml şırınga ile karıştırın.
- Sindirilmemiş lifleri kaldırmak için, 100 μm filtrelerle Mesh hücreleri 15 mL tüplere (her tüp için bir tane de filtre) takın. PBS 'yi 15 mL 'ye, 460 x g, 4 °c ' de 5 dk 'da santrifüjlere ekleyin ve supernatant 'ı çıkarın.
- Lizis tampon ile Lyse eritrositler (NH4CL 150 mm, KHCO3 10 mm, EDTA 0,1 mm, pH 7,3, 20 °c) her tüpün içine 1 ml ekleyerek. İyi karıştırın ve tüm tüplerden bir çözüm birleştirin. 11 mL buz soğuk (4 °C) DMEMc ile 2 dakika sonra reaksiyonu durdurun.
- 460 x g, 4 °c ' de 5 dakika santrifüjün ve süpernatant çıkarın. 15 ml soğuk PBS ile Pelet resuspend. 460 x g, 4 °c ' de 5 dakika santrifüjün ve süpernatant çıkarın.
- 1 ml PBS içinde Pelet resuspend. 3 mL FC blok antikorları (CD16/CD32, Stock 0,5 mg/mL) ekleyin ve 15 dakika boyunca buzun üzerinde inküye yapın.
- Antikorlar ekleyin: 10 mL Ly6G-PE (stok 0,2 mg/mL) ve 10 mL CD11b-APC (stok 0,2 mg/mL). 20 ml 6-diamidin-2-phenylindol canlılığı boya (dapi, stok 5 mg/ml) ekleyin ve 30 dakika boyunca karanlıkta buz üzerinde inkübe.
Not: canlılığı boyalar ve antikorların floresan Konjugatlar başka bir kombinasyonu kullanılabilir. - 15 mL 'ye kadar PBS, 460 x g, 4 °c ' de 5 dakika Santrifüjü ekleyin ve süpernatant 'ı çıkarın.
- Yaklaşık 10 x 106/ml konsantrasyonuna DMEMc içinde Pelet resuspend ve buz üzerinde tutun.
- Sıralama CD11b+ Ly6GHI Alive (DAPI-negatif) bir floresan-aktif hücre sıralayıcı ile nötrofiller (gating stratejisi bkz Şekil 2).
Not: 4 °C ' de sıralı hücreler için hücreli süspansiyon ve DMEMc ile tüp tutun. Aşağıdaki en uygun sıralama ayarlarını kullanın: 70 mm Nozul, maksimum 22.000 olay/saniye eşik oranı ve 1-3 akış hızı. - >% 95 ' in önerilen saflığı için bir sitometresi kullanarak sıralanmış nötrofiller saflığını kontrol edin.
- Santrifüjler sıralı nötrofiller 460 x g, 4 °c 5 dk için, ve supernatant çıkarın. DMEMc 'de sıralanmış hücreleri 1 x 106/ml. konsantrasyonuna yeniden resuspend.
Not: 1 14 günlük B16F10 tümör (10 mm çapı) yaklaşık 3 x 104 hücrelerde beklenen nötrofil sayısı.
4. in vitro TANs NAMPT inhibisyonu
- 100 mM 'Lik son konsantrasyonda dimetilsulfoxıde (DMSO) içinde FK866 (NAMPT inhibitörü) stokları hazırlayın.
- Tohum sıralanmış nötrofiller (adım 3,11) bir 96-iyi U-Bottom plaka 2 kuyuları içine (1,5 x 105 nötrofil/kuyu). Müdahale iyi (100 nM son konsantrasyon), ve DMSO ile DMEMc eşit miktarda kontrol iyi içine FK866 ekleyin. 37 °C ' de 2 h, nemli bir inkükote% 5 CO2 için kuluçk.
- 460 x g, 4 °c ' de 5 dakika santrifüjün ve süpernatant çıkarın. Her iyi PBS 200 mL resuspend. 2 kez tekrarlayın.
- 460 x g, 4 °c ' de 5 dakika santrifüjün ve süpernatant çıkarın. Ticari endotel hücre büyüme ortamında resuspend (4 μL/mL endotel hücre büyüme takviyesi ile tamamlayıcı, 0,1 ng/mL rekombinant insan epidermal büyüme faktörü, 1 ng/mL rekombinant insan temel fibroblast büyüme faktörü, 90 μg/mL heparin ve 1 μg/mL hidrokortizon) son konsantrasyon için 0,2 x 106 hücreler/ml (0,75 ml) (adım 5) veya PBS son konsantrasyonu için 0,6 x 106 hücreler/mL (içinde 0,25 ml) (için adım 6).
5. aort halka tahlil kullanarak TANs anjiyojenik özelliklerinin tahmini
- Bir erkek C57BL/6J (WT) fare Torasik aort incelemek. 0,5 mm genişliğindeki halkalar temiz ve kesilmiş. 1 mL ek endotel hücre büyüme orta ile 24-kuyu plaka bir kuyu tüm halkaları yerleştirin. Bir gecede 37 °C,% 5 CO2 ' de nemli bir kuluçko ile inkulat.
Not: aort diseksiyonu için genç (8 haftadan küçük) erkek farelerin kullanımı daha sağlam anjiyojenik yanıt verdikleri için tercih edilir,15. - 96-iyi düz alt plakanın kuyularını 50 μL çözünen Bodrum membran matrisiyle doldurun, jel için bir 37 °C ' de 30 dakika, matrisin polimerleştirmesine izin vermek için% 5 CO2 nemli kuluçvan ayarlayın. Durum başına en az 3 kuyu hazırlayın.
- Katı matris tabakası, her iyi merkezinde 1 halka üstüne bir aort halkası yerleştirerek çözünebilir Bodrum membran matris halkaları embed. Her yüzüğü kapsayacak şekilde başka bir 50 μL çözünmeli Bodrum membran matrisini ekleyin.
- Plakası, ikinci matris tabakasının polimerizasyonu için 30 dakika süreyle 37 °C,% 5 CO2 nemli kuluçka makinesine yerleştirin.
- Ekleme 150 ml/Well ek endotel hücre büyüme orta ve 2x104Ifnar1-/- tans (kontrol ve FK866-tedavi) (adım 4,4).
- Plakayı 37 °C,% 5 CO2 ' de nemli bir inkükote 14 gün boyunca kuluçat.
- Standart faz kontrast mikroskobu kullanarak görüntü ve endotel dallanma tahmin. Dallanma indeksi dahil olmak üzere gemi morfometrik ve uzamsal parametrelerin niceliksel değerlendirilmesi, bilimsel görüntüler için tasarlanmış görüntü işleme programı kullanılarak otomatik olarak gerçekleştirilebilir.
Not: temsili sonuçlar Şekil 3' te tasvir edilir.
6. Allogenik tümör modelinde tedavi nötrofillerin evlatlık aktarımı
- Hazırlamak B16F10 Melanom hücreleri (adım 1,6) PBS içinde bir konsantrasyon 6 x 106 hücreler/ml.
- 2 tür nötrofil hazırlayın: FK866-tedavi nötrofiller ve tedavi edilmemiş nötrofiller (adım 4,4) PBS 'de bir konsantrasyon 6 x 105 hücreler/ml. B16F10 Melanom hücreleri ile mix nötrofiller (tümör hücreleri oranı 1:10 son nötrofil) hücre karışımları 2 tip var.
- Her grupta 10 kadın WT fareler 8-12 hafta eski, 5 alın. Bir elektrikli tıraş makinesi ile kanatta cildi tıraş ve% 70 etanol ile dezenfekte.
- Hücre süspansiyon 100 μL enjekte (adım 6,2) subkutan bir insülin şırınga ve bir 0,4 mm çapında iğne, her iki fare gruplarına. 1-5 bir kafeste aynı gruptan fareler yerleştirin.
- 2. gün, 2 tür nötrofil hazırlayın: FK866-tedavi nötrofiller ve tedavi edilmemiş nötrofiller (adım 4,4) PBS 'de bir konsantrasyon 6 x 105 hücreler/ml. 100 μL hücre süspansiyonu (adım 6,4), her iki fare grubuna da bir insülin şırıngası ve bir 0,4 mm çapında iğne ile kuyruk damarına enjekte edilir. Fareler geri kafese yerleştirin.
7. tümör büyüme ölçümü, histolojik muayene
- Her gün tümör büyümesini izleyin. Tümör boyutunu kaliperlerle değerlendir ve V = 4/3 * π * (h * w2)/8 (h = yükseklik, w = genişlik, derinlik = genişlik) formülü ile tümör hacmini hesaplayın.
- CO2 odasında 14 gün içinde kurban fareler. Tümörlerin kaldırılması ve tümör ağırlıkları ölçmek.
- Sıvı nitrojen içinde optimum kesme sıcaklığı bileşik tümörleri dondurmak ve-80 °C ' de saklayın.
- Numuneleri-20 °C ' ye çözün ve 5 mm 'lik bölümleri bir cryotome kullanarak hazırlayın. 20 °C ' de 30 dakika boyunca cryocuts kurumasına izin verin. 2 dakika boyunca-20 °C soğuk aseton içindeki bölümleri düzeltin ve 20 °C ' de 30 dakika kuru bırakın.
- FC blok antikorları ile blok (CD16/CD32, stok 0,5 mg/mL 1:500) PBS için 20 °C ' de 1 saat.
- Tavşan Anti fare laminin gama antikor ile leke (1:1500 PBS, 200 μL) için 20 °C ' de 1 saat. PBS ile üç kez yıkayın.
- İkincil keçi Anti-tavşan antikor ile leke (stok 0,5 mg/mL, 1:400 PBS,), Anti-fare αSMA (1:500 PBS) ve 2 μL DAPı (stok 5 mg/mL, 1:100 PBS) son hacim içinde 200 μL antikor çözeltisi. Karanlıkta 20 °C ' de 1 saat boyunca inküye yapın. PBS ile üç kez yıkayın.
- Karanlıkta 20 °C ' de 20 dakika kuru kaydıraklar. Microskopi için susuz montaj ortamına sahip Mount ve bir coverslip ile kapak. 37 °C ' de 1 saat kurumasına izin verin.
- Mikroskopik muayene gerçekleştirin. Laminin+ gemilerinin toplam sayısını (opsiyonel alan) ve SMA+ geliştirilen gemilerin sayısını (alan) sayarak vaskülarizasyon miktarını ölçün.
Not: görüntü analizini gerçekleştirmek Için, tüm görüntüleri aynı koşullarda (ışık, kontrast, büyütme) alın. Bu durumda, işleme parametreleri sabit ve görüntü işleme tamamen otomatik hale gelir. Temsili sonuçlar Şekil 4 ve Şekil 5' te yansıtıldı.
Sonuçlar
Burada açıklanan prosedürü kullanarak, Ifnar1-/- nötrofiller tümörlerden izole edildi ve 2 h için nampt inhibitörü FK866 ile tedavi edildi. tedavi edilmemiş Ifnar1-/- nötrofiller bir kontrol olarak kullanıldı. Tedavinin etkinliği anjiyogenez (matris bozulması, göç, proliferasyon, yeniden yapılanma) içinde yer alan önemli adımları yansıtan aort halka tahlil kullanılarak değerlendirildi. FK866 tedavi nötrofiller, tedavi edilmemiş hücrelere kıyasla aort şube oluşumunu uyarmak için önemli ölçüde azalmış kapasiteye sahip olduğunu gösterebiliriz (Şekil 3A, 3B). FK866-tedavi edilen anti-anjiyojenik nötrofiller tümör taşıyan fareler içine subkutan enjekte edildi (gün 0 kanat ve gün 2 serum). Tedavi edilmemiş Ifnar1-/- nötrofiller (Şekil 4A, 4B) ile enjekte edilen fareler ile karşılaştırıldığında, önemli ölçüde bozulmuş tümör büyümesini gözlemleyebiliriz. Çıkarılan tümörlerin histolojik incelenmesi, FK866-tedavi edilmiş tans ile tedavi edilen farelerden izole edilmiş tümörlerde anjiyogenezin önemli bastırılmasına neden olduğu gibi, tedavi edilmemiş Ifnar1-/- nötrofiller ile enjekte edilenlere kıyasla ( Şekil 5A , B).
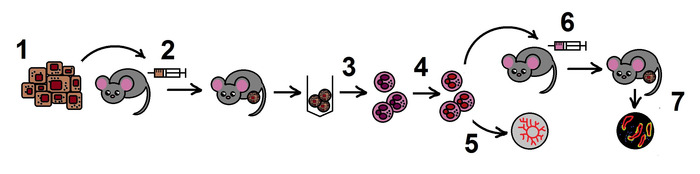
Şekil 1. Protokol şeması. Adım 1. B16F10 melanom hücre hattının hazırlanması; 2. farelerde Allogenik tümör modeli; 3. tümörlerden TANs yalıtım; 4. in vitro TANs NAMPT inhibisyonu; 5. aort halka tahlil TANs anjiyojenik özelliklerinin tahmini; 6. Allogenik tümör modelinde tedavi nötrofillerin evlatlık transferi; 7. tümör büyüme izleme, histolojik muayene. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
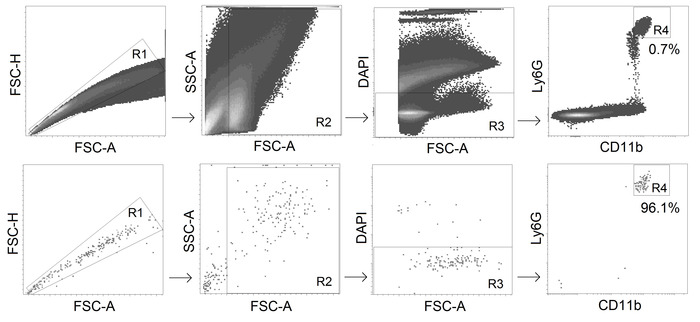
Şekil 2. TANs sıralama için strateji gating. CD11b+ Ly6GHi Alive nötrofiller saflık ile tümörlerden sıralanır ≥ 95%. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.

Şekil 3. FK866 tedavisinden sonra TANs anjiyojenik özelliklerinin bastırılması. FK866 veya orta ile tedavi sıralanmış Ifnar1-/-tans anjiyojenik özellikleri aort yüzük tahlil kullanılarak tahmin edildi. Şube oluşumu 14 gün boyunca izleniyor, 14 gün içinde temsili sonuçlar sunulmuştur (A). FK866 ile tedavi endotel dalları sayısını önemli ölçüde düşürüldü (B). Veriler medyan, çeyrek Aralık ve Min-Max, * p < 0.05 olarak gösterilir. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.

Şekil 4. FK866-tedavi nötrofiller evlatlık transferinden sonra tümör büyümesini geciktirme. TANs 'in tümör büyümesi üzerinde etkisi değerlendirildi. TANs izole edildi, FK866 ile tedavi ve yukarıda açıklandığı gibi tümör taşıyan fareler içine enjekte. Günde 14 fare feda edildi, tümörler kaldırıldı ve analiz edildi. Ifnar1-/- FK866 ile tedavi edilen TANs karşılaştırıldı. (A) tümör büyümesi ölçüldü, (B) tümör kütlesi ve (C) boyutu tahmin edildi. Veriler medyan, çeyrek Aralık ve Min-Max, * p < 0.05 olarak gösterilir. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
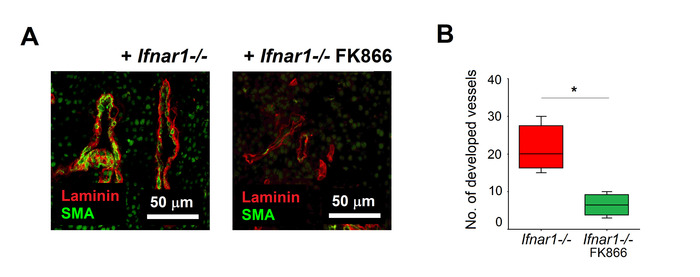
Şekil 5. FK866-tedavi nötrofiller evlatlık transferinden sonra bastırılmış tümör vaskülarizasyon. Tümörler yukarıda açıklandığı gibi izole edildi (şek 4). Gemi olgunlaşma Anti-SMA antikorları (olgun gemiler) ve anti-gama laminin (endotel hücreler) kullanılarak değerlendirildi. (A) tümörün boyama temsili GÖSTERILIR: sma (yeşil), laminin (kırmızı). Ölçek çubukları: 50 μm. (B) FK866 (yeşil) veya orta (kırmızı) Ile yetiştirilen tanların evlatlık transferinden sonra tümör vaskülarizasyonun ölçülmesini, medyan, ara dörtsel Aralık ve Min-Max, * p < 0.05 olarak gösterilir. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
Tartışmalar
Cerrahi ve farmakolojik kanser tedavisinde ilerlemeye rağmen başarılı tedavi bir zorluk olarak kalır. Bağışıklık hücrelerinin tümör büyümesi düzenlenmesi önemli bir rol oynamak için bilinen bu yana, bu tür hücrelerin tümörleri inhibe yeni yöntemler kurulmalıdır. Burada, Anti-anjiyojenik tümör ilişkili nötrofillerin evlatlık aktarımı yoluyla tümör büyümesini bastırmak için yeni bir yaklaşım gösteriyoruz. FK866 inhibitörü kullanarak TANs 'de Pro-anjiyojenik NAMPT sinyallerinin seçmeli olarak hedeflenmesi, sistemik FK866 tedavi üzerine gözlenen yan etkileri önler.
Protokolün en kritik kısmı, taze izole primer nötrofiller kullanma ihtiyacıdır. Nötrofiller, kısa yaşam hücreleridir, apoptozis geçiren veya yalıtım prosedürü sırasında aktive edilir. Murine nötrofiller, hücre sıralama da dahil olmak üzere tüm yalıtım adımları sırasında 4 °C ' de medyada tutulmalıdır. Nötrofiller izolasyonu mümkün olan en kısa sürede yapılmalıdır ve deneme duraklatılmamalıdır. FC-Block kullanımı, NK hücreleri gibi yüksek FC-reseptör ifadesi ile hücrelerin spesifik olmayan lekenin azaltılması sağlar. Ayrıca, gating stratejisini basitleştirmek ve antikor bağlayıcı nedeniyle nötrofiller aktivasyonunu önlemek için floresan konjuçe antikorların sayısını en aza indirmek için tavsiye ederiz.
Protokolün sınırlama adım tümörlerde bu hücrelerin nispeten düşük miktarda nedeniyle tümörler canlı nötrofil yalıtım (Melanoma tek canlı hücrelerin% 1 ' den fazla değil). Bu sadece akış cytometri tabanlı sıralama kullanılarak mümkün olabilir. Aynı zamanda, bu protokol için kan nötrofiller kullanımı NAMPT ifade sadece küçük düzenleme nedeniyle kaçınılmalıdır ve onların düşük işlevsellik, hangi tümör dokusu varış üzerine değiştirildi16. Muhtemelen, kan nötrofiller kullanmak için, daha önce tümör kaynaklı büyüme faktörleri kullanılarak aktive edilmelidir.
Nötrofil apoptoz önlemek için, FK866 ile kısa tedavi (2-4 h) tavsiye edilir, Tans canlılığı üzerinde etkisi olmadığı gibi, uzun süreli tedavi nötrofil apoptozis indükler16. Toplam olarak, protokol, fare Melanom tümör modelinde tümör büyümesini işlevsel olarak bastırmak için EX vitro manipüle edilmiş anti-anjiyojenik nötrofiller potansiyelini gösterir.
Açıklamalar
Yazarların ifşa etmesi gereken hiçbir şey yok.
Teşekkürler
Çalışmalarımız Deutsche Krebshilfe, Grant numarası: 111647 ve Alman Araştırma Konseyi (DFG), Grant numarası: JA 2461/2-1 ' den gelen hibe tarafından destekleniyordu.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 15 ml tubes | Sarstedt AG & Co., Nümbrecht, Germany | 62,554,502 | |
| 50 ml tubes | Cellstar, Greiner Bio One International GmbH, Frickenhausen, Germany | 227261 | |
| 5ml / 10ml / 25ml sterile tipps for the automatic pipette | Cellstar, Greiner Bio One International GmbH, Frickenhausen, Germany | 6006180 / 607180 / 760180 | |
| 6 well flat-bottom cell culture plates | Sarstedt AG & Co., Nümbrecht, Germany | 833,920 | |
| 96 well flat-bottom cell culture plates | Cellstar, Greiner Bio One International GmbH, Frickenhausen, Germany | 655180 | |
| 96 well U-bottom cell culture plates | Cellstar, Greiner Bio One International GmbH, Frickenhausen, Germany | 65018 | |
| AMG EVOS fl digital inverted microscope | AMG, Bothel, U.S. | ||
| anti-mouse CD11b | BD Pharmigen, Becton Dickinson, Franklin Lakes, U.S. | 553312 | clone M1/70, APC-conjugated, 0.2mg/mL |
| anti-mouse Ly6G | BioLegend, California, U.S. | 127608 | clone 1A8, PE-conjugated, 0.2mg/mL |
| BD FACS AriaII | BD Biosciences, Becton Dickinson, Franklin Lakes, U.S. | cell sorter | |
| Caliper | Vogel Germany, Kevelaer, Germany | ||
| Casy cell counter | Innovatis, Roche Innovatis AG, Bielefeld, Germany | ||
| Cell Trics 50µm / 100 µm sterile filters | Sysmex Partec GmbH, Goerlitz, Germany | 04-004-2327 / 04-004-2328 | |
| Centrifuge Rotina 420 R | Andreas Hettich, Tuttlingen, Germany | 4706 | |
| Collagenase D | Sigma-Aldrich/Merck, Darmstadt, Germany | 11088858001 | |
| DAPI (4',6-Diamidino-2-Phenylindole, Dilactate) | BioLegend, California, U.S. | 422801 | Stock: 5mg/ml |
| Dispase I | Sigma-Aldrich/Merck, Darmstadt, Germany | D4818-2MG | |
| DMEM | Gibco, Life Technologies/Thermo Fisher Scientific, Massachusetts, U.S. | 41966-029 | DMEM complete: DMEM + 10% FBS + 1% penicillin-streptomycin |
| DMSO (Dimethylsufoxide) | WAK-Chemie Medical GmbH, Steinbach, Germany | WAK-DMSO-10 | CryoSure-DMSO |
| DNase I | Sigma-Aldrich/Merck, Darmstadt, Germany | DN25-100MG | |
| DPBS | Gibco, Life Technologies/Thermo Fisher Scientific, Massachusetts, U.S. | 14190-094 | |
| Endothelial cell growth medium | PromoCell, Heidelberg, Germany | c-22010 | |
| FBS (Fetal Bovine Serum) | Biochrom, Berlin, Germany | S0115 | |
| Fc-block (Anti-mouse CD16/32) | BD Pharmingen, Becton Dickinson,Becton Dickinson, Franklin Lakes, U.S. | 553142 | clone 2.4G2, Stock: 0.5mg/mL |
| FK 866 hydrochloride | Axon Medchem, Groningen, Netherlands | Axon 1546 | Stock: 100 mM |
| Goat Anti-Rabbit IgG H&L | Abcam, Cambridge, U.K. | ab97075 | Cy3-conjugated, Stock: 0.5 mg/mL |
| Heracell 240i CO2 Incubator | Thermo Fisher Scientific, Waltham, U.S. | 51026334 | |
| IMDM | Gibco, Life Technologies/Thermo Fisher Scientific, Massachusetts, U.S. | 12440-053 | IMDM complete: IMDM + 10% FBS + 1% penicillin-streptomycin |
| Isis GT420 shaver | B. Braun Asculap, Suhl, Germany | 90200714 | |
| Matrigel Matrix basement membrane | Corning Life Sciences, Amsterdam, Netherlands | 7205011 | |
| Microtome Cryostat Microm HM 505 N | Microm International GmbH, Walldorf, Germany | ||
| Monoclonal Anti-Actin, α-Smooth Muscle | Sigma-Aldrich/Merck, Darmstadt, Germany | F3777 | FITC-conjugated, no information about stock concentration |
| Needles 0.4 mm x 16 mm | BD Microlance, Becton Dicson, Becton Dickinson, Franklin Lakes, U.S. | 302200 | |
| Neomount | Merck, Darmstadt, Germany | HX67590916 | |
| Normal goat serum | Jackson ImmunoResearch Laboratories, West Grove, U.S. | 005-000-121 | |
| Penicillin Streptomycin | Gibco, Life Technologies/Thermo Fisher Scientific, Massachusetts, U.S. | 15140-122 | |
| Pipetus automatic pipette | Hirschmann Laborgeräte, Eberstadt, Germany | 9907200 | |
| ProLong Gold Antifade Mountant with DAPI | Invitrogen, Thermo Fisher Scientific, Massachusetts, U.S. | P36935 | |
| rabbit anti mouse Laminin gamma 1 chain | Immundiagnostik, Bensheim, Germany | AP1001.1 | No information about stock concentration |
| StemPro Accutase | Gibco, Life Technologies/Thermo Fisher Scientific, Massachusetts, U.S. | A1105-01 | |
| Sterile disposal scalpel (no. 15) | MedWare, Naples, U.S. | 120920 | |
| Syringes 1 ml | BD Plastipak, Becton Dickinson, Franklin Lakes, U.S. | 303172 | |
| Syringes 10 ml | BD Discardit II, Becton Dickinson, Franklin Lakes, U.S. | 309110 | |
| T75 sterile cell culture flasks | Sarstedt AG & Co., Nümbrecht, Germany | 833,911,302 | |
| Tissue-Tek O.C.T. Compound | Sakura Finetek, Torrance, U.S. | 4583 | |
| Zeiss AxioObserver.Z1 Inverted Microscope with ApoTome Optical Sectioning | Carl Zeiss, Oberkochen, Germany |
Referanslar
- Jablonska, J., Leschner, S., Westphal, K., Lienenklaus, S., Weiss, S. Neutrophils responsive to endogenous IFN-beta regulate tumor angiogenesis and growth in a mouse tumor model. Journal of Clinical Investigation. 120 (4), 1151-1164 (2010).
- Andzinski, L., Wu, C. F., Lienenklaus, S., Kröger, A., Weiss, S., Jablonska, J. Delayed apoptosis of tumor associated neutrophils in the absence of endogenous IFN-β. International Journal of Cancer. 136, 572-583 (2015).
- Rongvaux, A., et al. Pre-B-cell colony-enhancing factor, whose expression is upregulated in activated lymphocytes, is a nicotinamide phosphoribosyltransferase, a cytosolic enzyme involved in NAD biosynthesis. European Journal of Immunology. 32, 3225-3234 (2002).
- Skokowa, J., et al. NAMPT is essential for the G-CSF-induced myeloid differentiation via a NAD(+)-sirtuin-1-dependent pathway. Nature Medicine. 15, 151-158 (2009).
- Yaku, K., Okabe, K., Hikosaka, K., Nakagawa, T. NAD Metabolism in Cancer Therapeutics. Frontiers in Oncology. 8, 622(2018).
- Audrito, V., et al. Extracellular nicotinamide phosphoribosyltransferase (NAMPT) promotes M2 macrophage polarization in chronic lymphocytic leukemia. Blood. 125, 111-123 (2015).
- Brentano, F., et al. Pre-B cell colony-enhancing factor/visfatin, a new marker of inflammation in rheumatoid arthritis with proinflammatory and matrix degrading activities. Arthritis & Rheumatology. 56, 2829-2839 (2007).
- Jablonska, J., Wu, C. -F., Andzinski, L., Leschner, S., Weiss, S. CXCR2-mediated tumor associated neutrophilrecruitment is regulated by IFN-beta. International Journal of Cancer. 134, 1346-1358 (2014).
- Andzinski, L., et al. Type I IFNs induce anti-tumor polarization of tumor associated neutrophils in mice and human. International Journal of Cancer. 138, 1982-1993 (2016).
- Wu, C. -F., et al. The lack of type I interferon induces neutrophil-mediated pre-metastatic niche formation in the mouse lung. International Journal of Cancer. 137, 837-847 (2015).
- Hansel, T. T., Kropshofer, H., Singer, T., Mitchell, J. A., George, A. J. The safety and side effects of monoclonal antibodies. Nature Reviews Drug Discovery. 9 (4), 325-338 (2010).
- Hasmann, M., Schemainda, I. FK866, a highly specific noncompetitive inhibitor of nicotinamide phosphoribosyltransferase, represents a novel mechanism for induction of tumor cell apoptosis. Cancer Research. 63, 7436-7442 (2003).
- Holen, K., Saltz, L. B., Hollywood, E., Burk, K., Hanauske, A. R. The pharmacokinetics, toxicities, and biologic effects of FK866, a nicotinamide adenine dinucleotide biosynthesis inhibitor. Investigational New Drugs. 26, 45-51 (2008).
- von Heideman, A., Berglund, A., Larsson, R., Nygren, P. Safety and efficacy of NAD depleting cancer drugs: results of a phase I clinical trial of CHS 828 and overview of published data. Cancer Cancer Chemotherapy and Pharmacology. 65, 1165-1172 (2010).
- De Rossi, G., Scotland, R., Whiteford, J. Critical Factors in Measuring Angiogenesis Using the Aortic Ring Model. Journal of Genetic Syndromes and Gene Therapy. 4 (5), (2013).
- Pylaeva, E., et al. NAMPT signaling is critical for the proangiogenic activity of tumor-associated neutrophils. International Journal of Cancer. 144 (1), 136-149 (2019).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır