Method Article
조작된 종양 관련 호중구를 종양 베어링 마우스로 옮겨 생체 내 혈관신생 잠재력을 연구합니다.
요약
여기에서, 우리는 종양 을 지탱하는 마우스로의 그들의 전송 후에 항 혈관신생 종양 관련 호중구의 치료 잠재력을 보여줍니다. 이 프로토콜은 생체외 호중구 활성을 조작하고 이후에 종양 을 개발하는 생체 내에서 그들의 기능을 평가하는 데 사용될 수 있다. 그것은 잠재적인 호중구 기지를 둔 면역 요법을 공부를 위한 적당한 모형입니다.
초록
종양 발생의 조절에 호중구의 기여는 증가 관심을 받고있다. 이들 세포는 이질적이며, 종양에 따라 milieu는 프로-또는 항종양 용량을 보유할 수 있다. 종양 문맥에서 호중구 기능을 조절하는 중요한 사이토카인 중 하나는 타입 I 인터페론이다. 인터페론이있는 경우 호중구는 세포 독성 또는 면역 계통의 자극을 포함한 항 종양 특성을 얻습니다. 반대로, 인터페론 신호의 부재는 종양 혈관 신생의 강한 자극을 특징으로하는 눈에 띄는 프로 종양 활성을 초래합니다. 최근, 우리는 호중구의 친 혈관 신생 특성이 이들 세포에서 니코틴아미드 포스포리보실 트랜스퍼라제 (NAMPT) 신호 전달 경로의 활성화에 의존한다는 것을 입증 할 수 있었다. 종양 관련 호중구에서이 통로의 억제는 강력한 항 혈관 신생 표현형으로 이어집니다. 여기에서, 우리는 조작된 종양 관련 호중구 (TAN)의 종양성 잠재력의 생체 내 평가를 허용하는 우리의 새로 확립된 모형을 설명합니다. 곧, 프로-혈관신생 종양 관련 호중구는 종양 베어링 인터페론 결핍 마우스로부터 분리되고 NAMPT 신호의 차단에 의해 항 혈관신생 표현형으로 재편분화될 수 있다. 이들 세포의 혈관신생 활성은 대동맥 고리 분석술을 사용하여 이후에 평가될 수 있다. 항-혈관신생 TAN은 종양을 지탱하는 야생형 수용자로 옮겨질 수 있으며 종양 성장은 14일 동안 모니터링되어야 한다. 일째에 14 마우스는 희생되고, 종양은 그들의 혈관세포로 제거되고 절단됩니다. 전반적으로, 우리의 프로토콜은 인공 호중구 세포주 모델을 사용할 필요 없이 종양 관련 호중구와 같은 1차 세포의 혈관신생 용량을 생체 내에서 평가하는 새로운 도구를 제공한다. Vc
서문
타입 I 인터페론(IFN)은 신생물에 대한 숙주 반응의 자극에 중요한 역할을 하며, I형 IFN 신호의결여는 종양 성장을 현저히 상승시키는 결과이다 1. 이 과정에 관여하는 메커니즘 중 하나는 종양 관련 호중구의 종양 성 활성의 조절이며, 이는 콜로니 자극 인자 3 수용체 (CSF3R) 다운스트림 신호에 의해 제어된다. 콜로니-자극 인자 3(CSF3) 또는 과립구 콜로니-자극 인자, 니코틴아미드 포스포리보실트랜스퍼라제(NAMPT)를 포함하는시그널링을 활성화시키는 것으로 나타났다 3,4. NAMPT는 니코틴아미드 아데닌 디뉴클레오티드 합성을 위한 속도 제한 효소로서, 이는 글리콜분해를 강화하고 DNA 수리, 유전자 발현 및 스트레스 반응을 조절하여 암세포의 생존및 증식을 촉진시킨다. 5. NAMPT는 대장, 난소, 유방, 위, 전립선암 및 글리오마 6을 포함하는다중 암 모형에서 과발현됩니다. NAMPT는 종양 세포뿐만 아니라 골수성 세포와 같은 종양에 존재하는 다양한 다른 세포 유형에 필수적입니다 - 그것은그들의 분화 4를 구동하고, 세포 자멸을 억제하고 다중 사이토카인의 발현을 자극하거나 대식세포에서 매트릭스 분해 효소7.
종양 관련 호중구는 종양 성장의 중요한 변조기를 나타냅니다. TAN 함수는 이들 사이토카인이 호중구의 항종양 활성을 주요화함에 따라 I IFN 유형의 가용성에 강하게 의존한다. 반대로 IFN의 부재는 이러한 세포, 특히 친 혈관 신생 특성의 종양 성 활성화를 지원합니다. 이에 동의하여 IFN결핍 마우스는 상당히 크고 더 나은 혈관화 종양을 개발하며, 이는 종양/친혈관성 호중구1, 2,8, 9,10. 중요한 것은, 이러한 친 혈관신생 TAn은 NAMPT의 높은 활성을 보여주며, 호중구의 종양 편광에 필수적인 역할을 시사합니다.
Ly6G 항체를 이용한 호중구의 고갈 또는 이들의 이동(CXCR2 항체)의 억제는 종양 혈관신생, 성장 및 전이 감소를 초래하는1,8. 그럼에도 불구하고, 생성된 단일클론 항체는 면역원성이며, 이들의 투여는 생명을 위협하는다양한 부작용(11)과 연관된다. 호중구 종양발생성을 조절하는 NAMPT 억제제 FK866과 같은 소분자를 치료하는 것은 그러한 합병증을 피하는 데 도움이 될 수 있다. 불행히도, 종양 성장에 대한 치료 효과 옆에 있는 NAMPT의 약리학적 전신 억제는 위장 독성 및 혈소판 감소증을 포함한 심각한 부작용을 초래한다. 따라서 NAMPT 억제제의 전신 적용은12,13,14.
이러한 이유로 NAMPT 활동이 격리된 TAN에서 직접 차단되는 프로토콜을 제안합니다. 이러한 항종양 호중구는 종양 베어링 숙주로 채택적으로 전달됩니다. 이 프로토콜은 화합물의 전신 독성 부작용을 피하는 데 도움이 될 것입니다., 대상 세포에 미치는 영향은 지속 될 것 이다 하는 동안.
프로토콜
동물 과목을 포함한 모든 절차는 규제 당국에 의해 승인되었습니다: LANUV (란데삼트 퓌르 나투르, 움웰트 und Verbraucherschutz NRW) 및 Regierungspräsidium 튀빙겐, 독일. 모든 조작은 멸균 시약 및 기기 (주사기, 가위, 집게, 일회용 메스, 페트리 접시)를 사용하여 멸균 조건 (층류 흐름 후드 아래)에서 수행해야합니다.
참고: 프로토콜의 전체 구성표는 그림1에 나와 있습니다.
1. B16F10 흑색종 세포주의 준비
- 마이코플라즈마-음성 세포를 90% 동급 단일층(약 10 x 106 세포/T75 플라스크)으로 완전히 이스코브의 변형된 덜베코 배지(IMDMc: IMDMc: IMDM + 10% 태아 소 세럼(FBS) + 1% 페니실린-스트렙토마이신)로 준비합니다.
- 배지를 제거하고, 인산완충식염수(PBS)로 세포를 헹구는다. 프로테올액 및 콜라주용 효소를 함유한 세포 분리 용액 6 mL을 적용하고(재료 표참조), 37°C에서 2분 동안 배양합니다.
- 플라스크를 부드럽게 두드려 바닥에서 남은 부착 세포를 동원합니다. 15 mL 튜브및 원심분리기에서 세포 현탁액을 7분 및 20°C에 300 x g에서 수집합니다.
- 상급체를 제거하고, PBS의 1 mL에서 펠릿을 잘 다시 놓습니다. PBS와 원심분리기 14mL(300 x g, 20°C를 7분 동안 추가).
- 상급체를 제거하고 PBS 의 1 mL에서 펠릿을 다시 일시 중단하십시오.
- 세포를 카운트하고, 주사를 위해 3 x 106/mLPBS(2단계) 또는 6 x 106/mLPBS(6단계)의 농도로 다시 중단한다. 최대 30분 동안 얼음 에 세포를 보관하십시오.
2. 마우스에 있는 동종 종양 모형
- 특정 병원균이 없는 (SPF) 조건하에서 보관되는 10암컷 Ifnar1-/- 마우스 8-12주령을 사용하십시오.
참고: 암컷 마우스는 종양 성장의 피하 모형에서 바람직합니다, 남성은 종양 성장에 영향을 미치는 종양 사이트의 위반에 더 공격적이고 그러므로 수그리기 때문에. - 전기 면도기로 측면에 마우스의 피부를 면도하고, 70 % 에탄올 젖은 조직으로 피부를 소독.
- 제조된 B16F10 흑색종 세포를 1 mL주사기 및 0.4 x 19 mm 바늘에서 3 x 10 6/mL PBS(단계 1 참조)의 농도로 수집한다. 현탁액의 100 mL을 피하로 주입하십시오.
- 모든 주입 전에 세포를 잘 섞으세요. 종양 세포를 방해하지 않도록 직경이 0.4 mm 이상인 바늘을 사용하십시오.
- 한 케이지에 최대 5마리의 마우스를 놓고, 14일 동안 캘리퍼스로 종양 크기(길이, 너비 및 깊이)를 조절합니다.
참고 : 동물 규정에 따르면 종양 크기는 직경이 15mm를 초과해서는 안되며, 더 크거나 괴사 / 열린 종양이있는 마우스는 사전에 희생해야합니다. - 14일째에, CO2 챔버에서 마우스를 희생한다.
- 70 % 에탄올로 피부를 소독하고 멸균 페트리 접시에 가위와 집게로 종양을 제거하십시오. 완전한 덜베코의 수정 된 독수리 매체 (DMEMc : DMEM + 10 % FBS + 1 % 페니실린 - 스트렙토 마이신)에 있는 50 mL 튜브에 종양을 얼음에 보관하십시오.
3. 탄 격리
- 종양을 멸균 된 6 웰 플레이트에 넣고 잘 당 5 개의 종양을 넣습니다. 종양을 멸균 가위로 2-3mm 조각으로 자릅니다.
- 종양 당 디스파제/콜라게나제 D/DNase I 용액 1 mL(0.2 mg/0.2 mg/100 mg의 DMEMc 1mL)으로 소화합니다. 습한 인큐베이터에서 37°C, 5% CO2에서 배양하고, 15분마다 3회마다 바늘 없이 10 mL 주사기와 혼합한다.
- 소화되지 않은 섬유를 제거하려면 100 μm 필터를 통해 15 mL 튜브 (튜브 당 필터 당 1 개)로 메쉬 세포. PBS를 15 mL에 추가하고 원심 분리 튜브를 460 x g, 4 °C에서 5 분 동안 추가하고 상한을 제거합니다.
- 라시스 완충액을 가진 리스적혈구(NH4Cl 150 mM, KHCO3 10 mM, EDTA 0.1 mM, pH 7.3, 20°C)를 각 튜브에 1 mL을 첨가하였다. 잘 혼합하고 모든 튜브의 용액을 하나로 결합합니다. 11 mL의 얼음-차가운(4°C) DMEMc로 2분 후에 반응을 멈춥니다.
- 460 x g, 4°C에서 5분 동안 원심분리기를 제거하고 상위를 제거한다. 차가운 PBS 15 mL로 펠릿을 다시 일시 중단하십시오. 460 x g, 4°C에서 5분 동안 원심분리기를 제거하고 상위를 제거한다.
- PBS의 1 mL에서 펠릿을 다시 일시 중단합니다. Fc 블록 항체 3 mL (CD16 / CD32, 재고 0.5 mg / mL)을 추가하고 15 분 동안 얼음에 배양하십시오.
- 항체 추가: Ly6G-PE 10 mL (재고 0.2 mg/mL) 및 CD11b-APC 10 mL (재고 0.2 mg/mL). 6-디아미딘-2-페닐린돌 생존용 염료 20 mL(DAPI, 스톡 5 mg/mL)를 넣고 30분 동안 얼음에 배양합니다.
참고 : 항체의 생존 성 염료와 형광 접합체의 또 다른 조합을 사용할 수 있습니다. - PBS를 최대 15 mL, 원심분리기를 460 x g,4°C에서 5분 동안 넣고 상한을 제거합니다.
- DMEMc의 펠릿을 약 10 x 106/mL의 농도로 다시 중단하고 얼음을 유지합니다.
- 정렬 CD11b+ Ly6Ghi alive (DAPI-음성) 형광 활성화 세포 선별기를 가진 호중구 (게이팅 전략 참조 도 2참조).
참고: 튜브를 셀 현탁액으로 유지하고 튜브를 DMEMc로 4°C에서 분류된 셀로 유지합니다. 70mm 노즐, 초당 최대 22,000개의 이벤트 임계값 및 1-3의 유량등 다음과 같은 최적의 정렬 설정을 사용합니다. - 세포계를 사용하여 분류된 호중구의 순도를 확인하여 >95%의 권장 순도를 확인하십시오.
- 원심분리기는 460 x g, 4°C에서 호중구를 5분 동안 분류하고, 상구체를 제거하였다. DMEMc에서 정렬된 셀을 1 x 106/mL의 농도로 다시 중단합니다.
참고: 14일 B16F10 종양(직경 10mm)에서 호중구의 예상 수는 약 3 x 104 세포입니다.
4. 시험관내 TAN에서의 NAMPT 억제
- FK866(NAMPT 억제제) 스톡을 디메틸설폭사이드(DMSO)에서 100 mM의 최종 농도로 준비한다.
- 종자 정렬 호중구 (단계 3.11) 2 웰의 96 웰 U-바닥 플레이트 (1.5 x 105 호중구 / 우물). FK866을 개입 웰(100 nM의 최종 농도)에 추가하고 DMSO를 제어하는 것과 동일한 양의 DMEMc를 제어웰에 추가합니다. 습한 인큐베이터에서 37°C에서 2시간 동안 배양하고, 5% CO2를 배양한다.
- 460 x g, 4°C에서 5분 동안 원심분리기를 제거하고 상위를 제거한다. 각 우물에서 PBS의 200 mL에 다시 일시 중단. 2회 반복합니다.
- 460 x g, 4°C에서 5분 동안 원심분리기를 제거하고 상위를 제거한다. 상업적인 내피 세포 성장 매체에 재중단 (4 μL/mL 내피 세포 성장 보충교재보충, 0.1 ng/mL 재조합 인간 표피 성장 인자, 1 ng/mL 재조합 인간 기본 섬유아세포 성장 인자, 90 μg/mL 헤파린 및 1 μg/mL 하이드로코르티손)의 최종 농도를 0.2 x 106 세포/mL(0.75 mL) (5단계) 또는 PBS에서 0.6 x 106 세포/mL(0.25 mL)의 최종 농도로(6단계)로.
5. 대동맥 고리 분석사를 사용하여 탄의 혈관신생 특성 추정
- 수컷 C57BL/6J(WT) 마우스에서 흉부 대흉을 해부합니다. 0.5mm 너비 의 반지로 청소하고 잘라냅니다. 보충 된 내피 세포 성장 매체의 1 mL와 24 잘 접시의 우물에 모든 반지를 배치합니다. 습한 인큐베이터에서 37°C, 5% CO2에서 밤새 배양한다.
참고: 대동맥 해부에 대한 젊은(8주 미만) 수컷 마우스의 사용은 보다 견고한 혈관신생반응(15)을주기 때문에 바람직하다. - 96웰 평평한 바닥 판의 웰을 용해된 지하 막 매트릭스의 50 μL로 채우고, 37°C, 5%CO2 습습 인큐베이터에서 30분 동안 젤세트를 설정하여 매트릭스가 중합되도록 한다. 조건당 적어도 3개의 웰을 준비합니다.
- 솔리드 매트릭스 층의 상단에 대동맥 링을 배치하여 용해 된 지하 멤브레인 매트릭스에 링을 포함, 각 우물의 중심에 1 링. 각 링을 덮기 위해 용해된 지하 멤브레인 매트릭스를 50 μL 더 추가합니다.
- 플레이트를 37°C, 5%CO2 습한 인큐베이터에 놓고 30분 동안 다른 30분 동안 제2 매트릭스 층의 중합을 허용한다.
- 보충된 내피 세포 성장 배지의 150 mL/well을 추가하고 2x104Ifnar1-/- TAN(대조군 및 FK866-처리)(단계 4.4)을 첨가합니다.
- 습한 인큐베이터에서 37°C, 5% CO2에서 14일 동안 플레이트를 배양한다.
- 표준 상 대비 현미경을 사용하여 이미지를 내피 분기를 추정합니다. 분기 인덱스를 포함한 선박 형태 및 공간 파라미터의 정량적 평가는 과학 이미지를 위해 설계된 이미지 처리 프로그램을 사용하여 자동으로 수행 될 수있다.
참고: 대표 결과는 그림 3에표시됩니다.
6. 알로겐성 종양 모델에서 치료 된 호중구의 채택 전달
- B16F10 흑색종 세포(단계 1.6)를 6 x 106 세포/mL의 농도로 PBS에 준비한다.
- 2가지 유형의 호중구를 준비합니다: FK866 처리호중구 및 PBS에서 처리되지 않은 호중구(단계 4.4)를 농도 6 x 105 세포/mL로 조절한다. 호중구를 B16F10 흑색종 세포(최종 호중구대 종양 세포 비율 1:10)와 혼합하여 2가지 유형의 세포 혼합물을 갖는다.
- 생후 8-12주 된 암컷 WT 마우스 10개, 각 군에서 5개씩 복용한다. 전기 면도기로 옆면의 피부를 면도하고 70 % 에탄올로 소독하십시오.
- 세포 현탁액의 100 μL을 주입 (단계 6.2) 피하 인슐린 주사기와 0.4 mm 직경 바늘, 마우스의 두 그룹에. 같은 그룹에서 1-5개의 마우스를 하나의 케이지에 놓습니다.
- 2일째에, 2종류의 호중구를 준비한다: FK866 처리호중구및 PBS에서 처리되지 않은 호중구(단계 4.4)를 농도 6 x 105 세포/mL로 조절한다. 100 μL의 세포 현탁액(단계 6.4) 즉, 인슐린 주사기와 0.4 mm 직경의 바늘로 꼬리 정맥내로, 두 마우스 의 두 그룹에 주입한다. 마우스를 케이지에 다시 놓습니다.
7. 종양 성장 측정, 조직학적 검사
- 격일로 종양 성장을 모니터링합니다. 캘리퍼스로 종양 크기를 평가하고 공식 V=4/3*π*(h*w 2)/8(h=높이, w=너비, 깊이= 폭)으로 종양 체적을 계산합니다.
- CO2 챔버에서 14일째에 마우스를 희생한다. 종양을 제거하고 종양 가중치를 측정하십시오.
- 액체 질소에서 최적의 절삭 온도 화합물로 종양을 동결하고 -80 °C에서 저장합니다.
- 샘플을 -20°C로 해동하고 저온 종으로 5mm 단면을 준비합니다. 저온 차단을 20 °C에서 30 분 동안 건조시키십시오. 단면을 -20°C 의 차가운 아세톤으로 2분 간 고정하고 20°C에서 30분 동안 건조시키십시오.
- 20 °C에서 1 시간 동안 PBS에서 Fc 블록 항체 (CD16 / CD32, 재고 0.5 mg / mL 1 : 500)로 차단하십시오.
- 토끼 항 마우스 라미닌 감마 항체 (PBS에서 1 :1500, 200 μL)로 얼룩을 20 °C에서 1 시간 동안. PBS로 세 번 씻으시다.
- 이차 염소 항 토끼 항체 (재고 0.5 mg / mL, PBS에서 1 :400), 항 마우스 αSMA (PBS에서 1 :500) 및 DAPI의 2 μL (스톡 5 mg / mL, PBS에서 1 :100)의 최종 부적에서 항체 용액의 최종 부적. 어둠 속에서 20 °C에서 1 시간 동안 배양하십시오. PBS로 세 번 씻으시다.
- 어둠 속에서 20 °C에서 20 분 동안 건조 슬라이드. 현미경 검사를 위해 무수 장착 매체로 장착하고 커버 슬립으로 덮습니다. 37 °C에서 1 h건조시키십시오.
- 현미경 검사를 수행합니다. Laminin+ 혈관의 총 개수(선택적으로 면적)와 SMA+ 개발된 선박의 개수(면적)를 계산하여 혈관을 정량화합니다.
참고: 이미지 분석을 수행하려면 동일한 조건(빛, 대비, 배율)에서 모든 이미지를 찍습니다. 이 경우 처리 매개 변수가 고정되고 이미지 처리가 완전히 자동화됩니다. 대표적인 결과는 그림 4 및 그림5에 도시되어 있습니다.
결과
여기에 기재된 절차를 사용하여, Ifnar1---- 호중구는 종양으로부터 분리되었고, 2시간 동안 NAMPT 억제제 FK866으로 처리하였다. 치료의 효과는 혈관 신생 (매트릭스 분해, 이동, 증식, 재구성)에 관련된 주요 단계를 반영하는 대동맥 고리 분석술을 사용하여 평가되었다. 우리는 FK866 처리된 호중구가 치료되지 않은 세포에 비해 대동맥 분지 형성을 자극하는 용량을 현저히 감소시키는 것을 입증할 수 있었다(도3A,3B). FK866-처리된 항혈관신생 호중구는 종양 베어링 마우스에 피하 주사되었다(0일째 및 2일째 i.v.). 치료되지 않은 Ifnar1-/- 호중구로 주입된 마우스와 비교하여 현저히 손상된 종양 성장을 관찰할 수 있었다(도4A,4B). 추출된 종양의 조직학적 검사는 FK866 처리된 TAN으로 처리된 마우스로부터 분리된 종양에서 혈관신생의 유의한 억제를 입증하였으며, 치료되지 않은 Ifnar1-/- 호중구로 주입한 것과 비교하여 그림 5A ,B).
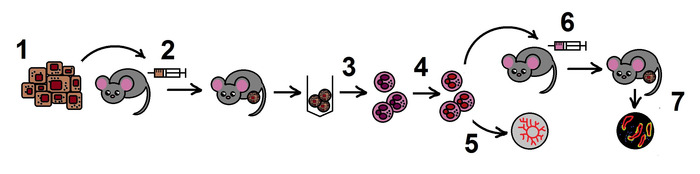
그림 1. 프로토콜의구성표입니다. 1단계. B16F10 흑색종 세포주의 제조; 2. 마우스에서의 동종 종양 모델; 3. 종양에서 TAN의 격리; 4. 시험관에서 TAN에서 NAMPT의 억제; 5. 대동맥 고리 분석에서 탄의 혈관신생 성질의 추정; 6. 종양 종자 모델에서 처리 된 호중구의 채택 적 전달; 7. 종양 성장 모니터링, 조직 학적 검사. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
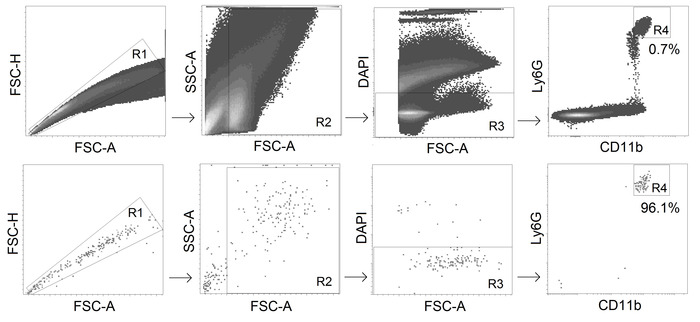
그림 2. TAN 정렬에 대한 게이팅 전략. CD11b+ Ly6Ghi 살아있는 호중구는 순도 ≥95%를 가진 종양으로부터 분류된다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 3. FK866 치료 후 탄의 혈관 신생 특성의억제. FK866 또는 배지로 처리된 이프나르1-/-TAn을정렬된 혈관생성 성질은 대치고리 분석기를 사용하여 추정하였다. 14일 동안 지부 형성을 모니터링하였고, 14일째에대표적인 결과가 제시되었다(A). FK866을 가진 처리는 내피 가지 (B)의 수를 현저하게 감소시었습니다. 데이터는 중앙값, 수분 간 범위 및 최소 최대, *p&0.05로 표시됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 4. FK866 처리 된 호중구의 입양 전이 후 종양 성장의지연. 종양 성장에 대한 TAN의 영향을 평가했습니다. TAN을 분리하고, FK866으로 처리하고, 전술한 바와 같이 종양 지지 마우스에 주입하였다. 일째에 14 마우스는 희생되었다, 종양을 제거하고 분석. Ifnar1-/- FK866과 대조군으로 처리된 TAN을 비교하였다. (a) 종양 성장을 측정하였고, (B) 종양 질량 및 (C) 크기를 추정하였다. 데이터는 중앙값, 수분 간 범위 및 최소 최대, *p&0.05로 표시됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
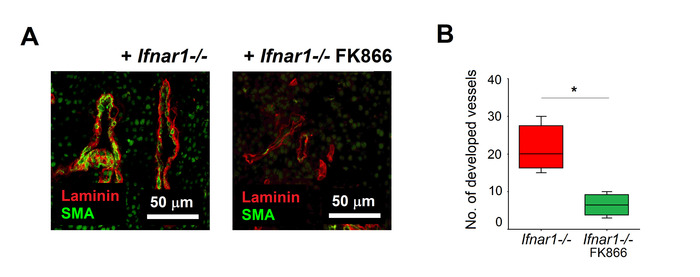
그림 5. FK866-처리된 호중구의 채택 전사 후 종양 혈관화를 억제하였다. 종양은 전술한 바와 같이 단리되었다(도 4). 혈관 성숙은 항-SMA 항체(성숙한 혈관) 및 항감마 라미닌(내피 세포)을 사용하여 평가하였다. (A) 종양의 대표적인 염색이 도시된다: SMA (녹색), 라미닌 (빨강). 스케일 바: 50 μm. (B) FK866(녹색) 또는 중간(적색)으로 배양된 TAN의 채택 전이 후 종양 혈관화의 정량화는 중앙값, 수족간 범위 및 최소 최대, *p&0.05로 나타내어. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
토론
외과 및 약리암 치료의 진행에도 불구하고 성공적인 치료는 여전히 도전과제로 남아 있습니다. 면역 세포는 종양 성장의 조절에 중요한 역할을 하는 것으로 알려져 있기 때문에, 이러한 세포의 종양 발생을 억제하는 새로운 방법이 확립되어야 한다. 여기에서 우리는 항 혈관신생 종양 관련 호중구의 입양 전달을 통해 종양 성장을 억제하는 새로운 접근법을 입증한다. FK866 억제제를 사용하여 탄에서 친 혈관 신생 NAMPT 신호의 선택적 표적화는 전신 FK866 치료 시 관찰되는 부작용을 방지합니다.
프로토콜의 가장 중요한 부분은 갓 분리 된 1 차 호중구를 사용할 필요성입니다. 호중구는 짧은 살아있는 세포, apoptosis를 겪고 또는 격리의 절차 도중 활성화됩니다. 뮤린 호중구는 세포 선별을 포함한 모든 절연 단계 동안 4°C 매체에 보관되어야 한다. 호중구의 격리는 가능한 한 빨리 수행되어야하며 실험을 일시 중지해서는 안됩니다. Fc-블록의 사용은 NK 세포와 같은 높은 Fc 수용체 발현을 가진 세포의 비특이적 염색을 감소시킬 수 있다. 또한 게이팅 전략을 단순화하고 항체 결합으로 인한 호중구의 활성화를 피하기 위해 형광-공액 항체의 수를 최소화하는 것이 좋습니다.
프로토콜의 제한 단계는 종양에서 이들 세포의 상대적으로 낮은 양으로 인해 종양에서 살아있는 호중구의 분리입니다 (흑색종에서 단일 살아있는 세포의 1 % 이상). 이는 유세포분석 기반 정렬을 통해서만 가능할 수 있습니다. 동시에, 이 프로토콜에 대한 혈액 호중구의 사용은 종양 조직 도착 시 변경되는 NAMPT 발현 및 그들의 낮은 기능성의 사소한 조절만으로 인해 피해야 한다16. 아마도, 혈액 호중구를 사용 하기 위해, 그들은 이전에 종양 파생 된 성장 인자를 사용 하 여 활성화 해야.
호중구 아자멸을 피하기 위해 FK866 (2-4 h)으로 짧은 치료가 제안되며, 장기간 치료는 호중구 아자멸을 유발하면서 TAN의 생존력에 영향을 미치지 않기 때문에16. 요약하면, 프로토콜은 마우스 흑색종 종양 모델에서 종양 성장을 기능적으로 억제하는 전외 생체외 조작 항 혈관신생 호중구의 잠재력을 보여준다.
공개
저자는 공개 할 것이 없다.
감사의 말
우리의 일은 도이치 크렙실페의 보조금에 의해 지원되었다, 보조금 번호: 111647, 독일 연구 위원회 (DFG), 보조금 번호: JA 2461/2-1.
자료
| Name | Company | Catalog Number | Comments |
| 15 ml tubes | Sarstedt AG & Co., Nümbrecht, Germany | 62,554,502 | |
| 50 ml tubes | Cellstar, Greiner Bio One International GmbH, Frickenhausen, Germany | 227261 | |
| 5ml / 10ml / 25ml sterile tipps for the automatic pipette | Cellstar, Greiner Bio One International GmbH, Frickenhausen, Germany | 6006180 / 607180 / 760180 | |
| 6 well flat-bottom cell culture plates | Sarstedt AG & Co., Nümbrecht, Germany | 833,920 | |
| 96 well flat-bottom cell culture plates | Cellstar, Greiner Bio One International GmbH, Frickenhausen, Germany | 655180 | |
| 96 well U-bottom cell culture plates | Cellstar, Greiner Bio One International GmbH, Frickenhausen, Germany | 65018 | |
| AMG EVOS fl digital inverted microscope | AMG, Bothel, U.S. | ||
| anti-mouse CD11b | BD Pharmigen, Becton Dickinson, Franklin Lakes, U.S. | 553312 | clone M1/70, APC-conjugated, 0.2mg/mL |
| anti-mouse Ly6G | BioLegend, California, U.S. | 127608 | clone 1A8, PE-conjugated, 0.2mg/mL |
| BD FACS AriaII | BD Biosciences, Becton Dickinson, Franklin Lakes, U.S. | cell sorter | |
| Caliper | Vogel Germany, Kevelaer, Germany | ||
| Casy cell counter | Innovatis, Roche Innovatis AG, Bielefeld, Germany | ||
| Cell Trics 50µm / 100 µm sterile filters | Sysmex Partec GmbH, Goerlitz, Germany | 04-004-2327 / 04-004-2328 | |
| Centrifuge Rotina 420 R | Andreas Hettich, Tuttlingen, Germany | 4706 | |
| Collagenase D | Sigma-Aldrich/Merck, Darmstadt, Germany | 11088858001 | |
| DAPI (4',6-Diamidino-2-Phenylindole, Dilactate) | BioLegend, California, U.S. | 422801 | Stock: 5mg/ml |
| Dispase I | Sigma-Aldrich/Merck, Darmstadt, Germany | D4818-2MG | |
| DMEM | Gibco, Life Technologies/Thermo Fisher Scientific, Massachusetts, U.S. | 41966-029 | DMEM complete: DMEM + 10% FBS + 1% penicillin-streptomycin |
| DMSO (Dimethylsufoxide) | WAK-Chemie Medical GmbH, Steinbach, Germany | WAK-DMSO-10 | CryoSure-DMSO |
| DNase I | Sigma-Aldrich/Merck, Darmstadt, Germany | DN25-100MG | |
| DPBS | Gibco, Life Technologies/Thermo Fisher Scientific, Massachusetts, U.S. | 14190-094 | |
| Endothelial cell growth medium | PromoCell, Heidelberg, Germany | c-22010 | |
| FBS (Fetal Bovine Serum) | Biochrom, Berlin, Germany | S0115 | |
| Fc-block (Anti-mouse CD16/32) | BD Pharmingen, Becton Dickinson,Becton Dickinson, Franklin Lakes, U.S. | 553142 | clone 2.4G2, Stock: 0.5mg/mL |
| FK 866 hydrochloride | Axon Medchem, Groningen, Netherlands | Axon 1546 | Stock: 100 mM |
| Goat Anti-Rabbit IgG H&L | Abcam, Cambridge, U.K. | ab97075 | Cy3-conjugated, Stock: 0.5 mg/mL |
| Heracell 240i CO2 Incubator | Thermo Fisher Scientific, Waltham, U.S. | 51026334 | |
| IMDM | Gibco, Life Technologies/Thermo Fisher Scientific, Massachusetts, U.S. | 12440-053 | IMDM complete: IMDM + 10% FBS + 1% penicillin-streptomycin |
| Isis GT420 shaver | B. Braun Asculap, Suhl, Germany | 90200714 | |
| Matrigel Matrix basement membrane | Corning Life Sciences, Amsterdam, Netherlands | 7205011 | |
| Microtome Cryostat Microm HM 505 N | Microm International GmbH, Walldorf, Germany | ||
| Monoclonal Anti-Actin, α-Smooth Muscle | Sigma-Aldrich/Merck, Darmstadt, Germany | F3777 | FITC-conjugated, no information about stock concentration |
| Needles 0.4 mm x 16 mm | BD Microlance, Becton Dicson, Becton Dickinson, Franklin Lakes, U.S. | 302200 | |
| Neomount | Merck, Darmstadt, Germany | HX67590916 | |
| Normal goat serum | Jackson ImmunoResearch Laboratories, West Grove, U.S. | 005-000-121 | |
| Penicillin Streptomycin | Gibco, Life Technologies/Thermo Fisher Scientific, Massachusetts, U.S. | 15140-122 | |
| Pipetus automatic pipette | Hirschmann Laborgeräte, Eberstadt, Germany | 9907200 | |
| ProLong Gold Antifade Mountant with DAPI | Invitrogen, Thermo Fisher Scientific, Massachusetts, U.S. | P36935 | |
| rabbit anti mouse Laminin gamma 1 chain | Immundiagnostik, Bensheim, Germany | AP1001.1 | No information about stock concentration |
| StemPro Accutase | Gibco, Life Technologies/Thermo Fisher Scientific, Massachusetts, U.S. | A1105-01 | |
| Sterile disposal scalpel (no. 15) | MedWare, Naples, U.S. | 120920 | |
| Syringes 1 ml | BD Plastipak, Becton Dickinson, Franklin Lakes, U.S. | 303172 | |
| Syringes 10 ml | BD Discardit II, Becton Dickinson, Franklin Lakes, U.S. | 309110 | |
| T75 sterile cell culture flasks | Sarstedt AG & Co., Nümbrecht, Germany | 833,911,302 | |
| Tissue-Tek O.C.T. Compound | Sakura Finetek, Torrance, U.S. | 4583 | |
| Zeiss AxioObserver.Z1 Inverted Microscope with ApoTome Optical Sectioning | Carl Zeiss, Oberkochen, Germany |
참고문헌
- Jablonska, J., Leschner, S., Westphal, K., Lienenklaus, S., Weiss, S. Neutrophils responsive to endogenous IFN-beta regulate tumor angiogenesis and growth in a mouse tumor model. Journal of Clinical Investigation. 120 (4), 1151-1164 (2010).
- Andzinski, L., Wu, C. F., Lienenklaus, S., Kröger, A., Weiss, S., Jablonska, J. Delayed apoptosis of tumor associated neutrophils in the absence of endogenous IFN-β. International Journal of Cancer. 136, 572-583 (2015).
- Rongvaux, A., et al. Pre-B-cell colony-enhancing factor, whose expression is upregulated in activated lymphocytes, is a nicotinamide phosphoribosyltransferase, a cytosolic enzyme involved in NAD biosynthesis. European Journal of Immunology. 32, 3225-3234 (2002).
- Skokowa, J., et al. NAMPT is essential for the G-CSF-induced myeloid differentiation via a NAD(+)-sirtuin-1-dependent pathway. Nature Medicine. 15, 151-158 (2009).
- Yaku, K., Okabe, K., Hikosaka, K., Nakagawa, T. NAD Metabolism in Cancer Therapeutics. Frontiers in Oncology. 8, 622(2018).
- Audrito, V., et al. Extracellular nicotinamide phosphoribosyltransferase (NAMPT) promotes M2 macrophage polarization in chronic lymphocytic leukemia. Blood. 125, 111-123 (2015).
- Brentano, F., et al. Pre-B cell colony-enhancing factor/visfatin, a new marker of inflammation in rheumatoid arthritis with proinflammatory and matrix degrading activities. Arthritis & Rheumatology. 56, 2829-2839 (2007).
- Jablonska, J., Wu, C. -F., Andzinski, L., Leschner, S., Weiss, S. CXCR2-mediated tumor associated neutrophilrecruitment is regulated by IFN-beta. International Journal of Cancer. 134, 1346-1358 (2014).
- Andzinski, L., et al. Type I IFNs induce anti-tumor polarization of tumor associated neutrophils in mice and human. International Journal of Cancer. 138, 1982-1993 (2016).
- Wu, C. -F., et al. The lack of type I interferon induces neutrophil-mediated pre-metastatic niche formation in the mouse lung. International Journal of Cancer. 137, 837-847 (2015).
- Hansel, T. T., Kropshofer, H., Singer, T., Mitchell, J. A., George, A. J. The safety and side effects of monoclonal antibodies. Nature Reviews Drug Discovery. 9 (4), 325-338 (2010).
- Hasmann, M., Schemainda, I. FK866, a highly specific noncompetitive inhibitor of nicotinamide phosphoribosyltransferase, represents a novel mechanism for induction of tumor cell apoptosis. Cancer Research. 63, 7436-7442 (2003).
- Holen, K., Saltz, L. B., Hollywood, E., Burk, K., Hanauske, A. R. The pharmacokinetics, toxicities, and biologic effects of FK866, a nicotinamide adenine dinucleotide biosynthesis inhibitor. Investigational New Drugs. 26, 45-51 (2008).
- von Heideman, A., Berglund, A., Larsson, R., Nygren, P. Safety and efficacy of NAD depleting cancer drugs: results of a phase I clinical trial of CHS 828 and overview of published data. Cancer Cancer Chemotherapy and Pharmacology. 65, 1165-1172 (2010).
- De Rossi, G., Scotland, R., Whiteford, J. Critical Factors in Measuring Angiogenesis Using the Aortic Ring Model. Journal of Genetic Syndromes and Gene Therapy. 4 (5), (2013).
- Pylaeva, E., et al. NAMPT signaling is critical for the proangiogenic activity of tumor-associated neutrophils. International Journal of Cancer. 144 (1), 136-149 (2019).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유