Method Article
Üç Afatinib dirençli akciğer adenokarsinoma PC-9 hücre hatları Afatinib artan dozlarda ile geliştirilen kurulması ve karakterizasyonu
Bu Makalede
Özet
Akciğer adenokarsinoma PC-9 hücrelerinden afatinib-direnç hücre hatları kurulması için bir yöntem geliştirilmiştir, ve dayanıklı hücreler karakterizedir. Dayanıklı hücreler epidermal büyüme faktörü reseptör Tirozin kinaz inhibitörü-direnç mekanizmaları, küçük hücreli olmayan akciğer kanseri olan hastalar için uygulanabilir araştırmak için kullanılabilir.
Özet
Moleküler hedef inhibitörlerine elde edilen direnç kanser tedavisinde ciddi bir sorundur. Akciğer kanseri çoğu ülkede kanser ile ilgili ölümün önde gelen nedeni kalır. Epidermal büyüme faktörü reseptörü (EGFR) gibi "Onkojenik sürücü mutasyonlarının" keşfi-mutasyonları aktive etmek ve EGFR Tirozin kinaz Inhibitörleri (tkis) (Gefitinib, erlotinib) moleküler hedeflenen ajanlarının sonraki gelişimi afatinib, dacomitinib ve osimertinib) son yıllarda akciğer kanseri tedavisini dramatik bir şekilde değiştirdi. Ancak, bu ilaçlar hala küçük hücreli olmayan akciğer kanseri olan hastalarda etkili değildir (NSCLC) EGFR-aktive mutasyonları taşıyan. Elde edilen direncin ardından, NSCLC 'nin sistemik ilerlemesi EGFR mutasyon pozitif NSCLC hastalarının tedavisinde önemli bir engel teşkil etmektedir. Burada, EGFR eXoN 19 ' da 15 baz çifti silme işlemlerinin EGFR aktive edilen mutasyonlarını barındıran NSCLC PC-9 hücrelerinden üç bağımsız elde edilen afatinib dirençli hücre hatları kurmak için kademeli bir doz yükselmesi yöntemi sunuyoruz. Üç bağımsız afatinib-direnç hücresi çizgilerinin karakterize edilmesi için yöntemler kısaca sunulmuştur. EGFR TKIs 'lere elde edilen direnç mekanizmaları heterojen. Bu nedenle, EGFR-TKIs ' e elde edilen direnç ile birden fazla hücre çizgisi incelenmelidir. On ila on iki ay bu kademeli doz yükselme yaklaşımı kullanarak elde direnç ile hücre hatları elde etmek için gereklidir. Yeni elde edilen direnç mekanizmalarının keşfi daha etkili ve güvenli terapötik stratejilerin gelişmesine katkıda bulunacak.
Giriş
Beş Tirozin kinaz inhibitörü, Gefitinib, erlotinib, afatinib, dacomitinib ve osimertinib dahil olmak üzere epidermal büyüme faktörü reseptörü (EGFR) hedefleme şu anda EGFR mutasyon-pozitif küçük hücreli olmayan akciğer hastaları tedavisinde kullanılabilir kanser (NSCLC). Son on yıl içinde, bu tür hastalar için tedaviler yeni potansiyel EGFR-TKIs keşfi ile dramatik gelişmeye uğramıştır. Akciğer adenokarsinomu olan hastalar arasında, EGFR 'de somatik mutasyonlar Asya 'nın yaklaşık% 50 ve Kafkas hastalarının% 15 ' inde1olarak tanımlanır. EGFR 'deki en yaygın mutasyonlar EGFR eXoN 21 ve 15 baz çifti (BP) silme işlemi olan EGFR eXoN 192' de L858R nokta mutasyonudur. NSCLC olan EGFR mutasyon-pozitif hastalarda, EGFR-TKIs, platin Doublet kemoterapi3' ün önceki standardına kıyasla reaksiyon oranlarını ve klinik sonuçları geliştirir.
Gefitinib ve erlotinib ilk onaylı küçük molekül inhibitörleri ve genellikle ilk nesil EGFR TKIs olarak adlandırılır. Bu EGFR TKIs 'ler ATP ile rekabet ederek Tirozin kinaz aktivitesini engelleyin ve ATP bağlama sitelerine4' e geri döndürülebilir şekilde baðla. Afatinib, EGFR 'nin Tirozin kinaz etki alanına geri dönülemez ve birbirine bağlayan ikinci nesil EGFR TKı 'dir ve Pan-Human EGFR aile inhibitörü5olarak karakterize edilir.
NSCLC hastalarında bu tedavilerin dramik yararına olmasına rağmen, elde edilen direnç kaçınılmazdır. İlk ve ikinci nesil EGFR tkis 'lere karşı en sık görülen direnç mekanizması, T790M% 50-70 ' de mevcut olan EGFR eXoN 20 ' de, tümör numunelerinin6,7,8' inde ortaya çıkmasıdır. Diğer direnç mekanizmaları arasında bypass sinyalleri (MET, ıGF1R, ve HER2), küçük hücreli akciğer kanserine dönüşüm ve epitelyal-mesenkimal geçiş indüksiyonu, klinik öncesi ve klinik olarak9. EGFR TKIs 'lere karşı direnç mekanizmaları heterojen. Preklinik çalışmalarda yeni direnç mekanizmaları tanımlayarak, direncin üstesinden gelmek için yeni terapikler geliştirmek mümkün olabilir. Hastaların klinik avantajını en üst düzeye çıkaracak optimum dizi terapileri direnç mekanizmalarını ve terapötik hedefi dikkate almanız gerekir.
Tüm sonraki deneylerin temeli olduğu için, sağ ebeveyn hücresi çizgisini seçmek zorunludur. Seçim stratejileri klinik alaka ile başlar; bir kemoterapi ve radyasyon naif hücre hattı seçmek için gereklidir. Önceki kemoterapötik ve/veya radyatif tedavi direnç yolları ve ilaç direnci işaretçileri ifade değişikliklerinin değiştirilmesi neden olabilir. Bu çalışmada, EGFR eXoN 19 ' da 15 BP silmeleri taşıyan PC-9 hücreleri, afatinib 'e elde edilen direnç kurulması için kullanılmaktadır. Bu hücre hattı, önceden kemoterapi ve radyasyon alamıyordu Japon NSCLC hasta, türetilmiştir.
Çünkü afatinib günlük bazda sözlü olarak uygulanır, sürekli in vitro tedavi, hücrelerin afatinib varlığında sürekli kültürlü olduğu klinik olarak alakalı olacaktır. Deney çeşitli adımlarda kullanılan ilaçların dozu seçilen ebeveyn hücre çizgisi için optimize edilmelidir. Bir sitotoksisite tahlil uygun bir ilaç aralığı belirlemek için kullanılabilir, hangi ilacın farmakokinetik bilgileri ile karşılaştırılabilir olmalıdır.
Seçim işlemi boyunca, hücrelerin tüm nüfusu tek bir grup olarak korunur; Klonlama veya diğer ayırma yöntemleri kullanılmaz. Hücreler önce sürekli olarak ilacın düşük bir seviyeye maruz kalır. Daha sonra, hücrelerin ilacın varlığında büyümeye adapte sonra, ilacın doz yavaş ilaç son optimum doz arttı10,11. Alternatif olarak, bir nabız ilaç yönetimi veya mutagenez de ilaç tedavisi öncesinde gerçekleştirilen direnç hücreleri seçmek için kullanılabilir 12,13. Ne yazık ki, ilaç direncinin gelişmemesi durumlarında genellikle rapor edilmez. Seçim stratejileri, klinik olarak ilgili direnç yeniden inşa etmek için kanser hastalarının koşullarını taklit etmeye çalışmak amacıyla geliştirilmiştir. Bazen, ilaç direnci mekanizmaları ile ilişkili moleküler değişiklikleri belirlemek için, yüksek bir ilaç konsantrasyonu kullanılır. Bu model daha az klinik olarak alakalı hale gelir.
Burada, EGFR eXoN 19 ' da 15 BP silmenin yanı sıra afatinib dirençli hücre hatlarının ilk karakterizasyonu ile PC-9 hücrelerinden üç bağımsız afatinib dirençli hücre hattı kurmak için bir yöntem açıklanmaktadır.
Protokol
1. üç bağımsız Afatinib-dayanıklı PC-9 hücre hatları kurulması
- 3-(4, 5-dimethylthiazol-2-yl) kullanarak PC-9 hücreleri için ilk afatinib pozlama konsantrasyonu belirlenmesi-2,5-difenyltetrazolium bromür (MTT) tahlil
- Bir hücre kültüründe fetal sığır serumu (% 10), penisilin (100 U/mL) ve streptomisin (100 μg/mL) içeren büyüme ortamında kültür PC-9 hücreleri, 37 °C ' de% 5 CO2 inkükoistte 10 cm 'lik bir tabak ile tedavi edilmiştir.
- Resuspend PC-9 hücreler 4 x 104 hücreler/ml büyüme orta ve sonra tohum at 50 μL/well bir 96-iyi Mikroplaka. Hücrelerin son konsantrasyonu 2,0 x 103 hücreler/50 μL/iyi 'dir. 37 °C ' de% 5 CO2 inkükodiye bir gecede kuluçat.
- Farklı konsantrasyonlarda 50 μL afatinib solüsyonu ekleyin: 0, 0,002, 0,006, 0,02, 0,06, 0,2, 0,6, 2, 6 ve 20 μM büyüme ortamını içeren kuyulara (50 μL). Afatinib 'in son hacmi ve konsantrasyonları sırasıyla 100 μL ve 0, 0,001, 0,003, 0,01, 0,03, 0,1, 0,3, 1, 3 ve 10 μM şeklindedir.
- 37 °C ' de% 5 CO2 inkükode 96 h için 96-kuyu plakasını kuluçsa.
- Her kuyunda 15 μL boya çözeltisi (bkz. malzeme tablosu) ekleyin ve 37 °c ' de 5% Co2 inkübörü içinde 4 h için kuluçk ve sonra 100 μL çözünme/stop-eriyik ekleyin ( malzeme tablosunabakın) her bir kuyunda bir gecede% 5 Co < C10 > 2 37 °c ' de inküvatör.
- 570 nm 'de (OD570) optik yoğunluğu bir Mikroplaka okuyucusu kullanarak ölçün ( malzeme tablosunabakın). Hazırlamak 6-12 çoğaltır ve en az üç kez denemeleri tekrarlayın.
- Grafik olarak bu verileri bir yarı günlük grafik olarak çizmek ve ıC50 değeri hesaplamak için istatistiksel yazılım ( malzeme tablosunabakın), maksimum% 50 yanıt azaltır ilaç konsantrasyonu (bkz: malzeme tablosu ).
- PC-9 hücrelerinin geri dönüşümsüz EGFR-TKı, afatinib, üç bağımsız 10 cm yemeklerle kademeli doz yükselmesi ile sürekli pozlama
- Kültür PC-9 hücreler P100 yemekleri içeren 10 mL büyüme orta. PC-9 hücreleri alt-konfluent aşamaya ulaştığında, 1 mL hücre süspansiyon üç yeni P100 yemekleri içine, 9 mL büyüme orta ile aktarın. 1:10 seyreltilmiş PC-9 hücreleri yaklaşık 4-5 x 105 hücre/ml 'lik bir hücre numarası ile 3-4 gün içinde alt-konfluent haline gelir.
- Ertesi gün, her üç P100 yemekleri içine afatinib ıC50 değeri 1/10 ekleyin.
Not: Afatinib, DMSO 'da 1 μM, 10 μM, 100 μM, 1 mM ve 5 mM 'Lik stok konsantrasyonlarda reconstituted. 1 ila 10 μL afatinib-çözüm, gerekli nihai konsantrasyonlara göre kültürde 10 mL büyüme ortamına eklenir. - Ne zaman afatinib-içeren P100 yemekleri hücreleri alt-konfluent, Mix iyi bir 1 mL pipet ile aspirasyon ve 1 mL hücre süspansiyonu 9 mL yeni bir P100 çanak taze büyüme orta ekleyin. Ardından, yeni kültüre% 10-20 daha yüksek afatinib konsantrasyonu ekleyin.
- 0,1 nM 'nin afatinib konsantrasyonunu arttırın, afatinib konsantrasyonu ile kademeli doz yükselmesi ile orta 1 μM ' ye kadar, 10-12 ay döneminde her adımda% 10-20 arttı.
Not: Afatinib konsantrasyonu ıC50 değerine yaklaştığında, hücre büyümesi oldukça yavaş olur. Hücreler bölünmüş 1:9 ise, bu hücreler afatinib daha yüksek konsantrasyonları tarafından öldürüldüğünde, onlar büyüyebilir değil. Bu nedenle, yüksek afanitib konsantrasyonlarda, hücreler 1:2 oranında bölünebilir. En dayanıklı hücreler afatinib içinde yetiştirilen-3-14 gün boyunca orta, ve dayanıklı hücreler geçmeli gereken kadar orta değişmedi. - 1 μM afatinib içeren büyüme ortamında 2-3 ay boyunca afatinib dirençli hücrelere kültür. 1 μM ' lik bir afatinib konsantrasyonunda, bu modelde afatinib 'e direnç geliştirmek için 10-12 ay gereklidir. Hücrelerin afatinib dirençli olduğunu onaylamak için MTT tahlil gerçekleştirin. Üç bağımsız olarak kurulan afatinib direnç hücre hatları AFR1, AFR2, ve AFR3 seçildi.
2. üç bağımsız Afatinib dirençli hücrelerin karakterizasyonu
- Ebeveyn PC-9 hücrelerinin büyüme eğrisi belirlenmesi ve afatinib dirençli hücrelerin kurulması
- 37 °C ' de% 5 CO2 inkükode büyüme ortamında PC-9, AFR1, AFR2 ve AFR3 hücrelerini kültür.
- 5 x 103 hücreler/ml büyüme orta ile hücreleri resuspend ve Seed 100 μL/iyi bir 96-iyi Mikroplaka içine, böylece hücrelerin son konsantrasyonu olduğunu 500 hücreler/100 μL/well.
Not: MTT tahlil 0, 1, 2, 3, 5 ve 7 gün OD570 değerleri ölçmek için gerçekleştirilir. 6 96-iyi Mikroplaka her gün için gereklidir. - MTT tahlil her 24 saat ve sonra gün 0, 1, 2, 3, 5 ve 7 gerçekleştirin. Ölçme OD570 değerleri ve hazırlamak 6-12 çoğaltır; deneyleri en az üç kez tekrarlayın ve istatistiksel bir yazılım kullanarak sonuçları grafiksel olarak çizin (bkz. malzeme tablosu).
- Gerçek zamanlı PCR tarafından EGFR 'deki genomik DNA değişikliklerini tanımlama
Not: Afatinib, EGFR Tirozin kinaz hedefleri olan küçük bir molekül inhibitörü. EGFR ifade durumu DNA ve protein seviyelerinde belirlenir.- Genomik DNA, üreticinin talimatlarını izleyerek DNA arıtma kiti (bkz. malzeme tablosu) kullanılarak izole edilir. Yalıtılmış genomik DNA 'nın bir Spektrofotometre ile konsantrasyonunu ölçün ( malzeme tablosunabakın) ve tüm genomik DNA örneklerini 25 ng/μL 'ye ayarlayın.
- 25 ng/μL stokların 2 μL 'ine eşdeğer olan genomik DNA 50 ng, SYBR yeşil ana karışımı (bkz. malzeme tablosu) kullanarak ve sonuçları floresans tabanlı bir RT-PCR-algılama sistemi (bkz. malzeme tablosu) kullanarak analiz eder.
Not: PCR Bisiklet koşulları, 20 s için 95 °C ' de ilk denatürasyon adımıyla başladı, ardından 3 s için 95 °C denatürasyon 40 döngüsü, 30 s için 60 °C tavlama. Belirli astar setleri aşağıdaki gibidir: EGFR F: 5 ′-CAAGGCCATGGAATCTGTCA-3 ′, R: 5 ′-CTGGAATGAGGTGGAGGAACA-3 ′. Normalleştirme gen hattı-1 F: 5 ′-AAAGCCGCTCAACTACATGG-3 ′, R: 5 ′-TGCTTTGAATGCGTCCCAGAG-3 ′.
- Protein değişikliklerin Batı leke analizi ile EGFR seviyesinde etkisinin değerlendirilmesi
- PBS ile iki kez 24 h. Wash PC-9, AFR1, AFR2 ve AFR3 hücreleri için deneyler önce sürekli afatinib ile hücreleri Treat ve sonra afatinib olmadan büyüme medyasında onları tohum. Yıkama PC-9, AFR1, AFR2, ve AFR3 hücreleri iki kez 5 mL buz-soğuk PBS ile.
- RIPA tampon hücrelerinde% 1 proteaz inhibitörü kokteyli (bkz. malzeme tablosu) ve fosfataz inhibitörü KOKTEYLI II ve III ( malzeme tablosunabakın) ve bu solüsyonu 4 °c ' de 30 dk. santrifüjle 10 dakika santrifüj eder. 100 x g ve 4 °c ' de ve temizlenmiş lysatları toplayın.
- Bikinkoninik asit tahlil kullanarak protein konsantrasyonlarını belirlemek ( malzeme tablosunabakın), tüm protein örneklerini ayarlamak 0,5 veya 1 μg/μL 4X örnek tampon kullanarak (500 mm TRIS (pH 6,8), 40% gliserol,% 8 SDS, 20% H2O, 0,02% bromophenol mavi) ve 96 °c ' de 5 dakika boyunca kaynatın. bu protein örneklerini Batı leke Analizi gerçekleştirilinceye kadar-80 °c ' de saklayın.
- Eşit miktarlarda protein örnekleri ayırın, tercihen 20-30 μL,% 8 SDS-sayfa ve proteinleri bir Poliviniliden florür (PVDF) membrandan aktarın.
Not: Sodyum Dodesil sülfat-Poliakrilamid jel elektroforez (SDS-sayfa) yaygın olarak moleküler ağırlıklarına göre proteinlerin ayrılması için laboratuvarda kullanılır.- Etanol ile temiz cam plakaları ve cam plaka ve Spacers birleştirin. Hazırlamak 8% poli-akrilamid jeller içeren 1,5 M Tris-HCl, pH 8,8, 40% bis-akrilamid, 10% SDS, 10% APS, ve TEMED. Oda sıcaklığında 30 dakika polimerize.
- Daha sonra, 0,5 M Tris-HCl, pH 6,8,% 40 bis-Acrylamid,% 10 SDS,% 10 APS ve TEMED içeren bir istifleme jeli hazırlayın. İstifleme jeli çözeltisi ekleyin, tarak takın ve 20-30 dk için jel polimerize oda sıcaklığında.
- Jelleri Elektroforez tertibatına yerleştirin ve tankı çalışan tampon ile doldurun (0,25 M Tris, 1,92 M gcine ve% 1 SDS). Yük eşit miktarda protein örnekleri (20-30 μL) ve jel çalıştırmak 180 V. boya ön jel dışarı akar sonra, yaklaşık 60 dakika sonra elektroforezi durdurun.
- TBST ile 1-2 dk için jel yıkayın ve sonra bir PVDF membran üzerinde yarı kuru şişme ile proteinleri aktarmak (bkz: malzeme tablosu) 1,5 h Için 300 mA sabit bir akım.
- Membranları blok% 5 yağ olmayan kuru süt ( malzeme tablosunaBAKıN) tbst çözeltisi ile seyreltilmiş (bkz. malzeme tablosu) Oda sıcaklığında 1 saat, ve daha sonra anti-EGFR ile membranlar prob, Anti-fosho-EGFR (Y1068), Anti-HER2, Anti-HER3, Anti-MET ve anti-aktik antikorlar (1:3000 TBST) (bkz. malzeme tablosu) 4 °c gecede.
- Membranların TBST ile 10 dakika boyunca üç kez yıkayın ve sonra membranları ikincil antikor (TBST içinde seyreltilmeli 1:200), oda sıcaklığında 1-1.5 saat için açığa çıkarın. Membranları 5 kez TBST ile Oda sıcaklığında 10 dakika yıkayın, ECL çözümüne maruz ( malzeme tablosunabakın) ve filmleri kullanarak sinyalleri görselleştirin.
- Sıralama ile EGFR mutasyonların Analizi
- EGFR ekzonlar 19-21 için spesifik astar kullanarak genomik DNA 'yı güçlendirin. PCR Bisiklet koşulları 1 dakika için 94 °C ' de ilk denatürasyon adımıyla başlar, 10 s için 98 °C ' de 30 denaturasyon döngüsü, 30 s için 55 °C ' de tavlama ve 1 dak için 72 °C ' de uzatma.
Not: EGFR eXoN için özel astar 19: F: 5 ′-GCAATATCAGCCTTAGGTGCGGCTC-3 ′ R: 5 ′-CATAGAAAGTGAACATTTAGGATGTG-3 ′, eXoN 20: F: 5 ′-CCATGAGTACGTATTTTGAAACTC-3 ′, R: 5 ′-CATATCCCCATGGCAAACTCTTGC-3 ′, ve eXoN 21: F: 5 ′-ATGAACATGACCCTGAATTCGG-3 ′, R: 5 ′- GCTCACCCAGAATGTCTGGAGA-3 ′. - Güçlendirilmiş PCR ürünlerini bir PCR arıtma kiti kullanarak arındırın (bkz. malzeme tablosu) ve amplicons dizisi.
- EGFR ekzonlar 19-21 için spesifik astar kullanarak genomik DNA 'yı güçlendirin. PCR Bisiklet koşulları 1 dakika için 94 °C ' de ilk denatürasyon adımıyla başlar, 10 s için 98 °C ' de 30 denaturasyon döngüsü, 30 s için 55 °C ' de tavlama ve 1 dak için 72 °C ' de uzatma.
Sonuçlar
PC-9 hücrelerinden üç tane afatinib direnci hücre hattı kurmak için şema, kademeli bir doz yükseltme prosedürü kullanarak Şekil 1' de gösterilir. Şekil 2 , afatinib konsantrasyonu ARTTıKÇA, PC-9 hücrelerinin afatinib pozlama duyarlı olduğunu BELIRTEN Ebeveyn PC-9 hücrelerinin hücre proliferasyonu bir azalma gösterir. Şekil 3 , üç hücre hattının afatinib-direncini gösterir. Üç afatinib dayanıklı hücre hatları, AFR1, AFR2, ve AFR3 hiçbiri, afatinib pozlama altında hücre proliferasyon bastırılması gösterdi. Şekil 4 , PC-9, AFR1, AFR2 ve AFR3 hücreleri için hücre proliferasyonu eğrilerini gösterir. Üç afatinib dirençli hücre hatları Ebeveyn PC-9 hücrelerden daha önemli ölçüde yavaş büyüme sergiledi. Şekil 5 , PC-9 ' d a EGFR gdna 'nın ifade düzeylerini ve afatinib 'e dayanıklı HÜCRELERIN Ebeveyn PC-9 hücrelerinden daha fazla EGFR gdna düzeylerini önemli ölçüde ifade ettiğini gösteren üç afatinib dirençli hücreleri gösterir. Şekil 6 , PC-9 ' d a EGFR protein ifadesini ve afatinib 'e dayanıklı hücreleri gösterir. Karşılaştırılabilir gDNA ifade seviyelerinde, EGFR protein ifadesi Ebeveyn PC-9 hücrelerinde daha dayanıklı hücrelerde daha yüksektir. Şekil 7 EGFR ekzonlar 19 ve 20 PC-9, AFR1, AFR2 ve AFR3 hücrelerinde sıralamanın sonuçlarını gösterir. PC-9 hücreleri, EGFR eXoN 19 ' da 15 BP silme ve eXoN 20 ' de vahşi tip EGFR gösterdi. Ancak, AFR1 ve AFR2 hücreleri vahşi tip EGFR eXoN 19 amplifikasyon sergiledi. AFR3 hücreler, PC-9 hücrelerinde olduğu gibi EGFR eXoN 19 ' da 15 BP silmeleri içeriyordu, ancak EGFR eXoN 20 ' de nokta mutasyonu T790M gözlendi.

Şekil 1 : PC-9 ' a üç afatinib dirençli hücre hattı kurmak için kullanılan sürecin şeması. İlk olarak, PC-9 hücreleri üç P100 yemekleri ayrılmış ve ıC50 değeri 1/10 at afatinib maruz. Ardından, büyüme ortamında afatinib konsantrasyonları kademeli doz yükselmesiyle 1 μM arttı. 10-12 ay sonra, üç bağımsız afatinib dirençli hücre hatları kuruldu ve adlı AFR1, AFR2, ve AFR3. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
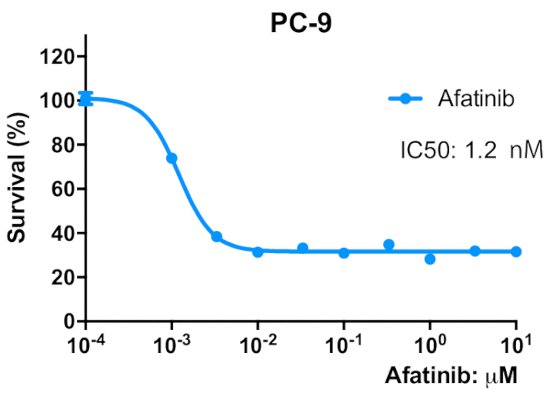
Şekil 2 : Ebeveyn PC-9 hücreleri geri dönüşümlü EGFR TKI, afatinib duyarlıdır. Hücreler, 2 x 103 hücrelerde/kuyu/50 μL büyüme ortamının bir 96-Well Mikroplaka içine tohumlanmış ve bir gecede preinkübe edildi. Hücreleri 96 h için afatinib belirtilen konsantrasyonlarda tedavi edildi. Bir MTT tahlil yapıldı, OD570 değerleri bir Mikroplaka Okuyucu kullanılarak ölçülmüştür ( malzeme tablosunabakın) ve kontrol hücreleri için elde edilen değerin bir yüzdesi olarak ifade edilir. Veriler, 6-12 çoğaltır kuyularından gelen değerlerin ortalama ± SEM olarak sunulur. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
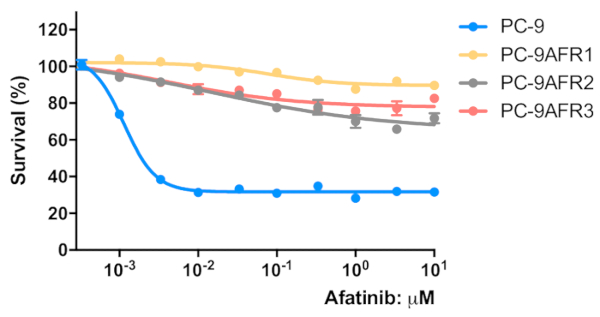
Şekil 3 : Kurulan hücreler geri dönüşümsüz EGFR TKİ, afatinib direnç sergiledi. Hücreler, 2 x 103 hücrelerde/kuyu/50 μL büyüme orta ve bir gecede prekulyaslanmış bir 96-kuyu Mikroplaka içine tohumlu edildi. Hücreleri 96 h için afatinib belirtilen konsantrasyonlarda tedavi edildi. Bir MTT tahlil yapıldı, OD570 değerleri bir Mikroplaka Okuyucu kullanılarak ölçülmüştür ( malzeme tablosunabakın) ve kontrol hücreleri için elde edilen değerin bir yüzdesi olarak ifade edilir. Veriler, 6-12 çoğaltır kuyularından gelen değerlerin ortalama ± SEM olarak sunulur. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
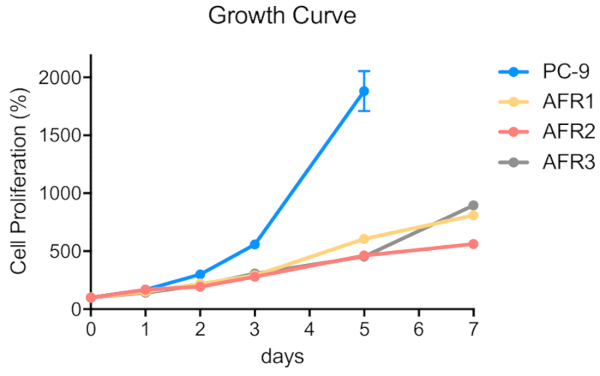
Şekil 4 : Afatinib dirençli hücre hatları Ebeveyn PC-9 hücrelerinden daha yavaş proliferasyonu gösterdi. Hücreler 5 x 102 hücreli/100 μL/well olarak 96-Well Mikroplaka içine tohumlandı. MTT tahlil yapıldı, ve OD570 değerleri gün 0, 1, 2, 3, 5 ve 7 bir Mikroplaka Okuyucu kullanarak ölçülen ( malzeme tablosunabakın) ve kontrol hücreleri için elde edilen değerin bir yüzdesi olarak ifade. Veriler, 6-12 çoğaltır kuyularından gelen değerlerin ortalama ± SEM olarak sunulur. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
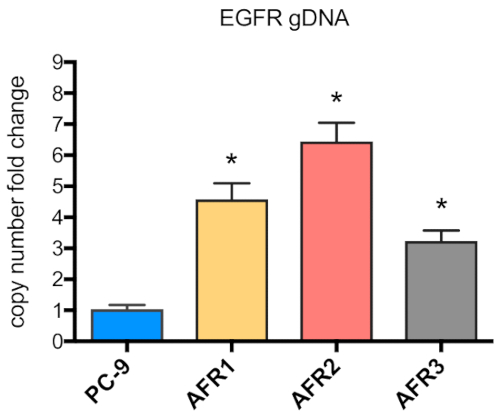
Şekil 5 : EGFR 'Nin gen kopyası sayısı afatinib dirençli hücrelerde yükselmiştir. EGFR gen kopya numarasının yükselmesi, PC-9, AFR1, AFR2 ve AFR3 hücrelerinden izole edilen genomik DNA 'nın nicel PCR ile ölçülmüştür. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.

Şekil 6 : Afatinib dirençli hücrelerde EGFR proteinin bazal seviyesi arttı. Batı leke Analizi phospho-EGFR, EGFR, HER2, HER3, ve met ifade PC-9, AFR1, AFR2 ve AFR3 hücreler. β-actin yükleme kontrolü olarak kullanıldı. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.

Şekil 7 : DNA dizisi EGFR ekzonlar 19 ve 20 okur. PC-9, AFR1, AFR2 ve AFR3 genomik DNA, EGFR eXoN 19 ve 21 için özel astar ile güçlendirildi ve sıralama için saflaştırılmış. Bu figürün daha büyük bir versiyonunu görmek Için lütfen tıklayınız.
Tartışmalar
Burada, üç bağımsız afatinib dirençli hücre hattı kurmak için bir yöntem tarif ve Ebeveyn PC-9 hücrelerine kıyasla bu hücreleri karakterize. Kademeli doz yükselmesi pozlama, Ebeveyn PC-9 hücreleri 10-12 ay bir süre içinde afatinib direnç elde. Klinik olarak, EGFR TKIs direnç mekanizmaları heterojen, ve bu nedenle, afatinib ile ilk tedavi sonra, PC-9 hücreler üç bağımsız P100 yemekleri ayrıldı ve afatinib daha fazla maruz kaldı. Başlangıçta, hücre büyümesi önemli ölçüde yavaşladı, ancak ilaç konsantrasyonu ıC50 değerine yaklaştı olarak, hücre proliferasyonu yavaşladı. Bu inhibitörler elde direnci ile hücreleri elde etmek için kritik bir adımdır. Proliferasyona hücreler bölünmüş ve yeni P100 yemekleri 1:10 veya 1:5 bir oranda transfer edilmelidir. Ne zaman PC-9 hücreler bir P100 çanak Kültürlenmiş, bazı yapışma gözlendi, ama çoğu hücre süspansiyon büyüdü. Afatinib konsantrasyonu arttıkça, hücreler doku kültürünün altına yapışmış yemekler tedavi. Çoğu hücre yapışksa, bir hücre kazıyıcısı ile ayrılabilir. Afatinib 'in son konsantrasyonu, maksimum Serum konsantrasyonu (CMax)14olan yaklaşık 5 kat olan 1 μM idi. Ebeveyn ve direnç klonlar arasında net farklar elde etmek için, son konsantrasyon CMaxdaha yüksek olarak ayarlandı.
Prosedür sırasında ciddi bir endişe bakteriyel kontaminasyon, RPMI-1640 penisilin ve streptomisin içerdiğinden bile. Bunu önlemek için, hücreler bölünmüş olduğunda taze büyüme ortamı içeren iki P100 yemekleri hazırlanabilir. Hücreler alt-konfluent aşamaya ulaştığınızda, bir P100 çanak hücreler daha da bölünmüş olabilir, diğer P100 çanak hücreleri de depolanabilir iken-80 °C ağoprezervasyon ortamında (bkz . malzeme tablosu) bir yedek olarak, böyle bir satır kontamine ise , depolanmış satır kullanılabilir.
Hücre kültürünü kullanan insanlarda afatinib direncinin edinimini tamamen çoğaltmak zor olacaktır. T790M mutasyonun EGFR eXoN 20 ' de ortaya çıkması afatinib 'e karşı baskın nedeni olarak bildirilmiştir. Raporumuzu, bir dayanıklı klon T790M mutasyon11yer aldı. Ayrıca, AFR1 ve AFR2 hücrelerinde olduğu gibi, vahşi tip EGFR artış bizim tarafımızdan ve diğer gruplar tarafından bildirilmiştir15,16. EGFR mutasyonu ve vahşi tip EGFR artışının kaybı, elde edilen direnç olan hastaların EGFR-tkis 17,18' e karşı klinik örneklerinde de bildirilmiştir. Bu nedenle, mevcut modelimizin in vitro çalışmaları, alınan direnç ile klinik numunelerin moleküler profillerini yansıtabilir.
Bu kademeli doz yükselme yöntemi elde edilen dirençli hücreler hatları elde etmek için en güvenilir olarak kabul edilir. Ancak, kültürlü hücrelerde ilk yüksek doz afatinib pozlama büyük olasılıkla daha iyi kanserli hastalarda afatinib tedavinin etkilerini yansıtacak, dayanıklı hücreler kurulması daha zordur rağmen. Bu yöntem için yalnızca PC-9 gibi kayan hücre çizgileri değil, HCC827, 11-18 veya HCC4006 gibi aynı zamanda uyumlu hücre çizgileri de kullanılabilir. Bu kademeli doz tırmanma yöntemi de diğer inhibitörleri, diğer hücre hatları kullanarak, kanser diğer türleri temsil dayanıklı klonlar kurmak için yararlıdır.
Ebeveyn hücrelerinin, n-etil-n-nitrosourea gibi mutajisik ajanlara maruz kalması, afatinib veya osimertinib tedavisine dayanıklı hücrelerin seçimine karşı dayanıklı klonların hızlı elde edilmesini sağlamak için bildirilmiştir 19 ,20. Ancak, bu yapay yöntem belirli temel değişimleri, GC gibi AT geçişleri ve AT TA transversions neden eğilimindedir. Dahası, EGFR TKI NSCLC hastalarında mutajizik bir ajan değildir. Bu nedenle, kademeli doz yükselmesi yöntemi mutajotik ajanlar kullanmaktan daha temsilcisidir.
EGFR TKIs başlangıçta etkili olmasına rağmen, hücreler sonunda böyle tek hedef ilaçlar direnç geliştirmek, zor kanser tedavisi için yapma. Birden fazla molekül hedefleyen inhibitörler bu nedenle geliştirmek için önemlidir. Bu amaçla, çok hedef inhibitörlerine elde edilen direnç ile hücreler elde etmek ve ilaç direnci temel mekanizmaları değerlendirmek gereklidir.
Açıklamalar
Yazarların ifşa etmesi gereken hiçbir şey yok.
Teşekkürler
Biz Ingilizce dil düzenleme ile yardım için onların düşünceli yorum ve Editage için gelişmiş kanser translational Araştırma Enstitüsü üyesi teşekkür ederiz. Bu çalışma JSPS KAKENHI tarafından desteklenmektedir (Grant numarası: 16K09590 to T.Y.).
Malzemeler
| Name | Company | Catalog Number | Comments |
| afatinib | Selleck | S1011 | |
| anti-EGFR monoclonal antibody | cell signaling technology | 4267S | |
| bicinchoninc acid assay | sigma | B9643 | |
| cell-culture treated 10 cm dish | Violamo | 2-8590-03 | |
| CELL BANKER1 | TakaRa | CB011 | cryopreservation media |
| CellTiter 96 | Promega | G4100 | Non-Radioactive Cell Proliferation Assay; Dye solution and Solubilization/Stop solution |
| DMSO | Wako | 043-07216 | |
| ECL solution | Perkin Elmer | NEL105001EA | |
| FBS | gibco | 26140-079 | |
| GeneAmp 5700 | Applied Biosystems | fluorescence-based RT-PCR-detection system | |
| GraphPad Prism v.7 software | GraphPad, Inc. | a statistical software | |
| NanoDrop Lite spectrophotometer | Thermo | spectrophotometer | |
| Nonfat dry milk | cell signaling technology | 9999S | |
| Pen Strep | gibco | 15140-163 | |
| phosphatase inhibitor cocktail 2 | sigma | P5726 | |
| phosphatase inhibitor cocktail 3 | sigma | P0044 | |
| Powerscan HT microplate reader | BioTek | ||
| Power SYBR Green master mix | Applied Biosystems | SYBR Green master mix | |
| protease inhibitor cocktail | sigma | P8340 | |
| QIAamp DNA Mini kit | Qiagen | 51306 | DNA purification kit |
| QIAquick PCR Purification Kit | QIAGEN | PCR purification kit | |
| RPMI-1640 | Wako | 189-02025 | with L-Glutamine and Phenol Red |
| TBST powder | sigma | T9039 | |
| Trans-Blot SD Semi-Dry Electrophoretic Transfer cell | Bio-Rad | semi-dry t4ransfer apparatus | |
| 96 well microplate | Thermo | 130188 |
Referanslar
- Chan, B. A., Hughes, B. G. Targeted therapy for non-small cell lung cancer: current standards and the promise of the future. Translational Lung Cancer Research. 4 (1), 36-54 (2015).
- Mitsudomi, T., Yatabe, Y. Mutations of the epidermal growth factor receptor gene and related genes as determinants of epidermal growth factor receptor tyrosine kinase inhibitors sensitivity in lung cancer. Cancer Science. 98 (12), 1817-1824 (2007).
- Yamaoka, T., Kusumoto, S., Ando, K., Ohba, M., Ohmori, T. Receptor tyrosine kinase-targeted cancer therapy. International Journal of Molecular Science. 19 (11), (2018).
- Marshall, J. Clinical implications of the mechanism of epidermal growth factor receptor inhibitors. Cancer. 107 (6), 1207-1218 (2006).
- Hirsh, V. Managing treatment-related adverse events associated with egfr tyrosine kinase inhibitors in advanced non-small-cell lung cancer. Current Oncology. 18 (3), 126-138 (2011).
- Arcila, M. E., et al. Rebiopsy of lung cancer patients with acquired resistance to EGFR inhibitors and enhanced detection of the T790M mutation using a locked nucleic acid-based assay. Clinical Cancer Research. 17 (5), 1169-1180 (2011).
- Sequist, L. V., et al. Genotypic and histological evolution of lung cancers acquiring resistance to EGFR inhibitors. Science Translational Medicine. 3 (75), 75ra26 (2011).
- Yang, J. C., et al. Osimertinib in pretreated T790M-positive advanced non-small-cell lung cancer: AURA study phase II extension component. Journal of Clinical Oncology. 35 (12), 1288-1296 (2017).
- Chong, C. R., Janne, P. A. The quest to overcome resistance to EGFR-targeted therapies in cancer. Nature Medicine. 19 (11), 1389-1400 (2013).
- Clynes, M., Redmond, A., Moran, E., Gilvarry, U. Multiple drug-resistance in variant of a human non-small cell lung carcinoma cell line, DLKP-A. Cytotechnology. 10 (1), 75-89 (1992).
- Yamaoka, T., et al. Distinct afatinib resistance mechanisms identified in lung adenocarcinoma harboring an EGFR mutation. Molecular Cancer Research. 15 (7), 915-928 (2017).
- Liang, X. J., Shen, D. W., Garfield, S., Gottesman, M. M. Mislocalization of membrane proteins associated with multidrug resistance in cisplatin-resistant cancer cell lines. Cancer Research. 63 (18), 5909-5916 (2003).
- Shen, D. W., Akiyama, S., Schoenlein, P., Pastan, I., Gottesman, M. M. Characterisation of high-level cisplatin-resistant cell lines established from a human hepatoma cell line and human KB adenocarcinoma cells: cross-resistance and protein changes. British Journal of Cancer. 71 (4), 676-683 (1995).
- Murakami, H., et al. Phase I study of continuous afatinib (BIBW 2992) in patients with advanced non-small cell lung cancer after prior chemotherapy/erlotinib/gefitinib (LUX-Lung 4). Cancer Chemotherapy and Pharmacology. 69 (4), 891-899 (2012).
- Nukaga, S., et al. Amplification of EGFR wild-type alleles in non-small cell lung cancer cells confers acquired resistance to mutation-selective EGFR tyrosine kinase inhibitors. Cancer Research. 77 (8), 2078-2089 (2017).
- Nakatani, K., et al. EGFR amplifications mediate resistance to rociletinib and osimertinib in acquired afatinib-resistant NSCLC harboring exon 19 deletion/T790M in EGFR. Molecualr Cancer Therapy. 18 (1), 112-126 (2019).
- Piotrowska, Z., et al. Heterogeneity underlies the emergence of EGFRT790 wild-type clones following treatment of T790M-positive cancers with a third-generation EGFR inhibitor. Cancer Discovery. 5 (7), 713-722 (2015).
- Ortiz-Cuaran, S., et al. Heterogeneous mechanisms of primary and acquired resistance to third-generation EGFR inhibitors. Clinical Cancer Research. 22 (19), 4837-4847 (2016).
- Kobayashi, Y., et al. Characterization of EGFR T790M, L792F, and C797S mutations as mechanisms of acquired resistance to afatinib in lung cancer. Molecular Cancer Therapy. 16 (2), 357-364 (2017).
- Uchibori, K., Inase, N., Nishio, M., Fujita, N., Katayama, R. Identification of mutation accumulation as resistance mechanism emerging in first-line osimertinib treatment. Journal of Thoracic Oncology. 13 (7), 915-925 (2018).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır