Method Article
Bir Gelişimi
Bu Makalede
Özet
Kontakt lens (ZL) ve diğer göz ile ilgili başvurularının değerlendirilmesi için mevcut in vitro modeller ciddi sınırlıdır. sunulan okular platformu fizyolojik gözyaşı akışı, gözyaşı hacmini, hava pozlama ve mekanik aşınma simüle. Bu sistem, çok yönlü ve CL analizler nitro çeşitli uygulanabilir.
Özet
Currently, in vitro evaluations of contact lenses (CLs) for drug delivery are typically performed in large volume vials,1-6 which fail to mimic physiological tear volumes.7 The traditional model also lacks the natural tear flow component and the blinking reflex, both of which are defining factors of the ocular environment. The development of a novel model is described in this study, which consists of a unique 2-piece design, eyeball and eyelid piece, capable of mimicking physiological tear volume. The models are created from 3-D printed molds (Polytetrafluoroethylene or Teflon molds), which can be used to generate eye models from various polymers, such as polydimethylsiloxane (PDMS) and agar. Further modifications to the eye pieces, such as the integration of an explanted human or animal cornea or human corneal construct, will permit for more complex in vitro ocular studies. A commercial microfluidic syringe pump is integrated with the platform to emulate physiological tear secretion. Air exposure and mechanical wear are achieved using two mechanical actuators, of which one moves the eyelid piece laterally, and the other moves the eyeballeyepiece circularly. The model has been used to evaluate CLs for drug delivery and deposition of tear components on CLs.
Giriş
kontakt lens (KL) arena içinde ilgi iki önemli alanlar rahatsızlık ve yeni CL uygulamalarının geliştirilmesini içermektedir. CL rahatsızlık altında yatan mekanizmaların tanıtılması yıllardır alanını atlatmış olan bir konudur. 8 romanın gelişimi, bu tür ilaç iletim cihazları 1,3,9 ve biyosensörler gibi fonksiyonel ZL, 10-12 büyüyen bir ilgi alanıdır, önemli potansiyel pazarları ile. Her iki durumlarda, in vitro model sofistike bir gelişim aşamasında lens malzemeleri veya tasarım özellikleri uygun seçilmesi ile yardımcı olmak için ilgili bilgileri sağlayacaktır. Ne yazık ki, cls ve diğer göz ile ilgili uygulamalar değerlendirilmesi için in vitro modellerinde geçerli nispeten kaba ve deneyimsiz bulunmaktadır. Geleneksel olarak, gözyaşı filmi birikimi veya ilaç dağıtım değerlendiren in vitro CL çalışmalar sabit bir sıvı hacmi içeren statik, büyük hacimli şişeler içinde yapılır hangi greatly fizyolojik miktarlarda aşmaktadır. Ayrıca, bu basit model, doğal gözyaşı akışı bileşen ve göz çevresinin faktörleri tanımlayarak, her ikisi de yanıp sönen refleks, yoksun.
Sofistike, fizyolojik ilgili göz "model" geliştirilmesi multi-disipliner bir yaklaşım gerektiren ve in vivo doğrulama önemli gerektirecektir. Bu nedenlerden dolayı, bizim in vitro göz modeli için temel çerçeve modeli sürekli gelecek yükseltmeleri ve modülasyon yoluyla geliştirilebilir şekilde, son derece çok yönlüdür. Bugüne kadar, bir model gözyaşı hacmini, yırtılma akışı mekanik aşınma ve hava maruz uyarabilmesi. Amaç vivo ve ex vivo gözlemlerinde için akıllı ve ücretsiz bir anlamlı sonuçlar verecektir in vitro bir model, yaratmaktır.
Protokol
Tüm deneyler Üniversitesi'nin Waterloo hayvan araştırma etik komitesi tarafından belirtilen tüm ilgili kılavuzlara uygun ve uyumlu tamamlanmıştır. sığır gözler cömertçe yerel mezbahaya bağışlanan.
1. Göz Modeli
- Tasarım ve Kalıp 13 Üretimi
- İnsan yetişkin gözlerin ortalama fizyolojik boyutlarına göre göz modelleri tasarlar. 13
- göz küresi ve göz modelinin göz kapağı parçaları arasında 250 mikron bir boşluk bırakın. bilgisayar destekli tasarım (CAD) yazılımı kullanılarak ilgili kalıp tasarımı.
- AutoCAD veya Solidworks ile yeni .cad dosyası veya .sldprt dosyası oluşturun. insan göz küresi / göz kapağı 3D modelleri oluşturun. modellerin kalıpları oluşturun ve stl dosyaları olarak kalıpları kaydedin.
- 3D yazıcı yazılımı içine İthalat stl dosyaları (replicator2 örneğin, makeware). Baskı parametrelerini (yer, seyrekliği, ölçek, oryantasyon, pürüzsüzlük, vb belirtin ) 13.
- 3D yazıcılar okumak için G-kod dosyası olarak kaydedin. Bu PLA (polilaktik asit), ABS (akrilonitril butadien stiren), PC (polıkarbonat) veya bunların bir kombinasyonu gibi seçin malzeme, kalıp 13 baskı.
- seçim malzemesi istenilen iplik takın. okumak için 3D yazıcının içine G-kod dosyasını içe aktarın. kalıp yazdırın.
NOT: Göz modeline yumuşak bir yüzey isteniyorsa, alternatif olarak, (CNC) makine kontrollü bir bilgisayar nümerik kullanarak göz kalıpları üretmek. CNC kalıp üretimi için kalıp malzemeleri artık termal plastik sınırlıdır, ancak metal, seramik ve bu Politetrafloroetilen gibi kimyasal direnç polimerler uzatmak. - Bir kesim matkap bağlı olan CNC yazılım arayüzü açın. Ön, üst, yan ve kontrol yazılımı arayüzü, daha önce inşa göz küresi / gözkapağı modeli kalıp perspektif görünümleri göre 3D kalıpları oluşturun. için uygun parametreleri seçinMakinede (bit boyutu, alt tabaka malzemesi, malzeme kalınlığı) ve kalıp kesim geçin.
- PDMS kullanılması Oküler sentezi
- Bir şırınga kullanılarak, PDMS (polidimetilsiloksan) baz 10 mi hacmini ölçmek ve 15-50 ml santrifüj tüpüne doldurun. PDMS toplam ağırlığına göre, elastomer çözeltisi ağ / hac% 10 ekleyin. Bir karıştırma çubuğu kullanarak, iyi çözüm karıştırın.
- göz küresi ve göz kapağı kalıpların içine PDMS çözüm dökün. PDMS RT O / N yerleşmek için izin verin (ya da en azından 12 saat süreyle) polimerizasyonu başlatmak ve kabarcıklar polimerin dışına çözünmesi için izin vermek.
NOT: yükselecek ya da genişletmek olabilir PDMS sol hava kabarcığı olmadığından emin olun. - Daha sonra, 1 saat, ya da 5 dakika için 150 ° C (302 ° F) 75 ° C (167 ° F) fırına kalıplar koydu. daha yumuşak bir jel, PDMS tamamen polimerize için en az 48 saat boyunca oda sıcaklığında bekletin.
- Bir kaç dakika dondurucuda örnekleri koymak; Bu PDMS küçültmek ve basitleştirecekkalıplardan numune alım. ince bir spatula kullanılarak kalıplardan oküler ekstrakte edin.
- göz küresi ve göz kapağı parçaları arasındaki boşluğa bir çözüm teslimi için, 1/16 "eşit bacak bağlantı borusu konnektörü ile 1/16" x 1/8 "politetrafloroetilen tüp bağlamak ve boru delik göz kapağı parça ekleyin .
- Agaroz kullanma Gözküresi Piece sentezi
NOT: gözün parçası örneğin agaroz gibi polimerler kullanılarak sentezlenebilir. Aşağıdaki prosedür, aynı zamanda, PDA (patates dekstroz ağar) ya da SDA'nın (Sabouraud Dextrose Agar) agar türleri, çeşitli göz parçaları üretmek için değiştirilebilir.- % 2 (2 g / 100 mi) jel, ölçü agaroz 2 g üretim ve ultra saf su ve 100 ml karıştırın. Agaroz tamamen eriyene şekilde Çıban (100 ºC) çözüm getirin. Çözelti 5 dakika soğumaya bırakın.
- göz küresi kalıba çözüm dökün ve çözüm 3 soğumasını bekleyinOda sıcaklığında 0 dak. bir spatula ile gözün parçalarını çıkarın. Bir de gözün agar Mağaza -20 daha sonra kullanmak üzere ° C dondurucu. Mikrobiyoloji çalışmaları için, otoklav ve / veya UV-ışıması ile gözün kalıpları sterilize edin.
- PDMS göz küresi üzerinde Sığır Kornea Ortaklığın
Not:. Bu protokol Parekh ark adapte edilmiştir 14- bir laminar akış başlığı altında steril şartlarda sığır kornea diseksiyon ve birleşme gerçekleştirmek. gözleri kazanmak ve aynı gün onları teşrih.
- Kullanmadan önce 10 dakika akış kaputu açın ve% 70 etanol alkol ile dezenfekte. Tüm malzemeler ve aletler 273 ° F / 45 dakika 133 ° C'de otoklav ile steril ve akış kaputu girişinde az 4 inç konumlandırılmış emin olun.
- 2 dakika için seyreltilmiş bir povidon-iyodin solüsyonu içeren bir cam kapta sığır göz bırakın. fosfat tamponlu tuzlu su ihtiva eden bir beher içinde göz yıkama (PBS) p-H 7.4. Forseps hafifçe cam petri, kornea yüzü yukarı göz yerleştirin.
- künt uç diseksiyon makas ile skleral eki noktalarında kesim tarafından aşırı kas ve yağ dokusu çıkarın. hayvan atıkları için belirlenmiş bir steril beher içine aşırı doku atınız.
- Mikro-makas kullanarak, gözün konjonktiva çıkarın. limbusta en az 1 cm'lik bir mesafeyi koruyarak, steril gazlı bez ile göz sarın.
- Altta yatan koroid ve vitreus penetrasyonunu önlemek ve yüzeysel şekilde bir neşter kullanılarak, yaklaşık 2 mm limbus bölgeden sklera insizyon. Dikkatle doğal eğrilik kornea deforme olmadan bir neşter veya diseksiyon makas kullanılarak 360 ° kesi uzatmak.
- ince forseps ile gözün kornea çıkarın. forseps kullanarak, dikkatli herhangi yapışan uveal dokuyu çıkarmak ve PBS ile kornea durulayın.
- Kültür steril bir kap içinde 31ºC kornea MağazaOrta (Medium 199 gibi), doku nem ve hücre besin sağlamak için% 3 fetal sığır serumu ihtiva eden.
- deney öncesinde, PDMS göz küresi üzerinde eksize kornea dinlenme ve özel bir klipsli ile birlikte iki adet kelepçe.
2. Blink platform
- Blink-platform Tasarımı ve Üretimi
NOT: kırpma platform üç fonksiyonel bölümden oluşmaktadır: göz modeli (bölüm 1 'de tarif edilmiştir), bir vites indirgeme sistemi, elektronik sistem.- Tasarım göz modeli (bölüm 1.1) için tarif edilene benzer CAD ve 3D baskı kullanarak yanıp platformu üretim ve. O eyepieces yanal ve dönme hareketleri içine motorların basit dönüşünü çevirir şekilde vites sistemi tasarlayın. 15
- pinyon ve dişli mekanizmasını kullanarak, kapak parçalarına bağlı olan bir dişli, yatay hareketine bir kademeli motorun dönme hareketi çevirir.
- Kullanmakkonjuge bir vites indirgeme sistemi, üç farklı küresi parçaları için üç (veya daha fazla) dönme hareketleri bir adım motoru ile ilgili bir dönme hareketi yükseltmek.
- ikisi arasındaki mesafenin sabit böylece, iki dişli sistemleri, göz kapağı diğeri göz küresi için bir hizaya getirin. bir mikro motor kalkan ve iki motor ile elektronik sistem monte edin.
NOT: yanıp sönen bir hareket içine dişli sistemi tarafından çevrilmiştir dönme motorları sağlamak için iki step motorlar kullanın. - mikrodenetleyici yığılmış bir motorlu kalkan oluşan bir sistem ile iki step motorlar bağlayın. Bağlayın ve açık kaynak kodlu yazılım ürünleri ile çalışmak için elektronik bileşenler yapılandırın.
- Böyle dakikada mermi (RPM), ileri mermi sayısı, geriye mermi sayısı ve dönme tarzı olarak motor parametrelerini kontrol etmek için sistemin programlanmasına.
NOT: Ayrıntılı bilgi için tamamlayıcı "Arduino kod dosyası" bölümüne bakın. - ma sistem yazılımını indirinnufacturers 'web sitesi.
- yazılımı yükleyin ve açın. İstenilen yapılandırmada step motorları kontrol etmek için bir kod yazın. araştırmacı tarafından tanımlanan motorlar istenilen şekilde hareket böylece elektronik sistem güç bir kaynağı ile bağlantı sistemi.
NOT: Ek "Arduino kod dosyası" bölümüne bakın.
- Mikroakiskan ile Meclisi (Yapay Gözyaşı Çözüm)
- Sentezlenen göz küresi ve göz kapağı parçaları alın ve göz modeli için bunlara karşılık gelen klip-ons üzerine onları kayma. gözkapağı parça (bölüm 1.2.5) ile mikroakışkan pompa üzerinde bir şırınga ile katıldı ve konumlandırılmış boru bağlayın. Test platformu çalıştırmak ve tutarlı hareket edin.
- Başbakan boru ve suni gözyaşı solüsyonu (ATS) sürekli bir akış kontrol edin. ATS için reçete daha önce rapor edilmiştir. 16
- El ile, bir seviye uçakta birlikte göz modeli parçaları taşımak şekilde göz küresi ve gözKapak temas halindedir. istenen değerlere mikroakışkan pompa akış hızını ayarlayın. 1-1.5 ul / dk fizyolojik debileri ayarlayın. 17
- deney başlamak için pompayı ve aktüatörler başlayın. ilaç verme deneyleri için, göz küresi parçasına ilaç içeren kontakt lens yerleştirin.
- akış sıvısı 12 plaka içine damla izin verin. İstenen belirlenen zaman aralıklarında, UV-Vis spektroskopisi veya floresan gibi ortak bulgulama yöntemleri kullanarak analit veya ilaç konsantrasyonunu ölçmek. 1,4,18
- kontakt lensler göz yaşartıcı bileşenlerinin birikimi değerlendirmek çalışmaları için, "göz küresi" parçasının üzerine kontakt lens yerleştirin. atılabilir akış sıvısı, toplayın.
- istenilen zaman aralıklarında sonra, göz küresi parçasından kontakt lensi çıkarın ve konfokal mikroskopi olarak daha fazla analiz için lensi hazırlamak.
Sonuçlar
Makine dükkandan ve 3-D baskı elde edilen sentez göz kalıplar, Şekil 1 'de gösterilmiştir. Bu kalıplar, istenen özelliklere sahip oküler üretilmesi için, örneğin agaroz PDMS ve benzeri gibi polimerler, çok çeşitli kullanılabilir. Mikroakışkan şırınga pompası göz modeli platformun işaret düzeneği, Şekil 2 'de gösterilmiştir. Platformu ve kapak parçasının hareketi üzerinden yan boyunca gözün parçasının döndürme ve havaya maruz vasıtasıyla mekanik aşınma taklit eder. Gözyaşı sıvısı istenilen akış hızında mikroakışkan pompadan göz kapağı infüze edilir ve akış boyunca sıvı 12 oyuklu bir plaka içerisinde toplanabilir.
Bir büyükbaş hayvan lens diseksiyon ve PDMS mercek üzerine monte edilmesi için işlem, Şekil 3'te gösterilmiştir. Aşırı doku göz ayrılır ve atılır uzaklaştırılarak elde edilmişkonjonktiva. Kornea çıkarma limbus yakınındaki sklera içine bir kesi ile başlar. 4 analizler nitro çeşitli için kullanılabilir okülerlerin çeşitli göstermektedir. Gösterilen monte gözün adet PDMS, ağar sentezlenir ve bir ex-vivo sığır kornea PDMS gözün parçası üzerine monte edilmiş.
Şekil 5 CL bir antibiyotik, moksifloksasin salınımını değerlendiren bir çalışma, göstermektedir. 18 geleneksel şişe modelinde ölçüldüğünde, ilaç salım bir plato fazının ardından ilk 2 saat içinde ortaya çıkar. Buna karşılık, yeni bir göz modeli kadar 24 saat. 18 CLS kolesterol birikmesini değerlendiren bir çalışma, Şekil 6'da gösterilmiştir ilaç salım yavaş ve sürdürülebilir gösterir. Çalışmada lipid floresan NBD şeklinde etiketlendi kolesterol (7-nitrobenz-2-oksa-1,3-diazol-4-il-kolesterol) ve DEPOSition lazer taramalı konfokal mikroskopi kullanılarak görüntülendi. Sonuçlar yerleştirme çalışmaları şişede gerçekleştirildiğinde gözü modelinde kıyasla önemli farklılıklar olduğunu göstermektedir.

Şekil 1. Vizör kalıpları. (A) makine atölyesi İstihbarat parça kalıp. 3-D baskı (B) Göz kapağı kalıp. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.

Şekil 2. Bir in vitro göz platformu. (A) Dairesel hareket mekanik aşınma taklit eder. (B) Lateral hareket aralıklı hava üretenmaruz kalma. (C) göz kapağı içine Gözyaşı sıvısı infüzyon. (D) kuyu plaka toplanıyor. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.
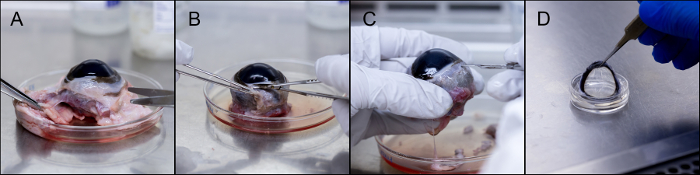
Şekil 3. Diseksiyon ve sığır kornea dahil edilmesi. Aşırı doku (A) Kaldırma. Konjonktiva (B) kaldırılması. Limbus bölgeye (C) İnsizyon. (D) eksize kornea saklanabilir veya bir PDMS göz top parçasına monte edilebilir. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.

Şekil 4. Örnek eyepieces. Bir kontakt lens, bir agar göz parça ve PDMS göz parçasının örnek ex vivo sığır kornea monte göz parçası. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.

In vitro göz platformunu kullanarak Şekil 5. İlaçların teslim. Günlük kullan-at kontakt lenslerden moksifloksasin Release (A) büyük hacimli statik flakon ve (B) göz modeli Vision Araştırma Derneği izni ile (Re-print ve Oftalmoloji). Tüm veriler ortalama ± standart sapma olarak rapor edilmiştir 18. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.

In vitro olarak, oküler platformu kullanılarak Şekil 6. kolesterol birikimi. Etafilcon A nelfilcon A, nesofilcon A, ocufilcon B, A delefilcon, somofilcon A, narafilcon A'nın bir kesitini gösteren Konfokal görüntüler NBD-kolesterol ile 4 saat inkübe edildikten sonra şişe ve göz modeli. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.
Tartışmalar
Orada özel dikkat gerektiren protokolü içinde üç kritik adımlar şunlardır: tasarım ve kalıp üretimi (bölüm 1.1), platformu montajı (bölüm 2.2.1-2.2.3) ve deneysel koşmak izleme (bölüm 2.2.4-2.2.7 ). tasarımı ve kalıplar (Bölüm 1.1) üretimi açısından, gözün parçası, bir insan kornea boyutlarına göre tasarlanmış olmalıdır. Ancak, mükemmel bir ticari kontakt lens (CL) uyuyor oluşturulabilir bir göz küresi parçasının önce kalıbın birden prototipler gerektirebilir. göz küresi ve göz kapağı parçası CL mevcut olduğunda gözyaşı sıvısı tüm göz modeli boyunca düzgün akar sağlamak için temas Buna ek olarak, 250 mikron ihtiyacı muhafaza edilmesi. Bu mesafe, gelecekteki tekrarlamalar değiştirilebilir olabilir, ama az 150 mikron bir CL sığacak kadar boşluk sağlamak için olmamalıdır. Platform montaj (bölüm 2.2.1-2.2.3) göz küresi ve göz kapağı parça conta girer şekilde dikkat gerektirirgöz kırpma hareketi sırasında ct. göz mercekleri mükemmel temas değilseniz, o zaman kapalı bir göz kapağı simülasyonu ve mekanik sürtünme başarısız olur. Operatör küresi ve göz kapağı hem temas ve programlı olarak bu sürtünme meydana sağlamak için birkaç döngüleri için hareket platformu dikkat etmelisiniz. Geçerli bir platform üzerinde bir ay sürekli çalışacak şekilde tasarlanmıştır, ancak bir deney (bölüm 2.2.4-2.2.7) çalıştırırken bir operatör her zaman sistemin istikrarı üzerinde her 24 saat kontrol etmelisiniz. Geçerli bir platform sıcaklık ve nem kontrolü sahip değildir ve bu parametrelerin dalgalanmalar CLS kadar kuru olabilir gibi bu önemlidir. Bu durum ortaya çıkarsa, kontrollü bir nem ve sıcaklık odasının içinde göz modeli yerleştirin. Buna ek olarak, ilaç salınım deneyleri için, toplanan akış boyunca sıvı analiz ya da numune önemli buharlaşmasını önlemek için en az 2 saat muhafaza edilmelidir.
sunulan iki sınırlama bulunmamaktadırGöz modeli. İlk sınırlama çevreye maruz kalma açısından olduğunu. Göz parçaları kontrollü odasının içine değil çünkü şu anda, böyle bir çalışma alanında sıcaklık ve nem gibi değişiklikler deneyler çeşitli yönlerini etkileyecektir. Çevre çok kuru ise Örneğin, sonra ZL hızlı kurur ve göz küresi parçasından ayrı olabilir, ya da akış akışkan buharlaşır olabilir. Bu sorunu çözmek için, gelecek tekrarlamalar kontrollü sıcaklık ve nem odasında göz modeli ev sahipliği yapacak. İkinci sınırlama karmaşıklığı göz küresi parçası ile ilgilidir. Şu anda, göz mercekleri, basit agaroz ya PDMS veya oluşan ikisi de gerçekten kornea yüzey özelliklerini temsil eder. Gelecekteki çalışmalar hangi yakın taklit kornea yüzey yapıları göz modelleri üretmek hedefleyecektir.
In vitro göz araştırmalar genellikle in vivo araştırma önceki test aşamasında olarak görülüyor. Bununla birlikte,aksi yalnız in vivo çalışmalardan elde edilemez kritik anlayışlar sağlayarak, in vitro araştırmalar da in vivo veri tamamlayıcı olabilir akılda tutmak önemlidir. Ne yazık ki, test CL için in vitro modeller mevcut gelişmemiş ve yeterince in vivo ortamda taklit için birkaç anahtar bileşenleri yoksundur. Örneğin, in vitro çalışmalar, CL, fosfat tamponlu tuzlu su 2-5 ml, büyük ölçüde 7.0 ± 2 ul fizyolojik gözyaşı hacimleri aşan 1-6 ihtiva eden viyaller içinde gerçekleştirilir. 7. Ayrıca, oküler ortam iki önemli faktör, doğal gözyaşı akışını ve yanıp sönen refleksi, basit bir statik flakon modelden yoktur. Bir mikroakışkan gözyaşı ikmal bileşeni 2 olmak üzere geleneksel flakon modeli sınırlamaları araştırmacılar tarafından kabul edilmiştir ve girişimleri göz çevreyi taklit in vitro göz modellerinde benzersiz yaratmak için yapılmıştır0-24 ve / veya aralıklı hava temasından. 25,26 Şaşırtıcı bir şekilde, bu deneylerde elde edilen sonuçlar, geleneksel flakon modeli ile elde edilen çok farklı olan ve daha yakından in vivo veriler benzeyebilir. 20-25 Bu durumda, bir gelişmeyen incelemek için in vitro göz modelinde karmaşık CLs göz yüzeyi ile lens malzemeleri etkileşimi yeni bir anlayış sağlamak ve yeni malzemeler ve gelecek yıllarda CL için yeni uygulamaların geliştirilmesi kolaylaştırmaya yardımcı olacaktır.
Tartışmasız, in vitro göz modelinin en çok tartışılan yönlerinden biri gözü bu CL ilaç dağıtım geldiğinde özellikle önemlidir sonsuz lavabo, benzer olup olmadığıdır. Sonsuz, çökelme koşulları altında, çevre çözeltisinin hacmi, ilaç salım ilacın çözünürlüğü etkilenmemektedir şekilde ilaç doygunluk hacmi önemli ölçüde daha yüksektir. Bir ACCE olarak şişenin 27 savunucularıptable göz modeli kornea, konjonktiva ve sonsuz lavabo olarak işlev göz dokuları bir arada çevredeki savunuyorlar. Teorik olarak bu doğru da, ilacın ilk gözyaşı sıvısının içine girmek gerekir. Bu oran sınırlayıcı adım olasılıkla bir lavabo durum değildir ve her ikisi de gözyaşı hacmine bağlı olduğu ve bizim model tarafından simüle olarak akacaktır.
sunulan modelin benzersiz kimlik gözyaşı filmi taklit yeteneği yatıyor. iki parçalı tasarım, "kornea / skleral" göz küresi bölümü ve bir "gözünü" benimseyerek, her iki parça temas ettiğinde göz küresi parça boyunca gözyaşı filminin bir yayılır ince bir tabaka oluşturmak mümkündür. ayrıca göz yüzeyi simüle etmek için, mekanik aşınma ve hava maruz kalma iki mekanik aktüatörler aracılığıyla modele dahil edilmiştir. gözkapağı parça yanal hareket ettikçe, gözün ve aralıklı hava maruziyetin kapanmasını taklit eder. gözün rotasyon durin üretilen mekanik aşınma simüleg yanıp sönen. Sistem fizyolojik akış oranında yırtılma sıvı veya arzu edilen herhangi bir akış oranı ile, göz modeli aşılar mikroakışkan pompa ile birleştirilir. gözyaşı filmi iki parça temas her zaman oluşturulur ve iki adet ayrı zaman gözyaşı kırılma meydana gelir.
Amaç analizleri in vitro çeşitli için CLS değerlendirmek için bir üniversal test platformu yaratmaktır. yönlü olması için, gözün parçaları çeşitli polimetilsiloksan gibi polimerler, (PDMS) ya da agar sentezlenebilir. Basit bir oküler çalışmalar için, sırası ile, hidrofobik ve hidrofilik yüzeylerini temsil Bu polimerler yeterli olacaktır. Daha karmaşık analizler gerekmektedir Ancak, örneğin, oküler ilaç penetrasyon veya toksisite çalışmaları için, göz parçaları daha fazla değiştirilmesi gerekir. Örneğin gösterildiği gibi bir ex vivo kornea dahil olarak modeli Bu ek modifikasyonlar nispeten mümkün bulunmaktadır. Ancak, daha fazla doğrulama çalışmalarıgereklidir ve gelecekteki çalışma in vivo modeller ile karşılaştırarak bu modelin geçerliliğini artırmak hedefleyecektir.
Açıklamalar
Yazarlar ifşa hiçbir şey yok.
Teşekkürler
Yazarlar Gelişmiş Oftalmik Malzemelerin Geliştirilmesi için fon kaynağı NSERC 20/20 Ağ kabul etmek istiyorum.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Arduino Uno R3 (Atmega328 - assembled) | Adafruit | 50 | Board |
| Stepper motor | Adafruit | 324 | Motor and Motor shield |
| Equal Leg Coupler 1.6mm 1/16" | VWR | CA11009-280 | 50 pcs of tube connector |
| Tubing PT/SIL 1/16"x1/8" | VWR | 16211-316 | Case of 50feet |
| PDMS | Dow Corning | Sylgard 184 Solar Cell Encapsulation | |
| Agarose, Type 1-A, low EEO | Sigma-Aldrich | A0169-25G | |
| PHD UltraTM | Harvard Apparatus | 703006 | MicroFluidic Pump |
| Bovine cornea | Cargill, Guelph/ON | ||
| Soldidworks | Dassault Systemes | Software | |
| 3-D printing | University of Waterloo - 3D Print Centre | ||
| Dissection tools | Fine Science Tools | General dissection tools | |
| Medium 199 | Sigma-Aldrich | Culture medium storage for cornea | |
| Fetal bovine serum | Thermo Fisher | Add to culture medium, 3% total volume |
Referanslar
- Phan, C. M., Subbaraman, L. N., Jones, L. In vitro drug release of natamycin from beta-cyclodextrin and 2-hydroxypropyl-beta-cyclodextrin-functionalized contact lens materials. J Biomater Sci Polym Ed. 25, 1907-1919 (2014).
- Peng, C. C., Kim, J., Chauhan, A. Extended delivery of hydrophilic drugs from silicone-hydrogel contact lenses containing vitamin E diffusion barriers. Biomaterials. 31, 4032-4047 (2010).
- Hui, A., Willcox, M., Jones, L. In vitro and in vivo evaluation of novel ciprofloxacin-releasing silicone hydrogel contact lenses. Invest Ophthalmol Vis Sci. 55, 4896-4904 (2014).
- Boone, A., Hui, A., Jones, L. Uptake and release of dexamethasone phosphate from silicone hydrogel and group I, II, and IV hydrogel contact lenses. Eye Contact Lens. 35, 260-267 (2009).
- Lorentz, H., Heynen, M., Trieu, D., Hagedorn, S. J., Jones, L. The impact of tear film components on in vitro lipid uptake. Optom Vis Sci. 89, 856-867 (2012).
- Hall, B., Phan, C. M., Subbaraman, L., Jones, L. W., Forrest, J. Extraction versus in situ techniques for measuring surface-adsorbed lysozyme. Optom Vis Sci. 91, 1062-1070 (2014).
- Mishima, S., Gasset, A., Klyce, S. D., Baum, J. L. Determination of tear volume and tear flow. Invest Ophthalmol Vis Sci. 5, 264-276 (1966).
- Nichols, J. J., et al. The TFOS international workshop on contact lens discomfort: executive summary. Invest Ophthalmol Vis Sci. 54, 7-13 (2013).
- Peng, C. C., Burke, M. T., Carbia, B. E., Plummer, C., Chauhan, A. Extended drug delivery by contact lenses for glaucoma therapy. J Control Release. 162, 152-158 (2012).
- Faschinger, C., Mossbock, G. Continuous 24 h monitoring of changes in intraocular pressure with the wireless contact lens sensor Triggerfish. First results in patients. Der Ophthalmologe : Zeitschrift der Deutschen Ophthalmologischen Gesellschaft. 107, 918-922 (2010).
- Shaw, A. J., Davis, B. A., Collins, M. J., Carney, L. G. A technique to measure eyelid pressure using piezoresistive sensors. IEEE transactions on bio-medical engineering. 56, 2512-2517 (2009).
- Liao, Y. T., Yao, H. F., Lingley, A., Parviz, B., Otis, B. P. A 3-mu W CMOS glucose sensor for wireless contact-lens tear glucose monitoring. Ieee J Solid-St Circ. 47, 335-344 (2012).
- Coster, D. J. . Cornea. , (2002).
- Parekh, M., et al. A simplified technique for in situ excision of cornea and evisceration of retinal tissue from human ocular globe. Journal of visualized experiments : JoVE. , e3765 (2012).
- Way, S. Gear and pinion. US patent. , (1942).
- Lorentz, H., et al. Contact lens physical properties and lipid deposition in a novel characterized artificial tear solution. Molecular vision. 17, 3392-3405 (2011).
- Furukawa, R. E., Polse, K. A. Changes in tear flow accompanying aging. American journal of optometry and physiological optics. 55, 69-74 (1978).
- Bajgrowicz, M., Phan, C. M., Subbaraman, L., Jones, L. Release of ciprofloxacin and moxifloxacin from daily disposable contact lenses from an in vitro eye model. Invest Ophthalmol Vis Sci. , (2015).
- Luensmann, D., Zhang, F., Subbaraman, L., Sheardown, H., Jones, L. Localization of lysozyme sorption to conventional and silicone hydrogel contact lenses using confocal microscopy. Current eye research. 34, 683-697 (2009).
- Tieppo, A., Pate, K. M., Byrne, M. E. In vitro controlled release of an anti-inflammatory from daily disposable therapeutic contact lenses under physiological ocular tear flow. Eur J Pharm Biopharm. 81, 170-177 (2012).
- Ali, M., et al. Zero-order therapeutic release from imprinted hydrogel contact lenses within in vitro physiological ocular tear flow. J Control Release. 124, 154-162 (2007).
- White, C. J., McBride, M. K., Pate, K. M., Tieppo, A., Byrne, M. E. Extended release of high molecular weight hydroxypropyl methylcellulose from molecularly imprinted, extended wear silicone hydrogel contact lenses. Biomaterials. 32, 5698-5705 (2011).
- Kaczmarek, J. C., Tieppo, A., White, C. J., Byrne, M. E. Adjusting biomaterial composition to achieve controlled multiple-day release of dexamethasone from an extended-wear silicone hydrogel contact lens. J Biomater Sci Polym Ed. 25, 88-100 (2014).
- Mohammadi, S., Postnikoff, C., Wright, A. M., Gorbet, M. Design and development of an in vitro tear replenishment system. Ann Biomed Eng. 42, 1923-1931 (2014).
- Lorentz, H., Heynen, M., Khan, W., Trieu, D., Jones, L. The impact of intermittent air exposure on lipid deposition. Optom Vis Sci. 89, 1574-1581 (2012).
- Peng, C. C., Fajardo, N. P., Razunguzwa, T., Radke, C. J. In vitro spoilation of silicone-hydrogel soft contact lenses in a model-blink cell. Optom Vis Sci. 92, 768-780 (2015).
- Liu, P., et al. Dissolution studies of poorly soluble drug nanosuspensions in non-sink conditions. AAPS PharmSciTech. 14, 748-756 (2013).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır