Method Article
Использование носимых устройств для спектроскопии в ближнем инфракрасном диапазоне для выявления центральных и периферических ограничений во время тренировки
* Эти авторы внесли равный вклад
В этой статье
Резюме
Этот протокол включает в себя технологию ближней инфракрасной спектроскопии (NIRS) для оценки локализованных гематологических изменений и изменений оксигенации в префронтальной коре, дыхательных (m.Intercostales) и локомоторных (m.Vastus Lateralis) мышцах во время сердечно-легочных тестов с физической нагрузкой, что позволяет идентифицировать центральные и периферические ограничивающие факторы, влияющие на производительность упражнений.
Аннотация
Золотым стандартом для оценки аэробной способности у физически активных испытуемых и спортсменов является тест на максимальное потребление кислорода (VO2–max), который включает в себя анализ выдыхаемых газов и кардиореспираторных переменных, полученных методом «вдох за вдохом» в эргоспирометре во время инкрементальной тренировки. Однако этот метод не может пролить свет на метаболические изменения на мышечном уровне. Ближняя инфракрасная спектроскопия (NIRS) стала ценной технологией для оценки локальных уровней кислорода (Tissular Saturation Index, TSI) путем количественного определения концентраций оксигенированного (O2-Hb) и дезоксигенированного (H-Hb) гемоглобина в микроциркуляторном русле тканей. Приложения NIRS распространяются на дыхательные и опорно-двигательные мышцы, оценивая метаболические изменения, связанные со стоимостью дыхания (COB) и периферической нагрузкой соответственно. Кроме того, церебральные области, такие как префронтальная кора, были исследованы с помощью технологии NIRS для оценки физиологических изменений, связанных с когнитивными потребностями, связанными с планированием или генерированием двигательных задач, связанных со спортивными результатами. Таким образом, анализируя вызванные физической нагрузкой изменения (D) в O2-Hb, H-Hb и TSI, можно выявить ограничения центральных и периферических упражнений, особенно когда тренировка на выносливость является основным компонентом физической формы (например, бег, езда на велосипеде, триатлон и т. д.). Работа с этими факторами имеет первостепенное значение для тренеров и физиологов ЛФК для оптимизации спортивных результатов, включая стратегии тренировок, ориентированные на основные факторы, ограничивающие физические упражнения. В этом исследовании изложен протокол использования носимых устройств, оснащенных технологией NIRS, для анализа изменений физических нагрузок в TSI, O2-Hb и H-Hb, а также кардиореспираторных переменных, обычно регистрируемых у спортсменов во время тестов VO2–max . Этот подход предлагает комплексный метод для определения основных систем, участвующих в остановке прогресса упражнений и улучшении спортивных результатов.
Введение
Спортсмены на выносливость полагаются на эффективный баланс доставки и поглощения кислорода для поддержания высокоинтенсивных упражнений и улучшения своих спортивных результатов 1,2. Тест на максимальное поглощение кислорода (VO2-max) является жизненно важной физиологической оценкой, которая определяет спортивные результаты путем анализа выдыхаемых газов и кардиореспираторных переменных во время инкрементальной интенсивности упражнений1. Эта оценка, известная как эргоспирометрия или кардиопульмональное тестирование с физической нагрузкой (CPET), отражает реакцию сердечно-сосудистой, дыхательной и мышечной систем на физическую нагрузку3. Кроме того, повышенные затраты энергии, связанные с дыханием, называемые затратами на дыхание (COB), повышают потребность в питательных веществах и кислороде в окружающих тканях. Было задокументировано, что это явление потенциально снижает приток крови к мышцам, участвующим в активных движениях, что приводит к снижению толерантности к физическим нагрузкам и раннему прекращению выполнения упражнений из-за метаболического рефлекса.
Во время теста VO2–max также можно определить вентиляционные пороги (VT), которые соответствуют конкретным интенсивностям упражнений, отмечающим переход от аэробного к анаэробному метаболизму (аэробный порог или вентиляционный порог 1 [VT1] и анаэробный порог или точка компенсации дыхания [RCP] или вентиляционный порог 2 [VT2])5. ЖТ отражают вентиляционные реакции, которые компенсируют метаболические изменения во время инкрементальных упражнений6. Определяя эти пороговые значения, CPET предлагает всестороннюю оценку, интегрируя реакции нескольких биологических систем, критически задействованных во время высокоинтенсивных упражнений.
Однако, несмотря на то, что эргоспирометрия считается золотым стандартом для оценки ХПЭТ, она не учитывает метаболические изменения, происходящие на мышечном уровне. Эти изменения имеют решающее значение для понимания физиологических ограничивающих факторов, связанных с отсутствием прогрессирования во время высокоинтенсивных упражнений у спортсменов на выносливость. В этом контексте технология NIRS стала ценным инструментом в науке о физических упражнениях, помогая в анализе гемодинамических переменных на уровне микрососудистых мышц7.
В последние годы спортивные профессионалы и исследователи использовали широкий спектр коммерческих носимых устройств, оснащенных технологией NIRS, для изучения неинвазивных мышечных изменений во время упражнений, обеспечивая возможность определения VT1 и VT2 с помощьюэтой технологии. Таким образом, интегративный анализ данных NIRS и CPET предлагает всестороннее понимание физиологических реакций на физические упражнения.
Технология NIRS использует модифицированный закон Бера-Ламберта для количественной оценки изменений (D) в концентрациях оксигемоглобина (O2-Hb) и дезоксигемоглобина (H-Hb) во время упражнения7. На местном тканевом уровне снижение уровня O2-Hb отражает увеличение местной метаболической потребности, в то время как увеличение H-Hb отражает увеличение экстракции кислорода. Общий гемоглобин (tHb), сумма O2-Hb и H-Hb, используется в качестве показателя местного тканевого кровотока. И наоборот, разница между O2-Hb и H-Hb (Hb diff) дает индекс тканевой экстракции кислорода9. Индекс циссуратурного насыщения (TSI), рассчитываемый как отношение O2-Hb к tHb, отражает уровень насыщения тканей кислородом и указывает на баланс между местной доставкой и поглощением кислорода10,11. Таким образом, данные NIRS дают критически важное представление о физиологическом состоянии на микрососудистом уровне, обеспечивая детальное понимание оксигенации тканей и гемодинамики, которое дополняет информацию, полученную от CPET.
Это детальное понимание, обеспечиваемое технологией NIRS, распространяется на множество практических применений. Недавние исследования подчеркивают универсальность NIRS и демонстрируют его практическое применение в мониторинге дыхательных12,13 и локомоторных мышц7, а также областей мозга, участвующих в формировании двигательных актов, таких как префронтальная кора (ПФК)14,15. Эта широкая применимость подчеркивает способность NIRS обеспечить всестороннее понимание физиологических реакций на различные типы мышечных сокращений (концентрические или эксцентрические или изометрические сокращения) и физические упражнения.
Анализируя DTSI, вызванный физическими упражнениями, как на мышечном, так и на мозговом уровнях, NIRS предоставляет ценный потенциал для выявления связей между периферическими и центральными ограничивающими факторами, которые влияют на прогрессию упражнений16,17. Например, среди центральных ограничивающих факторов снижение кровотока в результате сужения сосудов головного мозга, вызванного компенсаторной гипервентиляцией из-за повышенного уровня водорода в результате анаэробного метаболизма и повышенного уровня лактата в крови во время высокоинтенсивных упражнений, является значительным фактором снижения TSI в префронтальной коре17,18. Напротив, периферические ограничивающие факторы характеризуются дисбалансом между поступлением кислорода и потребностью в тренируемой мускулатуре19. Снижение местной доставки кислорода и повышенное потребление кислорода может привести к деоксигенации тканей, о чем свидетельствует снижение TSI20. Это различие подчеркивает многогранный характер ограничений производительности во время высокоинтенсивных упражнений, где критически важны как центральные, так и периферические механизмы. Это понимание предполагает, что отсрочка появления этих ограничивающих факторов во время тренировки может способствовать улучшению спортивных результатов.
Чтобы в полной мере использовать потенциал технологии NIRS для выявления этих ограничений, необходимы стандартизированные процедуры, обеспечивающие высококачественный сбор и анализ данных. В этом документе описываются методы проведения испытаний на максимальную выносливость с использованием технологии NIRS для сбора физиологических данных и выяснения взаимосвязи между центральными и периферическими ограничивающими факторами во время высокоинтенсивных упражнений у спортсменов на выносливость. Предложенный протокол обеспечивает стандартизированный подход для обеспечения согласованности и точности в оценке физиологических явлений, лежащих в основе этих ограничивающих факторов.
протокол
Протокол был одобрен Институциональным наблюдательным советом Папского католического университета Чили (проекты No 210525001 и 220608010), а исследование проводилось в соответствии с Хельсинкской декларацией. Все участники предоставили письменное информированное согласие перед участием в описываемом тестировании.
1. Размещение и настройка носимых устройств NIRS
ПРИМЕЧАНИЕ: Можно использовать различные носимые устройства NIRS и программное обеспечение для сбора данных. Исследователи должны тщательно ознакомиться с инструкциями и рекомендациями производителя, чтобы обеспечить надлежащую настройку и использование. В данном исследовании используются устройства, использующие непрерывный волновой регистр сигнала NIRS. Эти коммерческие устройства просты в использовании, но они могут обнаруживать изменения в затухании света только относительно опорной или базовой фазы и не могут обнаруживать абсолютные концентрации, как другие устройства, использующие регистр NIRS во временной области.
- Подготовка носимых устройств NIRS и общие рекомендации по их размещению
- Перед установкой устройств и началом измерений убедитесь, что все носимые устройства полностью заряжены.
ПРИМЕЧАНИЕ: Для устройств, использованных в этом исследовании, производитель сообщает, что аккумулятор с полным зарядом может регистрировать 6–8 часов непрерывно. - Наклейте двустороннюю клейкую ленту на все носимые устройства, чтобы закрепить их на коже участника, следя за тем, чтобы лента не загораживала излучатели света и детекторы.
- Накройте все носимые вещи слоем пищевой пленки, а затем слоем водостойкой клеевой повязки для защиты от пота.
- Перед установкой устройств очистите целевую область спиртовой салфеткой, чтобы удалить остатки, которые могут мешать работе регистра (например, кремы, косметика и т. д.). При необходимости побрейте область вокруг целевого участка, так как волосы могут мешать сигналам NIRS.
ПРИМЕЧАНИЕ: Рекомендуется тщательно мыть руки перед тем, как положить какое-либо устройство на кожу участника, чтобы предотвратить потенциальное загрязнение. Рекомендуется носить перчатки, так как это может еще больше снизить риск заражения. - После того, как все носимые устройства будут правильно размещены на коже участника (см. раздел 1.2), закрепите их слоем эластичной лечебной ленты. Если необходима дополнительная фиксация, используйте эластичную бинтовую повязку темного цвета, гарантируя, что чрезмерное сжатие не изменит измерения (давление капиллярной окклюзии менее 25 мм рт.ст., измеренное обычным сфигмоманометром).
- Накройте все носимые устройства черной тканью, чтобы предотвратить проникновение окружающего света. Если покрыть участок тканью невозможно (около 6 см2 см), используйте черную эластичную терапевтическую ленту для блокировки окружающего света.
- Перед установкой устройств и началом измерений убедитесь, что все носимые устройства полностью заряжены.
- Размещение устройства NIRS
ПРИМЕЧАНИЕ: Убедитесь, что носимые устройства NIRS размещены таким образом, чтобы кнопки включения/выключения и настройки были легко доступны.- Префронтальная кора: Поместите зонд NIRS на левую или правую дорсолатеральную префронтальную кору, примерно на 10 мм выше надбровной дуги участника, аналогично размещению электродов Fp1 в соответствии с модифицированной международной системой ЭЭГ 10-2021.
- m. межреберье: Поместите зонд NIRS над7-м межреберьем по правой передней подмышечной линии 22,23,24. Если по каким-то причинам он расположен не над правым гемитораксом, расположите его над левым гемитораксом, но сигнал от частоты сердечных сокращений может быть более выраженным с левой стороны.
- Чтобы подтвердить глубину проникновения NIRS, используйте ультразвуковое исследование в B-режиме, чтобы проверить расстояние от подкожной клетчатки до внешней границы межреберных впадин. Для измерений в m.Intercostales убедитесь, что расстояние между кожей и мышцами составляет менее 15 мм.
- m.Vastus Lateralis: Поместите зонд NIRS на 5 см латеральнее средней точки воображаемой линии, соединяя верхний край надколенника и большой вертел бедренной кости 24,25,26.
- Чтобы убедиться, что толщина жировой ткани (ATT) не изменяет регистр сигнала NIRS, измерьте толщину кожной складки для подтверждения глубины проникновения NIRS27. Для измерений на m.Vastus Lateralis убедитесь, что ATT меньше 20 мм.
- Настройка программного обеспечения NIRS
- После того, как все носимые устройства NIRS будут правильно размещены (см. раздел 1.2), включите их перед началом измерения.
- Запустите программное обеспечение для сбора данных, предоставленное производителем, создайте новый файл и свяжите носимые устройства NIRS.
- После того как все носимые устройства NIRS будут успешно подключены, установите частоту дискретизации на 10 Гц для сбора данных и аналого-цифрового преобразования для оцениваемых тканей. Для измерений префронтальной коры отрегулируйте дифференциальный фактор длины пути (DPF) в соответствии с зависящим от возраста DPF для каждого участника28. Для измерения мышечной массы установите DPF на 4, как это было в предыдущих протоколах со спортсменами в качестве субъектов исследования29,30.
2. Калибровка и настройка эргоспирометра
- Объемная калибровка
- Откройте программное обеспечение эргоспирометра, предоставленное производителем, чтобы начать процесс калибровки.
- Прикрепите расходомер к турбине диаметром 28 мм с помощью адаптера для шприца. Подсоедините одну гофрированную трубку к адаптеру для шприца, а другую — к калибровочному шприцу объемом 3 л.
- Выполните шесть маневров забора/впрыска, поддерживая постоянный расход. По завершении программное обеспечение автоматически подтвердит, пройден ли калибровочный тест.
- Калибровка газа
ПРИМЕЧАНИЕ: Перед началом калибровки газа убедитесь, что калибровка расхода выполнена.- Калибровка воздуха
- Убедитесь, что линия отбора проб от газоанализатора отсоединена от калибровочного порта и свободно подвешена. Затем инициализируйте процесс калибровки.
- Во время калибровки наблюдается стабильная ровная линия, так как концентрации кислорода (O2) и углекислого газа (CO2) существенно не изменяются (менее 5%). После успешного завершения калибровки воздуха приступайте к калибровке метаболических газов.
- Калибровка метаболических газов
- Откройте газовые клапаны и убедитесь, что в систему подается достаточное давление, проверив манометр (обратитесь к производителю за конкретными инструкциями).
- Подключите линию отбора проб к калибровочному порту и инициализируйте процесс калибровки. Перед началом калибровки выполните предварительный нагрев в течение 3 минут в соответствии с рекомендациями производителя.
- При правильном подходе после 3-минутного периода предварительного нагрева должны наблюдаться две плоские линии: одна колеблется между воздухом помещения (примерно 21,00%O2 и 0,04%CO2), а другая — между калибровочным газом (16,00%O2 и 5,00%CO2).
- Наконец, отсоедините линию отбора проб от калибровочного порта и прикрепите ее к мундштуку, который будет использоваться для предстоящего теста.
- Калибровка воздуха
3. Установка электродов ЭКГ (12 отведений)
- Подготовьте кожу, отшелушивая кремом и/или сбривая волосы в местах установки электродов, если это необходимо. Очистите участки спиртовой салфеткой, чтобы удалить остатки поверхностных тканей.
- Расположите электроды ЭКГ следующим образом31:
- Расположите биполярные отведения (электроды конечностей) следующим образом: Левая рука (LA): левая сторона подключичной ямки; Правая рука (РА): правая сторона подключичной ямки; Левая нога (LL): передняя проекция головки левой бедренной кости; Правая нога (РС): передняя проекция головки правой бедренной кости.
- Расположите прекардиальные электроды следующим образом: V1:4-е межреберье справа от грудины; V2:4-е межреберье слева от грудины (на одной линии с V1); V3: На полпути между V2 и V4; V4:5-е межреберье по среднеключичной линии; V5: передняя подмышечная линия на том же уровне, что и V4; V6: среднеподмышечная линия на том же уровне, что и V4 и V5.
4. Инкрементальный тест с максимальной нагрузкой (сердечно-легочный нагрузочный тест, CPET)
- Попросите участника сесть на велосипед, убедившись, что сиденье и руль отрегулированы по высоте для оптимального комфорта и положения.
ПРИМЕЧАНИЕ: Рекомендуется устанавливать высоту сиденья таким образом, чтобы колено было слегка согнуто при полном разгибании32. Руль должен быть расположен так, чтобы можно было слегка сгибать локти. - Приложите пульсоксиметр к мочке уха участника, обеспечив чистоту участка, протерев его спиртовой салфеткой.
- Объясните протокол и проинструктируйте участника дышать через маску до, во время и после теста.
ПРИМЕЧАНИЕ: Участник должен избегать разговоров или свиста во время ношения маски, так как это может повлиять на показания эргоспирометра33. - После того, как участник будет расположен и подготовлен, попросите его вытянуть правую ногу и подождите 2 минуты до начала инструктажа (начальная стадия отдыха). Пусть участник крутит педали с частотой вращения педалей в диапазоне 80–100 об/мин в течение 6 минут при давлении 0,6 Вт·кг-1 и 0,8 Вт·кг-1 для женщин/мужчин соответственно (фаза разминки). Затем увеличивайте нагрузку со скоростью 20 Вт·мин-¹ для женщин и 25 Вт·мин-¹ для мужчин, пока участник не достигнет истощения (фаза упражнений).
- После завершения фазы упражнения попросите участника оставаться неподвижным и продолжать дышать в маску в течение 3 минут (фаза заминки или восстановления).
- После того, как протокол упражнений будет завершен, осторожно снимите пульсоксиметр с мочки уха, маску, все три носимых устройства NIRS и электроды ЭКГ.
ПРИМЕЧАНИЕ: Для поддержания лабораторных условий окружающей среды (например, температура воздуха ~20 ± 2 °C, относительная влажность ~40% ± 5%) это является решающим критерием. У некоторых участников может наблюдаться высокая скорость потоотделения, что препятствует фиксации устройств на коже и влияет на запись данных NIRS. Использование аппаратов искусственной вентиляции легких может помочь снизить терморегуляцию при потоотделении.
Результаты
Во время завершения ХПЭТ у всех пациентов отмечались симптомы одышки, усталости ног и скорости воспринимаемой нагрузки (СИЗ). Дополнительное использование устройств NIRS не добавляло никакого дискомфорта к оценке чувствительности испытуемых. Кроме того, мы не прекращали оценку CPET в связи с каким-либо событием риска, связанным с чрезмерным физиологическим стрессом.
Мы изучили двух соревнующихся велосипедистов-мужчин, набранных из национального велосипедного клуба. Критериями включения в это исследование были физически активные участники (≥150 минут умеренной или ≥75 минут энергичной физической активности в неделю) с нормальным индексом массы тела (20–25 кг·м-2). Критериями исключения для этого исследования были наличие в анамнезе респираторных, сердечно-сосудистых, метаболических, скелетно-мышечных или опухолевых заболеваний, а также инфекционного или воспалительного процесса не менее чем за 2 недели до оценки исследования.
Проведение CPET, сопровождаемое неинвазивной регистрацией изменений гемодинамики и оксигенации тканей, вызванных метаболическими изменениями, вызванными увеличением интенсивности упражнений, с использованием устройств, оснащенных технологией NIRS, позволяет идентифицировать центральные ограничивающие факторы, связанные с изменениями в областях мозга, по сравнению с периферическими ограничивающими факторами, связанными с респираторными или скелетно-мышечными реакциями на повышенную интенсивность упражнений. Протокол тестирования включает в себя ряд этапов, включая подготовку участника, выполнение теста с физической нагрузкой и сбор соответствующих физиологических данных.
Об успешном выполнении протокола CPET–NIRS свидетельствуют четкие и согласованные данные по нескольким параметрам. Во время начальной стадии отдыха записываются такие измерения, как частота сердечных сокращений (ЧСС), пульсовое насыщение кислородом (SpO2) и показания NIRS для установления исходного уровня. Фаза разминки, характеризующаяся педалированием с низкой нагрузкой, подготавливает участника к фазе инкрементных упражнений, где нагрузка постепенно увеличивается (см. рис. 1).

Рисунок 1: Экспериментальный дизайн схемы протокола учений. Схематическое изображение этапов протокола упражнений, использованного в исследовании, с выделением ключевых событий, таких как отдых (R), разминка (W), упражнение (E), завершение (F) и остановка (S), которые соответствуют потоку протокола тестирования сердечно-легочной нагрузки. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
Представлены репрезентативные результаты данных CPET (Рисунок 2) и NIRS (Рисунок 3 и Рисунок 4) от двух спортсменов-мужчин, оцененных в контролируемых лабораторных условиях окружающей среды (температура воздуха ~20 ± 2 °C; относительная влажность ~40% ± 5 %). VO2-max: 46 мл·кг-1·мин-1, VE: 177 л·мин-1, HR-max (% прогноз, 220 лет): 100%, PetCO2: 27 мм рт.ст.); и (ii) Участник 2 (Рисунок 2B и Рисунок 4) (возраст: 26 лет, вес: 67 кг, рост: 178 см, максимальная рабочая нагрузка: 300 Вт, VO2-max: 51 мл·кг-1·мин-1, VE: 131 л·мин-1, HR-max (% прогнозируемых, 220-лет): 93%, PetCO2: 33 мм рт.ст.).
У обоих участников VO2 (потребление кислорода), VCO2 (производство углекислого газа), RQ (дыхательный коэффициент, VCO2· VO 2-1), HR, VE (вентиляция легких) и RR (частота дыхания) демонстрируют непрерывный рост по мере увеличения интенсивности упражнений до тех пор, пока не будет достигнуто максимальное значение VO2 (см. рис. 2).
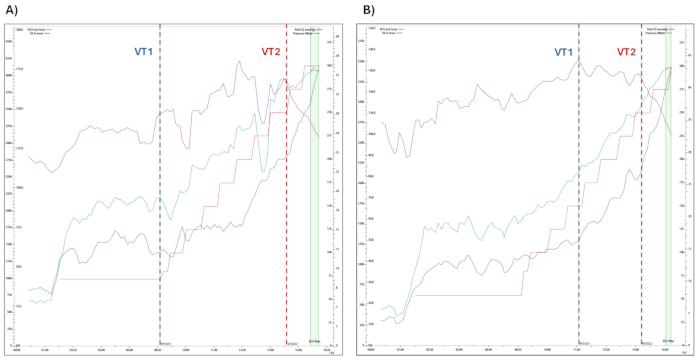
Рисунок 2: Изменения физиологических параметров, оцененные во время КТЭТ. Показана прогрессия физиологических переменных, измеренных во время сердечно-легочных тестов с физической нагрузкой, включая потребление кислорода (VO2), минутную вентиляцию (VE), давление CO2 в конце выдоха (PetCO2) и выходную мощность (Вт). Переходы между порогами вентиляции 1 и 2 (VT1 и VT2) обозначены в рамках этапов упражнений. (А) Участник 1 и (Б) Участник 2. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
Данные NIRS позволили получить представление о локальном метаболическом спросе во время CPET. Изменения, вызванные физической нагрузкой, наблюдаемые в целевой ткани (мышечной или мозговой), варьируются в зависимости от конкретной ткани и интенсивности анализируемой нагрузки. Таким образом, полезной физиологической основой для интерпретации данных NIRS, вызванных физическими упражнениями, является трехфазная модель интенсивности упражнений, предложенная Скиннером и Маклелланом34. В этой модели авторы выделяют три зоны, определяемые VT: Фаза I или аэробная, (ii) Фаза II или аэробно-анаэробный переход, и (ii) Фаза III или «метаболическая нестабильность».
При интенсивности упражнений ниже VT2 (фазы I и II) снижение O 2-Hb и увеличение H-Hb будет происходить на мышечном уровне – если не будет существенного изменения T-Hb как параметра местного кровотока. Наш протокол CPET-NIRS состоит из циклических упражнений с повторяющимися мышечными сокращениями/расслаблениями, поэтому ожидается минимальное изменение T-Hb. Тем не менее, изменения, вызванные физическими упражнениями, варьируются в зависимости от оцениваемой целевой мышечной ткани. В двигательных мышцах, таких как m.Vastus Lateralis, прогрессирующее увеличение интенсивности упражнений вызывает изменения данных NIRS в зависимости от нагрузки (см. рисунок 3A). Напротив, в вспомогательных дыхательных мышцах, таких как m.Intercostales, изменения происходят одновременно с изменениями вентиляции, а не с нагрузкой (см. рисунок 3B). При ПФК наблюдается увеличение O2-Hb, H-Hb и T-Hb, потому что кровоток превышает местную потребность, вызванную физическими упражнениями; кроме того, может наблюдаться небольшое снижение TSI (см. Рисунок 3C). Во всех оцениваемых тканях параметр TSI снижается по мере увеличения интенсивности упражнений, что делает изменения m.Vastus Lateralis более известными, чем m.Intercostales и PFC (см. Рисунок 3D).

Рисунок 3: Пример центрального ограничения (Участник 1). Данные NIRS во время протокола CPET (события: W = разминка, E = упражнение, VT1 = порог вентиляции 1 или порог аэробной вентиляции, VT2 = порог вентиляции 2 или порог анаэробной вентиляции, F = завершенное упражнение или VO2-max). (A) m.Vastus Lateralis, (B) m.Intercostales и (C) префронтальная кора (PFC). Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
По мере увеличения метаболической потребности, вызванной физическими упражнениями, особенно при интенсивности выше VT2 (фаза III или «метаболическая нестабильность»), интересные физиологические реакции, которые необходимо изучить, происходят как на мышечном (двигательные и дыхательные мышцы), так и на уровне ПФК. Они заключаются в заметном снижении O2-Hb и tHb наряду со значительным увеличением H-Hb, что способствует выраженному снижению TSI.
У пациентов с высокой потребностью в вентиляции во время высокоинтенсивных упражнений экспоненциальный рост ЖЭ и ОР вызывает повышенную гипервентиляцию из-за увеличенияСО2 «метаболического происхождения». Эта гипервентиляция может вызывать выраженную вазоконстрикцию мозга, тем самым ограничивая работоспособность центральным ограничением, как это наблюдается у данного репрезентативного субъекта. Теоретически изменения, наблюдаемые в данных NIRS, являются результатом вазоконстрикции головного мозга, вызванной гипокапнией, что вытекает из резкого снижения давления в конце выдоха CO2 (PetCO2), зарегистрированного в CPET (см. рис. 2). Было показано, что эти физиологические изменения имеют высокую корреляцию с увеличением одышки, вызванной физическими упражнениями, зарегистрированной с использованием модифицированной шкалы Борга35,36.
С другой стороны, у пациентов с высокой локомоторной потребностью, но не высокой дыхательной потребностью, не наблюдается вазоконстрикции головного мозга при гипокапнии. Следовательно, данные NIRS могут продолжать отражать изменения, подобные тем, которые наблюдаются при умеренной интенсивности упражнений. У этих испытуемых производительность упражнений ограничена скорее периферическими, чем центральными ограничивающими факторами (см. рисунок 4). Было показано, что эти физиологические изменения имеют высокую связь с повышенной утомляемостью ног, вызванной физическими упражнениями.
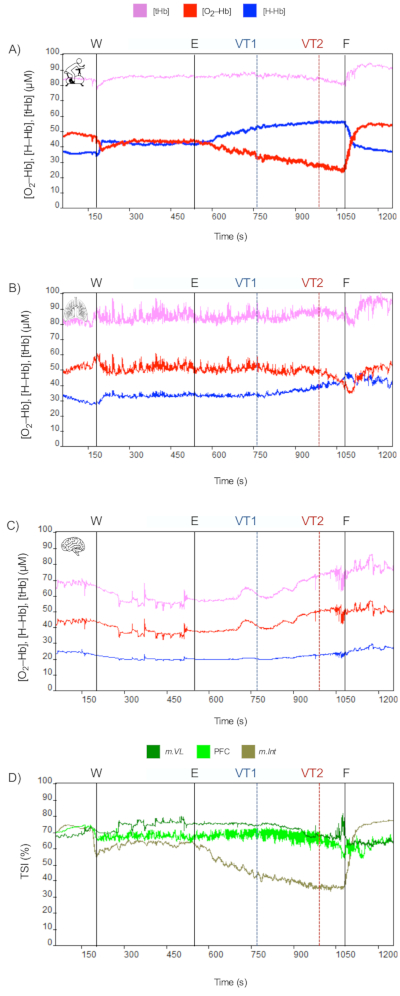
Рисунок 4:Пример ограничения периферии (Участник 2). Данные NIRS во время протокола CPET (события: W = разминка, E = упражнение, VT1 = порог вентиляции 1 или порог аэробной вентиляции, VT2 = порог вентиляции 2 или порог анаэробной вентиляции, F = завершенное упражнение или VO2–max). (A) m.Vastus Lateralis, (B) m.Intercostales и (C) префронтальная кора (PFC). Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
Обсуждение
Существует значительный потенциал использования носимых устройств NIRS в качестве дополнительного инструмента к CPET для оценки спортивных результатов и выявления центральных и периферических факторов, ограничивающих физические нагрузки, у спортсменов, занимающихся аэробными упражнениями или выносливостью, учитывая, что технология NIRS доказала свою валидность и надежность в оценке микрососудистой гемодинамики как в мозговых, так и в мышечных областях37,38. Тем не менее, чтобы получить максимальную отдачу от этой технологии, необходимо учесть несколько соображений для обеспечения точных измерений.
Общие рекомендации по размещению носимого устройства NIRS включают адаптацию позиционирования к целевой ткани и обеспечение надежного прикрепления к коже участника, поскольку движение во время тренировки может повлиять на сигналы (артефакты) NIRS7. Для этого устройство должно полностью соприкасаться с кожей и прикрепляться с помощью двустороннего скотча, обеспечивая беспрепятственное воздействие излучателей света и детекторов. Для дополнительной устойчивости на устройство можно наложить эластичную лечебную ленту. При размещении устройства на конечности, которая будет активно задействована во время упражнений, например, m.Vastus Lateralis, можно использовать эластичную бинтовую повязку для дополнительной устойчивости во время езды на велосипеде. Тем не менее, крайне важно избегать чрезмерной компрессии вокруг оптодов NIRS, так как это может изменить местный кровоток и потенциально повлиять на точность измерений NIRS (давление не должно быть выше давления капиллярной перфузии, ~25 мм рт.ст.)7. Рекомендуется, чтобы любая лента или бандаж, используемые на устройстве NIRS, были черного цвета для предотвращения помех от окружающего света39,40. Кроме того, приглушенное освещение в тестовой среде может свести к минимуму потенциальные нарушения точности сигнала NIRS.
Несмотря на то, что правильное размещение и фиксация устройств имеют важное значение, не менее важно учитывать индивидуальные анатомические характеристики, которые могут повлиять на измерения NIRS. Одним из основных ограничений является то, что на точность измерений NIRS могут влиять такие факторы, как толщина жировой ткани (ATT)41,42. Максимальная глубина проникновения для NIRS составляет примерно половину расстояния между источником света и детектором43. По мере увеличения АТТ доля сигнала NIRS, исходящего от нижележащей скелетной мускулатуры, уменьшается11. Это снижение вклада сигнала приводит к снижению уровней O2-Hb и H-Hb, среди других хромофоров42. Поэтому рекомендуется измерять АТТ, чтобы обеспечить надлежащее проникновение света в мышцы. Для этой цели можно использовать штангенциркуль или ультразвук, так как оба метода точно оценивают состав тела у спортсменов; Тем не менее, последний обеспечивает превосходную точность и может быть предпочтительным44.
Помимо ATT, на точность измерений NIRS также влияет дифференциальный коэффициент длины трассы (DPF), который используется для расчета концентраций O2–Hb и H–Hb с помощью модифицированного закона Бера-Ламберта45. В большинстве коммерческих устройств NIRS используются непрерывные волновые системы, которые излучают свет с постоянной интенсивностью и предполагают постоянный DPF11. Тем не менее, DPF не является фиксированной величиной, так как она варьируется из-за индивидуальных анатомических различий, включая череп и ATT41,46. Кроме того, вариабельность DPF у разных людей и различия в анатомических характеристиках между полами, такие как различия в костях, мышечной массе и распределении жировой ткани, также могут влиять наточность измерений. Из-за предположения о постоянном DPF эти устройства могут измерять только относительные изменения O2-Hb и H-Hb от исходного уровня, а не предоставлять абсолютные значения11. Таким образом, хотя технология NIRS ценна для мониторинга тенденций оксигенации тканей, следует проявлять осторожность при интерпретации этих измерений. Дальнейшие исследования должны быть сосредоточены на разработке методов точной оценки DPF в церебральных и мышечных тканях. В то же время рекомендуется документировать значения DPF, используемые в исследованиях, чтобы улучшить воспроизводимость результатов.
Еще одной анатомической характеристикой, которая может повлиять на измерения NIRS, является концентрация меланина в коже. Меланин, наряду с гемоглобином, является основным хромофором в коже47. Люди с более темной пигментацией кожи имеют более крупные и концентрированные меланосомы, что может привести к большему затуханию сигнала из-за повышенного поглощения света7. Мощность регистрируемого сигнала зависит от света, поглощаемого хромофорами, свойств рассеяния света в тканях, а также расстояния между источником света и детектором47. Следовательно, более высокие концентрации меланина могут влиять на качество сигнала NIRS, что приводит к ослаблению показателей насыщения тканей кислородом, в основном на мышечном уровне48,49. Чтобы учесть эти различия и повысить интерпретируемость данных NIRS в различных популяциях, рекомендуется сообщать о пигментации кожи с использованием шкалы классификации типов кожи по Фитцпатрику7.
Что касается применимости этого протокола при назначении упражнений, технология NIRS в первую очередь используется для оценки мышечного метаболизма во время упражнений на выносливость, особенно в протоколах, где окисление субстрата служит основным источником энергии для ресинтеза АТФ. Имеются ограниченные данные о его применении в тренировках с отягощениями, но обзор литературы предполагает, что острое воздействие силовых тренировок на TSI зависит от состава мышечных волокон. В частности, мышцы с более высокой долей волокон I типа, такие как m.Vastus Lateralis, демонстрируют больший ΔTSI по сравнению с другими группами мышц, тренируемыми с той же интенсивностью. Тем не менее, значительная гетерогенность методологий исследования продолжает ограничивать обобщение сообщаемых результатов. Предварительные результаты этого исследования, наряду с будущими публикациями стандартизированных протоколов, будут способствовать более широкому применению этой технологии для назначения интенсивности упражнений в различныхконтекстах.
В заключение, носимые устройства NIRS представляют собой значительный прогресс в неинвазивном мониторинге гемодинамических реакций на микрососудистом уровне во время физических упражнений, дополняя сердечно-легочные переменные, оцениваемые с помощью CPET. В отличие от инвазивных методов, NIRS предоставляет данные в режиме реального времени о балансе между доставкой и потреблением кислорода, не нарушая естественного движения спортсмена. Эта технология эффективно определяет центральные и периферические факторы, ограничивающие физическую нагрузку, обнаруживая изменения O 2-Hb, H-Hb и TSI в различных тканях и интенсивности упражнений. Подробное понимание изменений метаболической потребности и физиологических реакций подчеркивает потенциал NIRS для оптимизации тренировочных программ и повышения спортивных результатов. Кроме того, способность NIRS оценивать церебральную и мышечную микрососудистую гемодинамику открывает новые возможности для изучения физиологических реакций на различные модальности и интенсивность упражнений. В целом, технология NIRS имеет значительные перспективы для улучшения нашего понимания физиологии человека и внесения вклада в исследования в области науки о физических упражнениях, предоставляя ценный инструмент для улучшения спортивных результатов и совершенствования тренировочных стратегий.
Раскрытие информации
Авторы заявляют об отсутствии конфликта интересов.
Благодарности
Мы благодарим всех участников данного исследования и сотрудников технической лаборатории за поддержку в проведении измерений, проводимых в лаборатории физиологии упражнений. Авторы FC-B и ME-R были частично поддержаны III, IV и V конкурсами исследований и инноваций Школы медицинских наук (Медицинский факультет Папского католического университета Чили). Автор RC-C был профинансирован проектом, поддержанным Конкурсом регулярных исследовательских проектов, 2023 год, код LPR23-17, Universidad Tecnológica Metropolitana.
Материалы
| Name | Company | Catalog Number | Comments |
| Column Scale | SECA | 711 | There are numerous alternatives to this item |
| Portable Stadiometer | SECA | 217 | There are numerous alternatives to this item |
| 12-lead ECG | COSMED | Quark T12x | A 12-lead ECG provides a better understanding of HR during exercise and facilitates the detection of arrhythmias. |
| Pulse Oxymeter | COSMED | Integrated pulse oxymeter | |
| Ergoespirometer | COSMED | Quark-CPET | Calibration gases and calibration syringe are included |
| Cycle-ergometer | Ergoline GmH | ViaSprint 150P | There are numerous alternatives to this item. Must ensure compatibility with provided software |
| NIRS weareable | Artinis Medical Systems | Portalite | Articulated NIRS weareable fits the surface where it's placed upon. |
| NIRS weareable | Artinis Medical Systems | Portamon | Portamon device provides better results on high adipose-tissue surfaces. |
| Metabolic Data Management Software (OMNIA) | COSMED | Software will vary upon system choice | |
| NIRS Data Management Software (Oxysoft) | Artinis Medical Systems | Software will vary upon device choice | |
| Wireless Probe Type Ultrasound Scanner | SONUS | Duo LC | There are numerous alternatives to this item |
Ссылки
- Bassett, D. R. Limiting factors for maximum oxygen uptake and determinants of endurance performance. Med Sci Sports Exerc. 70 (1), 12-25 (2000).
- Seiler, S. What is best practice for training intensity and duration distribution in endurance athletes. Int J Sports Physiol Perform. 5 (3), 276-291 (2010).
- Palange, P., et al. Recommendations on the use of exercise testing in clinical practice. Eur Respir J. 29 (1), 185-209 (2006).
- Contreras-Briceño, F., et al. Intercostal muscles oxygenation and breathing pattern during exercise in competitive marathon runners. Int J Environ Res Public Health. 18 (16), 8287 (2021).
- Mier, C. M., Alexander, R. P., Mageean, A. L. Achievement of VO2max criteria during a continuous graded exercise test and a verification stage performed by college athletes. J Strength Cond Res. 26 (10), 2648-2654 (2012).
- Racinais, S., Buchheit, M., Girard, O. Breakpoints in ventilation, cerebral and muscle oxygenation, and muscle activity during an incremental cycling exercise. Front Physiol. 5, 142 (2014).
- Perrey, S., Quaresima, V., Ferrari, M. Muscle oximetry in sports science: An updated systematic review. Sports Med. 54 (4), 975-996 (2024).
- Contreras-Briceño, F., et al. Determination of the respiratory compensation point by detecting changes in intercostal muscles oxygenation by using near-infrared spectroscopy. Life (Basel). 12 (3), 444 (2022).
- Kozlova, S. G. The use of near-infrared spectroscopy in the sport-scientific context. J Neurol Neurol Diord. 4 (2), 203 (2018).
- Perrey, S. Non-invasive NIR spectroscopy of human brain function during exercise. Methods. 45 (4), 289-299 (2008).
- Barstow, T. J. Understanding near infrared spectroscopy and its application to skeletal muscle research. J Appl Physiol. 126 (5), 1360-1376 (2019).
- Kowalski, T., et al. Respiratory muscle training induces additional stress and training load in well-trained triathletes—randomized controlled trial. Front Physiol. 14, 1264265 (2023).
- Espinosa-Ramírez, M., et al. Sex-differences in the oxygenation levels of intercostal and vastus lateralis muscles during incremental exercise. Front Physiol. 12, 738063 (2021).
- Perrey, S. Evaluating brain functioning with NIRS in sports: Cerebral oxygenation and cortical activation are two sides of the same coin. Front Neuroergonomics. 3, 1022924 (2022).
- Thomas, R., Perrey, S. Prefrontal cortex oxygenation and neuromuscular responses to exhaustive exercise. Eur J Appl Physiol. 102 (2), 153-163 (2007).
- Kirby, B. S., Clark, D. A., Bradley, E. M., Wilkins, B. W. The balance of muscle oxygen supply and demand reveals critical metabolic rate and predicts time to exhaustion. J Appl Physiol. 130 (6), 1915-1927 (2021).
- Perrey, S. Training monitoring in sports: It is time to embrace cognitive demand. Sports (Basel). 10 (4), 56 (2022).
- Angius, L., et al. Transcranial direct current stimulation over the left dorsolateral prefrontal cortex improves inhibitory control and endurance performance in healthy individuals. Neuroscience. 419, 34-45 (2019).
- Dempsey, J. A., McKenzie, D. C., Haverkamp, H. C., Eldridge, M. W. Update in the understanding of respiratory limitations to exercise performance in fit, active adults. Chest. 134 (3), 613-622 (2008).
- Peltonen, J. E., et al. Cerebral and muscle deoxygenation, hypoxic ventilatory chemosensitivity and cerebrovascular responsiveness during incremental exercise. Respir Physiol Neurobiol. 169 (1), 24-35 (2009).
- Klem, G. H., Lüders, H. O., Jasper, H. H., Elger, C. The ten-twenty electrode system of the International Federation. Electroencephalogr Clin Neurophysiol Suppl. 52, 3-6 (1999).
- Vogiatzis, I., et al. Intercostal muscle blood flow limitation in athletes during maximal exercise. J Physiol. 587 (14), 3665-3677 (2009).
- Vogiatzis, I., et al. Intercostal muscle blood flow limitation during exercise in chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 182 (9), 1105-1113 (2010).
- Contreras-Briceño, F., et al. Reliability of NIRS portable device for measuring intercostal muscles oxygenation during exercise. J Sports Sci. 37 (23), 2653-2659 (2019).
- Crum, E. M., O'Connor, W. J., Van Loo, L., Valckx, M., Stannard, S. R. Validity and reliability of the Moxy oxygen monitor during incremental cycling exercise. Eur J Sport Sci. 17 (8), 1037-1043 (2017).
- Vogiatzis, I., et al. Quadriceps muscle blood flow and oxygen availability during repetitive bouts of isometric exercise in simulated sailing. J Sports Sci. 29 (10), 1041-1049 (2011).
- Grassi, B., Quaresima, V. Near-infrared spectroscopy and skeletal muscle oxidative function in vivo in health and disease: A review from an exercise physiology perspective. J Biomed Opt. 21 (9), 091313 (2016).
- Duncan, A., et al. Measurement of cranial optical path length as a function of age using phase resolved near infrared spectroscopy. Pediatr Res. 39 (5), 889-894 (1996).
- Aebi, M. R., Willis, S. J., Girard, O., Borrani, F., Millet, G. P. Active preconditioning with blood flow restriction or/and systemic hypoxic exposure does not improve repeated sprint cycling performance. Front Physiol. 10, 1393 (2019).
- Cocking, S., et al. Repeated sprint cycling performance is not enhanced by ischaemic preconditioning or muscle heating strategies. Eur J Sport Sci. 21 (2), 166-175 (2021).
- Kligfield, P., et al. Recommendations for the standardization and interpretation of the electrocardiogram. J Am Coll Cardiol. 49 (10), 1109-1127 (2007).
- Dillon, H. T., et al. The effect of posture on maximal oxygen uptake in active healthy individuals. Eur J Appl Physiol. 121 (5), 1487-1498 (2021).
- DeCato, T. W., Haverkamp, H., Hegewald, M. J. Cardiopulmonary exercise testing (CPET). Am J Respir Crit Care Med. 201 (1), P1-P2 (2020).
- Skinner, J. S., Mclellan, T. H. The transition from aerobic to anaerobic metabolism. Res Q Exerc Sport. 51 (1), 234-248 (1980).
- Elmberg, V., et al. Reference equations for breathlessness during incremental cycle exercise testing. ERJ Open Res. 9 (2), 00566-02022 (2023).
- Borg, G. A. Psychophysical bases of perceived exertion. Med Sci Sports Exerc. 14 (5), 377-381 (1982).
- Perrey, S. Could near infrared spectroscopy be the new weapon in our understanding of the cerebral and muscle microvascular oxygen demand during exercise. J Sport Health Sci. 13 (4), 457-458 (2024).
- Orcioli-Silva, D., et al. Cerebral and muscle tissue oxygenation during exercise in healthy adults: A systematic review. J Sport Health Sci. 13 (4), 459-471 (2024).
- Kovalenko, B., Roskosky, M., Freedman, B. A. Effect of ambient light on near infrared spectroscopy. J Trauma Treat. 04 (03), (2014).
- Wik, L. Near-infrared spectroscopy during cardiopulmonary resuscitation and after restoration of spontaneous circulation: A valid technology. Curr Opin Crit Care. 22 (3), 191-198 (2016).
- Pirovano, I., et al. Effect of adipose tissue thickness and tissue optical properties on the differential pathlength factor estimation for NIRS studies on human skeletal muscle. Biomed Opt Express. 12 (1), 571 (2021).
- Van Beekvelt, M. C. P., Borghuis, M. S., Van Engelen, B. G. M., Wevers, R. A., Colier, W. N. J. M. Adipose tissue thickness affects in vivo quantitative near-IR spectroscopy in human skeletal muscle. Clin Sci (Lond). 101 (1), 21-28 (2001).
- Homma, S. Influence of adipose tissue thickness on near infrared spectroscopic signal in the measurement of human muscle. J Biomed Opt. 1 (4), 418 (1996).
- Gomes, A. C., et al. Body composition assessment in athletes: Comparison of a novel ultrasound technique to traditional skinfold measures and criterion DXA measure. J Sci Med Sport. 23 (11), 1006-1010 (2020).
- Delpy, D. T., Cope, M., Zee, P. V. D., Arridge, S., Wray, S., Wyatt, J. Estimation of optical pathlength through tissue from direct time of flight measurement. Phys Med Biol. 33 (12), 1433-1442 (1988).
- Talukdar, T., Moore, J. H., Diamond, S. G. Continuous correction of differential path length factor in near-infrared spectroscopy. J Biomed Opt. 18 (5), 056001 (2013).
- Zonios, G., Bykowski, J., Kollias, N. Skin melanin, hemoglobin, and light scattering properties can be quantitatively assessed in vivo using diffuse reflectance spectroscopy. J Invest Dermatol. 117 (6), 1452-1457 (2001).
- Patel, N. A., Bhattal, H. S., Griesdale, D. E., Hoiland, R. L., Sekhon, M. S. Impact of skin pigmentation on cerebral regional saturation of oxygen using near-infrared spectroscopy: A systematic review. Crit Care Explor. 6 (2), e1049 (2024).
- Wassenaar, E. B., Van Den Brand, J. G. H. Reliability of near-infrared spectroscopy in people with dark skin pigmentation. J Clin Monit Comput. 19 (3), 195-199 (2005).
- Miranda-Fuentes, C., et al. Changes in muscle oxygen saturation measured using wireless near-infrared spectroscopy in resistance training: A systematic review. Int J Environ Res Public Health. 18 (8), 4293 (2021).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены