Method Article
Транскраниальная пульсовая стимуляция у пациентов с болезнью Альцгеймера
В этой статье
Резюме
В данной статье описана методика транскраниальной пульсовой стимуляции у пациентов с болезнью Альцгеймера. В нем подробно обсуждаются показания, методология и будущие перспективы.
Аннотация
Транскраниальная пульсовая стимуляция (TPS) — это неинвазивная нейромодуляционная терапия с маркировкой Conformité Européenne (CE) для лечения болезни Альцгеймера (БА). Первоначальные пилотные исследования продемонстрировали многообещающее влияние на когнитивные функции. Эта статья посвящена процедуре лечения пациентов с болезнью Альцгеймера с использованием устройства TPS под контролем МРТ с нейронавигацией. Протокол, которому необходимо следовать для этого, подробно описан, включая необходимые процедуры и настройки устройства. Также представлен краткий обзор репрезентативных клинических результатов, опубликованных на сегодняшний день. В дополнение к значительным клиническим улучшениям когнитивных функций и аффекта, представлены нежелательные явления (НЯ) и возможные нежелательные явления устройства (ADE) для получения данных по безопасности. Наконец, критически обсуждается метод. В будущем следует провести рандомизированные контролируемые исследования, чтобы исключить любые эффекты плацебо. В настоящее время также не хватает долгосрочных исследований с большим количеством пациентов. Несмотря на эти нерешенные вопросы, TPS имеет потенциал в качестве вспомогательного лечения для пациентов с болезнью Альцгеймера при использовании в контролируемых, научно обоснованных условиях.
Введение
Методы неинвазивной стимуляции мозга (NiBS) стали объектом растущего интереса в исследованиях деменции, предлагая потенциальные терапевтические стратегии для смягчения когнитивных и функциональных дефицитов, связанных с нейродегенеративными заболеваниями. Накопленные данные свидетельствуют о том, что NiBS может улучшать когнитивные функции или замедлять снижение когнитивных способностей у людей с болезнью Альцгеймера (БА) на различныхстадиях заболевания. Среди этих методов транскраниальная пульсовая стимуляция (TPS) особенно примечательна своей способностью обеспечивать высоконаправленную и точно направленную стимуляцию мозга не только на поверхности коры головного мозга, но и в более глубоких областях мозга 3,4. Побочные эффекты, связанные с ТПС, редки, средней степени тяжести и преходящие 3,5.
Было доказано, что терапевтическая ультразвуковая терапия и экстракорпоральная ударно-волновая терапия (ЭУВТ), первоначально разработанные в области ортопедии и кардиологии, способствуют заживлению тканей и улучшают кровоток. В ортопедии ЭУВТ особенно применялась для лечения заболеваний опорно-двигательного аппарата, таких как тендинопатии и проблемы заживления костей, в то время как в кардиологии ее влияниена здоровье сосудов изучалось 6,7. TPS был адаптирован для неврологических приложений, особенно в исследованиях болезни Альцгеймера, демонстрируя перспективы в борьбе со снижением когнитивных способностей и функциональными нарушениями 8,3,4. В этом методе используются ударные волны для облегчения симптомов у пациентов с болезнью Альцгеймера, как продемонстрировали данные пилотного проекта рабочей группы в этом учебном пособии5. Ударные волны отличаются от ультразвуковых тем, что в них не задействована высокочастотная переменная нагрузка9. Генерируемый профиль ударной волны, как показано на рисунке 1, наглядно иллюстрирует сингулярный импульс давления и последующее уплощение амплитуды во время TPS, а также более высокочастотную амплитуду, характерную для ультразвука. Из-за высокочастотного знакопеременного напряжения энергия ультразвуковых волн поглощается тканями, что может привести к разогреву тканей – эффекту, не наблюдающемуся при ударных волнах. В других приложениях используются высокоэнергетические ударные волны, тогда как в TPS энергия, вводимая в ткань, является низкоэнергетической9. О потенциальном воздействии на болезнь Альцгеймера впервые сообщалось в виде улучшений в Консорциуме по созданию реестра болезни Альцгеймера (CERAD)3, а также увеличения толщины коры головного мозга внескольких областях и изменений в связности МР-сети11.
Механизмы действия TPS в настоящее время изучаются, и исследования сосредоточены на том, как этот неинвазивный метод модулирует активность мозга на клеточном уровне, потенциально запуская процессы механотрансдукции, которые могут повысить нейропластичность и улучшить когнитивныефункции. При ударно-волновой терапии физическая энергия воздействует на локализованный участок ткани и индуцирует механотрансдукцию12, стимулируя высвобождение факторов роста13,14 и оксида азота15. Эти эффекты, в свою очередь, могут усиливать кровообращение и способствовать неоангиогенезу16.
Цель TPS заключается в том, чтобы обеспечить дополнительную терапию, которая является безопасной и может привести к улучшению симптомов. Стимулируемые области могут включать двустороннюю лобную кору, двустороннюю латеральную теменную кору, расширенную предклинительную кору и двустороннюю височную кору. Обычный протокол лечения состоит из шести сеансов с 6000 импульсов в течение 2 недель в качестве первого цикла лечения.
Процедура считается безопасной, так как примерно в 4% сеансов сообщалось о нежелательных явлениях, характеризующихся умеренной субъективной тяжестью, которая является преходящей и не имеет четкой причинно-следственной связи с нежелательными явлениями, связанными с устройством (ADE)5.
Несмотря на то, что эти первоначальные результаты обнадеживают, исследователям и клиницистам крайне важно оценить, подходит ли TPS для их конкретных применений. Факторы, которые следует учитывать, включают стадию болезни Альцгеймера, реакцию пациента на другие методы лечения и наличие учреждений, которые могут безопасно проводить TPS под руководством специалиста. Для людей на ранних и умеренных стадиях болезни Альцгеймера TPS может предложить потенциальные когнитивные преимущества с минимальными побочными эффектами, но он еще не считается самостоятельным лечением. Вместо этого он может дополнять существующие методы лечения, такие как фармакологические вмешательства или когнитивная тренировка. Результаты рандомизированных контролируемых исследований на сегодняшний день отсутствуют. Тем не менее, TPS может иметь потенциал в качестве дополнительного лечения для пациентов с болезнью Альцгеймера при контролируемом использовании и научных исследованиях.
протокол
Анализ всех пациентов, получавших TPS, был составлен в рамках местного регистра, утвержденного Комитетом по этике Региональной медицинской палаты (Ärztekammer Nordrhein, Nr. 2021026). Кроме того, все пациенты подписали письменное согласие на лечение. Лечение с ТПС прошли 11 пациентов (девять мужчин, две женщины, возраст 59-77 лет, М = 69,82). Перед началом лечения все пациенты прошли подробный процесс информированного согласия, в ходе которого они были подробно проинформированы о потенциальных преимуществах и рисках транскраниальной пульсовой стимуляции (TPS) с помощью системы NEUROLITH.
1. Отбор и подготовка пациентов
- Прежде чем начать эту стимуляцию, решающее значение имеет отбор пациентов и информированное согласие. Используйте маркировку CE для лечения болезни Альцгеймера. Подтвердите диагноз с помощью биомаркеров СМЖ на основе клинического синдрома Альцгеймера. Проводить лечение заболевания в соответствии с национальными или международными рекомендациями невролога или психиатра.
ПРИМЕЧАНИЕ: TPS может быть предложен в качестве дополнения к научным исследованиям. Поскольку TPS назначался в качестве дополнительного лечения, все пациенты продолжали выполнять свои обычные планы лечения на протяжении всего лечения. Некоторые пациенты принимали антидеменционные препараты и/или антипсихотики во время сеансов TPS; Тем не менее, эти препараты не были частью протокола исследования и не были модифицированы или стандартизированы в рамках вмешательства. - Используйте следующие критерии исключения для TPS: Лечение противопоказано при соответствующих внутримозговых патологиях, не связанных с болезнью Альцгеймера, включая сосудистую энцефалопатию, тромбоз в области лечения, степень Фазекаса 3, опухоли, сосудистые мальформации, металлические имплантаты и церебральную амилоидную ангиопатию (КАА) в соответствии с Бостонскими критериями. Дополнительными противопоказаниями являются терапия антителами в анамнезе или продолжающаяся терапия, нарушения свертываемости крови или пероральная антикоагуляция, лечение кортикостероидами в течение шести недель до первого применения, эпилепсия (либо множественные припадки, либо один приступ с очагом припадка), кардиостимуляторы, не одобренные для терапии TPS, рецидивирующие обмороки, тяжелые аффективные поведенческие расстройства, влияющие на повседневную жизнь, такие как агрессия или психоз, беременность, а также медицинские показания, которые могут привести к несоблюдению протокола. Что касается диагноза и критериев исключения, включая МРТ, ЭЭГ, СМЖ, анализы, лабораторные тесты и подробные когнитивные и аффективные оценки в ходе обследования.
2. Нейропсихологическое тестирование
- Проведите нейропсихологическое тестирование до первой стимуляции (исходный уровень) и после последней стимуляции (постстимуляция). Для этого исследования использовалась Шкала оценки болезни Альцгеймера (ADAS).
- Прежде чем начать ADAS, подготовьте испытательную среду, чтобы убедиться, что она тихая, комфортная и свободная от отвлекающих факторов. Проведите оценку с квалифицированным клиницистом или нейропсихологом, который следует структурированному формату для оценки конкретных когнитивных областей.
- ADAS состоит из двух основных компонентов: когнитивной субшкалы (ADAS-Cog) и некогнитивной субшкалы. Используйте ADAS-Cog, который используется чаще всего, для оценки памяти, языка, ориентации и практики с помощью серии задач, как описано ниже.
- Запоминание слов: Предоставьте пациенту список слов и попросите вспомнить их немедленно и после задержки.
- Называние предметов и пальцев: Покажите пациенту ряд предметов и попросите назвать их правильно.
- Следующие команды: Попросите пациента выполнить определенные действия на основе устных инструкций для оценки понимания и практики.
- Визуо-конструирование: Дайте пациенту задание копировать геометрические фигуры для оценки зрительно-пространственных навыков.
- Идеациональная практика: Попросите пациента продемонстрировать использование обычных предметов (например, карандаша или расчески).
- Ориентация: Спросите пациента о текущей дате, дне недели и месте.
- Распознавание слов: Попросите пациента распознать ранее представленные слова из списка отвлекающих слов.
- Языковые способности: Оцените беглость речи и понимание пациента с помощью структурированных бесед и построения предложений.
- Используйте некогнитивную субшкалу для оценки поведенческих симптомов, таких как изменения настроения, апатия или возбуждение.
- Для обеспечения последовательности попросите врача, проводящего тест, строго следовать инструкциям, изложенным в руководстве ADAS. Оценивайте каждую задачу на основе производительности, при этом более высокие баллы указывают на более серьезные нарушения.
- После последнего сеанса стимуляции повторите ADAS, используя параллельную версию теста, чтобы убедиться, что результаты отражают подлинные изменения в когнитивных функциях, а не практические эффекты.
3. Подготовка устройства и окружающей среды
- Включите устройство. Найдите главный выключатель питания на задней панели устройства и включите его.
- Нажмите кнопку перехода в режим ожидания на передней панели. Инициализация устройства займет около 5 минут.
- Расположите пациента. Убедитесь, что пациент удобно сидит, с возможной поддержкой шеи. Проследите, чтобы пациент носил очки с распознаванием линз. Закрепите очки на голове пациента с помощью ленты или ремешка, чтобы удерживать их на месте.
- Настройте камеру. Выровняйте камеру так, чтобы голова пациента была полностью видна в кадре. Эта камера имеет решающее значение для отслеживания и калибровки.
4. Испытание высоким напряжением (ежедневное техническое обслуживание)
- Проведите испытание высоким напряжением (HV-тест). Проводите этот тест один раз в 24 часа. Следуйте инструкциям на экране, чтобы завершить тест, нажав триггерную кнопку на ручном аппликаторе.
5. Подготовка наконечника
- Подготовьте наконечник, нанеся каплю силиконового масла на мембрану наконечника.
- Прикрепите предварительно заполненную соединительную мембрану (дистанционную часть) к наконечнику, убедившись, что она надежно закреплена для оптимальной работы.
6. Калибровка для новых пациентов
- Загрузите данные МРТ пациента. Для новых пациентов убедитесь, что доступны необходимые МРТ-сканирования (Т1-взвешенные изображения головы с высоким разрешением от лба до спины, охватывающие ухо до уха).
- Вставьте внешнее запоминающее устройство (USB или CD), содержащее данные МРТ, в USB-порт системы.
- Создайте профиль пациента. Выберите в системе «Новый пациент » и введите необходимую информацию. При создании нового профиля пациента в системе часть информации автоматически импортируется с МРТ-CD, в то время как другие детали нужно вводить вручную.
- После вставки компакт-диска в систему полное имя пациента и дата рождения автоматически извлекаются из метаданных на компакт-диске МРТ. Вручную введите план лечения в систему. Выберите предварительно настроенный протокол лечения болезни Альцгеймера (БА), уже сохраненный в системе. Этот протокол включает в себя следующие настройки: частота 4 Гц, уровень энергии 0,2 мДж/мм2 и 6 000 импульсов за сеанс. Протокол может быть использован как есть или скорректирован в зависимости от предпочтений врача.
- Загрузите данные МРТ и проверьте качество изображений. Чтобы проверить качество данных МРТ, вручную прокрутите отдельные срезы изображений МРТ в системе. Убедитесь, что все анатомические структуры четкие и четко очерченные, а также проверьте отсутствие артефактов движения или искажений. Подтвердите, что общее разрешение Т1-взвешенных изображений достаточно для точной нейронавиги. При необходимости отрегулируйте выделенные изображения и приступайте к калибровке.
- Чтобы откалибровать изображения, используйте калибровочный перо для проведения калибровочной ручки калибровки по 3 точкам по следующим путям.
Способ 1: От лба к затылку.
Путь 2: От одного уха к другому.
Способ 3: Выполняйте круговые или зигзагообразные движения по макушке. - Убедитесь, что линзы обнаружения всегда обращены к камере во время калибровки.
- Убедитесь, что 3D-модель головы на экране правильно выровнена по отношению к голове пациента, повернув ее для проверки точек контакта.
7. Настройка региона обработки (опционально)
- Определите регионы лечения в зависимости от конкретных потребностей пациента. Для этого исследования был использован предварительно настроенный протокол лечения болезни Альцгеймера, включающий двустороннюю лобную долю, двустороннюю теменную долю и предклинье. Дополнительно, к исходному протоколу, добавьте двустороннюю височную кору. Используйте снимки МРТ и конкретные анатомические ориентиры мозга, чтобы определить области, которые необходимо стимулировать.
- Отрегулируйте размер, форму и количество областей обработки на дисплее. Для корректировки ROI процесс выполняется полностью с помощью сенсорного дисплея.
- Начните с доступа к модулю «Планирование лечения» в главном интерфейсе системы. В этом модуле выберите опцию « Корректировка ROI », чтобы включить редактирование областей лечения. Как только система перейдет в режим настройки, на экране отобразится ROI по умолчанию.
- Чтобы расположить ROI над нужной анатомической областью, такой как лобная доля, теменная доля, предклинье или височная кора, используйте кнопки со стрелками на сенсорном дисплее. Кнопки позволяют постепенно перемещать ROI во всех направлениях (вверх, вниз, влево, вправо) для точного выравнивания с целевой областью мозга.
- После позиционирования ROI отрегулируйте его размеры (размер, глубину и форму) с помощью специальных экранных элементов управления:
Регулировка глубины (кнопка A): нажмите кнопку глубины и отрегулируйте уровень проникновения ROI в соответствии с требованиями к лечению.
Регулировка ширины (кнопка B): Используйте кнопку регулировки ширины, чтобы увеличить или уменьшить размер ROI по горизонтали.
Регулировка высоты (кнопка C): Измените вертикальный размер ROI, коснувшись элемента управления регулировкой высоты. Сохраните настройки после завершения.
8. Проведение процедуры
- Последовательно нанесите обильное количество геля для ультразвука на кожу головы пациента для оптимальной передачи энергии.
- Начните лечение. Выберите режим лечения на устройстве и убедитесь, что предварительно заполненная мембрана прикреплена правильно. Правильность крепления предварительно заполненной мембраны проверяется путем ее правильного защелкивания на наконечнике. По желанию пациент может использовать средства защиты органов слуха во время сеанса.
- Держите наконечник перпендикулярно коже головы пациента, обеспечивая его равномерное перемещение по поверхности. На рисунке 2 показано идеальное выравнивание между пациентом и NEUROLITH во время TPS. На рисунке 3 показан пример областей интереса (ROI) и моделирования стимулированной ткани на МРТ пациента. На рисунке 4 показана иллюстрация портативного устройства во время стимуляции.
- Следите за стимуляцией. Обрабатывайте каждую область до тех пор, пока целевые области на дисплее не станут зелеными, что указывает на правильное покрытие. Продолжайте перемещать наконечник, держа линзы обнаружения в поле зрения камеры, чтобы обеспечить непрерывное отслеживание.
ПРИМЕЧАНИЕ: Если очки распознавания немного смещаются во время лечения, сеанс можно продолжать. Однако, если стекла сняты, требуется повторная калибровка. - Завершите сеанс. Чтобы завершить процедуру, нажмите кнопку «Стоп » на устройстве. Конечная точка сеанса достигается при достижении 6000 импульсов.
9. Процедуры после лечения
- Очистите оборудование. Очистите наконечник и съемную мембрану с помощью одобренных салфеток (избегайте чистящих средств на спиртовой основе).
- Уход за пациентом: Аккуратно очистите область кожи головы, чтобы удалить остатки ультразвука. При необходимости высушите волосы пациента полотенцем или феном. После лечения посоветуйте пациентам оставаться рядом в течение следующих 10-15 минут в случае, если они испытывают какие-либо отсроченные или легкие побочные эффекты, такие как головокружение, головная боль или дискомфорт в коже головы, хотя активное наблюдение не требуется. Поощряйте пациентов избегать обезвоживания, так как это способствует общему восстановлению и благополучию. Посоветуйте пациенту избегать интенсивной физической активности до конца дня, особенно если он чувствует усталость или испытывает легкий дискомфорт после сеанса.
- Хранение данных о лечении: Сохраняйте все данные о лечении, включая определенные регионы, и корректируйте их для будущих сеансов. Любые наблюдения во время лечения или обратная связь должны быть задокументированы.
Результаты
Транскраниальная пульсовая стимуляция облегчила симптомы у пациентов с болезнью Альцгеймера, о чем свидетельствуют неконтролируемые пилотные данные 11 пациентов (девять мужчин, две женщины, возрастной диапазон 59-77 лет, M = 69,82), опубликованные рабочей группой этого урока1. Стимулированные области включали двустороннюю лобную кору, двустороннюю латеральную теменную кору и расширенную предклинельную кору. В протокол была добавлена двусторонняя височная кора. Лечение проводилось в шесть начальных сеансов с 6000 импульсов в течение 2 недель в качестве первого цикла лечения.
Протокол лечения во время стимуляции включал 4 Гц, 0,20 мДж/мм2 и 6000 импульсов. Трое из 11 пациентов (27%) сообщили о нежелательных явлениях в трех из 75 сеансов (4%). К ним относились боль в челюсти (NRS 4/10), тошнота (NRS 7/10) и сонливость (NRS 10/10). Тем не менее, ни один из них не длился более 24 часов, и не все из них можно было напрямую отнести к стимуляции как нежелательные явления устройства (ADE).
Наблюдалась достоверная разница в общем балле ADAS после стимуляции по сравнению с исходным уровнем, с улучшением с 30,2 до 25,8 (p = 0,01), и в балле ADAS-Cog, который улучшился с 25,8 до 23,3 (p = 0,04; Рисунок 5). В то время как у некоторых пациентов наблюдались лишь незначительные улучшения, наилучшее улучшение у пациента составило 40%, что привело к общему улучшению на 15,76% по общему баллу ADAS и на 8,65% по шкале ADAS Cog (Рисунок 6). Кроме того, значительная разница в симптомах депрессии была обнаружена в субшкале теста ADAS. Односторонний t-критерий показал значительное снижение депрессивных симптомов, что было измерено с помощью субшкалы теста ADAS. До стимуляции среднее значение составляло 0,7 (SD = 1,1), а после стимуляции снижалось до 0,2 (SD = 0,4; t (8) = 1,859, p < 0,01).
Субъективная шкала оценки была завершена до и после двухнедельного периода лечения. Эта шкала позволяет пациентам сообщать о тяжести симптомов и любых воспринимаемых нежелательных явлениях по числовой шкале от 0 до 10, где более высокие цифры указывают на большую интенсивность симптомов. Среднее субъективное улучшение тяжести симптомов, измеренное по данным NRS, составило от 5,7 до 3,4 (p = 0,023).
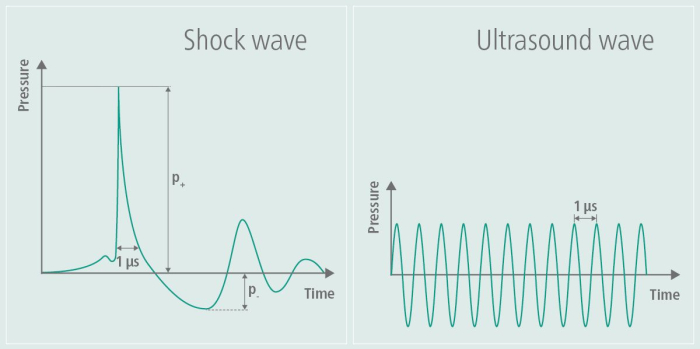
Рисунок 1: Ударная волна во время стимуляции. График иллюстрирует амплитуду TPS в левой части изображения и сравнивает ее с амплитудой ультразвука в правой части изображения. Во время TPS генерируется сингулярный импульс давления, за которым следует последующее сплющивание амплитуды. В отличие от этого, амплитуда ультразвука не выравнивается, а сохраняется, что приводит к непрерывным высокочастотным колебаниям с течением времени. Эта цифра была изменена с9. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.

Рисунок 2: Навигационная система МРТ. Изображение иллюстрирует идеальное выравнивание между пациентом и NEUROLITH во время TPS. 3D-камера контактирует с линзами обнаружения очков и наконечника. Только в том случае, если эта передача гарантирована, наконечник распознается в правильном пространственном положении и визуализация стимуляции на экране не нарушается. Эта цифра была изменена с9. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.

Рисунок 3: Области интереса и стимулируемые территории. На изображении показан пример областей интереса (ROI) и моделирования ткани, стимулированной на МРТ пациента. Цвета дополнительно дифференцируют количество импульсов, приложенных в соответствующих областях предклинья, а также в лобной и теменной областях. За зеленой окраской следуют бирюзовый, синий и фиолетовый. Фиолетовый цвет указывает на чрезмерную интенсивность, и его следует избегать. Стимулированные области визуализируются в виде смоделированных данных из навигационной системы в виде преимущественно достигнутых областей, но это не измеряется как реальная прикладная активация мозга. Дополнительная временная стимуляция добавляется в протокол Kempen, хотя она не предопределена как ROI. Слева: осевой вид, в центре: сагиттальный вид, справа: корональный вид. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.

Рисунок 4: Портативное устройство. На этом рисунке показано портативное устройство, используемое во время стимуляции. Важнейшие подготовительные шаги включают нанесение достаточного количества геля для ультразвука на кожу головы пациента для обеспечения оптимальной передачи энергии и проверку надежного и правильного прикрепления предварительно заполненной мембраны. Во время лечения наконечник держат перпендикулярно коже головы и равномерно перемещают по поверхности для поддержания постоянной стимуляции. Эта цифра была изменена с9. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
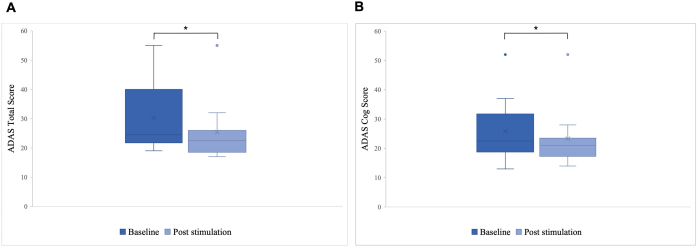
Рисунок 5: Шкала оценки болезни Альцгеймера (ADAS) перед первой стимуляцией. Среднее значение баллов группы пациентов по шкале оценки болезни Альцгеймера (ADAS) до первой стимуляции (темно-синий) и после последней стимуляции (светло-голубой). Более низкий балл указывает на более высокую производительность. Ящичковая диаграмма показывает распределение данных о пациентах. (A) Общий балл ADAS. Линия представляет медиану группы (исходный уровень = 24,5, после стимуляции = 22,5), а крестик представляет средние баллы (M исходный уровень = 30,2 (SD 11,55), M после стимуляции = 25,8 (SD 10,71), *p = 0,01). (B) Оценка по шкале ADAS. Линия представляет медиану группы (исходный уровень = 22,5, после стимуляции = 21), а крест представляет средние баллы (M исходный уровень = 25,8 (SD 10,77), M после стимуляции = 23,3 (SD 10,27), *p = 0,04). Эта цифра была изменена с5. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.

Рисунок 6: Индивидуальные результаты тестов пациентов в ADAS. Индивидуальные результаты тестов пациентов по шкале оценки болезни Альцгеймера (ADAS) до первой стимуляции (исходный уровень) и после последней стимуляции (постстимуляция). Более низкий балл указывает на более высокую производительность. Каждая строка представляет одного пациента. (A) Индивидуальные баллы каждого пациента в общем балле ADAS. Наилучшее улучшение составило 15 баллов (ID 3). (B) Индивидуальные баллы каждого пациента по подшкале ADAS cog score. Наилучшее улучшение составило 14 баллов (ID 3 и ID 4). Эта цифра была изменена с5. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
Обсуждение
В целом, TPS является возможным методом лечения болезни Альцгеймера. С практической точки зрения, процесс интенсификации разработан таким образом, чтобы быть удобным для оператора. Возможность определения областей интереса в начале процедуры, наряду с визуализацией количества импульсов, подаваемых с помощью цветовой маркировки во время лечения, значительно упрощает работу с пользовательским интерфейсом. Настройки областей интереса также могут быть свободно выбраны и скорректированы по мере необходимости. Стимулированные области четко визуализируются в виде смоделированных данных, хотя необходимы дальнейшие разработки со стороны производителя для отображения более глубоких областей, пораженных устройством, на более низких уровнях энергии.
Важнейшие шаги в протоколе TPS включают точное размещение устройства стимуляции над целевыми областями мозга, обеспечение правильной интенсивности и частоты пульсовых волн, а также тщательный мониторинг реакции пациента. Устранение неполадок может включать обеспечение оптимального контакта между наконечником и кожей головы для предотвращения потери энергии или неоптимальной стимуляции. Если наблюдается дискомфорт или побочные эффекты, может потребоваться коррекция интенсивности или изменение положения.
Опубликованные неконтролируемые данные продемонстрировали клинические когнитивные улучшения 5,3, а также увеличение толщины коры головного мозга в нескольких областях мозга10 и изменения связности МР-сети11. Также сообщалось об улучшении настроения 5,4. По сравнению с другими неинвазивными методами стимуляции мозга, TPS имеет несколько явных преимуществ. Во-первых, он сочетает в себе механические ударные волны с точной нейронавигацией, что позволяет целенаправленно воздействовать на пораженные участки мозга. В отличие от ТМС, которая обычно стимулирует только поверхностные корковые слои, глубина проникновения ТПС делает его особенно подходящим для лечения нейродегенеративных заболеваний, таких как болезнь Альцгеймера, где задействованы более глубокие структуры мозга. Кроме того, TPS, по-видимому, имеет благоприятный профиль безопасности, с минимальными и преходящими побочными эффектами, зарегистрированными только в 4% сеансов лечения, что указывает на то, что он может быть более переносимым вариантом для пациентов с умеренным и тяжелым AD5.
Для тщательного изучения механизмов действия и проведения детального анализа потенциальных факторов риска, связанных с терапией ТПС, требуются дополнительные фундаментальные исследования.
В недавнем исследовании, опубликованном этой исследовательской группой, активность сети мозга у пациентов с болезнью Альцгеймера изучалась до и после транскраниальной пульсовой стимуляции (TPS)17. Результаты показывают, что TPS может модулировать колебания мозга и связи, потенциально улучшая когнитивные функции при болезни Альцгеймера. Один из предполагаемых механизмов заключается в том, что повышенные гамма-колебания после TPS могут способствовать глимфатическому клиренсу в мозге. Это возможное влияние на глимфатический клиренс должно быть дополнительно изучено в будущих исследованиях. Кроме того, необходимы дальнейшие механистические исследования, чтобы выяснить, как TPS влияет на физиологию сети мозга и могут ли его нейропротекторные эффекты замедлить или остановить прогрессирование болезни Альцгеймера.
Доклинические исследования на животных, в которых изучается влияние TPS как на здоровый, так и на больной мозг, имеют решающее значение для более глубокого понимания основных механизмов. Важно отметить, что различные методы NiB работают через различные механизмы:1. В связи с этим важно выяснить, играют ли и каким образом эффекты, описанные для ультразвуковой терапии18 и ударно-волновойтерапии6 на ткани, роль в TPS-терапии. В первом из них описано возможное влияние ТПС на процессы механотрансдукции, а также его способность вызывать сосудистые, клеточные и молекулярные изменения, которые требуют тщательного изучения. Кроме того, модуляция нейровоспалительных процессов, с особым акцентом на динамику гематоэнцефалического барьера, представляет собой интригующую область для будущих исследований. Понимание этих эффектов может дать ценную информацию об основных механизмах и помочь оптимизировать TPS для терапевтических применений. Кроме того, это способствует изучению потенциального применения лечения TPS в лечении других нейродегенеративных заболеваний.
TPS является многообещающим терапевтическим подходом; Тем не менее, необходимо учесть несколько ограничений. Контролируемые клинические испытания с группами плацебо необходимы для точного определения специфических эффектов TPS. Существенной проблемой является высокая межиндивидуальная вариабельность в ответ на стимуляцию, на которую могут влиять такие факторы, как стадия болезни Альцгеймера (БА) и наличие сопутствующих заболеваний4. Кроме того, оптимальный протокол для долгосрочного лечения остается неопределенным. Современные подходы включают ежемесячные однократные сеансы бустерной вакцинации или повторение цикла лечения из 12 сеансов в течение года, но доказательства, подтверждающие превосходство одного подхода над другим, отсутствуют. В будущих клинических исследованиях приоритетное внимание должно уделяться определению оптимальных параметров стимуляции, оценке того, как специфические для пациента факторы (например, стадия БА) влияют на терапевтические результаты, а также изучению долгосрочных эффектов и устойчивости терапии ТПС.
Раскрытие информации
Автор Ларс Войтеки ранее получал гранты на финансирование и институциональную поддержку от Немецкого исследовательского общества, Hilde-Ulrichs-Stiftung für Parkinsonforschung и ParkinsonFonds Germany, BMBF/ERA-NETNEURON, DFG Forschergruppe (FOR1328), Deutsche Parkinson Vereinigung (DPV), Forschungskommission, Medizinische Fakultät, HHU Düsseldorf, UCB; Medtronic, UCB, Teva, Allergan, Merz, Abbvie, Roche, Bial, Merck, Novartis, Desitin, Spectrum. Автор Ларс Войтецки является консультантом следующих компаний: TEVA, UCB Schwarz, Desitin, Medtronic, Abbott/Abbvie, MEDA, Boehringer I, Storz Medical, Kyowa Kirin, Guidepoint, Merck, Merz, Synergia, BIAL, Zambon, Sapio Life, STADA, Inomed и Vertanical. Автор Селин Конт является консультантом Storz Medical. Остальные авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Благодарности
Мы благодарим пациентов за их соблюдение и участие. Техническая помощь и сбор данных были обеспечены с помощью Вероники Хирш и Михаэлы Весслер (медицинские технические ассистенты).
Материалы
| Name | Company | Catalog Number | Comments |
| Disinfectant Wipes: mikrozid universal wipes | schülke | GTIN: 4032651957774 | Used to clean the hand piece after each session to ensure hygiene |
| Dry Towels: Wisch-/Pflegetuch Kolibri | IGEFA Handelsgesellschaft mbH & Co. KG | PZN: 10417600 | Used to dry the patient's skin after the ultrasound gel has been cleaned |
| Handpiece | Storz Medical | HW 030816.01 (114) | Used to hold the device during treatment |
| NEUROLITH | Storz Medical | SN: 19880_0015 | The NEUROLITH system with TPS is a CE-certified device |
| Patient Chair | Adjustable chair for optimal patient positioning during the treatment | ||
| silicone oil | Storz Medical | 13330 | Applied onto the membrane of the handpiece before attaching the prefilled coupling membrane (the distance piece) to the handpiece |
| Sonosid Ultrasound Gel | Asid Bonz GmbH | PZN: 5362311 | Applied to the scalp to ensure optimal transmission of acoustic pulses through the skull |
| Wash Gloves: Esemtan wash mitts | schülke | GTIN: 4032651297016 | For removing the ultrasound gel from the patient post-treatment |
Ссылки
- Koch, G., et al. The emerging field of non-invasive brain stimulation in Alzheimer's disease. Brain. Epub ahead of print. , (2024).
- Menardi, A., et al. Toward noninvasive brain stimulation 2.0 in Alzheimer's disease. Ageing Res Rev. 75, 101555 (2022).
- Beisteiner, R., et al. Transcranial pulse stimulation with ultrasound in Alzheimer's disease-a new navigated focal brain therapy. Adv Sci. 7 (3), 1902583 (2019).
- Matt, E., Dörl, G., Beisteiner, R. Transcranial pulse stimulation (TPS) improves depression in AD patients on state-of-the-art treatment. Alzheimer's Dement. 8 (1), e12245 (2022).
- Cont, C., et al. Retrospective real-world pilot data on transcranial pulse stimulation in mild to severe Alzheimer's patients. Front Neurol. 13, 948204 (2022).
- Guo, J., Hai, H., Ma, Y. Application of extracorporeal shock wave therapy in nervous system diseases: A review. Front Neurol. 13, 963849 (2022).
- Khanna, A., Nelmes, R. T., Gougoulias, N., Maffulli, N., Gray, J. The effects of LIPUS on soft-tissue healing: a review of literature. Br Med Bull. 89, 169-182 (2009).
- Chen, X., You, J., Ma, H., Zhou, M., Huang, C. Transcranial pulse stimulation in Alzheimer's disease. CNS Neurosci Ther. 30 (2), e14372 (2024).
- . Website of Manufacturer Available from: https://www.storzmedical.com/en/physics-and-technology (2025)
- Popescu, T., Pernet, C., Beisteiner, R. Transcranial ultrasound pulse stimulation reduces cortical atrophy in Alzheimer's patients: a follow-up study. Alzheimer's Dement. 7 (1), e12121 (2021).
- Dörl, G., Matt, E., Beisteiner, R. Functional specificity of TPS brain stimulation effects in patients with Alzheimer's disease: A follow-up fMRI analysis. Neurol Ther. 11 (3), 1391-1398 (2022).
- d'Agostino, M. C., Craig, K., Tibalt, E., Respizzi, S. Shock wave as biological therapeutic tool: From mechanical stimulation to recovery and healing, through mechanotransduction. Int J Surg. 24, 147-153 (2015).
- Yahata, K., et al. Low-energy extracorporeal shock wave therapy for promotion of vascular endothelial growth factor expression and angiogenesis and improvement of locomotor and sensory functions after spinal cord injury. J Neurosurg. 25 (6), 745-755 (2016).
- Hatanaka, K., et al. Molecular mechanisms of the angiogenic effects of low-energy shock wave therapy: roles of mechanotransduction. Am J Physiol. 311 (3), C378-C385 (2016).
- Mariotto, S., et al. Extracorporeal shock waves: from lithotripsy to anti-inflammatory action by NO production. Nitric oxide. 12 (2), 89-96 (2005).
- Flournoy, J., Ashkanani, S., Chen, Y. Mechanical regulation of signal transduction in angiogenesis. Front Cell Dev Biol. 10, 933474 (2022).
- Wojtecki, L., Cont, C., Stute, N., Galli, A., Schulte, C., Trenado, C. Electrical brain networks before and after transcranial pulsed shockwave stimulation in Alzheimer's patients. Geroscience. Epub ahead of print. , (2024).
- Sarica, C., et al. Human studies of transcranial ultrasound neuromodulation: A systematic review of effectiveness and safety. Brain Stimul. 15 (3), 737-746 (2022).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены