Method Article
Твердофазный синтез функционализированных Бис-пептида Использование «Безопасность Поймать« Методология
В этой статье
Резюме
Эффективный твердофазный пептидный синтез функционализированных бис-пептида тример использовании "предохранитель" расщепление процедуру смолы HMBA описано.
Аннотация
В 1962 году Р. Merrifield опубликовал первую процедуру с использованием твердофазного синтеза пептидов в качестве нового маршрута для эффективного синтеза пептидов. Этот метод быстро доказал преимущество перед ее решения фазы предшественника во времени и труда. Улучшения, касающиеся природы твердой поддержке, защитные группы, используемые связи методы, используемые в течение последних пяти лет только увеличилась полезность оригинальная система Merrifield в. Сегодня, использование Бок основе защиты и базы / нуклеофила расщепляемые стратегии смолы или Fmoc основе защиты и кислой смолы расщепляемые стратегии, впервые RC Шеппард, которые наиболее часто используются для синтеза пептидов 1.
Вдохновленные твердой поддержкой стратегии Merrifield, мы разработали Бок / трет-бутил твердофазного синтеза стратегии для сборки функционализированных бис-пептиды 2, которая описана в этом документе. Применение твердофазного синтеза по сравнению тРешение о фазы методологии является не только выгодным во времени и труда, как описано Merrifield 1, но и обеспечивает большую легкость в синтезе бис-пептидные библиотеки. Синтез, который мы демонстрируем здесь включает в себя финальную стадию дробления, который использует два шага "предохранитель" механизм, чтобы освободить функциональными бис-пептида от смолы diketopiperazine образования.
Бис-пептиды являются жесткими, спиро-лестница олигомеров бис-аминокислоты, которые могут разместить функциональность в предсказуемом, проектируемые и путь, контролируемый тип и стереохимия мономерных единиц и связи между мономера. Каждый бис-аминокислоты стереохимически чистый, циклические леса, который содержит две аминокислоты (карбоновые кислоты с α-амин) 3,4. Наша лаборатория в настоящее время изучает возможности функционального бис-пептиды в самых различных областях, включая катализ, белок-белковых взаимодействий и пanomaterials.
протокол
1. Установка
- Реакция установка для твердофазного синтеза картридж полипропиленовый фильтр или стеклянный реактор, который подключен через полипропиленовые трубы для закрытых фильтрации под вакуумом колбу, как показано на рисунке 1. Реакция может быть смешан с помощью магнитной мешалкой или при пропускании азота через реактор.
- Газовый коллектор подключен к цилиндру Аргон оснащены сушкой трубы и нефть барботер Кроме того, рекомендуется, так как позволяет реакционного сосуда, которые должны содержаться в инертной атмосфере и позволяет избавиться от реагентов из герметичных контейнерах.
- Все операции выполняются в вытяжном шкафу и специальные средства защиты (защитные очки, халат и перчатки из нитрила) не требуется.
2. Загрузка первого Бис-пептида Onto смолы
- Взвесьте 114 мг HMBA-AM смолы (0,88 ммоль / г нагрузка, 100 мкмоль) в 8 мл реакционный сосуд и добавить магнитной мешалкой. Закройте начало йэлектронной сосуд с перегородкой резины и чистки трубки аргоном, по крайней мере 5 минут.
- В то же время, весит 117,3 мг соединения 1 на рисунке 3 (586,63 г / моль, 2EQ) и 59,2 мг 1 - (мезитилена-2-сульфонил)-3-нитро-1 ,2,4-триазола (MSNT, 296,0 г / моль, 2EQ) в 15 мл одноразовые трубки центрифуги и растворяют в 2 мл безводного дихлорметана (DCM). Добавить 24 мкл 1-метилимидазола (NMI, 80,81 мл / моль, 3eq) к решению и перемешать до полного растворения.
- Передача активированной решение реакционного сосуда с помощью шприца и позволит активизировать в атмосфере аргона в течение ночи (~ 10 часов).
- Удалить перегородки и слейте реакционной смеси. Вымойте смолы с DCM (5x) и диметилформамида (DMF) (5x). Выполните "метилового красного теста", описанный в разделе 10.1, чтобы оценить степень смолы нагрузки. Если смола остается красным во время теста метилового красного, то шаги 2.2 и 2.3 следует повторить. Желтый цвет, что указывает на отрицательный результат метилового красного, является предпочтительным;Однако, так как оставшиеся гидроксильные группы будет ограничено в следующем шаге, слегка положительный результат (легкие смолой оранжевого цвета) может быть приемлемым.
3. Снятие защиты первого Бис-пептида и одновременное смолы укупорки
- Добавить 1 мл DCM в реакционный сосуд затем добавьте 1 мл 33% бромистого водорода в уксусной кислоты по каплям в течение 30 секунд (восходящей происходит) и позволяет перемешивать в течение 15 минут. Слейте и промойте смолы с DCM (5 раз), а затем повторите еще раз.
- Вымойте смолы с DCM (5x), то DMF (5x). Нейтрализовать смолы промывкой в два раза с 5% объем / объем решение N, N-диизопропилэтиламин (DIPEA) в DMF затем смойте DCM (5x) и ДМФ (5 раз) еще раз. Выполните "метилового красного тест" и "хлоранила тест" обсуждается в разделе 10.1 и 10.2. Результат должен быть отрицательным для метилового красного и тест положительный тест хлоранила.
4. Муфта Бок / TBU-охраняемых функционализированных Бис-Амине кислота
- Вновь инертной атмосфере в смолу содержащие реакционного сосуда промывкой в три раза безводным DCM затем приложите перегородки и аргона линии. Очистить и вымыть сосуд, добавив 1-2 мл безводного DCM и дать движение в течение 30 секунд, а затем слив судна до линии аргона барботер начинает расти. Сделайте это по крайней мере еще раз.
- Приготовьте раствор 0,15 М функциональными бис-аминокислоты (3eq) и 245 мг 1-окси-7-azabenzotriazole (Хоат, 136,11 г / моль, 18eq) в 2 мл 2:1 DCM: DMF в пламени сухое испытание трубке в атмосфере аргона. Добавить 47 мкл диизопропилкарбодиимида (ДВС-синдром, 156,6 мл / моль, 3eq) и перемешивают в течение 90 минут.
- Добавить 35 мкл DIPEA (174,19 мл / моль, 2EQ) в 666 мкл безводного ДМФА в смолу и позволяет перемешивать в течение 5 минут.
- Передача предварительно активированного бис-аминокислоты решение реакционного сосуда с помощью шприца и позволит активизировать ночь.
- Слить в реакционную смесь и мыть дважды безводным DCM, находясь под аргона.
- Способствовать закрытию diketopiperazine, добавить 0,25 М раствора Хоат (136,11 г / моль, 10eq) и DIC (156,6 мл / моль, 10eq) в 4 мл 1:1 DCM: DMF и позволит активизировать в атмосфере аргона в течение 1 часа.
- Удалить перегородки и слейте реакционной смеси. Вымойте смолы с DCM (5x) и ДМФ (5 раз). При необходимости, выполнить "хлоранила тест" обсуждается в разделе 10.2.
5. Снятие защиты Вос / TBU-охраняемых функционализированных Бис-Аминокислоты
- Добавить 2 мл раствора кислоты trifluororacetic 95:5 (ТФК): triisopropylsilane (TIPS) в реакционный сосуд и дайте ему мешать в течение 1 часа. Слейте и промойте смолы в течение примерно 30 секунд и DCM (5 раз), а затем повторите еще раз.
- Вымойте смолы с DCM (5x), то DMF (5x). Нейтрализовать смолы промывкой в два раза с 5% объем / объем решение DIPEA в DMF затем промыть DCM (5x) и ДМФ (5 раз) еще раз. При необходимости, выполнить "хлоранила тест" обсуждается в разделе 10.2.
7. Функционализации Бис-пептида Prolidine End
- Prolidine конце вегетационного бис-пептиды могут быть ацилирована самостоятельно или совместно через diketopiperazine. Кроме того, этой цели можно не защищены, которые будут расщепляться последнего, при наличии свободных аминокислот. При необходимости, выполнить "хлоранила тест" обсуждается в разделе 10.2 для оценки эффективности связи.
8. Снятие защиты с Fmoc и ацилирования четвертичного Конец Бис-пептида
- 2 мл раствора 20% пиперидина в ДМФ и реакцию перемешивают в течение 20 минут. Слейте и промойте смолы с DMF (5 раз), а затем повторите еще раз.
- Вымойте смолы с DCM (5x), то DMF (5x).
- Подготовить 0,15 М раствора аминокислот (3eq) в 2 мл N-метилпирролидон (NMP) с 114 мг 2 - (7-аза-1Н-бензотриазол-1-ил) -1,1,3,3-tetramethyluronium гексафторфосфата (HATU, 380,2 г / моль, 3eq) и 104,5 мкл DIPEA (174,19 мл / моль, 6eq) и хорошо перемешать. Добавить в реакционном сосуде и позволяет перемешивать в течение 6 часов.
- Вымойте смолы с DCM (5x), то DMF (5x).
9. Удалить группу Бок из смолы Связанные аминокислот и Клив из смолы
- Добавить 2 мл 1:1 TFA: DCM решение реактора и позволяет перемешивать в течение 30 минут. Слейте и промойте смолы с DCM (5 раз), а затем повторите еще раз.
- Промойте и высушите смолы в течение 30 секунд с DCM (5 раз), то DMF (5 раз).
- Добавить 2 мл раствора 10% DIPEA в безводном ДМФА и позволит активизировать 24-48 часов.
- Соберите реакционной смеси в предварительно взвешенные круглодонную колбу. Трансфер 30 мкл этого раствора до 450 мкл ТГФ в LC-MS флакон и представить для анализа. Вымойте смолы с дополнительными порциями ДМФ и собирают в колбу с круглым дном, то удаления растворителя в вакууме.
10. Очистка Бис-пептида
- Растворите сырой бис-пептида в минимальном количестве диметилсульфоксида (100-250 мкл) и передачи в вставкой флакон высокоэффективной жидкостной хроматографии. Место вставки в автосамплером полу-prepitive ВЭЖХ системы (Hewlett Packard серии 1100), оснащенных Xterra Подготовка MS C18 5 мкм 7.8x150 колонке мм и 100 мкл цикл инъекций.
- Выполните несколько инъекций 50 мкл образца с использованием градиента программы 5-95% ацетонитрила в воде с 0,1% муравьиной кислоты в течение 30 минут, контролируя при 274 нм. Соберите продукт пика в предварительно взвешенные одноразовые центрифужные пробирки и заморозить сухой помощью лиофилизатор. С осторожностью следует принимать с первого запуска, как небольшой сдвиг в пиковое время удержания по сравнению с аналитическим LCMS обычно наблюдается.
11. Методы оценки
- Метиловый красный Испытание 7: Удалить ~ 1 мг сухой смолы через одноразовые пипетки и промыть в 4 мл реакционного сосуда. Добавить решение 20 мг метилового красного, 50 мкл N, N-диизопропилкарбодиимида (ОПК) и 5 мг 4-диметиламинопиридина (DMAP) в 500 мкл безводной DCM и позволяет перемешивать в течение 5-10 мин. Слейте и промойте смолы с DCM пока фильтрат становится бесцветным. Положительные указание гранул смолы остальные оранжевые или красные.
- Хлоранила TEST 12: Передача ~ 1 мг сухой смолы в небольшой флакон с помощью одноразовой пипетки. Добавить 3 капли и 0,8 мМ хлоранила в растворе ДМФА и 2% ацетальдегида в растворе ДМФА и оставьте при комнатной температуре в течение 5-10 минут. Положительные указание гранул смолы посинение / фиолетовый.
- АКТИВАЦИЯ TRAP TEST: активированного соединения в процессе синтеза можно оценить путем передачи небольшого количества (5-10 мкл) активированного решение жидкостной хроматографии-масс-спектрометрии (LC-MS) флакон, содержащий 50 мкл пирролидина. Смешать вручную в течение нескольких секунд (solutiна должна стать желтой), а затем разбавляют 450 мкл тетрагидрофурана (ТГФ) и представить на LC-MS анализа.
- АНАЛИТИЧЕСКАЯ LC-MS: конечный продукт и активированные промежуточные можно оценить, используя HP 1200 серии LC-MS системы, оснащенной воды Xterra MS C18 3,5 мкм 4,6 мм х 150 мм и колонки градиента система 5-95% ацетонитрила в воде с 0,1% муравьиной кислоты в течение 30 минут.
12. Представитель Результаты
Например, так сырой (рис. 4) и очищенного (рис. 5) LCMS следы предоставляются. Очищенная дает около 10%, как ожидается использование методов, описанных выше.

Рисунок 1. Схема экспериментальной установки для Твердофазный синтез.
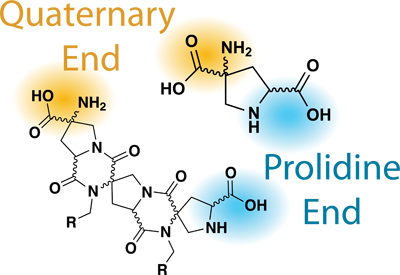
Рисунок 2.Соответствующие Номенклатура бис-аминокислоты / бис-пептиды.

Рисунок 3. В целом схема синтеза. Нажмите здесь, чтобы увеличить рисунок .

Рисунок 4а. ВЭЖХ следов сырого продукта при 274 нм.
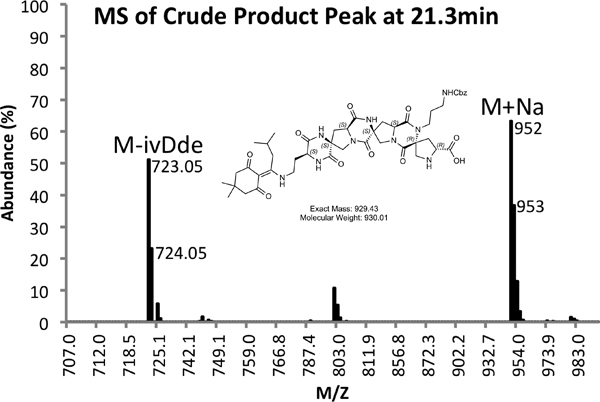
Рисунок 4б. MS спектр сырой пик продукта.
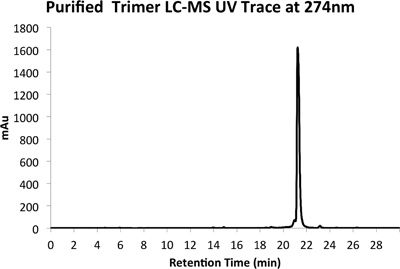
Рисунок 5а. ВЭЖХ След очищенного продукта при 274 нм.
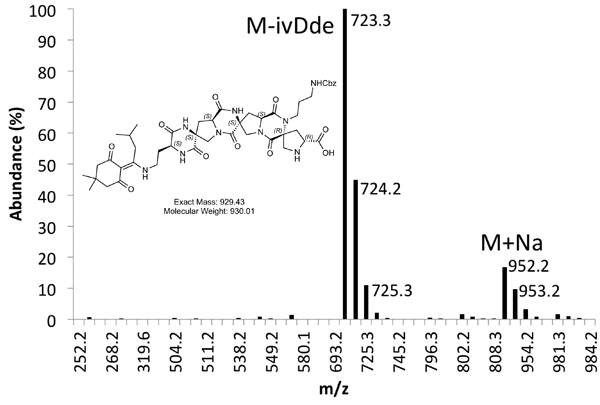
На рисунке 5б. MS спектр Очищенный изделит пик.
Обсуждение
Синтетический подход, представленный здесь представляет собой метод синтеза функционализированных бис-пептиды из бис-аминокислоты строительных блоков с использованием общих твердофазных методов синтеза пептидов. Мономер синтеза этих "Pro4« строительных блоков из транс-4-гидроксипролина 3 высокой масштабируемостью и был успешно завершен на сцену гидантоин на 600 ммоль (234 г), масштаб (не опубликовано). После мономеров в стороны, использование твердофазного методов обеспечивает более быстрый метод бис-синтеза пептидов, чем наши текущие решения фазы методология 4, устраняя необходимость в реакции работы окон и промежуточных очищения.
Основной проблемой в твердой фазе синтеза диагностики синтетических прогресса и решения проблем, поскольку ни промежуточные изолированы. Это привело к развитию многих колориметрических тестов в том числе для определения, если свободные амины (Kaiser испытаний 10) или свободного гидроксидаYLS (метиловый красный Испытание 7) выставлены на смолу. К сожалению, часто используется Kaiser Test 10 как правило, не применяется в нашей твердофазного синтеза в связи с почти исключительное использование вторичных аминов или аминов придает четвертичного углерода. Другие варианты оценки по смолы HMBA включает тест раскол помощью нуклеофила, таких как гидразин 11, количественные Fmoc расщепление контролируется UV / Vis 1,11 и захвата и анализа входящих активированного соединения.
Другой внимания вопросу твердофазного синтеза является повторяющийся характер синтетических шагов, необходимых оператору. Принимая это во внимание, авторы настоятельно рекомендуют использовать электронную таблицу или перечень при выполнении любой ручной твердофазного синтеза пептидов.
Сложно в использовании бис-пептиды для твердофазного синтеза по сравнению с обычными α-аминокислот включает в себя потенциал для более сложных соединений из-за стерических гинаdrance, необходимость по-смолы закрытия diketopiperazine, и одновременно deprotections (Boc / TBU; Cbz / TBU). Другим трудно заключается в достижении количественных освобождение от смолы с помощью этого "предохранитель" метод по сравнению с более традиционными средствами. С учетом этих факторов, вполне возможно, что дальнейшая оптимизация данного метода может быть достигнута и в настоящее время усилия предпринимаются в нашей группе, чтобы улучшить метод, представленный здесь.
Раскрытие информации
Нет конфликта интересов объявлены.
Благодарности
Авторы хотели бы поблагодарить д-ра З. Захари Браун и Дженнифер Alleva для начального развития этой серьезной техники синтеза и Мэтью Паркер FL за полезные обсуждения. Эта работа поддерживается сокращению военной угрозы агентства (DOD-DTRA) (HDTRA1-09-1-0009) и Хорст Witzel стипендий премии поддерживается Голова, Inc
Материалы
| Имя | Компания | Номер по каталогу | Комментарии |
| HMBA-Am смолы | NovaBiochem | 855018 | |
| MSNT | NovaBiochem | 851011 | |
| NMI | Sigma-Aldrich | 336092 | Токсичные, коррозионные |
| DCM | Sigma-Aldrich | D65100 | Канцерогенный |
| Безводный DCM | Acros | 34846 | Канцерогенный |
| 33% бромистого водорода в уксусной кислоте | Sigma-Aldrich | 248630 | Токсичные, Corrosive, дыма при открытии |
| DIPEA | Sigma-Aldrich | 387649 | Легковоспламеняющиеся, токсичные, коррозионные |
| DMF | Fisher Scientific | AC27960 | Горючих, токсичных газов |
| Безводный ДМФА | Acros | 34843 | Горючих, токсичных газов |
| Хоат | GenScript | C01568 | |
| DIC | Acros | BP590 | Легковоспламеняющиеся, токсичные, коррозионные |
| TFA | Sigma-Aldrich | T6508 | Токсичные, коррозионные |
| СОВЕТЫ | Acros | 21492 | Горючих, токсичных газов |
| Пиперидин | Sigma-Aldrich | 104094 | Легковоспламеняющиеся, токсичные, коррозионные |
| HATU | GenScript | C01566 | Токсичные |
| NMP | Acros | 36438 | Токсичный |
| DMAP | NovaBiochem | 851055 | Токсичный |
| Метиловый красный | Sigma-Aldrich | 250198 | |
| ТГФ | Sigma-Aldrich | 401757 | Легковоспламеняющиеся, токсичные, перекись Формирование |
| Пирролидина | Sigma-Aldrich | P73803 | Легковоспламеняющиеся, токсичные, коррозионные |
| Диметилсульфоксида | Рыбак | D1281 | |
| Реакция суда SPPS | Грейс | 211108 | |
| LCMS | Agilent | Серии 1200 | |
| Полу-Prep LC | Hewlett-Packard | 1100 Series | |
| Лиофилизатор | Labconco | 7934027 | |
| Rotovapor | Бюхи | R-210 серии | |
| Аргон | Airgas | AR PP300CT |
Ссылки
- Atherton, E., Sheppard, R. C. . Solid Phase Peptide Synthesis: A Practical Approach. , (1989).
- Brown, Z. Z., Alleva, J., Schafmeister, C. E. Solid-Phase Synthesis of Functionalized Bis-Peptides. Biopolymers. 96, 578-585 (2010).
- Schafmeister, C. E., Brown, Z. Z., Gupta, S. Shape-Programmable Macromolecules. Acc. Chem. Res. 41, 1387-1398 (2008).
- Brown, Z. Z., Schafmeister, C. E. Synthesis of Hexa- and Pentasubstituted Diketopiperazines from Sterically Hindered Amino Acids. Org. Let. 12, 1436-1439 (2010).
- Nielson, J., Lyngso, L. O. Combinatorial Solid-Phase Synthesis of Balanol Analogues. Tet. Lett. 37, 8439-8442 (1996).
- Blankemeyer-Menge, B., Nimtz, M., Frank, R. An Efficient Method for Anchoring Fmoc-Amino Acids to Hydroxyl-Functionalized Solid Supports. Tet. Lett. 31, 1701-1704 (1990).
- Komba, S., Sasaki, S., Machida, S. A New Colorimetric Test for Detection of Hydroxyl Groups in Solid-Phase Synthesis. Tet. Lett. 48, 2075-2078 (2007).
- Demner, O., Dijkgraaf, I., Schottelius, M., Wester, H. J., Kessler, H. Introduction of Functional Groups into Peptides via N-Alkylation. Org. Lett. 10, 2015-2018 (2008).
- Plas, S. E. V. a. n. d. e. r., Van Hoeck, E., Lynen, F., Sandra, P., Madder, A. Toward a New SPE Material for EDCs: Fully Automated Synthesis of a Library of Tripodal Receptors Followed by Fast Screening by Affinity LC. Eur. J. Org. Chem. 11, 1796-1805 (2009).
- Kaiser, E., Colescot, R. L., Bossinger, C. D., Cook, P. I. Color Test for Detection of Free Terminal Amino Groups in Solid-Phase Synthesis of Peptides. Anal. Biochem. 34, 595-598 (1970).
- Chan, W. C., White, P. D. . Fmoc Solid Phase Peptide Synthesis: A Practical Approach. , (2000).
- Vojkovsky, T. Detection of Secondary Amines on Solid-Phase. Peptide Research. 71, 236-237 (1995).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены