Method Article
Síntesis en fase sólida de un péptido funcionalizado Bis-El uso de "Cierre de seguridad" Metodología
En este artículo
Resumen
El eficiente síntesis en fase sólida de péptidos de un funcionalizado bis-péptido trímero utilizando un "cierre de seguridad" procedimiento de escisión de la resina HMBA se describe.
Resumen
En 1962, RB Merrifield publicado el primer procedimiento utilizando síntesis en fase sólida de péptidos como una nueva ruta para sintetizar péptidos eficientemente. Esta técnica demostró rápidamente una ventaja respecto a su antecesor en fase de solución en el tiempo y la mano de obra. Las mejoras sobre la naturaleza del soporte sólido, los grupos protectores empleados y los métodos de acoplamiento utilizados en los últimos cinco años sólo han aumentado la utilidad de sistema original de Merrifield. Hoy en día, el uso de una protección Boc-basado y la base / nucleófilo estrategia de resina de escindible o Fmoc basada en la protección y la estrategia de resina ácida escindible, por primera vez por RC Sheppard, son los más utilizados para la síntesis de péptidos 1.
Inspirados en sólida de Merrifield estrategia apoyado, hemos desarrollado un Boc / terc-butilo en fase sólida estrategia de síntesis para el montaje de funcionalizados bis-péptidos 2, que se describe en este documento. El uso de síntesis en fase sólida en comparación to en fase de solución metodología no es sólo ventajoso en tanto tiempo y trabajo como se describe por Merrifield 1, sino que también permite una mayor facilidad en la síntesis de bis-péptido bibliotecas. La síntesis que se demuestra aquí incorpora una etapa de escisión final que utiliza una de dos pasos "cierre de seguridad" mecanismo para liberar el funcionalizado bis-péptido de la resina por la formación de dicetopiperazina.
Bis-péptidos son rígidos, espiro-escalera oligómeros de bis-aminoácidos que son capaces de posicionar la funcionalidad de una manera predecible y diseñable, controlada por el tipo y la estereoquímica de las unidades monoméricas y la conectividad entre cada monómero. Cada ácido bis-amino es un estereoquímicamente puros, cíclico andamio que contiene dos aminoácidos (un ácido carboxílico con una α-amina) 3,4. Nuestro laboratorio está investigando el potencial de los péptidos funcionales bis-a través de una amplia variedad de campos incluyendo la catálisis, interacciones proteína-proteína y nanomaterials.
Protocolo
1. El programa de instalación
- La reacción puesta a punto para la síntesis en fase sólida es un cartucho de filtro de polipropileno o reactor de vidrio que está conectado a través de tubos de polipropileno a un matraz cerrado filtrado bajo vacío como se muestra en la Figura 1. La reacción se puede mezclar por una barra de agitación magnética o haciendo burbujear nitrógeno a través del reactor.
- Un colector de gas conectado a un cilindro de argón equipado con un tubo de secado y borboteador de aceite también se recomienda ya que permite al recipiente de reacción para ser contenida en una atmósfera inerte y permite la eliminación de los reactivos de recipientes herméticos.
- Todas las operaciones se llevan a cabo en una campana de humos y equipo de protección personal (anteojos de seguridad, bata de laboratorio y guantes de nitrilo) se requiere.
2. Cargando Primero Bis-péptido en la resina
- Pesar 114 mg de HMBA-AM Resina (0,88 mmol / g de carga, 100 mmol) en 8 ml recipiente de reacción y añadir la barra de agitación magnética. Tapar la parte superior de THe vasija con un tabique de caucho y el tubo de purga con argón durante al menos 5 minutos.
- Mientras tanto, pesan 117,3 mg del compuesto 1 de la Figura 3 (586,63 g / mol, 2eq) y 59,2 mg de 1 - (mesitileno-2-sulfonil)-3-nitro-1 ,2,4-triazol (MSNT, 296,0 g / mol, 2eq) en un tubo de centrífuga de 15 ml desechable y disolver en 2 ml de diclorometano anhidro (DCM). Añadir 24 l de 1-metilimidazol (NMI, 80,81 ml / mol, 3eq) a la solución y se mezcla hasta que esté completamente disuelto.
- Transferir la solución activada al recipiente de reacción mediante una jeringa y permita que se agita bajo argón durante la noche (aproximadamente 10 horas).
- Quitar el tabique y drenar la mezcla de reacción. Lavar la resina con DCM (5x) y dimetilformamida (DMF) (5x). Lleve a cabo el "metil rojo de prueba" que se describe en la sección 10.1 para evaluar el grado de carga de la resina. Si la resina permanece en rojo durante la prueba de rojo de metilo a continuación los pasos 2.2 y 2.3 se debe repetir. Un color amarillo, indicativo de un grupo metilo negativo en la prueba de color rojo, se prefiere;Sin embargo, puesto que ningún grupo hidroxilo restantes se limitará en la siguiente etapa, un resultado ligeramente positivo (color de la luz resina naranja) puede ser aceptable.
3. La desprotección de primera resina Bis-péptido y simultánea de límite
- Añadir 1 ml de DCM a la vasija de reacción a continuación, añadir 1 ml 33% gota a gota bromuro de hidrógeno en ácido acético durante 30 segundos (burbujeo se produce) y permitir a agitar durante 15 minutos. Escurrir y lavar la resina con DCM (5x) y luego repetir procesar una vez más.
- Lavar la resina con DCM (5x) y luego DMF (5x). Neutralizar la resina por lavado dos veces con un 5% v / v de solución de N, N-diisopropiletilamina (DIPEA) en DMF a continuación, se lava con DCM (5x) y DMF (5x) de nuevo. Realizar la "prueba de rojo de metilo" y "prueba de cloranil" discutido en las secciones 10.1 y 10.2. Los resultados deben ser negativos para el rojo de metilo prueba y positivo para la prueba de cloranil.
4. Acoplamiento Boc / tBu-Protegido funcionalizados Bis-Amisin ácido
- Reintroducir una atmósfera inerte a la resina que contiene recipiente de reacción por lavado tres veces con DCM anhidro después coloque un tabique y la línea de argón. Purgar y lavar el recipiente mediante la adición de 1-2 ml de DCM anhidro y dejar que se agita durante 30 segundos y luego vaciar el recipiente hasta que el argón línea de burbujeo empieza a subir. ¿Es esto por lo menos una vez más.
- Preparar una solución de 0,15 M funcionalizado bis-aminoácido (3eq) y 245 mg de 1-hidroxi-7-azabenzotriazol (HOAt, 136,11 g / mol, 18eq) en 2 mL de 2:1 DCM: DMF en una prueba de secado a la llama tubo bajo atmósfera de argón. Añadir 47 l de diisopropilcarbodiimida (DIC, 156,6 ml / mol, 3eq) y se agita durante 90 minutos.
- Añadir 35 l DIPEA (174,19 ml / mol, 2eq) en DMF anhidra 666 l de resina y permita que se agita durante 5 minutos.
- Transferir la pre-activado bis-amino solución de ácido al recipiente de reacción mediante una jeringa y permita que se agita durante la noche.
- Escurrir la mezcla de reacción y se lava dos veces con DCM anhidro mientras que bajo argón.
- Para promover el cierre de la dicetopiperazina, añadir una solución 0,25 M de HOAt (136,11 g / mol, 10eq) y DIC (156,6 ml / mol, 10eq) en un ml 4 de 1:1 DCM: DMF y permitir a agitar en atmósfera de argón durante 1 hora.
- Quitar el tabique y drenar la mezcla de reacción. Lavar la resina con DCM (5x) y DMF (5x). Si lo desea, realice la "prueba de cloranil" discutido en la sección 10.2.
5. La desprotección de Boc / tBu-Protegido funcionalizados Bis-aminoácido
- Añadir 2 ml de una solución de ácido 95:5 trifluororacetic (TFA): triisopropilsilano (TIPS) al recipiente de reacción y permitir que se agita durante 1 hora. Escurrir y lavar la resina durante unos 30 segundos con DCM (5x) y luego repita el proceso una vez más.
- Lavar la resina con DCM (5x) y luego DMF (5x). Neutralizar la resina por lavado dos veces con un 5% v / v de solución de DIPEA en DMF lavar DCM (5x) y DMF (5x) de nuevo. Si lo desea, realice la "prueba de cloranil" discutido en la sección 10.2.
7. El fin de funcionalización Prolidine Bis-péptido
- El extremo prolidine de la creciente bis-péptido puede ser acilado independientemente o conjuntamente a través de una dicetopiperazina. Además, este fin se puede dejar protegido, que se escinde último, proporcionando el aminoácido libre. Si lo desea, realice la "prueba de cloranil" discutido en la sección 10.2 para evaluar la eficiencia de acoplamiento.
8. La desprotección de Fmoc y acilación de la finalización del Cuaternario de la bis-Péptido
- Una solución 2 ml de 20% de piperidina en DMF se añade y la mezcla de reacción se durante 20 minutos. Escurrir y lavar la resina con DMF (5x) y luego repita el proceso una vez más.
- Lavar la resina con DCM (5x) y luego DMF (5x).
- Preparar una solución 0,15 M de ácido amino (3eq) en 2 ml de N-metilpirrolidona (NMP) con 114 mg de 2 - (7-aza-1H-benzotriazol-1-il) -1,1,3,3-tetrametiluronio hexafluorofosfato (HATU, 380,2 g / mol, 3eq) y 104,5 l DIPEA (174,19 ml / mol, 6EQ) y mezclar bien. Añadir al recipiente de reacción y permitir en agitación durante 6 horas.
- Lavar la resina con DCM (5x) y luego DMF (5x).
9. Eliminar el grupo Boc desde unido a la resina de aminoácidos y se unirá a partir de Resina
- Añadir 2 ml de una TFA 1:1: solución de DCM al recipiente de reacción y permitir en agitación durante 30 minutos. Escurrir y lavar la resina con DCM (5x) y luego repetir procesar una vez más.
- Lavar y escurrir la resina durante 30 segundos con DCM (5x) y luego DMF (5x).
- Añadir 2 ml de una solución de 10% DIPEA en DMF anhidro y permitir a agitar 24-48 horas.
- Recoger mezcla de reacción en previamente pesado matraz de fondo redondo. Transferir 30 l de esta solución a 450 l de THF en un frasco de LC-MS y presentar para su análisis. Lavar la resina con alícuotas adicionales de DMF y se recogen en el matraz de fondo redondo entonces eliminar el disolvente a vacío.
10. Purificación de Bis-Péptido
- Disolver crudo bis-péptido en una cantidad mínima de dimetilsulfóxido (100-250 l) y la transferencia en inserto vial de HPLC. Coloque el inserto en el muestreador automático de semi-prepitive sistema de HPLC (Hewlett Packard 1100 Series) equipado con un XTerra Prep MS C18 columna de 5 m mm 7.8x150 y un circuito de inyección de 100 l.
- Realizar múltiples inyecciones de 50 l de la muestra utilizando un programa de gradiente de 5-95% de acetonitrilo en agua con 0,1% de ácido fórmico durante 30 minutos mientras se monitoriza a 274 nm. Recoger el pico del producto en un tubo de centrífuga previamente pesado disponible y congelar en seco utilizando un liofilizador. Se debe tener precaución con la carrera por primera vez como un ligero cambio en el tiempo de retención de pico en comparación con el LCMS de análisis se observa típicamente.
11. Métodos de evaluación
- Rojo de metilo PRUEBA 7: Retire aproximadamente 1 mg de la resina seca a través de una pipeta desechable y enjuague en 4 ml recipiente de reacción. Añadir una solución de 20 mg de rojo de metilo, 50 N l, N'-diisopropilcarbodiimida (DIC), y 5 mg de 4-dimetilaminopiridina (DMAP) en 500 l DCM anhidro y permita que se agita durante 5-10 minutos. Escurrir y lavar la resina con DCM hasta que el filtrado se vuelve incolora. Indicación positiva es las perlas de resina restantes naranja o rojo.
- PRUEBA cloranil 12: Transferencia de ~ 1 mg de resina seca en un frasco pequeño a través de una pipeta desechable. Añadir 3 gotas de tanto un cloranilo 0,8 mM en solución de DMF y 2% de acetaldehído en solución de DMF y deje reposar a temperatura ambiente durante 5-10 minutos. Indicación positiva es las perlas de resina de inflexión azul / morado.
- Test de activación de TRAP: compuestos activados durante la síntesis se puede evaluar mediante la transferencia de una pequeña cantidad (l 5-10) de la solución activada a una cromatografía líquida-espectrometría de masas (LC-MS) frasco que contiene 50 l de pirrolidina. Mezclar con la mano durante unos segundos (solucidebe convertirse en amarillo) y luego se diluye con 450 l de tetrahidrofurano (THF) y someter a análisis de LC-MS.
- ANALÍTICA LC-MS: El producto final y los intermedios activados se puede evaluar utilizando una HP 1200 serie LC-MS sistema equipado con un Waters Xterra MS C18 3,5 m 4,6 mm x 150 mm de columna y un sistema de gradiente de 5-95% de acetonitrilo en agua con 0,1% de ácido fórmico durante 30 minutos.
12. Los resultados representativos
Un ejemplo de ambos crudo (Figura 4) y purificado (Figura 5) trazas LCMS se proporcionan. Purificadas de los rendimientos de aproximadamente el 10% se espera que mediante los métodos descritos anteriormente.

Figura 1. Diagrama del montaje experimental para la síntesis en fase sólida.
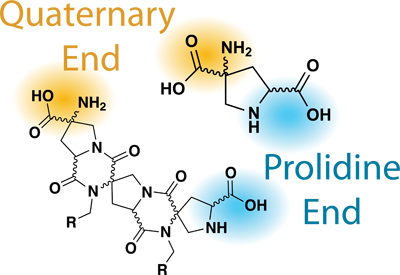
Figura 2.Nomenclatura pertinente de Bis-Aminoácidos Péptidos / Bis.

Figura 3. Esquema sintético general. Haga clic aquí para ver más grande la figura .

Figura 4a. Traza de HPLC del producto crudo a 274 nm.
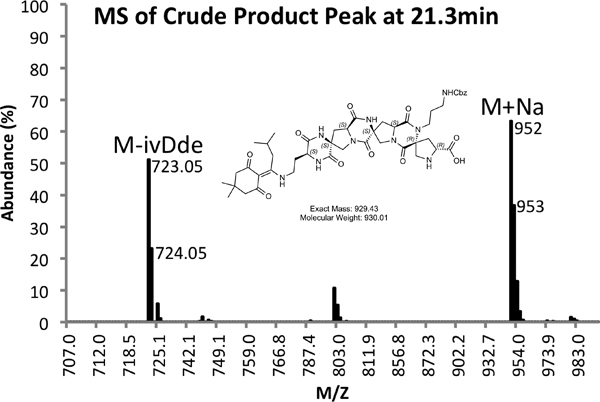
Figura 4b. Espectro MS del pico de producto bruto.
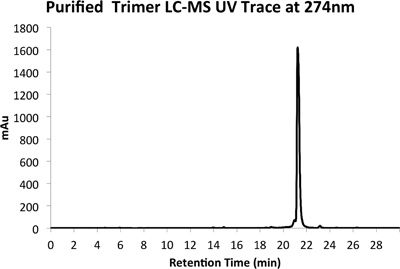
Figura 5a. HPLC de seguimiento de producto purificado a 274 nm.
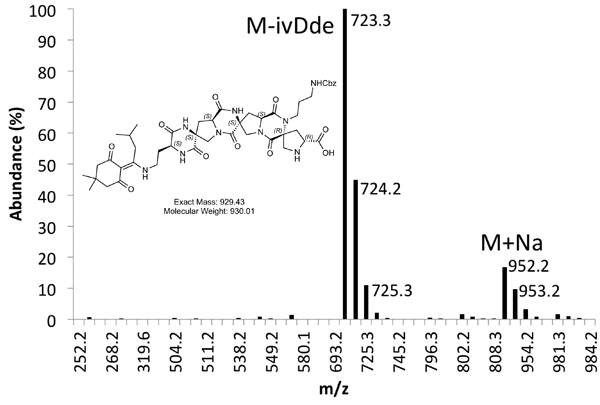
Figura 5b. MS Espectro de Produc purificadat pico.
Discusión
El enfoque sintético presenta en este documento proporciona un método para la síntesis de péptidos funcionalizados bis-bis-a partir de unidades de aminoácidos utilizando comunes en fase sólida técnicas de síntesis de péptidos. La síntesis de monómeros de estos bloques de construcción "Pro4" de trans-4-hidroxiprolina 3 es altamente escalable y se ha completado con éxito a la etapa de hidantoína en un 600 mmol (234 g) de escala (no publicado). Una vez que los monómeros están en la mano, el uso de técnicas en fase sólida proporciona un método más rápido de bis-péptido de síntesis que nuestro actual en fase de solución metodología 4, eliminando la necesidad de reacción de trabajo en marcha y purificaciones intermedias.
El principal desafío en la síntesis en fase sólida es el diagnóstico de los avances sintético y la resolución de problemas ya que no hay intermediarios están aislados. Esto ha llevado al desarrollo de muchos ensayos colorimétricos incluyendo aquellos para identificar si aminas libres (Kaiser Prueba 10) o Hydrox libreHMJM (metil rojo de prueba 7) se exponen en la resina. Desafortunadamente, el uso común de prueba Kaiser 10 no es aplicable en general en nuestra síntesis en fase sólida, debido al uso casi exclusivo de aminas secundarias o aminas unidas a un carbono cuaternario. Otras opciones para la evaluación en resina HMBA incluyen divisiones de prueba usando un nucleófilo tal como hidrazina 11, escisión cuantitativa Fmoc seguimiento por UV / Vis 1,11, y la captura y el análisis de entrantes compuestos activados.
Otra cuestión vecinos en síntesis en fase sólida es la naturaleza repetitiva de etapas sintéticas requeridos por el operador. Con esto en mente, los autores recomiendan el uso de una hoja de cálculo o lista de control al realizar cualquier manual de síntesis en fase sólida de péptidos.
La dificultad en el uso de bis-péptidos para síntesis en fase sólida en comparación con comunes α-aminoácidos incluye la posibilidad de acoplamientos más difícil debido a estérico HinDrance, la necesidad de cierres de dicetopiperazina en resina, y desprotecciones simultáneas (Boc / tBu; Cbz / tBu). Otra dificultad radica en conseguir la liberación cuantitativa de la resina usando este "cierre de seguridad" método en comparación con medios más convencionales. Con estos factores en mente, es muy posible que una mayor optimización de este método se puede lograr y los esfuerzos actuales están llevando a cabo en nuestro grupo para mejorar el método que aquí se presenta.
Divulgaciones
No hay conflictos de interés declarado.
Agradecimientos
Los autores desean agradecer al Dr. Zachary Z. Brown y Jennifer Alleva para el desarrollo inicial de esta técnica de síntesis en fase sólida y Matthew Parker FL útil para los debates. Este trabajo es apoyado por la Agencia de Defensa de Reducción de Amenazas (DOD-DTRA) (HDTRA1-09-1-0009) y el Premio Horst Witzel Beca financiada por Cephalon, Inc.
Materiales
| Nombre | Empresa | Número de catálogo | Comentarios |
| HMBA-Am Resina | Novabiochem | 855018 | |
| MSNT | Novabiochem | 851011 | |
| NMI | Sigma-Aldrich | 336092 | Tóxico, Corrosivo |
| DCM | Sigma-Aldrich | D65100 | Cancerígeno |
| DCM anhidro | Acros | 34846 | Cancerígeno |
| 33% de bromuro de hidrógeno en ácido acético | Sigma-Aldrich | 248630 | Corr. tóxico,osive, humos cuando está abierto |
| DIPEA | Sigma-Aldrich | 387649 | Inflamable, tóxico, corrosivo |
| DMF | Fisher Scientific | AC27960 | Inflamable, tóxico |
| DMF anhidra | Acros | 34843 | Inflamable, tóxico |
| HOAt | GenScript | C01568 | |
| DIC | Acros | BP590 | Inflamable, tóxico, corrosivo |
| TFA | Sigma-Aldrich | T6508 | Tóxico, Corrosivo |
| CONSEJOS | Acros | 21492 | Inflamable, tóxico |
| Piperidina | Sigma-Aldrich | 104094 | Inflamable, tóxico, corrosivo |
| HATU | GenScript | C01566 | Toxic |
| NMP | Acros | 36438 | Tóxico |
| DMAP | Novabiochem | 851055 | Tóxico |
| Rojo de metilo | Sigma-Aldrich | 250198 | |
| THF | Sigma-Aldrich | 401757 | Inflamable, tóxico peróxido, Formación |
| Pirrolidina | Sigma-Aldrich | P73803 | Inflamable, tóxico, corrosivo |
| Dimetilsulfóxido | Pescador | D1281 | |
| SPPS Los reactores | Gracia | 211108 | |
| LCMS | Agilent | Serie 1200 | |
| Semi-Prep LC | Hewlett Packard | Serie 1100 | |
| Liofilizador | Labconco | 7934027 | |
| Rotavapor | Buchi | R-210 Series | |
| Argón | Airgas | AR PP300CT |
Referencias
- Atherton, E., Sheppard, R. C. Solid Phase Peptide Synthesis: A Practical Approach. , Oxford University Press. (1989).
- Brown, Z. Z., Alleva, J., Schafmeister, C. E. Solid-Phase Synthesis of Functionalized Bis-Peptides. Biopolymers. 96, 578-585 (2010).
- Schafmeister, C. E., Brown, Z. Z., Gupta, S. Shape-Programmable Macromolecules. Acc. Chem. Res. 41, 1387-1398 (2008).
- Brown, Z. Z., Schafmeister, C. E. Synthesis of Hexa- and Pentasubstituted Diketopiperazines from Sterically Hindered Amino Acids. Org. Let. 12, 1436-1439 (2010).
- Nielson, J., Lyngso, L. O. Combinatorial Solid-Phase Synthesis of Balanol Analogues. Tet. Lett. 37, 8439-8442 (1996).
- Blankemeyer-Menge, B., Nimtz, M., Frank, R. An Efficient Method for Anchoring Fmoc-Amino Acids to Hydroxyl-Functionalized Solid Supports. Tet. Lett. 31, 1701-1704 (1990).
- Komba, S., Sasaki, S., Machida, S. A New Colorimetric Test for Detection of Hydroxyl Groups in Solid-Phase Synthesis. Tet. Lett. 48, 2075-2078 (2007).
- Demner, O., Dijkgraaf, I., Schottelius, M., Wester, H. J., Kessler, H. Introduction of Functional Groups into Peptides via N-Alkylation. Org. Lett. 10, 2015-2018 (2008).
- Plas, S. E. V. ander, Van Hoeck, E., Lynen, F., Sandra, P., Madder, A. Toward a New SPE Material for EDCs: Fully Automated Synthesis of a Library of Tripodal Receptors Followed by Fast Screening by Affinity LC. Eur. J. Org. Chem. 11, 1796-1805 (2009).
- Kaiser, E., Colescot, R. L., Bossinger, C. D., Cook, P. I. Color Test for Detection of Free Terminal Amino Groups in Solid-Phase Synthesis of Peptides. Anal. Biochem. 34, 595-598 (1970).
- Chan, W. C., White, P. D. Fmoc Solid Phase Peptide Synthesis: A Practical Approach. , Oxford University Press. (2000).
- Vojkovsky, T. Detection of Secondary Amines on Solid-Phase. Peptide Research. 71, 236-237 (1995).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados