Medições eletroquímicas de catalisadores suportados usando um potenciostato/galvanostato
Visão Geral
Fonte: Laboratório do Dr. Yuriy Román — Massachusetts Institute of Technology
Um potencialiostat/galvanostat (muitas vezes referido como simplesmente um potencialiostat) é um instrumento que mede a corrente em um potencial aplicado (operação potencializatática) ou mede potencialmente em uma corrente aplicada (operação galvanostática)(Figura 1). É o instrumento mais utilizado na caracterização eletroquímica de materiais de ânodo e cátodo para células de combustível, eletrólitos, baterias e supercapacitores.
Convencionalmente, esses materiais de ânodo e cátodo são interfaceados com um potencialiostat através de uma célula eletroquímica de três eletrodos. Os condutores de eletrodo do potencialiostat são conectados ao eletrodo de referência, ao eletrodo de contador (muitas vezes chamado de eletrodo auxiliar) e ao eletrodo de trabalho (que contém o material de teste de interesse). A célula eletroquímica é então preenchida com uma solução de eletrólito de alta resistência iônica, como uma solução ácida, alcalina ou salgada. A mídia para esta solução de alta resistência iônica é tipicamente aquosa; no entanto, para aplicações que exigem janelas potenciais celulares de maior funcionamento, como baterias e supercapacitores, a mídia não aquosa é frequentemente usada. A mídia celular é desgaseada com um gás inerte (para evitar reações laterais indesejadas) ou com um gás de teste (se a reação de teste envolve um gás em um dos eletrodos).
Alternativamente, uma ponte de sal ou membrana é empregada para manter contato iônico se as duas metades das células devem ser medidas em diferentes eletrólitos. Em eletrocatálise heterogênea, este tipo de célula "dois compartimentos" é frequentemente usada se a molécula de teste no eletrodo de trabalho também estiver reaativa na contraeledição. Isso acontece frequentemente, pois a contraeletrídua tipicamente empregada é a platina, que é um catalisador altamente ativo para muitas reações. Aqui, serão utilizadas células de compartimento único, onde os três eletrodos estão na mesma mídia.
Este vídeo explicará o processo de polimento de um eletrodo funcionando, preparando uma tinta catalisador, montando a tinta catalisador no eletrodo de trabalho, preparando a célula eletroquímica e, em seguida, realizando medições eletroquímicas. As medidas realizadas incluem: voltammemetria cíclica (CV), voltametria linear de varredura (LSV), cronootometria (CP) e cronoamperometria (AC).
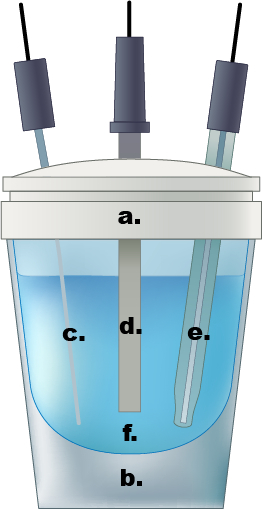
Figura 1. Um exemplo de uma única célula eletroquímica compartimental. a.) Teflon cap, b.) célula de vidro, c.) Eletrodo do contador de fios pt, d.) eletrodo de trabalho, e.) Eletrodo de referência Ag/AgCl, f.) Solução de eletrólito de ácido sulfúrico aquoso de 0,5 M.
Princípios
O potencialiostat pode ser usado para aplicar um potencial anodódico ou catódico constante ao eletrodo de trabalho e medir a corrente anocólica ou catódica resultante (cronoamperometria) ou o potencialiotato pode ser operado galvanostaticamente através de um loop de controle de feedback e aplicar uma corrente anodaídica ou catódica constante com o potencial medido variando com o tempo para manter esta corrente aplicada (cronoototricometria). Alternativamente, o espaço potencial pode ser explorado com o tempo usando voltametria cíclica ou voltammemetria de varredura linear para medir potenciais anoríficos e catódicos versus uma taxa de varredura potencial aplicada (a derivada do potencial em relação ao tempo).
Em todas essas técnicas, mesmo durante a operação galvanostática, o potencialiostat controla o potencial aplicado e mede o fluxo de elétrons de (to) o eletrodo de trabalho para (a partir) do eletrodo de contador quando o eletrodo de trabalho está agindo como o ânodo (cátodo). O potencial aplicado é referenciado contra o eletrodo de referência, que contém um sistema redox (como um eletrodo de cloreto de prata ou eletrodo de calomel saturado) com um potencial conhecido e estável que é interfaceado com a solução eletrólito através de um frit poroso. Durante a operação normal, o potencialiostat desenha uma corrente insignificante, mas não zero, através do eletrodo de referência para que um potencial preciso possa ser aplicado ao eletrodo de trabalho. Enquanto o potencialiostat mede o fluxo de elétrons para ou de uma reação meia para a próxima, a solução eletrólito completa o circuito impedindo o acúmulo de carga no ânodo ou no cátodo.
Procedimento
1. Preparação de tinta catalisador e eletrodos de trabalho
Precauções de segurança: Os metais suportados em preto carbono devem ser manuseados em um capô de fumaça ou em um compartimento de equilíbrio até que esteja em forma de suspensão, pois estes pós são riscos de inalação.
- Usando um equilíbrio fechado, pese de 5 a 10 mg de catalisador preto de metal/carbono e adicione a um frasco de vidro com uma tampa.
- Usando uma micropipette, dilua o catalisador com água de tal forma que a concentração final seja de 7,5 mg de catalisador por mL de água.
- Enquanto sonicante, 100 μL de solução Nafion 117 por mL de água é adicionado à suspensão.
- A tinta deve ser sônica por pelo menos 10 minutos para garantir a dispersão uniforme e a mistura completa do suporte preto carbono com o agente de ligação.
- Enquanto a tinta é sônica, um eletrodo de disco de carbono de 3 mm deve ser limpo e polido esfregando-o em um movimento circular giratório em uma almofada de alumina macia coberta com solução de alumina de 0,05 μm. Em seguida, deve ser lavado copiosamente com água para remover a alumina.
- Em seguida, 7 μL de tinta é pingado em um eletrodo de disco de carbono polido, verticalmente orientado 3 mm. O eletrodo de trabalho é então seco a 80 °C por 1 h se o catalisador estiver estável no ar ou evaporado sob um vácuo fraco por 30 minutos se o catalisador estiver sensível ao ar.
2. Preparação de células eletroquímicas
Precauções de segurança: Luvas, casaco de labcoat e óculos de segurança devem ser sempre usados, mas é especialmente primordial para trabalhar com a solução de ácido sulfúrico. Se alguma gota de solução derramar sobre os pulsos, deve ser lavada com água e sabão por 15 minutos. Para derramamentos graves, a remoção de roupas contaminadas e o uso de lavagem ocular ou chuveiros devem ser utilizados por 15 minutos seguidos de consulta médica. Os cabos elétricos não devem ser tocados uma vez colocados na célula eletroquímica.
- Uma célula de vidro é preenchida com 10 mL de 0,5 M H2SO4 e desgaseada por pelo menos 30 min com um fluxo de nitrogênio de alta pureza
- As tampas de Teflon das células eletroquímicas têm 3 portas para o eletrodo de trabalho, eletrodo de contador e eletrodo de referência
- O eletrodo de referência Ag/AgCl é removido de sua solução de 1 M KCl, enxaguado completamente com água DI e, em seguida, colocado na célula.
- O eletrodo do contador de fio de platina platinizado é lavado completamente com água DI e, em seguida, colocado na célula.
- O eletrodo de trabalho seco é enxaguado com água DI e depois colocado na célula.
- O potencialiostat está ligado.
- O chumbo eletrodo branco é conectado primeiro e conectado ao eletrodo de referência.
- O chumbo eletrodo vermelho é então conectado ao eletrodo do contador de fios Pt.
- O chumbo eletrodo verde é então conectado ao eletrodo de metal/carbono preto funcionando.
- Um pequeno fluxo de expurgo N2 é deixado continuamente borbulhando no eletrólito.
- Certifique-se de que nenhum cabo está tocando e que não há contato elétrico direto entre os 3 eletrodos que não sejam os 0,5 M H2SO4 eletrólitos.
3. Análise Eletroquímica
- Depois de ligar o potencialiostat, realize pelo menos 20 ciclos de condicionamento entre 0 e 0,4 V vs. RHE a 50 mV/s usando CV. Isso é realizado escolhendo cv como técnica e entrando nos limites potenciais superiores e inferiores, bem como na taxa de digitalização.
- A Voltametria de Varredura Linear (LSV) pode então ser realizada escolhendo o LSV como uma técnica e especificando um potencial inicial, um potencial final e uma taxa de digitalização. A taxa de varredura para LSV é tipicamente muito menor do que cv, geralmente 1 - 2 mV/s de modo que as correntes capacitivas se tornam muito menores do que as correntes decorrentes de reações de superfície faradaicas
- A cronoamperometria (CA) é realizada escolhendo CA ou "curva amperométrica i-t" como técnica e especificando o potencial fixo, bem como o tempo que o instrumento deve manter o eletrodo de trabalho como esse potencial fixo.
- A cronototricometria (CP) é realizada escolhendo CP como técnica. O CP pode ser realizado em uma série de etapas atuais onde uma corrente é especificada por um determinado período de tempo seguido por uma nova corrente por um período de tempo especificado. Essas correntes aplicadas podem abranger correntes anoódicas e catódicas dentro da mesma medição cp.
- Quando a análise eletroquímica estiver concluída, desligue o potencialiostat.
- Desconecte os cabos de eletrodos e armazene-os em um lugar seco longe de quaisquer líquidos para evitar corrosão.
- Remova o eletrodo de referência e enxágue com quantidades abundantes de água DI. Em seguida, devolva o eletrodo de referência diretamente à sua solução de armazenamento KCl de 1 M. A ponta deste eletrodo nunca deve ser permitida a ficar seca.
- Remova o eletrodo do contador de fios Pt e enxágue bem com água DI
- Remova o eletrodo de trabalho e enxágue bem com água DI e, em seguida, use um Kimwipe com acetona para remover facilmente a tinta catalisador seca da superfície do eletrodo em funcionamento. Recomenda-se polir eletrodos imediatamente após o uso.
- Desligue o expurgo N2.
- Esvazie o eletrólito usado em um recipiente de resíduos ácidos. Enxágüe a célula de vidro e a tampa de Teflon com quantidades abundantes de água DI.
Resultados
Este procedimento resultará em números contendo parcelas de corrente medida versus potencial para cada uma das quatro técnicas. Por convenção para CV e LSV, as parcelas também serão superadas como potencial de corrente medida, apesar da realidade de que são técnicas transitórias que medem a corrente versus a derivada temporal do potencial.
Aplicação e Resumo
CV, LSV, CP e CA são técnicas indispensáveis para determinar a eficácia de novos materiais eletrodos para células de combustível, eletrólitos, baterias e supercapacitores, bem como para o desenvolvimento de campos como a oxidação parcial seletiva ou redução de produtos químicos de commodities. Esses métodos permitem determinar superpotenciais de reações em diferentes materiais eletrodos em comparação com seus potenciais de equilíbrio termodinâmico. Esses métodos também permitem determinar a capacitância volumétrica ou gravimétrica dos supercapacitores. Da mesma forma, as taxas de carregamento/descarga de eletrodos de bateria ou supercapacitores podem ser determinadas com essas técnicas. Essas técnicas também permitem determinar a caracterização da estabilidade eletroquímica dos materiais. Além dessas técnicas básicas, técnicas mais avançadas incluem a combinação de técnicas potencialiométricas com métodos in-situ, como IR e espectrometria de massa.
Pular para...
Vídeos desta coleção:

Now Playing
Medições eletroquímicas de catalisadores suportados usando um potenciostato/galvanostato
Analytical Chemistry
51.3K Visualizações

Preparação da Amostra para Caracterização Analítica
Analytical Chemistry
84.2K Visualizações

Normas Internas
Analytical Chemistry
204.3K Visualizações

Método de adição de padrão
Analytical Chemistry
319.3K Visualizações

Curvas de calibração
Analytical Chemistry
794.6K Visualizações

Espectroscopia ultravioleta-visível (UV-Vis)
Analytical Chemistry
621.7K Visualizações

Espectroscopia raman para análise química
Analytical Chemistry
51.0K Visualizações

Fluorescência de raios X (XRF)
Analytical Chemistry
25.3K Visualizações

Cromatografia gasosa (GC) com detecção por ionização em chama
Analytical Chemistry
281.1K Visualizações

Cromatografia Líquida de Alta Eficiência (HPLC)
Analytical Chemistry
383.0K Visualizações

Cromatografia de troca iônica
Analytical Chemistry
263.9K Visualizações

Eletroforese Capilar (CE)
Analytical Chemistry
93.3K Visualizações

Introdução à Espectrometria de Massa
Analytical Chemistry
111.9K Visualizações

Microscopia Eletrônica de Varredura (MEV)
Analytical Chemistry
86.8K Visualizações

Voltametria Cíclica (CV)
Analytical Chemistry
124.2K Visualizações
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados