Method Article
Discectomia Cervical Anterior Assistida por Endoscópio e Fusão para o Tratamento da Mielopatia Espondilótica Cervical
Neste Artigo
Resumo
Descrevemos uma cirurgia minimamente invasiva usando discectomia cervical anterior assistida por endoscópio e fusão para a mielopatia espondilótica cervical.
Resumo
A mielopatia espondilótica cervical (MSC) é uma causa comum de doença da medula espinhal cervical. A endoscopia espinhal oferece vantagens cirúrgicas, como uma visão ampliada e um campo cirúrgico claro mediado por água. Este estudo descreve um procedimento de discectomia e fusão cervical anterior assistida por endoscópio (ACDF). A adição da endoscopia espinhal à cirurgia tradicional do ACDF amplia o campo cirúrgico e permite operações mais precisas, melhorando assim a segurança cirúrgica. No pós-operatório, os pacientes apresentaram melhorias significativas na função neurológica, sem complicações como disfagia, hematoma ou lesão medular. A imagem pós-operatória revelou que a compressão da medula espinhal foi completamente aliviada, com descompressão suficiente da medula espinhal e posicionamento ideal da gaiola de fusão. O campo visual claro fornecido pela endoscopia espinhal melhora a identificação das estruturas anatômicas cervicais durante a cirurgia, reduzindo efetivamente o risco de lesões na medula espinhal e nos nervos. A ACDF assistida por endoscópio demonstrou excelentes resultados clínicos e radiológicos no tratamento da MSC.
Introdução
A mielopatia espondilótica cervical (MSC) é uma das formas mais graves de espondilose cervical. A MSC é um grupo de síndromes causadas por alterações degenerativas na coluna cervical, levando à degeneração das estruturas circundantes, como discos intervertebrais e ligamentos. Essas estruturas subsequentemente comprimem a medula espinhal, resultando em disfunção dos membros ou mesmo paralisia. O diagnóstico precoce e a intervenção oportuna são essenciais para melhorar o prognóstico do paciente. A intervenção cirúrgica é frequentemente necessária quando os tratamentos conservadores falham ou a disfunção da medula espinhal piora 1,2.
Várias opções cirúrgicas estão disponíveis para o tratamento da mielopatia espondilótica cervical (MSC), incluindo discectomia e fusão cervical anterior tradicional (ACDF), corpectomia e fusão cervical anterior (ACCF), substituição do disco cervical (CDR) e cirurgia híbrida (HS), que combina ACDF e CDR3. A discectomia e fusão cervical anterior tradicional (ACDF) é uma abordagem de tratamento comum para MSC que alivia efetivamente os sintomas descomprimindo diretamente a medula espinhal e as raízes nervosas. No entanto, essa cirurgia tradicional tem limitações, incluindo um campo cirúrgico estreito e desafios com hemostasia intraoperatória. Esses problemas são particularmente pronunciados em pacientes com ossificação do ligamento longitudinal posterior (OPLL), o que impede que o material compressivo seja completamente removido durante a cirurgia e eleva substancialmente o risco de lesão medular 4,5,6. Em 1983, Bollati relatou 57 cirurgias cervicais anteriores realizadas com o auxílio de um microscópio; Esses pacientes demonstraram complicações pós-operatórias substancialmente reduzidas e aumento da segurança e eficácia7. Em comparação com o ACDF tradicional, as técnicas microcirúrgicas oferecem certas vantagens; No entanto, desafios como precisão insuficiente, má coordenação olho-mão e pontos cegos no campo cirúrgico ainda estão presentes, limitando a aplicação clínica dessas técnicas8.
As técnicas cirúrgicas endoscópicas da coluna vertebral, caracterizadas por maior clareza visual, excelente identificação tecidual e flexibilidade operacional, têm sido amplamente aplicadas em cirurgias da coluna lombar e têm alcançado resultados clínicos favoráveis 9,10,11. Portanto, integramos técnicas endoscópicas da coluna vertebral com ACDF tradicional para remover completamente a ossificação ou o tecido do núcleo pulposo livre localizado anteriormente à medula espinhal sob o campo cirúrgico claro fornecido pelo endoscópio espinhal. Essa abordagem elimina os pontos cegos associados às cirurgias tradicionais e reduz substancialmente o risco de lesão medular intraoperatória. Este artigo tem como objetivo apresentar os principais aspectos técnicos do ACDF assistido por endoscópio. Como a cirurgia tradicional de ACDF foi amplamente descrita em estudos anteriores12, ela não será reiterada neste artigo.
Protocolo
Este estudo foi aprovado pelo Comitê de Ética do Hospital Geral de Hebei. O consentimento informado foi obtido de todos os participantes individuais.
1. Preparo pré-operatório
- Antes da cirurgia, coloque o paciente em decúbito dorsal na cama do hospital, com travesseiros macios sob os ombros e um travesseiro cilíndrico sob o occipital para manter a coluna cervical em posição hiperestendida.
NOTA: Esta etapa serve a dois propósitos: (1) permitir que o paciente se adapte à posição cirúrgica e (2) avaliar, enquanto o paciente estava acordado, se a hiperextensão agrava algum sintoma neurológico. - Planejamento da operação na imagem: Adquirir tomografia computadorizada (TC) pré-operatória com reconstruções sagitais e coronais para detectar ossificação do ligamento longitudinal posterior (LLPO). Realize ressonância magnética (MRI) para avaliar a compressão pré-operatória da medula espinhal.
NOTA: A distância de ossificação nas imagens de TC sagital pode ajudar a determinar as faixas superior e inferior da janela.
2. Marcação da pele e anestesia
- Coloque o paciente em decúbito dorsal na mesa cirúrgica e faça marcações na pele no segmento cirúrgico.
- Desinfete o local da cirurgia aplicando iodo aplicado duas vezes e seguido de uma única aplicação de álcool a 75%, usando um movimento circular do local da incisão para fora. Planeje a incisão como uma incisão transversal no pescoço anterior direito.
- A gama de desinfeção cirúrgica abrange principalmente a parte anterior do pescoço e a parte superior do tórax. Certifique-se de que, verticalmente, ele se estenda da borda inferior da mandíbula até a borda superior do esterno e da clavícula e, horizontalmente, atinja as bordas laterais dos músculos esternocleidomastóideos em ambos os lados.
- Administre a pré-oxigenação usando uma máscara facial de oxigênio puro de 5 L/min por pelo menos 3 min para manter uma saturação de oxigênio de pulso de 100% antes de iniciar a indução da anestesia geral. Peça a um único anestesiologista que administre por via intravenosa injeção de citrato de sufentanil (0,3-0,5 μg/kg), besilato de cisatracúrio para injeção (0,15-0,20 mg/kg) e injeção de etomidato (0,2-0,4 mg/kg), enquanto monitora continuamente o eletrocardiograma (ECG), pressão arterial e saturação de oxigênio para garantir a segurança intraoperatória.
3. Exposição do segmento afetado
- Faça uma incisão transversal de aproximadamente 3 cm de comprimento no pescoço anterior direito (Figura 1).
- Usando a abordagem de Smith-Robinson, exponha a face anterior do corpo vertebral cervical e do disco intervertebral12. Use fluoroscopia intraoperatória do braço em C para confirmar o espaço do disco alvo.
- Incisar o anel fibroso do segmento afetado e remover gradualmente o disco intervertebral e as placas terminais da cartilagem até atingir a margem posterior do corpo vertebral.
- Instale um afastador Caspar e insira o sistema de endoscópio espinhal no espaço intervertebral (Figura 2).
4. Procedimentos endoscópicos para a coluna cervical
- Sob visualização endoscópica da coluna vertebral, abordar os esporões ósseos na margem posterior do corpo vertebral cervical e ampliar o espaço intervertebral. Use uma broca para remover os esporões ósseos superiores e inferiores, bem como os pontos de fixação do anel fibroso.
- A faixa de remoção óssea em ambos os lados se estende às articulações não covertebrais; determinar a extensão da excisão cranial e caudal com base na localização e tamanho da ossificação observada na imagem pré-operatória, garantindo excisão suficiente em ambas as extremidades.
- Extirpar o anel fibroso profundo. Use pinças de núcleo pulposo, punções de Kerrison e outras ferramentas alternadamente para descomprimir o canal vertebral, estendendo progressivamente a descompressão em direção à medula espinhal (Figura 3).
NOTA: Durante o processo de rebarbação, as técnicas de retificação lateral e retificação por tração ascendente foram priorizadas para evitar a remoção excessiva do osso superficial, protegendo assim a placa terminal óssea. O uso de um endoscópio espinhal com ângulo de 30°, capacidade de inclinação e broca multidirecional expandiu ainda mais a faixa de descompressão e garantiu maior precisão cirúrgica.
- Incise o ligamento longitudinal posterior (PLL) macio para expor a medula espinhal. Depois que o anel fibroso e a camada superficial do PLL forem incisados, use um punção Kerrison e uma faca de gancho para cortar o PLL macio e separar o espaço entre o PLL e a medula espinhal (Figura 4).
NOTA: Uma vez que o espaço entre a medula espinhal e o PLL são separados, a descompressão subsequente torna-se significativamente mais fácil. A remoção do PLL e a exposição da medula espinhal são etapas críticas neste procedimento. - Para pacientes com LLP, inicie o procedimento com a remoção do PLL mole e a exposição da medula espinhal. Use um dissector da raiz nervosa para avaliar o espaço entre a ossificação e a medula espinhal para confirmar se há adesão entre a ossificação e a dura-máter. Use uma pinça de núcleo pulposo de 45° ou um punção Kerrison para remover gradualmente o ligamento ossificado até que a dura-máter esteja totalmente exposta. Realizar visualização endoscópica para verificar se a pulsação da dura-máter é satisfatória (Figura 5).
NOTA: Durante este processo, uma broca, dissector da raiz nervosa, pinça do núcleo pulposo ou punção Kerrison foram usados alternadamente para aumentar a flexibilidade e a segurança operacional. - Use sondas de eletrocoagulação bipolar para hemostasia e aplique gelatina fluida para auxiliar no controle do sangramento. Uma vez confirmado que o campo cirúrgico está livre de sangramento ativo, retire lentamente o endoscópio espinhal (Figura 6).
NOTA: Evite a remoção rápida do endoscópio espinhal para evitar a hérnia dural causada por pressão negativa. - Encha uma gaiola de malha de titânio de tamanho adequado com osso autólogo e insira-a no espaço intervertebral. Selecione uma placa de titânio longa o suficiente para cobrir o segmento cirúrgico e implante seis parafusos nas vértebras para prender a placa de titânio, seguindo o procedimento padrão do ACDF12 tradicional para garantir a estabilidade pós-operatória e a fusão bem-sucedida.
5. Cuidados pós-operatórios
- Realizar monitoramento contínuo de ECG e administrar inalação e nebulização intermitentes de oxigênio; incentivar o paciente a tossir e expectorar.
- Avalie a intensidade da dor do paciente por meio de investigação e administre analgésicos não esteróides imediatamente, conforme necessário.
- Monitore de perto as mudanças na força muscular dos membros e na função sensorial.
- Remova o tubo de drenagem quando o volume de drenagem for inferior a 30 mL dentro de 24 h de pós-operatório.
Resultados
Este estudo incluiu 20 pacientes submetidos à cirurgia ACDF assistida por endoscópio de janeiro de 2024 a novembro de 2024. A média de idade foi de 62,2 anos, e a amostra do estudo incluiu 9 mulheres e 11 homens. O tempo operatório médio foi de 125,5 min e o volume médio de perda sanguínea foi de 59,0 mL (Tabela 1 e Tabela 2). Todos os pacientes obtiveram alívio bem-sucedido dos sintomas da medula espinhal, com escores mais baixos na escala visual analógica (EVA) pós-operatória em comparação com os escores pré-operatórios e escores JOA pós-operatórios significativamente melhorados. A taxa média de melhora do escore JOA foi de 60,7%. Não ocorreram complicações, como disfagia, hematoma ou lesão medular (Tabela 1 e Tabela 2). Os exames de imagem pós-operatórios confirmaram a remoção completa do material compressivo, descompressão medular suficiente e colocação adequada da gaiola de fusão (Figura 7 e Figura 8).
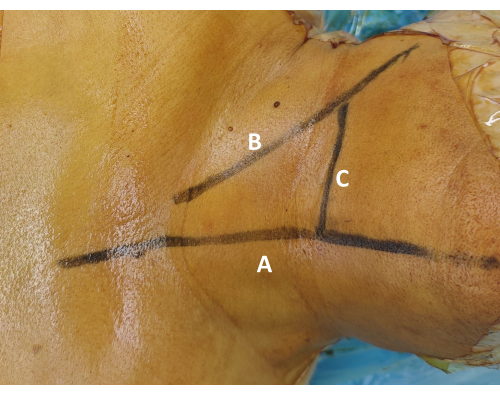
Figura 1: Marcação da superfície do segmento cirúrgico. (A) Desenhe a marcação da linha média ao longo da linha média da traqueia para garantir a simetria cirúrgica. (B) Desenhe a linha de localização transversal ao longo da borda superior da clavícula. Palpe o músculo esternocleidomastóideo e a cartilagem cricoide para guiar essa marcação. (C) Confirme a marcação do nível alvo usando orientação fluoroscópica e marque a projeção de pele correspondente do disco intervertebral pretendido. Clique aqui para ver uma versão maior desta figura.
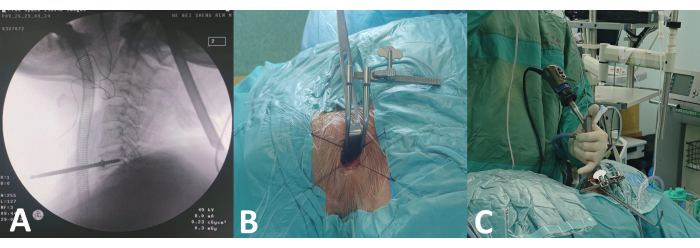
Figura 2: Procedimentos pré-operatórios para endoscopia espinhal. (A) Posicionamento intraoperatório da fluoroscopia do arco em C. (B) Instalação do afastador Caspar. (C) Endoscopia espinhal. Clique aqui para ver uma versão maior desta figura.
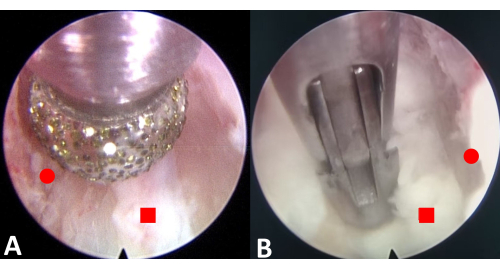
Figura 3: Excisão endoscópica dos osteófitos e anel fibroso. (A) Rebarbar os osteófitos superiores e inferiores. (B) Ressecar o anel fibroso. O círculo vermelho representa o osteófito e o quadrado vermelho representa o anel fibroso. Clique aqui para ver uma versão maior desta figura.
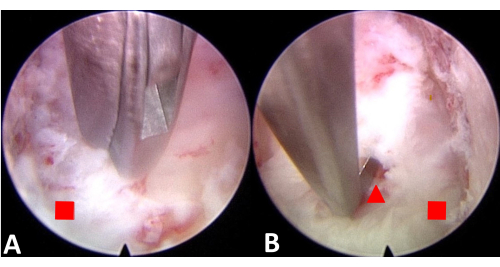
Figura 4: Incisão endoscópica do PLL e separação do PLL da medula espinhal para criar espaço. (A) Incisar o PLL. (B) Separe o PLL da medula espinhal. O quadrado vermelho representa o ligamento longitudinal posterior e o triângulo vermelho representa a medula espinhal. Clique aqui para ver uma versão maior desta figura.
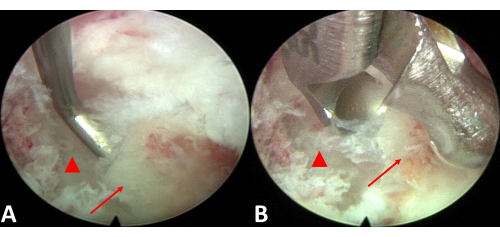
Figura 5: Excisão endoscópica da ossificação. (A) Avalie o espaço entre o tecido ossificado e a medula espinhal. (B) Extirpar o ligamento ossificado. O triângulo vermelho representa a medula espinhal e a seta vermelha aponta para a ossificação do ligamento longitudinal posterior. Clique aqui para ver uma versão maior desta figura.
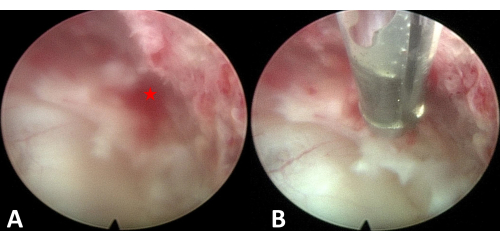
Figura 6: Hemostasia. (A) Ponto de sangramento. (B) Hemostasia sob visualização endoscópica. O asterisco representa o ponto de sangramento. Clique aqui para ver uma versão maior desta figura.

Figura 7: Imagem pré e pós-operatória. Paciente com mielopatia espondilótica cervical antes da cirurgia, após a cirurgia e 3 meses após a cirurgia. Clique aqui para ver uma versão maior desta figura.
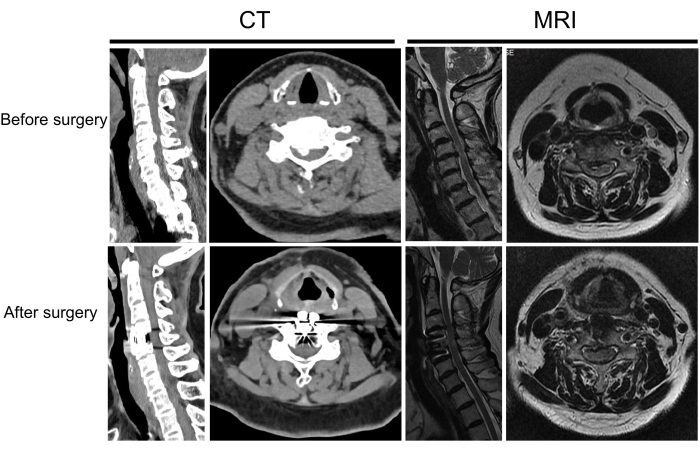
Figura 8: Imagem pré e pós-operatória de outro paciente. Paciente com mielopatia espondilótica cervical antes e após a cirurgia. Clique aqui para ver uma versão maior desta figura.
Tabela 1: Informações do paciente. Clique aqui para baixar esta tabela.
Tabela 2: Características cirúrgicas e resultados pós-operatórios. Clique aqui para baixar esta tabela.
Discussão
A discectomia e fusão cervical anterior (ACDF) é um método cirúrgico comum para o tratamento da mielopatia espondilótica cervical (MSC) e tem resultados clínicos satisfatórios13,14. No entanto, a cirurgia tradicional enfrenta desafios como um campo cirúrgico limitado e dificuldades com hemostasia. Esses problemas são particularmente pronunciados em casos de ossificação do ligamento longitudinal posterior (OPLL) ou hérnia de disco à distância; Nesses casos, o material compressivo não pode ser completamente removido no intraoperatório, e o risco de lesão medular permanece alto15.
Com os avanços nas técnicas de cirurgia minimamente invasiva da coluna vertebral, a aplicação da endoscopia microscópica no ACDF aumentou gradualmente, expandindo o campo cirúrgico e melhorando a precisão operatória. No entanto, o procedimento assistido por microscópio ainda apresenta limitações, como má coordenação olho-mão e pontos cegos no campo de visão8. A discectomia cervical anterior endoscópica total (DCFA) é um procedimento minimamente invasivo. Em comparação com a cirurgia convencional, o FACD reduz significativamente os danos aos tecidos moles, o tempo operatório e as complicações. O processo de recuperação é rápido, sem necessidade de intervenções cirúrgicas adicionais16.
No entanto, a ACDF assistida por endoscópio oferece várias vantagens sobre a descompressão cervical anterior endoscópica total, particularmente em termos de estabilidade pós-operatória, indicações mais amplas e facilidade de execução cirúrgica. Ao incorporar a fusão intersomática com uma gaiola de titânio e fixação em placa, aumenta a estabilidade segmentar e minimiza o risco de perda ou recorrência da altura do disco pós-operatório, o que é uma preocupação com as técnicas endoscópicas completas sem fusão. Além disso, a ACDF assistida por endoscópio é mais adequada para doença em vários níveis, degeneração discal grave e casos que envolvem ossificação do ligamento longitudinal posterior (LLP), onde a descompressão endoscópica total pode ser insuficiente. Essa técnica também fornece um campo cirúrgico mais amplo, permitindo uma descompressão neural mais abrangente e reduzindo o risco de compressão residual. Além disso, segue o procedimento padrão do ACDF, facilitando a adoção pelos cirurgiões em comparação com a abordagem endoscópica completa tecnicamente exigente.
Embora a descompressão anterior endoscópica total seja vantajosa para casos selecionados com hérnia de disco mole de nível único, a ACDF assistida por endoscópio continua sendo uma opção mais versátil e reprodutível para uma gama mais ampla de patologias da coluna cervical. O ACDF assistido por endoscópio alcançou excelentes resultados clínicos e radiológicos, demonstrando eficácia confiável e alta segurança cirúrgica. Wu et al.17. descobriram que a ACDF assistida por endoscópio oferece vantagens significativas sobre a ACDF tradicional, incluindo um campo cirúrgico mais claro, menos perda de sangue intraoperatório e menor risco de lesão nervosa. No entanto, eles também relataram um tempo operatório mais longo devido à complexidade das técnicas endoscópicas. Nossos achados são consistentes com seus resultados, pois nosso estudo também demonstrou um tempo cirúrgico ligeiramente prolongado com ACDF assistido por endoscópio. No entanto, a duração prolongada não afeta significativamente os resultados clínicos, e os benefícios da visualização aprimorada e do trauma reduzido superam essa limitação, tornando o ACDF assistido por endoscópio uma alternativa viável ao ACDF tradicional ACDF.As uma nova ferramenta de ampliação para ACDF, a endoscopia espinhal fornece visualização mais clara e maior flexibilidade operacional, abordando efetivamente essas questões.
As vantagens das operações assistidas por endoscopia são as seguintes. Primeiro, sob endoscopia espinhal, o PLL pode ser distinguido com mais detalhes, permitindo uma dissecção aguda usando punções Kerrison. O endoscópio fornece uma visão mais clara da medula espinhal, permitindo que o cirurgião avalie com precisão a adequação da descompressão e minimize efetivamente o risco de lesão da medula espinhal. Além disso, o uso de uma rebarba permite uma operação de proximidade, garantindo uma remoção mais precisa e completa dos esporões ósseos. Comparado com o olho nu e o microscópio, o endoscópio oferece visualização superior durante a exposição e descompressão das articulações não covertebrais bilaterais.
Em segundo lugar, o endoscópio espinhal oferece maior liberdade de operação com seu ângulo de visão integrado de 30° e cabeça de rebarba ajustável, permitindo uma faixa de descompressão mais ampla. Esse recurso aumenta a flexibilidade e a precisão ao trabalhar em regiões anatômicas complexas. Em terceiro lugar, a endoscopia mediada por água permite uma identificação mais precisa dos pontos de sangramento. Para sangramento na margem posterior do corpo vertebral, a sonda de radiofrequência curva pode alcançar e abordar o local do sangramento com precisão, melhorando significativamente a eficácia hemostática e a precisão cirúrgica. Em quarto lugar, o sistema endoscópico minimiza a interferência das mãos do cirurgião, reduzindo o número de pontos cegos no campo cirúrgico. O design coaxial do endoscópio se alinha com os hábitos operacionais dos cirurgiões endoscópicos, evitando colisões de instrumentos e garantindo procedimentos mais suaves e eficientes.
No entanto, a aplicação de técnicas endoscópicas da coluna vertebral também apresenta alguns desafios, como o tempo operatório prolongado e a necessidade de cirurgiões com habilidades cirúrgicas avançadas e conhecimento detalhado de microanatomia. Além disso, embora a cirurgia endoscópica ofereça um campo visual mais amplo, o campo ainda pode ser limitado em casos extremamente complexos. Com o avanço contínuo da tecnologia e melhorias nos instrumentos cirúrgicos, acreditamos que o uso da endoscopia espinhal na cirurgia da coluna cervical amadurecerá gradualmente e que o tempo operatório diminuirá ainda mais.
Divulgações
Os autores não têm conflitos de interesse a declarar.
Agradecimentos
Nenhum
Materiais
| Name | Company | Catalog Number | Comments |
| 75% alcohol | Hebei Ruihe Medical Equipment Co., Ltd | CC-01A | PEEK |
| Anterior Cervical Nail Plate Fixation System | Hebei Ruihe Medical Equipment Co., Ltd | PN-03 | Plate:TA3G, Nail:TC4 |
| Cervical Fusion Cage | |||
| cisatracurium besylate | SPINENDOS GmbH | SP081430.030 | Inner diameter:4.3 mm; Outer diameter:7.0 mm; Field angle: 80 °; Visual angle: 30 °; Working length: 181 mm |
| Endoscope system | SPINENDOS GmbH | SP082628.351 | Φ2.5 mm × 310 mm |
| Endoscopic forceps | SPINENDOS GmbH | SP082700.040L | Φ4.0 mm × 360 mm |
| Endoscopic hook | XIYI | MQZ | Φ3.2 mm × 328 mm |
| Endoscopic rongeur | ELLIQUENCE | DTF-40 | 40 cm |
| etomidate | SPINENDOS GmbH | SP082781.835 | Φ2.5 mm × 330 mm |
| High-speed burr | Neusoft Corporation | ||
| Interventional radiology | Ferrosan Medical Devices A/S | MS0010 | |
| iodine | Sichuan Guona Technology Co.,LTD | NNBP/40D/ | |
| Neusoft PACS/RIS | Elliquence, LLC | DTF-40 | |
| n-HA/PA66 | SPINENDOS GmbH | SP082615.265 | Φ7.2 mm × 178 mm |
| sufentanil citrate injection | |||
| SURGIFLO Haemostatic Matrix | |||
| Trigger-Flex Bipolar System | |||
| Working sheath |
Referências
- Bakhsheshian, J., Mehta, V. A., Liu, J. C. Current diagnosis and management of cervical spondylotic myelopathy. Global Spine J. 7 (6), 572-586 (2017).
- McCormick, J. R., Sama, A. J., Schiller, N. C., Butler, A. J., Donnally, C. J. III Cervical spondylotic myelopathy: A guide to diagnosis and management. J Am Board Fam Med. 33 (2), 303-313 (2020).
- Visocchi, M., et al. Hybrid implants in anterior cervical decompressive surgery for degenerative disease. J Craniovertebr Junction Spine. 12 (1), 54-60 (2021).
- Lee, C. J., Boody, B. S., Demeter, J., Smucker, J. D., Sasso, R. C. Long-term radiographic and functional outcomes of patients with absence of radiographic union at 2 years after single-level anterior cervical discectomy and fusion. Global Spine J. 10 (6), 741-747 (2020).
- Luo, H. T., et al. Meta-analysis of the treatment of cervical spondylosis by microscopy-assisted and traditional anterior cervical decompression under direct vision. Chin J Tissue Eng Res. 24 (9), 1369-1377 (2020).
- Marawar, S., et al. National trends in anterior cervical fusion procedures. Spine (Phila Pa 1976). 35 (15), 1454-1459 (2010).
- Bollati, A., Galli, G., Gandolfini, M., Marini, G., Gatta, G. Microsurgical anterior cervical disk removal without interbody fusion. Surg Neurol. 19 (4), 329-333 (1983).
- Damodaran, O., Lee, J., Lee, G. Microscope in modern spinal surgery: Advantages, ergonomics and limitations. ANZ J Surg. 83 (4), 211-214 (2013).
- Liu, L., Dong, J., Wang, D., Zhang, C., Zhou, Y. Clinical outcomes and quality of life in elderly patients treated with a newly designed double tube endoscopy for degenerative lumbar spinal stenosis. Orthop Surg. 14 (7), 1359-1368 (2022).
- Han, S., et al. Clinical application of large channel endoscopic systems with full endoscopic visualization technique in lumbar central spinal stenosis: A retrospective cohort study. Pain Ther. 11 (4), 1309-1326 (2022).
- Liang, J., Li, H., Tao, Y., Yuan, W., Wang, H. Efficacy and complications of unilateral biportal endoscopic spinal surgery for lumbar spinal stenosis: A meta-analysis and systematic review. World Neurosurg. 159, e91-e102 (2022).
- Tian, X., Rudd, S., Yang, D., Ding, W., Yang, S. Anterior cervical hybrid decompression and fusion surgery to treat multilevel cervical spondylotic myelopathy. J Vis Exp. (196), e65034(2023).
- Sun, X., et al. The frequency and treatment of dural tears and cerebrospinal fluid leakage in 266 patients with thoracic myelopathy caused by ossification of the ligamentum flavum. Spine (Phila Pa 1976). 37 (12), E702-E707 (2012).
- Wang, T., et al. Anterior cervical discectomy and fusion versus anterior cervical corpectomy and fusion in multilevel cervical spondylotic myelopathy: A meta-analysis. Medicine (Baltimore). 95 (49), e5437(2016).
- Nakajima, H., et al. Long-term outcome of anterior cervical decompression with fusion for cervical ossification of posterior longitudinal ligament including postsurgical remnant ossified spinal lesion. Spine (Phila Pa 1976). 44 (24), E1452-E1460 (2019).
- Ruetten, S., Komp, M., Merk, H., Godolias, G. Full-endoscopic anterior decompression versus conventional anterior decompression and fusion in cervical disc herniations. Int Orthop. 33 (6), 1677-1682 (2009).
- Wu, Z. P., Wei, Z. Y., Song, X. L. Comparison of efficacy between endoscope-assisted anterior cervical discectomy and fusion (ACDF) and open ACDF in the treatment of single-segment cervical spondylotic myelopathy. J Orthop Surg Res. 19 (1), 35(2024).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados