Method Article
Indução de choque hemorrágico padronizado guiada por oximetria cerebral e Monitorização hemodinâmica estendida em suínos
Neste Artigo
Resumo
O choque hemorrágico é uma complicação grave em pacientes gravemente feridos, o que leva à subalimentação de oxigênio com risco de vida. Nós apresentamos um método estandardizado para induzir o choque hemorrágico através da retirada do sangue nos porcos que é guiado pela hemodinâmica e pela oxigenação cerebral microcirculatória.
Resumo
O choque hemorrágico classifica entre as principais razões para a morte grave relacionada a lesões. A perda do volume circulatório e dos portadores do oxigênio pode conduzir a uma fonte insuficiente do oxigênio e a uma falha irreversível do órgão. O cérebro exerce somente capacidades limitadas da compensação e é particularmente no risco elevado de dano hypoxic severo. Este artigo demonstra a indução reprodutível do choque hemorrágico life-threatening em um modelo suínos por meio da retirada de sangue calculada. Nós titular a indução de choque guiada pela espectroscopia near-infrared e pela monitoração hemodynamic prolongada para indicar a falha circulatória sistemática, assim como a depleção de oxigênio microcirculatório cerebral. Em comparação com modelos similares que se concentram principalmente em volumes de remoção predefinidos para indução de choque, essa abordagem destaca uma titulação por meio da falha resultante da macro e da microcirculação.
Introdução
A perda de sangue maciça está entre as causas principais de mortes ferimento-relacionadas1,2,3. A perda de fluidos circulatórios e portadores de oxigênio leva a insuficiência hemodinâmica e undersupply de oxigênio grave e pode causar insuficiência de órgãos irreversíveis e morte. O nível de gravidade do choque é influenciado por fatores adicionais como hipotermia, coagulopatia e acidose4. Particularmente o cérebro, mas também os rins não têm capacidade de compensação devido à alta demanda de oxigênio e à incapacidade de uma adequada geração de energia anaeróbia5,6. Para fins terapêuticos, a ação rápida e imediata é crucial. Na prática clínica, a ressuscitação fluida com uma solução de eletrólitos equilibrada é a primeira opção para o tratamento, seguida pela administração de concentrados de glóbulos vermelhos e plasma fresco congelado. Os concentrados de trombócitos, catecolaminas e a otimização da coagulação e o status ácido-base apoiam a terapia para recuperar condições fisiológicas normais após trauma sustentado. Este conceito centra-se na restauração da Hemodinâmica e macrocirculação. Vários estudos, entretanto, demonstram que a perfusão microcirculatória não se recupera simultaneamente com a macrocirculação. Especialmente, a perfusão cerebral permanece prejudicada e pode ocorrer uma subalimentação de oxigênio7,8.
O uso de modelos animais permite que os cientistas estabeleçam estratégias novas ou experimentais. A anatomia, a homologia, e a fisiologia comparáveis dos porcos e dos seres humanos permitem conclusões em fatores patológicos específicos. Ambas as espécies têm um sistema metabólico semelhante e resposta a tratamentos farmacológicos. Esta é uma grande vantagem em comparação com pequenos modelos animais, onde as diferenças no volume sanguíneo, hemodinâmica e fisiologia geral tornam quase impossível imitar um cenário clínico9. Além disso, equipamentos médicos autorizados e consumíveis podem ser facilmente utilizados em modelos de suínos. Além disso, é facilmente possível obter suínos de fornecedores comerciais, o que permite uma alta diversidade de genética e fenótipos e é o custo de redução de10. O modelo de retirada de sangue via canulação de vasos é bastante comum11,12,13,14,15.
Neste estudo, nós estendemos o conceito da indução de choque hemorrágico através da retirada sanguínea arterial com um titulação exato da falha hemodynamic e do prejuízo cerebral do oxigenação. O choque hemorrágico é atingido se o índice cardíaco e a pressão arterial média decresce abaixo de 40% do valor basal, o que tem demonstrado causar uma deterioração considerável da saturação de oxigenação regional cerebral8. A medida de saída cardíaca de contorno de pulso (PiCCO) é usada para monitoramento hemodinâmico contínuo. Primeiro, o sistema deve ser calibrado por termodiluição transpulmonar, o que possibilita o cálculo do índice cardíaco do conteúdo de água pulmonar extravascular e do volume diastólico final global. Subseqüentemente, o índice cardíaco contínuo é calculado pela análise do contorno do pulso e igualmente fornece parâmetros dinâmicos da pré-carga como a variação do volume da pressão de pulso e do curso.
Esta técnica é bem estabelecida em configurações clínicas e experimentais. A espectroscopia de infravermelho próximo (NIRS) é um método clinicamente e experimentalmente estabelecido para monitorar as alterações no suprimento de oxigênio cerebral em tempo real. Os sensores Self-aderentes são Unidos à testa esquerda e direita e calculam o oxigenação cerebral não-invasora no córtice frontal cerebral. Dois comprimentos de onda de luz infravermelha (700 e 900 nm) são emitidos e detectados pelos sensores após serem refletidos a partir do tecido do córtex. Para avaliar o teor de oxigênio cerebral, as contribuições do sangue arterial e venoso são calculadas em 1:3 relações e atualizadas em intervalos de 5 s. A sensibilidade em profundidade de 1-4 cm é a diminuição exponencial e influenciada pelo tecido penetrado (por exemplo, pele e osso), embora o crânio seja translúcido à luz infravermelha. A técnica facilita ações terapêuticas rápidas para prevenir pacientes de desfechos adversos como Delirium ou lesão cerebral hipóxico e serve como parâmetro alvo em caso de comprometimento do débito cardíaco16,17. A combinação de ambas as técnicas durante choque experimental permite uma titulação exata da macrocirculação, assim como a deficiência microcirculatória cerebral, para estudar este evento life-threatening.
Protocolo
Os experimentos neste protocolo foram aprovados pela Comissão Estadual e institucional de cuidados com animais (Landesuntersuchungsamt Rheinland-Pfalz, Koblenz, Alemanha; Presidente: Dr. Silvia Eisch-Wolf; numero de referência: 23 177-07/G 14-1-084; 02.02.2015). os experimentos foram conduzidos de acordo com o relatório de pesquisa de animais das diretrizes de experimentos in vivo (chegada). O estudo foi planejado e conduzido entre novembro de 2015 e março de 2016. Após extensa pesquisa bibliográfica, o modelo de suínos foi escolhido como um modelo bem estabelecido para choque hemorrágico. Sete suínos machos anestesiados (Sus scrofa domestica) com peso médio de 28 ± 2 kg e idade de 2-3 meses foram incluídos no protocolo. Os animais foram atendidos por um reprodutor local recomendado pelo Comitê Estadual e institucional de cuidado animal. Os animais foram mantidos em seu ambiente conhecido o mais longo possível para minimizar o stress. O alimento, mas não a água foi negado 6 h antes que o experimento fosse programado, para reduzir o risco de aspiração. O curso de tempo representativo é exibido na Figura 1.
1. anestesia, intubação, e ventilação mecânica
- Suínos sedata com uma injecção combinada de cetamina (4 mg · kg-1) e azaperona (8 mg · kg-1) no pescoço ou no músculo glúteo com uma agulha para injecção intramuscular (1,2 mm). Assegure-se de que os animais permaneçam estáveis até que a sedação se defina.
Atenção: As luvas são absolutamente necessárias ao manusear animais. - Transportar os animais sedados para o laboratório.
Nota: Os animais caem profundamente adormecidos e não despertam durante a manipulação normal, como quando são levantados na gaiola do transporte. Neste cenário, o tempo de transporte foi de cerca de 20 min com uma van especial para o transporte de animais. - Monitore a saturação periférica de oxigênio (SpO2) com um sensor cortado na cauda ou orelha do porco diretamente após a chegada.
- Desinfete a pele com tintura de desinfecção incolor e aguarde 3 minutos antes de inserir um cateter de veia periférica (1,2 mm) numa veia da orelha. Em seguida, induzir anestesia por injeção intravenosa de fentanil (4 μg · kg-1) e propofol (3 mg · kg-1).
- Quando todos os reflexos estão ausentes e respiração espontânea expira, coloque os porcos em posição supina em uma maca e corrigi-los com bandagens.
Nota: Níveis adequados de anestesia devem ser confirmados por um pesquisador experiente pela ausência de reflexo palpebral e outras reações a estímulos externos. - Inicie imediatamente a ventilação não invasiva com uma máscara de ventilação do cão (tamanho 2). Use os seguintes parâmetros de ventilação: fração inspiratória de oxigênio (FiO2) = 1,0; frequência respiratória = 14-16 min-1; pressão inspiratória máxima < 20 cm H2o, pressão expiratória final positiva (PEEP) = 5 cm h2o.
- Manter a anestesia através de uma infusão contínua de fentanil (0,1-0,2 μg ·kg-1·h-1) e propofol (8-12 mg · kg-1· h-1) e iniciar uma infusão de solução eletrolítica balanceada (5 ml · kg-1· h-1).
- Facilitar a intubação endotraqueal pela aplicação de um relaxante muscular (Atracurium 0,5 mg · kg-1).
- Proteja as vias aéreas via intubação com um tubo endotraqueal comum (ID 6-7) e um introdutor. Use um laringoscópio comum com uma lâmina Macintosh (tamanho 4). Duas pessoas facilitam o procedimento.
- Pessoa 1: fixar a língua fora com um pedaço de tecido e abrir o focinho com a outra mão.
- Pessoa 2: realizar uma laringoscopia.
- Pessoa 2: quando a epiglote entra em vista, mova o laringoscópio ventralmente. Levante a epiglote e certifique-se de que as cordas vocais estejam visíveis.
Nota: Se a epiglote não se move dorsally, ele adere ao Palatino macio e pode ser mobilizado pela ponta do tubo. Alternativamente, uma lâmina com outro tamanho (3 ou 5) ou tipo (lâmina de Miller) pode ser usada.
- Mova o tubo cuidadosamente através das cordas vocais.
Nota: O ponto mais estreito da traquéia não está no nível das cordas vocais, mas subglottic. Se a inserção do tubo não for possível, tente girar o tubo ou usar um tubo menor. - Puxe o introdutor para fora do tubo, use uma seringa de 10 mL para bloquear o manguito com 10 mL de ar e controle a pressão do manguito com um gerente de manguito (30 cm H2O).
- Iniciar a ventilação mecânica após o tubo estar ligado a um ventilador (PEEP = 5 cm H2o; volume corrente = 8 ml · kg-1; FiO2 = 0,4; relação inspiração-expiração = 1:2; frequência respiratória = variável para atingir um CO2 de maré final de ≪ 6 kPa).
Nota: Evite a flutuação do CO2 para minimizar quaisquer efeitos respiratórios na perfusão cerebral. - Certifique-se de que a posição do tubo está correta por exhalação regular e periódica de CO2 via capnografia, e verificar a ventilação dupla face através da ausculta.
Nota: Se o tubo é coloc incorretamente, a inflação do ar no estômago forma ràpida uma protuberância visível na parede abdominal, mesmo antes que o capnografia esteja instalado. Neste caso, a substituição do tubo e a inserção de um tubo gástrico são absolutamente necessárias. - Com duas pessoas, coloque um tubo gástrico no estômago para evitar refluxo e vômitos.
- Pessoa 1: fixar a língua fora com um pedaço de tecido e abrir o focinho com a outra mão.
- Pessoa 2: realizar uma laringoscopia da laringe porcina.
- Pessoa 2: visualize o esôfago.
- Pessoa 2: empurre o tubo gástrico dentro do esôfago com um par de fórceps Magill até que o fluido gástrico é drenado.
Nota: Às vezes, a visualização não é fácil. Neste caso, mova o laringoscópio dorsalmente para o tubo e empurre-o ventralmente para abrir o esôfago. Durante o procedimento, o corpo animal é coberto com cobertores para evitar a hipotermia. Se a temperatura do corpo do animal diminui, use um sistema de aquecimento para estabilizar a temperatura em um nível fisiológico (veja a tabela de materiais). A temperatura do corpo é exibida na tela do PiCCO.
2. instrumentação
- Use ataduras para puxar para trás as patas traseiras para suavificar as dobras na área femoral para cateterismo de vasos.
- Prepare os seguintes materiais: uma seringa de 5 mL, uma seringa de 1 10 mL, uma seringa de 1 50 mL, uma agulha de Seldinger, bainhas do introdutor (2 milímetros, 2,7 milímetros, 2,7 milímetros), guidewires para as bainhas, um cateter venoso central com três portos (2,3 milímetros, 30 cm) com fio-guia, e um PiCCO cateter (1,67 mm, 20 cm).
- Desinfete a área inguinal com desinfecção colorida, aguarde 2 min e limpe a desinfecção com um tecido estéril. Repita este procedimento 3x. Após a terceira vez, não retire a desinfecção.
- Preencha todos os cateteres com soluções salinas.
- Aplique o gel do ultra-som à ponta de prova do ultra-som. Cubra a área inguinal com um Drape fenestrado estéril e escaneie os vasos femorais direito com ultra-som. Use a técnica de Doppler para distinguir entre a artéria e a veia18.
- Sangue pulsante vermelho brilhante confirma a posição da agulha aspirava. Desconecte a seringa e insira o fio-guia na artéria femoral direita.
- Visualize o eixo longitudinal da veia femoral direita e insira a agulha de Seldinger aspiração permanente com a seringa de 5 mL.
- Aspirar a obscuridade-sangue venoso nonpulsating vermelho.
- Visualize a artéria femoral direita axialmente e mude para uma visão longitudinal da artéria girando a sonda 90 °.
-
Perfure a artéria femoral direita a visualização do ultra-som com a agulha de Seldinger a aspiração permanente com a seringa de 5 mL.
Nota: a técnica de Seldinger guiada por ultrassom está associada a perda de sangue significativamente menor, trauma tecidual e consumo de tempo do que outros métodos de acesso vascular19,20.- Se a posição correta da agulha nos diferentes vasos não puder ser estabelecida com certeza, tome as sondas de sangue e analise o conteúdo de gás sanguíneo com um analisador de gás sanguíneo (veja a tabela de materiais). Um alto nível de oxigênio é um bom sinal de sangue arterial, e um baixo nível de oxigênio é um sinal de sangue venoso.
- Insira o fio-guia para o cateter venoso central na veia femoral direita após desconectar a seringa e retraindo a agulha de Seldinger.
- Visualize ambas as embarcações direitas com ultra-som para controlar a posição correta do fio.
- Empurre a bainha introdutor arterial (2 mm) sobre o fio-guia na artéria direita e fixe a posição com a aspiração de sangue.
- Use a técnica de Seldinger para posicionar a linha venosa central na veia femoral direita. Aspirar todas as portas e lave-as com solução salina.
- Realize o mesmo procedimento no lado inguinal esquerdo para inserir as outras bainhas de introdutor na técnica de Seldinger na artéria femoral esquerda (2,7 mm) e na veia femoral (2,7 mm).
- Conecte a bainha de introdutor arterial direita e o cateter venoso central com dois sistemas de transdutor para a medição da hemodinâmica invasiva e Posicione ambos os transdutores no nível do coração para obter os valores apropriados.
- Troque os três sentidos-stopcocks de ambos os transdutores abertos à atmosfera para calibrar os sistemas a 0 como é prescrito nas instruções da operação.
Nota: É absolutamente necessário evitar quaisquer bolhas de ar e manchas de sangue nos sistemas para gerar valores plausíveis. - Mude todas as infusões para manter a anestesia da veia periférica à linha venosa central.
- Tomar valores basais (hemodinâmica, espirometria, NIRS (ver secção 4) e PiCCO (ver secção 3) após 15 min de recuperação.
- Iniciar choque hemorrágico (ver secção 5).
3. medição PiCCO
Nota: Para o equipamento PiCCO, consulte a tabela de materiais.
- Insira o cateter PiCCO na bainha introdutor arterial direita.
Nota: Na medicina clínica, os cateteres PiCCO são diretamente colocados pela técnica de Seldinger. No entanto, a colocação através de uma bainha introdutora é viável também. - Conecte o cateter com o fio arterial do sistema PiCCO e o transdutor arterial diretamente com o porto PiCCO. Em seguida, recalibrar conforme descrito na etapa 2,17.
- Conecte a unidade de medição venosa do sistema PiCCO com a bainha do introdutor venoso esquerdo.
Nota: É necessário conectar as pontas de prova venosas e arteriais em alguma distância de se. Caso contrário, a medida será perturbada, pois a aplicação de solução salina fria no sistema venoso influenciará a medida arterial. Para mais detalhes sobre o PiCCO, veja Mayer e Suttner21. - Ligue o sistema PiCCO e confirme que um novo paciente é medido.
- Introduza o tamanho e o peso do animal e mude a categoria para adultos.
- Insira o nome do protocolo e a ID e insira Exit.
- Defina o volume de injeção para 10 mL.
Nota: O volume da solução de injeção escolhida pode ser variado. Um volume mais alto torna os valores medidos mais válidos. Escolha um pequeno volume para evitar quaisquer efeitos de hemodiluição através da aplicação repetitiva. - Entrar a pressão venosa central.
- Abra a torneira de três vias para a atmosfera, clique em zero para a calibração do sistema, e clique em sair.
- Calibre a medida contínua do débito cardíaco como descrito em seguida e estale sobre td (thermodilution). Prepare a solução salina fisiológica com uma temperatura de 4 ° c em uma seringa de 10 mL e clique em Iniciar.
- Injete 10 mL da solução salina fria de forma rápida e constante na unidade de medição venosa e aguarde até que a medição seja concluída e o sistema solicite uma repetição.
- Repita este procedimento até que três medições sejam concluídas.
- Deixe o sistema calcular a média de todos os parâmetros e clique em Exit.
- Após a calibração completa, inicie imediatamente a medição. Para monitorar a indução de choque, concentre-se no índice cardíaco do parâmetro derivado de PiCCO.
4. saturação de oxigenação regional cerebral
Nota: Para que o equipamento monitore a oxigenação regional cerebral, veja a tabela de materiais.
- Raspar a testa do porco com uma navalha descartável e água e furar dois sensores Self-aderentes (ver a tabela de materiais) para NIRs para a testa do porco.
- Conecte o pré-amplificador ao monitor e conecte os conectores de cabo do sensor codificados por cores ao pré-amplificador.
- Feche o mecanismo de travamento do pré-amplificador e conecte os sensores aos cabos do sensor.
Nota: A fim de gravar dados em tempo real, uma unidade flash USB deve ser conectada ao monitor NIRS. - Ligue o monitor, clique em novo paciente, digite o nome do estudo, e clique em Done.
- Verifique o sinal de entrada. Quando o sinal estiver estável, clique no menu linha de base e clique em definir linhasde base. Se a linha de base já tiver sido inserida, confirme a nova linha de base clicando em Sim e clique em marca de evento.
- Escolheu o evento com os botões de seta no teclado e com o próximo evento; Selecione o evento 3 indução e pressione selecionar evento.
Nota: Se for necessária informação adicional, consulte o manual de operação do sistema NIRS22.
5. indução de choque hemorrágico
- Conecte a bainha introdutor esquerda com um stopcock de forma de árvore. Ligue uma porta do torneira de três vias com uma seringa de 50 ml e uma com uma garrafa de perfusão vazia.
Nota: Alternativamente, o sangue retirado pode ser coletado em sacos citrados para a autotransfusão mais atrasada. Esta é uma grande vantagem de retirada de sangue controlada. - Mensurar e documentar os parâmetros hemodinâmicos exatos e calcular 40% do índice cardíaco e a pressão arterial média como alvos hemodinâmicos. Defina o evento 93 perda de sangue no sistema NIRs conforme descrito na etapa 4,6.
Nota: O choque hemorrágico é atingido se o índice cardíaco e a pressão arterial média decresce abaixo de 40% do valor basal. Uma saturação regional cerebral considerável da oxigenação (crSO2) declínio de 20% é preferível descrever o prejuízo microcirculatório. A perda de sangue média para conseguir este encontra-se dentro de uma escala de 25-35 mL · quilograma-1. - Aspirar 50 mL de sangue para dentro da seringa e mudar a torneira de três vias. Empurre o sangue para dentro da garrafa vazia.
- Anote o volume de sangue removido.
- Monitore a pressão arterial, o índice cardíaco e o crSO2 de perto. Repita a retirada de sangue até que a pressão arterial alvo e o índice cardíaco sejam alcançados (após 20-30 min).
- Defina o evento 97 hipotensão no dispositivo NIRs conforme descrito na etapa 4,6.
Nota: Não retire o sangue muito rapidamente, porque isso tem o risco de insuficiência cardio-circulatória imediata. Após o término do procedimento de indução de choque, os animais podem ser utilizados para diversas intervenções terapêuticas.
6. fim do experimento e eutanásia
- Injete 0,5 mg de fentanil na linha venosa central e aguarde 5 min.
- Injetar 200 mg de propofol na linha venosa central e eutanizar o animal com cloreto de potássio 40 mmol.
Resultados
Depois de iniciar a indução de choque, um curto período de compensação pode ser registrado. Com a retirada contínua do sangue, a descompensação cardio-circulatória acima mencionada, como monitorada por uma diminuição significativa do crSO2, o índice cardíaco, o índice de volume sanguíneo intratorácico e o índice global de volume diastólico final (Figura 2 , Figura 3e Figura 4), ocorre. Além disso, observa-se taquicardia significante e diminuição da pressão arterial como manifestações comuns de choque hemorrágico (Figura 2). A variação do volume do traço aumenta significativamente (Figura 3). O conteúdo de água pulmonar extravascular e a resistência vascular sistêmica geralmente não são afetados (Figura 3). Depois de terminar a retirada do sangue (28 ± 2 mL · kg-1), os valores hemodinâmicos permanecem em um nível criticamente baixo. Parallelly, crSO2 também desce significativamente. Esses sensores não iniciam regularmente no mesmo nível, mas a lista suspensa amarela é comparável. A Figura 4 mostra uma gravação representativa de um animal. O teor de hemoglobina e o hematócrito não diminuem diretamente no processo, mas os níveis de lactato aumentam e a saturação venosa central de oxigênio diminui (Figura 5).

Figura 1: gráfico de flUXO experimental . A linha de base é definida após a preparação e uma estabilização de 30 min. O choque é induzido por 30 min. os parâmetros de saída cardíaca do contorno do pulso e a oxigenação regional cerebral são medidos durante todo o experimento. Os tempos de medição são denominados como preparação, linha de basee choque.
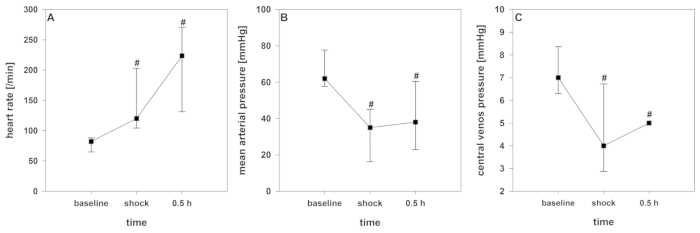
Figura 2 : Desenvolvimento de hemodinâmica durante choque hemorrágico. Os efeitos ao longo do tempo são analisados por ANOVA e post hoc Student-Newman-Keuls método. # p < 0, 5 para a linha de base. Os dados são apresentados como média e desvio padrão. (A) frequência cardíaca (B) pressão arterial média e (C) pressão venosa central são consideravelmente influenciadas neste modelo. Por favor clique aqui para ver uma versão maior desta figura.
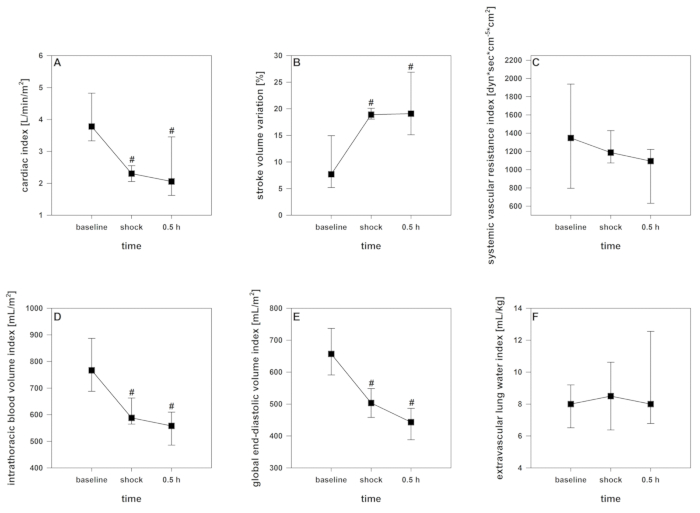
Figura 3 : Desenvolvimento da saída cardíaca do contorno do pulso e parâmetros thermodilution-derivados durante o choque hemorrágico. Os efeitos ao longo do tempo são analisados por ANOVA e post hoc Student-Newman-Keuls método. # p < 0, 5 para a linha de base. Os dados são apresentados como média e desvio padrão. (A) diminui o índice cardíaco, (B) aumenta a variação do volume do curso, (D) índice de volume sanguíneo intratorácico e (e) diminuição do índice de volume diastólico global final, (C) índice de resistência vascular sistêmica e (F ) o índice de água pulmonar extravascular permanece inalterado. Por favor clique aqui para ver uma versão maior desta figura.
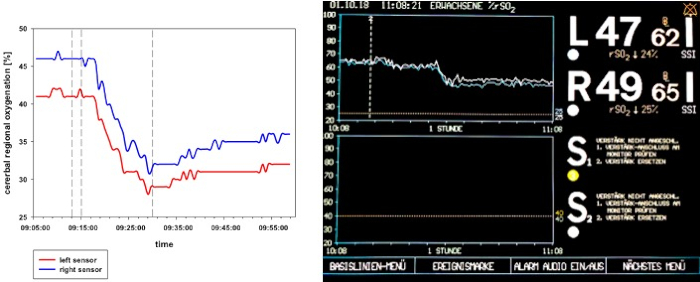
Figura 4 : Crso2 fluxograma durante o choque hemorrágico em um animal representativo. O painel esquerdo mostra uma apresentação esquemática do crSO2 durante o choque hemorrágico. O painel direito mostra a exibição do sistema NIRS. crSO2 decompõe-se significativamente através da indução de choque e permanece em um nível baixo depois que a retirada de sangue é terminada.

Figura 5 : Desenvolvimento de parâmetros hematológicos durante choque hemorrágico. Os efeitos ao longo do tempo são analisados por ANOVA e post hoc Student-Newman-Keuls método. # p < 0, 5 para a linha de base. Os dados são apresentados como média e desvio padrão. (A) hemoglobina e (D) excesso de base permanecem inalterados, (C) o nível de lactato aumenta significativamente, (B) diminui a saturação venosa central de oxigênio. Por favor clique aqui para ver uma versão maior desta figura.
Discussão
O protocolo descreve um método de indução de choque hemorrágico através de sangramento arterial controlado em suínos que é guiado por hemodinâmica sistêmica, bem como por comprometimento microcirculatório cerebral. As condições de choque foram conseguidas por uma retirada sanguínea calculada de 25-35 mL kg-1 e confirmadas pelo composto mencionado de parâmetros substitutos que indicam a falha cardio-circulatória considerável. Se não tratada, este procedimento foi letal dentro de 2 h em 66% dos animais, o que sublinha a gravidade e a reprodutibilidade do modelo. A ressuscitação fluida adequada, por outro lado, restabilizou a circulação e aprovou a patência para imitar um cenário clínico8. Entretanto, menos perda sanguínea não pode conduzir à instabilidade hemodynamic que igualmente afetou o crSO2 que conduz à falha experimental. A quantidade de sangue removido precisa ser adaptada ao peso corporal do animal, que correspondeu com o volume sanguíneo total8.
Este método permite que os cientistas examinem diferentes aspectos desta condição de risco de vida e abre a oportunidade de estudar uma ampla gama de intervenções terapêuticas em um cenário pseudoclinical. Neste contexto, é importante notar que durante o choque hemorrágico manifesto a macrocirculação por si só dificilmente indica uma microcirculação intacta ou prejudicada e suprimento de oxigênio de órgãos7. A vantagem do procedimento reside no seu design simples e usabilidade. A transferência para outros mamíferos de porte médio parece descomplicada, embora diferentes espécies possam apresentar desafios específicos. O projeto fornece a flexibilidade elevada porque os níveis diferentes de prejuízo cardio-circulatório podem facilmente ser escolhidos titating as variáveis do efeito. A combinação com NIRS fornece a informação sobre a fonte de oxigênio microcirculatória de outra maneira não reconhecida durante o choque hemorrágico.
Algumas das etapas críticas do modelo precisam ser destacadas e exigem atenção. A sedação adequada antes do transporte é essencial para evitar o estresse que pode complicar o manuseio dos animais e falsificar os resultados por liberação de catecolamina endogênica. O focamento porcino, com sua longa cavidade orofaríngea, complica a intubação e torna razoável a assistência de uma segunda pessoa. Regularmente, a epiglote adere ao palato e tem de ser mobilizada com a ponta do tubo. A parte mais estreita da via aérea não está no nível das cordas vocais, mas subglottic, como em pacientes pediátricos23. Estes aspectos tornam o relaxamento muscular adequado essencial porque a intubação é facilitada. O cateterismo de vasos guiados por ultrassom é preferível, embora o acesso cirúrgico também possa ser utilizado de forma reprodutível. A técnica minimamente invasiva precisa de treinamento e experiência especiais, mas pode minimizar sangramento descontrolado, dano tecidual, taxas de complicação, tempo de acesso e dor24. A indução do choque hemorrágico em si parece ser muito simples, mas o usuário deve estar ciente de várias armadilhas. É importante reduzir a velocidade de remoção de sangue para reconhecer a instabilidade hemodinâmica. A remoção arterial é eficiente, mas quando é realizada muito rápido, pode levar a insuficiência cardio-circulatória e experimental não planejada. O cálculo do volume aproximado de extração ajuda a administrar a remoção e evita níveis cardio-circulatórios criticamente baixos25,26,27. Outros protocolos publicados variam em termos de insuficiência hemodinâmica direcionada, quantidade de volume sanguíneo removido e período de retirada de sangue. A embarcação pontuada pode diferir também27,28.
NIRS permite medições em tempo real do crSO2. Em diversos ajustes clínicos, este método foi usado para reconhecer uma fonte de oxigênio cerebral danificada: particularmente durante a cirurgia vascular cardíaca e principal, NIRS representa uma ferramenta valiosa. Os parâmetros derivados de NIRS podem prever um desfecho neurológico pior e a sobrevida do paciente causada pela insuficiente oxigenação tecidual29. Curiosamente, o nível de lactato intracerebral diminui em correlação com os valores de NIRS. Estudos mostraram que durante o lactato de estresse oxidativo pode ser utilizado como uma fonte de piruvato, e o nível de lactato intracraniano diminui10. Esses achados e medições não são considerados nesta descrição básica do modelo. Alterações da pressão arterial média que influenciam a perfusão cerebral, PaO2Paco2, ou a hemoglobina afeta diretamente a crSO derivada de NIRS230,31. O NIRS tem um valor prognóstico em pacientes que sofrem de choque hemorrágico e instabilidade hemodinâmica, bem32,33,34,35,36,37,38,39. No entanto, várias limitações e desvantagens devem ser observadas. O tecido extracranial abaixo dos sensores, como a pele, os músculos, e a gordura, pode influenciar as medidas e pode conduzir aos resultados falsos negativos. A resolução espacial é baixa, e a profundidade de penetração é limitada32,33,34,40,41,42,43. O método não diferencia entre sangue arterial e venoso, nem entre a entrega de oxigênio e a demanda41,44,45. O dispositivo é aprovado primeiramente para a aplicação humana. Os sensores usados são projetados para adultos humanos. Sensores menores para crianças e recém-nascidos existem, mas estes não estavam disponíveis para este protocolo. Em suínos, a técnica é amplamente aceita, e crSO2correlaciona-se com uma pressão parcial do oxigênio, do electroencephalography quantitativo, e da saturação venosa cerebral do oxigênio46,47. Diversos dispositivos medem diretamente a pressão parcial do oxigênio no tecido cerebral. Para esta finalidade, as pontas de prova têm que ser inseridas cirùrgica no cérebro. Isto permite medidas não afetadas na região respectiva do interesse e evita distúrbios pelo tecido vasodilation circunvizinho. Esta aproximação é altamente invasora e rather apropriada para encenações especiais como procedimentos Neurosurgical48,49,50,51. O uso de modelos porcina para simular o Pathomechanisms humano é uma aproximação muito comum11,12,13,15. A vantagem reside na comparabilidade fisiológica entre as duas espécies. Experimentos que simulam condições clínicas com risco de vida requerem conhecimentos fundamentais em medicina intensiva e anestesia, mas também em características específicas relacionadas a espécies. Isso permite imitar cenários clínicos de forma realista para o teste translacional de novos dispositivos ou regimes terapêuticos no limiar para a aplicação clínica8,52. No entanto, temos de estar cientes de que as conclusões diretas ou imediatas relativas à aplicação clínica dificilmente podem ser extraídas de modelos experimentais. Algumas diferenças e limitações relevantes devem ser observadas: em relação ao choque ou hemorragia, o sistema de coagulação porcina parece ser mais eficaz e o teor de hemoglobina é significativamente menor. Além disso, os níveis plasmáticos de lactato e succinato diferem53. O sangue porcino consiste em um sistema de grupo sanguíneo "a0", comparado ao sistema humano "AB0"54. Alguns estudos discutem se a esplenectomia deve ser realizada para excluir a ocorrência de autotransfusão intrínseca em modelos de choque porcino. Por outro lado, durante a esplenectomia, o estresse oxidativo, a dor e a estimulação simpática ocorrem, e o procedimento está associado a reações de autotransfusão por si só. Por estas razões, a esplenectomia não é recomendada55,56. A utilização de dispositivos clinicamente aprovados tem algumas fontes de erro sistémicas. O sistema de PiCCO exige o cálculo da área de superfície do corpo, que difere entre porcos e seres humanos. Isso pode causar um erro sistêmico, mas a capacidade de tendência do dispositivo será afetada. Outros métodos da medida do débito cardíaco, como a Ecocardiografia ou um cateter arterial pulmonar, podem ser discutidos neste ajuste.
Conclui-se que este protocolo apresenta um modelo de choque hemorrágico padronizado, iniciado por retirada sanguínea arterial e controlado por Monitorização hemodinâmica prolongada, bem como crSO2. Em comparação com modelos similares que se concentram principalmente em volumes de remoção predefinidos para indução de choque, essa abordagem destaca uma titulação por meio da falha resultante da macro e da microcirculação.
Divulgações
O dispositivo NIRS foi fornecido incondicionalmente pela Medtronic PLC, EUA, para fins de pesquisa experimental. Alexander Ziebart, Andreas Garcia-Bardon, e Erik K. Hartmann receberam o instrutor honorários para cursos de treinamento do médico do PLC de Medtronic. Nenhum dos autores relata conflitos de interesses financeiros ou outros.
Agradecimentos
Os autores querem agradecer Dagmar Dirvonskis por seu excelente suporte técnico.
Materiais
| Name | Company | Catalog Number | Comments |
| 3-way-stopcock blue | Becton Dickinson Infusion Therapy AB Helsingborg, Sweden | 394602 | Drug administration |
| 3-way-stopcock red | Becton Dickinson Infusion Therapy AB Helsingborg, Sweden | 394605 | Drug administration/Shock induction |
| Atracurium | Hikma Pharma GmbH , Martinsried | AM03AC04* | Anesthesia |
| Canula 20 G | Becton Dickinson S.A. Carretera Mequinenza Fraga, Spain | 301300 | Vascular access |
| Datex Ohmeda S5 | GE Healthcare Finland Oy, Helsinki, Finland | - | Hemodynamic monitor |
| Desinfection | Schülke & Mayr GmbH, Germany | 104802 | Desinfection |
| Heidelberger Verlängerung 75CM | Fresenius Kabi Deutschland GmbH | 2873112 | Drug administration/Shock induction |
| INVOS 5100C Cerebral | Medtronic PLC, USA | - | Monitore for cerebral regional oxygenation |
| INVOS Cerebral/Somatic Oximetry Adult Sensors | Medtronic PLC, USA | 20884521211152 | Monitoring of the cerebral regional oxygenation |
| Endotracheal tube | Teleflex Medical Sdn. Bhd, Malaysia | 112482 | Intubation |
| Endotracheal tube introducer | Wirutec GmbH, Sulzbach, Germany | 5033062 | Intubation |
| Engström Carestation | GE Heathcare, Madison USA | - | Ventilator |
| Fentanyl | Janssen-Cilag GmbH, Neuss | AA0014* | Anesthesia |
| Gloves | Paul Hartmann, Heidenheim, Germany | 9422131 | Self-protection |
| Incetomat-line 150 cm | Fresenius, Kabi GmbH, Bad Homburg, Germany | 9004112 | Drug administration |
| Ketamine | Hameln Pharmaceuticals GmbH, Zofingen, Schweiz | AN01AX03* | Sedation |
| Laryngoscope | Teleflex Medical Sdn. Bhd, Malaysia | 671067-000020 | Intubation |
| Logical pressure monitoring system | Smith- Medical GmbH, Minneapolis, USA | MX9606 | Hemodynamic monitor |
| Logicath 7 Fr 3-lumen 30 cm | Smith- Medical GmbH, Minneapolis, USA | MXA233x30x70-E | Vascular access/Drug administration |
| Masimo Radical 7 | Masimo Corporation, Irvine, USA | - | Hemodynamic monitor |
| Mask for ventilating dogs | Henry Schein, Melville, USA | 730-246 | Ventilation |
| Original Perfusor syringe 50 mL Luer Lock | B.Braun Melsungen AG, Melsungen, Germany | 8728810F | Drug administration |
| PICCO Thermodilution. F5/20CM EW | MAQUET Cardiovascular GmbH, Rastatt, Germany | PV2015L20-A | Hemodynamic monitor |
| Percutaneous sheath introducer set 8,5 und 9 Fr, 10 cm with integral haemostasis valve/sideport | Arrow international inc., Reading, USA | AK-07903 | Vascular access/Shock induction |
| Perfusor FM Braun | B.Braun Melsungen AG, Melsungen, Germany | 8713820 | Drug administration |
| Potassium chloride | Fresenius, Kabi GmbH, Bad Homburg, Germany | 6178549 | Euthanasia |
| Propofol 2% | Fresenius, Kabi GmbH, Bad Homburg, Germany | AN01AX10* | Anesthesia |
| Pulse Contour Cardiac Output (PiCCO2) | Pulsion Medical Systems, Feldkirchen, Germany | - | Hemodynamic monitor |
| Sonosite Micromaxx Ultrasoundsystem | Fujifilm, Sonosite Bothell, Bothell, USA | - | Vascular access |
| Stainless Macintosh Size 4 | Teleflex Medical Sdn. Bhd, Perak, Malaysia | 670000 | Intubation |
| Sterofundin | B.Braun Melsungen AG, Melsungen, Germany | AB05BB01* | balanced electrolyte infusion |
| Stresnil 40 mg/mL | Lilly Germany GmbH, Wiesbaden, Germany | QN05AD90 | Sedation |
| Syringe 10 mL | Becton Dickinson S.A. Carretera Mequinenza Fraga, Spain | 309110 | Drug administration |
| Syringe 2 mL | Becton Dickinson S.A. Carretera Mequinenza Fraga, Spain | 300928 | Drug administration |
| Syringe 20 mL | Becton Dickinson S.A. Carretera Mequinenza Fraga, Spain | 300296 | Drug administration |
| Syringe 5 mL | Becton Dickinson S.A. Carretera Mequinenza Fraga, Spain | 309050 | Drug administration |
| Venous catheter 22 G | B.Braun Melsungen AG, Melsungen, Germany | 4269110S-01 | Vascular access |
| *ATC: Anatomical Therapeutic Chemical / Defined Daily Dose Classification |
Referências
- Kutcher, M. E., et al. A paradigm shift in trauma resuscitation: evaluation of evolving massive transfusion practices. JAMA Surgery. 148 (9), 834-840 (2013).
- Allen, B. S., Ko, Y., Buckberg, G. D., Sakhai, S., Tan, Z. Studies of isolated global brain ischaemia: I. A new large animal model of global brain ischaemia and its baseline perfusion studies. European Journal of Cardio-Thoracic Surgery. 41 (5), 1138-1146 (2012).
- Noll, E., et al. Comparative analysis of resuscitation using human serum albumin and crystalloids or 130/0.4 hydroxyethyl starch and crystalloids on skeletal muscle metabolic profile during experimental haemorrhagic shock in swine: A randomised experimental study. European Journal of Anaesthesiology. 34 (2), 89-97 (2017).
- Tisherman, S. A., Stein, D. M. ICU Management of Trauma Patients. Critical Care Medicine. , (2018).
- Nielsen, T. K., Hvas, C. L., Dobson, G. P., Tonnesen, E., Granfeldt, A. Pulmonary function after hemorrhagic shock and resuscitation in a porcine model. Acta Anaesthesiologica Scandinavica. 58 (8), 1015-1024 (2014).
- Bogert, J. N., Harvin, J. A., Cotton, B. A. Damage Control Resuscitation. Journal of Intensive Care Medicine. 31 (3), 177-186 (2016).
- Gruartmoner, G., Mesquida, J., Ince, C. Fluid therapy and the hypovolemic microcirculation. Current Opinion in Critical Care. 21 (4), 276-284 (2015).
- Ziebart, A., et al. Effect of gelatin-polysuccinat on cerebral oxygenation and microcirculation in a porcine haemorrhagic shock model. Scandinavian Journal Trauma Resuscitation Emergency Medicin. 26 (1), 15 (2018).
- Bassols, A., et al. The pig as an animal model for human pathologies: A proteomics perspective. Proteomics Clinical Applications. 8 (9-10), 715-731 (2014).
- Alosh, H., Ramirez, A., Mink, R. The correlation between brain near-infrared spectroscopy and cerebral blood flow in piglets with intracranial hypertension. Journal of Applied Physiology. 121 (1985), 255-260 (2016).
- Hartmann, E. K., et al. Ventilation/perfusion ratios measured by multiple inert gas elimination during experimental cardiopulmonary resuscitation. Acta Anaesthesiologica Scandinavica. 58 (8), 1032-1039 (2014).
- Hartmann, E. K., Duenges, B., Baumgardner, J. E., Markstaller, K., David, M. Correlation of thermodilution-derived extravascular lung water and ventilation/perfusion-compartments in a porcine model. Intensive Care Medicine. 39 (7), 1313-1317 (2013).
- Hartmann, E. K., et al. An inhaled tumor necrosis factor-alpha-derived TIP peptide improves the pulmonary function in experimental lung injury. Acta Anaesthesiologica Scandinavica. 57 (3), 334-341 (2013).
- Ortiz, A. L., et al. The influence of Ringer's lactate or HES 130/0.4 administration on the integrity of the small intestinal mucosa in a pig hemorrhagic shock model under general anesthesia. Journal of the Veterinary Emergency and Critical. 27 (1), 96-107 (2017).
- Ziebart, A., et al. Low tidal volume pressure support versus controlled ventilation in early experimental sepsis in pigs. Respiratory Research. 15, 101 (2014).
- Hoffman, G. M., et al. Postoperative Cerebral and Somatic Near-Infrared Spectroscopy Saturations and Outcome in Hypoplastic Left Heart Syndrome. The Annals of Thoracic Surgery. 103 (5), 1527-1535 (2017).
- Hickok, R. L., Spaeder, M. C., Berger, J. T., Schuette, J. J., Klugman, D. Postoperative Abdominal NIRS Values Predict Low Cardiac Output Syndrome in Neonates. World Journal for Pediatric and Congenital Heart Surgery. 7 (2), 180-184 (2016).
- Weiner, M. M., Geldard, P., Mittnacht, A. J. Ultrasound-guided vascular access: a comprehensive review. Journal of Cardiothoracic and Vascular Anesthesia. 27 (2), 345-360 (2013).
- Kumar, A., Chuan, A. Ultrasound guided vascular access: efficacy and safety. Best Practice & Research: Clinical Anaesthesiology. 23 (3), 299-311 (2009).
- Lamperti, M., et al. International evidence-based recommendations on ultrasound-guided vascular access. Intensive Care Medicine. 38 (7), 1105-1117 (2012).
- Mayer, J., Suttner, S. Cardiac output derived from arterial pressure waveform. Current Opinion in Anesthesiology. 22 (6), 804-808 (2009).
- Medtronic. . Operations Manual INVOS ® System, Model 5100C. , (2013).
- Wani, T. M., Rafiq, M., Akhter, N., AlGhamdi, F. S., Tobias, J. D. Upper airway in infants-a computed tomography-based analysis. Paediatric Anaesthesia. 27 (5), 501-505 (2017).
- Tuna Katircibasi, M., Gunes, H., Cagri Aykan, A., Aksu, E., Ozgul, S. Comparison of Ultrasound Guidance and Conventional Method for Common Femoral Artery Cannulation: A Prospective Study of 939 Patients. Acta Cardiologica Sinica. 34 (5), 394-398 (2018).
- Teeter, W. A., et al. Feasibility of basic transesophageal echocardiography in hemorrhagic shock: potential applications during resuscitative endovascular balloon occlusion of the aorta (REBOA). Cardiovascular Ultrasound. 16 (1), 12 (2018).
- Kontouli, Z., et al. Resuscitation with centhaquin and 6% hydroxyethyl starch 130/0.4 improves survival in a swine model of hemorrhagic shock: a randomized experimental study. European Journal of Trauma and Emergency Surgery. , (2018).
- Nikolian, V. C., et al. Improvement of Blood-Brain Barrier Integrity in Traumatic Brain Injury and Hemorrhagic Shock Following Treatment With Valproic Acid and Fresh Frozen Plasma. Critical Care Medicine. 46 (1), e59-e66 (2018).
- Williams, T. K., et al. Endovascular variable aortic control (EVAC) versus resuscitative endovascular balloon occlusion of the aorta (REBOA) in a swine model of hemorrhage and ischemia reperfusion injury. The Journal of Trauma and Acute Care Surgery. 85 (3), 519-526 (2018).
- Aly, S. A., et al. Cerebral tissue oxygenation index and lactate at 24 hours postoperative predict survival and neurodevelopmental outcome after neonatal cardiac surgery. Congenital Heart Disease. 12 (2), 188-195 (2017).
- Sorensen, H. Near infrared spectroscopy evaluated cerebral oxygenation during anesthesia. The Danish Medical Journal. 63 (12), (2016).
- Cem, A., et al. Efficacy of near-infrared spectrometry for monitoring the cerebral effects of severe dilutional anemia. Heart Surgery Forum. 17 (3), E154-E159 (2014).
- Edmonds, H. L., Ganzel, B. L., Austin, E. H. Cerebral oximetry for cardiac and vascular surgery. Seminars in Cardiothoracic and Vascular Anesthesia. 8 (2), 147-166 (2004).
- Murkin, J. M., et al. Monitoring brain oxygen saturation during coronary bypass surgery: a randomized, prospective study. Anesthesia & Analgesia. 104 (1), 51-58 (2007).
- Hong, S. W., et al. Prediction of cognitive dysfunction and patients' outcome following valvular heart surgery and the role of cerebral oximetry. European Journal of Cardio-Thoracic Surgery. 33 (4), 560-565 (2008).
- Al Tayar, A., Abouelela, A., Mohiuddeen, K. Can the cerebral regional oxygen saturation be a perfusion parameter in shock?. Journal of Critical Care. 38, 164-167 (2017).
- Torella, F., Cowley, R. D., Thorniley, M. S., McCollum, C. N. Regional tissue oxygenation during hemorrhage: can near infrared spectroscopy be used to monitor blood loss?. Shock. 18 (5), 440-444 (2002).
- Yao, F. S., Tseng, C. C., Ho, C. Y., Levin, S. K., Illner, P. Cerebral oxygen desaturation is associated with early postoperative neuropsychological dysfunction in patients undergoing cardiac surgery. Journal of Cardiothoracic and Vascular Anesthesia. 18 (5), 552-558 (2004).
- Slater, J. P., et al. Cerebral oxygen desaturation predicts cognitive decline and longer hospital stay after cardiac surgery. The Annals of Thoracic Surgery. 87 (1), 36-44 (2009).
- Brodt, J., Vladinov, G., Castillo-Pedraza, C., Cooper, L., Maratea, E. Changes in cerebral oxygen saturation during transcatheter aortic valve replacement. Journal of Clinical Monitoring and Computing. 30 (5), 649-653 (2016).
- Yoshimura, A., et al. Altered cortical brain activity in end stage liver disease assessed by multi-channel near-infrared spectroscopy: Associations with delirium. Scintific Reports. 7 (1), 9258 (2017).
- Douds, M. T., Straub, E. J., Kent, A. C., Bistrick, C. H., Sistino, J. J. A systematic review of cerebral oxygenation-monitoring devices in cardiac surgery. Perfusion. 29 (6), 545-552 (2014).
- Forman, E., et al. Noninvasive continuous cardiac output and cerebral perfusion monitoring in term infants with neonatal encephalopathy: assessment of feasibility and reliability. Pediatric Research. 82 (5), 789-795 (2017).
- Tweddell, J. S., Ghanayem, N. S., Hoffman, G. M. Pro: NIRS is " standard of care " for postoperative management. Seminars in Thoracic and Cardiovascular Surgery: Pediatric Cardiac Surgery Annual. 13 (1), 44-50 (2010).
- Lewis, C., Parulkar, S. D., Bebawy, J., Sherwani, S., Hogue, C. W. Cerebral Neuromonitoring During Cardiac Surgery: A Critical Appraisal With an Emphasis on Near-Infrared Spectroscopy. Journal of Cardiothoracic and Vascular Anesthesia. 32 (5), 2313-2322 (2018).
- Thudium, M., Heinze, I., Ellerkmann, R. K., Hilbert, T. Cerebral Function and Perfusion during Cardiopulmonary Bypass: A Plea for a Multimodal Monitoring Approach. Heart Surgery Forum. 2 (1), E028-E035 (2018).
- Putzer, G., et al. Monitoring of brain oxygenation during hypothermic CPR - A prospective porcine study. Resuscitation. 104, 1-5 (2016).
- Weenink, R. P., et al. Detection of cerebral arterial gas embolism using regional cerebral oxygen saturation, quantitative electroencephalography, and brain oxygen tension in the swine. Journal of Neuroscience Methods. 228, 79-85 (2014).
- Mader, M. M., et al. Evaluation of a New Multiparameter Brain Probe for Simultaneous Measurement of Brain Tissue Oxygenation, Cerebral Blood Flow, Intracranial Pressure, and Brain Temperature in a Porcine Model. Neurocritical Care. , (2018).
- Mikkelsen, M. L. G., et al. The influence of norepinephrine and phenylephrine on cerebral perfusion and oxygenation during propofol-remifentanil and propofol-remifentanil-dexmedetomidine anaesthesia in piglets. Acta Veterinaria Scandinavica. 60 (1), 8 (2018).
- Nelskyla, A., et al. The effect of 50% compared to 100% inspired oxygen fraction on brain oxygenation and post cardiac arrest mitochondrial function in experimental cardiac arrest. Resuscitation. 116, 1-7 (2017).
- Klein, K. U., et al. Intraoperative monitoring of cerebral microcirculation and oxygenation--a feasibility study using a novel photo-spectrometric laser-Doppler flowmetry. European Journal of Trauma and Emergency Surgery. 22 (1), 38-45 (2010).
- Ziebart, A., et al. Pulmonary effects of expiratory-assisted small-lumen ventilation during upper airway obstruction in pigs. Anaesthesia. 70 (10), 1171-1179 (2015).
- Reisz, J. A., et al. All animals are equal but some animals are more equal than others: Plasma lactate and succinate in hemorrhagic shock-A comparison in rodents, swine, nonhuman primates, and injured patients. The Journal of Trauma and Acute. 84 (3), 537-541 (2018).
- Smith, D. M., Newhouse, M., Naziruddin, B., Kresie, L. Blood groups and transfusions in pigs. Xenotransplantation. 13 (3), 186-194 (2006).
- Boysen, S. R., Caulkett, N. A., Brookfield, C. E., Warren, A., Pang, J. M. Splenectomy Versus Sham Splenectomy in a Swine Model of Controlled Hemorrhagic. Shock. 46 (4), 439-446 (2016).
- Wade, C. E., Hannon, J. P. Confounding factors in the hemorrhage of conscious swine: a retrospective study of physical restraint, splenectomy, and hyperthermia. Circulatory Shock. 24 (3), 175-182 (1988).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados