Method Article
Analisando celular superfície de adesão remodelação em resposta à tensão mecânica usando pérolas magnéticas
* Estes autores contribuíram igualmente
Neste Artigo
Resumo
aderências na superfície celular são centrais na mecanotransdução, como eles transmitem tensão mecânica e iniciar as vias de sinalização envolvidos na homeostase e desenvolvimento do tecido. Aqui, apresentamos um protocolo para dissecar as vias bioquímicas que são ativadas em resposta à tensão, utilizando microesferas magnéticas revestidas com ligando e aplicação de força para receptores de adesão.
Resumo
complexos de adesão da superfície celular Mechanosensitive permitir que as células para detectar as propriedades mecânicas dos seus arredores. Estudos recentes identificaram duas moléculas de detecção de força em locais de adesão e fatores de transcrição dependente da força que regulam a expressão de genes específicos de linhagem e impulsionam resultados fenotípicos. No entanto, as redes de sinalização de conversão de tensão mecânica em vias bioquímicas têm permanecido elusivos. Para explorar as vias de sinalização envolvidos em cima aplicada a tensão mecânica receptor da superfície celular, micropérolas superparamagnéticas pode ser usado. Aqui é apresentado um protocolo para a utilização de contas magnéticas para aplicar forças de proteínas de adesão da superfície celular. Utilizando esta abordagem, é possível investigar não apenas as vias de sinalização citoplasmática dependente da força por várias abordagens bioquímicas, mas também pode ser notada aderência por isolamento magnético de complexos de adesão ligados às esferas revestidas com ligando. Este protocolo inclui a preparação do ligando-coesferas superparamagnéticas ciados, e a aplicação de definir forças de tração, seguido por análises bioquímicas. Além disso, nós fornecemos uma amostra representativa de dados que demonstram que a tensão aplicada a aderência à base de integrina desencadeia adesão remodelação e altera a fosforilação da tirosina de proteína.
Introdução
Em metazoa, tensão mecânica dirige o desenvolvimento do tecido e da homeostase através da regulação de uma miríade de processos celulares, como a proliferação, diferenciação e sobrevivência 1, 2. tensão mecânica pode surgir a partir da matriz extracelular ou podem ser gerados por células aderentes, que amostra o ambiente extracelular através da maquinaria contrátil actomiosina que puxa na matriz extracelular e as sondas a sua rigidez por meio de moléculas sensíveis à tensão. Em resposta à tensão, proteínas de adesão mechanosensitive sofrer alterações conformacionais que desencadeiam cascatas de sinalização complexas. Por sua vez, estas vias de sinalização orquestrar uma mechanoresponse englobando a proliferação, diferenciação e sobrevivência que ajusta o comportamento celular para o ambiente extracelular. Tais processos podem ser resolvidos em um período de curto prazo (segundos a minutos) para alimentar rapidamente de volta para o loop de mecha notransduction modificando as estruturas mechanosensitive. Por exemplo, as adesões à base de integrina reforçar em resposta a tensão através de Rho GTPase mediada por remodelação do citoesqueleto 3, 4, 5. Em paralelo, outras vias de sinalização são ativados, durante horas e dias para controlar programas genéticos que, eventualmente, impactar o destino celular 6. Considerando que, muitos estudos têm destacado o efeito da rigidez da matriz no determinismo celular e desenvolvimento da doença 1, 2, os mecanismos moleculares precisos de mecanotransdução mediada por adesão continuam a ser evasivo.
Várias abordagens foram desenvolvidas para estudar os efeitos de forças gerado-celulares ou as forças externas sobre o comportamento das células, incluindo sistemas de fluxo, de transferência de energia de ressonância de fluorescência (FRET) -tension sensores 7,lass = "xref"> 8, 9 substratos compatíveis, pinças magnéticos, pinças ópticas 10 e de microscopia de força atômica (AFM) 11. Aqui apresenta-se um protocolo utilizando esferas superparamagnéticas para caracterizar vias mecanotransdução em resposta a forças de tensão aplicadas aos receptores de adesão específicas. superparamagnéticas grânulos são partículas que magnetizam reversivelmente, quando colocado num campo magnético. Uma vez revestida com um ligando para um receptor específico, estes grânulos de fornecer uma ferramenta poderosa para estudar os efeitos da aplicação de força extracelular. Este método foi validado por diversos estudos 3, 5, 12 - 17 e apresentam a vantagem de facilitar, em grande parte análises bioquímicas nas células aderentes. Usando esferas magnéticas revestidas com colagénio semelhante, seguido de análise bioquímica, os primeiros trabalhos relatados um aumento doa fosforilação da proteína tirosina e a activação de RhoA, em resposta à tensão 5, 18, 19. O método descrito abaixo foi também usado com fibronectina (FN) grânulos -Revestido para caracterizar as vias de sinalização a jusante da tensão aplicada às integrinas 3. Neste estudo, Guilluy et ai. mostrou que a tensão ativa RhoA através do recrutamento dos dois fatores de câmbio nucleótido guanina (GEFs), Larg e GEF-H1, a complexos de adesão integrina. Desde que, outros estudos mostraram que GEF-H1 é recrutado para complexos de adesão em resposta a tensão gerada por células utilizando diferentes métodos de 20, 21, demonstrando a robustez da metodologia aqui descrita. Como resultado, RhoA activada foi mostrado para promover a adesão de reforço, por meio de remodelação do citoesqueleto. Este sistema também foi utilizado para explorar a tensão aplicada tO receptores de adesão / célula a célula. A aplicação de forças sobre esferas magnéticas revestidas com o domínio extracelular da caderina-E induziu um aumento no recrutamento vinculina semelhante a integrina associada complexos de adesão 12. Collins e colegas observaram que a aplicação de tensão para PECAM-1 promove a integrina e ativação RhoA 13. Outra abordagem experimental utilizando esferas magnéticas é o estudo da tensão aplicada aos núcleos isolados. Usando esferas revestidas com anticorpos contra a proteína do envelope nuclear nesprin-1, os complexos de envelope nuclear foram purificados para mostrar que eles são regulados dinamicamente em resposta a tensão mecânica 22. Estes resultados suportam a powerfulness deste método no estudo das vias mecanotransdução. Além disso, enquanto que os sistemas de fluxo de força de tracção ou estimular os processos celulares gerais, esferas magnéticas visar especificamente um receptor de adesão de células utilizando um ligandos de receptores 3 ou anticorpos monoclonais contra o receptor de superfície da célula 13, 15.
Outra vantagem deste método é o isolamento de complexos de adesão por meio de um procedimento de purificação por afinidade de ligando simples. É bem sabido que a adição de contas revestidas com ligando se liga a receptores de adesão de células e induz o recrutamento de várias proteínas de adesão 23. Além disso a aplicação de forças de esferas magnéticas revestidas com ligando transforma estes complexos de adesão em plataformas macromoleculares que medeia várias vias de sinalização dependentes de tensão 4, 24. A lise celular seguido de concentração grânulo utilizando um íman permite o isolamento das plataformas de adesão. Outros métodos utilizados para purificar complexos de adesão já têm sido utilizados em células aderentes. Eles combinam reticulação química para conservar as interacções proteína-proteínae um passo de lise celular por detergente e sonicação ou fluxo de cisalhamento 20, 21, 25, 26, 27, 28. O último passo é a coleta das membranas plasmáticas ventral resultantes contendo os complexos de adesão. Ao contrário destes métodos, esferas magnéticas permitir um nível de purificação maior de complexos de adesão celular por segmentação selectivamente uma família específica de receptores de adesão. Esférulas magnéticas já têm sido utilizadas para purificar complexos de adesão em células não-aderentes ligadas a microesferas revestidas com ligando, 29 30. O método descrito abaixo imita situações biológicas, onde a força é aplicada por um curto período sustentado (segundos a minutos). Portanto, ele fornece uma ferramenta poderosa para investigar tanto a composição molecular de complexos de adesão purificada eas vias a jusante mechanosensitive de sinalização.
Aqui apresentamos um protocolo experimental detalhado para usando esferas magnéticas para aplicar forças de tracção às proteínas de superfície de adesão. Um íman de neodímio permanente é colocada no topo da superfície do prato de cultura. A face do polo do íman é colocado a uma altura de 6 mm, de modo que a força sobre uma única 2,8 uM esférulas magnéticas é constante (cerca de 30-40 PN) 31. A duração da estimulação tensão é determinado pelo operador, dependendo da molécula de interesse e o seu tempo de activação escala. As células são lisadas, finalmente, complexos de adesão são purificados por separação de grânulos utilizando um íman e análises bioquímicas são processados. Este protocolo inclui a preparação de grânulos superparamagnéticas recobertas pelo ligante, bem como a aplicação de tensão através do ímã seguido por análises bioquímicas. Além disso, nós fornecemos uma amostra representativa de dados que demonstram que a tensão aplicada à base ADH-integrinaesions induz adesão remodelação e altera a fosforilação da proteína tirosina.
Protocolo
1. Conjugação de ligando a esferas magnéticas
Nota: a conjugação ligando é realizada utilizando pérolas activadas por tosilo superparamagnéticas com um diâmetro de 2,8 uM (concentração da solução de estoque 10 8 esferas / mL, 30 mg de esferas / ml). O protocolo seguinte baseia-se amostras de cerca de 2 x 10 5 células, que correspondem a MRC 5-células cultivadas a 80% de confluência numa placa de cultura de tecidos de 60 mm. Ajuste o volume de contas e reagentes de acordo, se utilizando placas de diferentes tamanhos ou células em diferentes confluências. Usar uma quantidade de grânulos superparamagnéticas, a fim de ter 2 contas por célula. Portanto, 4 x 10 5 esferas são necessários para uma placa de 60 mm.
- Completamente ressuspender as contas dentro do recipiente original em vortex pelo menos 30 s. Aliquota de 40 ul das esferas superparamagnéticas ressuspenso (correspondendo a 4 x 10 6 grânulos) a 1,5 mL tubo de microcentrífuga.
- Colocar o tubo em um separati magnéticano suporte, a fim de separar as esferas magnéticas a partir da solução. Descartar o sobrenadante, remover o suporte do tubo de separação magnética e voltar a suspender as pérolas em 1 ml de 0,1 M fosfato de Na pH 7,4.
- Repetir o passo de lavagem duas vezes com 1 mL de 0,1 M fosfato de Na pH 7,4.
- Após a lavagem final, voltar a suspender as pérolas em 1 ml de 0,1 M de Na-fosfato pH 7,4.
- Combinar 100 ug Bovina A fibronectina (FN) ou qualquer outro ligando de receptor de adesão de célula a 1 mL de 0,1 M fosfato de Na pH 7,4 contendo esferas e misturar por pipetagem.
- Repetir os passos anteriores, substituindo FN ou qualquer outro ligando específico com BSA, poli-D-lisina ou apo-transferrina para controlos negativos.
- Opcionalmente, para análise em gel, ter uma alíquota de 10 ul de solução de ligando para análise de eficiência de ligação cruzada e misturar-se com um volume adequado de tampão de amostra de Laemmli concentrado.
- Incubar grânulos com a solução contendo ligando durante 12-24 h a 37 ° C num rotor.
- Se agregados talão aparecer após a reação ocorreu, sonicate (poder 39 W contínua) para não mais de 10-20 s.
- Isolar as contas usando suporte de separação magnética, aspirar a solução restante e adicionar 1 ml de PBS / BSA a 0,2% pH 7,6 solução. Incubar durante 1 h no rotor a 37 ° C.
- Lavar os grânulos utilizando um magnete duas vezes com 1 mL de PBS / BSA a 0,2%, pH 7,6. Ressuspender as pérolas em 1 ml PBS / BSA a 0,2%, pH 7,6.
- grânulos sonicate se agregados aparecer para não mais do que 20-30 s.
- Opcionalmente, remover uma alíquota de 10 uL para analisar a eficiência de acoplamento por Western blot (misturar com um volume adequado de tampão de amostra de Laemmli concentrado).
- Prossiga para a célula ensaios ou loja de esferas, a 4 ° C por até 1 mês.
- Opcionalmente, correr um gel de SDS-PAGE e mancha com azul de Coomassie para analisar FN reticulação às pérolas magnéticas.
2. Aplicação de forças de tensão sobre as esferas revestidas com ligando ligado à aderência receptores na dorsalSuperfície das células
- As células aderentes de cultura na placa de cultura de tecido de 60 mm de meio de crescimento adequado (geralmente DMEM 4,5 g / L de D-glucose suplementado com FCS a 10%) até atingir 80% de confluência.
- Preparar tampão de lise não desnaturante não-iónico (20 mM Tris-HCl pH 7,6, NaCl 150 mM, MgCl2 2 mM, 0,1% de NP-40) e tubos de microcentrífuga frio.
- Agregar as esferas revestidas com ligandos de secção 1.10 e ressuspender em 1 ml de PBS / 0,2% BSA a pH 7,6. Adicionar 100 ul da solução de pérolas revestidas com ligandos para 5 mL de meio de cultura quente e vortex.
- médio aspirado na placa de cultura 60 mm e adicionar 5 ml de meio de crescimento quente suplementado com grânulos.
- Incubar durante 20 min sob as condições de cultura de células (37 ° C e 5% de CO 2) para permitir que as esferas para sedimentar e aderir às células. É crucial para não exceder 20 min desde pérolas podem ser internalizados por fagocitose.
- Opcionalmente, observe as contas sob um microscópio de luz usando um 10X ou 20X objective e verificar a aderência do grânulo agitando levemente o prato para discriminar entre esferas ligadas e flutuantes.
- Enquanto se mantinha a placa de cultura na incubadora, trocar a tampa normal de prato para uma tampa com um íman de neodímio 38 milímetros rodada ligado na face superior. O íman está mantido no lugar por dois pequenos ímans de neodímio 13 mm posicionado na face inferior da tampa. Uma vez que os ímãs são muito poderosos, manipulá-los com cuidado.
- Incubar as células submetidas a tensão para os pontos de tempo desejados em condições de cultura de células (37 ° C e 5% CO 2).
- Após o tratamento, prato colocar em gelo e cuidadosamente aspirar todo o meio a partir do prato.
- Adicionar 300 ul de tampão de lise de células, e incuba-se durante 10 min em gelo. Recolhe-se o lisado usando um raspador de células e transferir para um tubo de microcentrífuga de 1,5 ml pré-arrefecido.
- Agregar as esferas magnéticas, utilizando o suporte de separação magnética e transferir o lisado celular total a um novo pré-frioed 1,5 mL tubo de microcentrífuga. Conserva-se a fracção de -20 ° C para posterior análise.
- Lavam-se as esferas 3 vezes com 1 mL de tampão de lise arrefecido com gelo. Adicionar 50 ul de tampão de amostra de Laemmli ao sedimento de grânulo, misturar por pipetagem e em ebulição a 95 ° C durante 5 min, utilizando um aquecedor de bloco seco. Esta fracção contém os complexos de adesão isoladas. Proceder à análise bioquímica ou armazenar a -20 ° C.
- A partir do lisado celular total obtida após separação de grânulos (cerca de 300 mL), remover uma alíquota de 50 uL para análise de mancha ocidental.
NOTA: Os 250 uL esquerda pode ser utilizado em estudos bioquímicos, tais como estudos de interacção proteína-proteína, ensaios de imunoprecipitação (GST pull-down) ou ensaios de actividade de GTPase (mudando o tampão de lise pode ser necessário, dependendo da GTPase de interesse).
Resultados
O esquema da técnica é ilustrada na figura 1a. Após a conjugação ligando, esferas magnéticas são incubados com as células durante 20 minutos, e, em seguida, um íman permanente é usada para aplicar forças de tracção de cerca de 30-40 NP para várias quantidades de tempo. A Figura 1b mostra 2,8 ^ M FN-esferas magnéticas revestidas com destino a receptores de adesão de células MRC5.
Os passos de lavagem de grânulos superparamagnéticas após lise celular são cruciais e determinar o grau de purificação. Um mínimo de três lavagens é recomendado. Imunotransferência de GADPH com exposições longas pode ser útil para testar a pureza de complexos de adesão (Figura 2a).
grânulos FN-revestidos foram utilizados para investigar os processos mecanotransdução que ocorrem ao longo do tempo nos complexos de adesão em resposta à tensão. Após separação magnética da fracção complexo de adesão, o lisado e o complexo de adesão fracção foram analisadas porWestern blot. Como esperado, observou-se a talina, vinculina e paxilina, mas não na fracção GAPDH complexos de adesão mesmo na ausência de estimulação mecânica (Figura 2b). Consistente com relatórios anteriores 32, 33, a tensão desencadeada recrutamento vinculin para complexos de adesão. Enquanto a tensão não afectou recrutamento paxilina para complexos de adesão, a sua fosforilação em tirosina 31 foi aumentada em resposta a uma tensão mecânica, tanto no lisado celular total e na fracção de complexo de adesão.
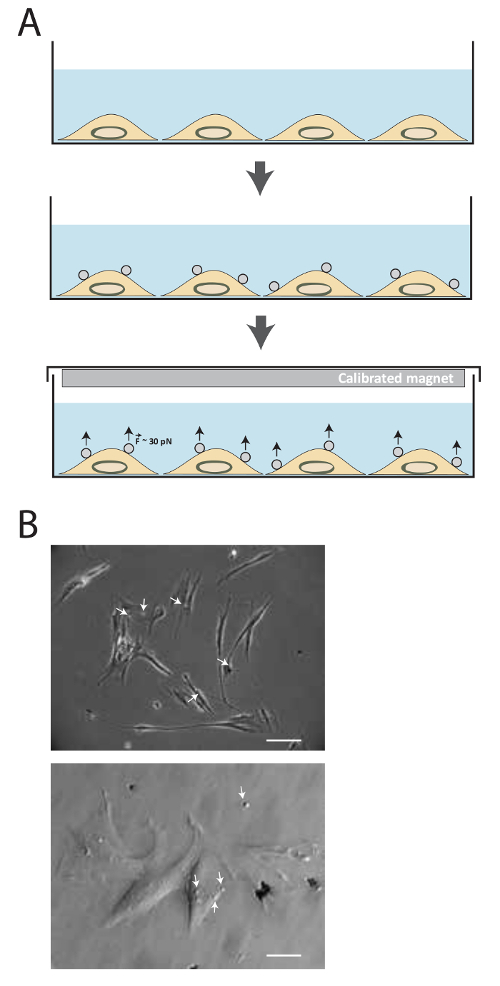
Figura 1. Descrição do método. (A) Representação esquemática da técnica. As células são primeiro cultivadas em meio de cultura até a confluência desejada seja atingida. Em seguida, as esferas superparamagnéticas são adicionados para 15-20 min. forças de tensão de cerca de 30-40 pN sãoem seguida, aplicado usando o magneto calibrado para a quantidade de tempo diferente. (B) os grânulos superparamagnéticas revestidas com fibronectina ligam-se a receptores de adesão celular. As células são fotografadas por contraste de fase em microscopia de luz de transmissão 15 minutos após a adição dos grânulos superparamagnéticas (seta branca) em meio. (Top imagem: Barra de escala = 25 mm, imagem de fundo: Barra de escala = 100 mm) Por favor clique aqui para ver uma versão maior desta figura.
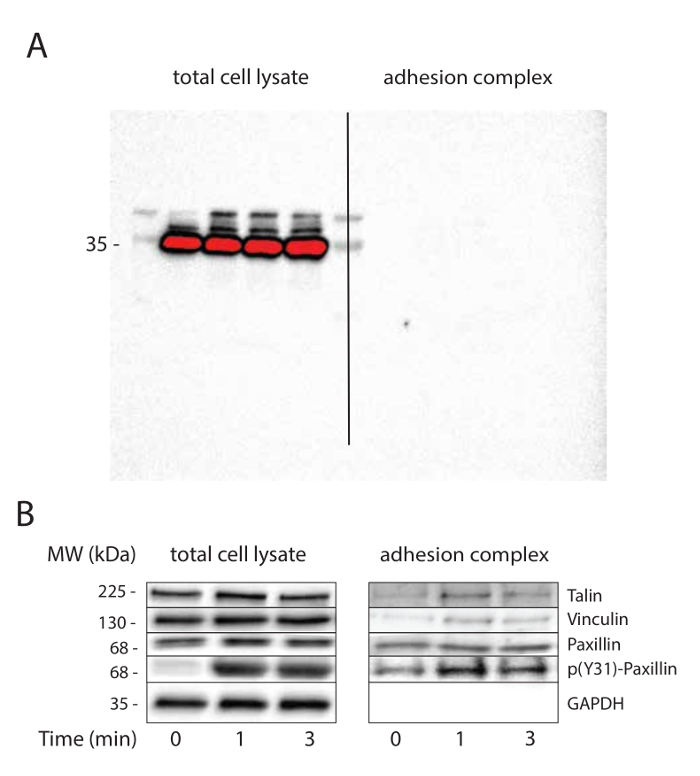
Figura 2. tensão mecânica induz a aderência de maturação. (A) Purificação de complexos de adesão. GAPDH imunotransferência é utilizado como controlo de carga para o lisado de células total e para verificar a pureza de complexos de adesão. A membrana de nitrocelulose foi fotografada usando uma exposição longa para demonstrar the ausência de sinal na fracção complexo de adesão. (B) A tensão induz a adesão de maturação. Carregando controle (GAPDH) e candidatos (vinculin, Talin e Paxillin) conhecidos de ser recrutado ou fosforilada no complexos de adesão em resposta à tensão mecânica são imunologicamente. Esta experiência foi realizada em células MRC5. Por favor clique aqui para ver uma versão maior desta figura.
Discussão
O método aqui descrito constitui uma abordagem simples para aplicar a tensão de receptores de adesão da superfície celular e permitir a sua purificação posterior. No entanto, alguns passos são essenciais para realizar a purificação eficiente de adesão e optimização de potencial pode ser feito em função dos receptores de adesão segmentados. Nós apresentamos os possíveis problemas que o usuário pode encontrar abaixo.
Utilizou-se 2,8 um de diâmetro, mas as esferas magnéticas grânulos maiores podem ser utilizadas, tais como 4,5 um de diâmetro. No entanto, o diâmetro do cordão deve ser limitada a 2-5 mm desde a fagocitose pode ocorrer mais rapidamente durante 30-60 min de incubação e os grânulos maiores têm aderência mais forte para que o deslocamento talão seria restrito sob campo magnético 34, 35. Portanto, é importante limitar o tempo de incubação para períodos curtos e usar o tamanho adequado do grânulo. O número de grânulos por célula incubadas terá impacto sobre a quantidade de fexperiência orce por uma única célula. Enquanto um quer para estimular eficientemente as células com tensão, muitos grânulos por célula pode levar à activação de vias de sinalização irrelevantes. Nós normalmente incubar uma média de duas esferas por células para os grânulos revestidos com FN-, mas esta quantidade pode ser ajustado [1 a 5 por célula grânulos] dependendo do tipo de célula e do receptor da superfície celular. Em relação ao íman, o método descrito aqui utilizado um íman para que a força resultante sobre um 2,8 uM foi medida (cerca de 30-40 pN por medição do deslocamento de esferas magnéticas em sem diluição glicerol, um líquido Newtoniano com viscosidade conhecida 31, embora é possível usar ímãs maiores para aplicar maior quantidade de força se necessário. é importante notar que estes ímãs são extremamente poderosos e manipulá-los com cuidado.
Após 12-24 h de incubação com o ligando de ECM (passo 1.7), bem como após 1 h de incubação (passo 1.9) com tampão PBS / BSA a 0,2%, pH 7,6, a mmicrobeads agnetic pode formar agregados. Em seguida, é crítico para separar os grânulos, tanto quanto possível respeitar a relação de 2 contas por célula. No entanto, ainda é aceitável ter uma relação de 5: 1. Grânulos de separação pode ser conseguida por mistura e pipetagem ou usando sonicação, embora por um período curto (20-30 s).
Várias proteínas podem ser conjugados com os grânulos, incluindo ligando de integrina (FN, colagénio), as proteínas recombinantes ou anticorpos dirigidos contra receptores específicos da superfície celular. O acessório de esferas magnéticas revestidas com ligando de superfície celular dorsal pode ser enfraquecida pela baixa eficiência de acoplamento do ligando sobre as esferas. Recomenda-se que vá para a ligação com os grânulos através da recolha de uma alíquota de solução de ligando diluída antes da adição aos grânulos e uma alíquota de pérolas no final do processo de acoplamento do ligando. Estas aliquotas podem ser processadas para análise de SDS-PAGE e coloração com azul de Coomassie.
Se nenhuma alteração emvias ou processos mechanosensing esperados são detectados sinalização, é importante considerar diferentes possibilidades. Uma maneira de identificar o problema é o de modular a duração da experiência com o imã. É bem conhecido que a velocidade de processos celulares varia dependendo do tipo de células utilizado. Outra opção seria testar moléculas sensíveis à tensão conhecidos e verificar suas modificações pós translacionais por western blot (por exemplo, fosforilação paxilina ou fosforilação FAK pode ser analisado). A quantidade de força pode ser também crítica e utilizando esferas de um íman mais espessa (mesmo grau N52) ou maiores podem ser uma opção. Além disso, a eficiência de ligação ligando / receptor pode ser explorada através da análise de complexo de adesão e olhar para os receptores da superfície das células (tais como caderina ou integrina). A confluência de células pode também afectar a resposta celular a tensão. Como foi observado que a adesão / célula a célula pode afectar o comportamento de células pré-esforço e cystokeletal, é important de notar que a confluência podem afectar a resposta celular a tensão. Mesmo que recomendamos 80% de confluência para a aplicação de tensão a aderências à base de integrina, diferentes condições podem ser testadas de modo a optimizar o sistema experimental.
Embora este método fornece uma ferramenta poderosa para decifrar a adhesome sensível tensão, bem como as vias de sinalização associadas, que também tinha algumas limitações. Em primeiro lugar, uma vez que a principal preocupação com tal dimensão pequena esferas magnéticas é o risco de a sua internalização pelas células, este método não pode ser usado para estudar as respostas celulares de sinalização mechanosensitive longo prazo que modificam o destino celular, tais como a diferenciação e proliferação. Outra limitação reside no modo de como as forças são aplicadas à camada de células na placa de cultura. Com efeito, uma vez que o campo magnético é sempre maior na periferia do íman, as forças podem variar na superfície da placa de cultura com um gradiente decrescente de célulasque se estende a partir da periferia para o centro e pode conduzir a respostas celulares heterogéneas.
O procedimento aqui descrito constitui um método simples e de baixo custo, que permite estudar vias celulares mechanosensitive bem como investigar a composição molecular de complexos de adesão submetidos a tensão. Outras abordagens, tais como o dispositivo que aplica tensão cíclico para células de alongamento, conduzir à aplicação de tensão para todos os receptores de superfície de célula que interagem com a matriz extracelular. O método aqui descrito tem a vantagem de permitir a estimulação força de um subconjunto específico de receptores da superfície celular e uma grande variedade de ligandos podem ser utilizados, tais como a integrina ligandos ou anticorpos dirigidos contra receptores de superfície celular, permitindo que o estudo de diversos sistemas mechanosensitive distintas. Outra vantagem deste método é que ele leva para a purificação dos complexos de proteínas que experimentaram a tensão e de suporte de carga para trabalhar em elemeNTS que são conhecidos por desempenhar um papel central na mecanotransdução 36. O complexo de adesão purificada também pode ser usado para várias abordagens bioquímicas 14, tais como ensaios de cinase para investigar a actividade de cinase em resposta à tensão, ou um ensaio de polimerização da actina. Além disso, este sistema experimental pode ser acoplado com uma pinça magnéticos para explorar a resposta mecânica celular e correlacionar esta resposta com as vias de sinalização identificados. Curiosamente, as nanopartículas magnetoplasmonic têm sido usadas recentemente por meios mecânicos Notch de carga e E-caderina com controle preciso no tempo e no espaço 37. Esta evolução recente pode ajudar a explorar vias de sinalização mechanosensitive com diferentes entradas espaciais, temporais e mecânicas.
Divulgações
Os autores declaram não haver interesses financeiros concorrentes.
Agradecimentos
CG é apoiada por doações da Agence National de la Recherche (ANR-13-JSV1-0008), a partir do Sétimo Programa-Quadro da União Europeia (Marie Curie Integração Carreira n˚8304162) e do Conselho Europeu de Investigação (ERC) no âmbito do Horizonte da União Europeia 2020 programa de inovação (ERC Starting Grant n˚639300) pesquisa e.
Materiais
| Name | Company | Catalog Number | Comments |
| Neodymium magnets (on the upper face of 60 mm dish) | K&J Magnetics, Inc | DX88-N52 | grade N52 dimension: 1 1/2" dia. x 1/2" thick |
| Neodymium magnets (on the lower face of 60 mm dish) | K&J Magnetics, Inc | D84PC-BLK | grade N42 dimension: 1/2" dia. x 1/4" thick Black Plastic Coated |
| Dynabeads M280 Tosylactivated | Thermofisher | 14203 | superparamagnetic beads |
| DynaMag-2 Magnet | Thermofisher | 12321D | |
| Fibronectin | Sigma-Aldrich | F1141-5MG | Fibronectin from bovine plasma |
| Poly-D-Lysine | Sigma-Aldrich | P7280-5MG | |
| Apo-Transferrin | Sigma-Aldrich | T1428-50MG | Bovine Apo-Transferrin |
| Bovine serum albumin | Sigma-Aldrich | A7906-500G | |
| DMEM high glucose, GlutaMAX supplement, pyruvate | Life Technologies | 31966-021 | DMEM+GlutaMAX-I 500 ml |
| 60*15 mm culture dish | Falcon | 353004 |
Referências
- Discher, D. E., Janmey, P., Wang, Y. -. L. . Tissue cells feel and respond to the stiffness of their substrate. 310 (5751), 1139-1143 (2005).
- DuFort, C. C., Paszek, M. J., Weaver, V. M. Balancing forces: architectural control of mechanotransduction. Nat Rev Mol Cell Biol. 12 (5), 308-319 (2011).
- Guilluy, C., et al. The Rho GEFs LARG and GEF-H1 regulate the mechanical response to force on integrins. Nat Cell Biol. 13 (6), 722-727 (2011).
- Matthews, B. D., Overby, D. R., Mannix, R., Ingber, D. E. Cellular adaptation to mechanical stress: role of integrins, Rho, cytoskeletal tension and mechanosensitive ion channels. J Cell Sci. 119 (3), 508-518 (2006).
- Zhao, X. -. H., et al. Force activates smooth muscle alpha-actin promoter activity through the Rho signaling pathway. J Cell Sci. 120 (Pt 10), 1801-1809 (2007).
- Engler, A. J., Sen, S., Sweeney, H. L., Discher, D. E. Matrix elasticity directs stem cell lineage specification. Cell. 126 (4), 677-689 (2006).
- Austen, K., Kluger, C., Freikamp, A., Chrostek-Grashoff, A., Grashoff, C. Generation and analysis of biosensors to measure mechanical forces within cells. Meth Mol Biol. 1066, 169-184 (2013).
- Grashoff, C., et al. Measuring mechanical tension across vinculin reveals regulation of focal adhesion dynamics. Nature. 466 (7303), 263-266 (2010).
- Pelham, R. J., Wang, Y. l. . Cell locomotion and focal adhesions are regulated by substrate flexibility. Proc Natl Acad Sci USA. 94 (25), 13661-13665 (1997).
- Choquet, D., Felsenfeld, D. P., Sheetz, M. P. Extracellular matrix rigidity causes strengthening of integrin-cytoskeleton linkages. Cell. 88 (1), 39-48 (1997).
- Chaudhuri, O., Parekh, S. H., Lam, W. A., Fletcher, D. A. Combined atomic force microscopy and side-view optical imaging for mechanical studies of cells. Nat Meth. 6 (5), 383-387 (2009).
- Bays, J. L., et al. Vinculin phosphorylation differentially regulates mechanotransduction at cell-cell and cell-matrix adhesions. J Cell Biol. 205 (2), 251-263 (2014).
- Collins, C., et al. Localized tensional forces on PECAM-1 elicit a global mechanotransduction response via the integrin-RhoA pathway. Curr Biol. 22 (22), 2087-2094 (2012).
- Gordon, W. R., et al. Mechanical Allostery: Evidence for a Force Requirement in the Proteolytic Activation of Notch. Dev Cell. 33 (6), 729-736 (2015).
- Lessey-Morillon, E. C., et al. The RhoA guanine nucleotide exchange factor, LARG, mediates ICAM-1-dependent mechanotransduction in endothelial cells to stimulate transendothelial migration. J Immunol. 192 (7), 3390-3398 (2014).
- Osborne, L. D., et al. TGF-β regulates LARG and GEF-H1 during EMT to affect stiffening response to force and cell invasion. Mol Biol Cell. 25 (22), 3528-3540 (2014).
- Scott, D. W., Tolbert, C. E., Burridge, K. Tension on JAM-A activates RhoA via GEF-H1 and p115 RhoGEF. Mol Biol Cell. 27 (9), 1420-1430 (2016).
- Glogauer, M., Ferrier, J., McCulloch, C. A. Magnetic fields applied to collagen-coated ferric oxide beads induce stretch-activated Ca2+ flux in fibroblasts. Am J Physiol - Cell Physiol. 269 (5), C1093-C1104 (1995).
- Glogauer, M., et al. Calcium ions and tyrosine phosphorylation interact coordinately with actin to regulate cytoprotective responses to stretching. J Cell Sci. 110 (Pt 1), 11-21 (1997).
- Kuo, J. -. C., Han, X., Hsiao, C. -. T., Yates, J. R., Waterman, C. M. Analysis of the myosin-II-responsive focal adhesion proteome reveals a role for β-Pix in negative regulation of focal adhesion maturation. Nat Cell Biol. 13 (4), 383-393 (2011).
- Schiller, H. B., et al. β1- and αv-class integrins cooperate to regulate myosin II during rigidity sensing of fibronectin-based microenvironments. Nat Cell Biol. 15 (6), 625-636 (2013).
- Guilluy, C., et al. Isolated nuclei adapt to force and reveal a mechanotransduction pathway in the nucleus. Nat Cell Biol. 16 (4), 376-381 (2014).
- Plopper, G. E., McNamee, H. P., Dike, L. E., Bojanowski, K., Ingber, D. E. Convergence of integrin and growth factor receptor signaling pathways within the focal adhesion complex. Mol Biol Cell. 6 (10), 1349-1365 (1995).
- Roca-Cusachs, P., Gauthier, N. C., Del Rio, ., A, M. P., Sheetz, Clustering of alpha(5)beta(1) integrins determines adhesion strength whereas alpha(v)beta(3) and talin enable mechanotransduction. Proc Natl Acad Sci USA. 106 (38), 16245-16250 (2009).
- Ajeian, J. N., et al. Proteomic analysis of integrin-associated complexes from mesenchymal stem cells. Proteomics Clin Appl. 10 (1), 51-57 (2016).
- Horton, E. R., Astudillo, P., Humphries, M. J., Humphries, J. D. Mechanosensitivity of integrin adhesion complexes: Role of the consensus adhesome. Exp Cell Res. , (2015).
- Jones, M. C., et al. Isolation of integrin-based adhesion complexes. Curr Protoc Cell Biol. 66, 9.8.1-9.8.15 (2015).
- Ng, D. H. J., Humphries, J. D., Byron, A., Millon-Frémillon, A., Humphries, M. J. Microtubule-dependent modulation of adhesion complex composition. PloS One. 9 (12), e115213 (2014).
- Byron, A., Humphries, J. D., Bass, M. D., Knight, D., Humphries, M. J. Proteomic analysis of integrin adhesion complexes. Sci Sign. 4 (167), pt2 (2011).
- Byron, A., Humphries, J. D., Craig, S. E., Knight, D., Humphries, M. J. Proteomic analysis of α4β1 integrin adhesion complexes reveals α-subunit-dependent protein recruitment. Proteomics. 12 (13), 2107-2114 (2012).
- Marjoram, R. J., Guilluy, C., Burridge, K. Using magnets and magnetic beads to dissect signaling pathways activated by mechanical tension applied to cells. Methods. , (2015).
- Pasapera, A. M., Schneider, I. C., Rericha, E., Schlaepfer, D. D., Waterman, C. M. Myosin II activity regulates vinculin recruitment to focal adhesions through FAK-mediated paxillin phosphorylation. J Cell Biol. 188 (6), 877-890 (2010).
- Sawada, Y., Sheetz, M. P. Force transduction by Triton cytoskeletons. J Cell Biol. 156 (4), 609-615 (2002).
- Grinnell, F., Geiger, B. Interaction of fibronectin-coated beads with attached and spread fibroblasts. Binding, phagocytosis, and cytoskeletal reorganization. Exp Cell Res. 162 (2), 449-461 (1986).
- Schroeder, F., Kinden, D. A. Measurement of phagocytosis using fluorescent latex beads. J Biochem Biophys Meth. 8 (1), 15-27 (1983).
- Hoffman, B. D., Grashoff, C., Schwartz, M. A. Dynamic molecular processes mediate cellular mechanotransduction. Nature. 475 (7356), 316-323 (2011).
- Seo, D., et al. A Mechanogenetic Toolkit for Interrogating Cell Signaling in Space and Time. Cell. 165 (6), 1507-1518 (2016).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados